предельные УВ.ppt
- Количество слайдов: 15
 Углеводороды. Предельные (насыщенные) углеводороды
Углеводороды. Предельные (насыщенные) углеводороды
 Определение l l Предельные углеводороды - это органические вещества, состоящие только из углерода и водорода, соответствующие общей формуле Сn Н 2 n +2. У этих веществ только простые одинарные связи между атомами углерода, которые соединяются с максимально возможным количеством числом атомов водорода. Их поэтому называют предельными или насыщенными.
Определение l l Предельные углеводороды - это органические вещества, состоящие только из углерода и водорода, соответствующие общей формуле Сn Н 2 n +2. У этих веществ только простые одинарные связи между атомами углерода, которые соединяются с максимально возможным количеством числом атомов водорода. Их поэтому называют предельными или насыщенными.
 Изомеры l l Изомеры - это вещества, имеющие одинаковый качественный и количественный состав, но отличающиеся по своему строению и свойствам Изомерия- это явление существования веществ с одинаковым качественным и количественным составом, но отличающимся по своему строению и свойствам
Изомеры l l Изомеры - это вещества, имеющие одинаковый качественный и количественный состав, но отличающиеся по своему строению и свойствам Изомерия- это явление существования веществ с одинаковым качественным и количественным составом, но отличающимся по своему строению и свойствам
 Примеры изомеров l Для вещества с общей молекулярной формулой С 4 Н 10 существуют 2 изомера: СН 3 -СН 2 -СН 3 (н - бутан, t кип. =-0, 50 С) СН 3 - СН -СН 3 | СН 3 (изобутан, t кип. =-11, 70 С)
Примеры изомеров l Для вещества с общей молекулярной формулой С 4 Н 10 существуют 2 изомера: СН 3 -СН 2 -СН 3 (н - бутан, t кип. =-0, 50 С) СН 3 - СН -СН 3 | СН 3 (изобутан, t кип. =-11, 70 С)
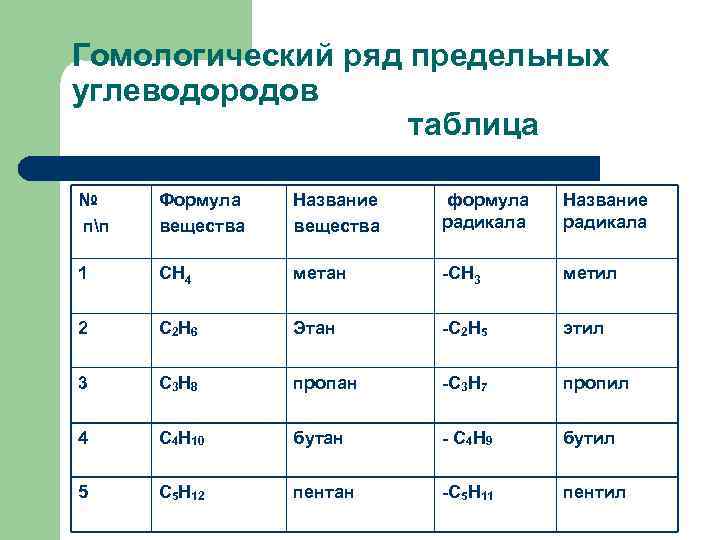 Гомологический ряд предельных углеводородов таблица № пп Формула вещества Название вещества формула радикала Название радикала 1 СН 4 метан -СН 3 метил 2 С 2 Н 6 Этан -С 2 Н 5 этил 3 С 3 Н 8 пропан -С 3 Н 7 пропил 4 С 4 Н 10 бутан - С 4 Н 9 бутил 5 С 5 Н 12 пентан -С 5 Н 11 пентил
Гомологический ряд предельных углеводородов таблица № пп Формула вещества Название вещества формула радикала Название радикала 1 СН 4 метан -СН 3 метил 2 С 2 Н 6 Этан -С 2 Н 5 этил 3 С 3 Н 8 пропан -С 3 Н 7 пропил 4 С 4 Н 10 бутан - С 4 Н 9 бутил 5 С 5 Н 12 пентан -С 5 Н 11 пентил
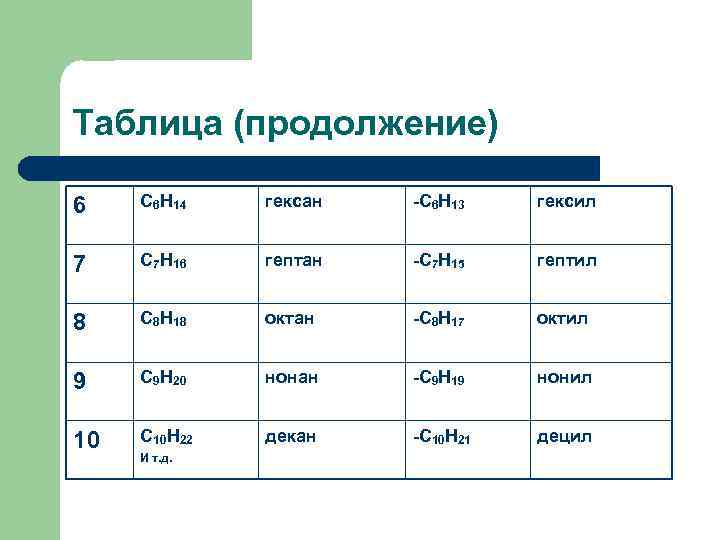 Таблица (продолжение) 6 С 6 Н 14 гексан -С 6 Н 13 гексил 7 С 7 Н 16 гептан -С 7 Н 15 гептил 8 С 8 Н 18 октан -С 8 Н 17 октил 9 С 9 Н 20 нонан -С 9 Н 19 нонил 10 С 10 Н 22 декан -С 10 Н 21 децил И т. д.
Таблица (продолжение) 6 С 6 Н 14 гексан -С 6 Н 13 гексил 7 С 7 Н 16 гептан -С 7 Н 15 гептил 8 С 8 Н 18 октан -С 8 Н 17 октил 9 С 9 Н 20 нонан -С 9 Н 19 нонил 10 С 10 Н 22 декан -С 10 Н 21 децил И т. д.
 Гомологи l l Гомологи – вещества, расположенные в порядке возрастания относительных молекулярных масс, сходных по строению и свойствам, но отличающихся друг от друга по составу на одну или несколько групп -СН 2 Гомологический ряд- ряд веществ, расположенных в порядке возрастания относительных молекулярных масс, сходных по строению и свойствам, но отличающихся друг от друга по составу на одну или несколько групп -СН 2 -
Гомологи l l Гомологи – вещества, расположенные в порядке возрастания относительных молекулярных масс, сходных по строению и свойствам, но отличающихся друг от друга по составу на одну или несколько групп -СН 2 Гомологический ряд- ряд веществ, расположенных в порядке возрастания относительных молекулярных масс, сходных по строению и свойствам, но отличающихся друг от друга по составу на одну или несколько групп -СН 2 -
 Физические свойства предельных углеводородов l l l Агрегатное состояние: первые четыре члена гомологического ряда(С 1 -С 4) – газы, С 5 -С 15 - жидкости, С 16 и более тяжелые – твердые вещества Температура кипения и плавления постепенно увеличиваются с ростом молекулярной массы вещества Растворимость в воде - плохая
Физические свойства предельных углеводородов l l l Агрегатное состояние: первые четыре члена гомологического ряда(С 1 -С 4) – газы, С 5 -С 15 - жидкости, С 16 и более тяжелые – твердые вещества Температура кипения и плавления постепенно увеличиваются с ростом молекулярной массы вещества Растворимость в воде - плохая
 Нахождение в природе и получение предельных углеводородов Предельные углеводороды встречаются: √ в природном газе (98%- метан); √ в попутном нефтяном газе (С 1 -С 6); ; √ в нефти (С 5 -С 50); √ в каменном угле Получают их из природного сырья.
Нахождение в природе и получение предельных углеводородов Предельные углеводороды встречаются: √ в природном газе (98%- метан); √ в попутном нефтяном газе (С 1 -С 6); ; √ в нефти (С 5 -С 50); √ в каменном угле Получают их из природного сырья.
 Химические свойства предельных углеводородов Для предельных углеводородов характерны следующие химические реакции: √ замещения (по свободно-радикальному механизму); √ окисления (полное и неполное); √ разложения (крекинг, дегидрирование); √ изомеризации. Для предельных углеводородов совсем не характерны реакции присоединения.
Химические свойства предельных углеводородов Для предельных углеводородов характерны следующие химические реакции: √ замещения (по свободно-радикальному механизму); √ окисления (полное и неполное); √ разложения (крекинг, дегидрирование); √ изомеризации. Для предельных углеводородов совсем не характерны реакции присоединения.
 Реакции замещения 1. Реакция хлорирования на свету 1 2 3 4 СН 4 →СН 3 Сl →СН 2 Сl 2 →СН Сl 3 →С Сl 4 СН 4 +Cl 2 → СН 3 Сl (первая стадия) хлорметан 2. СН 3 Сl +Cl 2 → СН 2 Сl 2 (вторая стадия) дихлорметан 3. СН 2 Сl 2 +Cl 2 → СН Сl 3 (третья стадия) тр ихлорметан 4. СН Сl 3 +Cl 2 → С Сl 4 (четвертая стадия) тетрахлорметан 1. 2. Реакция нитрования(реакция Коновалова) СН 4 +НNO 3→ СН 3 NO 2 +H 2 O
Реакции замещения 1. Реакция хлорирования на свету 1 2 3 4 СН 4 →СН 3 Сl →СН 2 Сl 2 →СН Сl 3 →С Сl 4 СН 4 +Cl 2 → СН 3 Сl (первая стадия) хлорметан 2. СН 3 Сl +Cl 2 → СН 2 Сl 2 (вторая стадия) дихлорметан 3. СН 2 Сl 2 +Cl 2 → СН Сl 3 (третья стадия) тр ихлорметан 4. СН Сl 3 +Cl 2 → С Сl 4 (четвертая стадия) тетрахлорметан 1. 2. Реакция нитрования(реакция Коновалова) СН 4 +НNO 3→ СН 3 NO 2 +H 2 O
 Реакции окисления 1. Полное окисление – горение СН 4 + 2 О 2→СО 2 +2 Н 2 О +Q 2. Неполное окисление СН 4 + [О] →метиловый спирт, м метаналь (формальдегид), метановая (муравьиная)кислота
Реакции окисления 1. Полное окисление – горение СН 4 + 2 О 2→СО 2 +2 Н 2 О +Q 2. Неполное окисление СН 4 + [О] →метиловый спирт, м метаналь (формальдегид), метановая (муравьиная)кислота
 Реакции разложения 1. крекинг (реакции идут при нагревании с разрывом углеродной цепи) 0 1500 С СН 4→ 2 С+2 Н 2 С 4 Н 10→ С 2 Н 4+С 2 Н 6 2. отщепление молекулы водорода (дегидрирование) С 2 Н 6→ С 2 Н 4+Н 2
Реакции разложения 1. крекинг (реакции идут при нагревании с разрывом углеродной цепи) 0 1500 С СН 4→ 2 С+2 Н 2 С 4 Н 10→ С 2 Н 4+С 2 Н 6 2. отщепление молекулы водорода (дегидрирование) С 2 Н 6→ С 2 Н 4+Н 2
 Реакции изомеризации В реакциях изомеризации не меняется количественный и качественный состав веществ, меняется лишь их пространственное строение кат. СН 3 -СН 2 -СН 3, → СН 3 - СН -СН 3 ! СН 3 н - бутан изобутан
Реакции изомеризации В реакциях изомеризации не меняется количественный и качественный состав веществ, меняется лишь их пространственное строение кат. СН 3 -СН 2 -СН 3, → СН 3 - СН -СН 3 ! СН 3 н - бутан изобутан
 Применение предельных углеводородов Предельные углеводороды находят свое применение как: √ топливо (бензин, керосин, мазут и др. ); √ растворители ; √ химическое сырье (для получения алкенов ацетилена, бутадиена и др. ); √ сырье для синтеза ( водорода, сажи, парафина, сероуглерода и др. )
Применение предельных углеводородов Предельные углеводороды находят свое применение как: √ топливо (бензин, керосин, мазут и др. ); √ растворители ; √ химическое сырье (для получения алкенов ацетилена, бутадиена и др. ); √ сырье для синтеза ( водорода, сажи, парафина, сероуглерода и др. )


