9b3a31fbf112b6f1fb947f64f2390523.ppt
- Количество слайдов: 38
 Углеводороды
Углеводороды
 l В начале XIX века в Англии стали модными плащи из водонепроницаемой ткани, называемые макинтошами. Это название они получили в честь английского химика и изобретателя Ч. Макинтоша, предложившего пропитывать плащевую ткань раствором натурального каучука. Однако на солнце такие плащи становились липкими, а в морозную погоду – ломкими. Предложите свой способ устранения этих недостатков, повторив тем самым открытие другого выдающегося англичанина – Ч. Гудьира.
l В начале XIX века в Англии стали модными плащи из водонепроницаемой ткани, называемые макинтошами. Это название они получили в честь английского химика и изобретателя Ч. Макинтоша, предложившего пропитывать плащевую ткань раствором натурального каучука. Однако на солнце такие плащи становились липкими, а в морозную погоду – ломкими. Предложите свой способ устранения этих недостатков, повторив тем самым открытие другого выдающегося англичанина – Ч. Гудьира.
 Промышленный способ получения бутадиена-1, 3 2 С 2 Н 5 -ОН СН 2=СН-СН=СН 2 + 2 Н 2 О+ Н 2
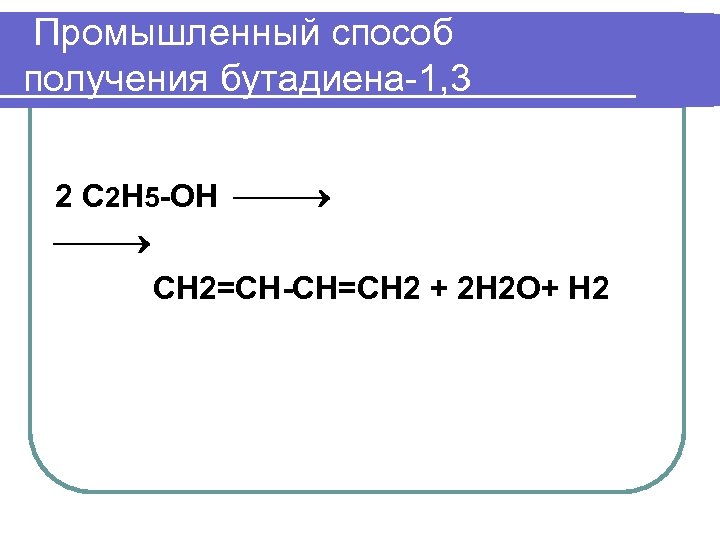
Промышленный способ получения бутадиена-1, 3 2 С 2 Н 5 -ОН СН 2=СН-СН=СН 2 + 2 Н 2 О+ Н 2
 Назовите имя отечественного химика. академика
Назовите имя отечественного химика. академика
 Чем являются между собой данные углеводороды? l С 4 Н 6 СН 2=СН-СН=СН 2 бутадиен-1, 3 l С 5 Н 8 СН 2=СН-СН 3 пентадиен-1, 3
Чем являются между собой данные углеводороды? l С 4 Н 6 СН 2=СН-СН=СН 2 бутадиен-1, 3 l С 5 Н 8 СН 2=СН-СН 3 пентадиен-1, 3
 Алкины
Алкины
 l Углеводороды, в молекулах которых содержится одна тройная углеродная связь С С, называются ацетиленовыми углеводородами или алкинами.
l Углеводороды, в молекулах которых содержится одна тройная углеродная связь С С, называются ацетиленовыми углеводородами или алкинами.
 Гомологический ряд алкинов: l С 2 Н 2 НС СН ацетилен l С 3 Н 4 l С 4 Н 6 НС С-СН 3 НС С-СН 2 -СН 3 С 4 Н 6 СН 3 -С С-СН 3 этин, пропин, бутин-1, бутин-2
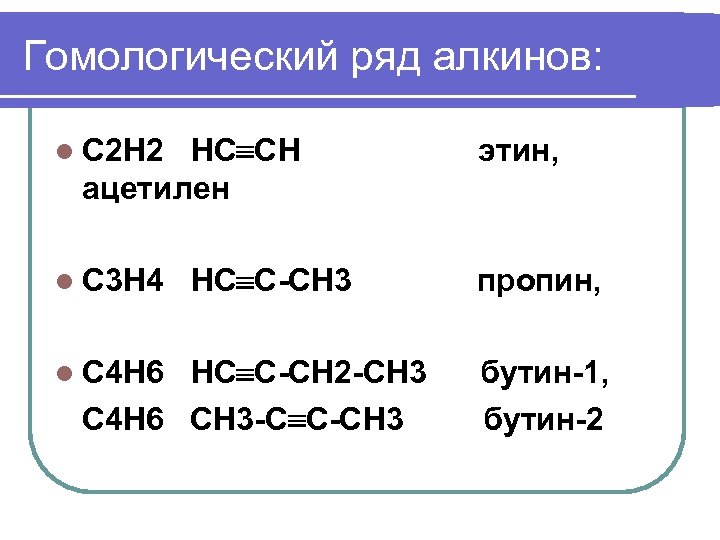
Гомологический ряд алкинов: l С 2 Н 2 НС СН ацетилен l С 3 Н 4 l С 4 Н 6 НС С-СН 3 НС С-СН 2 -СН 3 С 4 Н 6 СН 3 -С С-СН 3 этин, пропин, бутин-1, бутин-2
 l Ацетиленовые углеводороды (алкины) содержат в молекуле одну тройную углерод-углеродную связь С С и имеют общую формулу Сn. H 2 n-2.
l Ацетиленовые углеводороды (алкины) содержат в молекуле одну тройную углерод-углеродную связь С С и имеют общую формулу Сn. H 2 n-2.
 Получение ацетилена Ацетилен получают взаимодействием карбида кальция с водой или неполным разложением метана: Ca. C 2 + 2 H 2 O = C 2 H 2 + Ca(OH)2 2 СН 4 С 2 Н 2 + 3 Н 2
Получение ацетилена Ацетилен получают взаимодействием карбида кальция с водой или неполным разложением метана: Ca. C 2 + 2 H 2 O = C 2 H 2 + Ca(OH)2 2 СН 4 С 2 Н 2 + 3 Н 2
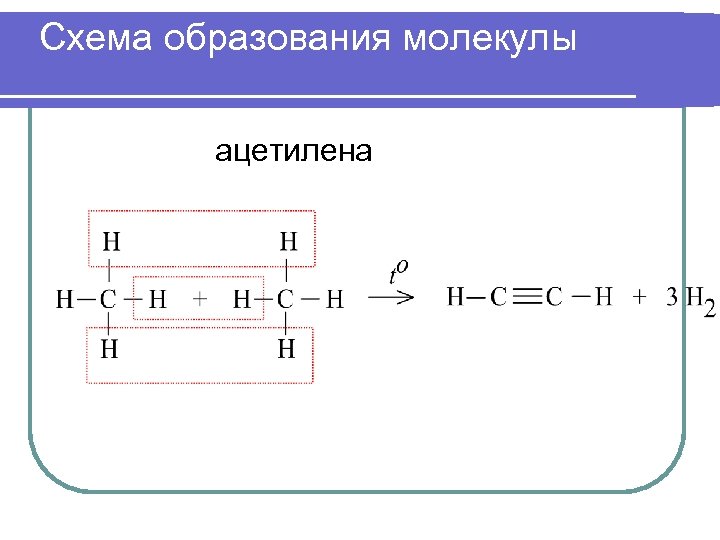 Схема образования молекулы ацетилена
Схема образования молекулы ацетилена
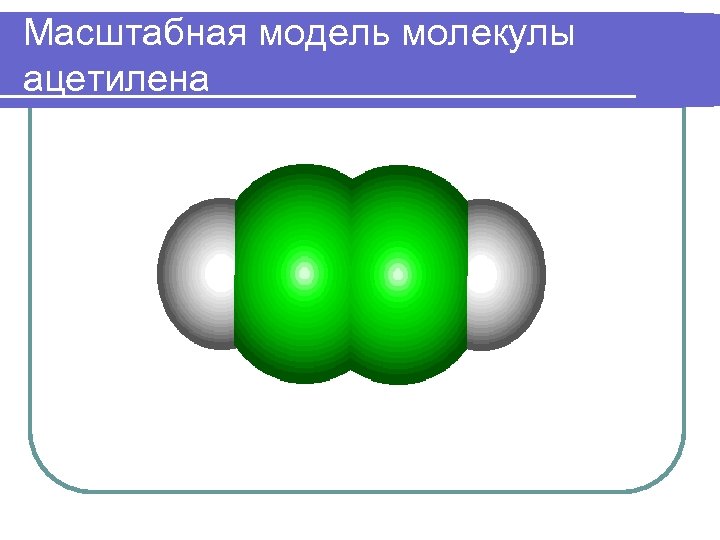 Масштабная модель молекулы ацетилена
Масштабная модель молекулы ацетилена
 l На воздухе ацетилен горит коптящим светящимся пламенем
l На воздухе ацетилен горит коптящим светящимся пламенем
 Ацетилен при горении в чистом кислороде дает очень горячее пламя. Его температура достигает 4000 о. С ! Сравните: температура плавления железа 1540 о. С.
Ацетилен при горении в чистом кислороде дает очень горячее пламя. Его температура достигает 4000 о. С ! Сравните: температура плавления железа 1540 о. С.
 Вывод очевиден: пламенем ацетилена можно резать и сваривать металлы. Так, спустя 60 лет после своего открытия, ацетилен обрел одну из самых главных своих профессий.
Вывод очевиден: пламенем ацетилена можно резать и сваривать металлы. Так, спустя 60 лет после своего открытия, ацетилен обрел одну из самых главных своих профессий.

 Химические свойства : l 1) Горение: 2 С 2 Н 2 + 5 О 2 4 СО 2 + 2 Н 2 О + + Q
Химические свойства : l 1) Горение: 2 С 2 Н 2 + 5 О 2 4 СО 2 + 2 Н 2 О + + Q
 l Для алкинов, как непредельных углеводородов, характерны реакции присоединения. l Как непредельный углеводород, ацетилен обесцвечивает: (а) бромную воду, (б) раствор перманганата калия.
l Для алкинов, как непредельных углеводородов, характерны реакции присоединения. l Как непредельный углеводород, ацетилен обесцвечивает: (а) бромную воду, (б) раствор перманганата калия.
 Химические свойства: В этом легко убедиться, проделав опыт. В прибор для получения газов наливаем около 1 мл воды и помещаем в неё карбид кальция. Выделяющийся газ пропускаем через раствор перманганата калия.
Химические свойства: В этом легко убедиться, проделав опыт. В прибор для получения газов наливаем около 1 мл воды и помещаем в неё карбид кальция. Выделяющийся газ пропускаем через раствор перманганата калия.
 Химические свойства: 2) С бромной водой НС СН + Br 2 CHBr=CHBr 1, 2 -дибромэтен и далее: CHBr=CHBr + Br 2 CHBr 2 -CHBr 2 1, 1, 2, 2 тетрабромэтан
Химические свойства: 2) С бромной водой НС СН + Br 2 CHBr=CHBr 1, 2 -дибромэтен и далее: CHBr=CHBr + Br 2 CHBr 2 -CHBr 2 1, 1, 2, 2 тетрабромэтан
 Химические свойства: 3). Аналогично будут протекать и другие реакции присоединения, например, гидрирование по схеме: С 2 Н 2 С 2 Н 4 С 2 Н 6 (смоделируем последовательно эти реакции)
Химические свойства: 3). Аналогично будут протекать и другие реакции присоединения, например, гидрирование по схеме: С 2 Н 2 С 2 Н 4 С 2 Н 6 (смоделируем последовательно эти реакции)
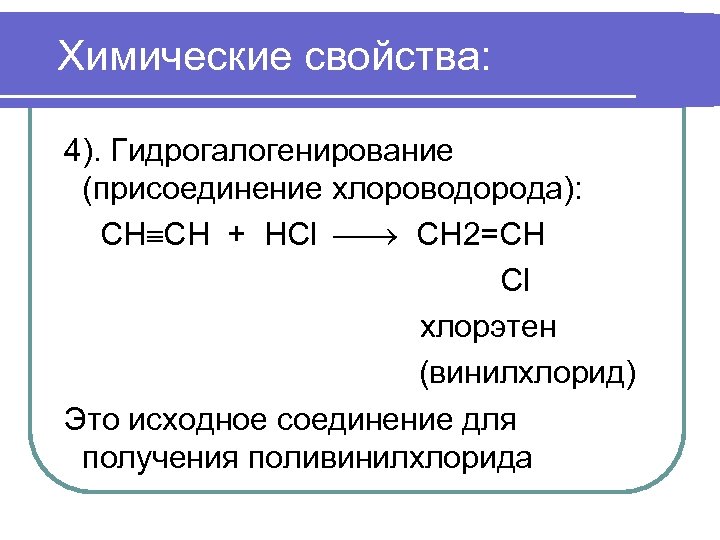 Химические свойства: 4). Гидрогалогенирование (присоединение хлороводорода): СН СН + HCl CH 2=CH Cl хлорэтен (винилхлорид) Это исходное соединение для получения поливинилхлорида
Химические свойства: 4). Гидрогалогенирование (присоединение хлороводорода): СН СН + HCl CH 2=CH Cl хлорэтен (винилхлорид) Это исходное соединение для получения поливинилхлорида
 Схема полимеризации винилхлорида в поливинилхлорид дана на странице 48. 1. Рассмотрев схему, попробуйте самостоятельно записать уравнение реакции. 2. Используя рисунок, познакомьтесь с применения поливинилхлорида.
Схема полимеризации винилхлорида в поливинилхлорид дана на странице 48. 1. Рассмотрев схему, попробуйте самостоятельно записать уравнение реакции. 2. Используя рисунок, познакомьтесь с применения поливинилхлорида.
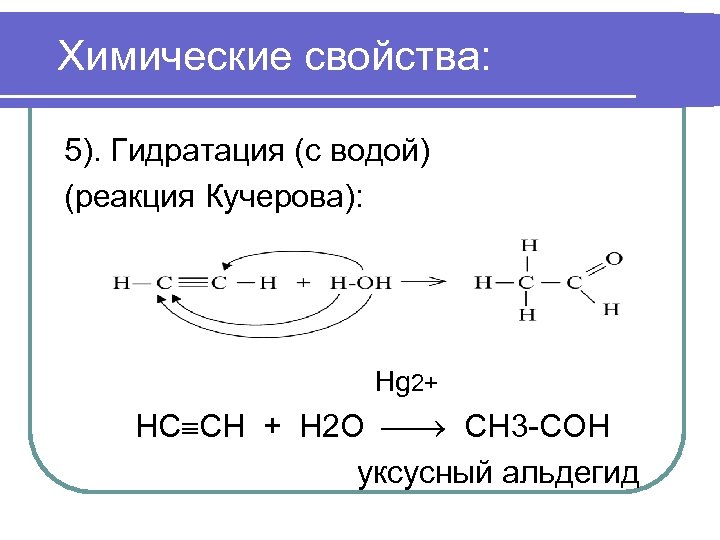 Химические свойства: 5). Гидратация (с водой) (реакция Кучерова): Hg 2+ НС СН + Н 2 О СН 3 -СОН уксусный альдегид
Химические свойства: 5). Гидратация (с водой) (реакция Кучерова): Hg 2+ НС СН + Н 2 О СН 3 -СОН уксусный альдегид
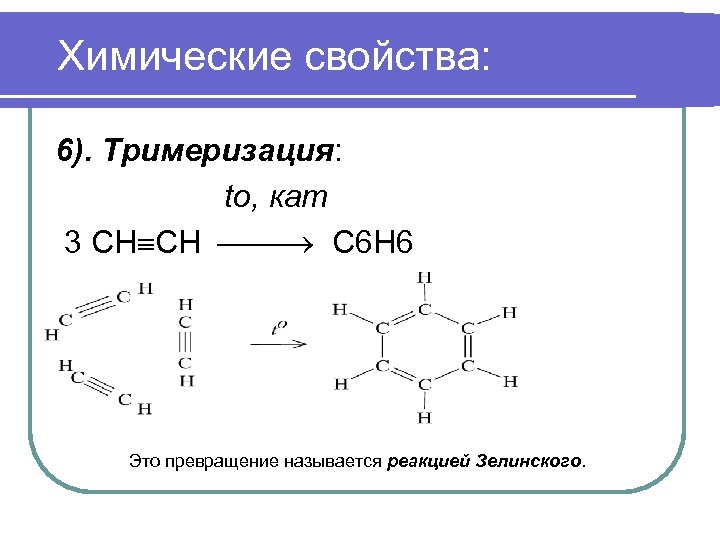 Химические свойства: 6). Тримеризация: to, кат 3 СН СН С 6 Н 6 Это превращение называется реакцией Зелинского.
Химические свойства: 6). Тримеризация: to, кат 3 СН СН С 6 Н 6 Это превращение называется реакцией Зелинского.
 Решить задачу (устно) По термохимическому уравнению реакции горения ацетилена С 2 Н 2 + 2, 5 О 2 2 СО 2+ Н 2 О+1300 к. Дж вычислите количество теплоты, которое выделится при сжигании 2 моль ацетилена (у. н. ).
Решить задачу (устно) По термохимическому уравнению реакции горения ацетилена С 2 Н 2 + 2, 5 О 2 2 СО 2+ Н 2 О+1300 к. Дж вычислите количество теплоты, которое выделится при сжигании 2 моль ацетилена (у. н. ).
 Задачи с нестандартными формулировками l Предложите способ, с помощью которого можно различить этан и ацетилен.
Задачи с нестандартными формулировками l Предложите способ, с помощью которого можно различить этан и ацетилен.
 Задачи с нестандартными l. Можно ли однозначно сказать, какому классу углеводородов формулировками принадлежит вещество с формулой С 4 Н 6, зная, что ей соответствует общая формула Сn. H 2 n-2.
Задачи с нестандартными l. Можно ли однозначно сказать, какому классу углеводородов формулировками принадлежит вещество с формулой С 4 Н 6, зная, что ей соответствует общая формула Сn. H 2 n-2.
 Задача Относительная молекулярная масса гомолога ацетилена равна 68. Определите его молекулярную формулу.
Задача Относительная молекулярная масса гомолога ацетилена равна 68. Определите его молекулярную формулу.
 Проверьте решение Cn. H 2 n-2 = 68 Ar(C)=12 Ar(H)=1 12 n+2 n-2 =68 14 n =70 n = 70 : 14= 5 Ответ: C 5 H 8
Проверьте решение Cn. H 2 n-2 = 68 Ar(C)=12 Ar(H)=1 12 n+2 n-2 =68 14 n =70 n = 70 : 14= 5 Ответ: C 5 H 8
 Мы узнали: l Ацетиленовые углеводороды (алкины) содержат в молекуле одну … углерод-углеродную связь С С и имеют общую формулу … l Алкины и алкадиены – межклассовые. . .
Мы узнали: l Ацетиленовые углеводороды (алкины) содержат в молекуле одну … углерод-углеродную связь С С и имеют общую формулу … l Алкины и алкадиены – межклассовые. . .
 Мы узнали: l Ацетилен получают взаимодействием карбида кальция с … или неполным разложением …
Мы узнали: l Ацетилен получают взаимодействием карбида кальция с … или неполным разложением …
 Мы узнали: l Для алкинов, как непредельных углеводородов, характерны реакции … , многие из которых протекают ступенчато.
Мы узнали: l Для алкинов, как непредельных углеводородов, характерны реакции … , многие из которых протекают ступенчато.
 Мы узнали: l Как непредельный углеводород, ацетилен обесцвечивает: l (а) … воду; l (б) раствор. . . …
Мы узнали: l Как непредельный углеводород, ацетилен обесцвечивает: l (а) … воду; l (б) раствор. . . …
 Мы узнали: l Ацетилен – важное сырье для получения винилхлорида, уксусного альдегида, используется для сварки и резки металлов.
Мы узнали: l Ацетилен – важное сырье для получения винилхлорида, уксусного альдегида, используется для сварки и резки металлов.
 Задание на дом: 1. Параграф 6, вопросы 4 и 6. Для имеющих ИНТЕРНЕТ: найти и оформить материал об истории появления именных реакций Зелинского и Кучерова;
Задание на дом: 1. Параграф 6, вопросы 4 и 6. Для имеющих ИНТЕРНЕТ: найти и оформить материал об истории появления именных реакций Зелинского и Кучерова;
 Проверьте карточки 1 вариант: l 1 2 3 4 5 6 7 l. А В Б В В Б А 2 вариант: l 1 2 3 4 5 6 l. Б Б А В Б Б 8 А 7 А 8 Б
Проверьте карточки 1 вариант: l 1 2 3 4 5 6 7 l. А В Б В В Б А 2 вариант: l 1 2 3 4 5 6 l. Б Б А В Б Б 8 А 7 А 8 Б
 Карточка самооценки(приложение 3) Правильно данное определение ___1 Самостоятельный ответ на вопрос - 2 Ответ у доски ________2 Эксперимент, моделирование ____ 1 Правильно заполненная карточка __3 Активное слушание _______ 1
Карточка самооценки(приложение 3) Правильно данное определение ___1 Самостоятельный ответ на вопрос - 2 Ответ у доски ________2 Эксперимент, моделирование ____ 1 Правильно заполненная карточка __3 Активное слушание _______ 1


