 Углерод, аллотропные модификации
Углерод, аллотропные модификации
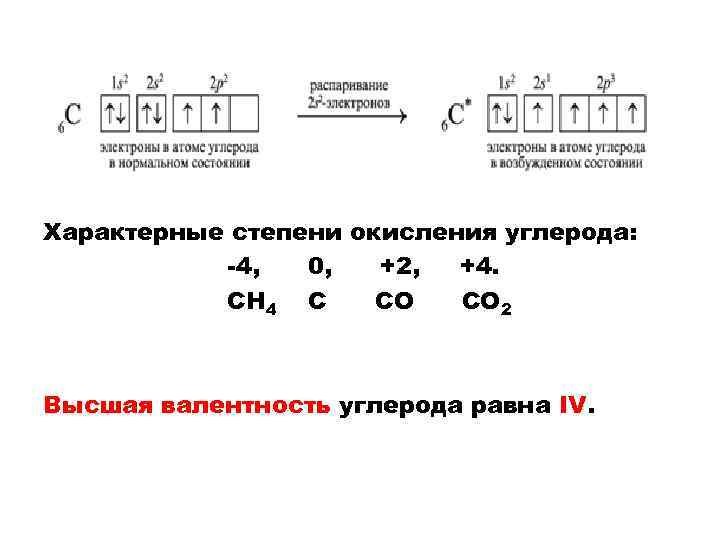 Характерные степени окисления углерода: -4, 0, +2, +4. СН 4 С СО СО 2 Высшая валентность углерода равна IV.
Характерные степени окисления углерода: -4, 0, +2, +4. СН 4 С СО СО 2 Высшая валентность углерода равна IV.
 Нахождение в природе. Углерод в природе встречается: Ø в виде простых веществ – графита и алмаза Ø в составе минералов – карбонатов кальция, магния, железа и др. Ø В воздухе – СО 2 (углекислый газ).
Нахождение в природе. Углерод в природе встречается: Ø в виде простых веществ – графита и алмаза Ø в составе минералов – карбонатов кальция, магния, железа и др. Ø В воздухе – СО 2 (углекислый газ).
 Аллотропные модификации углерода 1) Графит – темносерое тугоплавкое вещество с металлическим блеском и низкой твердостью, проводит электрический ток.
Аллотропные модификации углерода 1) Графит – темносерое тугоплавкое вещество с металлическим блеском и низкой твердостью, проводит электрический ток.
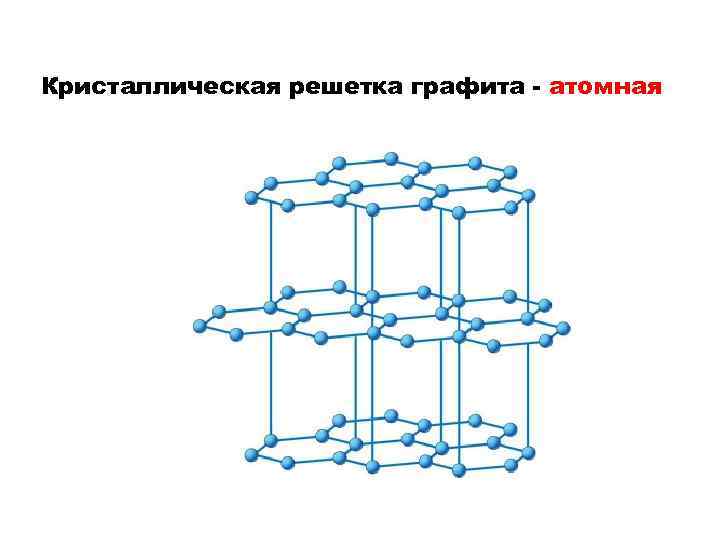 Кристаллическая решетка графита - атомная
Кристаллическая решетка графита - атомная
 2) Алмаз – бесцветное тугоплавкое вещество, с самой высокой твердостью из всех природных веществ.
2) Алмаз – бесцветное тугоплавкое вещество, с самой высокой твердостью из всех природных веществ.
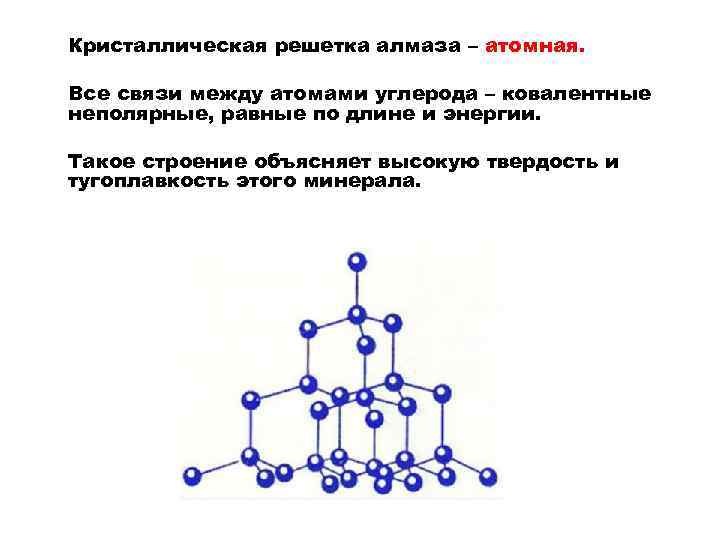 Кристаллическая решетка алмаза – атомная. Все связи между атомами углерода – ковалентные неполярные, равные по длине и энергии. Такое строение объясняет высокую твердость и тугоплавкость этого минерала.
Кристаллическая решетка алмаза – атомная. Все связи между атомами углерода – ковалентные неполярные, равные по длине и энергии. Такое строение объясняет высокую твердость и тугоплавкость этого минерала.
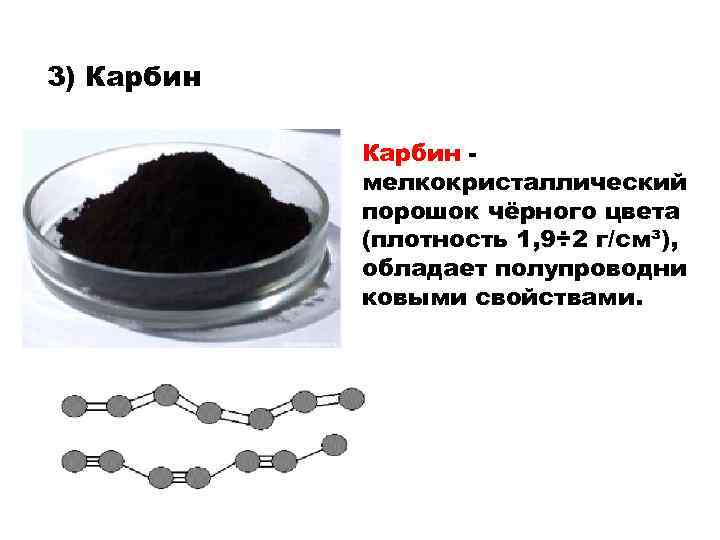 3) Карбин мелкокристаллический порошок чёрного цвета (плотность 1, 9÷ 2 г/см³), обладает полупроводни ковыми свойствами.
3) Карбин мелкокристаллический порошок чёрного цвета (плотность 1, 9÷ 2 г/см³), обладает полупроводни ковыми свойствами.
 4) Фуллерен молекулярное соединение, представляющее собой выпуклые замкнутые многогранники, составленные из чётного числа трёх координированных атомов углерода.
4) Фуллерен молекулярное соединение, представляющее собой выпуклые замкнутые многогранники, составленные из чётного числа трёх координированных атомов углерода.