инфекция 1.ppt
- Количество слайдов: 54

Учение об инфекции Лектор: ассистент каф. микробиологии Черепанова Т. А.

Задача инфектологии состоит в том, чтобы раскрыть и показать роль участников этого очень сложного процесса и обеспечить правильное воздействие на развитие и исход инфекционного заболевания. Врач должен эффективно влиять на возбудителя, назначая рациональное антибактериальное лечение, и влиять на организм человека, мобилизуя его защитные механизмы.

«Инфекция» - от латинского inficio –вношу что –либо вредное, заражаю, и поздне-латинского infectio - заражение» Под термином «инфекция» правильнее понимать процесс взаимодействия между макро- и микроорганизмом, протекающий в конкретных условиях внешней среды (в том числе социальной).

Болезнетворность определяется патогенностью и вирулентностью микробов зависит от определенных обстоятельств: • дозы инфекта, • пути инфицирования, • способности выживать во внешней среде, • наличия восприимчивого организма, лишенного видового иммунитета и т. д.

Патогенность (pathos- страдание, болезнь; genes –рождающий) — потенциальный признак, который раскрывается при определенном стечении обстоятельств. Их должно быть много для одних микробов и меньше для других. Этим определяется позиция на шкале болезнетворности — от безвредных комменсалов до возбудителей особоопасных инфекций.

Микробы делятся на: 1. непатогенные 2. патогенные 3. условно-патогенные. • Безвредность первых чаще всего абсолютна. • Патогенные виды облигатно болезнетворны. • Реализация условной патогенности решается в индивидуальных системах макро—микроорганизм.

Патогенные микроорганизмы опасны для практически здоровых людей. К ним относятся возбудители классических инфекционных заболеваний, с которыми имеют дело врачи специализированных (инфекционных) стационаров. Они всегда возникают при экзогенном заражении и обычно не привязаны к госпитальным условиям, так как иммуносупрессия не обязательна для их развития.

Способность патогенных микроорганизмов поражать здоровых людей является причиной групповой заболеваемости, вплоть до эпидемий и пандемий. • Высокая контагиозность микроба, • способность вызывать заболевания с тяжелым (опасным для жизни) течением определяет принадлежность его к возбудителям особо опасных инфекций.

Патогенность отражает болезнетворность на уровне вида. Признак подвержен внутривидовым колебаниям, т. е. неодинаково выражен у разных штаммов (в генетической интерпретации — клонов) микроорганизмов. Вирулентность (от лат. Virulentus –ядовитый), которое отражает степень болезнетворности штаммов внутри патогенного вида. Для количественного выражения вирулентности микроорганизмов используют три метода: • определение Dlm (dosis letalis minima) • Dlm 50 • Dcl (Dosis certa letalis – безусловно летальная доза)

Все признаки патогенности контролируются генами. У бактерий обнаружены три типа генов, осуществляющих контроль синтеза факторов патогенности: • гены собственной хромосомы; • гены, привнесенные плазмидами; • гены, привнесенные умеренными фагами. Включение и выключение таких генов ведет к появлению более или менее агрессивных клонов.

Болезнетворность штаммов (клонов) патогенных бактерий колеблется в широких пределах. Кроме генетически закрепленной клонированности. перетасовки генетических фрагментов, потери и приобретения подвижных генов (транспозонов, плазмид), мутаций, это связано с особенностями экспрессии генов, детерминирующих вирулентность. У ряда бактерий обнаружен универсальный механизм, контролирующий активность генов вирулентности. Включение — выключение таких генов ведет к появлению более или менее агрессивных клонов, отражая реакцию на среду обитания (температура, р. Н, концентрация кислорода, содержание кальция и др. ). Например, коклюшная палочка, попадая в бронхи, начинает продуцировать комплекс токсинов, но, подвергаясь «выселению» в носовые ходы, где температура гораздо ниже, трансформируется в невирулентный фенотип. Легко меняют свой фенотип иерсинии, в частности Y. enterocolitica: развиваясь при 37°С, она продуцирует комплекс белков наружной мембраны, сидерофоры, ферменты, которые повышают колонизирующую активность бактерий, усиливают их инвазивность, устойчивость к комплементу и фагоцитозу. Система включает сенсорный аппарат, воспринимающий сигналы из внешней среды, и внутриклеточные медиаторы, которые непосредственно выходят на хромосомные или плазмидные гены, меняя их транскрипцию. Принцип состоит в одновременной перестройке группы «вирулентных» генов (регулона) в ответ на общий стимул. В других ситуациях каждый из таких генов может экспрессироваться

Болезнетворность — многофакторный признак. Базисные факторы, определяющие болезнетворность: 1. способность к колонизации (заселению) зоны первичного инфицирования, т. е. входных ворот инфекции; 2. способность к инвазии, т. е. к выходу за пределы зоны первичной колонизации; 3. токсигенность; 4. способность к персистенции.

КОЛОНИЗАЦИЯ - закрепление (адгезия) и последующее размножение бактерий в зоне инфицирования. Для инфекции необходимыми этапами являются: • Преодоление колонизационной резистентности. • Подготовка участков для закрепления, обнажая клеточные рецепторы (например, при помощи нейраминидазы). • Вирусиндуцированная и цитокининдуцированная экспрессия эпителиальных рецепторов. • Использование дефектов в эпителиальном покрове. • Адсорбция на других бактериях, ранее обосновавшихся в данном биотопе, или взаимодействие с растворимыми белками (напр. , фибронектином).

Спектр бактериальных адгезинов обширен, определяя поливалентость феномена даже в масштабе одного вида. У грамотрицательных бактерий в адгезии участвуют микроворсинки (пили), белки и липополисахариды наружной мембраны. У грамположительных — белки клеточной стенки, липотейхоевые кислоты. У капсульных бактерий в адгезию включаются капсульные полисахариды. Адгезия создает предпосылки для размножения, является пусковым механизмом реализации патогенности бактерий. Чтобы добиться этого, они должны выстоять против биоцидных и биостатических факторов.

Среди паразитов слизистых оболочек распространена способность к продукции Ig. A-протеаз, которые расщепляют Ig. Aантитела. Многие бактерии нейтрализуют лизоцим, инактивируют оксиданты и другие потенциально вредные начала. Удивительной стойкостью, например, обладает Helicobacter pylori: он активно персистирует в желудке, нейтрализуя вокруг себя кислую среду благодаря высокой уреазной активности.

Один из базисных механизмов — конкуренция за железо. Его отсутствие гибельно для бактерий, так как блокируется построение окислительно-восстановительных ферментов. Ионы железа прочно связаны с белками хозяина, например, с ферритином, трансферрином, лактоферрином и гемоглобином. Бактерии пользуются разными (часто несколькими) способами, для того чтобы обеспечить себя этим важнейшим фактором роста. Они продуцируют сидерофоры, конкурируя с лактоферрином за ионы железа.

ИНВАЗИЯ Представляет собой факторы, с помощью которых бактерии проникают в клетку. • Внутриэпителиальная • Субэпителиальная • Внутрисосудистая (бактериемия) • Внутримакрофагальная.

Внутриэпителиальная инвазия Колонизация слизистых оболочек не всегда ограничивается их поверхностью. Патогенность ряда бактерий связана с проникновением (пенетрацией) в эпителиальные клетки, где они размножаются, вызывая повреждение (например, шигеллы, йерсинии, гонококк). Способность к пенетрации определяется особыми факторами, среди которых лучше всего охарактеризованы так называемые инвазины. Взаимодействуя с проадгезивными рецепторами клеток (интегринами), они индуцируют поглощение бактерий. На модели йерсиний (Y. pseudotuberculosis) идентифицирован ген инвазина, который передается непенетрирующему штамму кишечной палочки.

Субэпителиальная инвазия Нередко болезнетворность проявляется после размножения бактерий в субэпителиальных тканях. Фактически это та же колонизация, но уже иных тканей и в иных условиях. Разные бактерии неодинаково решают проблему прохождения через внешние покровы. Многие из них, особенно бактерии-оппортунисты, неспособны к обильной колонизации и активной пенетрации слизистых оболочек и кожи. Для этого они пользуются пассивной инвазией, проникая через повреждения эпителия, например, после травматичных врачебных процедур (абиогенная трансмиссия). Пассивная инвазия — практически единственный способ преодоления кожного барьера, так как не поврежденный эпидермис непроницаем для большинства бактерий.

Кроме микротравм и инородных тел микробы «научились» использовать кровососущих насекомых - биогенная трансмиссия. Вариантом пассивной, точнее спровоцированной, инвазии являются вторичные инфекции, которые развиваются на фоне вирусных поражений эпителия (например, бактериальные пневмонии при гриппе) или осложняют другие «первичные» бактериальные инфекции (например, коклюш, гонорею). Оказавшись во внутренней среде (под эпителиальным покровом), возбудители сталкиваются с еще более сложным набором факторов и механизмов иммунитета.

При стабилизации и начавшемся размножении бактерий главным антиинвазивным механизмом служит воспалительная реакция, которая обеспечивает мобилизацию и взаимодействие многих иммунитетных ресурсов. Центральным эффектором, нацеленным на уничтожение «вредных деятелей» , являются фагоциты, действующие в содружестве с гуморальными факторами — хемоаттрактантами и опсонинами. Отсюда первоочередная задача бактерий — задержать или ослабить фагоцитарную реакцию. Неслучайно, врожденные дефекты нейтрофилов и ассистирующих им факторов (комплемент, иммуноглобулины) чреваты серьезными осложнениями.

Бактерии оказывают сопротивление на всех этапах фагоцитоза—от хемотаксиса до внутрифагосомального уничтожения. Они располагают богатым тактическим арсеналом, который включает продукты, действующие на клетки и гуморальные факторы: • разрушают хемоаттрактанты (например, С 5 а) • продуцируют токсины, убивающие фагоциты (например, лейкоцидины золотистого стафилококка, фосфолипазы клостридий). • взаимодействие с фагоцитами блокируется капсулой и другими высокогидрофильными поверхностными структурами. • сорбируют белки хозяина, обретая нечто вроде псевдокапсулы (например, фибриновая пленка коагулазопозитивных стафилококков).

• В фагосомах блокируют их слияние с лизосомами • лизируют фагосомы фосфолипазами, «ускользая» в цитоплазму • ослабляют закисление среды внутри фагосом • устойчивы к биоцидным факторам фагоцитов, сохраняя жизнеспособность даже в активированных макрофагах. Внутри фаголизосом бактерии инактивируют супероксиданион (за счет супероксиддисмутазы), подавляют действие Н 2 О 2 (за счет каталазы), экранируют собственную ДНК от оксидантов (антиоксидантные белки) • индукцируют апоптоз зараженных макрофагов.

Апоптозные макрофаги секретируют флогогенные цитокины, поддерживая и расширяя зону повреждения. В расширении зоны инвазии участвуют и бактериальные ферменты, которые разрушают основное вещество соединительной ткани и базальную мембрану эндотелия (гиалуронидаза, эластаза, коллагеназа), устраняют механический барьер из сгустков фибрина (фибринолизин), разжижают гнойный экссудат (ДНК-аза, протеиназы).

Внутрисосудистая инвазия (бактериемия) Попав в кровяное русло, бактерии быстро погибают или фагоцитируются макрофагами, некоторые из них в этих условиях выживают. А в ряде случаев бактериемия является обязательной фазой инфекционного процесса (возбудители брюшного тифа, менингита, бруцеллеза и др. ). • Бактерии способны противостоять комплементу (особенно важно для грамотрицательных форм высокочувствительных к литическому действию МАК). Без поддержки антител комплемент почти бессилен против инкапсулированных бактерий, благодаря структурным особенностям капсульных полисахаридов избегают активации комплемента по альтернативному (антителонезависимому) пути.

• Сальмонеллы и бруцеллы вносятся в кровь инфицированными лимфоцитами. • Золотистый стафилококк циркулирует внутри микротромбов, образующихся под влиянием коагулазы. В целом, выживание в крови создает дополнительные шансы для реализации патогенетического потенциала бактерий: находя подходящие условия внутри сосудистого русла (повреждение эндотелия, тромбы, внутрисосудистые протезы) или в тканях, они формируют вторичные очаги инфекции.

Внутримикрофагальная инфекция Фагоциты «сознательно» используются рядом бактерий, грибов и простейших как экологическая ниша, из которой они угрожают хозяину. •

ИНТОКСИКАЦИЯ является главным механизмом инфекционного процесса. Токсины - ведущий фактор болезнетворности бактерий - (греч. toxicon — яд) — продукты бактерий, которые в малых дозах вызывают структурные или функциональные повреждения клеток. Токсины бактерий принято делить на две категории: экзо - и эндотоксины.

ЭРНСТ ТЕОДОР РИТШЕЛ, ХЕЛЬМУТ БРАДЕ «Эндотоксины таят в себе такие загадки, что прямо-таки неправдоподобны. Как будто сама природа наделила их пороками и добродетелями точно в той пропорции, которая делает их неподдающимися самому пытливому исследованию. »

Эндотоксины входят в состав клеточной стенки, высвобождаются после разрушения бактерий и накапливаются в среде при отмирании клеток. Токсичность ЛПС (липид А отвечает за токсичность молекулы), пептидогликана, тейхоевых кислот чаще проявляется в условиях, обеспечивающих всасывание значительной порции токсических веществ (есть примеры катастрофического повышения чувствительности к ЛПС).
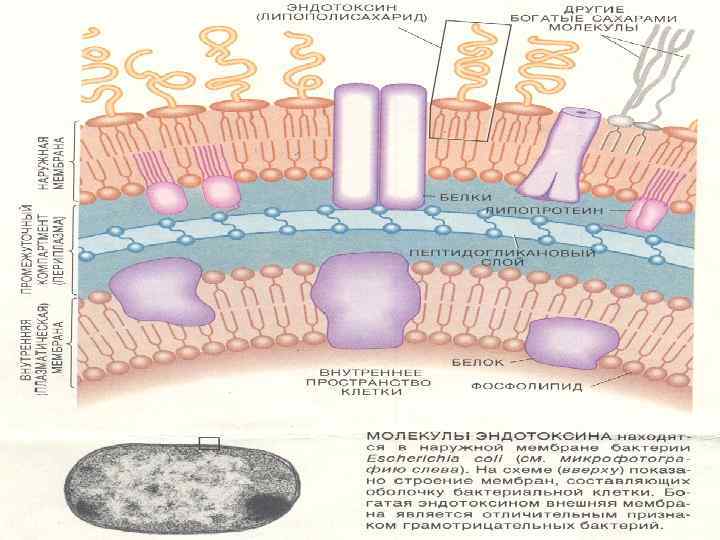

В патогенезе эндотоксиновой интоксикации задействовано множество мишеней, но далеко не все из них первичны. Центральным звеном являются макрофаги, с которых начинается каскад реакций, инициируемых ЛПС и функционально сходными продуктами грамположительных бактерий. Напрямую ЛПС-эндотоксины слабо стимулируют фагоциты, но их активность возрастает при взаимодействии с комплементом и ЛПС-связывающими белками плазмы. Главный из них принадлежит к семейству острофазовых белков и после связывания с липидным фрагментом ЛПС воспринимается клеточными рецепторами (CD 14), которых особенно много на мононуклеарных фагоцитах. Это сопровождается гиперпродукцией цитокинов (вторичных токсинов).
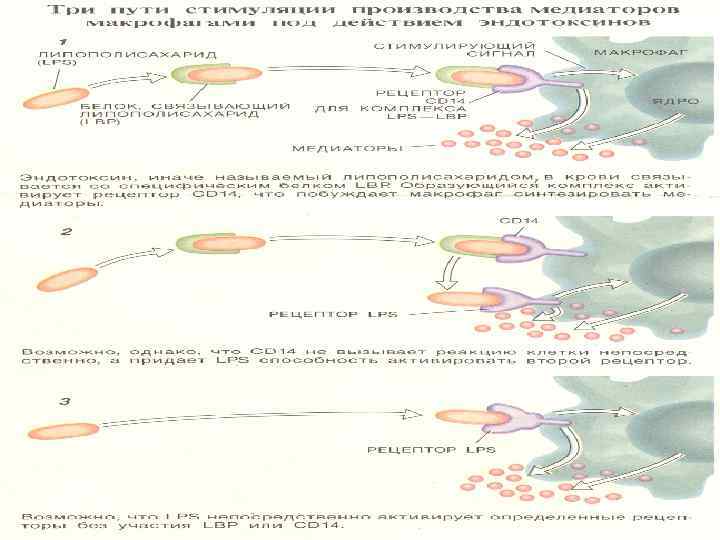

Макрофаги, стимулированные эндотоксином секретируют: • интерлейкины • фактор некроза опухолей • различные липиды (некоторые из них играют роль в повышении температуры и регулируют активность клеток иммунной системы) • свободные кислородные радикалы и оксид азота • факторы, активирующие свертывающую систему, вызывающие диссеминированное свертывание крови
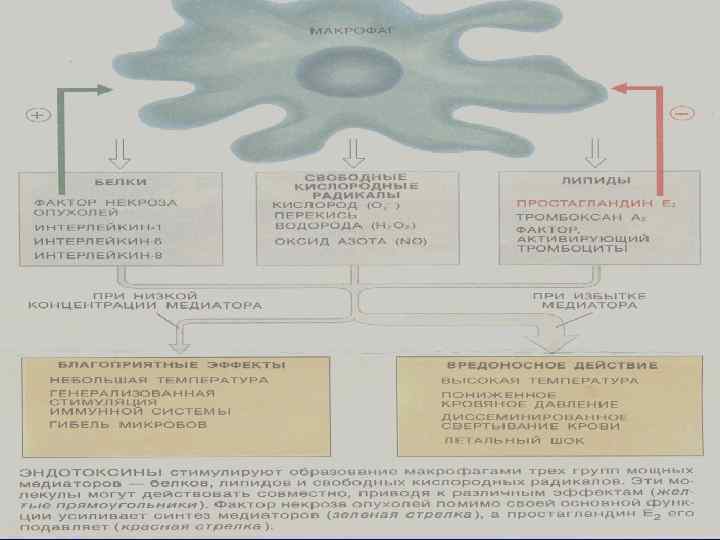

Одним из главных медиаторов действия эндотоксинов является фактором некроза опухолей, который вырабатывается макрофагами и в свою очередь усиливающий выброс макрофагами медиаторов. Когда в ткань попадает грамотрицательная бактерия и из нее выделяется умеренное количество эндотоксинов, производимые макрофагами агенты способствуют уничтожению инфекции, инициируя локальный регулируемый иммунный ответ. Типичные эффекты — небольшая температура, мобилизация иммунных компонентов, как специфичных, так и менее специализированных, — обычно обеспечивают выздоровление и защищают организм от атаки со стороны других микробов. Но если инфекция тяжелая, то в кровотоке накапливается так много эндотоксинов, создаются благоприятные условия для контакта с макрофагами. В этой ситуации системное высвобождение мощных медиаторов (накапливаются свободные радикальные формы кислорода, оксид азота, факторы, активирующие свертывающую систему) вызывая диссеминированное свертывание крови, . Что может привести к опасному для жизни шоку. По мере ухудшения кровообращения нарушается функционирование клеток и нарастает их гибель.

экзотоксины Экзотоксины являются белками и обычно секретируются в виде предшественников — протоксинов. Их активация связана с протеолизом эндопептидазами клеток-мишеней и собственными ферментами бактерий.

Экзотоксины аккумулируются в цитоплазме, выделяясь путем активной секреции либо при аутолизе бактериальных клеток (например, у клостридий). Чаще обнаруживаются в фазе активного роста бактерий. Активность бактериальных токсинов колеблется в широких пределах. Для самого мощного из них, ботулинического, хватило бы 6 кг, чтобы истребить все человечество. 1 мг столбнячного токсина способен убить 150 млн. мышей, a такое же количество токсина дифтерийной палочки смертельно для 150 тыс. морских свинок.

• Токсины могут определять клиническую картину заболевания (токсины дифтерийной палочки, холерного вибриона, клостридий столбняка и ботулизма, возбудителя сибирской язвы, некоторых стафилококков и стрептококков, энтеротоксигенных энтеробактерий). • Токсины второго типа «парциальные токсины» или «токсины частного приложения» • Вторичные токсины выделяются при повреждении или активации клеток хозяина. •

Названия экзотоксинов традиционно базируются на категории поражаемых мишеней. Ниже приведена терминология, которая с известной долей условности отражает биологическую активность бактериальных токсинов. • Энтеротоксины поражают эпителий (энтероциты) тонкого кишечника. Иногда под эту рубрику попадают токсины, проникающие через кишечник, но не оказывающие на него прямого действия (энтеротоксины золотистого стафилококка). • Нейротоксины вызывают избирательное поражение нервных клеток, межнейронных и нервномышечных синапсов. • Дермонекротоксины поражают кожу. К этой группе относятся эксфолиатины золотистого стафилококка, обладающие уникальной способностью разрушать эпителиальные десмосомы.

Гемолизины лизируют эритроциты, цитотоксичность гемолизинов не ограничивается лизисом эритроцитов. Лейкоцидины — антифагоцитарные факторы, повреждающие лейкоциты (нейтрофилы), иногда макрофаги. Избирательность токсического эффекта определяется спецификой клеточных рецепторов. По механизму действия можно выделить несколько групп токсинов (Кларр К. Шмитт и со-авт. , 2000): 1. Повреждающие клеточные мембраны. 2. Ингибиторы синтеза белков. 3. Активаторы вторичных мессенджеров. 4. Активаторы иммунного ответа. 5. Протеазы.
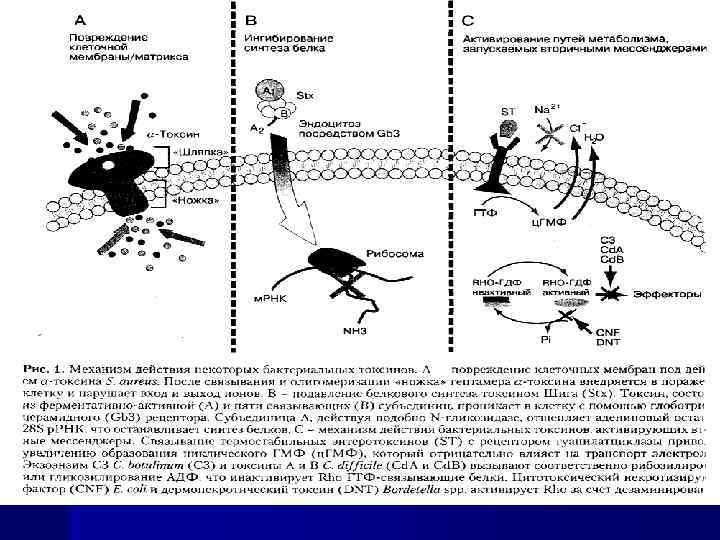

Токсины действующие на клеточную мембрану Структурное повреждение мембран и лизис клеток-мишеней вызывают фосфолипазы (например, альфа-токсин Clostridium perfringens), детергенты (альфа- токсин Staphylococcus aureus), факторы, агрегирующие холестерол (0 -стрептолизин Streptococcus pyogenes). Повреждение может быть функциональным, ограничиваясь нарушением активности мембранных ферментов. Иногда это смертельно для клетки, хотя и не сопровождается цитолизом.

Бактериальные токсины, объединенные во второй класс, поражают клетки-мишени за счет подавления синтеза белка. Субстратами для этих токсинов являются фактор элонгации и рибосомальная РНК.

Бактериальные токсины третьей группы могут вызывать активацию или модификацию различных внутриклеточных белков -мессенджеров, что приводит к резким нарушениям функциональной активности клеток без их гибели. Некоторые бактериальные токсины, отнесенные к четвертой группе, являются суперантигенами.

Суперантигены обладают наведенным токсическим эффектом, неспецифически стимулируют Тлимфоциты. Действуют главным образом через иммунные рецепторы Т-лимфоцитов, вызывая поликлональную стимуляцию лимфоцитов, способствуя гиперсекреции цитокинов и синдрому вторичной (цитокинопосредованной) интоксикации. Свойствами суперантигенов обладают энтеротоксины и токсин токсического шока стафилококка, скарлатинозный токсин стрептококка, антигены микоплазм и др. Суперантигены, неспецифически стимулирующие В-лимфоциты, вызывая поликлональный синтез иммуноглобулинов.

Внутриклеточные токсины Внедряются в клетку, атакуя внутриклеточные мишени. Этому обычно, предшествует активация токсина. При активации от молекулы отщепляется фрагмент, который проникает в клетку, оказывая каталитическое действие. Структуру таких токсинов (бинарные токсины) описывают формулой А-В, где, «В» выполняет рецепторную функцию, а «А» отвечает за токсичность. Один из универсальных каталитических эффектов — АДФ-рибозилирование ключевых ферментов клетки. Принцип сводится к отщеплению АДФ-рибозы от НАД и ее присоединению к белку-мишени. Токсины этого типа (точнее их А-фрагмент) являются бифункциональными ферментами действуя как НАД-гидролазы и АДФрцбозилтрансферазы. A-фрагменты бинарных токсинов обладают еще одним важным свойством — высокой избирательностью катализа. Попав в клетку, каждый из них находит собственную мишень, модифицируя строго определенные ферменты.

В сочетании со спецификой связывания В-фрагмента это объясняет особенности биологического эффекта разных токсинов ( дифтерийный токсин инактивирует фактор элонгации-2, нарушая сборку пептидов на рибосомах. Энтеротоксин холерного вибриона (холероген) модифицирует белок, блокирующий аденилатциклазу энтероцитов; это ведет к повышению внутриклеточного уровня циклического аденозинмонофосфата (ц. АМФ), гиперсекреции изотонической жидкости в тонком кишечнике и дегидратации организма. Известны токсины, обладающие прямой аденилатциклазной активностью (один из минорных токсинов коклюшной палочки, комплексный токсин сибиреязвенных бацилл). Они извращают функции клеток, нарушая внутриклеточный гомеостаз по ц. АМФ.

Разновидностью внутриклеточных токсинов являются нейротоксины клостридий столбняка и ботулизма. Их тропизм к нервной ткани определяется ганглиозидными рецепторами нейронов, нервных окончаний. При столбняке токсин (тетаноспазмин) образуется в ране и после связывания окончаниями периферических нервов, достигает спинного мозга. В спинном мозге он воспринимается регуляторными нейронами, блокируй секрецию глицина и гаммааминобутировой кислоты ингибиторных нейротрансмиттеров. Это вызывает перевозбуждение моторных нейронов, приводя к стойким мышечным контрактурам — спастическим параличам. Ботулинический токсин поступает с пищей, контаминированной клостридиями. Он устойчив к протеолитическим ферментам пищеварительного тракта и после всасывания в кровь достигает нервно-мышечных синапсов, где связывается рецепторами пресинаптической мембраны двигательных нервов, блокирует секрецию ацетилхолина. Это обрывает нервные импульсы, приводя к необратимой релаксации мышц — вялым параличам.

Все токсины — отличные иммуногены, но протективность антител лучше всего выражена в реакциях с экзотоксинами. Нейтрализовать эндотоксины труднее, возможно потому, что антигенные и токсические свойства ЛПС связаны с разными участками молекулы. В отличие от эндотоксинов, экзотоксины легко подаются обезвреживанию без потери иммуногенности (например, формалином) и могут быть использованы в качестве вакцинных препаратов — анатоксинов. Однако антитела нейтрализуют только свободные токсины.

ПЕРСИСТЕНЦИЯ Длительное сожительство бактерий с хозяином широко распространенное явление. Достаточно напомнить об огромном количестве бактериальных видов, составляющих нормальную микрофлору. Но бессимптомное носительство возможно и для патогенных бактерий. Принципиально, что оно протекает на фоне приобретенного иммунитета, эффекторы которого оказываются бессильны против утвердившегося инфекта. Еще удивительнее, что для некоторых бактерий персистенция — норма, определяющая сущность инфекционного процесса (микобактерии, трепонемы, бруцеллы, гонококк, хламидии). Это означает, что возбудитель располагает механизмами, которые обеспечивают его выживание и даже агрессивность в условиях иммунитетного пресса.

Селекция иммунорезистентных клонов является одной из причин стабилизации хронического гонорейного процесса. Есть и более простой способ уклонения от эффекторов иммунитета. Некоторые бактерии фиксируют на своей поверхности белки хозяина, прикрывая ими собственные антигены. Мы уже говорили о фибриновой псевдокапсуле стафилококка. Нечто подобное образует возбудитель сифилиса, сорбируя тканевой мукополисахарид. Хорошо известна бактериотропность фибронектина (например, в отношении стафилококков и трепонем), но её влияние на взаимоотношения с хозяином остается неясным.

L-формы. Все бактерии, за исключением микоплазм, обладают жесткой оболочкой (клеточной стенкой). У большинства бактерий механическая прочность клеточной стенки зависит от пептидогликана или муреина. Повреждение пептидогликана (например, лизоцимом) или нарушение его синтеза (бета-лактамные антибиотики) ведет к гибели бактерий. Некоторые из бактериальных клеток не только выживают без стенки-(протопласты, сферопласты), но и сохраняют способность к размножению. Они получили название «L-форм» . Много внимания уделяется персистенции L-форм, которая способствует длительному выживанию ряда патогенных бактерий в организме человека и животных (туберкулезная палочка, стрептококки, гонококки, листерии, бруцеллы, трепонемы и пр. ).

инфекция 1.ppt