05_учение об иммунитете-1.ppt
- Количество слайдов: 97
УЧЕНИЕ ОБ ИММУНИТЕТЕ. ИММУНОПРОФИЛАКТИКА И ИММУНОТЕРАПИЯ
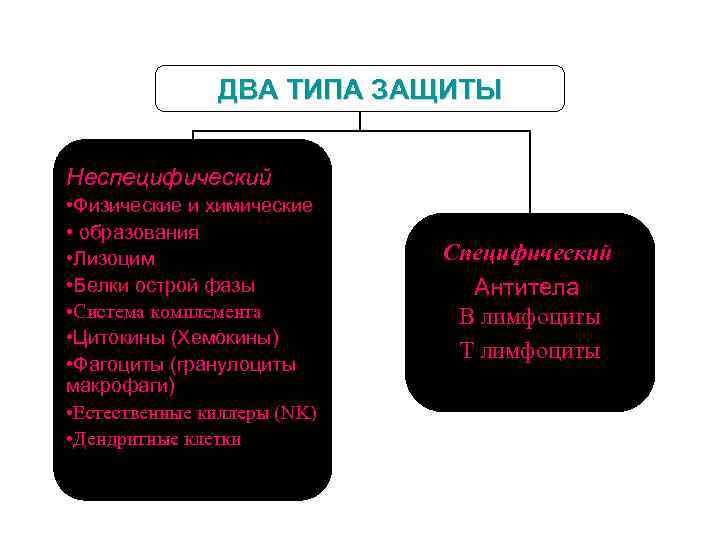
ДВА TИПА ЗАЩИТЫ Неспецифический • Физические и химические • образования • Лизоцим • Белки острой фазы • Система комплемента • Цитокины (Хемокины) • Фагоциты (гранулоциты макрофаги) • Естественные киллеры (NK) • Дендритные клетки Специфический Антитела B лимфоциты T лимфоциты
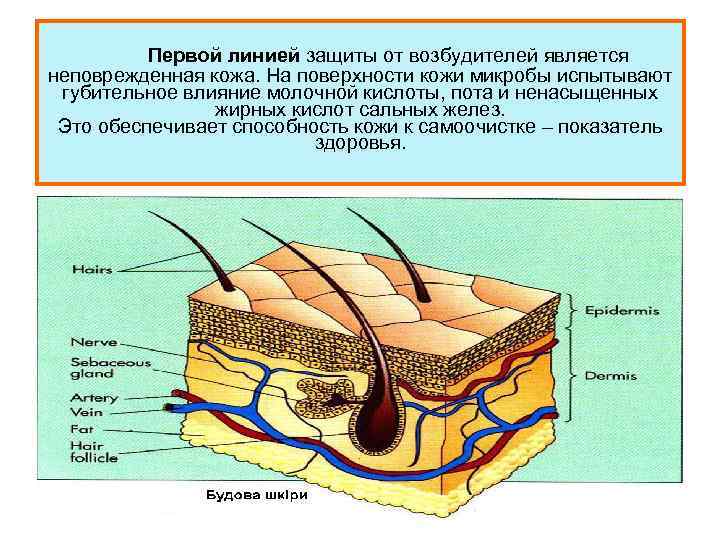
Первой линией защиты от возбудителей является неповрежденная кожа. На поверхности кожи микробы испытывают губительное влияние молочной кислоты, пота и ненасыщенных жирных кислот сальных желез. Это обеспечивает способность кожи к самоочистке – показатель здоровья.
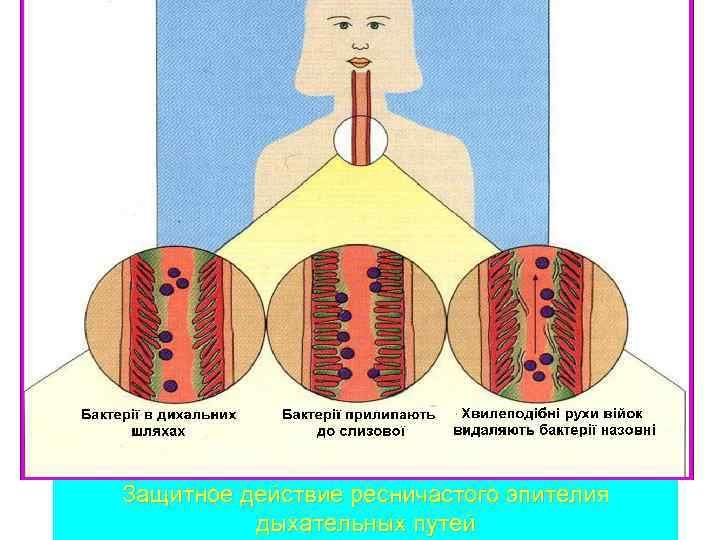
Защитное действие ресничастого эпителия дыхательных путей
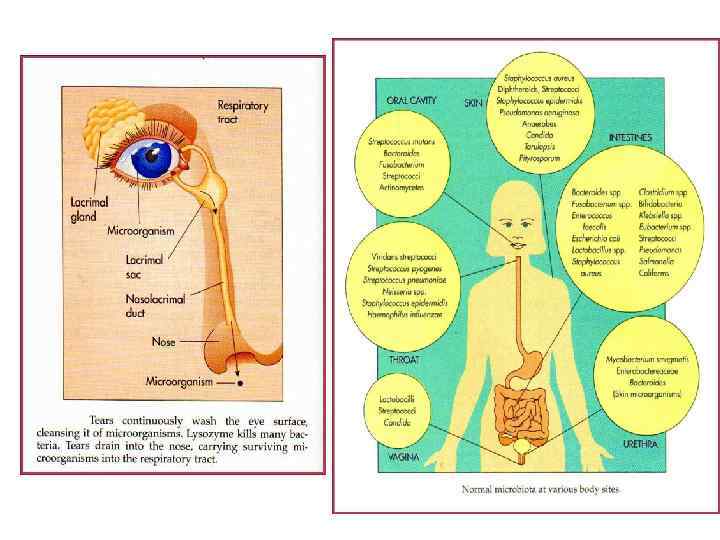

Гуморальные факторы неспецифической резистентности Лейкины – вещества, полученные из нейтрофилов, которые губительно действуют на грамположительную флору, Эритрин, полученный из эритроцитов, убивает дифтерийную палочку -лизины - выделяются тромбоцитами и задерживают рост в основном спороносных микробов Пропердин способствует лизису клеток Спермин и спермидин, которые содержатся в вилочковой железе, селезенке и почках, инактивируют микобактерии туберкулеза.
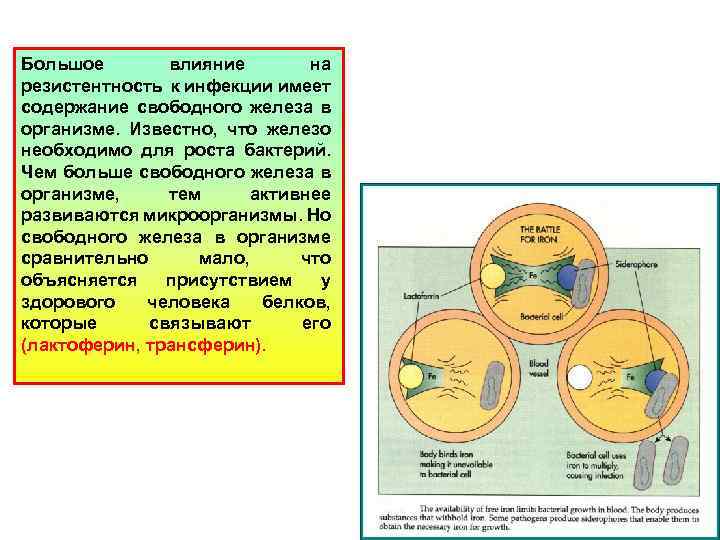
Большое влияние на резистентность к инфекции имеет содержание свободного железа в организме. Известно, что железо необходимо для роста бактерий. Чем больше свободного железа в организме, тем активнее развиваются микроорганизмы. Но свободного железа в организме сравнительно мало, что объясняется присутствием у здорового человека белков, которые связывают его (лактоферин, трансферин).

Особенное значение в системе неспецифической защиты организма имеют интерфероны. Различают три типа интерферонов: -интерферон (лейкоцитарный) -интерферон (фибробластный) и -интерферон (иммунный). альфа-интерферону присуще антивирусное и антипролиферативное действие. Усиливает киллерную активность лимфоцитов в отношении опухолей. Бета-интерферон - регулирует пролиферацию и функциональную активность макрофагов, усиливает их противоопухолевую активность, активирует естественные киллеры. Гамма-интерферон - природный регулятор иммунного ответа, владеет также противовирусной и противоопухолевой активностью, повышает выраженность (экспрессию) антигенов гистосовместимости I и ІІ классов. Синтез этого вида интерферона происходит под воздействием бактериальных и вирусных антигенов, лектинов.
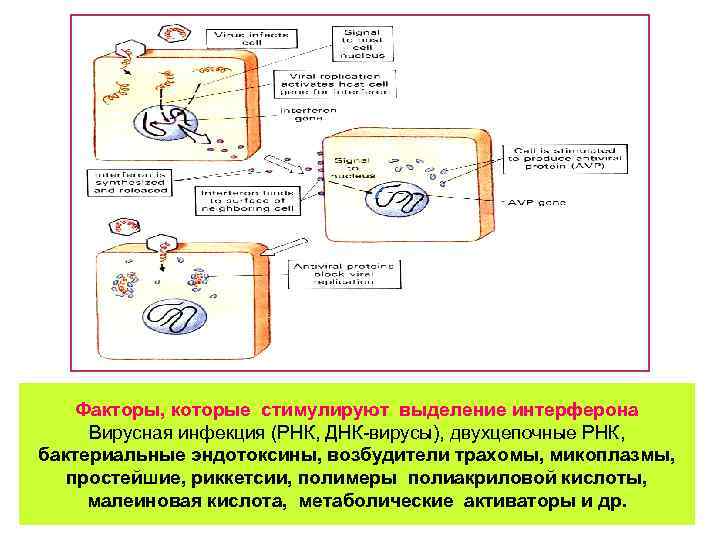
Факторы, которые стимулируют выделение интерферона Вирусная инфекция (РНК, ДНК-вирусы), двухцепочные РНК, бактериальные эндотоксины, возбудители трахомы, микоплазмы, простейшие, риккетсии, полимеры полиакриловой кислоты, малеиновая кислота, метаболические активаторы и др.

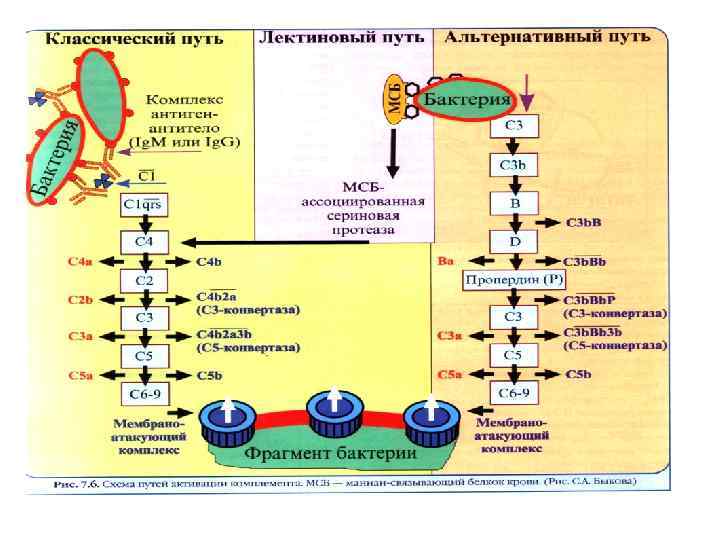
Система комплемента • Комплемент- это сложный комплекс белков (около 20), которые формируют каскадную ферментную систему. Компоненты комплемента обозначаются буквой С (С 1, С 2, С 3. . . С 9). В норме компоненты комплемента находятся в сыворотке крови в неактивном состоянии. Сутью каскадной активации системы комплемента является то, что каждый из первых пяти компонентов в результате активации превращается в фермент, который расщепляет следующий компонент и предоставляет ему свойств фермента. Система комплемента активируется по разному в зависимости от того, или в организме уже синтезировались антитела на данный агент, или таких антител еще нет. Поэтому различают классический путь активации комплемента (при наличии антител) и альтернативный путь (при их отсутствии).
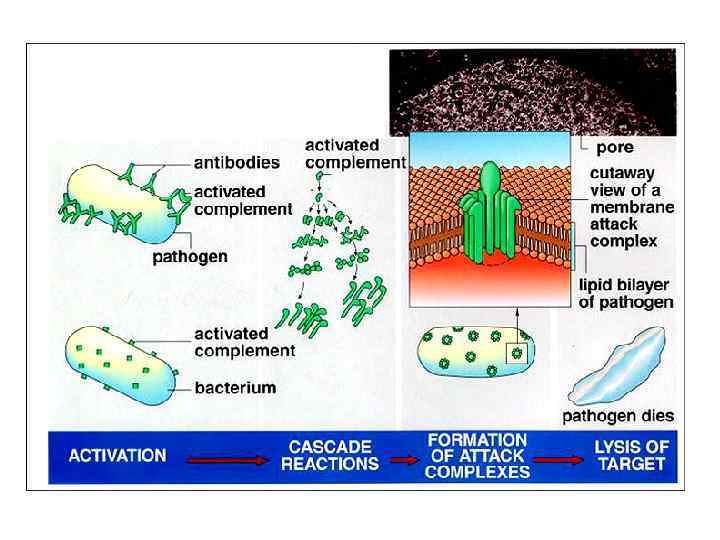

Фагоцитоз Большое значение в неспецифической защите организма играет явление фагоцитоза, которое впервые было открыто выдающимся отечественным ученым И. И. Мечниковим. • Захватывание и переваривание бактерий осуществляется двумя типами клеток - микро- и макрофагами. К микрофагам относят полиморфноядерные нейтрофилы. Они принадлежат к так назы ваемым «профессиональным фагоцитам» . Полиморфноядерные лейкоциты - это непродолжительно существующая популяция клеток, которая первой появляется в очаге воспаления. В результате стимуляции через дыхательный взрыв накапливается большое количество метаболитов и гидролитических продуктов, направленных на уничтожение бактерий как в клетках, так и вне их границ.

Основные стадии фагоцитоза : 1. Приближение фагоцита и микроба в результате положительного хемотаксиса. 2. Адгезия микроорганизма на поверхности фагоцита. 3. Активация мембраны фагоцита, что обусловливает поглощение микроорганизма. 4. Внутриклеточное переваривание инородной частицы и удаление продуктов распада за пределы клетки.

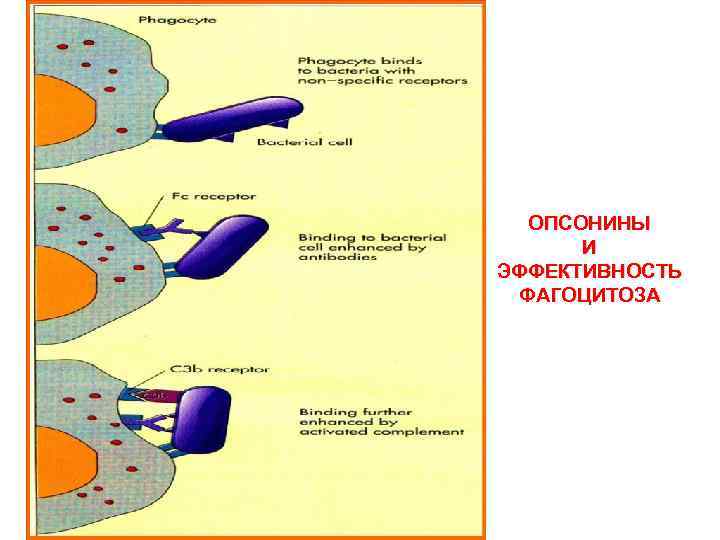
ОПСОНИНЫ И ЭФФЕКТИВНОСТЬ ФАГОЦИТОЗА

Естественные киллеры (ЕК) – это большие гранулярные лимфоциты, в гранулах которых содержится белок перфорин и сериновые эстеразы – гранзимы. Их основными маркерами являются антигены CD 56 и CD 57. Их содержание в крови составляет 5 -20 % от общего количества лимфоцитов. Природные киллеры выполняют в организме разнообразные функции: контролируют рост первичных и метастатических опухолевых клеток, контролируют развитие микробных и вирусных инфекций, продуцируют медиаторы, принимают участие в иммунорегулирующих процессах, контролируют пролиферацию и дифференциацию гемопоетических клеток, трансплантационного иммунитета. Естественные киллеры резистентные к ионизирующей радиации и не фагоцитируются.
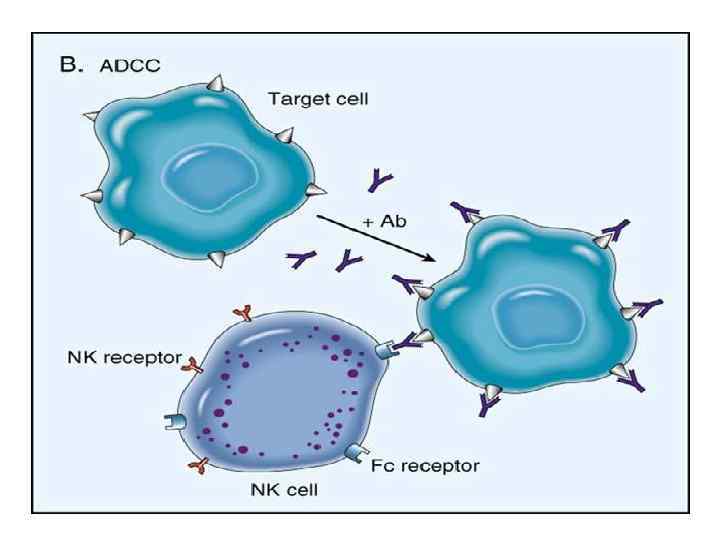

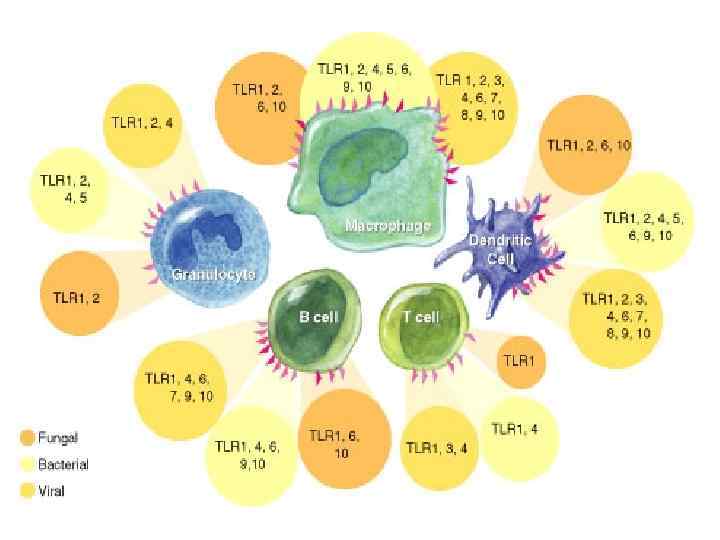
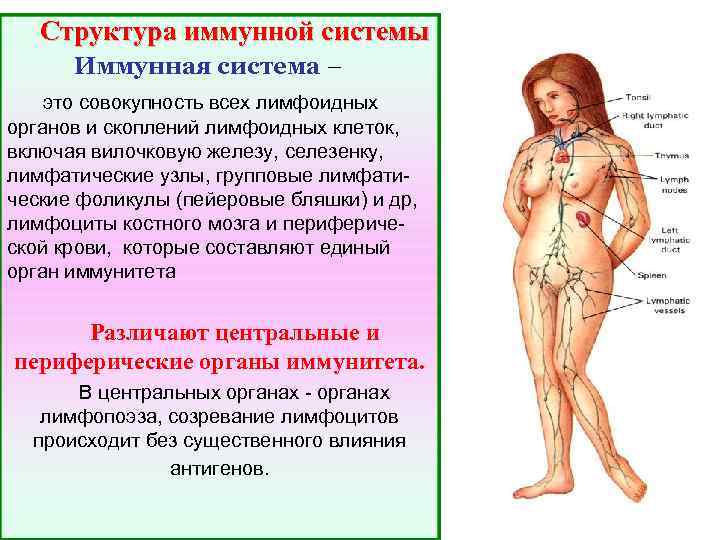
Структура иммунной системы Иммунная система – это совокупность всех лимфоидных органов и скоплений лимфоидных клеток, включая вилочковую железу, селезенку, лимфатические узлы, групповые лимфатические фоликулы (пейеровые бляшки) и др, лимфоциты костного мозга и периферической крови, которые составляют единый орган иммунитета Различают центральные и периферические органы иммунитета. В центральных органах - органах лимфопоэза, созревание лимфоцитов происходит без существенного влияния антигенов.

Центральными органами иммунной системы у млекопитающих являются вилочковая железа и костный мозг. Периферическими лимфоидными органами являются селезенка, лимфатические узлы, миндалины, лимфоидная ткань кишечника, бронхов. Центральной фигурой иммунной системы является лимфоцит. Лимфоциты - это специализированные клетки, которые способны реагировать (отвечать ) только на отдельную группу структурно похожих антигенов. Каждый клон лимфоцитов отличается от другого структурой антигенсвязывающего участка своих рецепторов. Таким образом, каждый клон реагирует только на определенные, соответствующие ему антигены.


Характеристика В-лимфоцитов Основным свойством В-лимфоцитов является наличие на их поверхности антигенраспознавательных иммуноглобулиновых рецепторов. После взаимодействия антигена с этими рецепторами В -лимфоциты дифференцируются в плазмоциты, основной функцией которых является продукция иммуноглобулинов – антител.

L H Рецептор В лимфоцита В-лимфоцит

Активация В-клеток происходит в две фазы: пролиферация и дифференциация. В результате пролиферации увеличивается количество клеток, способных вступать в реакцию, реагировать с введенным в организм чужеродным антигеном.
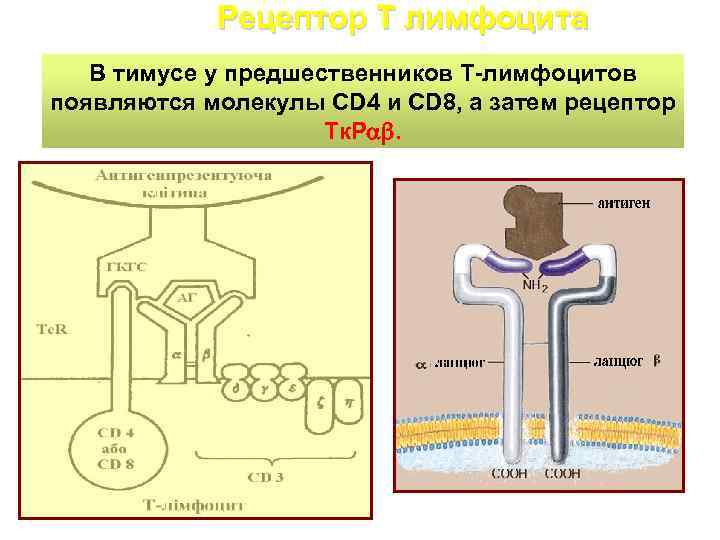
Рецептор Т лимфоцита В тимусе у предшественников Т-лимфоцитов появляются молекулы CD 4 и CD 8, а затем рецептор Tк. Р .
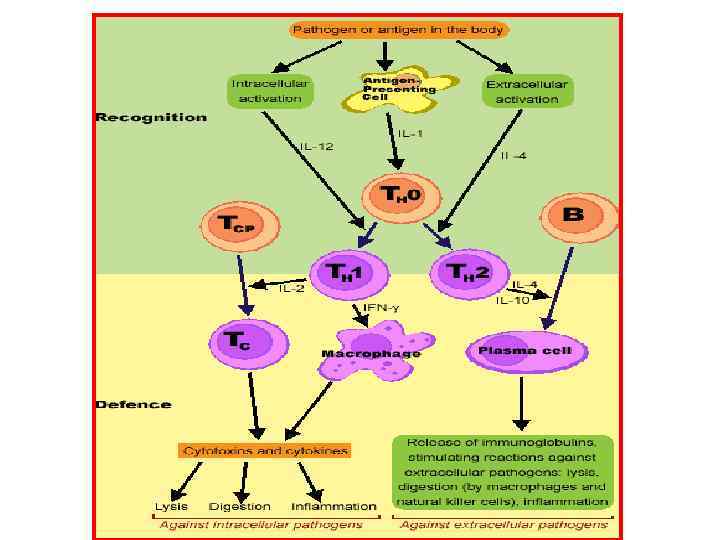

Цитокины и их характеристика Значительная роль в иммунной защите принадлежит цитокинам. С помощью цитокинов лимфоциты взаимодействуют между собой и одновременно с клетками других тканей организма, которые тоже способны выделять большое количество этих биологически активных веществ и в свою очередь влияют на лимфоциты. Цитокины являются тем мостиком, который связывает систему иммунитета с целым организмом. 1. Монокины – выделяются мононуклеарными фагоцитами 2. Лимфокины – продуцируются активированными Т клетками, в первую очередь Т хелперами. 3. Интерлейкины – много цитокинов, которые обозначаются абревиатурой ИЛ с соответствующей нумерацией

Общая характеристика антигенов Антигены - это биополимеры, естественные или синтетические соединения, которые разпознаются лимфоидными клетками и способны вызывать иммунный ответ.

Иммунный ответ: • синтез антител, • гиперчувствительность, • иммунологическая память, • иммунологическая толерантность Антигены характеризуются двумя занными свойствами: взаимосвя - 1. избирательно взаимодействуют с специализированными рецепторами лимфоцитов (антигенная специфичность) и тем самим вызывают синтез антител, 2. и реагируют с синтезированными антителами.

Антигенами являются белки, некоторые естественные и синтетические полипептиды, полисахариды и их комплексы с белками, липидами, нуклеиновые кислоты.
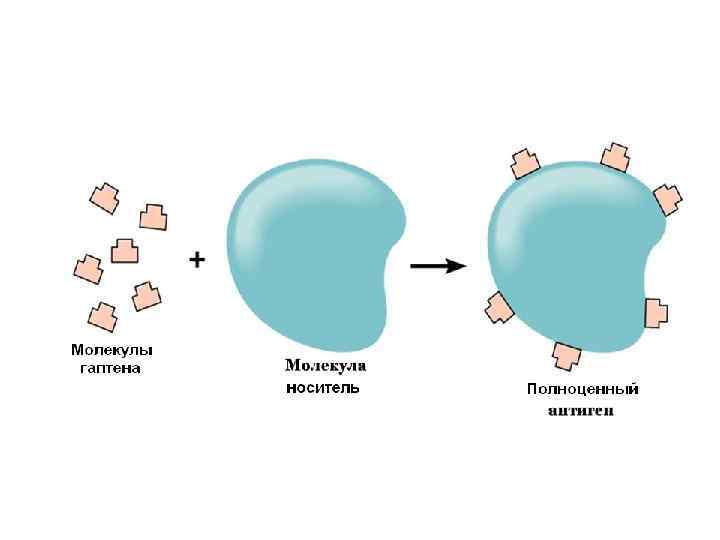
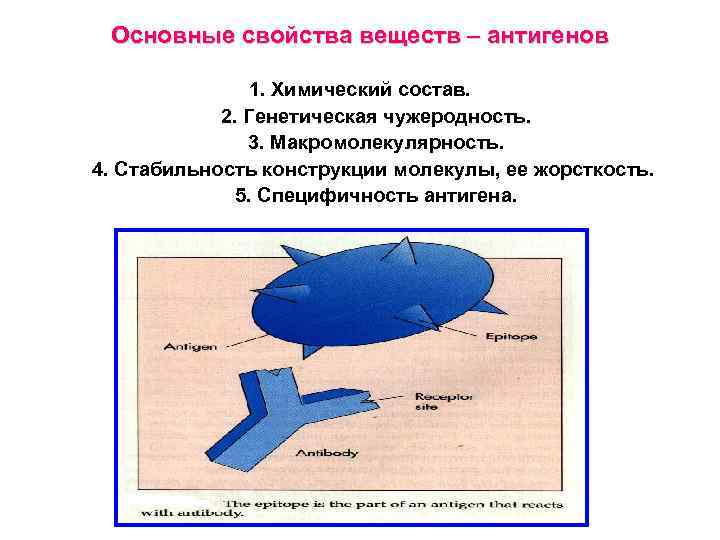
Основные свойства веществ – антигенов 1. Химический состав. 2. Генетическая чужеродность. 3. Макромолекулярность. 4. Стабильность конструкции молекулы, ее жорсткость. 5. Специфичность антигена.

Специфичность антигена зависит от детерминантной группы (эпитопа). Эпитоп - это та часть антигена, которая соединяется с активным центром антитела. На одном носителе может быть много детерминантных групп, и на каждую из них синтезируются отдельные антитела
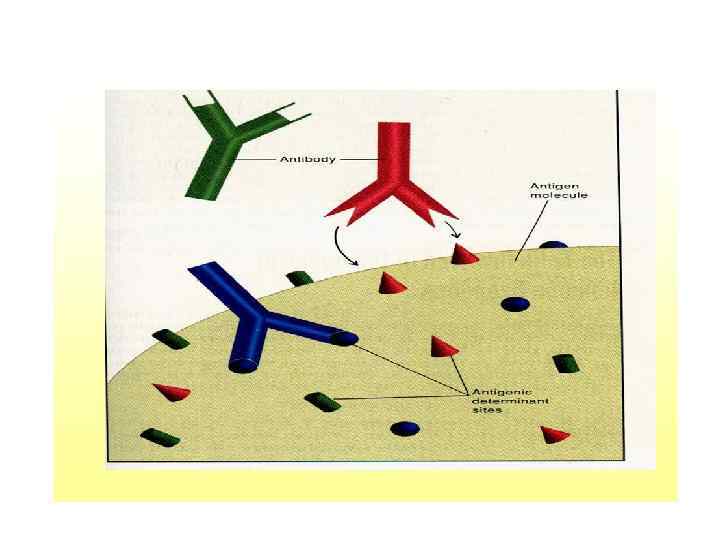

В состав микроорганизмов входят белки, полисахариды, соединения белков с полисахаридами и липидами, нуклеиновые кислоты. Поэтому антигенное строение бактерий довольно мозаично. У сальмонел различают: соматический - О-, жгутиковый - Н- и капсульный К-антигены, каждый из них стимулирует синтез специфических антител. Знание антигенной структуры бактерий необходимо для серологической идентификации микробной культуры, получения вакцинных препаратов, диагностических и лечебнопрофилактических сывороток.
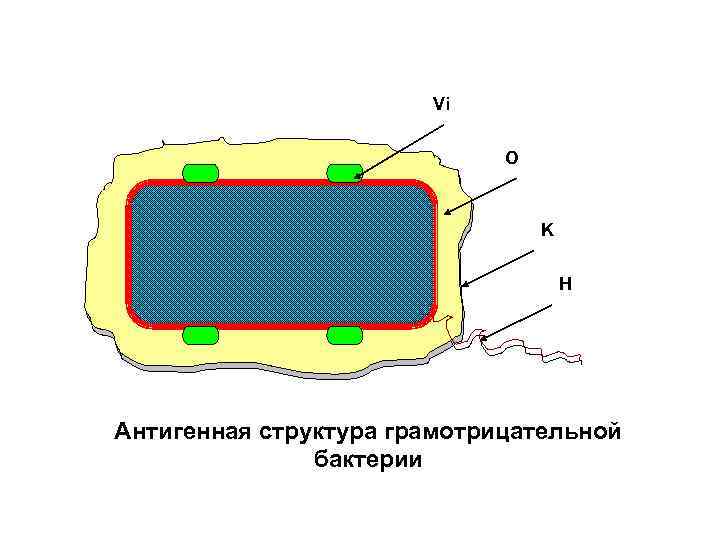
Vi O K H Антигенная структура грамотрицательной бактерии

Антигены вирусов H N Высокими иммуногенными свойствами владеют пептиды вирусных гликопротеидов, которые содержат гидрофильные группы (гемагглютинин (H) и нейраминидаза (N) вируса гриппа

В организме есть вещества и ткани, которые в эмбриональном периоде развития не контактировали с лимфоидной тканью, поэтому иммунная система “не знает” об их существовании. При определенных патологических процессах эти вещества попадают в кровь, и иммунная система реагирует на них как на чужеродные. Такие вещества являются антигенными для собственного организма и називаются аутоантигенами. • • хрусталик глаза, щитовидная железа, мозговая ткань, сперматозоиды

Перехрестные антигены млекопитающих и микроорганизмов Обнаружены общие антигены у стрептококков и клеток эндокарда, клапанов сердца и почек. Коклюшные бактерии имеют общие антигены с нервной тканью кролика. Ряд штаммов кишечной палочки - с изоантигенами А и В эритроцитов человека. С эритроцитарными антигенами имеют общие антигени холерный вибрион, возбудитель чумы, бактерии тифо-паратифозной группы, вирус оспы. Перехрестные антигены микробов и вирусов могут стимулировать в организме синтез антител (аутоантител), которые повреждают определенные ткани организма. Такие патогенетические механизмы четко видны при ревматизме, язвенном колите, некоторых поствакцинальных осложнениях.
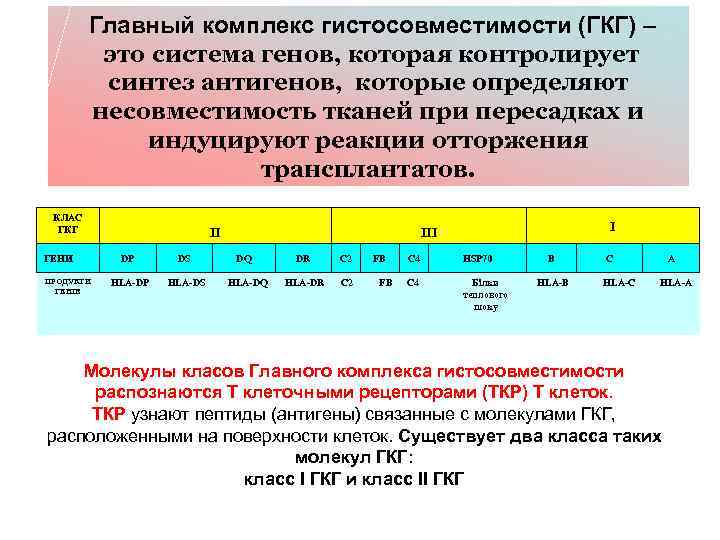
Главный комплекс гистосовместимости (ГКГ) – это система генов, которая контролирует синтез антигенов, которые определяют несовместимость тканей при пересадках и индуцируют реакции отторжения трансплантатов. КЛАС ГКГ ГЕНИ ПРОДУКТИ ГЕНІВ II DP DS HLA-DP HLA-DS І III DQ HLA-DQ DR C 2 HLA-DR C 2 FB FB C 4 HSP 70 C 4 Білки теплового шоку B HLA-B C HLA-C A HLA-A Молекулы класов Главного комплекса гистосовместимости распознаются Т клеточными рецепторами (ТКР) Т клеток. ТКР узнают пептиды (антигены) связанные с молекулами ГКГ, расположенными на поверхности клеток. Существует два класса таких молекул ГКГ: класс І ГКГ и класс ІІ ГКГ

Антитела (иммуноглобулины). Характеристика основных классов иммуноглобулинов. Наиболее критический момент в процессе иммунного ответа - это распознание, выявление химического маркера, который свойственный “чужому” агенту в отличие от “своего” организма. Это задание выполняют особые белки, которые отличаются удивительным разнообразием молекулярной структуры. Основными распознающими белками являются антитела или иммуноглобулины (Ig). Существует пять классов иммуноглобулинов человека - G, M, А, E, D. Молекулы каждого класса состоят из тяжелых и легких полипептидных цепей. Легкие полипептидные цепи (L) бывают двух видов или , или и одинаковые для всех классов иммуноглобулинов. Тяжелые цепи (Н) у каждого класса разные, и в зависимости от названия тяжелой цепи и происходит название класса иммуноглобулинов.

У каждого иммуноглобулина - только один тип легких цепей или , или . Таким образом, структурные формулы каждого класса иммуноглобулина можна записать таким образом: Тяжелые цепи Класс иммуноглобулинов Ig G Ig M Ig A Ig E Ig D Ig G - 2 2, , 2 2 Ig M - ( 2 2)5, ( 2 2)5 Ig A - ( 2 2)n , ( 2 2)n, , Ig E - 2 2, 2 2 Ig. D - 2 2, 2 2
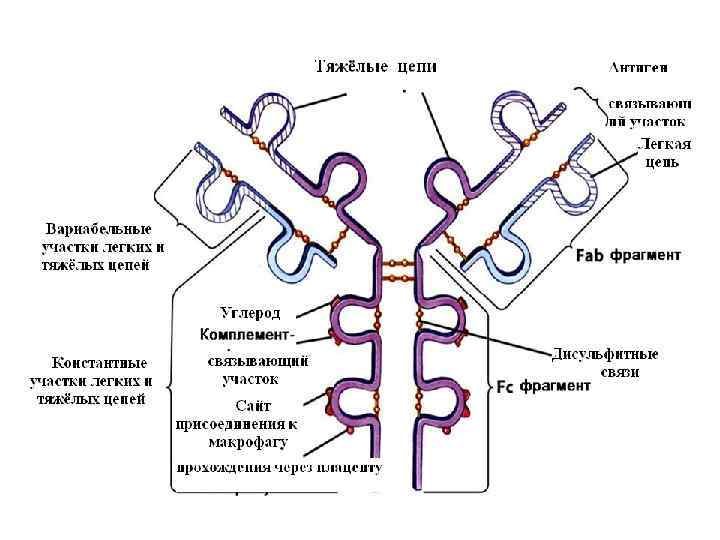

Ig. G - основной класс иммуноглобулинов, который составляет 70 % всех иммуноглобулинов. В значительной мере он выделяется в ответ на повторное попадание антигена в организм. В процессе иммунного ответа происходит переключение синтеза Ig. M на Ig. G сравнительно термостабильные (выдерживают нагревание при 75 С 30 мин). При такой экспозиции Ig. M быстро разрушаются. Период полураспада Ig. G - 23 суток. Ig. G нейтрализуют вирусы, токсины, опсонизирующе действуют на бактерии, связывают комплемент. Ig. G - единственный иммуноглобулин, который проходит через плаценту и защищает в первое время после рождения ребенка от возбудителей дифтерии, столбняка, коклюша, кори и др. По структуре тяжелых цепей среди Ig. G различают четыре подкласса: Ig. G 1, Ig. G 2, Ig. G 3, Ig. G 4.
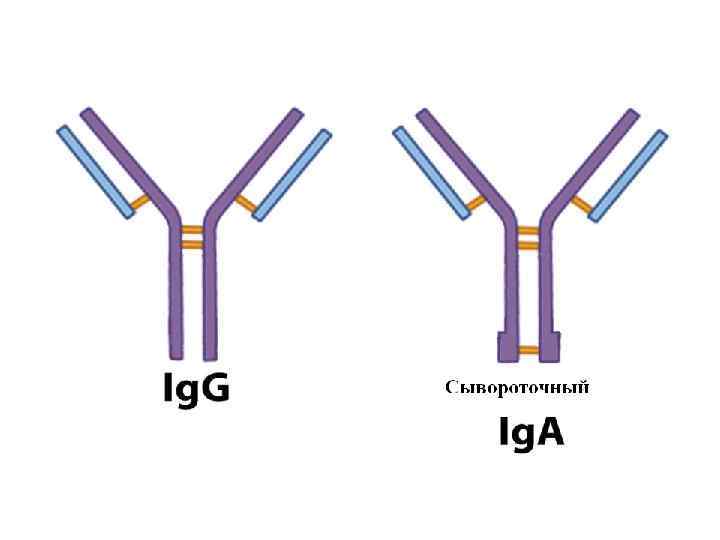

Ig. А. Различают сывороточные и секреторные Ig. А. Сывороточные Ig. A могут иметь структуру мономера (80 % ), димера- или полимера. У последних двух есть дополнительная цепь J, которая объединяет эти мономеры. Сывороточные иммуногло- булины А составляют 10 -20 % всех иммуноглобулинов сыворотки. • Секреторные иммуноглобулины чаще всего бывают в виде димера, к которому присоединяется секреторный компонент (СК-фрагмент), который защищает Ig. A от разрушения протеазами. •
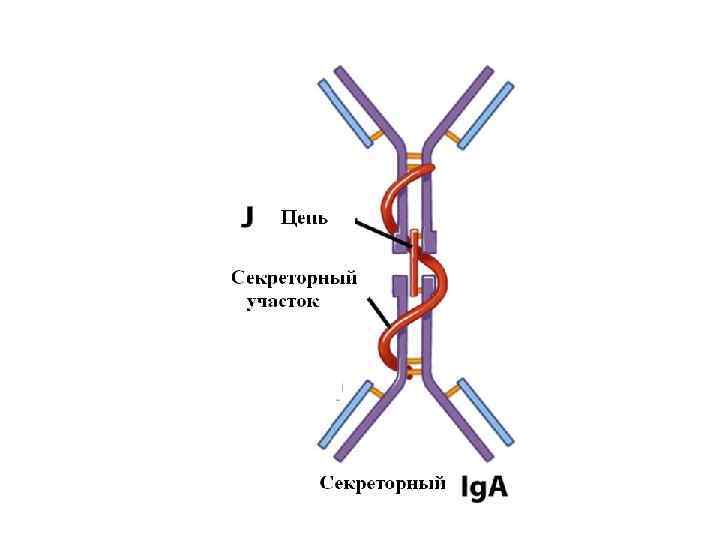

Секреторный Ig А имеет выраженные бактерицидные свойства. Он в несколько раз более активный по отношению к грамотрицательной флоре, чем Ig. M и в десятки раз в сравнении с Ig. G. S Ig. A - основной защитный фактор от вирусов и существует независимо от сывороточного. Местная резистентность слизистых оболочек от вирусных инфекций тесно связана с количеством S Ig. A на их поверхности. S Ig. A также защищает слизистые оболочки от адгезии на них патогенных микроорганизмов.
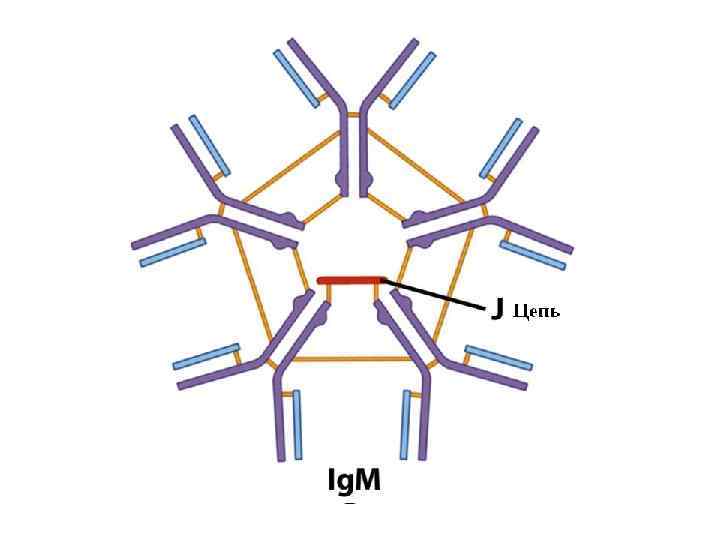

Ig. M. Иммунный ответ организма начинается из синтеза Ig. M. Они синтезируются быстро, но иммунологическая память клеток, которые их синтезируют либо отсутствует, либо сохраняется кратковременно. Период полураспада - 5 суток. Ig. M содержит дополнительную цепь J, которая объединяет 5 мономеров в одну структуру. Ig. M имеет 10 активных центров и дополнительный домен СH 4, который активно фиксирует комплемент. Основным источником Ig. M является селезенка. Ig. M находится в крови и секретах, и им, в основном, обусловлены бактерицидные свойства этих веществ.
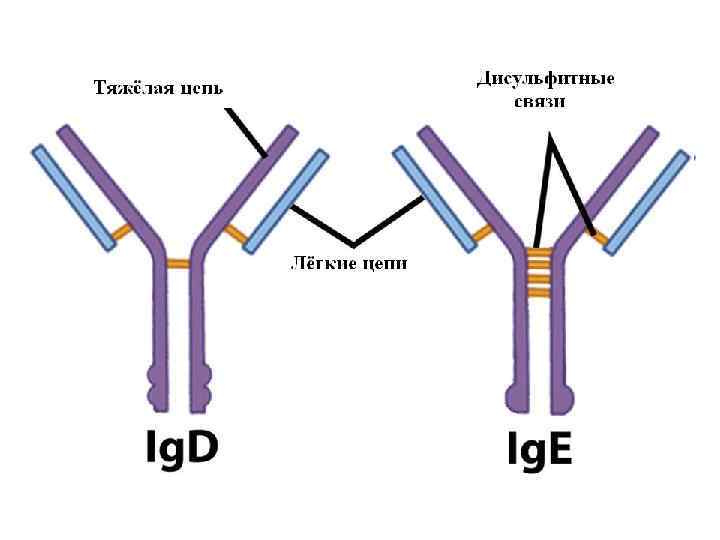

Ig. E- реагины играют основную патогенетичную роль в аллергических реакциях немедленного типа. Ig E синтезируются в коже, лимфоидной ткани дыхательных путей и кишечника. По своей структуре они несколько отличаются от Ig. G. У Ig. E на один домен больше (СН 4). Это свойство обусловливает особенности биологической функции Ig. E – способность адсорбироваться на базофилах и тучных клетках при помощи домена СН 4 Fc - фрагмента.

Ig. D. Строение этого класса иммуноглобулинов сходное с Ig. G. Однако они не способны фиксировать комплемент. Сравнительно большее их количество находится в сосудах, чем за их пределами. Ig. D как и Ig. М, является одним из поверхностных рецепторов В-лимфоцитов.

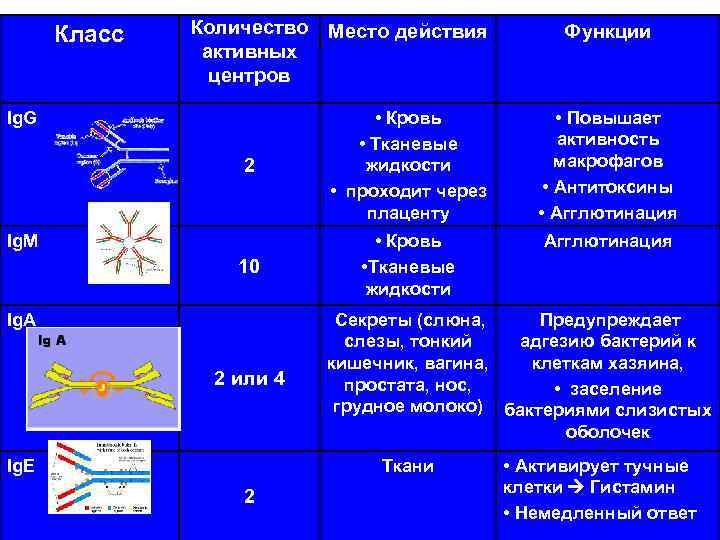
Количество активных центров Место действия Функции 2 • Кровь • Тканевые жидкости • проходит через плаценту • Повышает активность макрофагов • Антитоксины • Агглютинация • Кровь • Тканевые жидкости Агглютинация 10 Класс Ig. G Ig. M Ig. A 2 или 4 Ig. E Секреты (слюна, Предупреждает слезы, тонкий адгезию бактерий к кишечник, вагина, клеткам хазяина, простата, нос, • заселение грудное молоко) бактериями слизистых оболочек Ткани 2 • Активирует тучные клетки Гистамин • Немедленный ответ

Как работают антитела? Функции антител: Нейтрализация Опсонизация Антитело-зависимая цитотоксичность Активация комплемента Специализированная роль: Иммунитет слизистых оболочек Иммунитет новорожденных
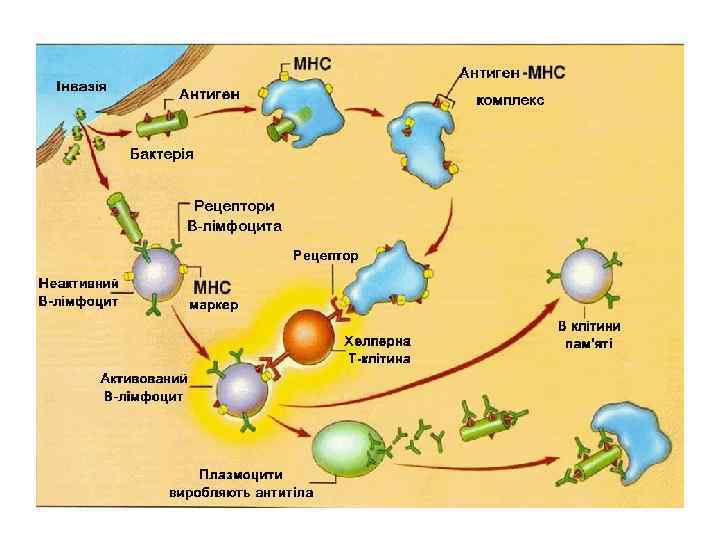
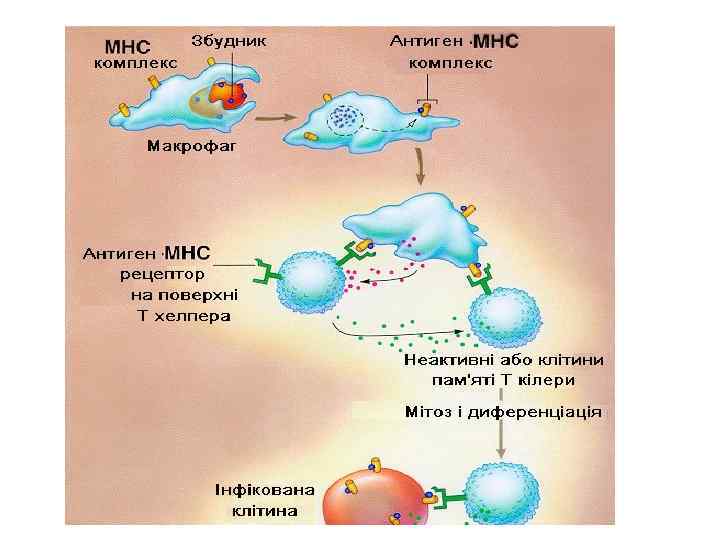

Аллергия Классификация гиперчувствительность по Coombs и Gell 1. Реакции анафилактические, атопические. 2. Реакции цитолитические, цитотоксические. 3. Реакции иммунных комплексов (гистотоксические). 4. Реакции туберкулинового типа. Причиной возникновения первых трех типов реакции является взаимодействие антигена с антителом, и они принадлежат к, так называемым, реакциям (гиперчувствительности) немедленного типа. Реакции четвертого типа базируются на взаимодействии рецепторов Тлимфоцитов с соответствующими антигенами и принадлежат к реакциям замедленного типа.

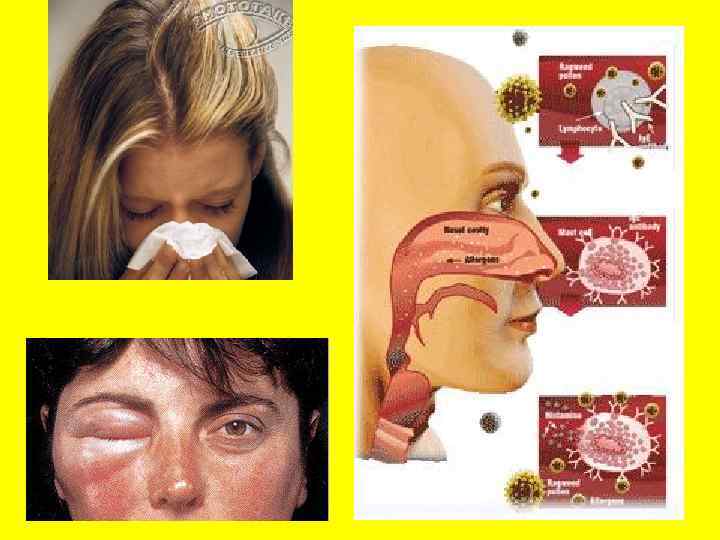
Аллергены разделяются на неинфекционные и инфекционные. Наиболее многочисленной и многообразной является группа неинфекционных аллергенов. К ним относятся: пыльцевые, бытовые, эпидермальные, пищевые аллергены. Одной из наиболее распространенных групп неинфекционных аллергенов является группа аллергенов с пыльцы растений, которая влечет массовые аллергические заболевания – полинозы. Полиноз тесно связанные с сезоном цветения многообразных растений. В это время в воздухе одновременно может находиться несколько десятков видов пыльцы. Различают такие виды пыльцевых аллергенов: 1. Из пыльцы сорняков – амброзии, лебеды, полыни, пырея и т. п. . 2. Из пыльцы деревьев – клена, дуба, березы, лещины, ясеня. 3. Из пыльцы злаков – рожь, соолнешника, кукурузы. 4. Из пыльцы луговых трав.

К бытовым аллергенам относятся: аллергены домашней и библиотечной пыли, аллергены из пуха подушки и клещевые аллергены. Эпидермальные аллергены – аллергены из шерсти собак, кошек, кроликов, гвинейских свинок, лупы коней, волоса человека. Группа пищевых аллергенов тоже многосчисленная и многообразная: аллергены куриного яйца, коровьего молока, аллергены из рыб, круп, мяса, цитрусовых Среди инфекционных аллергенов различают: бактериальные (стафилококка, стрептококка, кишечной палочки, коринебактеий, протея, пневмококка), грибковые (кандиды, аспергилловых грибков, мукора, ризопуса), вирусные (аденовирусные, герпетические, гриппозные. ).
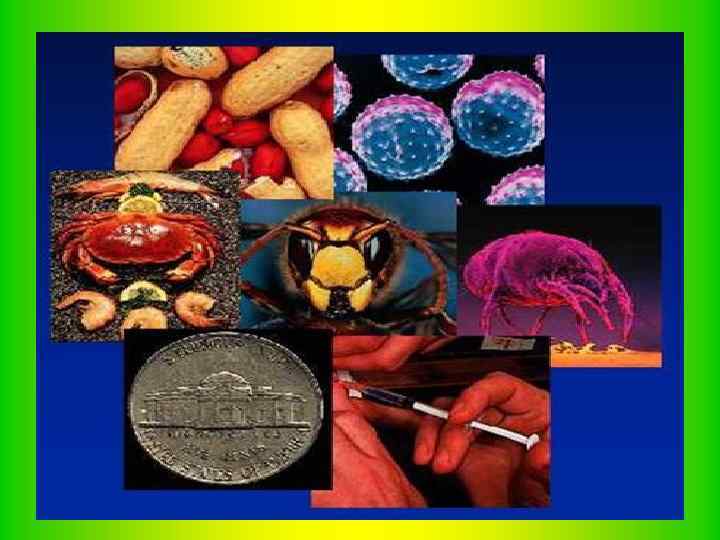


Гиперчувствительность І типа Реакции первого типа (анафилактические, атопические). Этот тип rиперчувствительности связан с присутствием в крови Ig. E pearинов и наблюдается при бронхиальной астме, крапивнице, отеке Квинке, анафилактическом шоке и т. п. При анафилактических реакциях встречаются и анафилактические антитела Ig. Gr При первичном попадании аллергена в организм синтезируются Ig. E, которые адсорбируются на тучных клетках (аллергоцитах) и базофильных лейкоцитах. Соединение Ig. E с этими клетками происходит с помощью специфических рецепторов R 1 и R 2 к епсилон цепи этого иммуноглобулина. Каждая клетка имеет от 104 до 106 рецепторов, что разрешает двум молекулам Ig. E соединяться с одной молекулой антигена. При повторном контакте одна молекула антигена связывается с двумя молекулами Ig Е, что обусловливает дегрануляцию алергоцитов и базофилов.
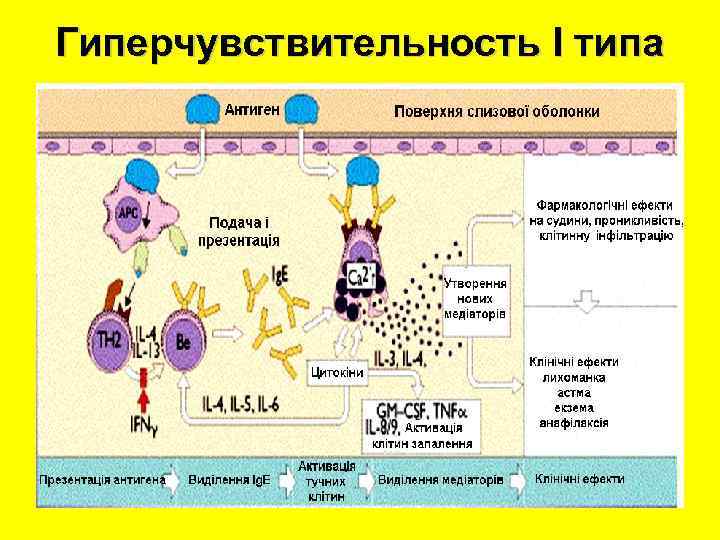
Гиперчувствительность І типа

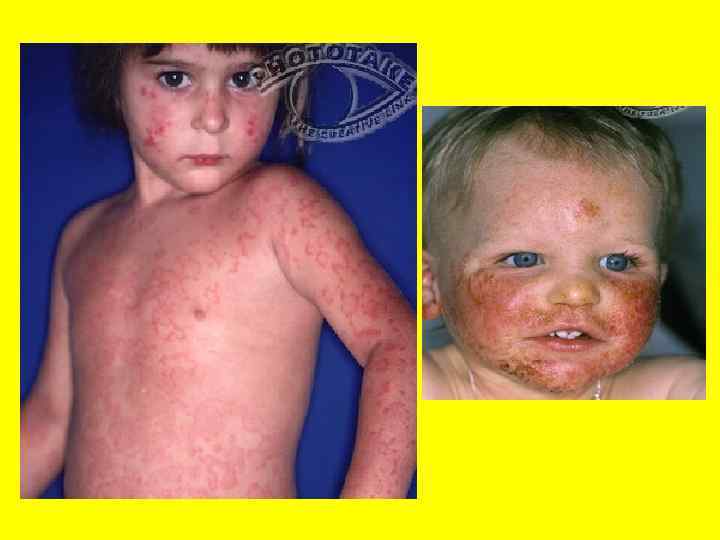
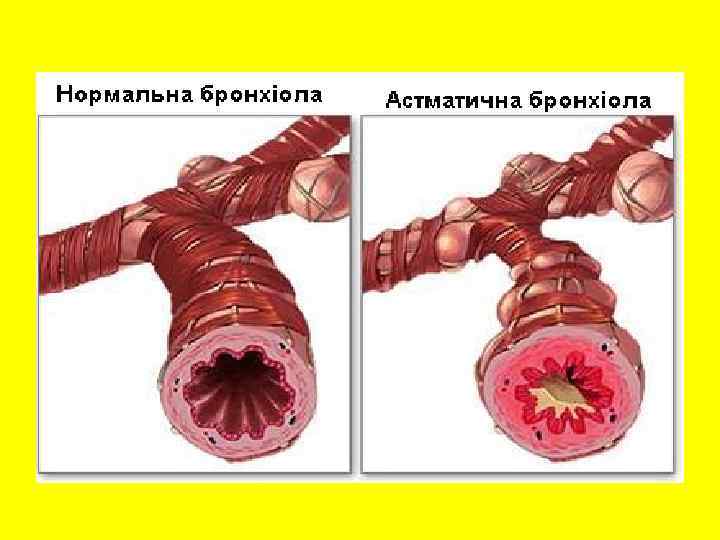

Реакции второго типа (цитотоксические). Эти реакции наблюдаются при переливании употреблении разных лекарственных средств. крови и Изоиммунные реакции при переливании крови: а) при переливании группонесовместимой крови изогемагглютинины обуславливают склеивание введенных эритроцитов, что приводит к их лизису; б) гемолитическая болезнь новорожденных при резус конфликте.
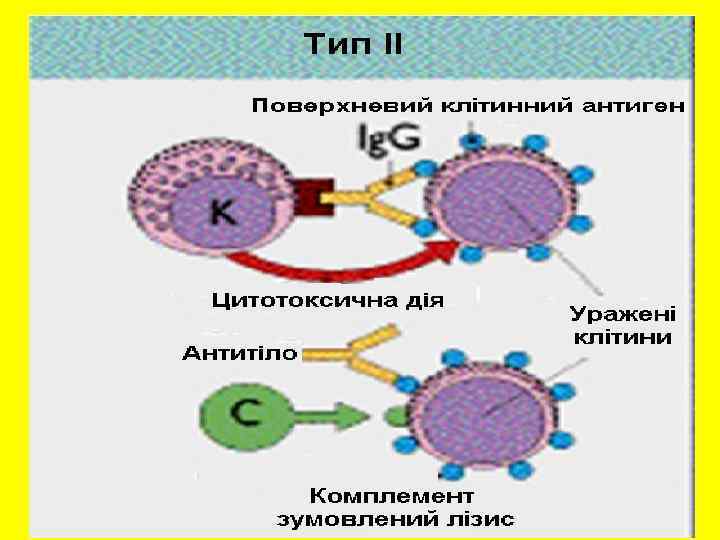

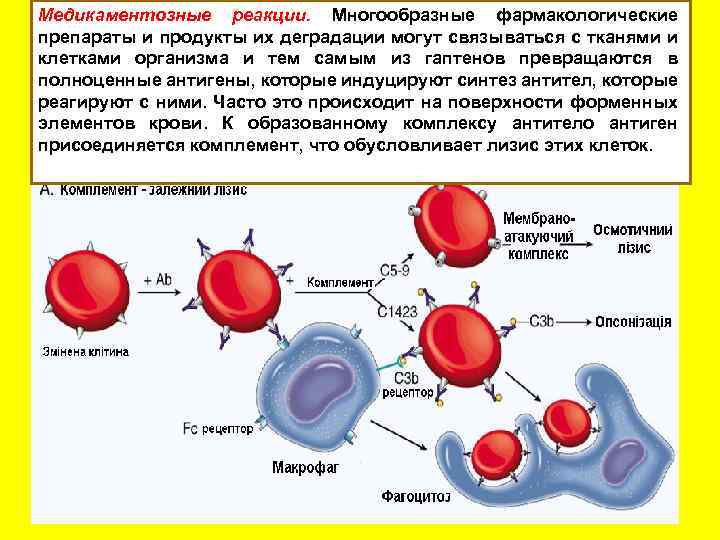
Медикаментозные реакции. Многообразные фармакологические препараты и продукты их деградации могут связываться с тканями и клетками организма и тем самым из гаптенов превращаются в полноценные антигены, которые индуцируют синтез антител, которые реагируют с ними. Часто это происходит на поверхности форменных элементов крови. К образованному комплексу антитело антиген присоединяется комплемент, что обусловливает лизис этих клеток.

Реакции третьего типа - иммунокомплексные (феномен Артюса) При длительном пребывании в организме антигена его взаимодействие с антителом приводит к образованию нерастворимых иммунных комплексов-преципитатов, которые откладываются на стенках кровеносных сосудов и блокируют циркуляцию крови, что влечет нарушение трофики в данном участке. Если с такими комплексами связываются компоненты комплемента, то образуются СЗа и C 5 a - анафилатоксины. Они вызывают выделение активных биологических факторов из тучных клеток, которые повышают проницаемость сосудов и привлекают в зону воспаления полиморфноядерные лейкоциты, которые фагоцитируют эти комплексы. При этом выделяется содержимое лизосом (протеолитические ферменты, которые образуют кинины и поликатионные белки), которые вызывают местное повреждение ткани и стимулируют воспалительный процесс.
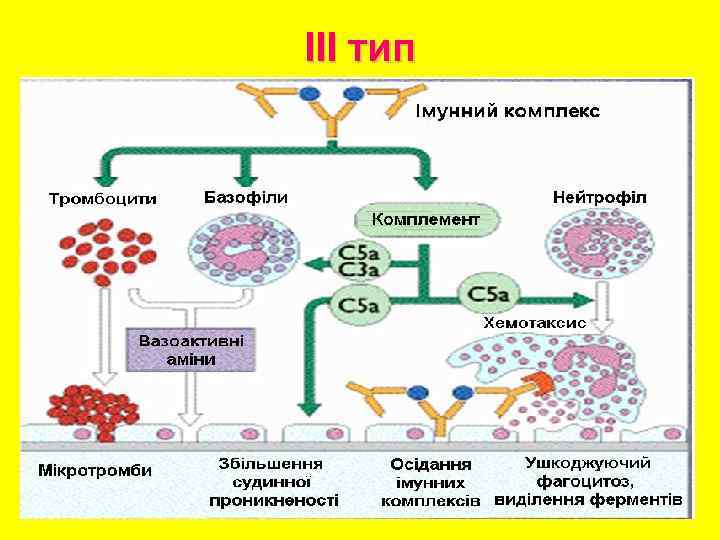
ІІІ тип
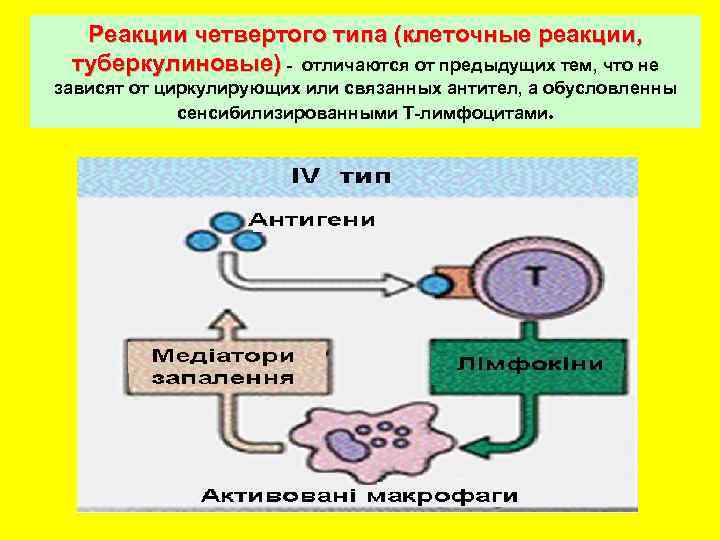
Peaкции четвертого типа (клеточные реакции, туберкулиновые) - отличаются от предыдущих тем, что не зависят от циркулирующих или связанных антител, а обусловленны сенсибилизированными Т-лимфоцитами.
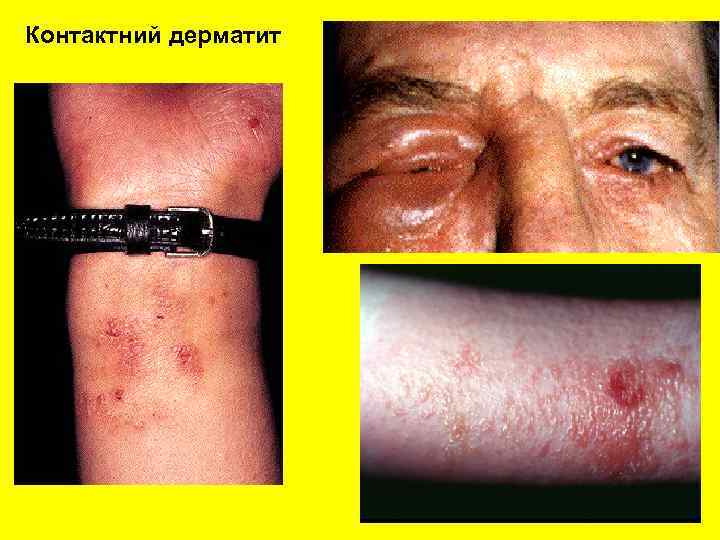
Контактний дерматит

Обнаружить состояние сенсибилизации организма можно с помощью клинических аллергических проб. Пробы in vivo 1. Епикутанная проба 2. Cкарификационная кожная проба 3. Аппликационная проба 5. Внутрикожные пробы. 6. Коньюктивальная проба 7. Назальная провокационная проба. Пробы in vitro Реакция повреждения нейтрофилов–лейкоцитолиза Реакция агломерации лейкоцитов. Реакция дегрануляции базофилов за Шелли. Реакция специфической бласттрансформации лейкоцитов (РБТЛ
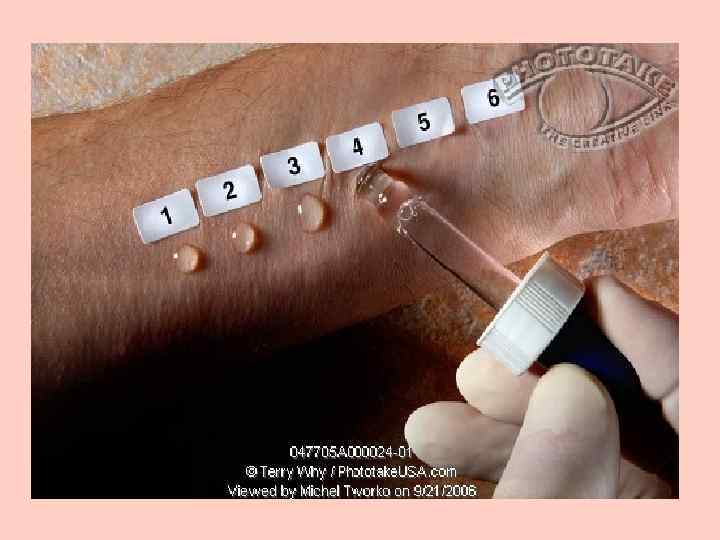

Общая характеристика вакцинных препаратов Вакцины - препараты, полученные из бактерий, вирусов и других микроорганизмов, их химических компонентов, продуктов жизнедеятельности или искусственным путем, которые применяются для активной иммунизации людей и животных с целью профилактики и лечения инфекционных болезней. Классификация вакцин 1. Живые (аттенуированные) вакцины 2. Убитые (инактивированные) вакцины 3. Химические, субединичные вакцины 4. Анатоксины 5. Рекомбинантные вакцины 6. Векторные вакцины 7. Антиидиотипные вакцины

Живые вакцины – биологические препараты, изготовленные из живых бактерий или вирусов с сниженной вирулентностью, но вира же ими иммуногенными свойствами. Они не способны в обычных условиях вызывать заболевания, но слабый инфекционный процесс при этом имеет место. Поэтому живые вакцины, как наиболее эффективные препараты для прививки, индуктируют долговременный и напряженный поствакцинальный иммунитет. Достаточно однократного введения препарата, чтобы развилась невосприимчивость к возбудителю. Живые вакцины можно получить путем аттенуации (ослабление вирулентности) или путем селекции. Л. Пастер впервые разработал метод аттенуации вирулентных свойств микроорганизмов и получил первые живые вакцины (против сибирки, бешенства и куриной холеры).


Инактивированные вакцины В отличие от живых, убитые (инактивированные) вакцины готовят из наиболее вирулентных штаммов с ярко выраженными антигенными свойствами. Для инактивации микроорганизмы подвергают действиям разнообразных физических и химических факторов. Однако инактивация должна быть щадящей, чтобы не допустить разрушения самых важных антигенных структур бактерий. Препараты поддают обязательной проверке на стерильность, антигенность, иммуногенность, реактогенность и т. п. Убитые вакцины менее иммуногенные, чем живые, их эффективность значительно ниже. Из убитых вакцин в данное время используют лептоспирозную, гонококковую, гриппозную, полиомиелитную Солка, японского энцефалита, клещевого энцефалита, антирабическую.

Анатоксины При многих инфекционных заболеваниях решающую патогенетическую роль играют бактериальные токсины. Поэтому для их предупреждения необходимо иммунизировать организм препаратом, который получают из токсинов. Анатоксины - препараты, которые получают из бактериальных белковых токсинов при действии на них формалина (0, 3 -0, 5 %) в течение 3 -4 недель при температуре 39 -40 С. После такой обработки токсин теряет ядовитые свойства, но сохраняет антигенные. Микробиологическая промышленность выпускает столбнячный, дифтерийный, ботулиновые, гангренозные, стафилококковый и холерный анатоксины.

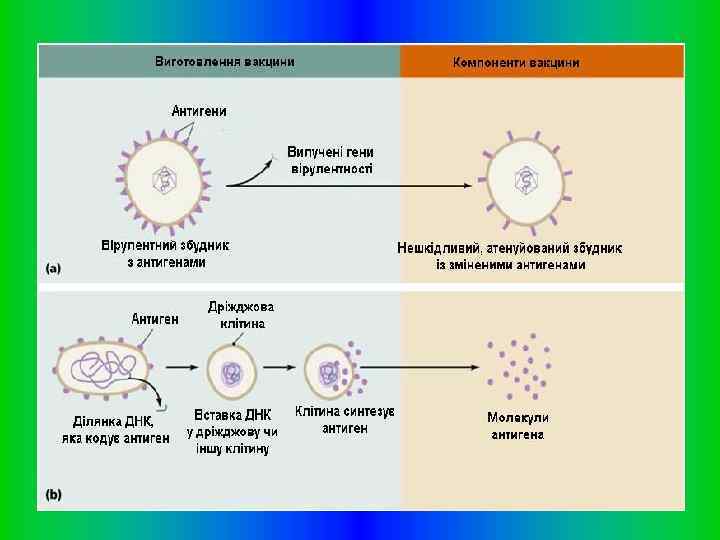
Субединичные вакцины – вакцины, которые содержат лишь отдельные компоненты патогенного микроорганизма. Для их создания успешно используется технология рекомбинантных ДНК. Преимуществами таких вакцин является то, что они содержат очищенный иммуногенный белок, они безопасные, не способны вызывать заболевания, стабильные. Их химические свойства известны, в их составе отсутствуют другие белки и нуклеиновые кислоты, которые могли бы вызывать нежелательные побочные эффекты в организме.

РЕКОМБИНАНТНЫЕ ВАКЦИНЫ Искусственное копирование антигенов и детерминант методами генной инженерии может способствовать созданию вакцин без балластных примесей. Для получения антигенов с необходимыми детерминантами без посторонних субстанций существует два направления: 1) выделение высокоочищенного антигена с естественного материала методами биохимии препарата или генной инженерии; 2) химический синтез антигенных детерминант. Как правило, виделяют или конструируют протективные антигены, адгезины, ферменты, протеины оболочки, токсины. Основой таких рекомбинантных вакцин является перенос в плазмиды или вирус гена, ответственного за продукцию необходимого антигена. Такие препараты разделяют на генноинженерные вакцины из антигенов, синтезированных в рекомбинантных бактериальных системах и дрожжах; векторные генно- инженерные живые вакцины на основе вируса осповакцины и другие.

Векторные вакцины чаще всего готовятся на основе вируса осповакцины. В геном вируса одновременно вносят гены, которые кодируют антигенные детерминанты разных возбудителей (вирусов бешенства, гриппа, ВИЧ, гепатита В, простого герпеса и т. п). Прививку осуществляют таким модифицированным вирусом осповакцины. В качестве векторов также используют аденовирусы, полиовирус, вирус ветрянки. Таким образом, векторные вакцины позволяют провести иммунизацию одномоментно против нескольких заболеваний, индуктируя эффективный иммунный ответ.

Основные виды побочного действия вакцин: 1. Фармакологическое действие. Вакцины вызывают выделение разнообразных медиаторов, которые имеют выраженный фармакологический эффект. Например, интерферон вызывает лихорадку, гранулоцитопению и токсичные явления в центральной нервной системе, а интерлейкин - 1 является одним из факторов воспаления. 2. Поствакцинальный инфекционный процесс. Причиной инфекционного процесса при вакцинации является остаточная вирулентность вакцинного штамма и реверсия его патогенных свойств. Как пример таких осложнений могут быть лимфадениты и остеомиелиты, которые иногда возникают после введения вакцины БЦЖ.

3. Туморогенное действие. В связи с развитием биотехнологии и рекомбинантной техники, использованием клеточных линий и гибридом особенное значение приобретает безопасность генноинженерных вакцин в контексте влияния на генетический аппарат клетки. 4. Аллергия. Вакцины содержат разнообразные сенсибилизирующие субстанции. Столбнячный анатоксин способен вызывать атопию. Большинство вакцин содержат разные примеси: гетерологический белок, консерванты, ростовые факторы, стабилизаторы, сорбенты и т. п. Они могут быть причиной аллергических осложнений. 5. Имуномодулирующее действие. Многие возбудители (микобактерии, коринебактерии, возбудители коклюша и др. ) и бактериальные препараты (пептидогликан, ЛПС) владеют ярко выраженными неспецифическими иммуномодулирующими свойствами, которые влияют на развитие иммунного ответа к другим антигенам.

6. Индукция аутоиммунных состояний. Ряд вакцин (коклюшная) вызывают поликлональную актиацию и, таким образом, могут стимулировать образование аутоантител и специфических клонов лимфоцитов, направленных против собственных тканей. С другой стороны возникновение аутоиммунной патологии может быть связано с феном мимикрии, например, наличие общих антигенов у менингококковой вакцини-В и гликопротеином клеточных мембран млекопитающих. 7. Индукция иммунодефицитных состояний. При определенных условиях попадания вакцины в организм (срок, доза, и т. п. ) имеет место супрессия иммунного ответа, который зависит от способности микробных антигенов активировать клетки супрессоры, вызывать выделение супрессорных факторов.

Серотерапия и серопрофилактика Лечебно-профилактические сыворотки разделяют на антитоксичные, антимикробные и антивирусные. Нативные антитоксичные сыворотки (противостолбнячная, противодифтерийная, противоботулиновые, противогангренозные и др. ) готовят в научно-исследова тельских институтах путем гипериммунизации лошадей соответствующими анатоксинами (дифтерийными, ботулиновыми, гангренозными и т. п. ). Антимикробные (антивирусные) сыворотки изготовляют путем гипериммунизации животных соответствующими убитыми бактериями (вирусами) или их антигенами. В последнее время вместо нативних антитоксичных и антимикробных (антивирусных) сывороток изготовляют соответствующие гамма-глобулины.

Различают гамма-глобулины специфического действия и нормальный гамма-глобулин. К гамма-глобулинам специфического действия относятся: противостолбнячный, противодифтерийный, противостафилококковый и др. Нормальный гамма-глобулин получают из плазмы крови нескольких тысяч здоровых доноров и используют для предупреждения респираторных инфекций у детей, для профилактики гепатита А, эпидемического паротита, кори, ветрянки. Очищая гамма-глобулины от неспецифических антител, получают иммуноглобулины направленного действия (антистафилококковый, против синегнойной палочки). Иммуноглобулины человека: противогриппозный, противококлюшный, противодифтерийный, противостолбнячный, против клещевого энцефалита, ветряной оспы, гепатита А, противостафилококковый, противоботулиновые. Гетерологичные сыворотки и иммуноглобулины: противодифтерийная, противостолбнячная, противоботулиновые А, В, Е, противогангренозные лошадиные; антирабический иммуноглобулин, противосибироязвенный иммуноглобулин, полученные из сыворотки лошадей, иммуноглобулин против клещевого энцефалита.
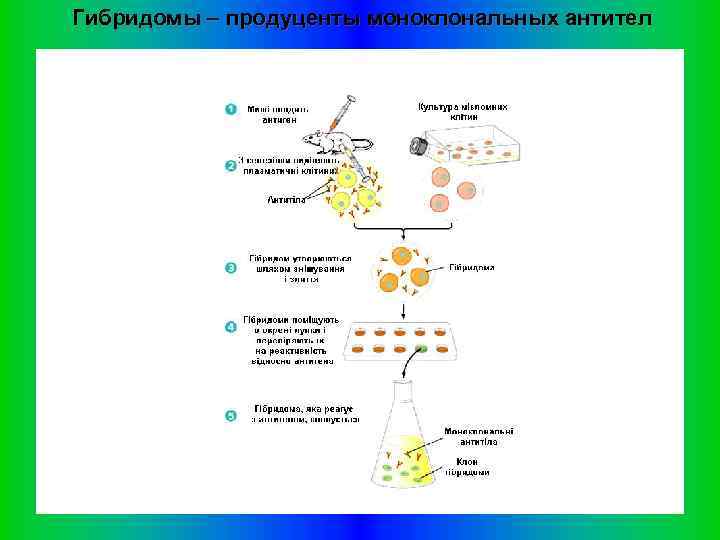
Гибридомы – продуценты моноклональных антител
05_учение об иммунитете-1.ppt