Состав, свойства воды.ppt
- Количество слайдов: 30

Учение о гидросфере

Минерал рингвудит имеет голубой оттенок n Вода эта содержится в горной породе рингвудит, которая залегает на глубине 700 км в земной мантии. Это форма уже давно известного минерала оливина, из которого в основном состоит земная мантия.

Содержание воды В современную эпоху основные запасы воды сосредоточены в Мировом океане (96. 5%). Пресных вод 2. 58% от общих запасов воды. В ледниках и снежном покрове Антарктиды, Арктики и горных стран 1. 78% объема гидросферы или 69. 3% от запасов пресных вод на Земле. Громадные запасы воды аккумулированы в литосфере. Доля пресных подземных вод от общего запаса пресных вод на земле составляет 29. 4%. На долю рек приходится 0. 006%, пресных озер – 0. 25%, на воду, содержащуюся в атмосфере - 0. 03% от общего количества пресных вод
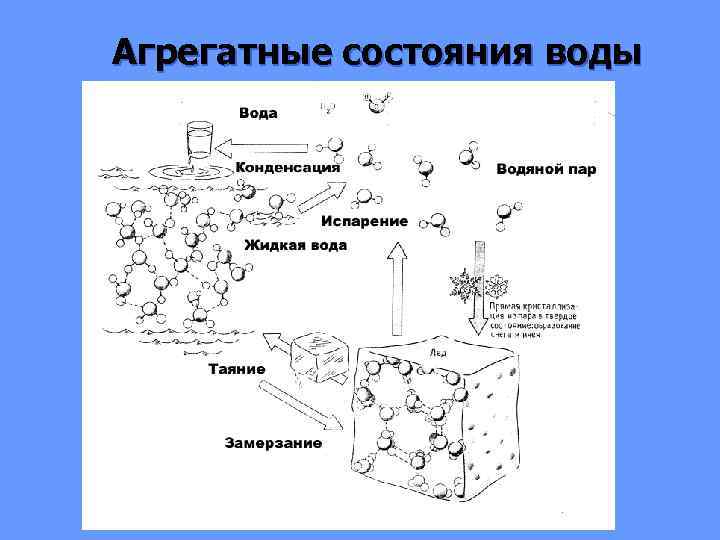
Агрегатные состояния воды

Переход воды из одного состояния в другое сопровождается затратами (испарение, таяние) или выделением (конденсация, замерзание) соответствующего количества тепла. На таяние 1 г льда - 677 кал, на испарение 1 г воды — 597 кал.
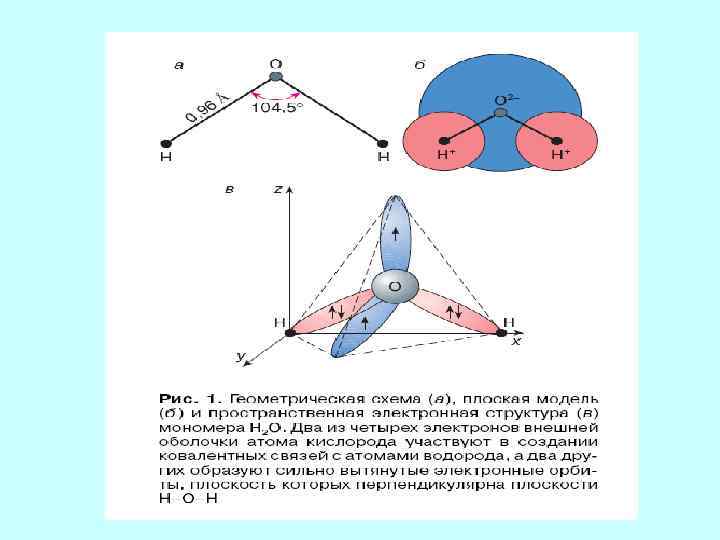

Аномальные свойства воды вызваны наличием водородных связей. Ион водорода, связанный с какимто ионом другого элемента, способен электростатически притягивать к себе ион того же элемента из другой молекулы.

У гидридов (элементы VI группы селена H 2 Se, теллура Н 2 Те) температура кипения воды должна быть — 60° С, температура замерзания — ниже 100° С.

Аномальные свойства воды • высокая скрытая теплота плавления должна быть порядка – 60° С, а температура замерзания – ниже 100° С, но при нормальном давлении в 1 атм вода кипит при +100° С, а замерзает при 0° С, • максимальная плотность дистиллированной воды наблюдается при +4° С), т. е. при и температуре выше точки затвердевания (замерзания), • при возрастании температуры от 0 до 4°С объем нагреваемой воды уменьшается и только при дальнейшем возрастании начинает увеличиваться, • высокая теплоемкость в 3000 раз больше, чем воздух. При охлаждении 1 м 3 воды на 1° С на столько же нагревается З 000 м 3 воздуха, • у воды самое высокое поверхностное натяжение и поверхностное давление, • высокая термической устойчивость, • плохой проводник электричества, • вследствие малой сжимаемости в воде хорошо распространяются звуковые и ультразвуковые волны, • универсальный природный растворитель.


Структура льда • В жидкой воде имеются ассоциаты – зародыши кристаллических образований, существующие очень короткий промежуток времени. • Лед - наименее плотная водная структура. • Размеры пустот превышают размеры молекул воды. • Упаковка молекул становится более плотной. Поэтому при плавлении льда объем, занимаемый водой уменьшается, а ее плотность возрастает. • При +4 С вода имеет самую плотную упаковку.

Формы молекул воды • Молекулярный вес от 18 до 22 • Изотопы кислорода и водорода (дейтерий, тритий). • Обычная вода с массой 18, тяжелая вода с – 20, составляя менее 0. 02% всех запасов воды. • Присутствие тяжелой воды придает "обычной" воде большую плотность.

Влияние давления и температуры При росте давления • температура кипения воды повышается, • температура замерзания понижается. С повышением температуры • уменьшаются поверхностное натяжение, плотность и вязкость воды, • возрастают электропроводность и скорость звука в воде.

Вода - самый универсальный природный растворитель • Лучше всего она растворяет соли, • Электрические заряды ионов значительно больше, чем заряды на полюсах молекул воды, поэтому в отсутствие воды они формируют кристаллы с очень плотно упакованными молекулами.

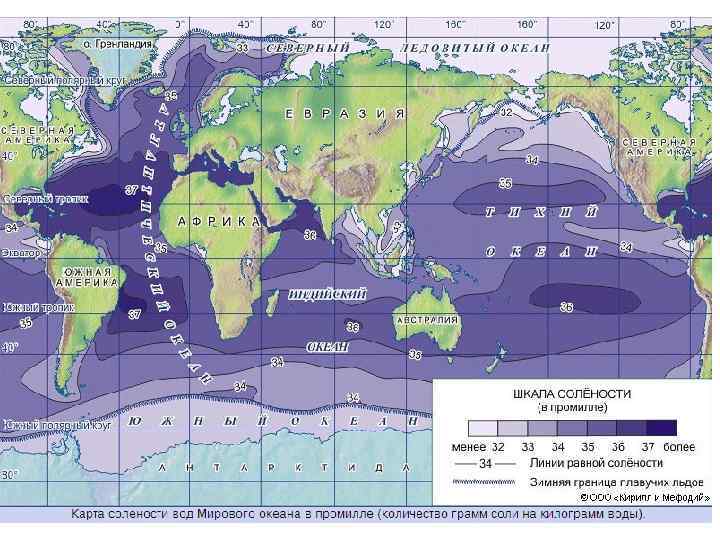
Соленость Общее количество твердых веществ в граммах на килограмм морской воды при условии, что все карбонаты переведены в оксиды, бром и йод замещены хлором и все органическое вещество окислено. Ш Относительное содержание различных солей, растворенных в морской воде, постоянно. Ш Соленость = 1, 80655 х Хлорность Ш Ш водах мировых морей и океанов В содержится количество соли, равное столбу диаметром 1 км, высотой в 47 раз больше расстояния от Земли до Луны.

Ш Соленость выражают в количестве граммов солей на 1000 г морской воды, т. е. в тысячных долях общего веса воды. Ш Единица измерения поэтому называется промилле (дословно "тысячная доля") и обозначается знаком %о.

Соленость Характерное для морских вод постоянство соотношения ионов нарушается при солености ниже 5— 8%о и выше 42— 45%о. Ниже 5— 8%0 и выше 42— 45°/00 соленость действует как осмотический и рапический фактор одновременно, тогда как внутри этого диапазона, очень широкого и охватывающего основную массу морских и океанических вод, соленость действует только как фактор осмотический.
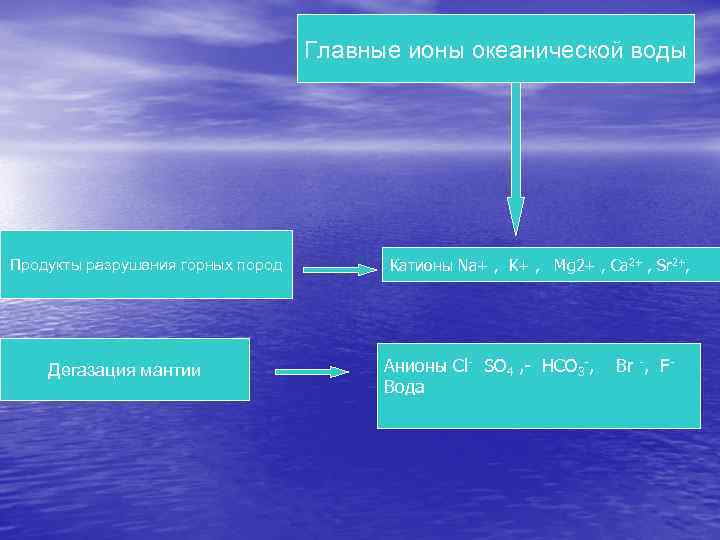
Главные ионы океанической воды Продукты разрушения горных пород Дегазация мантии Катионы Na+ , K+ , Mg 2+ , Ca 2+ , Sr 2+, Анионы Cl- SO 4 , - HCO 3 -, Вода Br -, F-
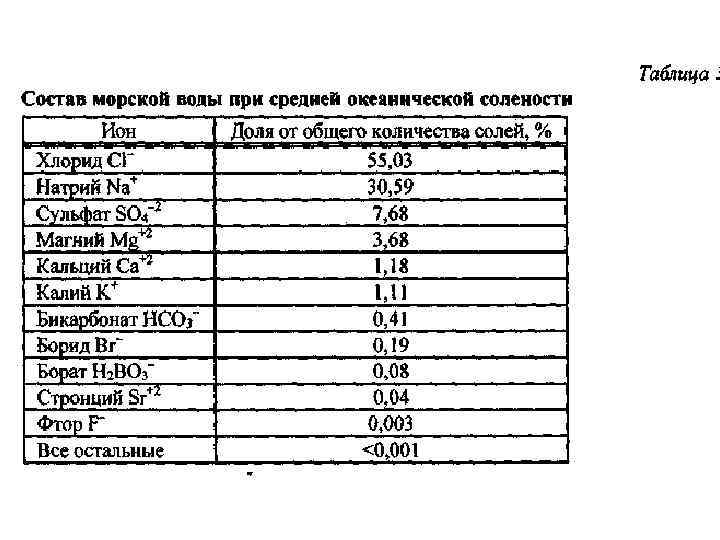

Венецианская классификация природных вод по степени солености

Средиземном море 39 ‰ Красное море 41‰ Черное и Балтийское 3 – 23 ‰. Тихий океан 34. 6 – 34. 7‰ Атлантический океан 35. 4‰.

Состав воды • Биогенные вещества • Микроэелементы (все металлы, кроме главных • • ионов и железа (Cu 2+ , Mn 2+), другие ионы переходных металлов), а также ионы (Br- , F-, I- и др. ). Растворенные газы (O 2, СO 2, N 2, H 2 S, CH 4). В противоположность твердым веществам газы лучше растворяются в холодной воде и плохо – в теплой. Поэтому дефицит кислорода и связанные с ним заморные явления чаще наблюдаются в теплых водах.

CO 2 • Основным резервуаром СО 2 в биосфере является карбонатная • • система океанов. Источник питательных веществ Буфер, поддерживающий концентрацию водородных ионов в водных средах на уровне, близком к нейтральному значению. Небольшое повышение содержания СО 2 в воде повышает интенсивность фотосинтеза и стимулирует процессы развития многих организмов. Высокие концентрации СО 2 определенно могут быть лимитирующим фактором лишь для животных, особенно потому, что высокое содержание двуокиси углерода обычно связано с низким содержанием кислорода. Рыбы весьма чувствительны к повышению концентрации СО 2: при слишком высоком содержании свободного СО 2 в воде многие рыбы погибают.
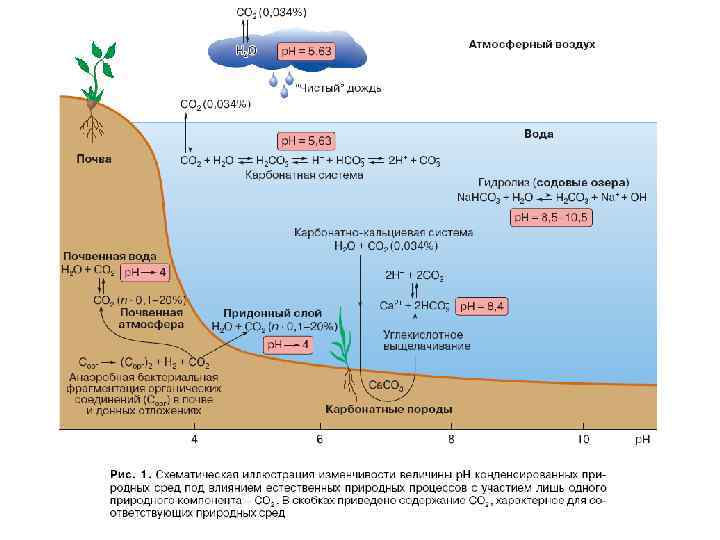

Кислотность (p. H) • Водородный показатель (p. H) – это величина, • характеризующая кислотность воды. Он определяется как концентрации ионов водорода (-lg H+) в воде при 22°С, выраженный в молях на литр. В морских водах p. H преимущественно изменяется в незначительных пределах – 6 -7.
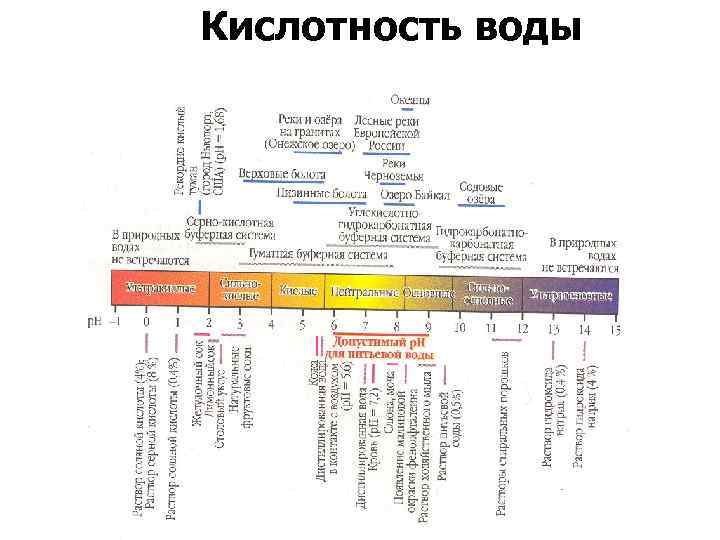
Кислотность воды

Давление • Вода во много раз тяжелее воздуха, давление с глубиной • • растет очень быстро. Давление на дне глубоководных океанических желобов достигает тысячи атмосфер. При погружении на каждые 10 м давление увеличивается на одну атмосферу. Если давление на суше и у поверхности воды равно одной атмосфере, то уже на глубине 10 м оно удваивается. растворимость газов с ростом давления увеличивается. При резком изменении давления избыток газа не успевает диффундировать в окружающую среду, и газ выделяется в виде пузырьков. Свободные пузырьки газа, появившиеся в жизненно важных органах, становятся причиной гибели организма. Это явление известно в водолазном деле и называется кессонной болезнью.
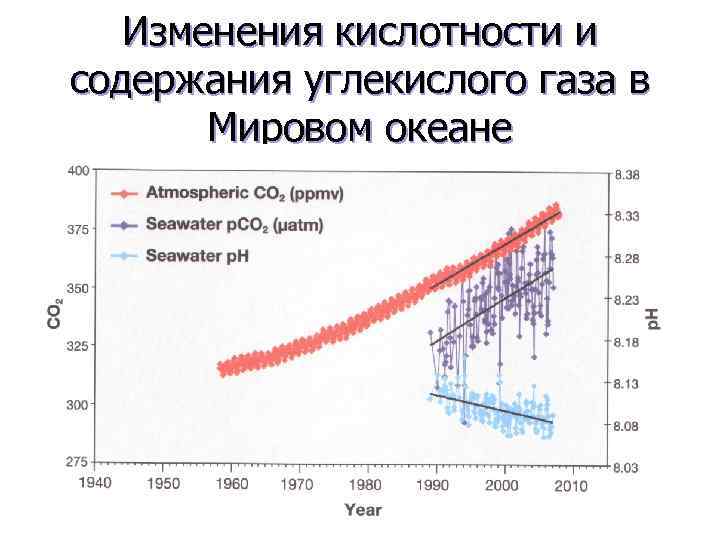
Изменения кислотности и содержания углекислого газа в Мировом океане
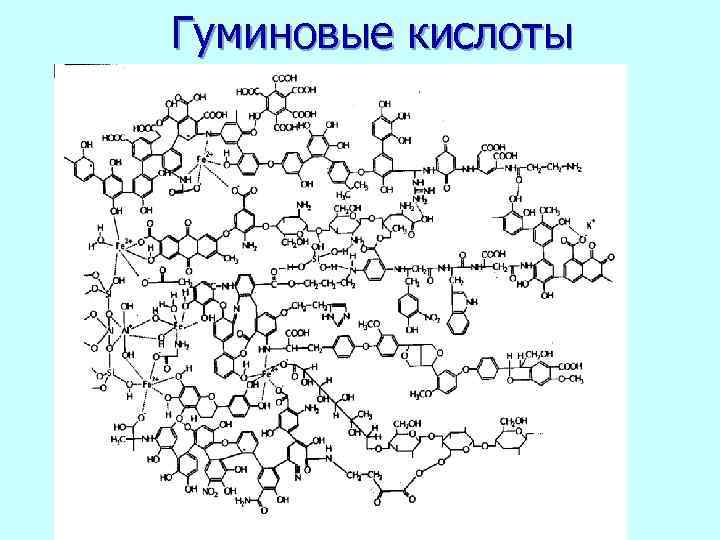
Гуминовые кислоты
Состав, свойства воды.ppt