Лк.2. Химические и физические свойства вод.ppt
- Количество слайдов: 61
 Учение о гидросфере Лекция № 2 Химические и физические свойства природных вод
Учение о гидросфере Лекция № 2 Химические и физические свойства природных вод
 План: 1. Вода как химическое соединение, ее молекулярная структура и изотопный состав. 2. Химические свойства природных вод. 3. Понятие о качестве воды. 4. Физические свойства природных вод. Агрегатные состояния воды: жидкая вода, водяной пар, лед. Фазовые переходы. 5. Плотность воды и ее зависимость от температуры, минерализации и давления. 6. Тепловые свойства воды. 7. Вязкость воды. Поверхностное натяжение. 8. Общие закономерности распространения света и звука в воде. 9. Гидрологическое и физико-географическое значение физических свойств и «аномалий» воды.
План: 1. Вода как химическое соединение, ее молекулярная структура и изотопный состав. 2. Химические свойства природных вод. 3. Понятие о качестве воды. 4. Физические свойства природных вод. Агрегатные состояния воды: жидкая вода, водяной пар, лед. Фазовые переходы. 5. Плотность воды и ее зависимость от температуры, минерализации и давления. 6. Тепловые свойства воды. 7. Вязкость воды. Поверхностное натяжение. 8. Общие закономерности распространения света и звука в воде. 9. Гидрологическое и физико-географическое значение физических свойств и «аномалий» воды.
 Вода как химическое соединение, ее молекулярная структура и изотопный состав. Вода состоит из 11, 11% водорода и 88, 89% кислорода (по весу). При образовании воды с одним атомом кислорода соединяются два атома водорода – Н 2 О.
Вода как химическое соединение, ее молекулярная структура и изотопный состав. Вода состоит из 11, 11% водорода и 88, 89% кислорода (по весу). При образовании воды с одним атомом кислорода соединяются два атома водорода – Н 2 О.
 • Молекулы воды оказываются чрезвычайно устойчивыми, поскольку атомы кислорода и водорода связаны друг с другом посредством образования электронных пар. Это так называемая ковалентная связь • Сконструированные наподобие магнитов молекулы воды и взаимодействуют как настоящие магниты, создавая пространственные структуры, так каждая вершина тетраэдра или лопасти может притянуть по одной молекуле воды, а всего — четыре молекулы. Электрические взаимодействия между водородом одной молекулы и сравнительно свободными парами электронов другой образуют так называемую водородную связь. Такие связи и возникающие пространственные структуры молекул определяют межмолекулярную структуру воды, которая служит одной из причин ее уникальности.
• Молекулы воды оказываются чрезвычайно устойчивыми, поскольку атомы кислорода и водорода связаны друг с другом посредством образования электронных пар. Это так называемая ковалентная связь • Сконструированные наподобие магнитов молекулы воды и взаимодействуют как настоящие магниты, создавая пространственные структуры, так каждая вершина тетраэдра или лопасти может притянуть по одной молекуле воды, а всего — четыре молекулы. Электрические взаимодействия между водородом одной молекулы и сравнительно свободными парами электронов другой образуют так называемую водородную связь. Такие связи и возникающие пространственные структуры молекул определяют межмолекулярную структуру воды, которая служит одной из причин ее уникальности.
 Вода гидросферы • это смесь нескольких разновидностей воды с общей формулой Н 2 О, представляющих собой соединения изотопов кислорода и водорода. Кроме обычного водорода (протий, Н) в природе встречается водород с массой 2, называемый дейтерий (D), и еще более тяжелый водород с массой 3, называемый тритий (Т). У кислорода выявлены, кроме обычного с атомным весом 16, еще два более тяжелых изотопа: с атомными весами 17 и 18. • Теоретически может существовать 42 разнообразных изотопных разновидностей воды, из которых только 7 устойчивы, т. е. не радиоактивны. 99, 73% гидросферы состоит из обычной воды с молекулярным составом H 2 О(16). Еще 0, 04% — это тяжелокислородная вода с составом Н 2 О(17) и 0, 02% — вода с составом Н 2 О(18). Доля тяжелой воды с составом DO 2 в природных водах составляет в среднем 1/6800, или примерно 0, 15 мл на 1 л природной воды.
Вода гидросферы • это смесь нескольких разновидностей воды с общей формулой Н 2 О, представляющих собой соединения изотопов кислорода и водорода. Кроме обычного водорода (протий, Н) в природе встречается водород с массой 2, называемый дейтерий (D), и еще более тяжелый водород с массой 3, называемый тритий (Т). У кислорода выявлены, кроме обычного с атомным весом 16, еще два более тяжелых изотопа: с атомными весами 17 и 18. • Теоретически может существовать 42 разнообразных изотопных разновидностей воды, из которых только 7 устойчивы, т. е. не радиоактивны. 99, 73% гидросферы состоит из обычной воды с молекулярным составом H 2 О(16). Еще 0, 04% — это тяжелокислородная вода с составом Н 2 О(17) и 0, 02% — вода с составом Н 2 О(18). Доля тяжелой воды с составом DO 2 в природных водах составляет в среднем 1/6800, или примерно 0, 15 мл на 1 л природной воды.
 • Разница в изотопном составе сказывается на физических свойствах воды. Так, тяжелая вода имеет плотность 1, 104 г/см 3, кипит при 101, 43°С, а лед из тяжелой воды плавится при 3, 813 °С. Тяжелая вода испаряется медленнее, чем обыкновенная, и, может быть, поэтому в некоторых замкнутых водоемах происходит обогащение тяжелой водой. Эксперименты показывают, что она угнетает растения, а в больших дозах даже вызывает их гибель. • При О °С вода состоит из мономеров Н 2 О только частично, большая же ее часть при этой температуре состоит из тримеров (Н 2 О)3, в то время как при температуре 4 °С основную массу воды составляют димеры (Н 2 О)2. (помните про домашнее задание с круговыми диаграммами, которое проверю завтра? )
• Разница в изотопном составе сказывается на физических свойствах воды. Так, тяжелая вода имеет плотность 1, 104 г/см 3, кипит при 101, 43°С, а лед из тяжелой воды плавится при 3, 813 °С. Тяжелая вода испаряется медленнее, чем обыкновенная, и, может быть, поэтому в некоторых замкнутых водоемах происходит обогащение тяжелой водой. Эксперименты показывают, что она угнетает растения, а в больших дозах даже вызывает их гибель. • При О °С вода состоит из мономеров Н 2 О только частично, большая же ее часть при этой температуре состоит из тримеров (Н 2 О)3, в то время как при температуре 4 °С основную массу воды составляют димеры (Н 2 О)2. (помните про домашнее задание с круговыми диаграммами, которое проверю завтра? )
 Аномалия точек кипения и замерзания воды в сравнении с другими соединениями водорода, обладающими похожей молекулярной структурой • Аналогом кислорода по таблице Менделеева служит ряд: сера (S), селен (Se), теллур (Те). Их соединения с водородом, подобные воде, называют гидратами: H 2 S, H 2 Se и Н 2 Те. Заряд ядра определяет физические свойства веществ этого ряда. Действительно, если Н 2 Те (вещество с самым тяжелым молекулярным весом этого ряда) кипит при 4 °С, а замерзает при 51 °С, то два других, более легких, соединения (H 2 Se и H 2 S) кипят и замерзают при более низкой температуре, прямо пропорциональной их молекулярным весам. Но самое легкое из этого ряда соединений — вода — не признает никаких закономерностей: она должна была бы замерзать при 90°С, а она замерзает при 0°С, кипеть при 70°С, а она кипит при 100°С.
Аномалия точек кипения и замерзания воды в сравнении с другими соединениями водорода, обладающими похожей молекулярной структурой • Аналогом кислорода по таблице Менделеева служит ряд: сера (S), селен (Se), теллур (Те). Их соединения с водородом, подобные воде, называют гидратами: H 2 S, H 2 Se и Н 2 Те. Заряд ядра определяет физические свойства веществ этого ряда. Действительно, если Н 2 Те (вещество с самым тяжелым молекулярным весом этого ряда) кипит при 4 °С, а замерзает при 51 °С, то два других, более легких, соединения (H 2 Se и H 2 S) кипят и замерзают при более низкой температуре, прямо пропорциональной их молекулярным весам. Но самое легкое из этого ряда соединений — вода — не признает никаких закономерностей: она должна была бы замерзать при 90°С, а она замерзает при 0°С, кипеть при 70°С, а она кипит при 100°С.
 Химические свойства природных вод. Вода как растворитель. • Вода самый сильный природный растворитель: в воде растворяются в той или иной мере почти все вещества. Сильный разнос центров положительных и отрицательных зарядов в молекуле воды приводит к тому, что молекулы ориентируются в электрическом поле, стремясь нейтрализовать его. Иными словами, обладают высоким дипольным моментом, что обеспечивает уникально большую диэлектрическую постоянную воды, наиболее высокую среди всех жидкостей. В результате любые заряды в воде отталкиваются или притягиваются с силой, в 80 раз большей, чем в вакууме. Это обеспечивает высокую растворимость веществ в воде, так как молекулы воды «растаскивают» частицы или ионы веществ, сила притяжения между которыми ослаблена.
Химические свойства природных вод. Вода как растворитель. • Вода самый сильный природный растворитель: в воде растворяются в той или иной мере почти все вещества. Сильный разнос центров положительных и отрицательных зарядов в молекуле воды приводит к тому, что молекулы ориентируются в электрическом поле, стремясь нейтрализовать его. Иными словами, обладают высоким дипольным моментом, что обеспечивает уникально большую диэлектрическую постоянную воды, наиболее высокую среди всех жидкостей. В результате любые заряды в воде отталкиваются или притягиваются с силой, в 80 раз большей, чем в вакууме. Это обеспечивает высокую растворимость веществ в воде, так как молекулы воды «растаскивают» частицы или ионы веществ, сила притяжения между которыми ослаблена.
 Процессы, происходящие в воде при растворении • Если в дистиллированной воде растворить обычную поваренную соль (Na. Cl) с таким расчетом, чтобы получился 1 кг морской воды, то понижение температуры воды будет соответствовать потере примерно 2514 Дж. Кроме того, объем раствора окажется меньше суммы первоначальных объемов воды и соли. Раствор как бы сожмется. Это явление называется электрострикцией. Каждый ион в растворе обволакивают молекулы воды — гидратируют его.
Процессы, происходящие в воде при растворении • Если в дистиллированной воде растворить обычную поваренную соль (Na. Cl) с таким расчетом, чтобы получился 1 кг морской воды, то понижение температуры воды будет соответствовать потере примерно 2514 Дж. Кроме того, объем раствора окажется меньше суммы первоначальных объемов воды и соли. Раствор как бы сожмется. Это явление называется электрострикцией. Каждый ион в растворе обволакивают молекулы воды — гидратируют его.
 • Одни ионы и частицы уплотняют воду, а другие могут делать ее более рыхлой. • К разуплотняющим воду веществам, которые снижают давление внутри нее, относятся ионы калия, рубидия, цезия, брома, йода.
• Одни ионы и частицы уплотняют воду, а другие могут делать ее более рыхлой. • К разуплотняющим воду веществам, которые снижают давление внутри нее, относятся ионы калия, рубидия, цезия, брома, йода.
 Вода — это инертный растворитель, который обычно не вступает в реакцию с растворенным веществом. • Природные растворы в одних случаях бывают насыщенными и даже перенасыщенными, а в других случаях — слабыми; иногда они равновесные, а иногда — неравновесные. Чем быстрее жидкая вода движется по поверхности суши, тем дальше она от насыщения растворенными веществами (поэтому реки обладают способностью к самоочищению). Но большая часть гидросферы малоподвижна, а потому она соленая и близка к равновесию.
Вода — это инертный растворитель, который обычно не вступает в реакцию с растворенным веществом. • Природные растворы в одних случаях бывают насыщенными и даже перенасыщенными, а в других случаях — слабыми; иногда они равновесные, а иногда — неравновесные. Чем быстрее жидкая вода движется по поверхности суши, тем дальше она от насыщения растворенными веществами (поэтому реки обладают способностью к самоочищению). Но большая часть гидросферы малоподвижна, а потому она соленая и близка к равновесию.
 Растворенные в воде вещества, изменяя ее структуру, меняют и свойства. • Электропроводность растворов обычно возрастает в десятки тысяч раз, что объясняется появлением в воде большого количества ионов, переносящих электрические заряды. • Падает температура замерзания воды морская вода замерзает в среднем при температуре — 1, 9 °С. • Если в воду попадают тонкодисперсные частицы, не растворяющиеся в ней, то молекулы воды, вступая в контакт с адсорбирующей поверхностью, теряют свою подвижность, связываются с этой поверхностью, выделяя при этом внутреннюю кинетическую энергию, которую называют теплотой смачивания.
Растворенные в воде вещества, изменяя ее структуру, меняют и свойства. • Электропроводность растворов обычно возрастает в десятки тысяч раз, что объясняется появлением в воде большого количества ионов, переносящих электрические заряды. • Падает температура замерзания воды морская вода замерзает в среднем при температуре — 1, 9 °С. • Если в воду попадают тонкодисперсные частицы, не растворяющиеся в ней, то молекулы воды, вступая в контакт с адсорбирующей поверхностью, теряют свою подвижность, связываются с этой поверхностью, выделяя при этом внутреннюю кинетическую энергию, которую называют теплотой смачивания.
 Классификация природных вод по величине минерализации, то есть суммы найденных в воде ионов: пресные - до 1, 0 г/кг солоноватые - 1— 25 воды с морской соленостью - 25— 50 воды соленые (с соленостью выше морской) - выше 50 • Область пресных вод, установленная до 1 г/кг, основана на восприятии человеком вкуса солености при наличии ионов свыше 1 г/кг. • Граница в 25 г/кг между солоноватыми водами с морской соленостью установлена на том основании, что примерно при этой минерализации (24, 695) температуры замерзания и максимальной плотности воды равны между собой. А эти характеристики весьма важны для гидрологии. • Граница между водами с морской соленостью и солеными водами установлена потому, что в морях не наблюдается минерализации свыше 50 г/кг, более высокие ее величины характерны только для соляных озер и сильно минерализованных подземных вод.
Классификация природных вод по величине минерализации, то есть суммы найденных в воде ионов: пресные - до 1, 0 г/кг солоноватые - 1— 25 воды с морской соленостью - 25— 50 воды соленые (с соленостью выше морской) - выше 50 • Область пресных вод, установленная до 1 г/кг, основана на восприятии человеком вкуса солености при наличии ионов свыше 1 г/кг. • Граница в 25 г/кг между солоноватыми водами с морской соленостью установлена на том основании, что примерно при этой минерализации (24, 695) температуры замерзания и максимальной плотности воды равны между собой. А эти характеристики весьма важны для гидрологии. • Граница между водами с морской соленостью и солеными водами установлена потому, что в морях не наблюдается минерализации свыше 50 г/кг, более высокие ее величины характерны только для соляных озер и сильно минерализованных подземных вод.
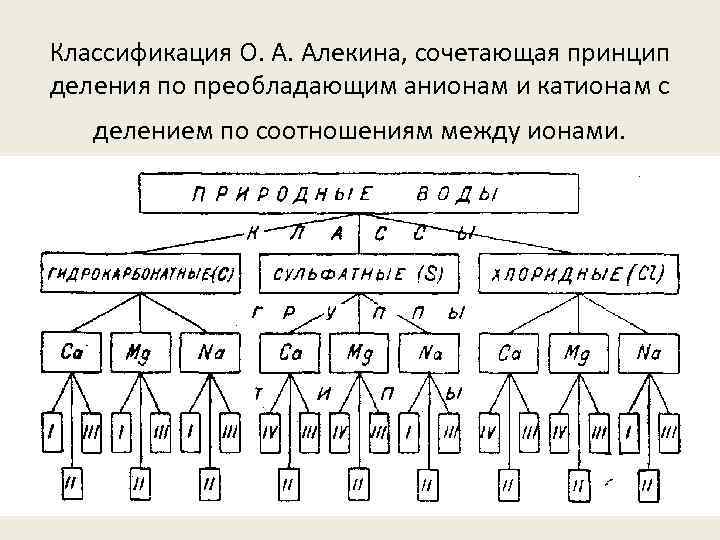 Классификация О. А. Алекина, сочетающая принцип деления по преобладающим анионам и катионам с делением по соотношениям между ионами.
Классификация О. А. Алекина, сочетающая принцип деления по преобладающим анионам и катионам с делением по соотношениям между ионами.
 • Первый тип: НСО 3 > Са + Мg. Чаще характерны для бессточных озер. • Второй тип: НСО 3 < Са + Мg < НСО 3 + S 04. К этому типу относится большинство рек, озер и подземных вод малой и умеренной минерализации. • Третий тип: НСО 3 + SO 4 < Са + Мg, или Cl > Na. К этому типу принадлежат воды океана, морей, лиманов, реликтовых водоемов и многих сильно минерализованных подземных вод. • Четвертый тип: НСО 3 = 0, т. е. воды этого типа кислые. Поэтому в класс карбонатных вод этот тип не входит, а его воды находятся только в сульфатном и хлоридном классах, в группах Са и Мg, где нет первого типа.
• Первый тип: НСО 3 > Са + Мg. Чаще характерны для бессточных озер. • Второй тип: НСО 3 < Са + Мg < НСО 3 + S 04. К этому типу относится большинство рек, озер и подземных вод малой и умеренной минерализации. • Третий тип: НСО 3 + SO 4 < Са + Мg, или Cl > Na. К этому типу принадлежат воды океана, морей, лиманов, реликтовых водоемов и многих сильно минерализованных подземных вод. • Четвертый тип: НСО 3 = 0, т. е. воды этого типа кислые. Поэтому в класс карбонатных вод этот тип не входит, а его воды находятся только в сульфатном и хлоридном классах, в группах Са и Мg, где нет первого типа.
 Классификация вод по величине р. Н • Водород — самый распространенный химический элемент во Вселенной. • Известные свойства кислот независимо от их анионов будут характеризоваться наличием положительно заряженного иона водорода. Основания же независимо от катионов при электролитической диссоциации воды образуют гидроксильные ионы ОН, имеющие отрицательные заряды. • Концентрацию водородных ионов выражают в виде их логарифмов, взятых с обратным знаком, и обозначают символом р. Н. Следовательно, р. Н = lg (Н+). И кислую, и щелочную реакцию выражают концентрацией водородных ионов, так как их легче определять, чем концентрацию ионов гидроксильных. При р. Н = 7 реакция воды нейтральная, при р. Н < 7 — кислая, при р. Н > 7 — щелочная. • Величина р. Н в природных водах зависит от содержания в них различных форм угольной кислоты, от присутствия органических кислот, газов, микроорганизмов, от гидролиза солей и т. д.
Классификация вод по величине р. Н • Водород — самый распространенный химический элемент во Вселенной. • Известные свойства кислот независимо от их анионов будут характеризоваться наличием положительно заряженного иона водорода. Основания же независимо от катионов при электролитической диссоциации воды образуют гидроксильные ионы ОН, имеющие отрицательные заряды. • Концентрацию водородных ионов выражают в виде их логарифмов, взятых с обратным знаком, и обозначают символом р. Н. Следовательно, р. Н = lg (Н+). И кислую, и щелочную реакцию выражают концентрацией водородных ионов, так как их легче определять, чем концентрацию ионов гидроксильных. При р. Н = 7 реакция воды нейтральная, при р. Н < 7 — кислая, при р. Н > 7 — щелочная. • Величина р. Н в природных водах зависит от содержания в них различных форм угольной кислоты, от присутствия органических кислот, газов, микроорганизмов, от гидролиза солей и т. д.
 • Для большинства природных вод р. Н определяется главным образом соотношением концентраций угольной кислоты и ее ионов. Угольная кислота в воде диссоциирует с образованием ионов Н+. Угольная кислота является слабой кислотой и в нормальных условиях диссоциирует незначительно.
• Для большинства природных вод р. Н определяется главным образом соотношением концентраций угольной кислоты и ее ионов. Угольная кислота в воде диссоциирует с образованием ионов Н+. Угольная кислота является слабой кислотой и в нормальных условиях диссоциирует незначительно.
 Величины р. Н, наиболее характерные для разных природных вод. По значению р. Н природные воды в зависимости от назначения делят на несколько групп. Подземные воды по значению р. Н рационально делить на семь групп: 1) сильнокислые воды (р. Н < 3) ; 2) кислые воды (р. Н = 3 -5); 3) слабокислые воды (р. Н = 5 -6, 5); 4) нейтральные воды (р. Н = 6, 5 -7, 5): 5) слабощелочные воды (р. Н = 7, 5 -8, 5); 6) щелочные воды (р. Н = 8, 5 -9, 5); 7) сильнощелочные воды (р. Н > 9, 5). р. Н служит критерием для определения возможности существования в водных растворах многих компонентов (H 2 S, Si. О 3, тяжелых металлов и пр. ).
Величины р. Н, наиболее характерные для разных природных вод. По значению р. Н природные воды в зависимости от назначения делят на несколько групп. Подземные воды по значению р. Н рационально делить на семь групп: 1) сильнокислые воды (р. Н < 3) ; 2) кислые воды (р. Н = 3 -5); 3) слабокислые воды (р. Н = 5 -6, 5); 4) нейтральные воды (р. Н = 6, 5 -7, 5): 5) слабощелочные воды (р. Н = 7, 5 -8, 5); 6) щелочные воды (р. Н = 8, 5 -9, 5); 7) сильнощелочные воды (р. Н > 9, 5). р. Н служит критерием для определения возможности существования в водных растворах многих компонентов (H 2 S, Si. О 3, тяжелых металлов и пр. ).
 Главные ионы в водах и их происхождение • К числу главных ионов, содержащихся в природных. водах, относятся ионы Cl, SO 4, HCO 3, Na, Mg, Ca и K, которые образуют основную часть их минерального состава. Главные ионы определяют химический тип вод, иначе их называют макрокомпонентами. • Микрокомпоненты содержатся в водах в гораздо меньших количествах и не определяют химического типа воды. Ряд компонентов, растворенных в водах, занимает промежуточное положение между макро и микрокомпонентами. К их числу относятся Н, NH 4, NO 3, H 2 Si. O 3. • Массовая концентрация главных ионов в весьма пресных водах выражается первыми единицами миллиграммов в литре, в рассолах же достигает нескольких сотен граммов на 1 кг (промилле, %о).
Главные ионы в водах и их происхождение • К числу главных ионов, содержащихся в природных. водах, относятся ионы Cl, SO 4, HCO 3, Na, Mg, Ca и K, которые образуют основную часть их минерального состава. Главные ионы определяют химический тип вод, иначе их называют макрокомпонентами. • Микрокомпоненты содержатся в водах в гораздо меньших количествах и не определяют химического типа воды. Ряд компонентов, растворенных в водах, занимает промежуточное положение между макро и микрокомпонентами. К их числу относятся Н, NH 4, NO 3, H 2 Si. O 3. • Массовая концентрация главных ионов в весьма пресных водах выражается первыми единицами миллиграммов в литре, в рассолах же достигает нескольких сотен граммов на 1 кг (промилле, %о).
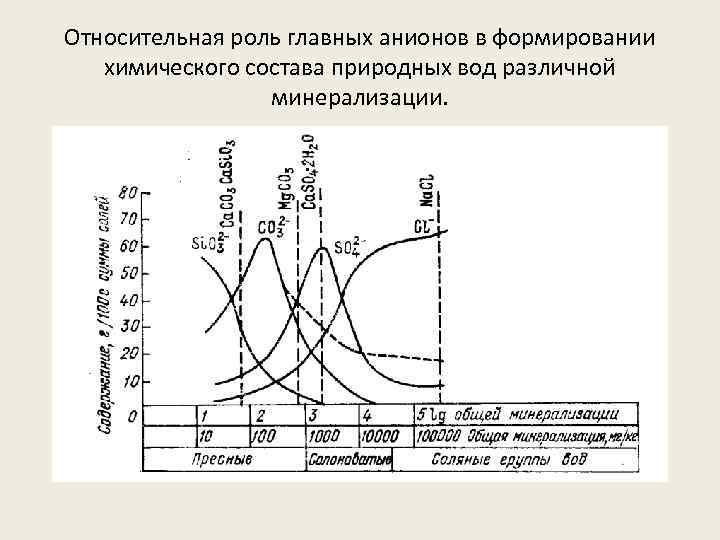 Относительная роль главных анионов в формировании химического состава природных вод различной минерализации.
Относительная роль главных анионов в формировании химического состава природных вод различной минерализации.
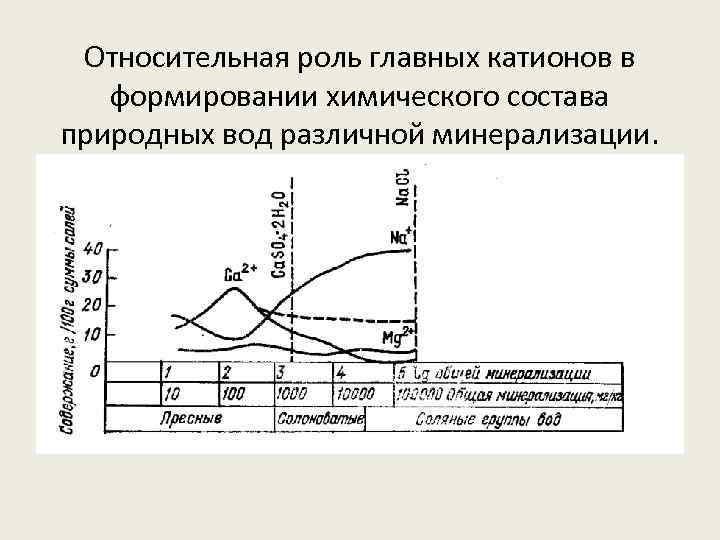 Относительная роль главных катионов в формировании химического состава природных вод различной минерализации.
Относительная роль главных катионов в формировании химического состава природных вод различной минерализации.
 Понятие о качестве воды Вода для хозяйственно-питьевых целей • При установлении норм хозяйственно питьевых вод принимается во внимание минерализация (сухой остаток), содержание макро и микрокомпонентов, физические свойства воды и ее санитарное состояние. К питьевой воде предъявляются следующие требования: • она должна быть прозрачной, бесцветной, освежающего вкуса и без запаха; • присутствие веществ, растворенных обычно в природной воде, не должно превышать некоторых пределов; • содержание вредных для здоровья человека веществ (меди, свинца, мышьяка и пр. ) не должно превышать установленных для этих компонентов значений; • вода должна быть свободной от болезнетворных микроорганизмов.
Понятие о качестве воды Вода для хозяйственно-питьевых целей • При установлении норм хозяйственно питьевых вод принимается во внимание минерализация (сухой остаток), содержание макро и микрокомпонентов, физические свойства воды и ее санитарное состояние. К питьевой воде предъявляются следующие требования: • она должна быть прозрачной, бесцветной, освежающего вкуса и без запаха; • присутствие веществ, растворенных обычно в природной воде, не должно превышать некоторых пределов; • содержание вредных для здоровья человека веществ (меди, свинца, мышьяка и пр. ) не должно превышать установленных для этих компонентов значений; • вода должна быть свободной от болезнетворных микроорганизмов.
 Вода для технических целей • Используемая в области производства вода имеет различное назначение. • В отличие от питьевых вод, при оценке качества технической воды прежде всего учитывается жесткость. • Жесткость воды, согласно введенному в настоящее время стандарту, выражается в миллимолях количества вещества эквивалента Са 2+ и Mg 2+, содержащихся в 1 л воды.
Вода для технических целей • Используемая в области производства вода имеет различное назначение. • В отличие от питьевых вод, при оценке качества технической воды прежде всего учитывается жесткость. • Жесткость воды, согласно введенному в настоящее время стандарту, выражается в миллимолях количества вещества эквивалента Са 2+ и Mg 2+, содержащихся в 1 л воды.
 Понятие о жесткости воды • По жесткости воды классифицируются следующим образом (в ммоль/л количества вещества эквивалента): Очень мягкие до 1, 5 Мягкие 1, 5— 3, 0 Средние 3, 0— 6, 0 Жесткие 6, 0— 10, 0 Очень жесткие более 10
Понятие о жесткости воды • По жесткости воды классифицируются следующим образом (в ммоль/л количества вещества эквивалента): Очень мягкие до 1, 5 Мягкие 1, 5— 3, 0 Средние 3, 0— 6, 0 Жесткие 6, 0— 10, 0 Очень жесткие более 10
 Оценка природных вод для орошения • Чтобы дать оценку пригодности воды для орошения, необходимо знать: 1) температуру, 2) минерализацию, 3) солевой состав и 4) ирригационный коэффициент. • Температура воды. Низкая температура является недостатком, так как задерживает рост растений. • Минерализация. Безвредной считается вода, содержащая не более 1— 1, 5 г/л растворенных солей. При содержании же солей от 1, 5 до 3, 0 г/л необходимо проведение на орошаемом массиве мелиоративных мероприятий. Предельная норма допустимого общего содержания солей в воде 5, 0 г/л.
Оценка природных вод для орошения • Чтобы дать оценку пригодности воды для орошения, необходимо знать: 1) температуру, 2) минерализацию, 3) солевой состав и 4) ирригационный коэффициент. • Температура воды. Низкая температура является недостатком, так как задерживает рост растений. • Минерализация. Безвредной считается вода, содержащая не более 1— 1, 5 г/л растворенных солей. При содержании же солей от 1, 5 до 3, 0 г/л необходимо проведение на орошаемом массиве мелиоративных мероприятий. Предельная норма допустимого общего содержания солей в воде 5, 0 г/л.
 • Солевой состав. Среди солей, растворенных в поливной воде, наиболее вредными считаются соли натрия. масс: Na 2 CO 3: Na. Cl: Na 2 SO 4= 1 : 3 : 10. Для хорошо водопроницаемых почв принимаются следующие предельные нормы содержания солей (в г/л): Na 2 CO 3— 1, 0, Na. Cl — 2, 0; Na 2 SO 4 — 5, 0. При совместном присутствии этих солей в поливной воде нормы снижаются. • Ирригационный коэффициент. Этот коэффициент был предложен Стеблером как критерий оценки качества ирригационной воды. Ирригационный коэффициент Ка вычисляется для каждого типа вод по концентрации соответствующих ионов в мг/л. Значением данных коэффициентов определяется качество воды: Ка > 18 — хорошее; от 18 до 6 — удовлетворительное; от 5, 9 до 1, 2— неудовлетворительное и при Ка < 1, 2 — плохое, т. е. вода является непригодной для орошения.
• Солевой состав. Среди солей, растворенных в поливной воде, наиболее вредными считаются соли натрия. масс: Na 2 CO 3: Na. Cl: Na 2 SO 4= 1 : 3 : 10. Для хорошо водопроницаемых почв принимаются следующие предельные нормы содержания солей (в г/л): Na 2 CO 3— 1, 0, Na. Cl — 2, 0; Na 2 SO 4 — 5, 0. При совместном присутствии этих солей в поливной воде нормы снижаются. • Ирригационный коэффициент. Этот коэффициент был предложен Стеблером как критерий оценки качества ирригационной воды. Ирригационный коэффициент Ка вычисляется для каждого типа вод по концентрации соответствующих ионов в мг/л. Значением данных коэффициентов определяется качество воды: Ка > 18 — хорошее; от 18 до 6 — удовлетворительное; от 5, 9 до 1, 2— неудовлетворительное и при Ка < 1, 2 — плохое, т. е. вода является непригодной для орошения.
 Физические свойства природных вод. Агрегатные состояния воды: жидкая вода, водяной пар, лед. Фазовые переходы. • Только воды в нормальных земных условиях может находится в трех агрегатных состояниях. • Жидкая вода в тонких слоях бесцветна, в толстых имеет голубовато зеленый оттенок. • Чистая вода, без примесей, почти не проводит электрический ток. • Температура замерзания дистиллирован ной воды принята за 0° С, а температура кипения при нормальном давлении за 100° С.
Физические свойства природных вод. Агрегатные состояния воды: жидкая вода, водяной пар, лед. Фазовые переходы. • Только воды в нормальных земных условиях может находится в трех агрегатных состояниях. • Жидкая вода в тонких слоях бесцветна, в толстых имеет голубовато зеленый оттенок. • Чистая вода, без примесей, почти не проводит электрический ток. • Температура замерзания дистиллирован ной воды принята за 0° С, а температура кипения при нормальном давлении за 100° С.
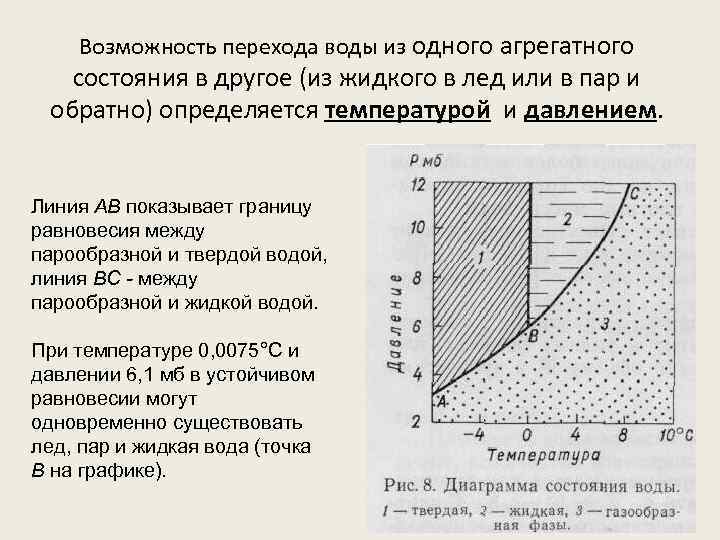 Возможность перехода воды из одного агрегатного состояния в другое (из жидкого в лед или в пар и обратно) определяется температурой и давлением. Линия АВ показывает границу равновесия между парообразной и твердой водой, линия ВС - между парообразной и жидкой водой. При температуре 0, 0075°С и давлении 6, 1 мб в устойчивом равновесии могут одновременно существовать лед, пар и жидкая вода (точка В на графике).
Возможность перехода воды из одного агрегатного состояния в другое (из жидкого в лед или в пар и обратно) определяется температурой и давлением. Линия АВ показывает границу равновесия между парообразной и твердой водой, линия ВС - между парообразной и жидкой водой. При температуре 0, 0075°С и давлении 6, 1 мб в устойчивом равновесии могут одновременно существовать лед, пар и жидкая вода (точка В на графике).
 Плотность и удельный объем. • Под плотностью воды понимается отношение ее массы m к объему V, занимаемому ею при данной температуре, т. е. = m/ V , где в г/см 3. • За единицу плотности принята плотность дистиллированной воды при 4° С. • Величина, обратная плотности, т. е. отношение единицы объема к единице массы, называется удельным объемом: • v = V/m где v - в см 3/г.
Плотность и удельный объем. • Под плотностью воды понимается отношение ее массы m к объему V, занимаемому ею при данной температуре, т. е. = m/ V , где в г/см 3. • За единицу плотности принята плотность дистиллированной воды при 4° С. • Величина, обратная плотности, т. е. отношение единицы объема к единице массы, называется удельным объемом: • v = V/m где v - в см 3/г.
 Плотность воды зависит от ее: • • температуры, минерализации, давления, количества взвешенных частиц и растворенных газов.
Плотность воды зависит от ее: • • температуры, минерализации, давления, количества взвешенных частиц и растворенных газов.
 Зависимость плотности воды от температуры: • С повышением температуры плотность всех жидкостей, как правило, уменьшается. Вода в этом отношении ведет себя аномально: при температурах выше 4° С плотность ее с повышением температуры уменьшается, а в интервале температур 0 4° С увеличивается. • Изменения плотности воды на один градус температуры в различных интервалах температуры неодинаковы. Они очень малы около температуры наибольшей плотности и быстро возрастают по мере удаления от нее. Так, при температуре, близкой к 4°С, изменение плотности воды на один градус температуры составляет 8*10 6, при температуре около 30°С до 3*10 4.
Зависимость плотности воды от температуры: • С повышением температуры плотность всех жидкостей, как правило, уменьшается. Вода в этом отношении ведет себя аномально: при температурах выше 4° С плотность ее с повышением температуры уменьшается, а в интервале температур 0 4° С увеличивается. • Изменения плотности воды на один градус температуры в различных интервалах температуры неодинаковы. Они очень малы около температуры наибольшей плотности и быстро возрастают по мере удаления от нее. Так, при температуре, близкой к 4°С, изменение плотности воды на один градус температуры составляет 8*10 6, при температуре около 30°С до 3*10 4.
 • При переходе воды из жидкого состояния в твердое (лед) плотность резко, скачкообразно изменяется приблизительно на 9%; плотность дистиллированной воды при 0°С равна 0, 99987, а плотность льда, образовавшегося из той же воды при 0°С, равна 0, 9167. • С понижением температуры плотность чистого льда несколько возрастает и при 20° С достигает 0, 92.
• При переходе воды из жидкого состояния в твердое (лед) плотность резко, скачкообразно изменяется приблизительно на 9%; плотность дистиллированной воды при 0°С равна 0, 99987, а плотность льда, образовавшегося из той же воды при 0°С, равна 0, 9167. • С понижением температуры плотность чистого льда несколько возрастает и при 20° С достигает 0, 92.
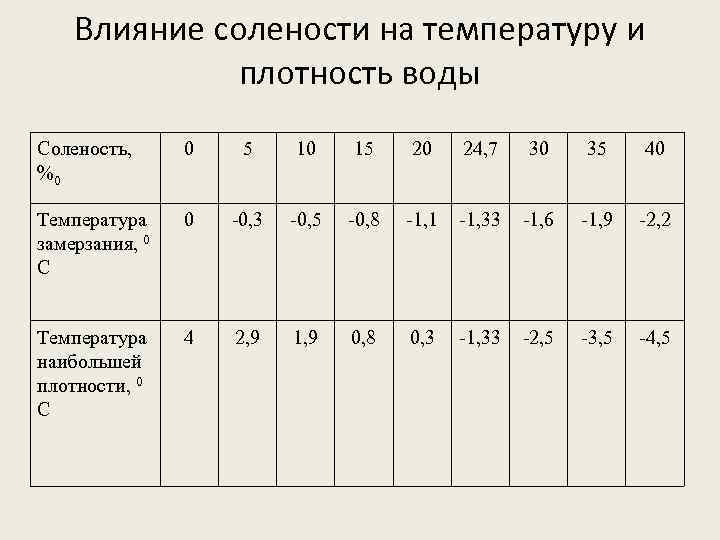 Влияние солености на температуру и плотность воды Соленость, %0 0 5 10 15 20 24, 7 30 35 40 Температура замерзания, 0 С 0 -0, 3 -0, 5 -0, 8 -1, 1 -1, 33 -1, 6 -1, 9 -2, 2 Температура наибольшей плотности, 0 С 4 2, 9 1, 9 0, 8 0, 3 -1, 33 -2, 5 -3, 5 -4, 5
Влияние солености на температуру и плотность воды Соленость, %0 0 5 10 15 20 24, 7 30 35 40 Температура замерзания, 0 С 0 -0, 3 -0, 5 -0, 8 -1, 1 -1, 33 -1, 6 -1, 9 -2, 2 Температура наибольшей плотности, 0 С 4 2, 9 1, 9 0, 8 0, 3 -1, 33 -2, 5 -3, 5 -4, 5
 Зависимость свойств воды от давления и температуры Чистая под давлением 1 атм. замерзает при 0, под давлением 600 атм. при 5, под 2200 атм. – при 22, под 3500 атм. – при 17, под 6380 атм. – при +0, 16, под 20670 атм. при +76 – горячий лед.
Зависимость свойств воды от давления и температуры Чистая под давлением 1 атм. замерзает при 0, под давлением 600 атм. при 5, под 2200 атм. – при 22, под 3500 атм. – при 17, под 6380 атм. – при +0, 16, под 20670 атм. при +76 – горячий лед.
 Тепловые свойства воды. 1. Удельная теплота парообразования воды и плавления снега и льда 2. Теплоемкость 3. Теплопроводность
Тепловые свойства воды. 1. Удельная теплота парообразования воды и плавления снега и льда 2. Теплоемкость 3. Теплопроводность
 Удельная теплота парообразования L – это количество тепла, необходимое для перевода 1 г воды из жидкого состояния в парообразное без изменения температуры при нормальном атмосферном давлении. Скрытая теплота испарения воды при 0°С равна 597 кал/г, при температуре 100°С 539 кал/г, или 2, 23*106 Дж/кг. При переходе водяного пара в жидкую воду выделяется такое же количество тепла
Удельная теплота парообразования L – это количество тепла, необходимое для перевода 1 г воды из жидкого состояния в парообразное без изменения температуры при нормальном атмосферном давлении. Скрытая теплота испарения воды при 0°С равна 597 кал/г, при температуре 100°С 539 кал/г, или 2, 23*106 Дж/кг. При переходе водяного пара в жидкую воду выделяется такое же количество тепла
 Удельная теплота плавления снега и льда Lпл – это количество тепла, поглощаемого при переходе 1 г снега или льда в жидкую воду той же температуры. Удельная теплота плавления чистого льда равна 79, 9 кал/г при 0° С и нормальном атмосферном давлении. Это же количество тепла выделяется при замерзании 1 г воды.
Удельная теплота плавления снега и льда Lпл – это количество тепла, поглощаемого при переходе 1 г снега или льда в жидкую воду той же температуры. Удельная теплота плавления чистого льда равна 79, 9 кал/г при 0° С и нормальном атмосферном давлении. Это же количество тепла выделяется при замерзании 1 г воды.
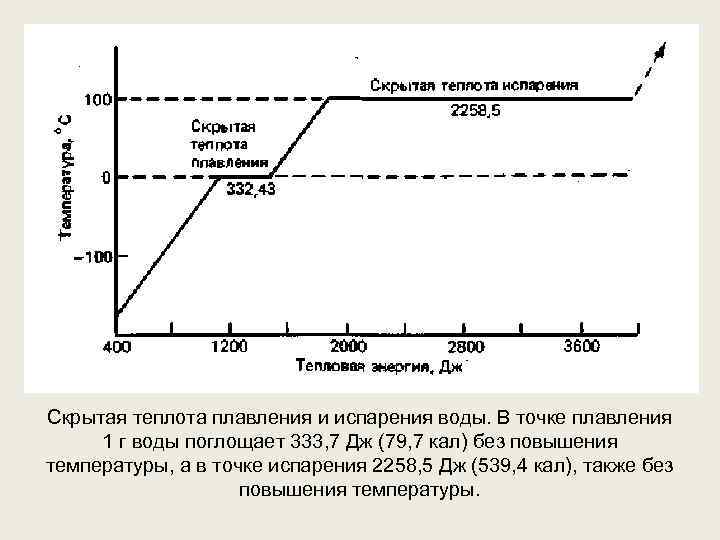 Скрытая теплота плавления и испарения воды. В точке плавления 1 г воды поглощает 333, 7 Дж (79, 7 кал) без повышения температуры, а в точке испарения 2258, 5 Дж (539, 4 кал), также без повышения температуры.
Скрытая теплота плавления и испарения воды. В точке плавления 1 г воды поглощает 333, 7 Дж (79, 7 кал) без повышения температуры, а в точке испарения 2258, 5 Дж (539, 4 кал), также без повышения температуры.
 Удельная теплота испарения воды и удельная теплота плавления льда значительно больше, чем многих других жидкостей. Скрытая теплота плавления у воды наиболее высокая среди всех веществ, за исключением аммиака и водорода, скрытая теплота испарения — наиболее высокая из всех веществ. • Эта аномалия объясняется, так же как и аномалия плотности, особенностями строения воды. При переходе жидкой воды в пар и льда в жидкую воду энергия затрачивается не только на преодоление сил взаимного притяжения молекул, но и на разрушение агрегатов двойных и тройных молекул.
Удельная теплота испарения воды и удельная теплота плавления льда значительно больше, чем многих других жидкостей. Скрытая теплота плавления у воды наиболее высокая среди всех веществ, за исключением аммиака и водорода, скрытая теплота испарения — наиболее высокая из всех веществ. • Эта аномалия объясняется, так же как и аномалия плотности, особенностями строения воды. При переходе жидкой воды в пар и льда в жидкую воду энергия затрачивается не только на преодоление сил взаимного притяжения молекул, но и на разрушение агрегатов двойных и тройных молекул.
 • Каждую минуту на испарение с поверхности океана уходит 2 • 1018 Дж солнечной энергии. Но это тепло не потеряно для планеты. При конденсации пара в верхней части тропосферы тепло, затраченное на испарение, вновь выделяется. Водяной пар выступает как теплоноситель, перемещающий тепло Солнца, для излучения которого атмосфера прозрачна, от поверхности океана и увлажненной поверхности суши к уровню конденсации в атмосфере. Мощные импульсы тепла, возникающие при конденсации, служат одним из двигателей циркуляции атмосферы и, возможно, источниками энергии тропических ураганов.
• Каждую минуту на испарение с поверхности океана уходит 2 • 1018 Дж солнечной энергии. Но это тепло не потеряно для планеты. При конденсации пара в верхней части тропосферы тепло, затраченное на испарение, вновь выделяется. Водяной пар выступает как теплоноситель, перемещающий тепло Солнца, для излучения которого атмосфера прозрачна, от поверхности океана и увлажненной поверхности суши к уровню конденсации в атмосфере. Мощные импульсы тепла, возникающие при конденсации, служат одним из двигателей циркуляции атмосферы и, возможно, источниками энергии тропических ураганов.
 • Пары воды в атмосфере играют и другую, не менее важную роль: они перехватывают и поглощают тепловое (инфракрасное) излучение Земли, создавая парниковый эффект. Роль водяного пара в парниковом эффекте значительно существеннее, чем роль углекислого газа. • В течение весеннего и осеннего сезонов за счет скрытой теплоты плавления (замерзания) происходит обмен таким количеством тепла, которое эквивалентно 2 • 1011 т сожженного угля, что намного превышает годовую добычу его во всем мире.
• Пары воды в атмосфере играют и другую, не менее важную роль: они перехватывают и поглощают тепловое (инфракрасное) излучение Земли, создавая парниковый эффект. Роль водяного пара в парниковом эффекте значительно существеннее, чем роль углекислого газа. • В течение весеннего и осеннего сезонов за счет скрытой теплоты плавления (замерзания) происходит обмен таким количеством тепла, которое эквивалентно 2 • 1011 т сожженного угля, что намного превышает годовую добычу его во всем мире.
 Теплоемкость • Количество тепла, необходимое для нагревания 1 г воды на 1°С, называется удельной теплоемкостью. В гидрологии теплоемкость обычно выражается в кал/(г*град), или Дж. • Вода характеризуется наибольшей теплоемкостью по сравнению с другими жидкими и твердыми веществами, за исключением водорода и аммиака, и примерно в 10 раз больше, чем у пород, слагающих земную кору. • Так же как и плотность, теплоемкость воды изменяется с температурой аномально: при 30°С она наименьшая 0, 9975 кал/(г*град) при 15 и 70°С равна 1, 000, при 3, 6 и 100°С возрастает до 1, 0057; теплоемкость водяного пара при 100°С и давлении 760 мм равна 0, 462, теплоемкость льда при 0°С 0, 485, а при 10°С 0, 444 кал/(г*град).
Теплоемкость • Количество тепла, необходимое для нагревания 1 г воды на 1°С, называется удельной теплоемкостью. В гидрологии теплоемкость обычно выражается в кал/(г*град), или Дж. • Вода характеризуется наибольшей теплоемкостью по сравнению с другими жидкими и твердыми веществами, за исключением водорода и аммиака, и примерно в 10 раз больше, чем у пород, слагающих земную кору. • Так же как и плотность, теплоемкость воды изменяется с температурой аномально: при 30°С она наименьшая 0, 9975 кал/(г*град) при 15 и 70°С равна 1, 000, при 3, 6 и 100°С возрастает до 1, 0057; теплоемкость водяного пара при 100°С и давлении 760 мм равна 0, 462, теплоемкость льда при 0°С 0, 485, а при 10°С 0, 444 кал/(г*град).
 Теплопроводность • Передача тепла путем молекулярной теплопроводности состоит в том, что повышенные колебания молекул в более нагретых слоях постепенно передаются молекулам смежных слоев и таким образом энергия теплового движения постепенно передается от слоя к слою. В результате возникает поток тепла от более нагретых слоев к слоям с более низкой температурой. • Коэффициент теплопроводности воды ( ) при 0° С равен 0, 001358 кал/(см*с*град). С повышением температуры он увеличивается и при температуре 20° С равен 0, 00143 кал/(см*с*град). • Вследствие малых значений коэффициента молекулярной теплопроводности перенос тепла с помощью описанного механизма не играет существенной роли в термическом режиме водных объектов. В природных условиях решающую роль при переносе тепла в воде играют турбулентные процессы.
Теплопроводность • Передача тепла путем молекулярной теплопроводности состоит в том, что повышенные колебания молекул в более нагретых слоях постепенно передаются молекулам смежных слоев и таким образом энергия теплового движения постепенно передается от слоя к слою. В результате возникает поток тепла от более нагретых слоев к слоям с более низкой температурой. • Коэффициент теплопроводности воды ( ) при 0° С равен 0, 001358 кал/(см*с*град). С повышением температуры он увеличивается и при температуре 20° С равен 0, 00143 кал/(см*с*град). • Вследствие малых значений коэффициента молекулярной теплопроводности перенос тепла с помощью описанного механизма не играет существенной роли в термическом режиме водных объектов. В природных условиях решающую роль при переносе тепла в воде играют турбулентные процессы.
 • Коэффициент теплопроводности чистого, лишенного пузырьков воздуха льда равен 0, 0054 кал/(см*с*град). С понижением температуры теплопроводность льда несколько уменьшается. • Теплопроводность снега зависит в значительной мере от его плотности. Зависимость коэффициента теплопроводности снега К от его плотности может быть выражена в следующей форме: с = 0, 0067 с2, где с плотность снега; с в кал/(см*с*град).
• Коэффициент теплопроводности чистого, лишенного пузырьков воздуха льда равен 0, 0054 кал/(см*с*град). С понижением температуры теплопроводность льда несколько уменьшается. • Теплопроводность снега зависит в значительной мере от его плотности. Зависимость коэффициента теплопроводности снега К от его плотности может быть выражена в следующей форме: с = 0, 0067 с2, где с плотность снега; с в кал/(см*с*град).
 Молекулярная вязкость • Вязкостью жидкости называется ее свойство оказывать сопротивление взаимному передвижению смежных слоев. • Вязкость играет двойную роль при движении жидкости: С одной стороны, она выступает как фактор, формирующий скоростное поле потока, передающий скорости от одного слоя к другому, сглаживающий различие скоростей в соседних точках, с другой как фактор, оказывающий сопротивление движению, т. е. способствующий превращению механической энергии в тепловую. • Коэффициент вязкости воды ( ) зависит от температуры: с повышением температуры он значительно уменьшается.
Молекулярная вязкость • Вязкостью жидкости называется ее свойство оказывать сопротивление взаимному передвижению смежных слоев. • Вязкость играет двойную роль при движении жидкости: С одной стороны, она выступает как фактор, формирующий скоростное поле потока, передающий скорости от одного слоя к другому, сглаживающий различие скоростей в соседних точках, с другой как фактор, оказывающий сопротивление движению, т. е. способствующий превращению механической энергии в тепловую. • Коэффициент вязкости воды ( ) зависит от температуры: с повышением температуры он значительно уменьшается.
 Поверхностное натяжение • Силы притяжения, действующие между молекулами воды, вызывают на поверхностях раздела вода - воздух - твердое тело явление, называемое поверхностным натяжением. Оно проявляется на границе раздела вследствие разности сил молекулярного притяжения, так как поверхностные молекулы испытывают притяжение, направленное к массе воды, большее, чем в направлении парообразных частиц воды, находящихся в воздухе.
Поверхностное натяжение • Силы притяжения, действующие между молекулами воды, вызывают на поверхностях раздела вода - воздух - твердое тело явление, называемое поверхностным натяжением. Оно проявляется на границе раздела вследствие разности сил молекулярного притяжения, так как поверхностные молекулы испытывают притяжение, направленное к массе воды, большее, чем в направлении парообразных частиц воды, находящихся в воздухе.
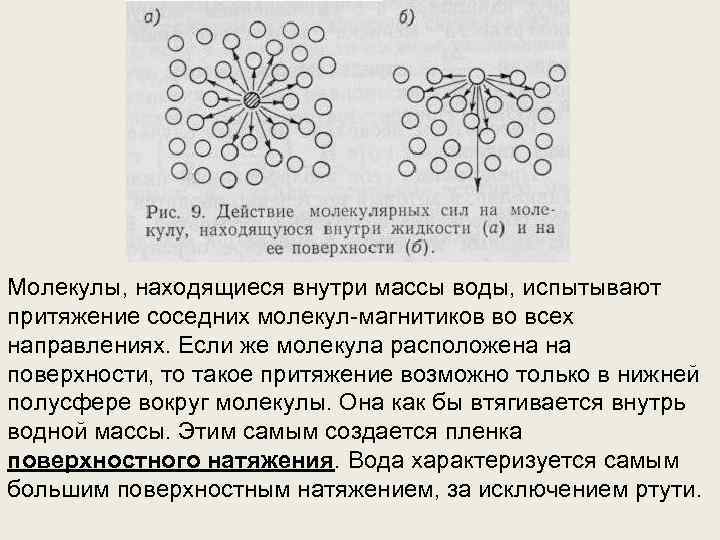 Молекулы, находящиеся внутри массы воды, испытывают притяжение соседних молекул-магнитиков во всех направлениях. Если же молекула расположена на поверхности, то такое притяжение возможно только в нижней полусфере вокруг молекулы. Она как бы втягивается внутрь водной массы. Этим самым создается пленка поверхностного натяжения. Вода характеризуется самым большим поверхностным натяжением, за исключением ртути.
Молекулы, находящиеся внутри массы воды, испытывают притяжение соседних молекул-магнитиков во всех направлениях. Если же молекула расположена на поверхности, то такое притяжение возможно только в нижней полусфере вокруг молекулы. Она как бы втягивается внутрь водной массы. Этим самым создается пленка поверхностного натяжения. Вода характеризуется самым большим поверхностным натяжением, за исключением ртути.
 Способность к смачиванию • Вода обладает высокой способностью смачивать твердые тела, т. е. прилипать к ним при соприкосновении. При смачивании тонким слоем за счет поверхностного натяжения она может прочно удерживаться на поверхности твердых частиц.
Способность к смачиванию • Вода обладает высокой способностью смачивать твердые тела, т. е. прилипать к ним при соприкосновении. При смачивании тонким слоем за счет поверхностного натяжения она может прочно удерживаться на поверхности твердых частиц.
 Поглощение и рассеяние водой (снегом, льдом) солнечной энергии. • Солнечная энергия, поступающая к поверхности воды (снега, льда), частично проникает в воду и поглощается ею, частично отражается. Поглощенная лучистая энергия превращается в тепловую. • Количество отражаемой от поверхности воды прямой солнечной радиации зависит от угла падения лучей или высоты солнца; отражение рассеянной радиации от высоты солнца не зависит и происходит по другим законам. • Отношение отраженной солнечной энергии к поступающей носит название коэффициента отражения, или альбедо.
Поглощение и рассеяние водой (снегом, льдом) солнечной энергии. • Солнечная энергия, поступающая к поверхности воды (снега, льда), частично проникает в воду и поглощается ею, частично отражается. Поглощенная лучистая энергия превращается в тепловую. • Количество отражаемой от поверхности воды прямой солнечной радиации зависит от угла падения лучей или высоты солнца; отражение рассеянной радиации от высоты солнца не зависит и происходит по другим законам. • Отношение отраженной солнечной энергии к поступающей носит название коэффициента отражения, или альбедо.
 Отражательная способность снега и льда, помимо высоты солнца, зависит от их структуры, степени загрязненности и пр. • В среднем для условий Европейской территории СССР альбедо снежного покрова для свежевыпавшего сухого снега составляет 0, 82, а для мокрого 0, 50. Коэффициент отражения в период снеготаяния быстро изменяется от 0, 70 0, 82 в начале до 0, 30 в конце снеготаяния; он закономерно убывает вместе с уменьшением высоты снега и скачкообразно возрастает при каждом новом снегопаде. Наиболее быстро коэффициент отражения уменьшается с уменьшением высоты при небольшой толщине снежного покрова (до 10 см), медленнее при высоте от 10 до 30 см и остается почти неизменным при высоте 40 50 см.
Отражательная способность снега и льда, помимо высоты солнца, зависит от их структуры, степени загрязненности и пр. • В среднем для условий Европейской территории СССР альбедо снежного покрова для свежевыпавшего сухого снега составляет 0, 82, а для мокрого 0, 50. Коэффициент отражения в период снеготаяния быстро изменяется от 0, 70 0, 82 в начале до 0, 30 в конце снеготаяния; он закономерно убывает вместе с уменьшением высоты снега и скачкообразно возрастает при каждом новом снегопаде. Наиболее быстро коэффициент отражения уменьшается с уменьшением высоты при небольшой толщине снежного покрова (до 10 см), медленнее при высоте от 10 до 30 см и остается почти неизменным при высоте 40 50 см.
 Поглощение солнечной энергии • Изменяется в зависимости от длины световой волны и наличия в воде взвешенных и растворенных веществ. • Наибольшего значения он достигает в инфракрасной части спектра; наименьшие его значения приходятся на видимую световую часть спектра. В ультрафиолетовой части спектра коэффициент поглощения снова возрастает. Таким образом, вода хуже пропускает инфракрасные лучи и лучше световые (видимые) лучи, которые, проникая вглубь, обусловливают освещенность воды. В видимой части спектра более интенсивно поглощается длинно волновое излучение. • В зависимости от коэффициента поглощения, изменяющегося с изменением длин световых волн, на различные глубины проникает разное количество солнечной энергии. На глубину 1, 0 см проникает 74% поступающей солнечной энергии, на глубину 100 см 36%, а до глубины 10 м доходит 18%; остальная часть солнечной энергии поглощается вышележащим слоем воды и расходуется на нагревание. На глубину свыше 200 м солнечный свет практически не проникает.
Поглощение солнечной энергии • Изменяется в зависимости от длины световой волны и наличия в воде взвешенных и растворенных веществ. • Наибольшего значения он достигает в инфракрасной части спектра; наименьшие его значения приходятся на видимую световую часть спектра. В ультрафиолетовой части спектра коэффициент поглощения снова возрастает. Таким образом, вода хуже пропускает инфракрасные лучи и лучше световые (видимые) лучи, которые, проникая вглубь, обусловливают освещенность воды. В видимой части спектра более интенсивно поглощается длинно волновое излучение. • В зависимости от коэффициента поглощения, изменяющегося с изменением длин световых волн, на различные глубины проникает разное количество солнечной энергии. На глубину 1, 0 см проникает 74% поступающей солнечной энергии, на глубину 100 см 36%, а до глубины 10 м доходит 18%; остальная часть солнечной энергии поглощается вышележащим слоем воды и расходуется на нагревание. На глубину свыше 200 м солнечный свет практически не проникает.
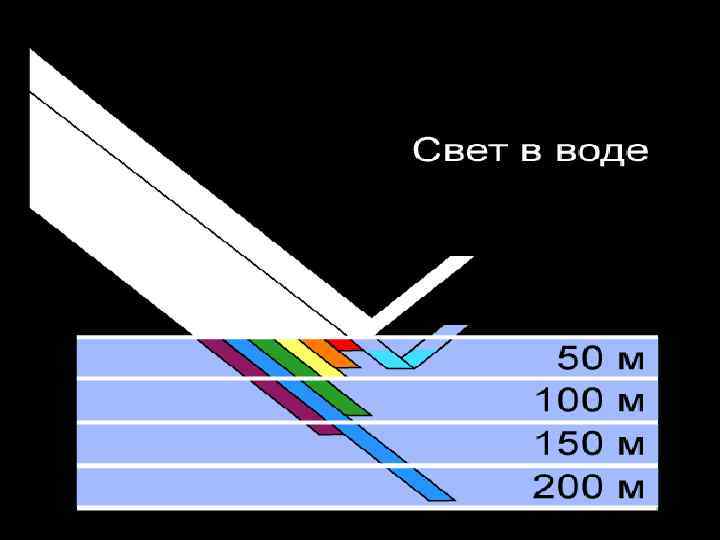
 Рассеяние света • Происходит как в самой водной массе, так и под влиянием взвешенных в ней частиц. Чем длиннее волна, тем она меньше рассеивается; поглощаются же, наоборот, сильнее длинные волны и слабее короткие.
Рассеяние света • Происходит как в самой водной массе, так и под влиянием взвешенных в ней частиц. Чем длиннее волна, тем она меньше рассеивается; поглощаются же, наоборот, сильнее длинные волны и слабее короткие.
 Распространение звука в воде • Звук распространяется в воде в пять раз быстрее, чем в воздухе. Средняя скорость равняется 1400 — 1500 м/сек (скорость распространения звука в воздухе 340 м/сек). Энергия звуковой волны в морской воде постепенно убывает из за ее поглощения, обусловленного в основном двумя процессами: внутренним трением среды и диссоциацией растворенных в ней солей.
Распространение звука в воде • Звук распространяется в воде в пять раз быстрее, чем в воздухе. Средняя скорость равняется 1400 — 1500 м/сек (скорость распространения звука в воздухе 340 м/сек). Энергия звуковой волны в морской воде постепенно убывает из за ее поглощения, обусловленного в основном двумя процессами: внутренним трением среды и диссоциацией растворенных в ней солей.
 Распространение звука в воде • Расходимость. Звуковое излучение, удаляясь от источника, расходится в пространстве, как свет и радиоволны; в результате этого интенсивность звука ослабевает пропорционально квадрату расстояния от излучателя. • Рассеяние. Затухание звука в море происходит и из за его рассеяния на различных неоднородностях среды взвешенных частицах, микроорганизмах и тепловых аномалиях. Рассеяние следом корабля или большим рыбным косяком может дать до 90% всех потерь, и его необходимо учитывать особо. Более важным следствием рассеяния оказывается то, что звук попадает в т. н. зоны акустической тени, где он рассеивается в многократных отражениях от граничных поверхностей.
Распространение звука в воде • Расходимость. Звуковое излучение, удаляясь от источника, расходится в пространстве, как свет и радиоволны; в результате этого интенсивность звука ослабевает пропорционально квадрату расстояния от излучателя. • Рассеяние. Затухание звука в море происходит и из за его рассеяния на различных неоднородностях среды взвешенных частицах, микроорганизмах и тепловых аномалиях. Рассеяние следом корабля или большим рыбным косяком может дать до 90% всех потерь, и его необходимо учитывать особо. Более важным следствием рассеяния оказывается то, что звук попадает в т. н. зоны акустической тени, где он рассеивается в многократных отражениях от граничных поверхностей.
 Распространение звука в воде • Отражение. Поверхность океана активно отражает звук, но ее волны и рябь вызывают разброс направлений и фаз отраженных звуков, и между падающим и отраженным звуковыми пучками возникает интерференция, так что интенсивность звука в фиксированной точке пространства изменяется со временем по сложному закону. Дно тоже отражает звуки, но его коэффициент отражения сильно зависит от структуры дна и глубины. Илистое дно плохой отражатель, а песчаное или скалистое очень хороший. На небольших глубинах над дном из твердых пород вследствие многократных отражений звука от него и от водной поверхности возникает подводный звуковой канал, в котором создаются благоприятные условия для гидролокации.
Распространение звука в воде • Отражение. Поверхность океана активно отражает звук, но ее волны и рябь вызывают разброс направлений и фаз отраженных звуков, и между падающим и отраженным звуковыми пучками возникает интерференция, так что интенсивность звука в фиксированной точке пространства изменяется со временем по сложному закону. Дно тоже отражает звуки, но его коэффициент отражения сильно зависит от структуры дна и глубины. Илистое дно плохой отражатель, а песчаное или скалистое очень хороший. На небольших глубинах над дном из твердых пород вследствие многократных отражений звука от него и от водной поверхности возникает подводный звуковой канал, в котором создаются благоприятные условия для гидролокации.
 Распространение звука в воде • Рефракция. Искривление звуковых "лучей" вызывается тем, что в разных (по глубине) слоях воды скорость звука различна и звуковой пучок отклоняется в сторону слоя с наименьшей скоростью. Влияние давления хорошо известно и зависит лишь от глубины. Весьма существенно влияние температуры, а она переменчива, и для определения профиля скорости звука по глубине нужно измерять температуру воды на разных глубинах.
Распространение звука в воде • Рефракция. Искривление звуковых "лучей" вызывается тем, что в разных (по глубине) слоях воды скорость звука различна и звуковой пучок отклоняется в сторону слоя с наименьшей скоростью. Влияние давления хорошо известно и зависит лишь от глубины. Весьма существенно влияние температуры, а она переменчива, и для определения профиля скорости звука по глубине нужно измерять температуру воды на разных глубинах.
 Распространение звука в воде • Подводный звуковой канал — слой воды в морях и океанах, в котором возможно сверхдальнее распространение звука вследствие рефракции. • На некоторой глубине под поверхностью воды находится слой, в котором звук распространяется с наименьшей скоростью; выше этой глубины скорость звука увеличивается из за повышения температуры, а ниже — вследствие увеличения гидростатического давления с глубиной. • Этот слой представляет собой своеобразный подводный звуковой канал (ПЗК). Луч, отклонившийся от оси канала вверх или вниз, вследствие рефракции всегда стремится попасть в него обратно. В таком канале звуковые лучи, отклоняясь от его оси вверх или вниз, попадают в области большей скорости звука и вновь стремятся к оси канала. Когда они ее пересекают, процесс повторяется, и звуковой пучок оказывается в продольной ловушке, на оси которой скорость звука минимальна.
Распространение звука в воде • Подводный звуковой канал — слой воды в морях и океанах, в котором возможно сверхдальнее распространение звука вследствие рефракции. • На некоторой глубине под поверхностью воды находится слой, в котором звук распространяется с наименьшей скоростью; выше этой глубины скорость звука увеличивается из за повышения температуры, а ниже — вследствие увеличения гидростатического давления с глубиной. • Этот слой представляет собой своеобразный подводный звуковой канал (ПЗК). Луч, отклонившийся от оси канала вверх или вниз, вследствие рефракции всегда стремится попасть в него обратно. В таком канале звуковые лучи, отклоняясь от его оси вверх или вниз, попадают в области большей скорости звука и вновь стремятся к оси канала. Когда они ее пересекают, процесс повторяется, и звуковой пучок оказывается в продольной ловушке, на оси которой скорость звука минимальна.
 Гидрологическое и физико-географическое значение физических свойств и «аномалий» воды. 1. Аномальные изменения плотности воды в зависимости от температуры. 2. Аномальные изменения теплоемкости воды в зависимости от температуры. 3. Сила поверхностного натяжения. 4. Поглощение и рассеяние света.
Гидрологическое и физико-географическое значение физических свойств и «аномалий» воды. 1. Аномальные изменения плотности воды в зависимости от температуры. 2. Аномальные изменения теплоемкости воды в зависимости от температуры. 3. Сила поверхностного натяжения. 4. Поглощение и рассеяние света.
 Задания на дом: • Письменно дать характеристики физических свойств снега: соотношения льда и воздуха по массе и по объему, влагоемкость, влажность, водоотдача.
Задания на дом: • Письменно дать характеристики физических свойств снега: соотношения льда и воздуха по массе и по объему, влагоемкость, влажность, водоотдача.
 Всего доброго!
Всего доброго!


