АДАПТ-ИО-лекция-ИВ.ppt
- Количество слайдов: 57

ТЮМЕНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА КЛИНИЧЕСКОЙ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ ФПК И ППС АДАПТИВНЫЙ ИММУНИТЕТ. Пашкина Ирина Валерьевна доцент кафедры КЛД, к. м. н.

Приобретенный иммунитет (адаптивный, специфический): формируется при специфическом воздействии клеток иммунной системы с антигеном (АГ) в результате появляются антитела (АТ) и лимфоциты, направленно, адекватно распознающие данный АГ и, в норме, нейтрализующие его потенциально вредное воздействие на организм.

Виды адаптивного иммунитета: Активный приобретенный иммунитет – формируется в результате перенесенной инфекции (естественный) или вакцинации (искусственный). Пассивный приобретенный иммунитет – формируется в результате введения препаратов иммунных сывороток или иммуноглобулинов (искусственный). У новорожденных имеется пассивный транспланцентарный иммунитет, в результате передачи плоду через плаценту Ig. G –антител (естественный).

Виды адаптивного иммунитета (продолжение) Клеточный (Т-цитотоксические лимфоциты) – противоопухолевый, трансплантационный, противовирусный, противогрибковый Гуморальный (В-лимфоциты и их продуценты – антитела) – противобактериальный, антитоксинемический, противопаразитарный Клеточные и гуморальные факторы иммунитета действуют в тесном взаимодействии с более выраженным: - клеточным звеном – клеточно-гуморальный ИО - гуморальным звеном – гуморально-клеточный ИО

Виды адаптивного иммунитета (продолжение) По природе и свойствам антигена: Антитоксический Противовирусный Противобактериальный Противопротозойный Противоопухолевый Трансплантационный Др. виды

Виды адаптивного иммунитета (продолжение) По наличию - отсутствию антигена в организме: Стерильный – сохраняется при полной элиминации антигена, который играет только роль «пускового» фактора (например, поствакцинальный при введении убитых вакцин) Нестерильный – поддерживается только в присутствии антигена в организме (например, при туберкулезе)

Виды адаптивного иммунитета (продолжение) По распространенности резистентности к антигену: Местный (например, мукозальный иммунитет верхних дыхательных путей) Общий (системный, генерализованный)

Активация иммунной системы связана с развитием продуктивной иммунной реакции в ответ на появление АГ (экзогенно или эндогенно) или продуктов деструкции тканей макроорганизма (эндогенно). Активация иммунной системы происходит при невозможности элиминации АГ факторами неспецифической резистентности Этот сложный многоступенчатый процесс требует около 4 -х суток для своей индукции.

При первичном контакте с патогеном сначала развиваются полноценные реакции врожденного иммунитета: Распознавание патогена по принципу паттернов (паттерны – консервативные неизменяющиеся молекулы, характерные для многих патогенов). 1 -я задача – организовать воспаление (для ограничения распространения патогена). В очаг внедрения патогена мигрируют макрофаги. Макрофаги выделяют IL-1, 6, 8, TNF-α, привлекающие нейтрофилы. IL-8 – хемокин, обеспечивает хемотаксис нейтрофилов. Эти цитокины действуют также на клетки эндотелия сосудов, повышается экспрессия молекул адгезии (селектинов) для «вылавливания» нейтрофилов.

Развитие реакций неспецифического воспаления реализуется механизмами нейро-иммунной регуляции: если обнаружен патоген, необходимо «сообщить» ЦНС: IL-1, 6, TNF-α воздействуют на клетки гипоталямуса возникает лихорадка. Сила сигнала зависит от количества задействованных макрофагов. IL-1, TNF-α печень выработка Среактивного белка (СРБ) и других белков острой фазы. IL-1 фибробласты ограничение воспаления, замещение дефекта.

Если патогена (ПГ) мало, то и ИО нет. Если ПГ размножается, его много стимуляция костного мозга: из депо к. м. выбрасываются нейтрофилы, макрофаги синтезируют M-CFS, TNF, GM-CFS, G-CFS, IL-1, 6, 11, 12 стволовая клетка активация гемопоэза

Таким образом: Врожденный иммунитет – естественный, наследственный, неспецифический (неспецифическая резистентность) – воздействует на АГ неспецифически, направляя неспецифические факторы защиты на повреждение, нейтрализацию и выведение разнообразных АГ. Врожденный иммунитет является первичной воспалительной защитной неспецифической реакцией организма на АГ.

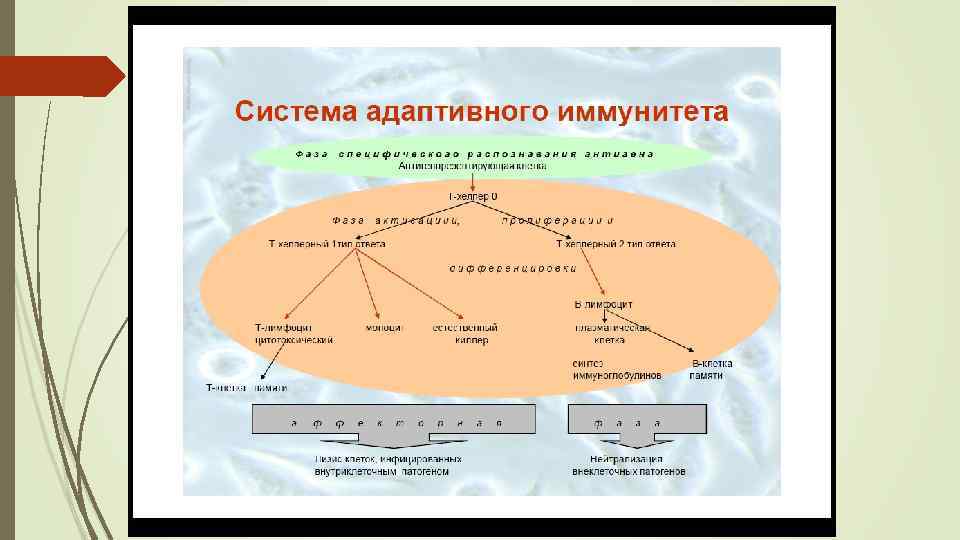
Включение механизмов адаптивного ИО Фазы иммунного ответа: 1. Распознавание 2. Фаза активации: Клонирование Дифференцировка 4. Эффекторная фаза: Удаление (эрадикация) гуморальный и клеточный ответ 5. Гомеостаз (лишние клетки должны уйти в апоптоз) 6. Должны остаться клетки памяти

Пусковой механизм адаптивного иммунитета – распознавание «свой – чужой» Это осуществляют Т-лимфоциты при помощи своих иммунорецепторов TCR. В случае установления чужеродности биомолекул происходит тиражирование клона высокоспецифичных к данному АГ лимфоцитовэффекторов для нейтрализации патогена, а также накопление Т- и В-клеток иммунологической памяти – гарантии более быстрого и продуктивного иммунного ответа при повторных встречах с этим АГ (экспансия клона)

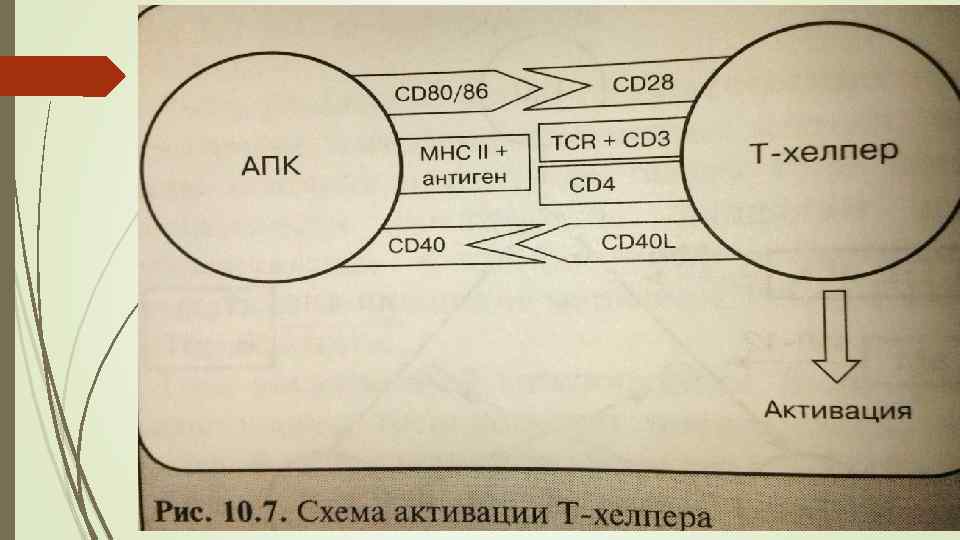
Фаза распознавания антигена АПК – антигенпредставляющие клетки: дендритные клетки, В-лимфоциты, макрофаги АПК поглощает молекулярный АГ-пептид, процессирует его (ограниченный протеолиз) во внутриклеточных везикулах на более мелкие фрагменты АПК встраивает образовавшиеся олигопептиды в молекулу МНС – II класса и выставляет полученный комплекс на своей наружной мембране АПК экспрессирует на своей поверхности также костимулирующие факторы – молекулы CD 40, CD 86

Активация Т-хелпера Т-хелпер при помощи своих молекул адгезии прочно соединяется с АПК Иммунорецептор TCR Т-хелпера совместно с рецептором CD 3 и ко-рецептором CD 4 взаимодействует с комплексом антиген – MHC II класса Происходит анализ «чужеродности» продуктивность анализа зависит от контактов CD 28 T- хелпера с CD 80/86 на поверхности АПК, а CD 40 -лиганд Т-хелпера со своей парой CD 40 на поверхности АПК
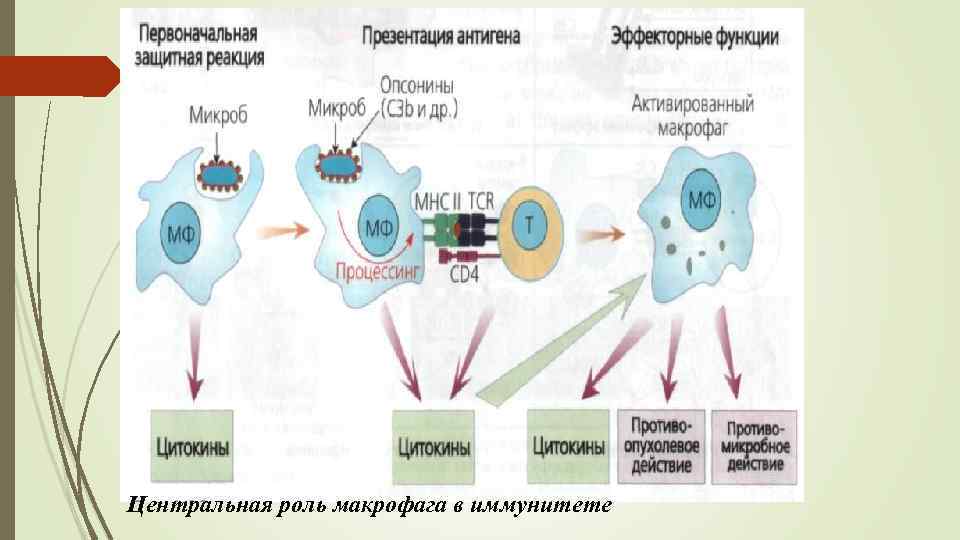
Центральная роль макрофага в иммунитете

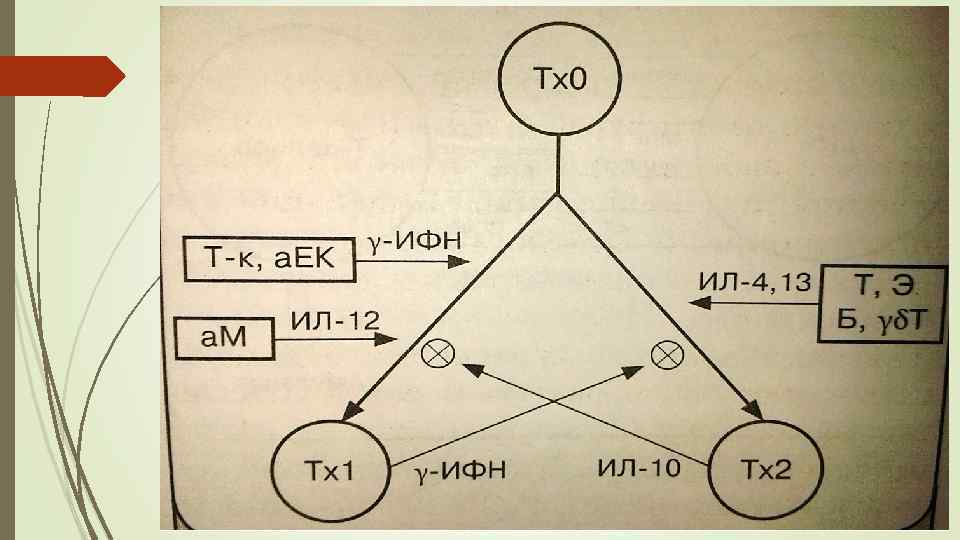
Размножение и дифференцировка Т-хелпера В случае признанания чужеродности комплекса антиген МСН II класса (точнее «не своего» ) Т-хелпер активируется Т-хелпер начинает экспрессировать рецептор к ИЛ-2, ИЛ-2 и другие цитокины Итог активации Т-хелпера – его размножение и дифференцировка в Т 1 -х и Т 2 -х Параллельно стимулируются клетки эффекторы

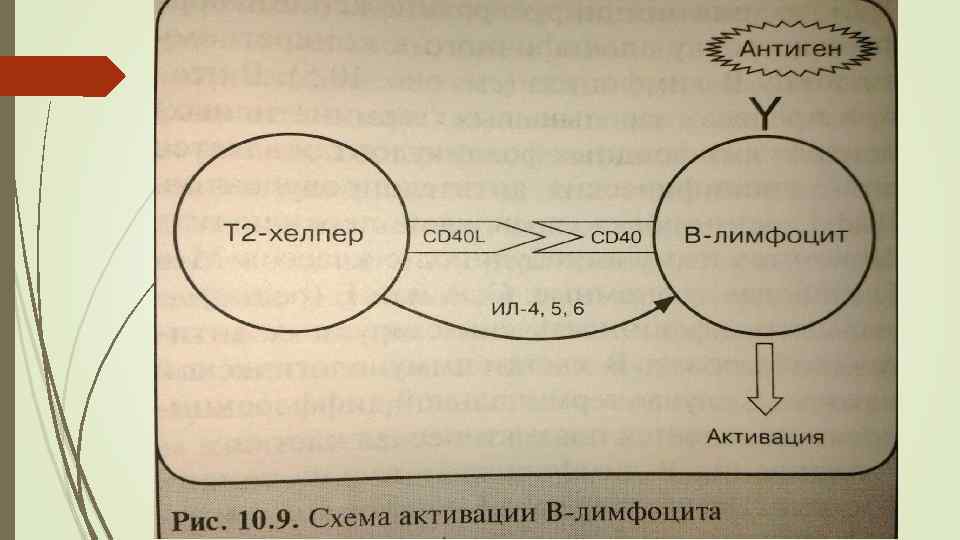
Гуморальный иммунный ответ (антителообразовние ) Основой гуморального (от лат. humor – жидкость) иммунного ответа является активация В- лимфоцитов и их дифференцировка в антителообразующие плазматические клетки – плазмоциты. В–лимфоцит играет роль антигенраспознающей, антигенпрезентирующей клетки и антителообразующей клетки.

Гуморальный иммунный ответ (антителообразовние) Иммуноглобулиновый рецептор В-лимфоцитов (ВСR) распознает антиген, и клетка поглощает его. После процессинга (расщепления поглощенного антигена до низкомолекулярных пептидов и встраивания их в HLA II класса) В-лимфоциты представляют образовавшийся комплекс Тh 2 хелперам, которые взаимодействуют с ним рецептором ТСR и корецептором СD 4. Происходит активация и пролиферация В-лимфоцитов.

Гуморальный иммунный ответ (антителообразовние) Размножаясь в геометрической прогрессии (7 -9 делений), В-клетка формирует клон плазматических клеток. Начинается активный синтез иммуноглобулинов. Плазматические клетки в основном все уходят в к. м. , и там продуцируют до 30 000 молекул Ig в мин. Первые АТ появляются в крови на 5 -е сутки (от момента проникновения патогена) класса Ig. M (можно диагностировать о. фазу инфекции) Maксимальный синтез Ig. M – на 14 день К концу месяца – уровень ↓ до нормы

Гуморальный иммунный ответ (антителообразовние) Когда Тh 2 -хелперы начинают секретировать ИЛ-6, происходит переключение иммуноглобулиновых генов В-лимфоцитов на синтез Ig. G (на 7 -е сутки). По соотношению Ig. M и Ig. G можно определить стадию болезни: Острая - + Ig. M Подострая - +Ig. M и Ig. G Затяжное, хрон. течение, ремиссия - +Ig. G Max. синтез Ig. G – на 30 день Срок жизни – до 60 дней
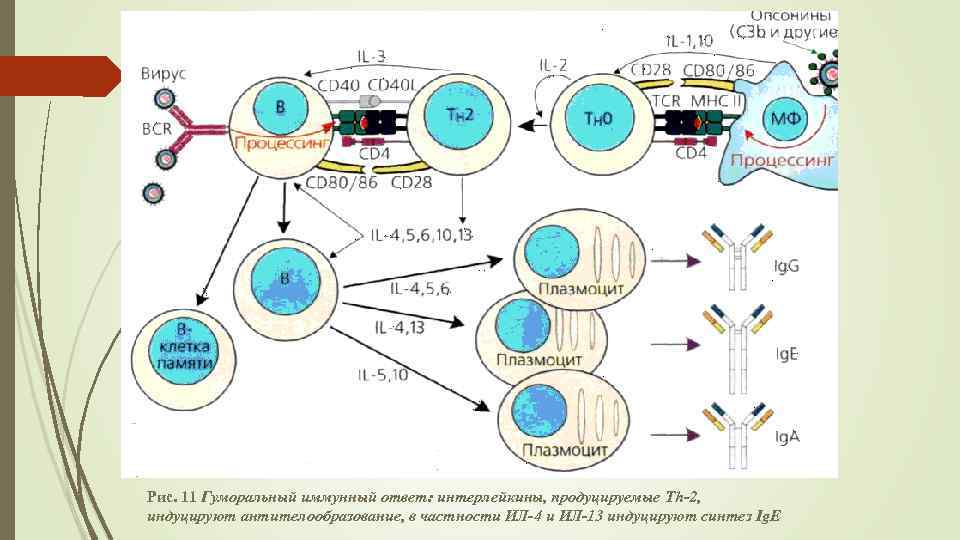
Рис. 11 Гуморальный иммунный ответ: интерлейкины, продуцируемые Th-2, индуцируют антителообразование, в частности ИЛ-4 и ИЛ-13 индуцируют синтез Ig. E

Гуморальный иммунный ответ (антителообразовние) Клетки памяти формируются после 30 дня заболевания. У взрослых ~ 85% лимфоцитов – клетки памяти. Клеток памяти нет до встречи с антигеном. Формирование клеток памяти – главное в иммунном ответе.
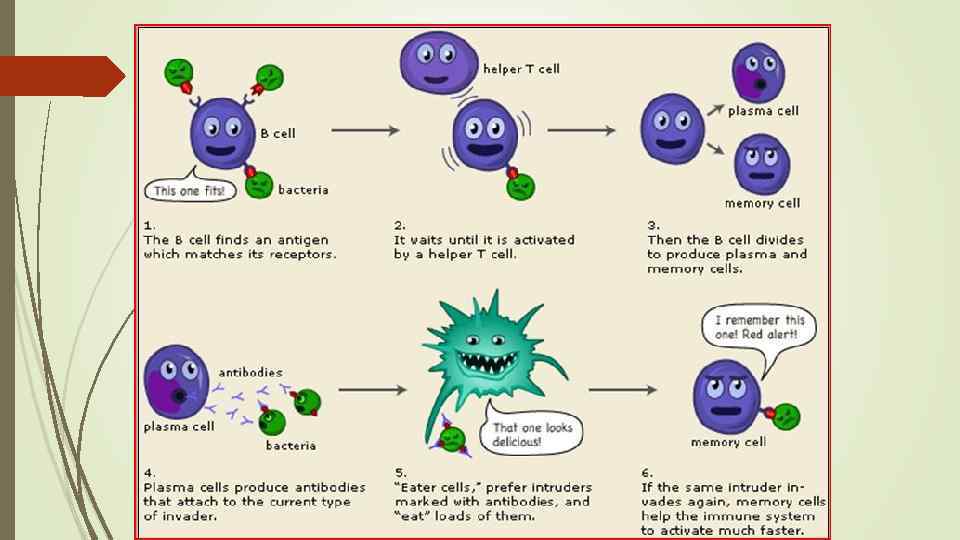

Клеточный иммунный ответ. Участвуют популяции Тh 1 -хелперов CD 4+ и цитотоксических Т-лимфоцитов CD 8+ (ЦТЛ). АПК (макрофаги и дендритные клетки) после процессинга поглощенного антигена представляют ЦТЛ микробные пептиды в комплексе с МНС І класса. ЦТЛ с помощью антигенраспознающего рецептора (ТСR) и его корецептора CD 8 распознают соответственно микробный пептид и МНС І класса (двойное распознавание).
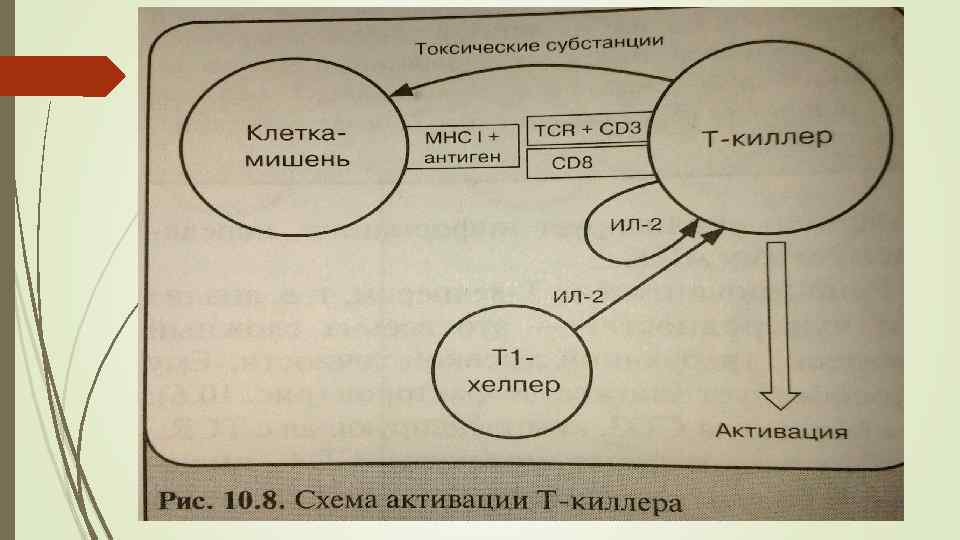

Клеточный иммунный ответ. Активированные дифференцированные ЦТЛ вызывают гибель клеток-мишеней посредством выделения многих ферментов-белков (эндоцитоз): Перфорина Гранзимов гранулизинов Fas-рецепторов ФНО
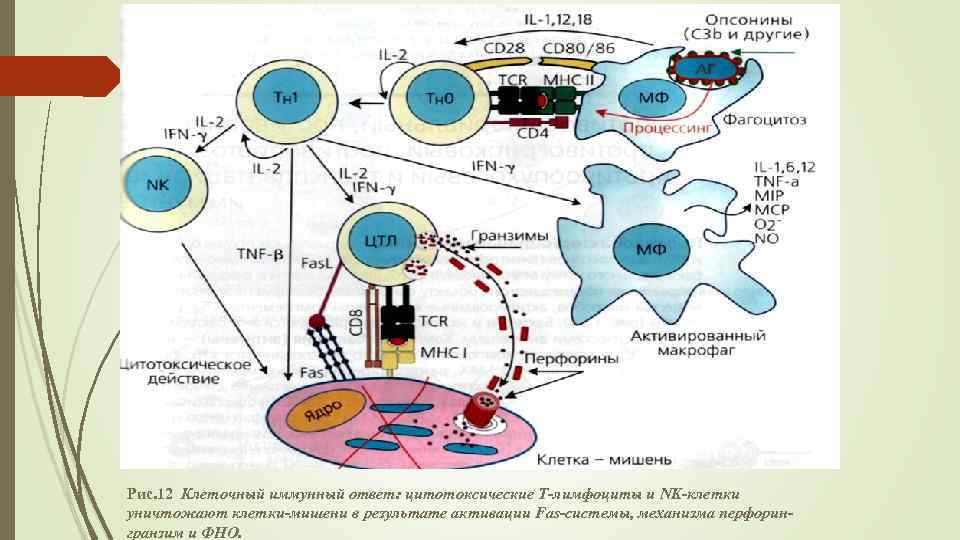
Рис. 12 Клеточный иммунный ответ: цитотоксические Т-лимфоциты и NK-клетки уничтожают клетки-мишени в результате активации Fas-системы, механизма перфорингранзим и ФНО.

Иммунологическая память Имеет высокую специфичность к конкретному АГ Распространяется на гуморальное и клеточное звено иммунитета Обусловлена Т- и В-лимфоцитами Образуется практически всегда Сохраняется годами и десятилетиями Защищает от повторных антигенных воздействий

Механизмы формирования иммунологической памяти 1. Длительное сохранение АГ в организме: (инкапсулированный возбудитель туберкулеза, персистирующий вирус кори, полиомиелита, ветряной оспы и др. ) - поддержание напряжения иммунной системы; сохранение муляжа АГ (образ в антиидиотипических антителах); длительное удерживание АГ-детерминант дендритными клетками 2. Дифференцировка в процессе продуктивного иммунного ответа части Т- и В- лимфоцитов в малые

Иммунологическая толерантность Явление, противоположное иммунному ответу и иммунологической памяти Проявляется отсутствием продуктивного специфического ИО на антиген в связи с невозможностью его распознавания В отличие от иммуносупрессии предполагает изначальную ареактивность иммунокомпетентных клеток к определенному антигену

ИТ вызывают толерогены (наиболее толерогенны полисахариды) Врожденная ИТ (отсутствие ИО на собственные АГ тканей) Приобретенная ИТ формируется при введении: - антигена в эмбриональном периоде или в первые дни жизни – временной фактор важен!!! - Толерогена - активная ИТ - Веществ, тормозящих биосинтетическую и пролиферативную активность иммунокомпетеных клеток (иммунодепрессанты, цитостатики, антилимфоцитарная сыворотка) – пассивная ИТ

Свойства ИТ Специфичность Поливалентность (ко всем антигенным детерминантам АГ) или (реже)моновалентность Зависимость от возраста и иммунореактивности пациента Чем менее чужероден толероген для организма, тем лучше для ИТ ИТ развивается легче на тимуснезамисимые АГ, например бактериальные полисахариды Возможны высокодозовая и низкодозовая ИТ

Механизмы развития ИТ (супрессия иммунного ответа) 1. Элиминация из организма антигенспецифических клонов лимфоцитов: Активация антигенспецифического рецептора (TCR или BCR) незрелого лимфоцита на ранних стадиях онтогенеза индуцирует в нем апоптоз. Этот феномен обеспечивает ареактивность (невосприимчивость) к аутоантигенам – центральная толерантность.

Элиминации путем апоптоза подвергаются клетки: Терминально дифференцированные лимфоциты, завершившие свою биологическую программу Активированные лимфоциты, не получившие антигенного стимула «изношенные» лимфоциты Аутореактивные клетки

Механизмы развития ИТ (продолжение) 2. Блокада биологической активности иммунокомпетентных клеток: Обеспечивается «негативными» эффектами иммуноцитокинов: - Дифференцировку Т 0 в Т 1 -хелпер тормозит ИЛ 4, 13, а в. Т 2 -хелпер – ИФН-гамма - Пролиферацию Т- и В-лимфоцитов активно тормозит в-ТФР - ИЛ-4, 13, в-ТФР подавляют активность макрофагов

Механизмы развития ИТ (продолжение) 3. Быстрая нейтрализация антигена антителами. - Биосинтез в В-лимфоците и его превращения в плазмоцит подавляется высоким уровнем Ig. G. - Инактивация АГ антителами предотвращает их связывание с иммунокомпетентными клетками, т. е. исчезает специфический активирующий фактор для иммунного ответа. - Нейтрализация антигена может достигаться плазмо - и лимфосорбцией в клинической практике

Особенности иммунитета при различных состояниях

Иммунный ответ при бактериальных инфекциях Антибактериальный иммунитет – против структурнофункциональных компонентов бактериальных клеток Антитоксический иммунитет – против белковых токсинов Основная роль – у антител (гуморальный ИО) и фагоцитов Клеточный ИО – необходим для факультативных внутриклеточных паразитов, устойчивых к действию комплемента, лизоцима, фагоцитов (незавершенный фагоцитоз). Это: микобактерии, сальмонеллы, бруцеллы и др. Это приводит к аллергизации макроорганизма по типу ГЗТ Важную роль играют белки ОФВ (СРБ, маннозосвязывающий протеин), и лизоциму
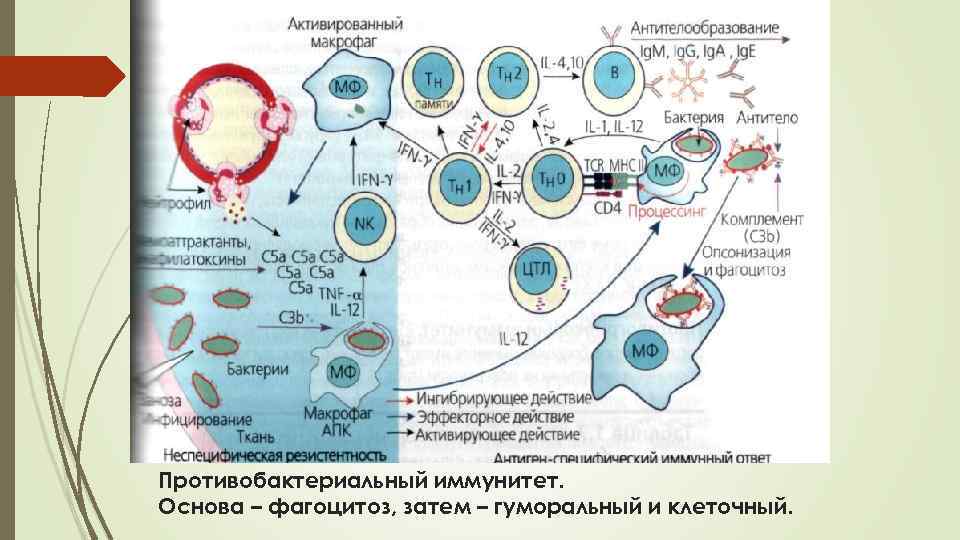
Противобактериальный иммунитет. Основа – фагоцитоз, затем – гуморальный и клеточный.

Иммунный ответ при вирусных инфекциях Основные факторы: Т-киллеры (ЦТЛ): вирусные белки экспрессируются на клеточной мембране в составе MHC I класса - активация Т -киллеров и уничтожение зараженных вирусом клеток Антитела: взаимодействуют с внеклеточным вирусом, нейтрализуют вирусную частицу, препятствуют ее адсорбции на клетке-мишени, связывают вирусные белки и нуклеиновые кислоты из разрушенных вирусами клеток Интерферон: не действует непосредственно на вирус, но связывается с рецептором на мембране клетки и индуцирует ферментные системы для подавления метаболизма клетки Сывороточные ингибиторы вирусных частиц
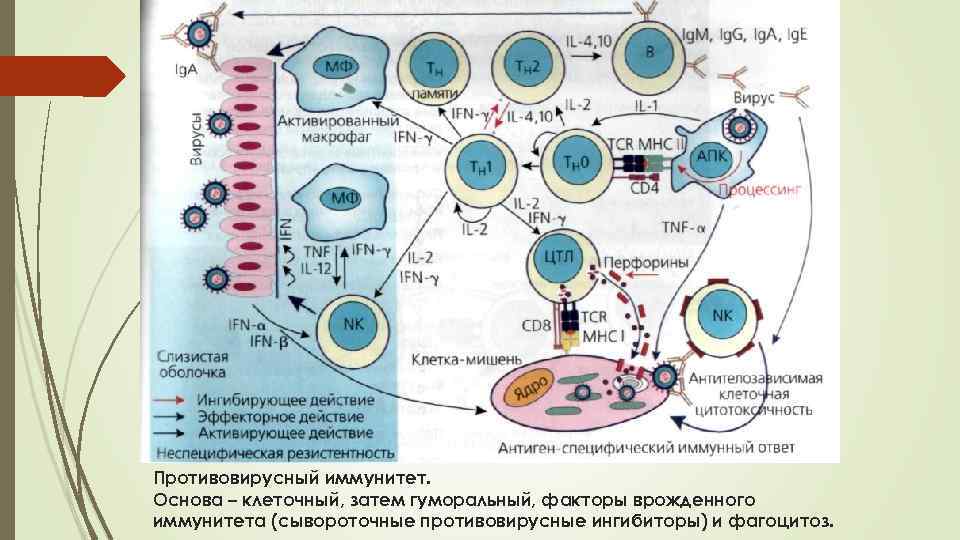
Противовирусный иммунитет. Основа – клеточный, затем гуморальный, факторы врожденного иммунитета (сывороточные противовирусные ингибиторы) и фагоцитоз.

Особенности противогрибкового иммунитета Антигены грибов имеют низкую иммуногенность Плохо индуцируют антителообразование Стимулируют клеточное звено иммунитета Основной фактор – активированные макрофаги путем антителозависимой клеточноопосредованной цитотоксичности

Противогрибковый иммунитет Основой противогрибкового иммунитета является клеточный иммунитет: фагоцитоз эпителиоидная гранулематозная реакция ГЗТ Аллергия Ig. Eантитела против антигенов грибов ГЗТ и ГНТ. Антитела (Ig. M, Ig. G) при микозах выявляются в низких титрах. Факторы противогрибковой неспецифической резистентности кожи, слизистых оболочек рта и слюны

Противоопухолевый иммунитет Антигены опухоли слабо иммуногенны. Антитела, соединяясь с антигенными детерминантами на опухолевых клетках, экранируют их от цитопатогенного действия иммунных лимфоцитов. Механизм презентации антигена часто нарушается, нет достаточного уровня ФНО, интерферонов, ИЛ-2 и др. цитокинов. Опухоли запускают феномен «ускользания» от иммунитета. Уменьшение экспрессии МНС на опухолевых клетках ведет к отмене распознавания опухоли. Неспецифические факторы, повреждающие опухолевые клетки: - 1) NK-клетки, система мононуклеарных фагоцитов, противоопухолевая активность которых усиливается под действием ИЛ-2 и ИФН-α, -β; - 2) цитокины (ИФН-α, -β, ФНО-α и ИЛ-2).

Трансплантационный иммунитет Клеточное звено ИО – Т-киллеры: после сенсибилизации антигенами донора мигрируют в ткани трансплантата и оказывают на них цитотоксичность Гуморальное звено ИО – специфические антитела: образуются на чужеродные антигены – гемолизины, лейкотоксины, цитотоксины. Запускаю антитело-опосредованный цитолиз трансплантата Фазы иммунного отторжения: 1 фаза – лимфоидная инфильтрация (скопление иммунокомпетентных клеток (в т. ч. Т-киллеров) 2 фаза – деструкция клеток трансплантата Т-киллерами, активация макрофагов, НК, специфический антителогенез Возникает иммунное воспаление – тромбоз, ишемия трансплантата и его гибель. Разрушенные ткани утилизируются фагоцитами клон Т- и В-клеток памяти – повторная попытка пересадки этой ткани приводит к быстрому отторжению

Лабораторные показатели для оценки иммунного статуса Иммунный статус – состояние иммунной системы человека, оцениваемое комплексом качественных и количественных клинико-лабораторных показателей. Гематологические показатели: 1. Количество лейкоцитов, эритроцитов, тромбоцитов, гемоглобина в эритроците и в эритроцитах; цветовой показатель. 2. Процентное содержание нейтрофилов, лимфоцитов, моноцитов, эозинофилов, базофилов. 3. Показатели СОЭ.

Оценка Т-клеточной системы иммунитета (клеточного иммунитета): 1. Определение общего числа лимфоцитов. 2. Определение числа зрелых Т-лимфоцитов (CD 3+) и их субпопуляций – хелперов (CD 4+) и цитотоксических Т-лимфоцитов (CD 8+). 3. Определение соотношения CD 4+CD 8+ (иммунорегуляторный индекс). 4. Определение реакции Т-лимфоцитов на активацию фитогемагглютинином (Т-митоген) в реакции бластной трансформации (РБТЛ). 5. Постановка кожных проб ГЗТ. 6. Дополнительные уточняющие методы: • определение маркера ранней активации CD 25 (рецептор для ИЛ-2) и HLA-DR на Т-лимфоцитах; • исследование продукции цитокинов (ИФН-γ, ИЛ-2, -4, -6, ФНО); определение пролиферативного ответа на специфический антиген в РБТЛ; • определение готовности Т-лимфоцитов к апоптозу (определение апоптозного антигена Fas – CD 95).

Оценка В-клеточной системы иммунитета (гуморального иммунитета): 1. Определения числа В-лимфоцитов (CD 19+ или CD 20+). 2. Определение количества неспецифических иммуноглобулинов (Іg. A, Ig. M, Ig. G, Ig. E). 3. Определение циркулирующих в крови иммунных комплексов. 4. Определение функциональной активности лимфоцитов с помощью РБТЛ на В-клеточный митоген. 5. Дополнительные уточняющие методы: • определение количества специфических иммуноглобулинов (Іg. A, Ig. M, Ig. G, Ig. E); • определение продукции ИЛ-6; • определение секреторного Іg. A.

Показатели системы комплемента: Определение компонентов комплемента (С 1 q, С 1, С 3, С 4, С 5 и др. ) в сыворотке крови. Система фагоцитов (нейтрофилов): 1. Определение числа нейтрофилов. 2. Определение индекса фагоцитоза (процент клеток, участвующий в фагоцитозе) и фагоцитарного числа (число микробов или др. частиц, захваченных одной клеткой). Определение индекса завершенности фагоцитоза. 3. Определение бактерицидности фагоцитов (по НСТ-тесту и др. ). 4. Дополнительные уточняющие методы: • определение активности хемотаксиса фагоцитов; • определение способности нейтрофилов к адгезии к пластику и наличия клеток с адгезивными молекулами CD 11 CD 18.

Оценка функциональной активности лимфоцитов: (пролиферативный ответ на Т- и Вмитогены, цитотоксическая активность NK-клеток. Оценка цитокинового профиля: Определение ИЛ-1, -2, -4, -6 и др. Оценка интерферонового профиля: Определение ИФН-α и ИФН-γ.

Спасибо за внимание
АДАПТ-ИО-лекция-ИВ.ppt