Тюменская область. Ханты – Мансийский


Тюменская область. Ханты – Мансийский автономный округ. Нижневартовский район. МОУ Охтеурская ОСШ Задачник Разработал: Учитель химии – биологии первой квалификационной категории Баженов Алексей Анатольевич Закрой просмотр слайда. Прочти пояснение под слайдом. Выдели и удали эту запись. 28. 04. 2008 aleksei. bazhenov@mail. ru

Содержание: 1. Основные физические величины в химии. 2. Основные уравнения связи. 3. Правило пользования треугольником. 4. Расчеты по химическим уравнениям. Примерный порядок действий. 5. Сборник задач и их решений. 6. Тренировочная карточка.

Основные физические величины в химии Величина Характеристика Относительная атомная масса 1. Определение Относительная - это величина, показывающая, во сколько это количество вещества, содержащее - это число частиц (атомов, молекул или количество атомов углерода в 12 г молекулярная масса столько же частиц, больше массы атома раз масса атома больше 1/12 массы молекулы сколько содержится углерода (6, 02 1023 ). других частиц), х выраженных в молях. атомов углерода атома углерода. в 12 г углерода. Масса 2. Буквенное обозначение Моль MА N rr A m n Количество вещества 3. Единицы измерения Число Авогадро г; кг моль-1 Очистить
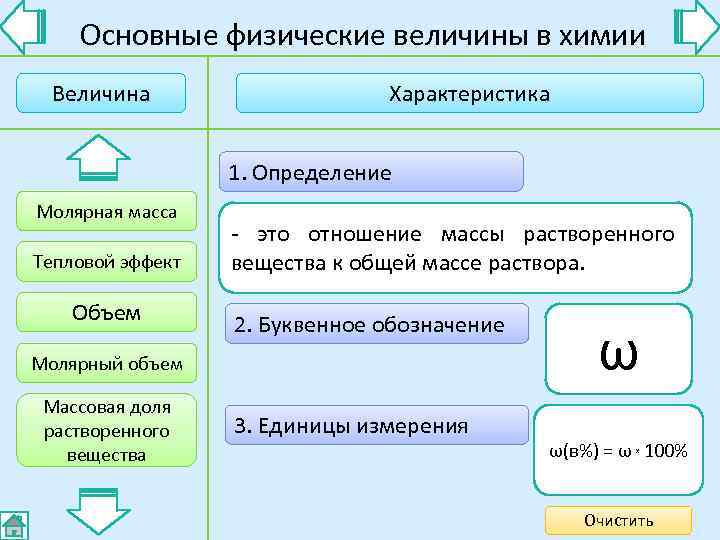
Основные физические величины в химии Величина Характеристика 1. Определение Молярная масса - это количество теплоты, которое - это объем 1 моль данного газа при это отношение массы растворенного - это масса одного моля вещества. выделяется или поглощается при Тепловой эффект вещества к общей массе раствора. нормальных условиях (22, 4 л). химической реакции. Объем 2. Буквенное обозначение Молярный объем Vм M ω Q V Массовая доля растворенного 3. Единицы измерения вещества г/моль мл; л к. Дж л/моль ω(в%) = ω 100% х Очистить
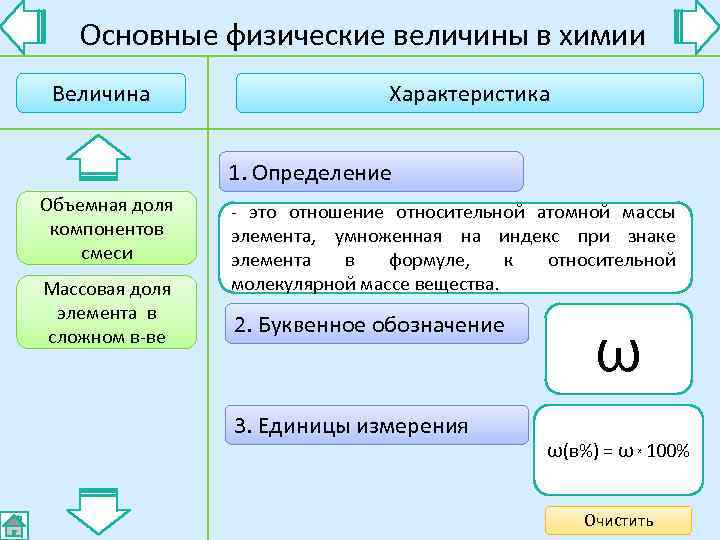
Основные физические величины в химии Величина Характеристика 1. Определение Объемная доля - это отношение относительной атомной массы компонентов - это отношение объема компонента смеси элемента, умноженная на индекс при знаке смеси элемента объему смеси. к к общему в формуле, относительной Массовая доля молекулярной массе вещества. элемента в 2. Буквенное обозначение сложном в-ве ω φ 3. Единицы измерения ω(в%) = φ 100% φ(в%) ω 100% хх Очистить
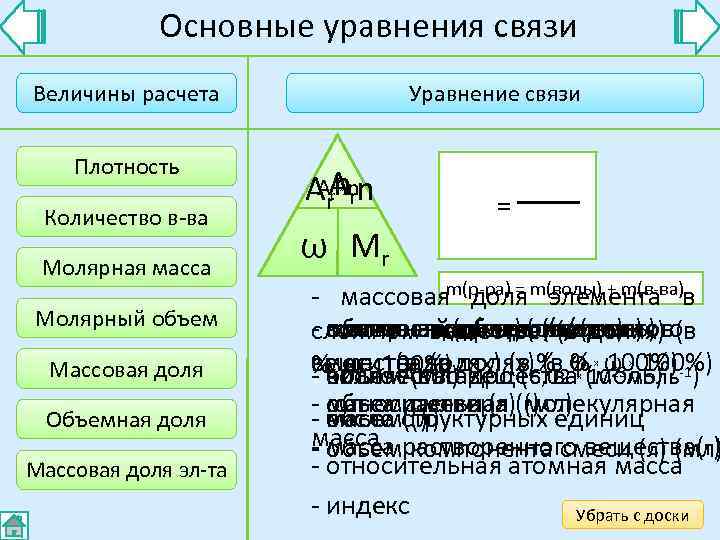
Основные уравнения связи Величины расчета Уравнение связи Плотность AVвв Amnn Vr N A xx rn r = Количество в-ва ρ m M Vсм ω V n nr Vm Maр φ N Молярная масса - массоваяm(р-ра) = m(воды) + m(в-ва)в доля элемента Молярный объем - плотностьдоля растворенного сложном веществе(л/моль) (в объемная вещества(моль) массовая (г/мл) количествообъем (в долях) молярныйдоля (г/моль) молярная массакомпонентов Массовая доля смеси 100%) долях)% %10100%) веществадолях) (в 6, 02φ(моль) -1) %объем. Авогадро ( (в ω моль φ (в (в вещества 23 100%) - количество число (мл) х х х - масса раствора)((мл) объем смеси (л г) относительная молекулярная Объемная доля - масса структурных единиц число (л) объем(г) масса растворенного вещества(г) - масса компонента смеси (л) (мл) объем Массовая доля эл-та - относительная атомная масса - индекс Убрать с доски
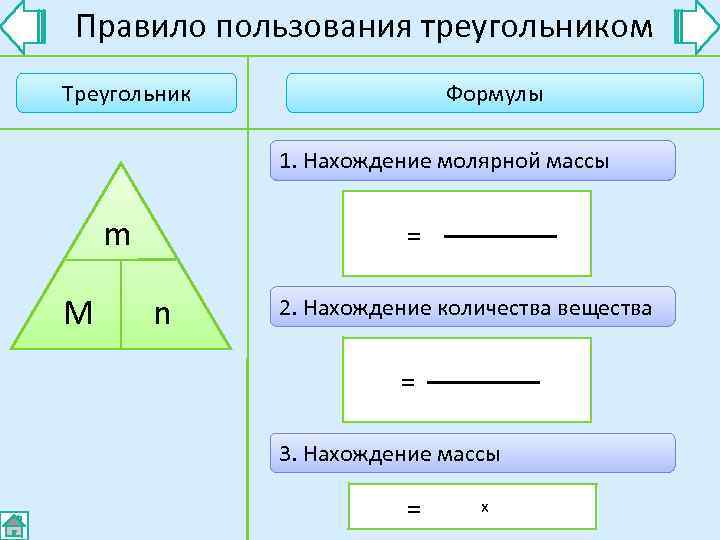
Правило пользования треугольником Треугольник Формулы 1. Нахождение молярной массы m = M n 2. Нахождение количества вещества = 3. Нахождение массы = х

Расчеты по химическим уравнениям Рассчитайте объем водорода (н. у. ), который потребуется Задача для взаимодействия с 480 г оксида железа (III). 3. Подчеркнуть вещества, речь овещества веществ в 4. Перевестиколичество количества которых идет и 6. Провести конечный у всех значения в моли. 7. Определить значения расчет. Действия 8. Полученные все известные подчеркнутых 5. Записать данные из условия задачи. записать 2. Рассчитать и записать количество у подчеркнутых 1. формулами веществ в уравнении реакции. условии над уравнениеуравнении реакции. записать задачи. над химической реакции. веществ по уравнению химической реакции. формулой в Дано: Решение: m(Fe 2 O 3) = 480 г 1 3 моль 9 моль Fe 2 O 3 + 3 H 2 2 Fe + 3 H 2 O 1 моль 3 моль m Найти: 2 n(Fe 2 O 3) - ? n = М(Fe 2 O 3) = 160 г/моль M V(H 2) - ? n(Fe 2 O 3) = 480 г : 160 г/моль = 3 моль 3 V(H 2) - ? V = Vm nx V(H 2) = 22, 4 л/моль x 9 моль = 201, 6 л Закрой просмотр слайда. Прочти Ответ: V(H 2) = 201, 6 л пояснение под слайдом. Выдели и удали эту запись.

Сборник задач и их решений. Задача № 1 Сколько молекул содержится в 11 г углекислого газа СО 2. Задача № 2 Найдите массу 15 x 1023 молекул кислорода. Задача № 3 Найдите массу 33, 6 л аммиака NH 3 при н. у. Найдите объем при н. у. , который имеют 1 8 x 10 23 Задача № 4 молекул сероводорода H 2 S. В 150 г воды растворили 50 г фосфорной кислоты. Найти Задача № 5 массовую долю кислоты в растворе. Сколько граммов воды и нитрата натрия нужно взять, Задача № 6 чтобы приготовить 80 г 5% -го раствора? Сколько литров кислорода может быть получено из 800 л Задача № 7 жидкого воздуха? Объемная доля кислорода в воздухе 0, 21.
Сборник задач и их решений. Найдите массу азота, полученного из 280 л воздуха (н. у. ), Задача № 8 если объемная доля азота в воздухе составляет 78%. Какой объем кислорода (н. у. ) потребуется для Задача № 9 взаимодействия с 270 г алюминия, содержащего 20% примесей. Какой объем водорода (н. у. ) выделится при Задача № 10 взаимодействии 730 г 30% соляной кислоты с цинком.

Задачи по теме: «Количество вещества» Сколько молекул содержится в 11 г углекислого Задача № 1 газа СО 2. Дано: Решение: m(CO 2) = 11 г 1 М(CO 2) - ? М(CO 2) = 12 + 16 2 = 44(г/моль) х m 2 n(CO 2) - ? n = M Найти: n(CO 2) = 11 г : 44 г/моль = 0, 25 моль N(CO 2) - ? 3 N(CO 2) - ? N = NA n x N(CO 2) = 6 1023 моль-1 0, 25 моль = 1, 5 1023 x x Ответ: N(CO 2) = 1, 5 1023 молекул x

Задачи по теме: «Количество вещества» Найдите массу 15 1023 молекул кислорода. x Задача № 2 Дано: Решение: N(O 2) = 1 М(O 2) - ? = 15 1023 x М(O 2) = 16 2 = 32(г/моль) х (молекул) N 2 n(O 2) - ? n = NA Найти: n(O 2) = 15 1023 : 6 1023 моль-1 = 2, 5 моль x x m(CO 2) - ? 3 m(O 2) - ? N = NA nx m(O 2) = 32 г/моль 2, 5 моль = 80 г x Ответ: m(O 2) = 80 г

Задачи по теме: «Молярный объем газов» Найдите массу 33, 6 л аммиака NH 3 при н. у. Задача № 3 Дано: Решение: V(NH 3) = 1 М(NH 3) - ? = 33, 6 л М(NH 3) = 14 + 1 3 = 17(г/моль) х V 2 n(NH 3) - ? n = Vm Найти: n(NH 3) = 33, 6 л : 22, 4 л/моль = 1, 5 моль m(NH 3) - ? 3 m(NH 3) - ? m = M n x m(NH 3) = 17 г/моль 1, 5 моль = 22, 5 г x Ответ: m(NH 3) = 22, 5 г

Задачи по теме: «Молярный объем газов» Найдите объем при н. у. , который имеют Задача № 4 18 1023 молекул сероводорода H 2 S. x Дано: Решение: N(H 2 S) = N 1 n(H 2 S) - ? n = = 18 1023 x NA (молекул) n(H 2 S) = 18 1023 : 6 1023 моль-1 = 3 моль x x 2 V(H 2 S) - ? V = Vm n x Найти: V(H 2 S) = 22, 4 л/моль 3 моль = 67, 2 л x V(H 2 S) - ? Ответ: m(H 2 S) = 67, 2 л

Задачи по теме: «Массовая доля» В 150 г воды растворили 50 г фосфорной кислоты. Найти Задача № 5 массовую долю кислоты в растворе. Дано: Решение: 1 mp- ? mp = mв + m(H 2 O) m(H 3 PO 4) = 50 г mp= 50 г + 150 г = 200 г m(H 2 O) = 150 г mв 2 ω(H 3 PO 4) - ? ω = mр Найти: ω(H 3 PO 4) = 50 г : 200 г = 0, 25 (25%) ω(H 3 PO 4) - ? Ответ: ω(H 3 PO 4) = 0, 25 (25%)

Задачи по теме: «Массовая доля» Сколько граммов воды и нитрата натрия нужно взять, Задача № 6 чтобы приготовить 80 г 5% -го раствора? Дано: Решение: mp = 80 г 1 m(Na. NO 3) - ? mв = mр ω x ω(Na. NO 3) = m(Na. NO 3) = 80 г 0, 05 = 4 г х = 0, 05 2 m(H 2 O) - ? m(H 2 O) = mp - mв Найти: m(H 2 O) = 80 г – 4 г = 76 г m(Na. NO 3) - ? m(H 2 O) - ? Ответ: m(Na. NO 3) = 4 г; m(H 2 O) = 76 г

Задачи по теме: «Объемная доля» Сколько литров кислорода может быть получено из 800 л Задача № 7 жидкого воздуха? Объемная доля кислорода в воздухе 0, 21. Дано: Решение: V(возд) = = 1 V(O 2) - ? Vв = Vсм φ x 800 л V(O 2) = 800 л 0, 21 = 168 л х φ(O 2) = 0, 21 Найти: V(O 2) - ? Ответ: V(O 2) = 168 л

Задачи по теме: «Объемная доля» Найдите массу азота, полученного из 280 л воздуха (н. у. ), Задача № 8 если объемная доля азота в воздухе составляет 78%. Дано: Решение: V(возд) = 1 V(N 2) - ? Vв = Vсм φx = 280 л V(N 2) = 280 л 0, 78 = 218, 4 л х φ(N 2) = 0, 78 V 2 n(N 2) - ? n= Vm Найти: n(N 2) = 218, 4 л : 22, 4 л/моль = 9, 75 моль m(N 2) - ? 3 m(N 2) - ? m=M n x m(N 2) = 28 г/моль 9, 75 моль = 273 г x Ответ: m(N 2) = 273 г

Расчеты по химическим уравнениям Какой объем кислорода (н. у. ) потребуется для Задача № 9 взаимодействия с 270 г алюминия, содержащего 20% примесей. Дано: Решение: m(Al) =270 г 6 моль 1 ω ( примесей ) = 4 Al + 3 O 2 2 Al 2 O 3 = 20% (0, 2) 4 моль 3 моль 2 m(чист)(Al) - ? m(чист) = m(см) х ω(Al) Найти: ω(Al) = 1 - ω(прим) ω(Al) = 1 - 0, 2 = 0, 8 V(O 2) - ? m(Al) = 270 г x 0, 8= 216 г 3 m n(Al) - ? n = n(Al) = 216 г : 27 г/моль = 8 моль 8 моль M 4 V(O 2) - ? V = Vm n x V(O 2)= 22, 4 л/моль x 6 моль = 134, 4 л Ответ: V(O 2) = 134, 4 л

Расчеты по химическим уравнениям Какой объем водорода (н. у. ) выделится при Задача № 10 взаимодействии 730 г 30% соляной кислоты с цинком. Дано: Решение: 3 моль mр-ра(HCl) =730 г 1 ω (HCl) = 30 % Zn + 2 HCl Zn. Cl 2 + H 2 2 моль 1 моль (0, 3) 2 m(HCl) - ? m (в-ва) = m(р-ра) х ω Найти: m(HCl) = 730 г x 0, 3 = 219 г V(H 2) - ? 3 m n(HCl) - ? n= M n(HCl) = 219 г : 36, 5 г/моль = 6 моль 4 V(H 2) - ? V = Vm n x V(H 2)= 22, 4 л/моль x 3 моль = 67, 2 л Ответ: V(H 2) = 67, 2 л

Найти соответствие. Масса л/моль л ω Объем моль m г/моль Массовая доля г/мл % n Количество вещества V M г Молярная масса кг мл а. е. м. Ошибки 10 9 8 7 6 5 4 3 2 1

