Гемолитическая болезнь плода и новорожденного.pptx
- Количество слайдов: 29
 Тюменская Государственная Медицинская Академия Кафедра акушерства и гинекологии Гемолитическая болезнь плода и новорожденного. Выполнила: Студентка 408 группы Безель Т. В Тюмень 2012
Тюменская Государственная Медицинская Академия Кафедра акушерства и гинекологии Гемолитическая болезнь плода и новорожденного. Выполнила: Студентка 408 группы Безель Т. В Тюмень 2012
 Гемолитическая болезнь новорожденного – заболевание, возникающее в результате несовместимости крови матери и ребенка по некоторым антигенам.
Гемолитическая болезнь новорожденного – заболевание, возникающее в результате несовместимости крови матери и ребенка по некоторым антигенам.
 Распространенность и актуальность Гемолитическая болезнь новорождённых (ГБН) в России диагностируется у 0, 6% всех новорождённых. Перинатальная летальность в настоящее время среди этих детей составляет до 2, 5%. Среди детей, перенесших ГБН наблюдаются тяжёлые органические поражения ЦНС, отмечается повышенная инфекционная заболеваемость, 52% из этих детей имеет экссудативно-катаральный диатез, в последующем эволюционирующий в экзему и нейродермит.
Распространенность и актуальность Гемолитическая болезнь новорождённых (ГБН) в России диагностируется у 0, 6% всех новорождённых. Перинатальная летальность в настоящее время среди этих детей составляет до 2, 5%. Среди детей, перенесших ГБН наблюдаются тяжёлые органические поражения ЦНС, отмечается повышенная инфекционная заболеваемость, 52% из этих детей имеет экссудативно-катаральный диатез, в последующем эволюционирующий в экзему и нейродермит.
 История Впервые признаки ГБН были описаны Гиппократом за 400 лет до нашей эры Первый клинический случай описан французкими акушерами в 1609 году: недоношенная двойня, второй плод имел выраженную желтуху и вскоре умер Diamond с соавторами описал экстрамедуллярный эритропоэз и гемолиз эритроцитов у детей с ГБН в 1932. Патофизиологический механизм оставался неизвестным до 1940 года, когда Landsteiner открыл Rh антиген, вводя кровь Macaca mulatta (обезьян rhesus) морским свинкам и кроликам, они получили антиэритроцитарную сыворотку, и когда ввели её другим обезьянам, произошла агглютинация эритроцитов. Агглютинация была прямым результатом присутствия антигенов, которые они назвали rhesus (Rh). В 1941 году Levine наблюдал Rh- женщин подвергшихся воздействию Rh+ эритроцитов, у которых сформировались антитела, вызывающие гемолиз эритроцитов
История Впервые признаки ГБН были описаны Гиппократом за 400 лет до нашей эры Первый клинический случай описан французкими акушерами в 1609 году: недоношенная двойня, второй плод имел выраженную желтуху и вскоре умер Diamond с соавторами описал экстрамедуллярный эритропоэз и гемолиз эритроцитов у детей с ГБН в 1932. Патофизиологический механизм оставался неизвестным до 1940 года, когда Landsteiner открыл Rh антиген, вводя кровь Macaca mulatta (обезьян rhesus) морским свинкам и кроликам, они получили антиэритроцитарную сыворотку, и когда ввели её другим обезьянам, произошла агглютинация эритроцитов. Агглютинация была прямым результатом присутствия антигенов, которые они назвали rhesus (Rh). В 1941 году Levine наблюдал Rh- женщин подвергшихся воздействию Rh+ эритроцитов, у которых сформировались антитела, вызывающие гемолиз эритроцитов
 История 1948 год – Wiener постулирует, что трансплацентарный пассаж фетальных эритроцитов является триггером продукции антител против фетальных клеток и предложил для лечения ОЗПК. В середине 1950 х – Chow подтвердил материнскую сенсибилизацию через трансплацентарный пассаж Rh. D+ крови 1961 год - Finn предложил анти-D антитела для профилактики ГБН
История 1948 год – Wiener постулирует, что трансплацентарный пассаж фетальных эритроцитов является триггером продукции антител против фетальных клеток и предложил для лечения ОЗПК. В середине 1950 х – Chow подтвердил материнскую сенсибилизацию через трансплацентарный пассаж Rh. D+ крови 1961 год - Finn предложил анти-D антитела для профилактики ГБН
 Основные виды конфликтов Rh Kell-23 антигена гены которых на 7 хромосоме, наиболее сильные К 1 и К 2, 91% людей Kell негативны, только у 5% появляются анти. Эр антитела после переливания несовместимой крови АВО Duffy, Diego, Kidd, MNSs, P, C, c, и E
Основные виды конфликтов Rh Kell-23 антигена гены которых на 7 хромосоме, наиболее сильные К 1 и К 2, 91% людей Kell негативны, только у 5% появляются анти. Эр антитела после переливания несовместимой крови АВО Duffy, Diego, Kidd, MNSs, P, C, c, и E
 Патофизиология Rh. D изоиммунизации ГБН – гемолиз эритроцитов плода и новорожденного ребенка в результате присутствия анти. D антител в крови больного Изоиммуннизация развивается вследствие попадания Rh+ эритроцитов плода в кровоток Rh– беременной женщины. Данный процесс может быть либо следствием трансфузии крови в ассоциации с беременностью или в результате аборта, или спонтанно при беременности через асимптоматический трансплацентарный пассаж Rh+ эритроцитов плода – фетоматеринская траснфузия, имеющая место в 7% в 1 триместре, в 16% во 2 триместре и в 29% в 3 триместре беременности. В интранатальном периоде отмечаются фетоматеринские геморрагии превышают 50% случаев. Для анти. D-изоиммунизации достаточно утечки 0, 2 мл крови плода
Патофизиология Rh. D изоиммунизации ГБН – гемолиз эритроцитов плода и новорожденного ребенка в результате присутствия анти. D антител в крови больного Изоиммуннизация развивается вследствие попадания Rh+ эритроцитов плода в кровоток Rh– беременной женщины. Данный процесс может быть либо следствием трансфузии крови в ассоциации с беременностью или в результате аборта, или спонтанно при беременности через асимптоматический трансплацентарный пассаж Rh+ эритроцитов плода – фетоматеринская траснфузия, имеющая место в 7% в 1 триместре, в 16% во 2 триместре и в 29% в 3 триместре беременности. В интранатальном периоде отмечаются фетоматеринские геморрагии превышают 50% случаев. Для анти. D-изоиммунизации достаточно утечки 0, 2 мл крови плода
 Факторы, способствующие изоиммуннизации Спонтанный аборт – 2%-3% Медицинский аборт – 4%-5% Эктопическая беременность – 2%-5% Биопсия ворсин хориона – 50% Амниоцентез – 10% Кордоцентез – 40% Отслойка/предлежание плаценты Интранатальные кровотечения Травма Перинатальный период (28 недель гестации, до 72 часа после родов) 7%-8% до 15% Роды 50%
Факторы, способствующие изоиммуннизации Спонтанный аборт – 2%-3% Медицинский аборт – 4%-5% Эктопическая беременность – 2%-5% Биопсия ворсин хориона – 50% Амниоцентез – 10% Кордоцентез – 40% Отслойка/предлежание плаценты Интранатальные кровотечения Травма Перинатальный период (28 недель гестации, до 72 часа после родов) 7%-8% до 15% Роды 50%
 Попадание Rh + эритроцитов плода в кровоток матери не всегда приводит к изосенсибилизации, в некоторых случаях это объясняется защитным действием одновременной несовместимости по АВО системе. В этих условиях гемолиз, активируемый АВО несовместимостью разрушает фетальные эритроциты в материнском кровотоке. В результате Rh. D антиген не распознается Rh системой и изосенсибилизации по Rh не происходит. С АВО несовместимостью риск Rh несовместимости снижается на 16%.
Попадание Rh + эритроцитов плода в кровоток матери не всегда приводит к изосенсибилизации, в некоторых случаях это объясняется защитным действием одновременной несовместимости по АВО системе. В этих условиях гемолиз, активируемый АВО несовместимостью разрушает фетальные эритроциты в материнском кровотоке. В результате Rh. D антиген не распознается Rh системой и изосенсибилизации по Rh не происходит. С АВО несовместимостью риск Rh несовместимости снижается на 16%.
 Клинические формы Внутриутробная смерть и мацерация плода Отечная (Гемолитическая анемия с водянкой) Анемическая (Гемолитическая анемия без желтухи и водянки) Желтушная (Гемолитическая анемия с желтухой)
Клинические формы Внутриутробная смерть и мацерация плода Отечная (Гемолитическая анемия с водянкой) Анемическая (Гемолитическая анемия без желтухи и водянки) Желтушная (Гемолитическая анемия с желтухой)
 По тяжести Легкая Средней тяжести Тяжелая
По тяжести Легкая Средней тяжести Тяжелая
 По осложнениям Неосложненная Ядерная желтуха Синдром сгущения желчи Геморрагический синдром Поражение почек Поражение надпочечников Гипогликемия и др.
По осложнениям Неосложненная Ядерная желтуха Синдром сгущения желчи Геморрагический синдром Поражение почек Поражение надпочечников Гипогликемия и др.
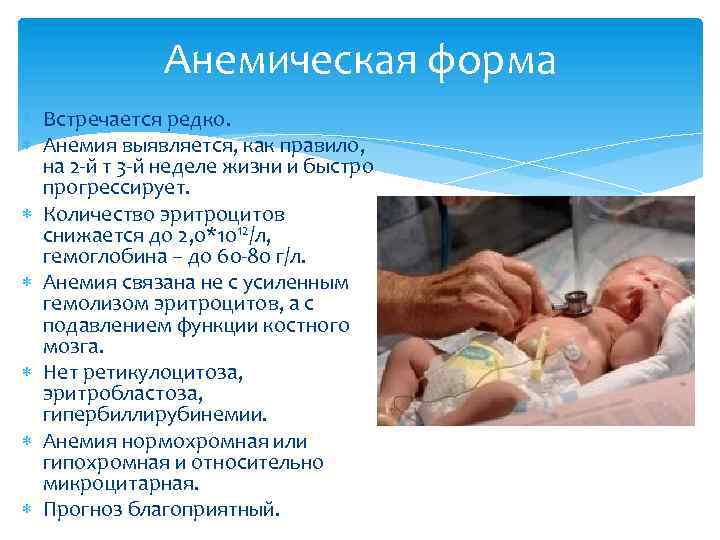 Анемическая форма Встречается редко. Анемия выявляется, как правило, на 2 -й т 3 -й неделе жизни и быстро прогрессирует. Количество эритроцитов снижается до 2, 0*1012/л, гемоглобина – до 60 -80 г/л. Анемия связана не с усиленным гемолизом эритроцитов, а с подавлением функции костного мозга. Нет ретикулоцитоза, эритробластоза, гипербиллирубинемии. Анемия нормохромная или гипохромная и относительно микроцитарная. Прогноз благоприятный.
Анемическая форма Встречается редко. Анемия выявляется, как правило, на 2 -й т 3 -й неделе жизни и быстро прогрессирует. Количество эритроцитов снижается до 2, 0*1012/л, гемоглобина – до 60 -80 г/л. Анемия связана не с усиленным гемолизом эритроцитов, а с подавлением функции костного мозга. Нет ретикулоцитоза, эритробластоза, гипербиллирубинемии. Анемия нормохромная или гипохромная и относительно микроцитарная. Прогноз благоприятный.
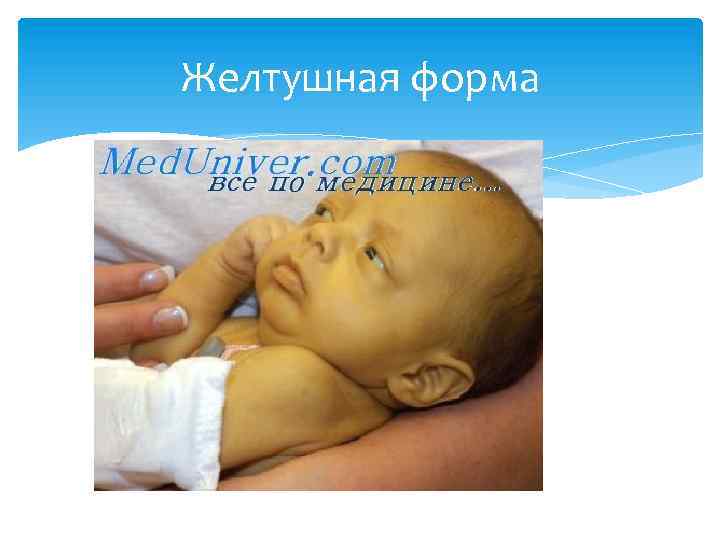
 Желтушная форма Встречается наиболее часто. Легкая форма заболевания чаще наблюдается при несоответствии крови матери и ребенка по групповым антигенам системы АВО. Тяжелая форма иногда выявляется уже при рождении ребенка: кожные покровы бледно-желтушные, печень и селезенка увеличены, мышечный тонус и рефлексы снижены, недостаточно активен крик. Снижение активности сосания, беспокойство, вскрикивания, глазодвигательные нарушения, судороги, расстройства дыхания, сердцебиения, резкое повышение температуры до 40 -41 С и наступает смерть. В агональном периоде нередко отмечают геморрагические явления – кровоизлияния в кожу, кишечник, легкие. Перед смертью может развиться отек легких и пневмония, чаще геморрагического характера.
Желтушная форма Встречается наиболее часто. Легкая форма заболевания чаще наблюдается при несоответствии крови матери и ребенка по групповым антигенам системы АВО. Тяжелая форма иногда выявляется уже при рождении ребенка: кожные покровы бледно-желтушные, печень и селезенка увеличены, мышечный тонус и рефлексы снижены, недостаточно активен крик. Снижение активности сосания, беспокойство, вскрикивания, глазодвигательные нарушения, судороги, расстройства дыхания, сердцебиения, резкое повышение температуры до 40 -41 С и наступает смерть. В агональном периоде нередко отмечают геморрагические явления – кровоизлияния в кожу, кишечник, легкие. Перед смертью может развиться отек легких и пневмония, чаще геморрагического характера.
 Желтушная форма В некоторых случаях после ядерной желтухи наступает выздоровление, все симптомы исчезают, ребенок становится активным, хорошо сосет, увеличивается масса тела. В клинической картине тяжелой желтушной формы ГБ степень анемизации ребенка к моменту рождения не имеет решающего прогностического значения. Основным показателем тяжести заболевания является интенсивность прироста билирубина в крови.
Желтушная форма В некоторых случаях после ядерной желтухи наступает выздоровление, все симптомы исчезают, ребенок становится активным, хорошо сосет, увеличивается масса тела. В клинической картине тяжелой желтушной формы ГБ степень анемизации ребенка к моменту рождения не имеет решающего прогностического значения. Основным показателем тяжести заболевания является интенсивность прироста билирубина в крови.
 Желтушная форма
Желтушная форма
 Отечная форма Плод чаще погибает внутриутробно Наиболее тяжелая форма заболевания Если плод не погибает, то ребенок рождается преждевременно и имеет характерный внешний вид: бледные слизистые оболочки и кожные покровы, видны петехии и геморрагии. Асцит, увеличение печени и селезенки. В крови число эритроцитов не превышает 1, 5*1012/л, содержание гемоглобина до 80 г/л, значительно увеличено число ядерных форм эритроцитов ( «фетальный эритробластоз» )
Отечная форма Плод чаще погибает внутриутробно Наиболее тяжелая форма заболевания Если плод не погибает, то ребенок рождается преждевременно и имеет характерный внешний вид: бледные слизистые оболочки и кожные покровы, видны петехии и геморрагии. Асцит, увеличение печени и селезенки. В крови число эритроцитов не превышает 1, 5*1012/л, содержание гемоглобина до 80 г/л, значительно увеличено число ядерных форм эритроцитов ( «фетальный эритробластоз» )
 Антенатальная диагностика Определение групп крови и резус принадлежности ПЦР (генетический анализ) – предимплантационное исследование или в первый триместр беременности HLA типирование (выявление HLA-DQB 1 allele 0201 ) Непрямая проба Кумбса в первый триместр беременности Анти-D титр 1: 8 (если да, то ежемесячно); 1: 16 – необходимость в инвазивном исследовании. Методы: ИФА (ELISA), проточно-лазерная цитометрия, радиоиммуноанализ, Auto. Analyzer (Technicon Corporation, UK) - Антителзависимая клеточная цитотоксичность Амниоцентез или кордоцентез, если первая изосенсибилизационная беременность в 26 -28 недель. Однако если отек плода развивается в 22 нед, то в это время может понадобиться кордоцентез. Если титр 1: 128, то кордоцентез следует выполнить в 20 – 24 недели гестации АОК: Эр, Hb, Ht, ретикулоциты, нормобласты, лейкоциты Билирубин и его фракции, ЩФ, ГГТ, АСТ, АЛТ, глюкоза, белок и фракции (альбумин, глобулины) Систолическая скорость кровотока средней мозговой артерии плода – Доплер Спектрофотометрия околоплодных вод Изучение продукции СО Транскутанная билирубинометрия
Антенатальная диагностика Определение групп крови и резус принадлежности ПЦР (генетический анализ) – предимплантационное исследование или в первый триместр беременности HLA типирование (выявление HLA-DQB 1 allele 0201 ) Непрямая проба Кумбса в первый триместр беременности Анти-D титр 1: 8 (если да, то ежемесячно); 1: 16 – необходимость в инвазивном исследовании. Методы: ИФА (ELISA), проточно-лазерная цитометрия, радиоиммуноанализ, Auto. Analyzer (Technicon Corporation, UK) - Антителзависимая клеточная цитотоксичность Амниоцентез или кордоцентез, если первая изосенсибилизационная беременность в 26 -28 недель. Однако если отек плода развивается в 22 нед, то в это время может понадобиться кордоцентез. Если титр 1: 128, то кордоцентез следует выполнить в 20 – 24 недели гестации АОК: Эр, Hb, Ht, ретикулоциты, нормобласты, лейкоциты Билирубин и его фракции, ЩФ, ГГТ, АСТ, АЛТ, глюкоза, белок и фракции (альбумин, глобулины) Систолическая скорость кровотока средней мозговой артерии плода – Доплер Спектрофотометрия околоплодных вод Изучение продукции СО Транскутанная билирубинометрия
 Лечение Супрессивная терапия – внутривенный иммуноглобулин человека, обратное ингибирования синтеза антител, блокировка ретикулоэндотелиальных Fc рецепторов, блок трансплацентарного транспорта АТ, может ограничить внутриутробные трансфузии Внутриутробные трансфузии: показания – Ht<30%; цель – достигнуть гематокрита 40%. Переливают восстановленную кровь с гематокритом 90%. Посттрансфузионный гематокрит плода не должен превышать 55%. Выбор времени для родов.
Лечение Супрессивная терапия – внутривенный иммуноглобулин человека, обратное ингибирования синтеза антител, блокировка ретикулоэндотелиальных Fc рецепторов, блок трансплацентарного транспорта АТ, может ограничить внутриутробные трансфузии Внутриутробные трансфузии: показания – Ht<30%; цель – достигнуть гематокрита 40%. Переливают восстановленную кровь с гематокритом 90%. Посттрансфузионный гематокрит плода не должен превышать 55%. Выбор времени для родов.
 Лечение Начальные и реанимационные мероприятия по приказу 372 Прикладывание к груди и грудное вскармливание (индивидуально) Очистительная клизма в первые 2 часа после рождения снижает риск и степень желтухи Эффективность назначения энтеросорбентов не исследовалась Иммуноглобулин Фототерапия ОЗПК Эритропоэтины Препараты железа
Лечение Начальные и реанимационные мероприятия по приказу 372 Прикладывание к груди и грудное вскармливание (индивидуально) Очистительная клизма в первые 2 часа после рождения снижает риск и степень желтухи Эффективность назначения энтеросорбентов не исследовалась Иммуноглобулин Фототерапия ОЗПК Эритропоэтины Препараты железа
 Лечение иммуноглобуллинами Раннее введение в первые 2 часа 1 г/кг каждые 4 часа 500 мг/кг каждые 2 часа 800 мг/кг ежедневно в течении 3 дней
Лечение иммуноглобуллинами Раннее введение в первые 2 часа 1 г/кг каждые 4 часа 500 мг/кг каждые 2 часа 800 мг/кг ежедневно в течении 3 дней
 Системы фототерапии
Системы фототерапии
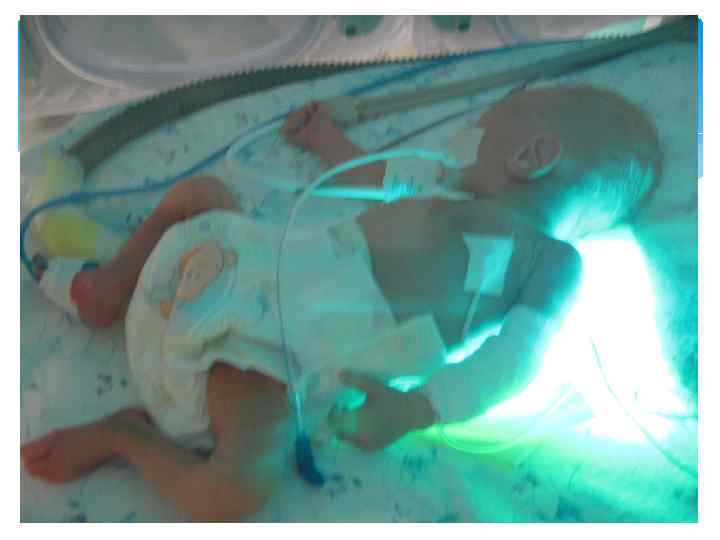

 Прекращение фототерапии Снижение общего билирубина менее 220 мкмоль/л Через сутки после прекращения провести контроль уровня билирубина в крови Осложнения фототерапии Синдром бронзового ребенка Пурпура Поражения кожи Фотодерматит у больных порфирией
Прекращение фототерапии Снижение общего билирубина менее 220 мкмоль/л Через сутки после прекращения провести контроль уровня билирубина в крови Осложнения фототерапии Синдром бронзового ребенка Пурпура Поражения кожи Фотодерматит у больных порфирией
 Заменное переливание крови Наиболее эффективным способом снижения уровня билирубина является заменное переливание крови. Показаниями к нему у доношенных детей являются положительная проба Кумбса, содержание гемоглобина ниже 90 г/л, билирубина 342 мкмоль/л, темп нарастания (в час) билирубина выше 6, 0 мкмоль/л и уровень его в пуповинной крови 60 мкмоль/л. Сущность его состоит в том, чтобы заменить кровью донора кровь ребенка, содержащую неполноценные, гемолизированные эритроциты. Кровь донора временно выполняет обычную функцию крови. Собственное кроветворение ребенка в первое время подавляется. При АВО несовместимости используется кровь группы 0(I), совпадающая с кровью ребенка по резус-фактору.
Заменное переливание крови Наиболее эффективным способом снижения уровня билирубина является заменное переливание крови. Показаниями к нему у доношенных детей являются положительная проба Кумбса, содержание гемоглобина ниже 90 г/л, билирубина 342 мкмоль/л, темп нарастания (в час) билирубина выше 6, 0 мкмоль/л и уровень его в пуповинной крови 60 мкмоль/л. Сущность его состоит в том, чтобы заменить кровью донора кровь ребенка, содержащую неполноценные, гемолизированные эритроциты. Кровь донора временно выполняет обычную функцию крови. Собственное кроветворение ребенка в первое время подавляется. При АВО несовместимости используется кровь группы 0(I), совпадающая с кровью ребенка по резус-фактору.
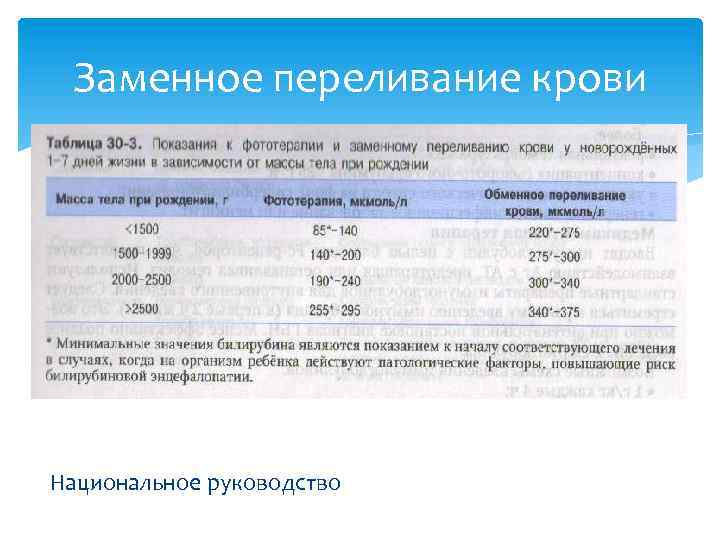 Заменное переливание крови Национальное руководство
Заменное переливание крови Национальное руководство
 Заменное переливание крови Количество переливаний крови определяется из расчета 150 -160 мл на 1 кг массы тела, в среднем при операции вводится 500 мл крови донора выводится на 50 мл меньше (450 мл). Если после первого ЗПК желтуха продолжает нарастать, уровень билирубина снова повышается до критических величин, требуются повторные ЗПК.
Заменное переливание крови Количество переливаний крови определяется из расчета 150 -160 мл на 1 кг массы тела, в среднем при операции вводится 500 мл крови донора выводится на 50 мл меньше (450 мл). Если после первого ЗПК желтуха продолжает нарастать, уровень билирубина снова повышается до критических величин, требуются повторные ЗПК.



