Твердые тела Лекция по курсу «Химия














кристаллы_химия радиоматерилов.ppt
- Количество слайдов: 21
 Твердые тела Лекция по курсу «Химия радиоматериалов»
Твердые тела Лекция по курсу «Химия радиоматериалов»
 Аморфные вещества Главный признак аморфного (от греческого "аморфос" - бесформенный) состояние вещества - отсутствие атомной или молекулярной решетки, то есть трехмерной периодичности структуры, характерной для кристаллического состояния. ØАморфные тела изотропны, то есть их механические, оптические, электрические и другие свойства не зависят от направления. ØУ аморфных тел нет фиксированной температуры плавления: плавление происходит в некотором температурном интервале. ØПереход аморфного вещества из твердого состояния в жидкое не сопровождается скачкообразным изменением свойств.
Аморфные вещества Главный признак аморфного (от греческого "аморфос" - бесформенный) состояние вещества - отсутствие атомной или молекулярной решетки, то есть трехмерной периодичности структуры, характерной для кристаллического состояния. ØАморфные тела изотропны, то есть их механические, оптические, электрические и другие свойства не зависят от направления. ØУ аморфных тел нет фиксированной температуры плавления: плавление происходит в некотором температурном интервале. ØПереход аморфного вещества из твердого состояния в жидкое не сопровождается скачкообразным изменением свойств.
 Кристаллические вещества Кристалл (от греч. "кристаллос" – лед) химические частицы (атомы, молекулы, ионы) расположены в определенном порядке, образуя в пространстве кристаллическую решетку Кристаллическое состояние характеризуется наличием дальнего порядка в расположении частиц и симметрией кристаллической решетки
Кристаллические вещества Кристалл (от греч. "кристаллос" – лед) химические частицы (атомы, молекулы, ионы) расположены в определенном порядке, образуя в пространстве кристаллическую решетку Кристаллическое состояние характеризуется наличием дальнего порядка в расположении частиц и симметрией кристаллической решетки
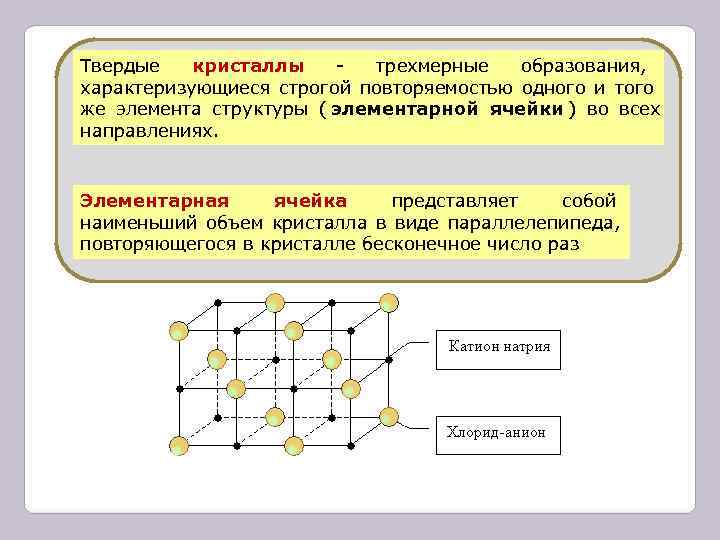
 Твердые кристаллы - трехмерные образования, характеризующиеся строгой повторяемостью одного и того же элемента структуры ( элементарной ячейки ) во всех направлениях. Элементарная ячейка представляет собой наименьший объем кристалла в виде параллелепипеда, повторяющегося в кристалле бесконечное число раз
Твердые кристаллы - трехмерные образования, характеризующиеся строгой повторяемостью одного и того же элемента структуры ( элементарной ячейки ) во всех направлениях. Элементарная ячейка представляет собой наименьший объем кристалла в виде параллелепипеда, повторяющегося в кристалле бесконечное число раз
 Типы кристаллических решеток (по виду химической связи)
Типы кристаллических решеток (по виду химической связи)
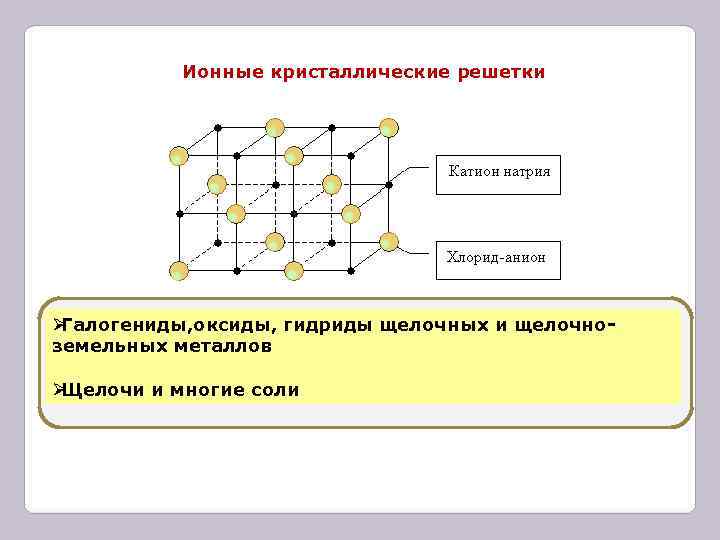
 Ионные кристаллические решетки ØГалогениды, оксиды, гидриды щелочных и щелочно- земельных металлов ØЩелочи и многие соли
Ионные кристаллические решетки ØГалогениды, оксиды, гидриды щелочных и щелочно- земельных металлов ØЩелочи и многие соли
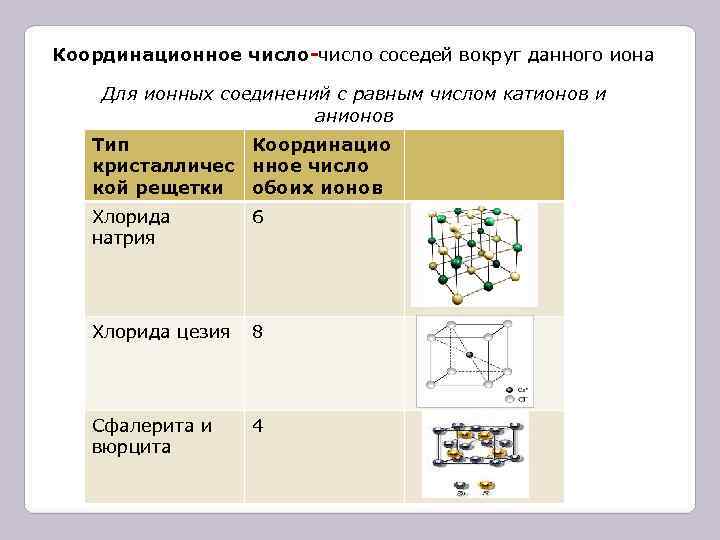
 Координационное число-число соседей вокруг данного иона Для ионных соединений с равным числом катионов и анионов Тип Координацио кристалличес нное число кой рещетки обоих ионов Хлорида 6 натрия Хлорида цезия 8 Сфалерита и 4 вюрцита
Координационное число-число соседей вокруг данного иона Для ионных соединений с равным числом катионов и анионов Тип Координацио кристалличес нное число кой рещетки обоих ионов Хлорида 6 натрия Хлорида цезия 8 Сфалерита и 4 вюрцита
 Если число катионов вдвое меньше числа анионов, то координационное число катионов должно быть вдвое больше координационного числа анионов. Тип Координацио кристалличес нные числа кой решетки Флюорита 8 и 4 Рутила 6 и 3 Кристобалита 4 и 2
Если число катионов вдвое меньше числа анионов, то координационное число катионов должно быть вдвое больше координационного числа анионов. Тип Координацио кристалличес нные числа кой решетки Флюорита 8 и 4 Рутила 6 и 3 Кристобалита 4 и 2
 Координационные числа в ионных решетках зависят от соотношения радиуса катиона (Rк) и аниона (Rа) Для бинарных ионных соединений типа К+А- их определяют по правилу Магнуса—Брэгга
Координационные числа в ионных решетках зависят от соотношения радиуса катиона (Rк) и аниона (Rа) Для бинарных ионных соединений типа К+А- их определяют по правилу Магнуса—Брэгга
 Свойства ионных кристаллов Øтвердые, но хрупкие Øдиэлектрики Øвысокие температуры плавления. Øв расплавленном состоянии вещества, образующие ионные кристаллы, электропроводны
Свойства ионных кристаллов Øтвердые, но хрупкие Øдиэлектрики Øвысокие температуры плавления. Øв расплавленном состоянии вещества, образующие ионные кристаллы, электропроводны
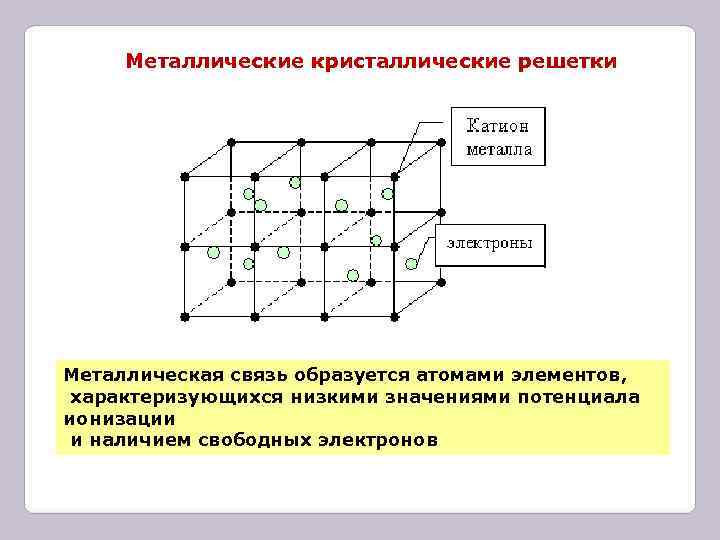
 Металлические кристаллические решетки Металлическая связь образуется атомами элементов, характеризующихся низкими значениями потенциала ионизации и наличием свободных электронов
Металлические кристаллические решетки Металлическая связь образуется атомами элементов, характеризующихся низкими значениями потенциала ионизации и наличием свободных электронов
 Свойства веществ с металлическим типом связи ØКоординационные числа- 12 и 8 ØТвердые ØТугоплавкие ØМалолетучие ØВысокая электропроводность
Свойства веществ с металлическим типом связи ØКоординационные числа- 12 и 8 ØТвердые ØТугоплавкие ØМалолетучие ØВысокая электропроводность
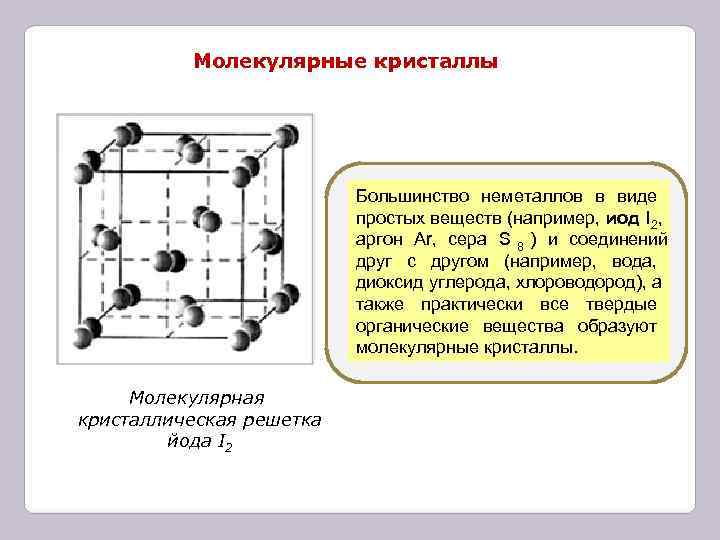
 Молекулярные кристаллы Большинство неметаллов в виде простых веществ (например, иод I 2 , аргон Ar, сера S 8 ) и соединений друг с другом (например, вода, диоксид углерода, хлороводород), а также практически все твердые органические вещества образуют молекулярные кристаллы. Молекулярная кристаллическая решетка йода I 2
Молекулярные кристаллы Большинство неметаллов в виде простых веществ (например, иод I 2 , аргон Ar, сера S 8 ) и соединений друг с другом (например, вода, диоксид углерода, хлороводород), а также практически все твердые органические вещества образуют молекулярные кристаллы. Молекулярная кристаллическая решетка йода I 2
 Межмолекулярные силы возникают за счет электростатического взаимодействия отрицательно заряженных электронов одной молекулы с положительно заряженными ядрами соседних молекул. Свойства молекулярных кристаллов Øнизкие температуры плавления, малая твердость, Ø высокая летучесть. Øне обладают электрической проводимостью, Ø их растворы и расплавы не проводят электрический ток.
Межмолекулярные силы возникают за счет электростатического взаимодействия отрицательно заряженных электронов одной молекулы с положительно заряженными ядрами соседних молекул. Свойства молекулярных кристаллов Øнизкие температуры плавления, малая твердость, Ø высокая летучесть. Øне обладают электрической проводимостью, Ø их растворы и расплавы не проводят электрический ток.
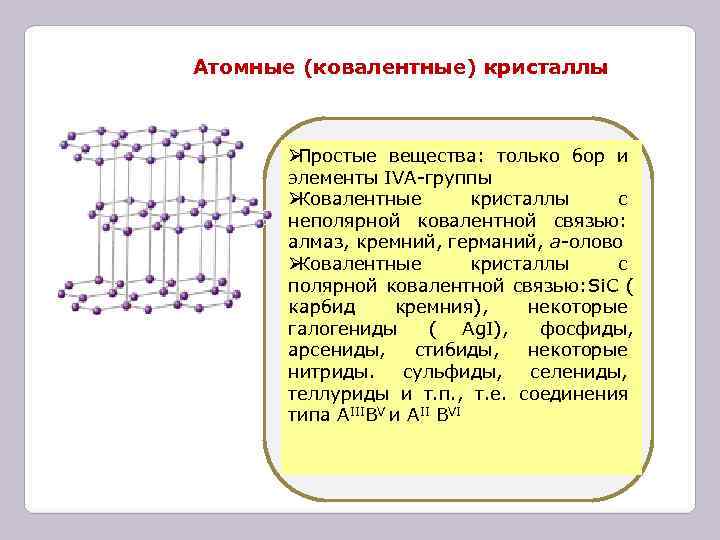
 Атомные (ковалентные) кристаллы ØПростые вещества: только бор и элементы IVA-группы ØКовалентные кристаллы с неполярной ковалентной связью: алмаз, кремний, германий, а-олово ØКовалентные кристаллы с полярной ковалентной связью: Si. C ( карбид кремния), некоторые галогениды ( Ag. I), фосфиды, арсениды, стибиды, некоторые нитриды. сульфиды, селениды, теллуриды и т. п. , т. е. соединения типа АIIIBV и AII BVI
Атомные (ковалентные) кристаллы ØПростые вещества: только бор и элементы IVA-группы ØКовалентные кристаллы с неполярной ковалентной связью: алмаз, кремний, германий, а-олово ØКовалентные кристаллы с полярной ковалентной связью: Si. C ( карбид кремния), некоторые галогениды ( Ag. I), фосфиды, арсениды, стибиды, некоторые нитриды. сульфиды, селениды, теллуриды и т. п. , т. е. соединения типа АIIIBV и AII BVI
 Основное условие образования бинарных соединений типа АIIIBV с тетраэдрической координацией атомов в кристаллической решетке заключается в следующем: Ø среднее число валентных электронов, приходящихся на один атом, должно быть равно четырем. для образования стабильной кристаллической решетки электронные пары четырех Ø δ-связей, образуемых каждым атомом, подвергаются, sp 3 - гибридизации, а образовавшиеся гибридные орбитали располагаются в пространстве в направлении углов тетраэдра.
Основное условие образования бинарных соединений типа АIIIBV с тетраэдрической координацией атомов в кристаллической решетке заключается в следующем: Ø среднее число валентных электронов, приходящихся на один атом, должно быть равно четырем. для образования стабильной кристаллической решетки электронные пары четырех Ø δ-связей, образуемых каждым атомом, подвергаются, sp 3 - гибридизации, а образовавшиеся гибридные орбитали располагаются в пространстве в направлении углов тетраэдра.
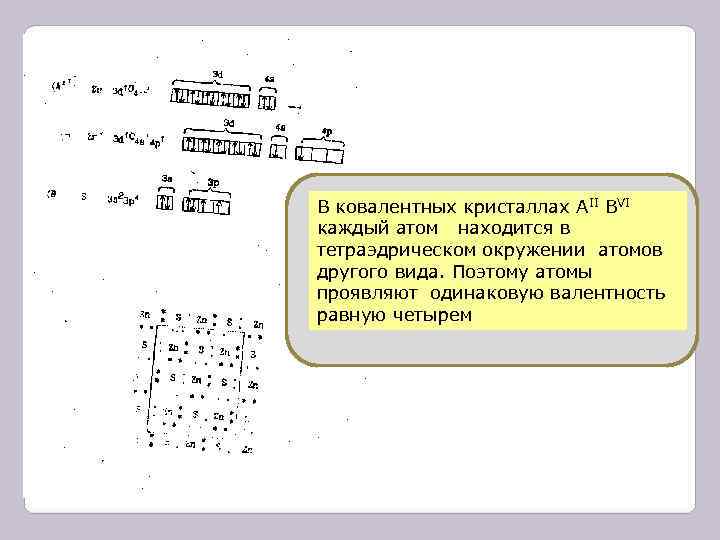
 В ковалентных кристаллах AII BVI каждый атом находится в тетраэдрическом окружении атомов другого вида. Поэтому атомы проявляют одинаковую валентность равную четырем
В ковалентных кристаллах AII BVI каждый атом находится в тетраэдрическом окружении атомов другого вида. Поэтому атомы проявляют одинаковую валентность равную четырем
 Координационные числа ковалентных кристаллов Координационное число определяются валентностью атомов элементов, из которых они построены. Как правило, координационное число (к. ч. ) можно рассчитать по формуле к. ч. = 8 — N, где N-номер группы, в которой находится элемент в периодической системе элементов Д. И. Менделеева. Например, для Si: координационное число равно 4 (8— 4 = 4), для Аs — 3 (8 — 5 — 3). для S — 2 (8 — 6=2). Таким образом, в ковалентных кристаллах принцип плотнейшей упаковки нарушается, и для них, характерны низкие координационные числа (4, 3, 2, ).
Координационные числа ковалентных кристаллов Координационное число определяются валентностью атомов элементов, из которых они построены. Как правило, координационное число (к. ч. ) можно рассчитать по формуле к. ч. = 8 — N, где N-номер группы, в которой находится элемент в периодической системе элементов Д. И. Менделеева. Например, для Si: координационное число равно 4 (8— 4 = 4), для Аs — 3 (8 — 5 — 3). для S — 2 (8 — 6=2). Таким образом, в ковалентных кристаллах принцип плотнейшей упаковки нарушается, и для них, характерны низкие координационные числа (4, 3, 2, ).
 Изоморфизм и полиморфизм Изоморфизм заключается в способности атомов, ионов или молекул замещать друга в кристаллических структурах. Закон изоморфизма бы сформулирован Э. Мичерлихом в 1821 г. таким образом: "Одинаковые количества атомов, соединенные одинаковым способом, дают одинаковые кристаллические формы; при этом кристаллическая форма не зависит от химической природы атомов, а определяется только их числом и относительным положением". Zn. S и Fe. S Это возможно лишь в том случае, если замещающие друга частицы мало различаются по размерам (не более 15%). Кроме того, изоморфные вещества должны иметь сходное пространственное расположение атомов или ионов и, значит, сходные по внешней форме кристаллы. Zn. S и Fe. S
Изоморфизм и полиморфизм Изоморфизм заключается в способности атомов, ионов или молекул замещать друга в кристаллических структурах. Закон изоморфизма бы сформулирован Э. Мичерлихом в 1821 г. таким образом: "Одинаковые количества атомов, соединенные одинаковым способом, дают одинаковые кристаллические формы; при этом кристаллическая форма не зависит от химической природы атомов, а определяется только их числом и относительным положением". Zn. S и Fe. S Это возможно лишь в том случае, если замещающие друга частицы мало различаются по размерам (не более 15%). Кроме того, изоморфные вещества должны иметь сходное пространственное расположение атомов или ионов и, значит, сходные по внешней форме кристаллы. Zn. S и Fe. S
 Изоморфное замещение определяет многие полезные свойства искусственных материалов современной техники - полупроводников, ферромагнетиков, лазерных материалов.
Изоморфное замещение определяет многие полезные свойства искусственных материалов современной техники - полупроводников, ферромагнетиков, лазерных материалов.
 Многие вещества могут образовывать кристаллические формы, имеющие различные структуру и свойства, но одинаковый состав (полиморфные модификации). Полиморфизм ( аллотропия) - способность твердых веществ и жидких кристаллов существовать в двух или нескольких формах с различной кристаллической структурой и свойствами при одном и том же химическом составе. О 2 и О 3 модификации углерода (алмаз, графит, карбины и фуллерены
Многие вещества могут образовывать кристаллические формы, имеющие различные структуру и свойства, но одинаковый состав (полиморфные модификации). Полиморфизм ( аллотропия) - способность твердых веществ и жидких кристаллов существовать в двух или нескольких формах с различной кристаллической структурой и свойствами при одном и том же химическом составе. О 2 и О 3 модификации углерода (алмаз, графит, карбины и фуллерены

