Кристаллические решетки.ppt
- Количество слайдов: 65

Твердые кристаллы • это трехмерные образования, характеризующиеся строгой повторяемостью одного и того же элемента структуры (элементарной ячейки) во всех направлениях. 1

Элементарная ячейка • представляет собой наименьший объем кристалла в виде параллелепипеда, повторяющегося в кристалле бесконечное число раз. 2

Геометрически правильная форма кристаллов • обусловлена, прежде всего, их строго закономерным внутренним строением. Если вместо атомов, ионов или молекул в кристалле изобразить точки как центры тяжести этих частиц, то получится трехмерное регулярное распределение таких точек, называемое кристаллической решеткой. Сами точки называют узлами кристаллической решетки. 3

Типы кристаллических решеток • Всего существует 14 типов кристаллических решеток. (куба, призмы, октаэдра). 4

4 класса кристаллических решеток • В зависимости от характера частиц, образующих кристалл, и от типа ХС связи между ними различают 4 класса кристаллических решеток: металлические, ионные, молекулярные и макромолекулярные (атомные). 5

кристаллические вещества • По типу химической связи кристаллические вещества делятся на металлические, ионные, ковалентные и молекулярные. Кристаллы этих классов могут иметь любой из приведенных типов кристаллических решеток. 6

Металлические структуры • Атомы в металлах упакованы максимально плотно и образуют простейшие кристаллические структуры, при этом атомы упрощенно рассматривают в виде шаров. Упаковать, уложить шары так, чтобы они заполнили все пространство (чтобы между ними не было промежутков) невозможно. 7

Плотноупакованные структуры • Если же эти промежутки сведены к минимуму, говорят о плотноупакованных структурах 8
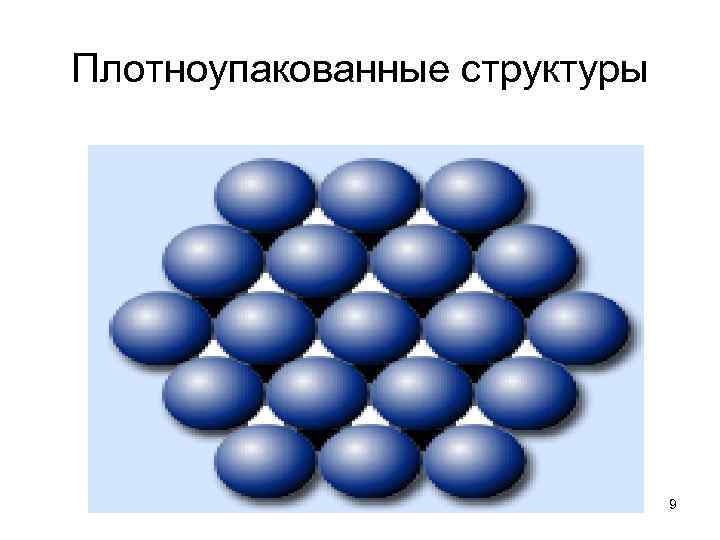
Плотноупакованные структуры 9

плотнейшие упаковки шаров • ПРИ ТАКОЙ УПАКОВКЕ соответственно получается две плотнейшие упаковки шаров в кристаллах • Если шары 3 слоя чередуются как АВАВАВ (шары 3 слоя заполняют лунки и точно повторяют 1 слой – гексагональная плотнейшая упаковка (ГПУ) 10

Гексагональная плотнейшая шаровая упаковка 11

гексагональная упаковка • В гексагональной упаковке шаров третий слой точно повторяет первый, и упаковка оказывается двухслойной 12

Гексагональная упаковка • Число ближайших соседей 12, коэффициент заполнения пространства такой же, как в кубической упаковке – 74, 05 %. Такая упаковка характерна для магния, бериллия, кадмия, стронция и др. 13

Кубическая плотнейшая шаровая упаковка • В кубической упаковке шаров шары третьего слоя находятся над пустотами первого, вся упаковка трехслойная, повторение мотива наступает в четвертом слое 14

Кубическая плотнейшая шаровая упаковка • Каждый шар имеет 12 соседей (4 шара в том же слое, 4 сверху и 4 снизу). Коэффициент заполнения пространства достигает максимальной величины ¾ – 74, 05 %. Симметрия этой укладки кубическая, Такую структуру имеют медь, золото, алюминий, свинец и др. 15

ГПУ и КПУ • – самые плотные упаковки – шары занимают ¾ всего объема. Координационное число в них равно 12 16

кубическая объемноцентрированная структура • Помимо ГПУ и КПУ для многих металлов характерна кубическая объемноцентри • рованная структура 17

Кубическая объемоцентрированная упаковка 18

Кубическая объемоцентрированная упаковка • получается при последовательной укладке слоев с квадратной упаковкой слоев. Эта структура не является плотноупакованной. Шары занимают в ней только 68 % имеющегося объема 19

Кубическая объемоцентрированная упаковка • Каждый шар находится в центре куба, вершины которого заняты другими шарами. Таким образом, координационное число равно 8. Так построены железо, вольфрам, молибден и др. 20

Объемноцентрированная кубическая упаковка (ОЦКУ) • Объемноцентрированная кубическая упаковка (ОЦКУ) в отличие от первых двух не является плотноупакованной 21

Пустоты в плотнейших шаровых упаковках • Свободное пространство между шарами в плотнейших упаковках соответствует пустотам двух родов. Одни окружены 4 шарами и имеют координационное число – 4, другие располагаются между 6 шарами и имеют координационное число – 6. 22
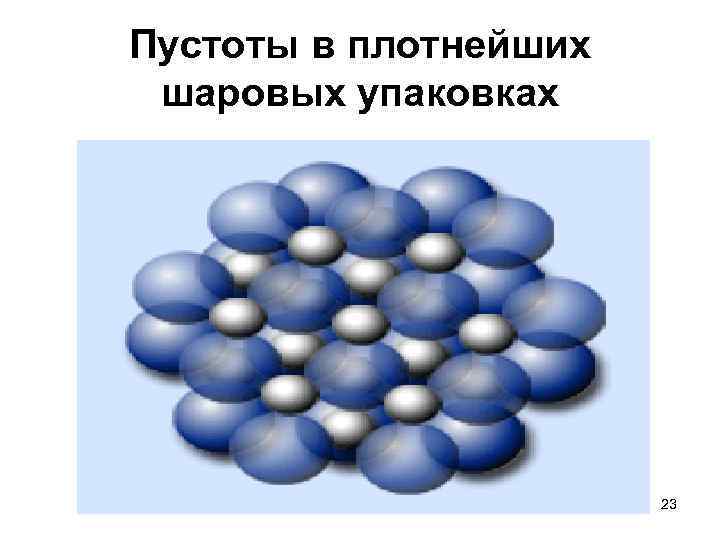
Пустоты в плотнейших шаровых упаковках 23

Тетраэдрические пустоты • Центры 4 шаров, между которыми образуется пустота первого рода, располагаются по вершинам тетраэдра, поэтому пустоты с координационным числом 4 называются тетраэдрическими. 24

Тетраэдрические пустоты 25

Октаэдрические пустоты • Центры 6 шаров, замыкающих пустоту второго рода, расположены по вершинам октаэдра и называются октаэдрическими. • На каждый шар приходится 2 тетраэдрические и 1 октаэдрическая пустоты. 26
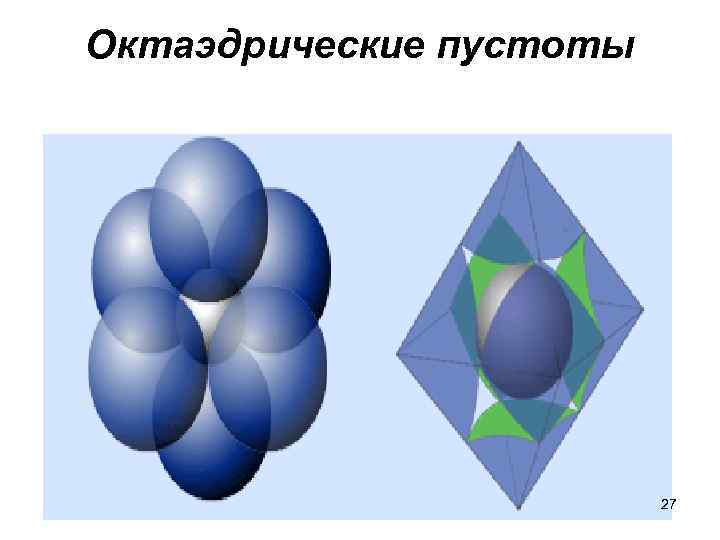
Октаэдрические пустоты 27

Ионные кристаллы • Ионы, из которых состоят ионные кристаллы, удерживаются вместе силами электростатического взаимодействия 28

Нейтральность ионных кристаллов • Поэтому структура кристаллической решетки ионных кристаллов должна обеспечивать их нейтральность 29

Структурные типы • Наиболее распространенные структуры ионных кристаллов с позиций шаровых упаковок. В этом случае принято, что большие ионы образуют плотнейшую упаковку, а мелкие занимают пустоты в ней. • Na. Cl, Cs. Cl, Ca. F 2, Zn. S, Ca. Ti. O 3 (перовскит) • Структурные типы • хлорида натрия, хлорида цезия, • Флюорита, сфалерита, перовскита 30
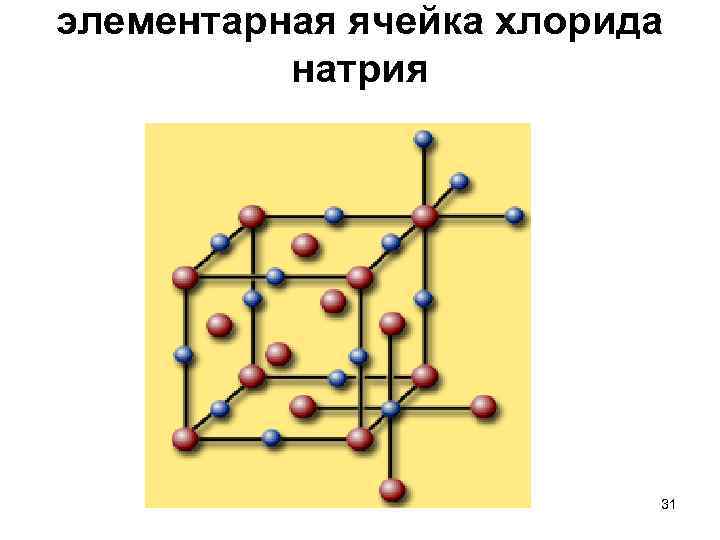
элементарная ячейка хлорида натрия 31

ХЛОРИД НАТРИЯ • Представлена (красные – ионы хлора Cl-; синие – ионы натрия Na+) • В вершинах находятся атомы хлора, а атомы натрия занимают все октаэдрические пустоты. 32

Кубическая гранецентрированная элементарная ячейка (хлорид натрия) • Ближайшее окружение атомов хлора составляют 6 атомов натрия и для атомов натрия – 6 атомов хлора. Катионы и анионы в этой структуре имеют октаэдрическое окружение с координацией 6 : 6. 33

Структурный тип – Cs. Cl кубическая примитивная ячейка • Каждый ион цезия окружен восьмью ионами хлора, его координационное число равно 8. Аналогично координационное число хлора также равно 8. Структуру можно представить двумя взаимопроникающими кубическими решетками – катионной и анионной 34
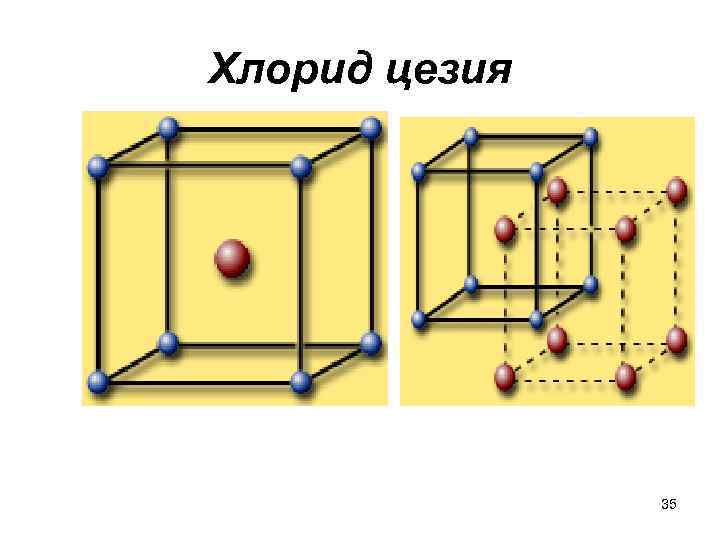
Хлорид цезия 35

Структурный тип-кубическая примитивная ячейка • Катионы и анионы в этой структуре имеют кубическое окружение с координацией 8 : 8. В этом структурном типе кристаллизуются бромид цезия, йодид цезия, хлорид аммония, хлорид таллия и др. 36
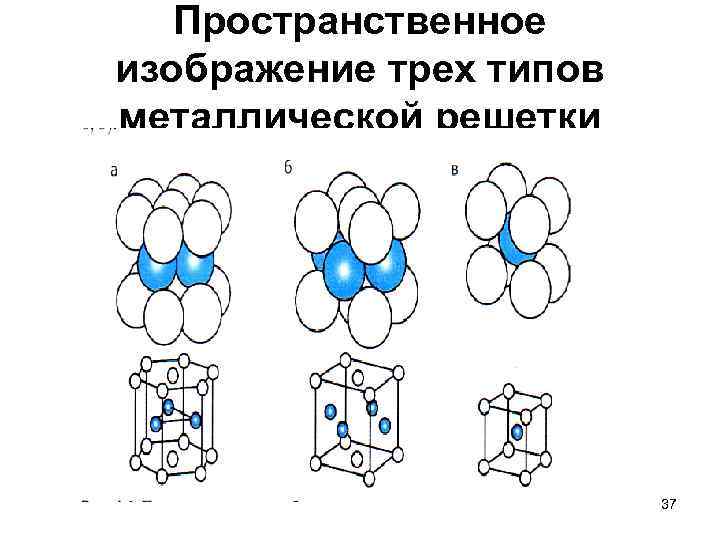
Пространственное изображение трех типов металлической решетки 37

ОТВЕТ • А) ГПУ Гексональная плотная упаковка • Б) ГКУ гранецентрированная кубическая упаковка • В) ОЦКУ объемоцентрированная кубическая решетка 38

Сфалерит • Структурный тип сфалерита (Zn. S) имеет гранецентрированную кубическую решетку. • (красные – ионы серы S 2 - ; синие – ионы цинка Zn 2+) 39
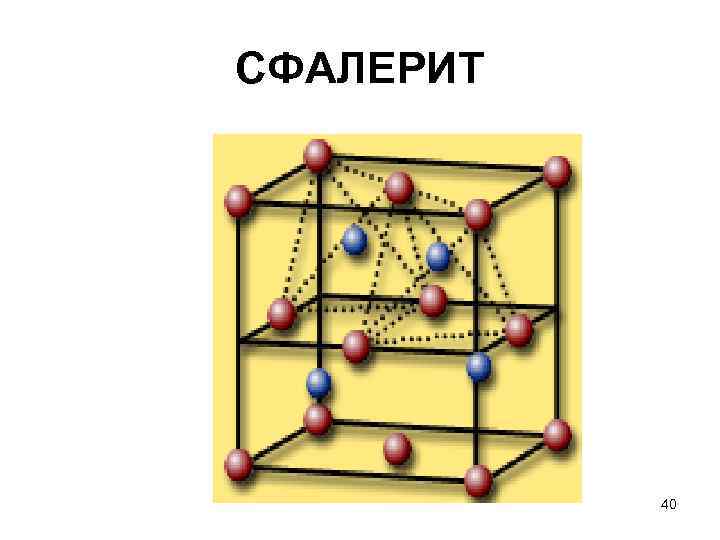
СФАЛЕРИТ 40

СФАЛЕРИТ • Её можно рассматривать таким образом, что катионы образуют кубическую структуру, а анионы имеют тетраэдрическую структуру внутри куба • ИЛИ если рассматривать анионы как кубическую структуру, то катионы имеют в ней тетраэдрическое расположение. Катионы и анионы в этой структуре имеют тетраэдрическое окружение с координацией 4 : 4. 41

СФАЛЕРИТ • В этом структурном типе кристаллизуются фторид меди (I), селенид кадмия, сульфид бериллия, фосфид галлия, сульфид ртути (II) и др. 42

Флюорит • Структура флюорита (Ca. F 2) отличается от рассмотренных тем, что она имеет состав АВ 2 и два различных координационных числа: для кальция – 8, для фтора – 4. • (красные – ионы фтора F-; синие – ионы кальция Сa 2+) 43

флюорит • Если число катионов вдвое меньше числа анионов, то реализуется структура флюорита 44
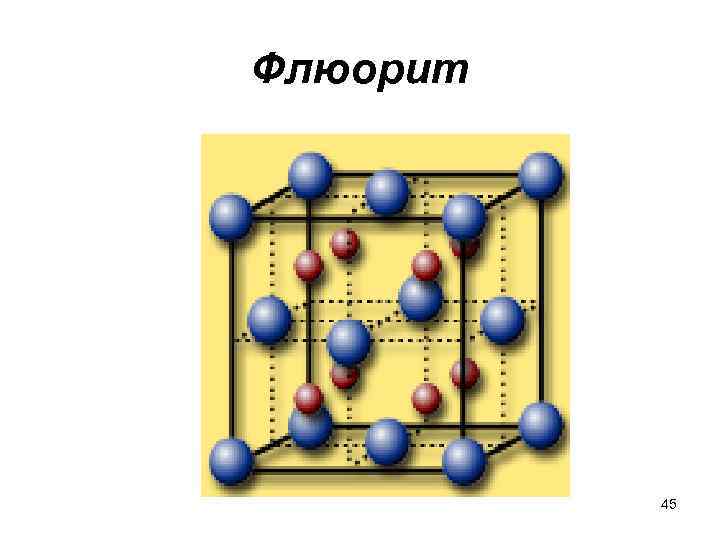
Флюорит 45

кубическая гранецентрированная решетка • Структуру флюорита можно представить как кубическую гранецентрированную катионную решетку, внутри которой имеется тетраэдрическое расположение анионов. Координация катионов и анионов 8 : 4. В этом структурном типе кристаллизуются фторид бария, фторид ртути (II), оксид урана (IV), оксид циркония (VI) и др. 46

Шпинель • Наиболее сложная структура типа шпинели Mg. Al 2 O 4. • (красные – ионы кислорода О 2 -; синие – ионы алюминия Al 3+; желтые – ионы магния Mg 2+) 47
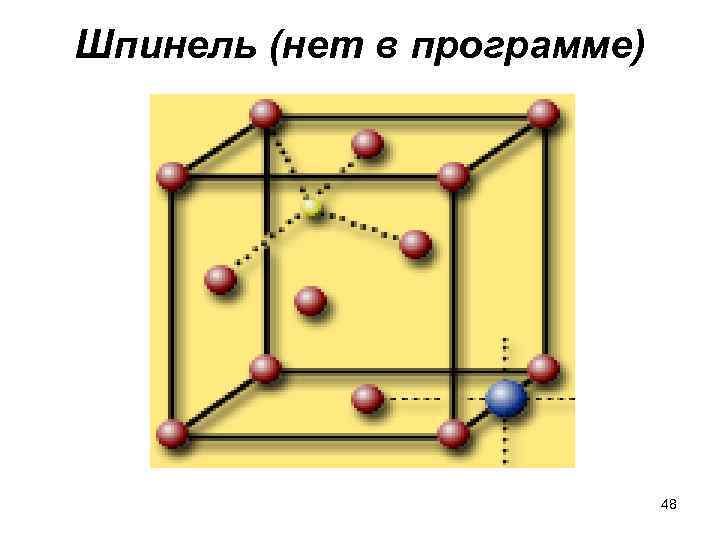
Шпинель (нет в программе) 48

Пояснения • О – в узлах, • Аl – внизу, Mg - вверху 49

Она может быть представлена • как кубическая плотнейшая упаковка из атомов кислорода, в которой половина октаэдрических пустот занята ионами алюминия, а четверть тетраэдрических пустот – ионами магния. Координационное число магния – 4, алюминия – 6, кислорода – 4. В этом структурном типе кристаллизуются хромат железа, феррат никеля и др. 50

Молекулярные кристаллы • Молекулярные кристаллы состоят из молекул, которые удерживаются в определенных положениях кристаллической решетки слабыми межмолекулярными взаимодействиями – силами Ван-дер -ваальса и водородными связями 51

Например, • лед состоит из молекул воды, удерживаемых в кристаллической решетке водородными связями. Лед имеет тетраэдрическую структуру, напоминающую структуру алмаза, но, конечно же, принципиально другую. 52

Молекулярные кристаллы • Большинство неметаллов в виде простых веществ (например, йод I 2, аргон Ar, сера S 8) и соединений друг с другом (например, вода, диоксид углерода, хлороводород), а также практически все твердые органические вещества образуют молекулярные кристаллы. 53

гранецентрированная кубическая решетка • Кристалл йода. Он имеет гранецентрированную кубическую решетку. Узлы его структуры заняты молекулами йода 54
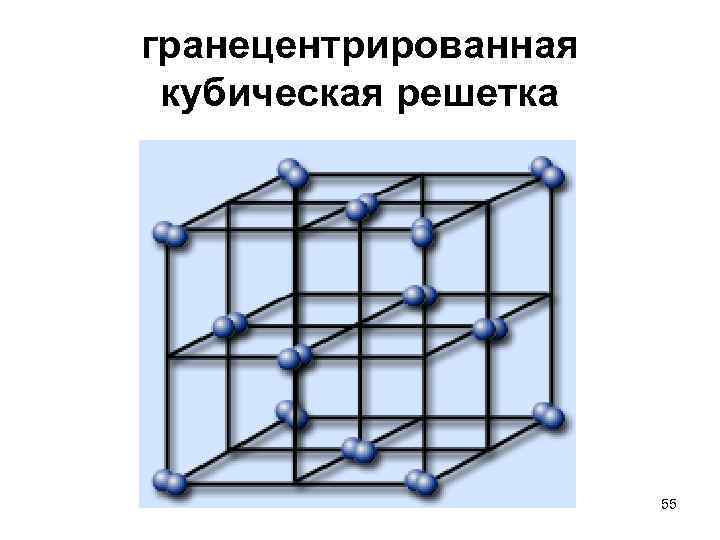
гранецентрированная кубическая решетка 55

кристалл йода • Показано, что и в кристалле сохраняются двухатомные молекулы. • Узлы кристаллической решетки кристаллов йода заняты двухатомными молекулами йода. Хлор и бром образуют подобные структуры при более низких температурах. 56

Подобную структуру • имеют твердый углекислый газ, кислород, азот, многие органические вещества. 57

Ковалентные кристаллы • Эти кристаллы также называют координационными. В отличие от ионных и металлических кристаллов, которые состоят из ионов, и молекулярных, образованных молекулами, ковалентные кристаллы состоят из атомов. Их можно разделить на три типа: цепочечные, слоистые и каркасные структуры. 58

Цепочечные кристаллы • состоят из полимерных цепочек одномерных макромолекул. Примером таких кристаллов является асбест, многие органические вещества. 59

Слоистые структуры • можно рассматривать как двухмерные макромолекулы. Классический пример – графит. Каждый его слой состоит из атомов углерода ковалентно связанных между собой в правильные шестиугольники. Соседние слои удерживаются силами Ван-дер. Ваальса. 60

Графит • Классическим примером является графит – другая аллотропная форма углерода. Образуется плоская сетка из шестиугольников. Плоскости в графите соединяются только Ван-дер. Ваальсовыми силами, их легко заставить скользить относительно друга, если приложить усилие. Этим объясняются пишущее свойство графита. 61

ГРАФИТ 62

Каркасные структуры • представляют собой трехмерные макромолекулы. Например, в структуре алмаза каждый атом углерода ковалентно связан с четырьмя другими атомами, образуя тетраэдрическую структуру. 63

полиморфизм • Твердые вещества могут существовать в различных кристаллических формах. Это явление называется полиморфизмом. Примером такого соединения является оксид кремния (IV). 64

Цепочечные структуры • Некоторые вещества образуют структуры, похожие на цепочки. (оксид серы IV). 65
Кристаллические решетки.ppt