95c9488064ae36892fdc9a3666a926e4.ppt
- Количество слайдов: 27

TÜV SÜD Product Service Gmb. H Medical and Health Services Safely and successfully on the health market. TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 1

Arzneimittel/Medizinprodukt-Kombinationen: Die Anforderungen einer heterogenen Produktgruppe an die klinische Bewertung durch die Benannte Stelle TÜV SÜD Product Service Gmb. H • TÜV SÜD Gruppe

Inhalt • • Definitionen Relevante Verordnungen und Richtlinien Das Standardverfahren Neue Kombinationsprodukte TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 3

Definitionen • Medizinprodukt RL 93/42/EWG, RL 2007/47/EG Zertifizierung durch Benannte Stelle Nicht anwendbar für humane Zellen / Gewebe • Arzneimittel RL 2001/83/EG Zulassung durch die nationalen Behörden oder durch die European Agency for the Evaluation of Medicinal Products (EMEA) Anwendbar für humane Zelltherapie-Produkte TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 4

Zulassungsverfahren New EU Framework Richtlinie 93/42/EWG Medizinprodukt TÜV SÜD Product Service Gmb. H Verordnung für Advanced Therapies ATMP Tissue Engineering Zell- und Gentherapie Richtlinie 2001/83/EG Arzneimittel Prof. Dr. Sabine Kloth 3/16/2018 5
Definitionen ATMP • Gentherapeutika • Somatische Zelltherapeutika • Tissue engineering Produkte TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 6
Produktbeispiele • Hautersatz • Matrix-gebundene Chondrocyten oder Osteocyten • Gekapselte Zellpräparationen • Stammzellen / Hüftimplantat • Stammzellen / Stent • Leberunterstützungssystem TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 7

Kombinationsprodukte Medizinprodukt Arzneimittel Medizinprodukt Blutprodukt Medizinprodukt Gentherapeutikum Medizinprodukt Humane Zellen / Gewebe TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 8

Zulassung von Kombinationsprodukten Das anzuwendende Verfahren ist abhängig vom • Bestimmungsgemäßen Gebrauch • Der Form der Kombination • Der Hauptwirkung im Hinblick auf die Komponenten Ausnahme: ATMP TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 9
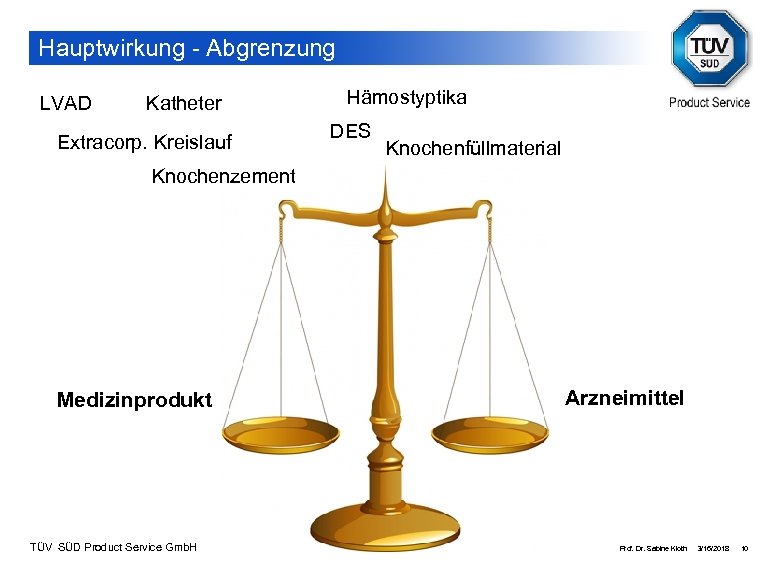
Hauptwirkung - Abgrenzung LVAD Katheter Extracorp. Kreislauf Hämostyptika DES Knochenfüllmaterial Knochenzement Medizinprodukt TÜV SÜD Product Service Gmb. H Arzneimittel Prof. Dr. Sabine Kloth 3/16/2018 10

Konsultationsverfahren gem. RL 93/42/EWG Vorbedingungen: 1. Der vom Hersteller definierte bestimmungsgemäße Gebrauch ist der eines Medizinproduktes. 2. Die Arzneimittelkomponente bildet einen integralen Bestandteil des Produktes. 3. Die Hauptwirkung wird durch das Medizinprodukt vermittelt. TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 11
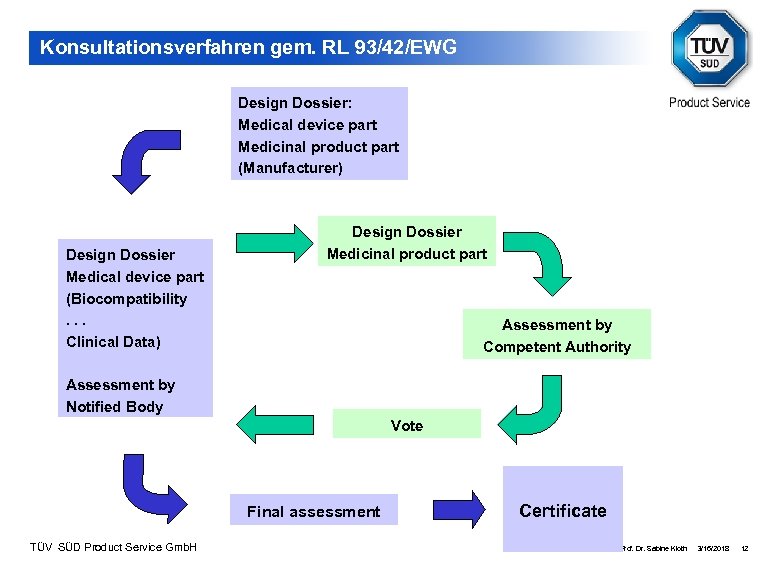
Konsultationsverfahren gem. RL 93/42/EWG Design Dossier: Medical device part Medicinal product part (Manufacturer) Design Dossier Medical device part (Biocompatibility. . . Clinical Data) Design Dossier Medicinal product part Assessment by Competent Authority Assessment by Notified Body Vote Final assessment TÜV SÜD Product Service Gmb. H Certificate Prof. Dr. Sabine Kloth 3/16/2018 12
Bewertung klinischer Daten – MDD, Anhang X • Bewertung der merkmals- und leistungsrelevanten Anforderungen des Produktes bei normalen Einsatzbedingungen auf der Grundlage klinischer Daten • Beurteilung unerwünschter Nebenwirkungen • Annehmbarkeit des Nutzen-/Risiko. Verhältnisses TÜV SÜD Product Service Gmb. H Abteilung: 3/16/2018 13

Quellen klinischer Daten – MDD, Anhang X • • • Bewertung veröffentlichter und/oder unveröffentlichter Berichte über sonstige klinische Erfahrungen mit dem betreffenden Produkt oder Bewertung der klinischen Prüfung/en des betreffenden Produkts oder Bewertung der klinischen Prüfung/en oder sonstigen in der wissenschaftlichen Fachliteratur wiedergegebene Studien über ein ähnliches Produkt, dessen Gleichartigkeit mit dem betreffenden Produkt nachgewiesen werden kann TÜV SÜD Product Service Gmb. H Abteilung: 3/16/2018 14
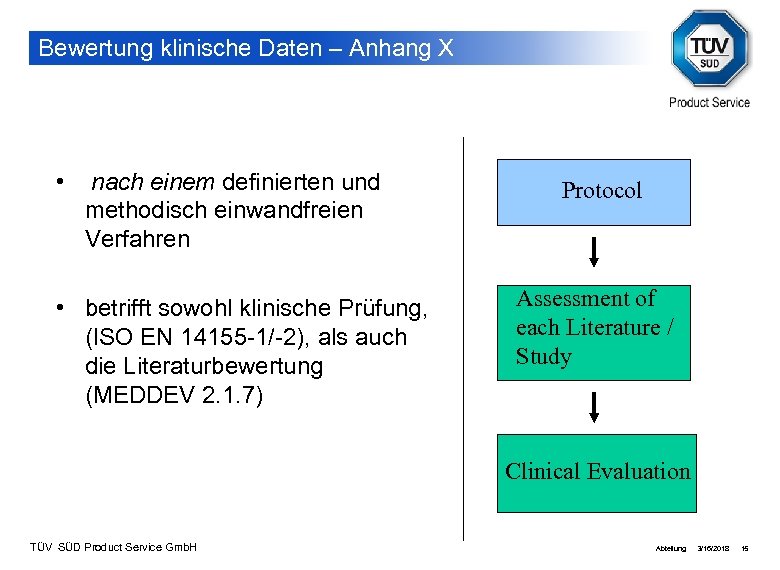
Bewertung klinische Daten – Anhang X • nach einem definierten und methodisch einwandfreien Verfahren • betrifft sowohl klinische Prüfung, (ISO EN 14155 -1/-2), als auch die Literaturbewertung (MEDDEV 2. 1. 7) Protocol Assessment of each Literature / Study Clinical Evaluation TÜV SÜD Product Service Gmb. H Abteilung: 3/16/2018 15

Änderungen gem. der revidierten Fassung der MDD • Die Benannte Stelle erstellt einen Bericht zur Qualität, Sicherheit und Nützlichkeit des Produktes für die Prüfung durch die Behörde. • Die Behörde erstellt ein Gutachten zur Qualität und Sicherheit der Arzneimittelkomponente. • Kombinationsprodukte, die ein aktives implantierbares Medizinprodukt enthalten sind zu konsultieren. • Zeitrahmen für die Bewertung durch die Behörde: 210 Tage TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 16

Konsultation – Kombinationsprodukte, MDD Anhang I • Die Benannte Stelle ersucht die Behörde um ein wissenschaftliches Gutachten zur Qualität und Sicherheit der Arzneimittelkomponente. Die Behörde berücksichtigt das klinische Risiko/Nutzen. Profil der Verwendung des Arzneimittels in dem Produkt. • Bei der Erstellung des Gutachtens berücksichtigt die Behörde den Herstellungsprozess und die Angaben im Zusammenhang mit dem Nutzen der Verwendung des Stoffes in dem Produkt, wie von der Benannten Stelle ermittelt. Gilt auch für AIMD ! TÜV SÜD Product Service Gmb. H Abteilung: 3/16/2018 17
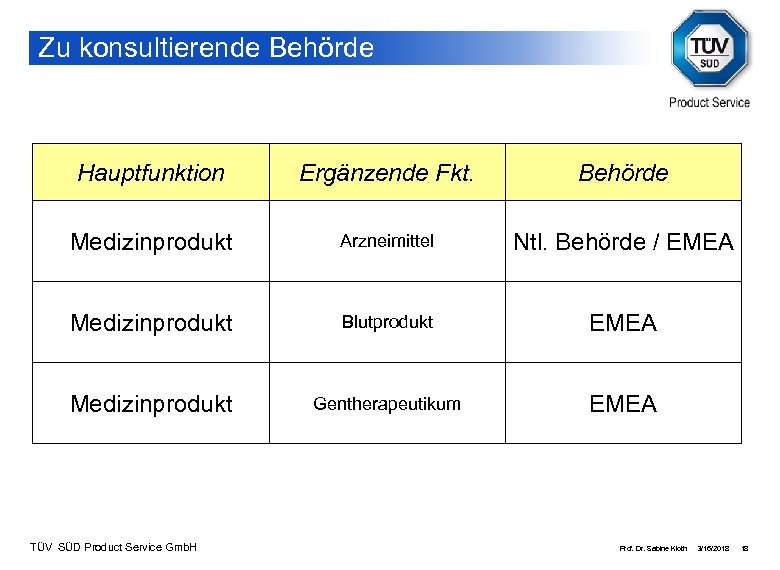
Zu konsultierende Behörde Hauptfunktion Ergänzende Fkt. Behörde Medizinprodukt Arzneimittel Ntl. Behörde / EMEA Medizinprodukt Blutprodukt EMEA Medizinprodukt Gentherapeutikum EMEA TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 18
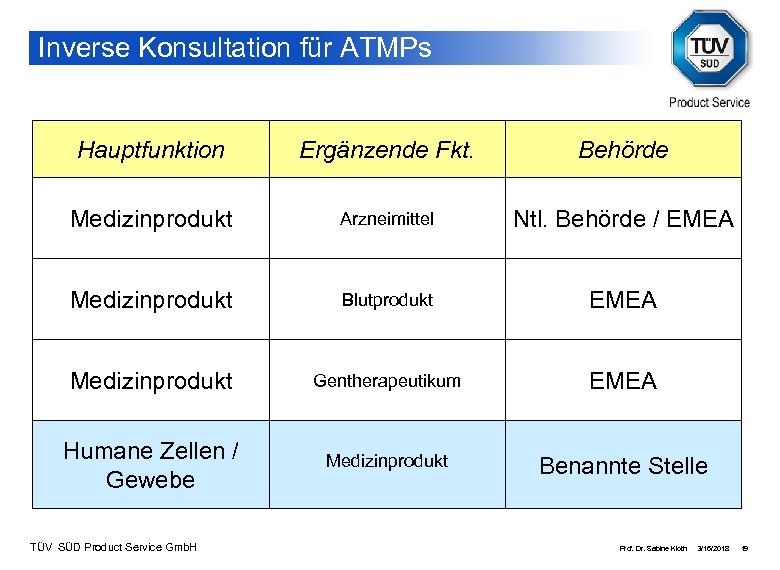
Inverse Konsultation für ATMPs Hauptfunktion Ergänzende Fkt. Behörde Medizinprodukt Arzneimittel Ntl. Behörde / EMEA Medizinprodukt Blutprodukt EMEA Medizinprodukt Gentherapeutikum EMEA Humane Zellen / Gewebe Medizinprodukt Benannte Stelle TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 19

ATMP, Artikel 2 Kombinationsprodukt • Ein Medizinprodukt gem. Artikel 1(2)(a) der RL 93/42/EWG oder • Ein aktives, implantierbares Medizinprodukt gem. Artikel 1(2)(c) der RL 90/385/EWG, bilden einen integralen Bestandteil und • Es enthält viable Zellen / Gewebe; oder • Es enthält non-viable Zellen / Gewebe von denen die Hauptwirkung des Produktes ausgeht. TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 20

Zu beachten: Enthält ein Produkt lebende Zellen oder Gewebe, so wird diesem Produktbestandteil grundsätzlich die Hauptwirkung zugesprochen. TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 21

ATMP, Artikel 9 – Zulassungsverfahren EMEA Committee for Medicinal Products for Human Use (CHMP) Committee for Advanced Therapy (CAT) TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 22

ATMP Verordnung: Art. 10 Zulassung Kombinationsprodukte • Das finale Produkt ist durch die EMEA zu bewerten. • Der Zulassungsantrag eines Kombinationsproduktes muss Evidenz für die Konformität mit den Grundlegenden Anforderungen der MDD enthalten. TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 23

Artikel 6 Kombinationprodukte 1. Ein Medizinprodukt, das Bestandteil eines Kombinationsproduktes ist muss die Grundlegenden Anforderungen der MDD erfüllen (Annex I, RL 93/42/EWG). 2. Ein aktives, implantierbares Medizinprodukt, das Bestandteil eines Kombinationsproduktes ist muss die Grundlegenden Anforderungen der RL erfüllen (Annex I, RL 90/385/EWG). TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 24

Konformitätsbewertungsverfahren Drei unterschiedliche Startpunkt sind denkbar: Der Medizinprodukt-Bestandteil wurde durch eine Benannte Stelle bewertet. wurde nicht durch eine Benannte Stelle bewertet. CAT hält eine Bewertung für unnötig. TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 25

Einige offene Punkte • Die ATMP-Verordnung enthält keine Definitionen für Gentherapeutika und somatische Zelltherapie. • Die Hauptwirkung für Tissue Engineering Produkte folgt einer Legaldefinition. • Bislang liegt kein Leitfaden für das inverse Konsultationsverfahren vor. • Grauzone: non-viable humane Materialien. TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 26
Links: EU Internet page: http: //www. europa. eu. int Contact: sabine. kloth@tuev-sued. de TÜV SÜD Product Service Gmb. H Prof. Dr. Sabine Kloth 3/16/2018 27
95c9488064ae36892fdc9a3666a926e4.ppt