Занятие 32. ВИЧ-инфекция.ppt
- Количество слайдов: 114

Тульский государственный университет ВИЧ-ИНФЕКЦИЯ Медицинский институт Лечебный факультет

ВИЧ-инфекция – длительно текущая инфекционная болезнь, развивающаяся в результате инфицирования вирусом иммунодефицита человека. При ВИЧ-инфекции прогрессирует поражение иммунной системы, приводящее к состоянию, известному под названием «синдром приобретенного иммунного дефицита» (СПИД), при котором у больного развиваются «оппортунистические заболевания» : тяжелые формы инфекций, вызванных условнопатогенными возбудителями и онкологические заболевания.
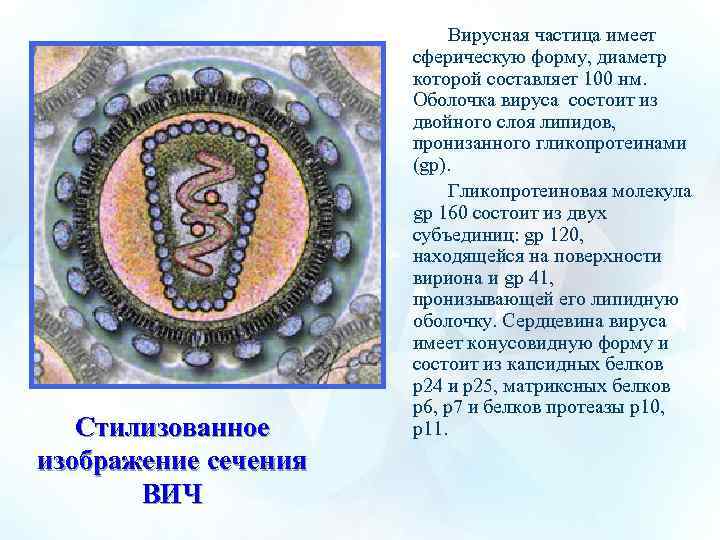
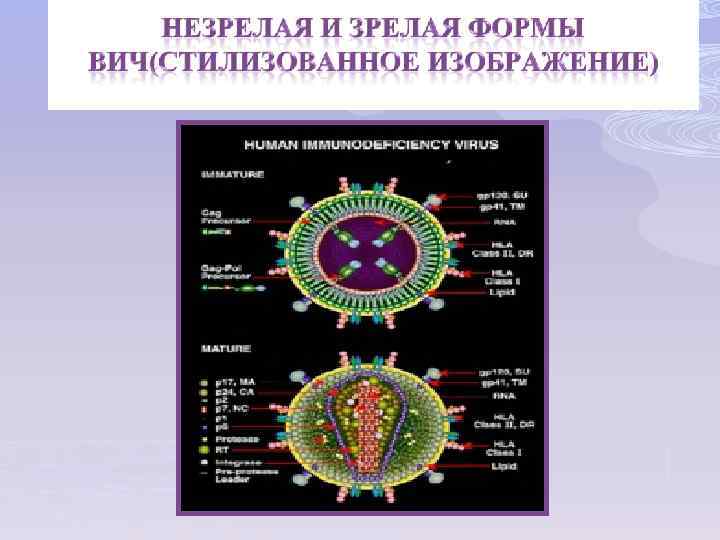
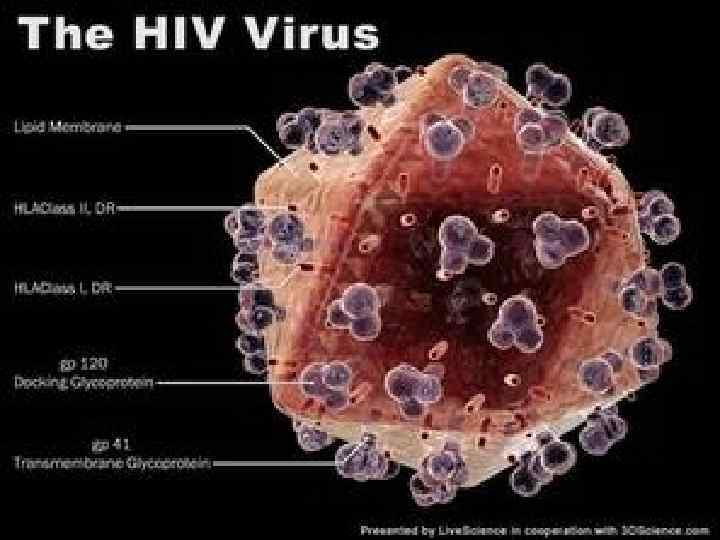
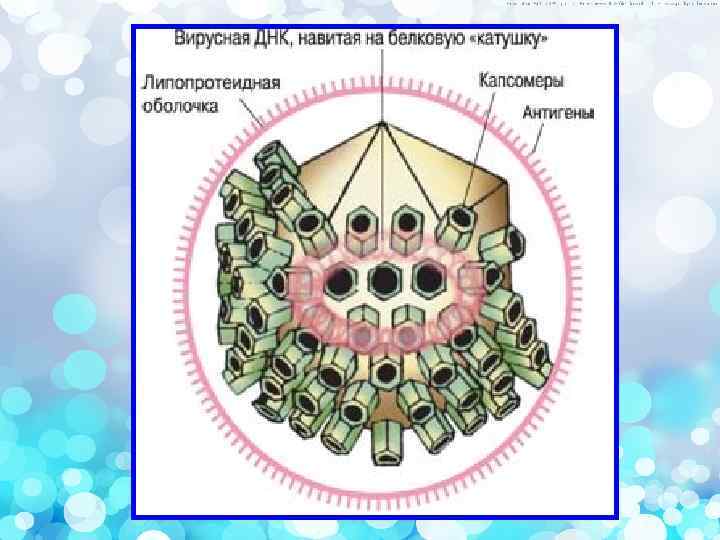
Стилизованное изображение сечения ВИЧ Вирусная частица имеет сферическую форму, диаметр которой составляет 100 нм. Оболочка вируса состоит из двойного слоя липидов, пронизанного гликопротеинами (gp). Гликопротеиновая молекула gp 160 состоит из двух субъединиц: gp 120, находящейся на поверхности вириона и gp 41, пронизывающей его липидную оболочку. Сердцевина вируса имеет конусовидную форму и состоит из капсидных белков р24 и р25, матриксных белков р6, р7 и белков протеазы р10, р11.
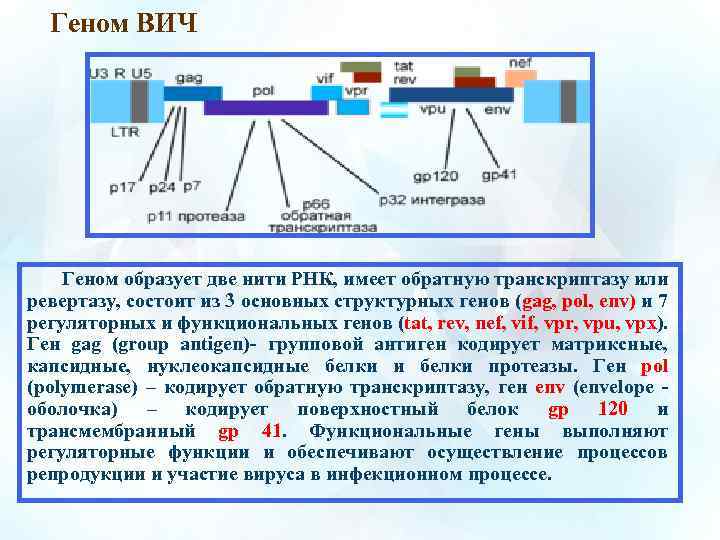
Геном ВИЧ Геном образует две нити РНК, имеет обратную транскриптазу или ревертазу, состоит из 3 основных структурных генов (gag, pol, env) и 7 регуляторных и функциональных генов (tat, rev, nef, vif, vpr, vpu, vpx). Ген gag (group antigen)- групповой антиген кодирует матриксные, капсидные, нуклеокапсидные белки и белки протеазы. Ген pol (polymerase) – кодирует обратную транскриптазу, ген env (envelope оболочка) – кодирует поверхностный белок gp 120 и трансмембранный gp 41. Функциональные гены выполняют регуляторные функции и обеспечивают осуществление процессов репродукции и участие вируса в инфекционном процессе.

Выделяют два типа вируса, отличающихся, структурой генома и серологическими характеристиками: ВИЧ-1 и ВИЧ-2. В частности, геном ВИЧ-2 отличается от генома ВИЧ-1 структурой гена env и заменой гена vpu на vpx. Так, ВИЧ-2 вместо белков gp 120, gp 41, gp 160, gp 24 содержит белки gp 140, gp 105, gp 36. Это обусловливает различия в течении заболеваний, вызываемых инфекциями ВИЧ-1 и ВИЧ-2.

ВИЧ-2 – вид вируса иммунодефицита ВИЧ-2 человека, идентифицированный в 1986 году. По сравнению с ВИЧ-1, ВИЧ-2 изучен в значительно меньшей степени. Известно, что ВИЧ-2 менее патогенен и передается с меньшей вероятностью, чем ВИЧ 1 Отмечено, что люди, инфицированные. ВИЧ-2 обладают слабым иммунитетом к ВИЧ-1. Глобальная эпидемия ВИЧ-инфекции главным образом обусловлена распространением ВИЧ-1, ВИЧ-2 распространен преимущественно в Западной Африке. В подавляющем большинстве случаев, если не оговорено иначе, под ВИЧ подразумевается ВИЧ-1.
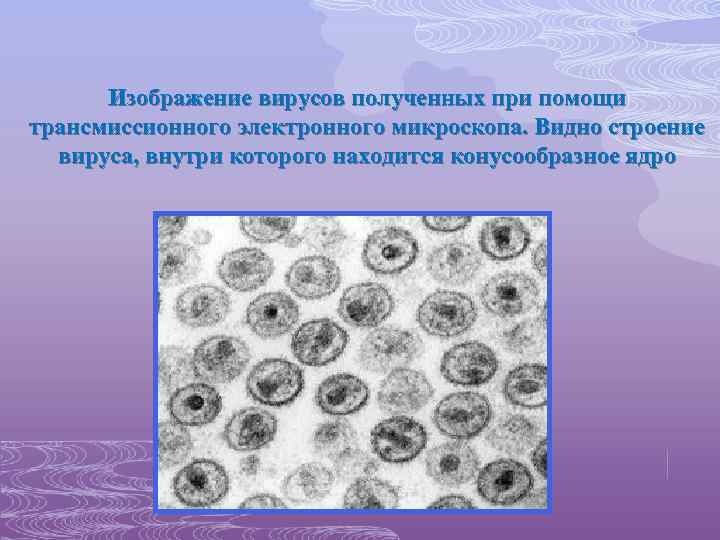
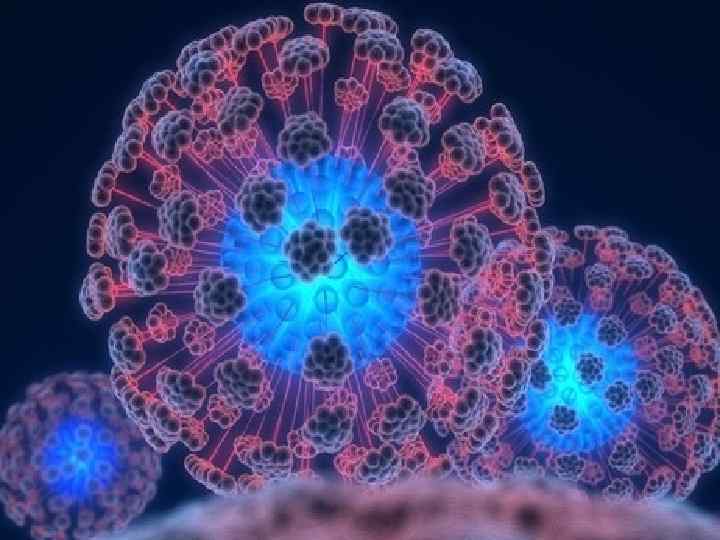
Изображение вирусов полученных при помощи трансмиссионного электронного микроскопа. Видно строение вируса, внутри которого находится конусообразное ядро
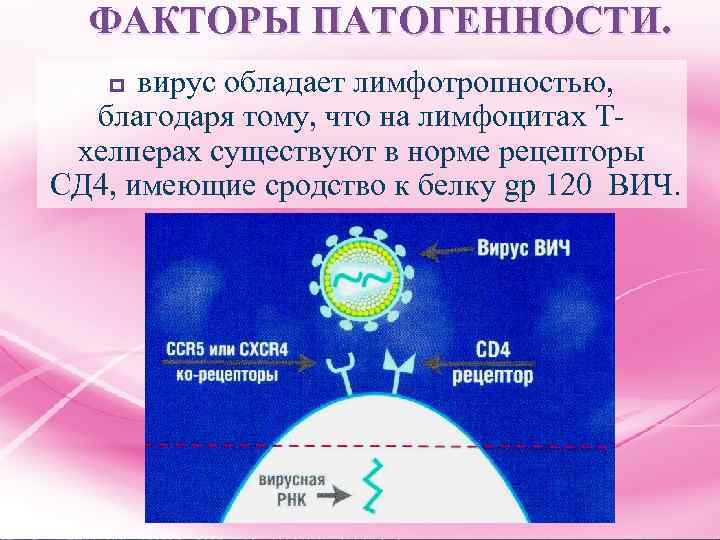
ФАКТОРЫ ПАТОГЕННОСТИ. вирус обладает лимфотропностью, благодаря тому, что на лимфоцитах Тхелперах существуют в норме рецепторы СД 4, имеющие сродство к белку gp 120 ВИЧ. p
поражает не только Т-хелперы, но и Влимфоциты, лейкоциты, клетки Лангерганса, макрофаги и др. p

p снижается число Т-4 -лимфоцитов, а также соотношение Т-4/ Т-8.

Источниками вируса являются больные и вирусоносители. Пути передачи вируса: 1) при половом контакте; 2) парентеральное заражение кровью при гемотрансфузиях, медицинских манипуляциях, операциях; 3) передача новорожденным через плаценту, в родовых путях, при грудном вскармливании. Возможно заражение в парикмахерских, при пользовании зубными щетками, нанесении татуировок.



ВИЧ присутствует у больного человека во всех клетках, где есть СД-4 рецепторы – это Тхелперы, тканевые макрофаги, в клетках кишечника, слизистых и т. д. У инфицированного человека вирус выделяется со всеми биологическими жидкостями: максимальное его количество находится в крови и в семенной жидкости. Среднее количество вируса – в лимфе, ликворе, отделяемом влагалища. Еще меньше вируса в слюне, слезах, поте. Содержание вируса в них таково, что этого недостаточно, чтобы вызвать инфекцию.

Группы повышенного риска: p p p наркоманы, употребляющие инъекционные наркотики, использующие общую посуду для приготовления наркотика (распространение вируса через иглу шприца и общую посуду для растворов наркотиков); а также х половые партнёры. мужчины — гомосексуалы и бисексуалы, практикующие незащищённый анальный секс; гетеросексуалы обоего пола, практикующие незащищённый анальный секс; лица, которым сделали переливание непроверенной донорской крови; больные венерическими заболеваниями; проститутки.

Несколько лет назад был описан генотип человека, устойчивый к ВИЧ. Проникновение вируса в иммунную клетку связано с его взаимодействием с поверхностным рецептором: белком CCR 5. Но делеция (утеря участка гена) CCR 5 -дельта 32 приводит к невосприимчивости её носителя к ВИЧ. Предполагается, что эта мутация возникла примерно две с половиной тысячи лет назад и со временем распространилась в Европе. Сейчас к ВИЧ "виртуально устойчив" в среднем 1% европейцев, 10 -15% европейцев имеют частичную сопротивляемость к ВИЧ.

Учёные Ливерпульского университета объясняют такую неравномерность тем, что мутация CCR 5 увеличивает сопротивляемость к бубонной чуме. Поэтому после эпидемий «чёрной смерти» 1347 года (а в Скандинавии ещё и 1711 года) доля этого генотипа выросла. Существует небольшой процент людей (около 10% всех ВИЧ-положительных), в крови которых присутствует вирус, однако СПИД у них не развивается в течение долгого времени (т. н. нон-прогрессоры). Обнаружено, что одним из главных элементов антивирусной защиты человека и других приматов является белок TRIM 5 a, способный распознавать капсид вирусных частиц и препятствовать размножению вируса в клетке. Данный белок у человека и других приматов имеет различия, которые обуславливают врожденную устойчивость шимпанзе к ВИЧ и родственным ему вирусам, а у человека - врожденную устойчивость к вирусу Pt. ERV 1.

Клинические проявления ВИЧ-инфекция - антропонозное вирусное ВИЧ-инфекция заболевание, в основе патогенеза которого лежит прогрессирующий иммунодефицит и развитие вследствие этого вторичных оппортунистических инфекций и опухолевых процессов. Патогенез ВИЧ-инфекции включает в себя пять основных периодов.

инкубационный период продолжается от инфицирования до появления антител и составляет от 7 до 90 дней. Никаких симптомов не наблюдается. Человек становится заразным через неделю p
стадия первичных проявлений характеризуется взрывообразным размножением вируса в различных клетках, содержащих СД-4 рецептор. В этот период начинается сероконверсия. Клинически эта стадия напоминает любую острую инфекцию: наблюдается головная боль, лихорадка, утомляемость, может быть диарея, единственным настораживающим симптомом является увеличение шейных и подмышечных лимфоузлов. Эта стадия продолжается 2 -4 недели p

в латентный период вирус замедляет свою репликацию и переходит в состояние персистенции. Латентный период длится 5 -10 лет. Единственным клиническим симптомом является лимфаденопатия – увеличение практически всех лимфоузлов. Уменьшается количество Т-хелперов по отношению к Т-супрессорам, исчезают реакции гиперчувствительности замедленного типа; p

СПИД-ассоциированный комплекс (стадия вторичных заболеваний). Вирус начинает интенсивно размножаться во всех тканях и органах, взрывообразно реплицироваться с повреждением клеток. Наиболее сильно повреждаются Т-хелперы, происходит полная их деструкция, что приводит к дерегуляции всей иммунной системы, резко снижается иммунитет как гуморальный, так и клеточный. На фоне иммунодефицита происходит развитие вторичных (оппортунистических) заболеваний, инфекционных и онкологических; p

собственно СПИД (терминальная стадия). Наблюдается полное отсутствие иммунного ответа. Длительность – примерно 1 -2 года, непосредственной причиной смерти являются вторичные инфекции. p

Наиболее частым клиническим проявлением ВИЧ-инфекции у детей является задержка темпов психомоторного и физического развития. У детей чаще, чем у взрослых, встречаются рецидивирующие бактериальные инфекции, а также интерстициальные лимфоидные пневмонии и гиперплазия пульмональных лимфоузлов, энцефалопатия. Часто встречается тромбоцитопения, клинически проявляющаяся геморрагическим синдромом, который может быть причиной смерти детей. Нередко развивается анемия. ВИЧ-инфекция у детей, рожденных от ВИЧ-инфицированных матерей, характеризуется более быстро прогрессирующим течением. У детей, зараженных в возрасте старше одного года, заболевание, как правило, развивается более медленно.

ЛАБОРАТОРНАЯ ДИАГНОСТИКА. Материалом для исследования является сыворотка крови больного ВИЧ-инфекцией. Забор крови производится из локтевой вены в чистую сухую пробирку в количестве 3 -5 мл. У новорожденных можно брать пуповинную кровь. Цельную кровь нельзя хранить более 12 часов при комнатной температуре и более суток в холодильнике, так как гемолиз эритроцитов может повлиять на результаты анализа. Сыворотка отделяется центрифугированием и переносится в чистую (лучше стерильную) пробирку и в таком виде она может храниться до 7 дней при температуре 4 -80 С.

Антитела к ВИЧ появляются у 90 -95% зараженных в течение 3 месяцев после заражения, у 5 -9% - через 6 месяцев от момента заражения, и у 0, 5 -1% - в более поздние сроки. Наиболее ранний срок обнаружения антител – 2 недели от момента заражения. Обнаружение антител к ВИЧ включает два этапа : На первом этапе проводится выявление суммарного спектра антител против антигенов ВИЧ с помощью иммуноферментного анализа. На втором этапе методом иммунного блоттинга проводится определение антител к отдельным белкам вируса.

Неспецифические лабораторные признаки ВИЧ-инфекции При ВИЧ-инфекции могут наблюдаться такие нарушения, как снижение количества СД 4 -лимфоцитов, увеличение процентного содержания СД 8 -лимфоцитов, инверсия соотношения СД 4/СД 8 (если его значение меньше 1), повышение уровня бета-2 микроглобина, неоптерина, возрастание количества иммуноглобулинов и другие.

необходимость создания охранительного психологического режима; p своевременное начало эффективной этиотропной (противоретровирусной) терапии и профилактики вторичных заболеваний; p тщательный выбор лекарственных препаратов с подбором необходимого минимума; p своевременное лечение вторичных заболеваний, для чего необходима их ранняя диагностика. p

1. Информация о неизлечимости ВИЧинфекции и ее фатальном прогнозе вызывает у инфицированного ВИЧ тяжелые эмоциональные реакции, связанные с внезапным осознанием неизбежности смерти. Наиболее доступной формой психологической помощи является индивидуальная беседа, а также семейная психотерапия. В случаях, когда больной не соглашается в этих вопросах, применяется рациональная психотерапия. Существенной чертой этого метода является воздействие логическим убеждением.

2. Одной из особенностей ВИЧ-инфекции является полиэтиологичность развивающихся при ней вторичных заболеваний и полиорганность поражений. К основным направлениям химиотерапии больных ВИЧ-инфекцией можно отнести лечение противоретровирусными препаратами, химиопрофилактику и лечение вторичных заболеваний. Лабораторными показаниями к проведению противоретровирусной терапии является снижение уровня СД 4 -лимфоцитов менее 0, 3 х109/л или повышение концентрации РНК ВИЧ в крови, так называемая «вирусная нагрузка» более 60000 копий в мл.

Монотерапия может проводиться по следующей Монотерапия схеме: тимазид (АЗТ), капсулы по 0, 1 г по 2 капсулы 3 раза в день (0, 6 г в сутки). Фосфазид (Ф-АЗТ), таблетки по 0, 2 г, по 2 таблетки 2 раза в день (0, 8 г в сутки) или по 1 таблетке (0, 2 г) 3 раза в день (суточной дозе 0, 6 г). Битерапия - применение одного из препаратов Битерапия ингибиторов обратной транскриптазы производных тимидина (азидотимидин (АЗТ), фосфазид (Ф-АЗТ), ставудин (d 4 Т) и одного из препаратов производных аденина (диданозин (dd I), ламивудин (3 ТС), зальцитабин (dd. С), абакавир). Высокоинтенсивная противовирусная терапия – использование препаратов из группы ингибиторов протеазы и ингибиторов обратной транскриптазы: фосфазид по 0, 4 г 2 раза в сутки, диданозин по 0, 2 г 2 раза в сутки, невирапин по 0, 2 г 2 раза в сутки.

ПРОФИЛАКТИКА. Специфическая профилактика не разработана, разработана но ведутся интенсивные работы по созданию профилактической вакцины. В настоящее время профилактика ВИЧинфекции сводится к социальным и противоэпидемическим мероприятиям, а именно: к мероприятиям механической защите от инфицирования с помощью презервативов, к пользованию одноразовыми шприцами, иглами, медицинскими инструментами, системами для переливания крови. Борьба с проституцией, наркоманией, гомосексуализмом, безнравственностью.

Статья 122 Уголовного кодекса РФ: "Заражение ВИЧ-инфекцией". 1. Заведомое поставление другого лица в опасность заражения ВИЧ-инфекцией - наказывается ограничением свободы на срок до трех лет, либо арестом на срок от трех до шести месяцев, либо лишением свободы на срок до одного года. 2. Заражение другого лица ВИЧинфекцией лицом, знавшим о наличии у него этой болезни, - наказывается лишением свободы на срок до пяти лет.

3. Деяние, предусмотренное частью второй настоящей статьи, совершенное в отношении двух или более лиц либо в отношении заведомо несовершеннолетнего, - наказывается лишением свободы на срок до восьми лет. 4. Заражение другого лица ВИЧинфекцией вследствие ненадлежащего исполнения лицом своих профессиональных обязанностей - наказывается лишением свободы на срок до пяти лет с лишением права занимать определенные должности или заниматься определенной деятельностью на срок до трех лет

КРАТКИЕ ГЛОБАЛЬНЫЕ ДАННЫЕ ОБ ЭПИДЕМИИ ВИЧ-ИНФЕКЦИИ И СПИДА (Согласно докладу «Объединённой программы ООН по ВИЧ/СПИДу» декабрь 2006 г) Количество людей, живущих с ВИЧ, в 2008 г. Всего — 39, 5 миллиона (34, 1 - 47, 1 миллиона) Взрослых — 37, 2 миллиона (32, 1 - 44, 5 миллиона) Женщин — 17, 7 миллиона (15, 1 - 20, 9 миллиона) Детей моложе 15 лет — 2, 3 миллиона (1, 7 - 3, 5 миллиона) Количество людей, заразившихся ВИЧ в 20086 г. Всего — 4, 3 миллиона (3, 6 - 6, 6 миллиона) Взрослых — 3, 8 миллиона (3, 2 - 5, 7 миллиона) Детей моложе 15 лет — 530, 000 (410, 000 — 660, 000) Количество смертей от СПИДа в 2008 г. Всего — 2, 9 миллиона (2, 5 - 3, 5 миллиона) Взрослых — 2, 6 миллиона (2, 2 - 3, 0 миллиона) Детей моложе 15 лет — 380, 000 (290, 000 - 500, 000)
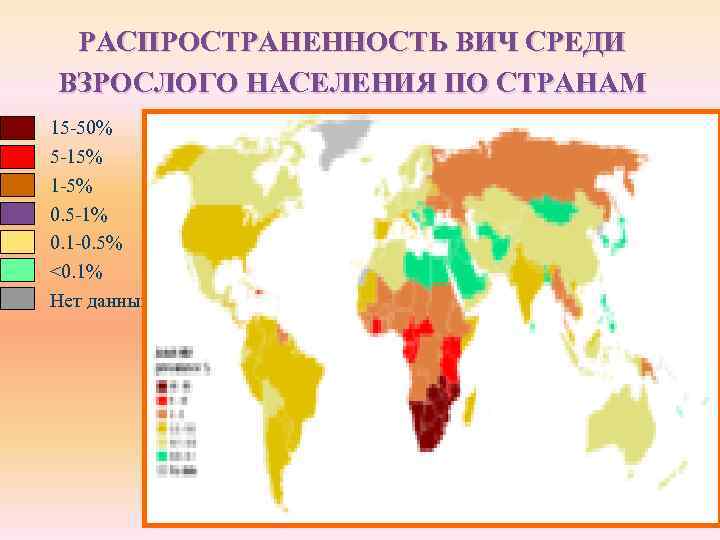
РАСПРОСТРАНЕННОСТЬ ВИЧ СРЕДИ ВЗРОСЛОГО НАСЕЛЕНИЯ ПО СТРАНАМ 15 -50% 5 -15% 1 -5% 0. 5 -1% 0. 1 -0. 5% <0. 1% Нет данных

При этом, из общего числа инфицированных, две трети (63 % — 24, 7 млн. [21, 8 - 27, 7 млн. ]) всех взрослых и детей с ВИЧ в мире живут в странах Африки к югу от Сахары, в основном в южной части Африки. Одна треть (32 %) всех людей с ВИЧ в мире живет в этом субрегионе, и здесь же произошли 34 % всех смертей в связи со СПИДом в 2011 году.

ОБЗОР ГЛОБАЛЬНОЙ ЭПИДЕМИОЛОГИИ ВИЧИНФЕКЦИИ/СПИДА Всего в мире около 40 миллионов человек живут с ВИЧинфекцией. Более двух третей из них населяют Африку южнее Сахары. Эпидемия началась здесь в конце 1970 -х — начале 1980 -х. Эпицентром считается полоса, протянувшаяся от Западной Африки до Индийского океана. Затем ВИЧ перекинулся южнее. Больше всего носителей ВИЧ в ЮАР — около 5 миллионов. Но в пересчёте на душу населения этот показатель выше в Ботсване и Свазиленде. В Свазиленде инфицирован каждый третий взрослый. За исключением стран Африки быстрее всего ВИЧ распространяется сегодня в Центральной Азии и Восточной Европе. С 1999 по 2012 годы количество инфицированных здесь почти утроилось. Эти регионы сдерживали эпидемию до конца 1990 -х, а затем количество заражённых стало резко увеличиваться — в основном за счёт наркоманов.

ВИЧ-ИНФЕКЦИЯ В РОССИИ К концу 2011 года в Российской федерации было официально зарегистрировано около 370, 000 ВИЧинфицированных. Однако реальное число носителей инфекции, по оценке на конец 2011, составляет ~940, 000 [560, 000 – 1, 6 млн. ]. Показатель распространенности ВИЧинфекции среди взрослых достиг значения ~1, 1%. От болезней связанных с ВИЧ и СПИДом умерли ок. 16, 000 человек, среди них 208 детей. Около 60 % случаев ВИЧ-инфицирования среди россиян приходится на 11 из 86 российских регионов (Иркутская, Саратовская обл. Калининградская, Ленинградская, Московская, Оренбургская, Самарская, Свердловская и Ульяновская области, Санкт-Петербург и Ханты-Мансийский автономный округ).
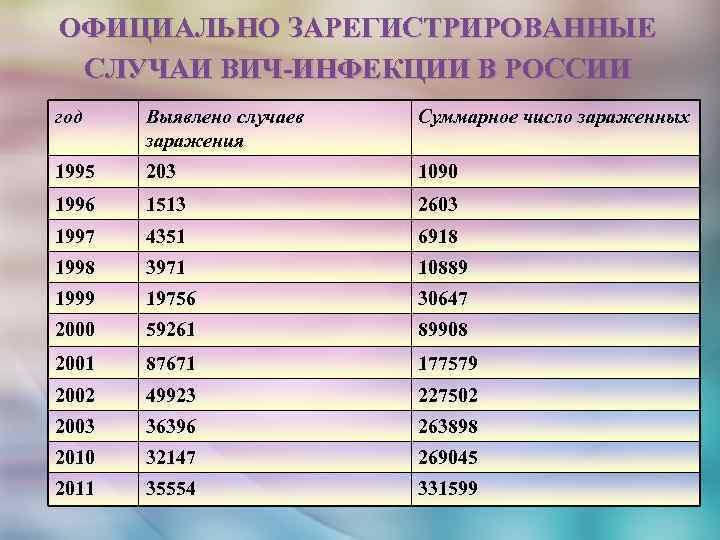
ОФИЦИАЛЬНО ЗАРЕГИСТРИРОВАННЫЕ СЛУЧАИ ВИЧ-ИНФЕКЦИИ В РОССИИ год Выявлено случаев заражения Суммарное число зараженных 1995 203 1090 1996 1513 2603 1997 4351 6918 1998 3971 10889 1999 19756 30647 2000 59261 89908 2001 87671 177579 2002 49923 227502 2003 36396 263898 2010 32147 269045 2011 35554 331599

В 2011 г. было обследовано 232, 9 тыс. человек, выявлено 454 ВИЧ-инфицированных. На реализацию данного направления дополнительно из бюджета Тульской области в рамках реализации целевой областной программы "Предупреждение и борьба с заболеваниями социального характера" и обеспечение "холодовой цепи" в 2010 г. выделено 8, 2 млн. рублей. Напомним, что в Тульской области первый случай ВИЧинфекции был зарегистрирован в 1994 году. Среди ВИЧинфицированных умерли по разным причинам 494 туляка.

На начало 2012 года в области выявлен 4441 случай заражения ВИЧ-инфекцией, в том числе 113 человек с диагнозом СПИД. От ВИЧ-инфицированных матерей родились 312 детей, диагноз врожденной ВИЧинфекции установлен 6 детям. Причем если раньше большинство заражений приходилось на долю наркоманов, то с 2006 года отмечен рост числа заражений половым путем. Наиболее поражаемой возрастной группой остаются молодые люди в возрасте 18 -35 лет (79% от общего числа заболевших), т. е. самые активные с социальной точки зрения туляки. В области нет ни одного среднетехнического и высшего учебного заведения, где бы не регистрировались случаи ВИЧ-инфекции.

Как отмечено на официальном сайте департамента здравоохранения по Тульской области, на 1 января 2013 г. в регионе зарегистрировано 4921 человек, инфицированных ВИЧ, а в минувшем году выявлено 512 новых случаев ВИЧ-инфекции. Начиная с 2001 г. , заболеваемость регистрируется на всех административных территориях области, 45% случаев выявлено в г. Туле. Далее, по числу выявленных больных, следуют Алексинский, Киреевский, Ленинский, Щекинский районы.

За последние 10 лет в Тульской области число ВИЧ-инфицированных среди беременных увеличилось в 124 раза. p В 70% случаев беременности среди ВИЧпозитивных женщин завершается родами. p В течение 10 лет зарегистрировано 400 детей, рожденных от ВИЧ-инфицированных матерей. p У 27 новорожденных установлен диагноз врожденной ВИЧ-инфекции. p На конец 2011 года уровень распространенности ВИЧ в области составил 305, 48 на 100 тыс. населения против 271, 9 на 100 тыс. населения по Российской Федерации. p

КОЛИЧЕСТВО ВИЧ-ИНФИЦИРОВАННЫХ ПОДРОСТКОВ ПО ТО Состояло на начало года Выявлено в течении года 2010 34 4 2011 10 5 2012 5 3 37 1 15 -- 8 -- 3 7 20 8 1 4 7 3 -2 2 4 Пути заражения: половой Через употребление наркотиков Контингент: Уч-ся средних школ Студенты Не работающие
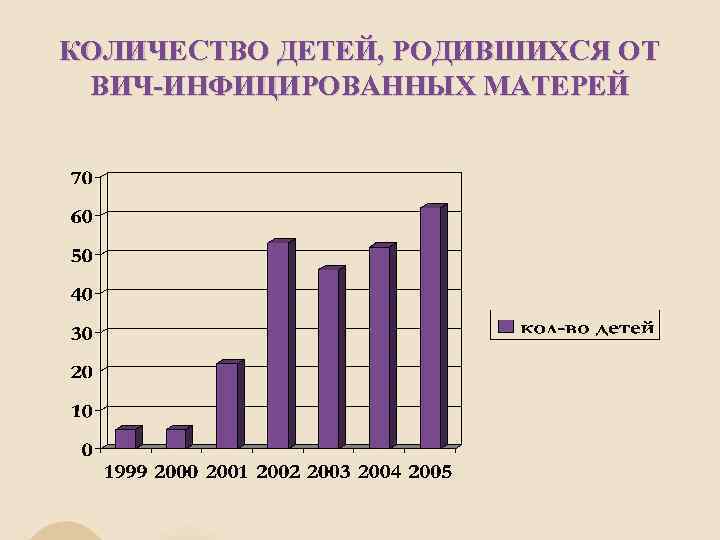
КОЛИЧЕСТВО ДЕТЕЙ, РОДИВШИХСЯ ОТ ВИЧ-ИНФИЦИРОВАННЫХ МАТЕРЕЙ
Медленные вирусные инфекции и прионные болезни

Термин «медленная инфекция» указывает на затяжной характер заболеваний, растягивающихся на месяцы и годы. Медленные инфекции имеют следующие особенности: p длительный инкубационный период (месяцы и годы); p своеобразные и необратимые изменения ткани, преимущественно ЦНС; p медленное прогрессирование болезни; p летальный исход.
Медленные инфекции Вызываемые вирусами Вызываемые прионами

Медленные вирусные инфекции В основе патогенеза медленных вирусных инфекций лежат длительное персистирование возбудителя в организме и замедленное повреждающее действие на клетки.

По мере изучения этих болезней были установлены неожиданные на первый взгляд, факты: медленные инфекции могут вызывать возбудители острых вирусных заболеваний – кори (подострый склерозирующий и послекоревой панэнцефалиты), краснухи (прогрессирующая врожденная краснуха, прогрессирующий краснушный панэнцефалит), герпеса (подострый герпетический энцефалит, хронический инфекционный мононуклеоз, цитомегаловирусное поражение мозга) и др. p
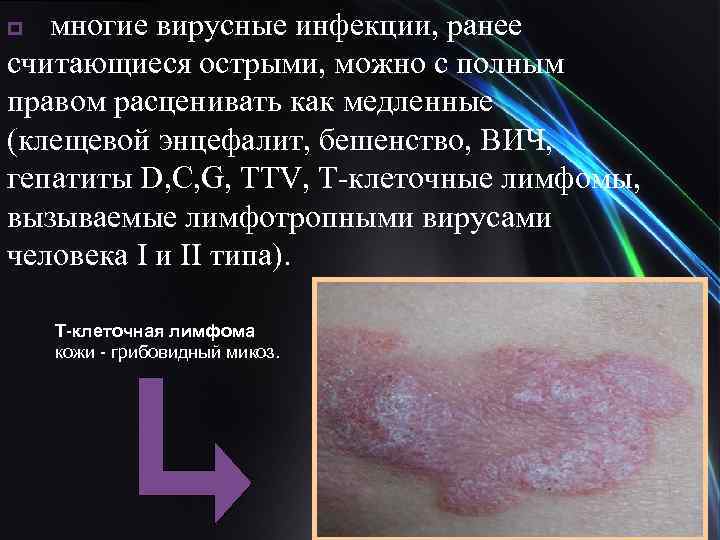
многие вирусные инфекции, ранее считающиеся острыми, можно с полным правом расценивать как медленные (клещевой энцефалит, бешенство, ВИЧ, гепатиты D, C, G, TTV, Т-клеточные лимфомы, вызываемые лимфотропными вирусами человека I и II типа). p Т-клеточная лимфома кожи - грибовидный микоз.

Возбудители некоторых медленных вирусных инфекций человека. Возбудитель Болезнь Вирус кори Подострый склерозирующий панэнцефалит Вирус краснухи Прогрессирующая врожденная краснуха, прогрессирующий краснушный панэнцефалит Вирус клещевого энцефалита Прогредиентная форма клещевого энцефалита Вирус простого герпеса Подострый герпетический энцефалит Вирус иммунодефицита человека ВИЧ-инфекция, СПИД HTLV -1, -2 Т-клеточная лимфома Полиомавирус JC Прогрессирующая многоочагова лейкоэнцефалопатия

Подострый склерозирующий панэнцефалит - прогрессирующее дегенеративное заболевание нервной системы с характерной клинической картиной, включающей умственные и двигательные нарушения, миоклонические судороги, электроэнцефалографические дизритмии. Заболевание наблюдают у лиц в возрасте 2 -30 лет, обычно оно заканчивается смертью пациента в течение года. Возбудитель псп - вирус кори с измененными свойствами, что способствует длительному персистированию в организме.

Репродукция вируса в клетках нейроглии происходит с образованием вирусных белков и РНК, но без формирования дочерних популяций. Репродуктивный цикл заканчивается гибелью нейронов и олигодендроцитов. Аналогичные поражения также наблюдают как осложнения коревой инфекции и классифицируют как подострый послекоревой панэнцефалит. Диагностика основана на выявлении противокоревых АТ в сыворотке крови и СМЖ.

Погрессирующая многоочаговая лейкоэнцефалопатия. - подостро протекающее демиелинизирующее заболевание, возникающее у пациентов с различными нарушениями иммунного статуса: СПИДом, лейкемии, лимфомами и др. Болезнь протекает с тяжелыми неврологическими нарушениями, приводящими к летальному исходу.

Возбудитель полиомавирус JC, избирательно повреждающий клетки нейроглии (астроциты и олигодендроциты). p Нейротропизм обуславливают специфические клеточные факторы, активизирующие промотры в геноме возбудителя. Основным механизмом, определяющим повреждение глиальных клеток, являются мутации гена-промотора, в результате которых репродукция вируса происходит более активно. Указанное объясняет тот факт, что заболевание развивается только у ограниченной части больных, хотя не менее 75% взрослых лиц сероположительны. p

У лиц с нормальным иммунным статусом геном вируса остается неинтегрированным в геном клетки, и инфекция протекает латентно. При иммунодефицитах возбудитель переходит в активную фазу репликации и гематогенно диссеминирует. Диагностика включает обнаружение в биотопах олигодендроцитов и астроцитов, содержащих тельца включений, а так же выделение возбудителя путем заражения культур клеток приматов.

Прионовые инфекции Особую группу медленных инфекций составляют поражения ЦНС, проявляющиеся вакуолизацией серого вещества – так называемым губкообразным перерождением нервных тканей. Ему предшествует развитие первичнодегенеративных процессов при полном отсутствии воспалительных реакций. Своеобразие патоморфологической картины обусловило первичное название заболеваний – трансмиссивные спонгиоформные (от греч. Spongia – губка) энцефалопатии.

Было установлено, что их возбудители проходят через бактериальные фильтры, не размножаются на искусственных питательных средах, воспроизводят феномен интерференции, что дало основание отнести их к вирусам. Однако американский вирусолог Гайдушек установил, что эти «вирусы» обладают необычными свойствами, так как они оказались устойчивы к действию многих вирулицидных факторов, а материалом, полученным от погибших людей и животных, невозможно заразить клеточные культуры.

В начале 80 -х годов американских биохимик Прузинер установил, что возбудителем скрепи (спонгиоформной энцефалопатии овец и коз) выступает не аномальный вирус, а безнуклеиновый низкомолекулярный белок, названный им инфекционным прионовым белком или прионом. Дальнейшие исследования позволили установить, что прионы вызывают все известные спонгиоформные энцефалопатии. В настоящее время эти заболевания обозначают термином «Прионовые инфекции» .

Патогенез прионовых инфекций Патогенез поражений обусловлен способностью инфекционного прионового белка Pr. PSc (от англ. scrapie, скрепи, являющиеся самой распространенной прионной болезнью) вызывать мутацию гена, кодирующего синтез нормального нейронального прионового белка Pr. PC ( от англ. cell, клетка), в результате чего синтезируется инфекционный прионовый белок Pr. PSc , отличающийся нарушенной конфигурацией молекулы.

Молекула Pr. PSc соединяется с молекулой Pr. PC с образованием димерного продукта, трансформирующегося в 2 молекулы Pr. PSc. в следующем цикле 2 молекулы Pr. PC соединяются с 2 молекулами Pr. PSc , давая начало 4 молекулам Pr. PSc , что обеспечивает экспоненциальное образование молекул Pr. PSc. Таким образом, образование инфекционных прионовых белков происходит не за счет репродукции молекулы Pr. PSc , попавшей в организм, а за счет синтеза новых молекул, кодируемых мутировавшим геном Pr. PC.

Физиологическое значение белка Pr. PC связывают с реализацией функций синапсов, сохранением клеток Пуркинье, регуляцией внутриклеточного содержания Са 2+ в нейронах, поддержанием трофики некоторых их популяций и сохранением резистентности нейронов и астроцитов к повреждающим факторам. Белок Pr. PC – короткоживущий (период полураспада 5 -6 часов).
В противоположность этому инфекционный прионовый белок Pr. PSc накапливается в цитоплазменных визикулах, что приводит к последующему нарушению функций синапсов и развитию глубоких неврологических дефектов. Позднее Pr. PSc высвобождается во внеклеточное пространство и откладывается амилоидных бляшках.

У человека прионы вызывают: - болезнь Куру, - болезнь Кройтцфельдта-Якоба, - синдром Герстмана-Штраусслера-Шайнкера - фатальную семейную бессонницу. Их характерная особенность – практически полное отсутствие иммунных реакций к инфекционным прионовым белкам, что связанно с их внутриклеточной локализацией и структурным сходством с нейрональными белками. Гистологически в тканях мозга выявляют выраженную губчатую дегенерацию, генерализованную гипертрофию астроцитов и амилоидные бляшки, состоящие из белка Pr. PSc.

Изучение условий возникновения прионовых болезней выявило уникальные особенности их эпидемиологии, отличающие их от прочих инфекционных заболеваний. Они могут вызывать как инфекционные спорадические, так и наследственные поражения. В последнем случае предполагают наличие генетической предрасположенности к прионовым инфекционным белкам.

Болезнь Куру Это инфекционная прионная болезнь, ранее распространенная среди папуасов в Новой Гвинее, где ритуально было развито каннибальство. Заболевание проявляется расстройствами функций мозжечка – нарушениями походки, координации движений, артикуляции, а также тремором. Болезнь длится 9 -24 мес. и заканчивается смертью больного. Инфекционная природа Куру доказана группой Гайдушека, подтвердившей возможность заражения шимпанзе клетками мозга больного.

Лабораторная диагностика основана на внутримозговом заражении мышат-сосунков или хомяков, в след за чем развивается специфическая клиническая картина болезни. Средства специфической лекарственной терапии отсутствуют. p Лечение симптоматическое и патогенетическое. Борьба с каннибальскими обрядами привела к практически полной ликвидации болезни. p
Болезнь Кройтцфельдта-Якоба форма спонгиозной энцефалопатии, характеризующаяся слабоумием, миоклониями, атаксией и другими неврологическими проявлениями (быстро приводит к коме и смерти). -

Продолжительность инкубационного периода варьирует от 18 мес до 20 лет. Первоначально развиваются гиперестензия, нарушения зрения и боли в конечностях, затем присоединяются слабоумие, миоклония, атаксия, паркинсонизм и др. Пациент погибает через 7 -24 мес. Инфекционная природа заболевания доказана группой Гайдушека. Средний возраст больных 50 -60 лет. Заболевание может протекать по типу спорадических, наследственных или инфекционных (в том числе и ятрогенных) поражений.

Спорадические и наследственные случаи заболевания возникают при мутациях (в том числе соматических) гена PRNP, кодирующего синтез прионового белка Pr. PC в организме (локализован в хромосоме 20). Для наследственной формы характерен семейный характер проявлений. p

Передача инфекционного прионового белка Pr. PSc при употреблении в пищу недостаточно хорошо термически обработанного мяса и мозга больных коров, коз, овец, а также при употреблении в пищу сырых морских моллюсков возможна, но остается предметом дискуссий. Также доказана возможность инокуляции белка Pr. PSc во время хирургических операций, при пересадке роговицы или твердой мозговой оболочки, при прозекторских манипуляциях и после введения донорского соматотропина. p

Лабораторная диагностика также основана на внутримозговом заражении мышатсосунков или хомяков, у которых развивается специфическая картина болезни. p Лечение симптоматическое и патогенетическое p

Синдром Герстмана-Штраусслера. Шайнкера - наследственная прионовая патология, носящая семейный характер. По сравнению с болезнью Кройтцфельдта-Якоба заболевают люди более молодого возраста (в среднем на 10 лет раньше).

Продолжительность инкубационного периода варьирует в пределах 5 -30 лет. Типичны постепенная утрата рефлексов с нижних конечностей, нарушения глотания, мышечная гипотония, дизартрия, слабоумие. Заболевание медленно прогрессирует в течение 4 -5 лет и заканчивается гибелью пациента. Диагностика, лечение и профилактика аналогичны таковым при болезни Кройтцфельдта. Якоба.

Фатальная семейная бессонница. - наследственная прионовая болезнь, описанная в 1986 г. как аутосомно-доминантная патология и зарегистрированная у лиц в возрасте от 25 до 70 лет. p

Первое проявление – прогрессирующее нарушение сна, сопровождающееся повышенной утомляемостью и не поддающееся лечению. К ним присоединяется артериальная гипертензия, тахикардия, запоры, импотенция. Позднее – двигательные расстройства (атаксия, дизартрия, судороги, дистонические приступы) и нарушение циркадных ритмов сердца. Смерть больного наступает в результате прогрессирующей легочно-сердечной недостаточности. p

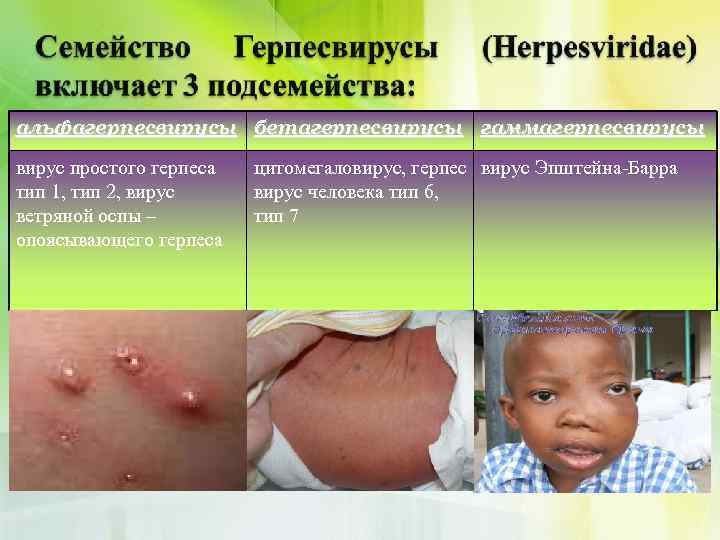
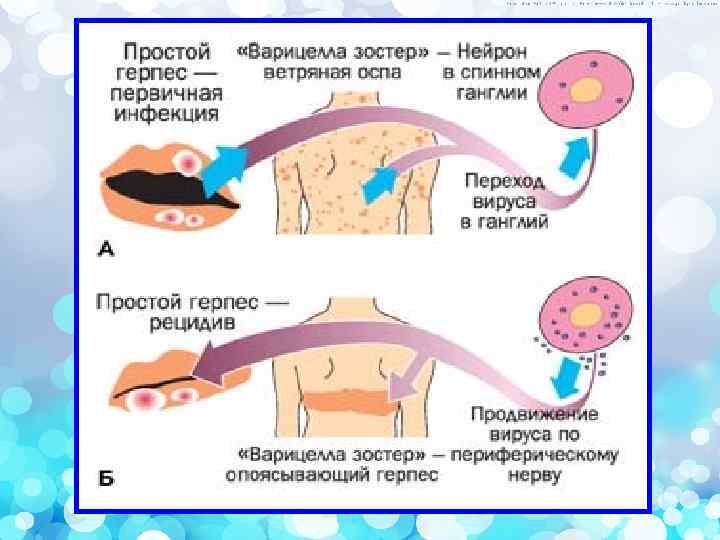
альфагерпесвирусы бетагерпесвирусы гаммагерпесвирусы вирус простого герпеса тип 1, тип 2, вирус ветряной оспы – опоясывающего герпеса цитомегаловирус, герпес вирус Эпштейна-Барра вирус человека тип 6, тип 7

p – инфекция, вызываемая возбудителем из группы бетагерпесвирусов, для которого основными клетками-мишениями в организме человека являются моноциты, макрофаги, гранулоциты, эпителиальные и эндотелиальные клетки, фибробласты, гладкомышечные клетки. p ЦМВИ характеризуется многообразными проявлениями от бессимптомного до генерализованного (септического) течения с тяжелым поражением ЦНС и других органов.

Источником инфекции является человек, зараженный ЦМВ. Выделение вируса из организма реконвалесцента обычно продолжается несколько месяцев. При заражении в перинатальный период непрерывное выделение вируса продолжается 4 -8 лет. p У инфицированного человека вирус находится во внутренних органах, крови, ликворе, слюне, моче, влагалищном секрете, сперме, грудном молоке, слезной жидкости. p

Основными механизмами заражения ЦМВ заражения являются перкутанный и аспирационный (аэрогенный). p Перкутанный механизм реализуется естественными и искусственными путями. p При естественных путях передачи заражение передачи человека происходит при непосредственном контакте с источникомом инфекции (оральнооральный, сексуально-трансмиссивный пути) или опосредованно – через контаминированную вирусом посуду, зубные щетки, игрушки. p Инфекция может передаваться от матери к плоду. Врожденная ЦМВИ встречается у 1% новорожденных. p Искусственный путь передачи - заражение передачи ЦМВ реципиентов крови. Фактором передачи инфекции может быть не только перелитая кровь, но и пересаженный орган. p
p Вирус имеет выраженный тропизм к эпителию слюнных желез и канальцев почек, где способен длительно реплицироваться и выделяться из организма со слюной, мочой.

имеет продолжительный инкубационный период 3 -8 недель. У подавляющего большинства (более 90%) детей и взрослых протекает бессимптомно и после окончания периода вирусовыделения приобретает характер латентной инфекции. Только у небольшой части инфицированных возникают клинические симптомы – сиалоаденит - увеличение слюнных желез (чаще углочелюстных) и мононуклеозоподобный синдром. Мононуклеозоподобный синдром характеризуется умеренной лихорадкой, недомоганием, гепатоспленомегалией, увеличением шейных лимфатичесикх узлов. p

Больные с различными видами иммунодефицитных состояний, в т. ч. ВИЧинфицированные в стадии СПИДа, подвергаются более высокому риску развития висцеральных и диссеминированных форм ЦМВИ. Особенно часто возникает пневмония. Поражения печени многообразны – от гепатомегалии до тяжелого гепатита и деструктивного холангиолита с холестазом. Поражения желудочно-кишечного тракта отличаются чрезвычайным полиморфизмом: эзофагит, гастродуоденит, энтероколит, колит. В процесс часто вовлекается нервная система. Наряду с тяжелыми энцефалитами развиваются вялотекущие энцефалопатии, заканчивающиеся слабоумием. Описаны переферические нейропатии. Кроме того, ЦМВИ может сопровождаться васкулитом, тромбоцитопенией и др. синдромами. p

p обычно обусловлена развившейся иммуносупрессией и по своему характеру во многом соответствует первичной приобретенной инфекции.

Врожденная инфекция у новорожденных в большинстве случаев (95%) протекает бессимптомно. Однако, почти у 10% из них впоследствии возникают односторонняя или двусторонняя нейросенсорная тугоухость, замедление психического развития или нарушение двигательных функций. Инфицирование плода на ранних стадиях его развития приводит к уродствам и гибели плода или новорожденного. Заражение на поздних сроках не нарушает строение органов и проявляется в постнатальном периоде в виде желтухи, гепатоспленомегалии, тромбоцитопенической пурпуры, поражений центральной нервной системы и пневмонии. p
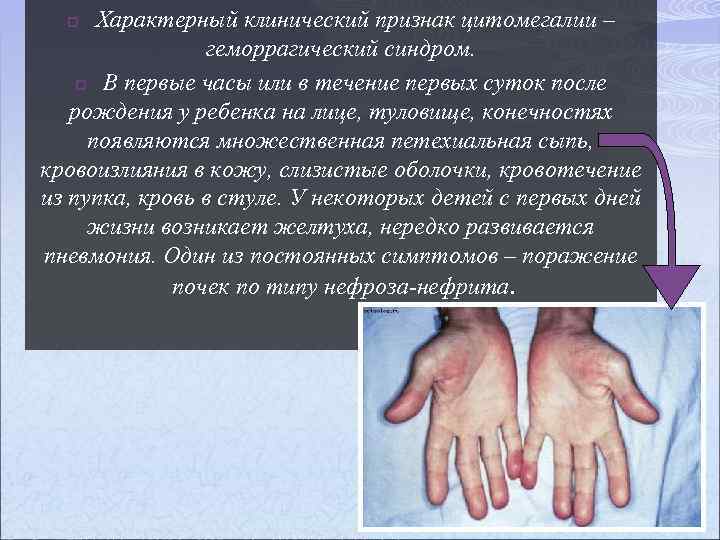
Характерный клинический признак цитомегалии – геморрагический синдром. p В первые часы или в течение первых суток после рождения у ребенка на лице, туловище, конечностях появляются множественная петехиальная сыпь, кровоизлияния в кожу, слизистые оболочки, кровотечение из пупка, кровь в стуле. У некоторых детей с первых дней жизни возникает желтуха, нередко развивается пневмония. Один из постоянных симптомов – поражение почек по типу нефроза-нефрита. p

Микроскопический метод p Вирусологический метод p Молекулярно-генетические методы (ПЦР) p Серологические методы: Выявление вирусных антигенов Выявление специфических антител (Ig M- и Ig G) p

– это инфекция, которая вызывается вирусами простого герпеса 1 и 2 типов и характеризуется тегментальными поражениями, т. е. поражениями кожи и слизистых оболочек, поражением центральной нервной системы, а также других систем организма. Ее проявления часто ассоциированы с иммуносупрессией, а у иммунокомпрометированных лиц она может иметь диссеминированное, септическое течение. Особое значение имеет то, что герпетическая инфекция способна вызывать врожденную патологию плода и заболевания у новорожденных. p

Возбудители герпетической инфекции – Herpes simplex virus type 1 и 2 (HSV-1, 2 или ВПГ-1, 2) относятся к роду Simplexvirus, подсемейству Simplexvirus Alphaherpesvirinae, семейству Herpesviridae. p ВПГ – 1 чаще обусловливает поражение респираторных органов, а ВПГ-2 – развитие ВПГ-2 генетального герпеса и генерализованной инфекции у новорожденных. p

Источником заражения являются люди, инфицированные ВПГ, независимо от того, протекает у них инфекция бессимптомно или манифестно. Основными механизмами заражения являются перкутанный и аспирационный. p Перкутанный механизм заражения реализуется в естественных и искусственных условиях. p Аспирационный (аэрогенный) механизм заражения реализуется воздушно-капельным путем. p Искусственный путь передачи ВПГ – парентерально
Простой герпес врожденный приобретенный первичный вторичный

возникает при первом контакте человека с вирусом. Инкубационный период длится от 2 до 14 дней. Первичный простой герпес наблюдается преимущественно у детей в возрасте от 6 мес. До 5 лет и значительно реже – у взрослых. У 80 -90% первично инфицированных детей заболевание протекает в бессимптомной форме и только у 10 -20 % зараженных имеются клинические проявления (манифестная форма). Наиболее частыми формами первичного герпеса является острое респираторное заболевание и острый герпетический стоматит (гингивостоматит). Первичный герпес может проявляться различными поражениями кожи, конъюнктивы или роговицы глаза. Первичный генитальный герпес возникает в более позднем возрасте с началом сексуальной жизни. p

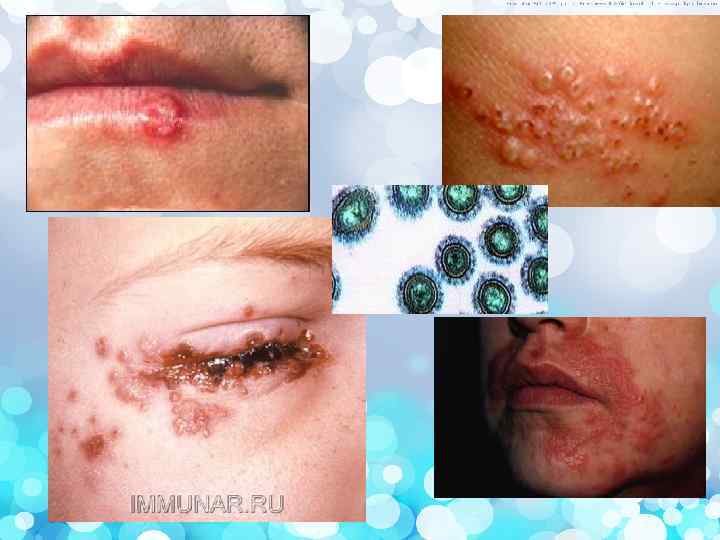
p возникает в результате реактивации имеющегося в организме вируса. Тегментальный простой герпес. Типичными являются пузырьковые высыпания, чаще локализуются в области красной каймы губ и крыльев носа. Могут быть поражения кожи: лба, шеи, туловища, конечностей. У многих пациентов высыпаниям предшествуют чувство жжения, кожный зуд, гиперемия, отек. Затем появляются папулы, превращающиеся в везикулы, наполненные серозным содержимым. p

имеют многообразные проявления. Резкий отек подкожной клетчатки или гиперемия, что может привести к диагностическим ошибкам и даже неправильному диагнозу «флегмона» с последующим хирургическим вмешательством. p Иногда высыпания при простом герпесе локализуются по ходу нервных стволов, напоминая опоясывающий лишай. Это зоостериформный простой герпес, чаще встречающийся у лиц с иммуносупрессией. p

протекает тяжело. Развиваются отек и гиперемия наружных половых органов, затем появляются везикулярные высыпания на половом члене, в области вульвы, сопровождается регионарным лимфаденитом. Везикулы быстро вскрываются, образуя эрозивные, эрозивно-язвенные поверхности. Все это сопровождается чувством жжения, зудом, болезненностью, делает невозможными половые контакты, что приводит к развитию невротических состояний. Рецидивирующий генитальный герпес сопровождается регионарным лимфаденитом, иногда развивается лимфостаз и как результат – слоновость половых органов. У женщин рецидивирующий герпес может способствовать развитию карциномы шейки матки. p

Наиболее часто в патологический процесс вовлекается нервная система, в результате чего возникают серозный менингит, энцефалит или менингоэнцефалит. На втором месте по частоте висцеральных поражений стоит печень. Развивающийся герпетический гепатит имеет общие клинико-лабораторные признаки с гепатитом В, С. Герпетическая пневмония наблюдается у лиц с выраженными иммунодефицитными состояниями, в т. ч. с ВИЧ/СПИДом. p

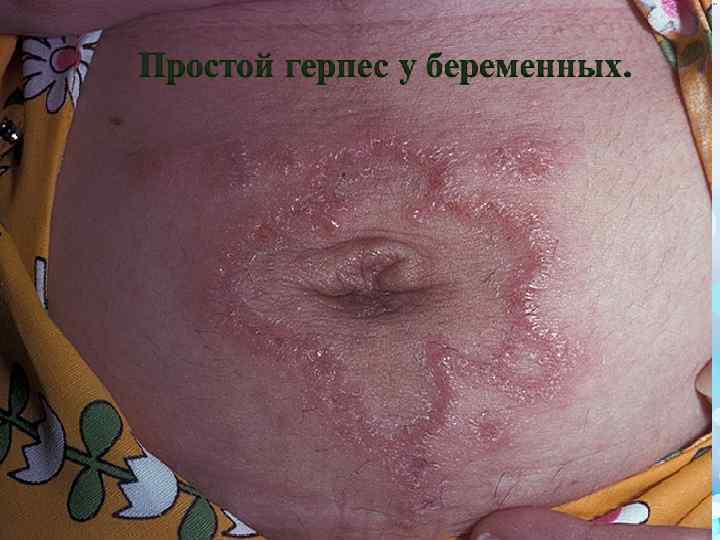
p встречается только у лиц с тяжелым иммунодефицитом и у детей до 1 мес. , относится к СПИД-индикаирным болезням. Летальность составляет около 80%. Повышается вероятность самопроизвольного аборта и преждевременных родов. Особенно неблагоприятно воздействие первичного простого герпеса на развивающуюся беременность и плод при ее возникновении в первом триместре беременности. При восходящем пути инфицирования (из шейки матки) нередко наблюдается многоводие, невынашивание беременности, задержка внутриутробного развития, p

может протекать в виде следующих форм: p Генерализованная (диссеминированная) форма с церебральными и висцеральными повреждениями. p Локализованная форма: поражение кожи, слизистых полости рта, глаз. p Висцеральная (поражение легких, печени, селезенки, надпочечников). p Поражение нервной системы (транзиторные неврологические изменения, кистозные полости в белом веществе лобных и теменных долей, субэпендимальные кисты, энцефалит, менингоэнцефалит). p

Забор материала проводится в зависимости от клинической формы. В лабораторной диагностике используются следующие методы: методы p. Вирусологический; Вирусологический p Микроскопический (цитологическая Микроскопический диагностика); p Молекулярно-генетический (ПЦРМолекулярно-генетический диагностика); p. Серологические методы.

Терапия больных простым герпесом индивидуальна и зависит от формы инфекции, тяжести, частоты рецедивов. p Она включает этиотропное, патогенетическое и симптоматическое патогенетическое направления. p


Патогенетическая терапия направлена на нормализацию функции иммунной системы организма, в том числе на активацию системы интерфероновой защиты, и проводится под контролем иммунограммы. К числу натуральных интерферонов (ИФН) относятся: альфаферон, вэлферон, эгиферон.

В ранний период рецидива показано введение иммуноглобулинов, содержащих повышенный титр антител к герпетическим вирусам. Для лечения часто рецидивирующего простого герпеса применяются также инактивированные противогерпетические вакцины.
Занятие 32. ВИЧ-инфекция.ppt