a4f597837a93a7524be12a94c13b6ac7.ppt
- Количество слайдов: 68

ТТА, Кафедра детских болезней, неонатологии и медицинской генетики. Лекция 2: МОНОГЕННЫЕ БОЛЕЗНИ МУЛТИФАКТОРИАЛЬНЫЕ БОЛЕЗНИ МЕТОДЫ ПРЕНАТАЛЬНОЙ ДИАГНОСТИКИ. СКРИНИНГ ПРОГРАММА ЛЕКТОР: д. м. н. Шарапова М. Х.

Классифиация моногенных заболеваний: Аутосомно-доминантные: синдром Марфана, хорея Гентингтона, миопия Минковского-Шаффара… Ø Аутосомнорецессивные: ФКУ, галактоземия, гликогенозы, с индром. Тея-Сакса, Нимана –Пика, Гоше , миопия и др. Ø Сцепленные с Ххромосомой, доминантные: фосфатдиабет, хронический гематурический нефрит. Ø Сцепленные с Х-хромосомой, рецессивные: миодистрофия Дюшена. Ø

НЕКОТОРЫЕ БОЛЕЗНИ НАРУШЕНИЯ ОБМЕНА ВЕЩЕТВ НАРУШЕНИЯ АМИНОКИСЛОТНОГО ОБМЕНА

ФЕНИЛКЕТОНУРИЯ (ФКУ) Фенилпировиноградная олигофрения была открыта в 1934 г. Феллингом. Это наследственное заболевание аминокислотного обмена, обусловленное мутациями в гене фенилаланингидроксилазы, печеночного фермента, осуществляющего реакцию гидроксилирования фенилаланина, т. е. его превращение в тирозин. Мутации в пределах этого крупного гена человеческого генома затрагивают различные его участки и по-разному повреждают функцию фермента. Болезнь распространена в популяциях, где распространён кровнородственный брак. Заболевание передаётся по аутосомнорецессивному типу.

ПАТОГЕНЕЗ. Фенилаланин является незаменимой аминокислотой для человеческого роста и развития и содержится во всех белковых продуктах. В основе патогенеза заболевания лежит недостаточность фермента печени - фенилаланингидроксилазы, которая приводит к нарушению обмена фенилаланина и возрастанию в 10 и более раз концентрации токсических продуктов нарушения метаболизма - фенилуксусной, фенилмолочной и фенилпировиноградной кислот, которые обладают нейротоксическим действием. Увеличение концентрации фенилаланина ограничивает транспорт тирозина и триптофана через гематоэнцефалический барьер. Накопление фенилаланина в мозгу больного также угнетает активность ферментов, участвующих в синтезе цереброзидсульфатов, которые защищают мозг от демиелинизации.

КЛИНИКА. Заболевание обычно проявляется в первые месяцы после рождения задержкой психического и моторного развития. Клинические проявления весьма разнообразны. Зачастую эти больные идут под диагнозом ДЦП, умственная отсталость. Ø Ранними проявлениями заболевания являются срыгивание, рвота, понос. Неврологические симптомы проявляются несколько позже в виде нарушения сна, судорожного синдрома, умственной отсталости. Развивается мышечная гипо- или гипертония. Моторное развитие задержано. Ø Дети начинают сидеть и ходить с запозданием, появляется специфический запах пота и мочи - ''мышиный запах''. Со стороны кожи отмечаются понижение или отсутствие пигментации, дерматиты, экземы, светочувствительность. Волосы и радужные оболочки глаз также теряют пигментацию. Нарушения со стороны черепно-мозговых нервов проявляются косоглазием, нистагмом, нарушением координации движения. В более позднем возрасте появляется характерная поза больного - ''поза портного'’ и своеобразная походка. Больные стоят широко расставив ноги, согнутые в коленях и тазобедренных суставах, опустив плечи и голову. При ходьбе делают маленькие шаги и покачиваются. Ø

ДИАГНОЗ основывается на клинической картине и данных биохимических молекулярно-генетических исследований. Из-за клинического полиморфизма ФКУ следует исключать у каждого умственно отсталого ребенка. Наиболее доступной и простой является проба Феллинга. К 2 -3 мл подкисленной хлористым водородом мочи добавляют реактив Феллинга (10% раствор трёхвалентного хлорида железа – Fe. Cl 3) в количестве 0, 5 – 1 мл. Проба считается положительной при появлении зелёного окрашивания. Повышение концентрации фенилаланина в моче и плазме могут быть выявлены с помощью тонкослойной хроматографии. Ø При определении фенилаланина в плазме крови используется проба Гатри, основанная на хорошем росте В. subtil в среде, содержащей фенилаланин. Ø

Ø ЛЕЧЕНИЕ. Фенилаланин является незаменимой аминокислотой и минимальное введение с пищей абсолютно необходимо. Для лечения ФКУ используют аминокислотные смеси или белковые гидролизаты с низким содержанием фенилаланина. Эта основная диета дополняется безбелковыми и малобелковыми продуктами, витаминами, микроэлементами. Ограничиваются продукты, содержащие в большом количестве фенилаланин, в том числе и грудное молоко, и молоко животных. Такая диета должна назначаться не позже 2 -3 недели жизни и продолжаться до 5 летнего возраста. В более старшем возрасте снижается чувствительность ЦНС к повреждающему действию фенилаланина и продуктов его обмена, а основные этапы развития мозга к этому времени уже закончены.

Потребность в белках обеспечивается белковыми гидролизатами или смесями аминокислот, например, “Гипофенат'', ''Берлафен'' и др. После снижения уровня фенилаланина в крови до нормы постепенно начинают вводить белки животного происхождения под контролем биохимических исследований, чтобы общее содержание фенилаланина в суточном рационе не превышало 25 мг на 1 кг массы ребёнка. Ø Из рациона исключают мясо, рыбу, печень, почки, яйца, сыр, изделия из пшеничной и ржаной муки, творог, орехи, бобы и др. , молоко и картофель даются с учётом содержания в них фенилаланина в ограниченных количествах. Ø

Ø ПРОФИЛАКТИКА. В 1954 году была доказана, что диета с низким содержанием фенилаланина предотвращает развитие клинических симптомов у больных, которым диагноз был поставлен сразу после рождения. На этом основании в США в 1964 г. Была разработана и внедрена в практику здравоохранения первая программа массового скрининга (т. е. просеивания) новорожденных на ФКУ. После этого программы массового скрининга новорожденных на ФКУ быстро распространились по всему миру, и в настоящее время около 10 миллионов новорожденных тестируется на ФКУ ежегодно. Массовый скрининг на ФКУ дают 7 -10 - кратный экономический эффект по сравнению с их пожизненным содержанием в домах для инвалидов.

ЦИСТИНОЗ (СИНДРОМ ФАНКОНИ) Наследственное заболевание, связанное с нарушением обмена цистина вследствие ферментативного блокирования (биохимический механизм до конца не выяснен). В связи с плохой растворимостью цистина в биологических жидкостях при чрезмерном накоплении его в клетках, он легко выпадает в осадок в виде кристаллов, вызывая различные функциональные нарушения в деятельности внутренних органов, главным образом, почек. Ø Частота – 1: 600 000 населения. Ø Заболевание наследуется по аутосомнорецессивному типу. Ø

Ø КЛИНИКА. Болезнь проявляется в конце первого или в начале второго полугодия жизни. У больных ухудшается аппетит, возникают постоянная жажда, запоры, рвота после приёма пищи и пития или не связанные с кормлением. Снижается сопротивляемость ребёнка к инфекциям. Развивается поражение глаз в виде конъюнктивита, сходящегося косоглазия. В роговице и конъюнктиве наблюдаются дистрофические изменения из-за отложения в них кристаллов цистина. Бывает выражена светобоязнь. Позднее у больных увеличиваются печень и селезёнка, появляется частое мочеиспускание с нарушением функции почек. Одним из типичных симптомов заболевания является прогрессирующее отставание в росте вплоть до выраженной формы нанизма. Затем присоединяются рахитоподобные изменения костной системы. Однако многие дети погибают до появления развёрнутых рахитоподобных изменений от гипертермии, комы, коллапса.

У части детей изменения костной системы, наоборот, становится главным признаком заболевания. Дети отстают в росте. У них отмечаются искривления трубчатых костей, теменные бугры, деформации грудной клетки, позвоночного столба, гипотония мышц, “чётки” на рёбрах, “рахитические браслеты” и т. д. Клинически и рентгенологически эти явления аналогичны проявлениям рахита, связанным с дефицитом витамина Д. Ø От болезни де-Тони-Дебре-Фанкони цистиноз отличается развитием в более раннем возрасте и более неблагоприятным течением. Ø

ДИАГНОЗ основывается на характерной клинической картине, лабораторных методах исследований: гипераминоацидурия, фосфатурия, глюко-зурия, кальцийурия. Кристаллы цистина могут быть обнаружены в роговице при обследовании щелевой лампой. С помощью биопсии конъюнктивы, почек или пункции лимфатического узла можно установить наличие кристаллов в них. Ø ЛЕЧЕНИЕ цистиноза полностью не разработано. Применяют большие дозы витамина Д (до 100 000 МЕ в сутки), что препятствует прогрессированию рахитоподобных изменений в костях, а также уменьшает аминоацидурию, глюкозурию, фосфат - и кальцийурию. Показано лечение анаболическими гормонами. В борьбе с ацидозом показано назначение цитратной смеси, 4% раствора соды. Применение пенициллина способствует образованию соединения цистина, легко растворимого в воде. Ø ПРОГНОЗ обычно неблагоприятен, через 2 -3 года от начала болезни наступает летальный исход. Ø

ТИРОЗИНОЗ Развитие болезни связано с недостаточностью оксидазы парагидроксифенилпировиноградной кислоты. У здоровых людей этот фермент обеспечивает превращение указанной кислоты в гомогентезиновую. При наличии ферментативного дефекта обмен тирозина нарушается, что приводит к развитию тирозинемии и тирозинурии. В патологический процесс рано вовлекаются печень, почки, костная система (рахитоподобные изменения). Ø Заболевание передается по аутосомнорецессивному типу. Ø

Ø КЛИНИКА. Заболевание начинает проявляться в первые месяцы жизни рвотой, отставанием в физическом развитии, увеличением печени. В связи с развитием цирроза появляются желтуха, асцит, кровоизлияния в кожу. Вследствие поражения почек развивается глюкоамино-фосфат диабет, который служит причиной рахитоподобных изменений костной ткани: остеопороз, остеомаляция, искривления трубчатых костей и т. д. Во многих случаях задерживается умственное развитие.

ДИАГНОЗ основывается на клинических симптомах, раннем появлении признаков печеночной недостаточности, а также на данных биохимического обследования (положительная проба Миллона с мочой, повышение уровня тирозина в плазме крови до 10 мг % и более, наличие парагидроксифенил- пировиноградной кислоты в моче). Отсутствие энзима можно установить гистохимически в пунктатах печени. Ø ДИФФЕРЕНЦИАЛЬНУЮ ДИАГНОСТИКУ проводят с синдромом де-Тони-Дебре-Фанкони, при котором нет значительного поражения печени и отрицательны биохимические пробы на тирозиноз; с наследственным внутриутробным гепатитом, проявляющимся в отличие от тирозиноза уже при рождении; с галактоземией, главным образом, на основании биохимических данных. Ø

Ø ЛЕЧЕНИЕ заключается в ограничении фенилаланина и тирозина в диете и во многом сходно с лечением ФКУ. Ø ПРОГНОЗ неблагоприятен. При отсутствии соответствующего лечения дети погибают в возрасте до 10 лет от печеночной недостаточности.

АЛКАПТОНУРИЯ Ø Ø Заболевание известно более 100 лет. С мочой больных выделяется гомогентензиновая кислота, отсутствующая в норме. В печени и почках больных отсутствует энзим оксидазы гомогентензиновой кислоты, что приводит к ее накоплению и усиленному выделению с мочой. Частота заболевания – 1: 1000000 населения. Заболевание наследуется по аутосомнорецессивному пути. Патогенетический механизм заболевания до конца не изучен.

КЛИНИКА. Заболевание клинически проявляется 3 симптомами: потемнением мочи, пигментацией хрящей и соединительной ткани, артропатией. Ø Моча, имеющая в момент мочеиспускания нормальный цвет, в течение 12 -24 часов на воздухе темнеет. В связи с этим заболевание обнаруживается очень поздно, несмотря на то, что существует с рождения. У ребенка грудного возраста окрашенная моча обнаруживается на пеленках. Она чаще бывает от темно-розового до красного цвета. В детстве этот симптом является единственным проявлением болезни. Серо-голубая пигментация (охроноз) появляется после 20 -30 летнего возраста. Чаще она бывает на ушной раковине и склерах, иногда на носу, спине, шее и руках. После 30 -40 лет возникают суставные симптомы, определяющие тяжесть заболевания. Развивается алкилозирующий «ревматизм» , поражающий чаще позвоночный столб, реже крупные суставы. Он проявляется приступообразными болями и приводит к инвалидизации. Рентгенологическое исследование обнаруживает изменения в межпозвонковых дисках, кальцификаты и остеофиты. Ø Заболевание не сокращает продолжительность жизни Ø

ДИАГНОЗ устанавливается при обнаружении гомогентензиновой кислоты в моче. Ее почернение при добавлении раствора Nа. С 03 достаточно специфично для заболевания. Достоверный диагноз ставится после хроматографического исследования мочи. Ø ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ проводится с порфирией, аргирией, меланомой. Ø ЛЕЧЕНИЕ преимущественно симптоматическое. Ø

ГИСТИДИНЕМИЯ Гистидинемия относится к наследственным нарушениям обмена гистидина и обусловлена отсутствием или же недостаточной активностью фермента гистидазы. Ø Частота заболевания аналогична частоте ФКУ (1 : 7000, 1 : 10000). Ø Заболевание наследуется по разному в зависимости от генетических вариантов заболевания. Ø В результате метаболического блокирования происходит накопление в крови гистидина и его производных и снижение концентрации уроканиновой, глютаминовой и других кислот Ø

КЛИНИКА. Для детей первого года жизни гистидин является незаменимой аминокислотой. При недостатке гистидина отмечается плохая прибавка массы тела, проявления шелушения кожи, экзематозные высыпания и др. Ø При недостатке гистидина у взрослых отмечаются проявления нарушения эритропоэза, отрицательный азотистый баланс, снижение сывороточного альбумина, анорексия, шелушение и сухость кожи, недомогание, эритематозные высыпания и др. Признаки анемии с нарушением эритропоэза объясняются уменьшением образования гемоглобина, в состав которого входит большое количество гистидина. Ø Для больных с гистидинемией характерны светлые волосы и голубые глаза. В клинической картине на первый план выступают поражения нервной системы в виде снижения интеллекта, нарушения речи, судороги, иногда обнаруживается гидроцефалия, гипо- или гипертонус мышц, мозжечковая атаксия. В ряде случаев гистидинемия сочетается с железодефицитной анемией, патологией почек, костной системы и др. Ø

Ø Ø ДИАГНОЗ. К сожалению диагностика доступна только крупным хорошо оснащенным лабораториям, т. к. требует применения современных биохимических методов. Для больных характерна высокая концентрация гистидина в биологических жидкостях. Экскреция гистидина почками повышена. Отмечено увеличение гистидина в ликворе. В связи с возможностью катаболизма гистидина по основному пути, компенсаторно усиливается его превращение в другие метаболиты. В результате повышается экскреция имидазолпировиноградной, имидазол- молочной и имидазолуксусной кислот, что является характерным признаком заболевания. Эти кислоты подобно фенилпировиноградной кислоте реагируют с реактивом Феллинга, но реакция бывает резко положительной. Очень важным специфичным признаком заболевания служит отсутствие метаболитов основного пути обмена гистидина (уроканиновой, глютаминовой и др. кислот). Подтверждает диагноз непосредственное определение активности гистидазы в роговом слое кожи и печени.

Ø Ø Ø Важным признаком заболевания является патологическая реакция на пероральную нагрузку гистидином. После нагрузки уровень гистидина повышается еще в большей степени и достигает до 300 -400 мг/л через 1 -3 часа (N - от 2 до 25 мг/л) и возвращается к исходному уровню не ранее чем через 5 часов. У здоровых после нагрузки уровень гистидина не достигает указанных величин и возвращается к норме через 3 -4 часа. ДИФФЕРЕНЦИРОВАТЬ гистидинемию нужно с ФКУ. ЛЕЧЕНИЕ заключается в назначении малобелковой диеты со сниженным содержанием гистидина. ПРОГНОЗ заболевания зависит от генетических вариантов заболевания.

ГОМОЦИСТИНУРИЯ Ø Ø Ø Ø В основе заболевания лежит отсутствие или снижение активности фермента цистатионинсинтетазы, что обусловливает нарушение в обмене метионина. У больных обнаруживается повышение в крови концентрации метионина и гомоцистина (отсутствующего в норме) и снижение цистина, появление в моче гомоцистина и цистеина. Заболевание наследуется по аутосомно-рецессивному пути. Заболевание проявляется марфаноподобными синдромами. Симптомокомплекс гомоцистинурии: 1) аномалии скелета: диспропорциональность телосложения в виде укорочения туловище, удлинения конечностей, воронкообразная грудная клетка, нарушение осанки, “крыловидные” лопатки, “башенный” череп, неправильный прикус и рост зубов, высокое нёбо, вальгусная деформация коленных суставов, ограничение подвижности суставов, плоскостопие, остеопороз, склонность к переломам; 2) изменения нервной системы: снижение интеллекта, обедненная речь, дизлалия, спастическая походка, эписиндром; 3) нарушение зрения: подвывих хрусталика, вторичная глаукома, изменение глазного дна; 4) со стороны сердечно-сосудистой системы: нарушение обменных процессов в миокарде, склонность к артериальным и венозным тромбозам; 5) внешние признаки: светлые, мягкие, вьющиеся крупными завитками волосы, голубой цвет радужной оболочки.

Ø Ø Ø Ø Гомоцистинурия генетически гетерогенна. Помимо классической, встречаются ещё 2 формы: с дефицитом витамина В 6 и с нарушением метаболизма фолиевой кислоты. ДИАГНОЗ основывается на определении метионина и цистина в сыворотке крови и моче, определении активности цистатионинсинтетазы в печени. ДИФФЕРЕНЦИАЛЬНУЮ ДИАГНОСТИКУ нужно проводить с болезнью Марфана (нарушение соединительнотканного обмена). Для болезни Марфана больше характерны: 1) поражение митрального и аортального клапанов; 2) мышечная дистрофия; 3) интеллект не всегда снижен, эписиндром отсутствует. ЛЕЧЕНИЕ состоит в назначении диеты, обогащенной цистином и лишенной метионина. Эффект лечения зависит от срока назначения терапии. Получены также удовлетворительные результаты от лечения пиридоксином, стимулирующим другие пути метаболизма серосодержещих аминокислот. Терапевтический эффект витамина В 6 связан с повышением активности цистатионинсинтетазы

АЛЬБИНИЗМ Группа заболеваний, в основе которых лежит наследственный дефект метаболизма меланина, приводящий к снижению или отсутствию пигмента в коже, слизистых оболочках, волосах, глазах. Меланин играет роль защиты поверхностных сосудов и ядер мальпигиевых клеток от солнечной радиации. Меланин образуется главным образом из тирозина. Этот многоэтапный процесс последовательно катализируется рядом ферментов: тирозиназой, пероксидазой и другими. Ø Различают следующие клинические формы альбинизма: глазнокожный, глазной и кожный. Ø Глазно-кожный альбинизм наследуется по аутосомно-рецессивному типу. Существуют несколько форм этого типа: альбинизм глазнокожный неполный, синдром Чедиака-Хигаши; альбинизм полный совершенный, альбинизм I типа; альбинизм II типа; альбинизм с геморрагическим диатезом пигментацией ретикуло-эндотелиальных клеток, синдром Германски-Пудлака. Ø Частота альбинизма колеблется от 1: 5000 до 1: 40 000 населения Ø

Ø КЛИНИКА. Окраска кожи и волос молочно-белая. Радужная оболочка в косо падающем свете выглядит прозрачно-серой или голубой. Характерны светобоязнь и нистагм. В прямом свете выражен красный зрачковый рефлекс. Пигмент на глазном дне отсутствует. Полное отсутствие пигмента в коже определяет её повышенную чувствительность к солнечным лучам.

Кожный альбинизм. Различают; кожный альбинизм с гиперпигментацией и глухотой (синдром Ципрковского-Марголиса); кожный альбинизм с глухотой (синдром Ваарденбурга). Ø Кожный альбинизм наследуется по аутосомно-доминантному типу. Ø КЛИНИКА. Характеризуется врождёнными депигментированными пятнами определённой локализации: на голове в виде треугольника с основанием у бровей и вершиной в области волос; в центре подбородка, на передней поверхности туловища – от сосков до подвздошных ямок; на руках – от предплечья до запястья. В местах депигментации могут быть пигментированные островки с гиперпигментированной границей. Ø

Кожный альбинизм с гиперпигментацией и глухотой (Ципрковского – Марголиса синдром) наследуется сцепленно с Х-хромосомой рецессивно. Ø КЛИНИКА. Проявляется при рождении общей депигментацией волос кожи за исключением ягодиц и мошонки. В последующем на конечностях появляются круглые, овальные или неправильной формы, разной величины симметричные очаги гиперпигментации. Очаги могут быть также на туловище, но не на лице и не в волосах, которые остаются светлыми. Окраска пятен может быть от светло-жёлтой до тёмно-коричневой и создаёт впечатление “леопардовой шкуры”. Нистагм, фотофобия и другие симптомы глазного альбинизма отсутствуют. У всех больных отмечается врождённая неврогенная глухота. Ø Кожный альбинизм с глухотой (Ваарденбурга синдром) наследуется аутосомно-доминантно с различной экспрессивностью и составляет 1 -2 % всех случаев врождённой глухоты. Ø

Глазной альбинизм. Наследуется сцепленно с Х-хромосомой рецессивно. КЛИНИКА. Характеризуется отсутствием пигмента только в глазах, тогда как в коже и в волосах он присутствует в нормальном количестве или снижен. Радужные оболочки слегка пигментированы. Пигментация глазного дна весьма незначительна, что видны хориоидальные сосуды. Ø Наблюдаются светобоязнь, нистагм. Иногда глазной альбинизм сочетается с нарушением цветового зрения. У гетерозиготных женщин наблюдается повышенная прозрачность радужных оболочек и мозаичная окраска глазного дна либо нарушение цветового зрения. Ø ЛЕЧЕНИЕ альбинизма не разработано. Рекомендуется ношение тёмных очков, избегать пребывания на солнце. Ø Ø Ø

МУКОВИСЦИДОЗ Ø Ø Ø «Если при поцелуе ребенка ощущается соль, значит, он скоро умрет» - так писали в старых немецких книгах по медицине про детей, больных муковисцидозом. В настоящее время больные живут более 20 лет, т. е. на 10 лет больше, чем раньше. Муковисцидоз – это самое распространненое наследственное заболевание. Носителем муковисцидоза является каждый 25 й европеец. Заболевание относится к наследственным болезням обмена веществ. При этом заболевании нарушается деятельность всех экзокринных желез организма (потовые, слезные, слюнные, железы дыхательной системы и пищеварительного тракта). Частота болезни в популяциях различная. В среднем встречается с частотой 1: 2500, 1: 5000. Около 96% больных муковисцидозом погибают от легочной патологии. Тип наследования – аутосомно-рецессивный.

Проявляется болезнь в периоде новорожденности и у детей раннего возраста. Для заболевания характерно повышения вязкости панкреатического и бронхиального секрета, а также желчи, что влечет за собой нарушение проходимости выводных протоков. В процесс вовлекаются слизистые, потовые и слюнные железы. Содержание натрия в слюне и поте повышается 2 – 5 раз, что патогномично для этой болезни. Ø Признаком муковисцидоза у новорожденных является мекониальный илеус. Клиническая картина связана с повышением вязкости первородного кала. Он закупоривает просвет кишки, ккак пробкой, что приводит к явлениям полной низкой кишечной непроходимости (т. е. непроходимости в нижних отделах кишечника). Заболевание носит наследственный характер и вызвано нарушением обмена веществ. Ø Симптомы и течение довольно характерны: рвота с первого дня жизни, в начале с примесью желчи, затем коричневого цвета – «каловая» , живот резко вздут, стул отсутствует. Возможны осложнения в виде заворота кишечника, нарушения целостности его стенки с последующим развитием перитонита Ø

Ø Ø При несвоевременной постановке диагноза, особенно, если непроходимость частичная, наступает интоксикация организма и ухудшение состояния уже в предоперационном периоде, что сказывается на состоянии после операции и обусловливает высокую смертность. При легочной форме у детей грудного возраста отмечаются бледность, недостаточная прибавка в массы, иногда с первых дней жизни появляется кашель постепенно усиливающийся, который сопровождается цианозом, одышкой. Часто кашель заканчивается рвотой. В легких обычно выслушивается масса сухих хрипов. Влажные хрипы появляются при длительном течении заболевания. Мокрота больных вязкая, трудно отделимая. При кишечной форме дети резко теряют в весе, появляется неоднократная рвота после кормления, испражнения обычно обильные зловонные, живот вздут, метеоризм. ДИАГНОСТИКА. Для диагностики определение концентрации хлора и натрия в поте методом электрофореза с пилокарпином. Существенно обнаружение повышения вязкости дуоденального содержимого, снижение активности липазы, трипсина, диастазы. Клинико-генеалогический анализ позволяет определить наследственный характер заболевания, тип наследования и прогноз.

ЛЕЧЕНИЕ. При меконеальном илеусе обычно проводится хирургическое лечение. Дальнейший прогноз зависит от сроков оперативного вмешателььства (чем раньше, тем лучше) и от состояния ребенка. Ø При частичной непроходимости в начале следует попытаться растворить меконий с помощью 5% раствора панкреатина, введенного через рот и с помощью клизмы в кишку. Можно также применить гастрографин – вещество, применяемое для рентгенологических исследований ЖКТ. Имеются указания на эффективность этого метода. Ø При легочной форме обычно антибиотикотерапия малоэффективна. В основном рекомендуется разжижающие мокроту (дорназа – снтезированный генно-инженерным путем природный фермент человека для разжижения мокроты) и бронхорасширяющие препараты в сочетании с кинезитерапией (специальный комплекс упражнений и дыхателььной гимнастики, позволяющий очистить бронхи). Антибиотики назначаются присоединении бактериальной инфекции. Ø При кишечной форме рекомендуется диета, бедные жирами и богатая белками, обильное питье (соки, компоты, минеральные воды). В рационе больных увеличивают поваренную соль, учитывая потерю хлоридов с потом. Назначают большие дозы пищеварительных ферментов (уреодеоксихолевая кислота, микросферические ферменты, замещающие работу поджелудочную железу) и жирорастворимых витаминов. Ø

Болезни нарушения обмена углеводов Ø Углеводы поступают в организм в виде моносахаридов (глюкоза, фруктоза), дисахаридов (лактоза, мальтоза, сахароза) и полисахаридов (гликоген, крахмал). В первые месяцы жизни основным углеводом пищи является дисахарид лактоза, или молочный сахар, состоящий из глюкозы и галактозы. Содержание лактозы в женском молоке составляет в среднем 70 г/л, в коровьем - 48 г/л. Центральное место в углеводном обмене занимает глюкоза. Дисахариды и полисахариды подвергаются расщеплению в ЖКТ до моносахаридов. Галактоза преобразуется в глюкозу в печени и эритроцитах. Ключевое значение в этом процессе имеет фермент галактоза -1 - фосфат-уридилтрансфераза

ГАЛАКТОЗЕМИЯ Ø Ø Галактоземия относится к группе аномалий обмена углеводов, для которых характерны поражения центральной нервной системы, мышечной системы, нарушения функции печени, аномалии эритроцитов, гипогликемические состояния. Типичный вариант галактоземии наследуется аутосомнорецессивно. Частота заболевания составляет приблизительно 1: 30 000 новорожденных, но по данным разных авторов она колеблется от 1: 8000 до 1: 187000 населения. В основе первичного биохимического дефекта при галактоземии лежит дефицит фермента галактоза-1 фосфатуридилтрансферазы (ГА-1 -ФУТ), в результате чего в тканях организма накапливается избыточное количество галактоза-1 -фосфата и других продуктов неполного распада лактозы, вызывающих клинические проявления галактоземии

Ø Ø Кроме классического типа галактоземии встречаются ещё 2 варианта: форма Дуарте с 50% активностью фермента и негритянский тип, при котором активность фермента снижена лишь в некоторых клетках (эритроциты, фибробласты). КЛИНИКА может быть различной степени тяжести. Наиболее лёгкие случаи обнаруживаются в семьях, где имеются больные галактоземией. Такие дети рано отказываются от груди и плохо переносят молоко. При наиболее тяжелой форме клинические проявления выявляются в первые дни после рождения. Масса тела детей при рождении, как правило, бывает большая (свыше 4 кг). У больных после кормления грудью возникает обильная и упорная рвота, понос, уменьшение массы тела, развивается желтуха, нарастает гепатомегалия, возникают кровотечения и геморрагии на коже. Часто отмечаются гипогликемия, судороги, в дальнейшем появляется катаракта, признаки цирроза печени и отставание в нервно-психическом и физическом развитии

Ø ДИАГНОЗ. Наличие большого числа фенокопий и сложность биохимических методов диагностики галактоземии объясняют тот факт, что заболевание не всегда распознается своевременно. Часто дети с галактоземией поступают в клинику с диагнозом сепсис, билиарный цирроз печени, острые расстройства пищеварения, затяжная желтуха новорожденных т. д. Целый ряд заболеваний периода новорожденности обладает сходством клинических проявлений с галактоземией; гемолитическая болезнь новорожденных, врожденный гепатит, атрезия желчных путей, цитомегалия, врожденный токсоплазмоз, наследственные гипербилирубинемии (типа Криглера – Найяра) и т. д. Необходимость проведения дифдиагностики может возникнуть при затяжной желтухе недоношенных и новорожденных. Установление точного диагноза галактоземии требует комплекса диагностических методов. Обнаружение галактозы в моче новорожденного ребенка служит основанием для его комплексного обследования на галактоземию. Наиболее надежными диагностическими методами являются определение концентрации галактозы в крови с помощью хроматографии на бумаге, прямое определение активности фермента галактоза-1 - фосфат - уридилтрансферазы (ГА-1 -ФУТ) в эритроцитах и определение галактозы в моче. Кроме этого в диагностике может оказать помощь правильно собранный семейный анамнез.

Ø ЛЕЧЕНИЕ. С первых дней жизни ребёнок должен быть переведён на безмолочную диету. В качестве заменителей молока можно использовать смеси, приготовленные на миндальном и соевом молоке

ГЛИКОГЕНОЗЫ Ø Ø Ø Ø Под этим общим названием объединяется группа заболеваний, для которых свойственно накопление гликогена в органах и тканях, связанное с нарушением активности одного из ферментов, участвующих в обмене гликогена. Заболевания наследуются по аутосомно-рецессивному пути. Частота гликогенозов всех типов составляет 1: 40000 населения. Наиболее хорошо описаны 6 типов гликогенозов, хотя их существует значительно больше. КЛИНИКА. Общими клиническими симптомами являются: начало болезни в детском возрасте, симптомы гипогликемии (рвота, судороги, потеря сознания, кома). Гликоген наиболее интенсивно накапливается в тех органах, в которых он синтезируется, т. е. в печени, почках и мышцах. В зависимости от того какой орган наиболее вовлечен в патологический процесс, различают 3 основные формы заболевания: 1. Печеночная 2. Мышечная 3. Генерализованная

Печеночная форма Признаки заболевания проявляются обычно на первом году жизни, хотя развитие ребенка в этом периоде протекает нормально или несколько замедляется. Начиная с 8 -9 месяцев жизни 1 раз в 2 месяца, либо чаще отмечаются приступы гипогликемии (потеря сознания, клонические судороги конечностей). Приступы начинаются до еды или рано утром, их появление можно предотвратить приемом сладкой воды. Ø Внешний вид больных: маленький рост, большой живот, непропорционально худые конечности, « кукольное лицо » . Печень бывает увеличенной. Наиболее тяжело заболевание протекает в возрасте 4 -5 лет. Интеркуррентные заболевания утяжеляют течение основного патологического процесса. Ø С возрастом состояние больных может улучшиться, что можно объяснить развитием компенсаторных механизмов обмена. Интеллект как правило не нарушается. Ø Ø

Мышечная форма Ø Основные симптомы этой формы заболевания проявляются с 7 - 10 лет. Больные становятся малоподвижными, быстро утомляются при физической нагрузке. В дальнейшем мышечная слабость прогрессирует. Появляются боли в интенсивно работающих мышцах после длительных физических упражнений, отмечается тахикардия, одышка. Перечисленные симптомы в основном появляются к 25 -35 годам. Внешний вид больных обычно не изменяется. Границы сердца обычно расширяются. Со стороны печени и почек выраженных изменений не бывает. Ø Прогноз заболевания в основном благоприятен, хотя и известны летальные исходы в возрасте 25 -30 лет. Ø

Ø Ø Ø Ø Ø Генерализованная форма Эта форма гликогенозов характеризуется тем, что практически во всех органах и тканях больного накапливается значительное количество гликогена. Клиническая картина этой формы не похожа на картину печеночной и мышечной форм. К этой форме относятся биохимические типы гликогеноза III и IY типов (болезни Кори и Андерсена). Биохимические типы гликогенозов: 1. Болезнь Гирке (I тип) - дефицит фермента глюкоза-6 фосфатазы. 2. Болезнь Помпе (II тип) - дефицит фермента кислая глюкозидазы. 3. Болезнь Кори (Ш тип) - дефицит фермента 1, 6 -глюкозидазы. 4. Болезнь Андерсена (IY тип) - дефицит ветвящего фермента. 5. Болезнь Мак-Ардля (Y тип) - дефицит фермента фосфорилазы мышц. 6. Болезнь Герса (YI тип) - дефицит фермента фосфорилазы печени.

БОЛЕЗНЬ ГИРКЕ (I тип) Клиническая картина болезни обусловлена в основном отсутствием активности специфического фермента глюкозо-6 -фосфатазы в печени и слизистой кишечника, а в некоторых случаях и в почках. Клиническую картину болезни обусловливает в основном нарушение обмена гликогена в печени. Клиническая картина болезни очень похожа на печеночную форму болезни, которая была описана выше. В период новорожденности кардинальными симптомами являются гипогликемические судороги и гепатомегалия. Задержка роста начинает отмечаться с 1 -го года жизни. Характерен внешний вид больных: большая голова, «кукольное лицо» , короткая шея, большой живот. Особенностью этого типа гликогеноза является то, что у детей в возрасте 5 -7 лет бывают геморрагические высыпания, а также частые носовые кровотечения. В 10% случаев имеется ксантоматоз. Ø Заболевание наследуется по аутосомно-рецессивному типу Ø

БОЛЕЗНЬ ПОМПЕ (II тип) Заболевание обусловлено отсутствием фермента – кислая альфа - глюкозидаза или гамма – амилазы в печени и мышцах, что приводит к деструктивным изменениям тканей и, в первую очередь, интенсивно работающих мышц, таких, как мышцы сердца. Ø Болезнь, как правило, проявляется с первого года жизни в виде сипмтомо-комплекса сердечной недостаточности. Вскоре после рождения развивается беспокойство ребенка, появляется нарастающий цианоз, расстройство дыхания. При обследовании обнаруживается «шаровидное» сердце, гепатомегалия, умеренная гипертрофия мышц, макроглоссия. В отличие от гликогеноза I типа не отмечаются гипогликемия и ацидоз. Больные дети погибают на 1 году жизни. Ø При легкой форме болезни Помпе отсутствует активность альфаглюкозидазы только в мышцах. В этих случаях заболевание, как правило, проявляется в более позднем возрасте и по клинической картине сходно с миопатией. Прогноз при этой форме различен, возможен летальный исход. Ø

Ø ЛЕЧЕНИЕ гликогенозов недостаточно разработано. Применение адреналина, гидрокортизона, способных в норме повышать сахар в крови за счет распада гликогена оказалось неэффективным. Некоторыми авторами рекомендуется использование глюкагона и малых доз тиреоидина. Большое значение уделяют диетотерапии, которая заключается в увеличении в рационе больных легкоусвояемых углеводов и в учащении приема пищи

ФРУКТОЗЕМИЯ Причиной заболевания является дефицит фермента фруктозо - I- моно-фосфатальдолазы в печени, почках, слизистой оболочке, а также снижение активности фруктозо-1, 6 -дифосфатальдолазы. Изменение одного фермента влияет на другого. Дефицит указанных ферментов приводит к накоплению в крови и тканях фруктозы и фруктозо-I-фосфата, обладающих токсическим действием и определяющих симптоматику заболевания. Наиболее тяжелые патоморфологические изменения наступают в печени: цирроз, стеатоз, некроз клеток. Ø Частота заболевания- 1: 130000 населения. Ø Заболевание наследуется по аутосомно-рецессивному типу. Ø

КЛИНИКА. Болезнь проявляется в период, когда грудным детям дают фруктовые соки, сахар или при раннем переводе детей на смешанное и искусственное вскармливание. У детей наблюдается упорная анорексия, рвота, гипотрофия, гепатомегалия и желтуха, которые отмечаются при тяжелой форме болезни. При доброкачественной форме в раннем детстве наблюдаются только желудочно-кишечные расстройства и затруднения при кормлении. Дети отказываются от продуктов, содержащих глюкозу. С возрастом больные начинают легче переносить небольшие количества продуктов, содержащих фруктозу. При увеличении количества фруктозы в рационе состояние больных ухудшается из-за гипогликемии и гиперфруктоземии. Ø ДИАГНОЗ основывается на обнаружении в моче фруктозы с помощью реакции Селиванова. Ø

ДИФФЕРЕНЦИАЛЬНУЮ ДИАГНОСТИКУ нужно проводить с галактоземией, в отличие от которой при фруктоземии не развивается катаракта, дети хорошо переносят молоко, значительно меньше выражена умственная отсталость. Ø ЛЕЧЕНИЕ. Детям назначают диету, не содержащую фруктозу в течение первых лет жизни: тростниковый сахар, сахарная свекла, мед, яблоки, груши, слива, арбуз, клубника, апельсины, морковь, репа, какао. В дальнейшем по мере повышения толерантности к фруктозе рацион больных можно постепенно расширять. Ø

Болезни нарушения обмена липидов Роль липидов в жизнедеятельности организма человека велика. Ø Известно, что на разных этапах онтогенеза липидный обмен имеет свои особенности. У детей раннего возраста для нормального течения процессов роста и развития очень велика потребность в пластическом и энергетическом материалах. При этом, чем моложе организм, тем потребность выше. В связи с этим большое значение в липидном обмене принадлежит качественному составу пищи. Ø Одной из особенностей организма ребенка раннего возраста является склонность к кетозу, т. е. накоплению в тканях кетоновых тел. Ø

Нарушения липидного обмена являются частым спутником патологических процессов у детей. По своему генезу они могут быть разделены на 2 группы: Ø Наследственные и приобретенные заболевания. Ø Наследственные дефекты обмена липидов делят на 2 группы: Ø 1). Липидозы или сфинголипидозы – болезни нарушения катоболизма структурных липидов, приводящих к накоплению сфинголипидов в клетках разных тканей; Ø 2). Болезни, обусловленные с нарушением обмена липидов, содержащихся в крови. Ø

Выделяют около 10 сфинголипидозов, для которых выяснен биохимический дефект. Большинство из этих форм имеют сходную клиническую картину, обусловленную нарушением катоболизма разных, но близких по структуре сфинголипидов. Клиническая картина характеризуется прогрессирующим слабоумием, двигательными расстройствами, поражением костей, внутренних органов (печени, селезенки, почек), кожи и сетчатки глаз. Ø Значение липопротеидов в организме заключается в транспорте и распре-делении по органам холестерина и триглицеридов. Метаболизм липопротеидов не только находится под контролем генетических факторов, но и в значительной степени зависит от характера питания. Поэтому расстройства обмена липидов плазмы крови представляют собой сложную группу состояний, из которой лишь в последние годы стали вычленять моногенно обусловленные формы. Гиперлипопротеидемия является важным фактором развития атеросклероза и ишемической болезни сердца. Для большинства форм гиперлипопротеидемий характерно ранее (в возрасте 15 -20 лет) развитие атеросклеротического процесса с клинической картиной стенокардии, инфаркта миокарда, ксантоматоза. Большинство гиперлипопротеидемий наследуется по аутосомнорецессивному типу. Ø

Клинические симптомы и биохимические изменения, характерные для гиперлипопротеидемии, весьма вариабельны и могут изменяться под влиянием перемены диеты и других факторов. Поэтому диагноз может быть поставлен на основании всего комплекса клинических симптомов заболевания, данных анамнеза и лабораторных обследований. Ø Наследственные нарушения обмена липидов привлекли к себе внимание исследователей тем, что они обуславливают развитие атеросклероза и других форм сердечно-сосудистой патологии. Согласно статистике, ишемическая болезнь сердца (ИБС) занимает одно из первых мест в структуре заболеваемости и смертности населения. Четкая взаимосвязь между гиперлипидемией и повышенным риском развития ИБС неоднократно подтверждалась разными исследователями. Ø Степень риска находится в определенной зависимости от уровня холестерина в крови. Частота этого заболевания в популяции считается довольно высокой – от 7 до 28%. Ø

АМАВРОТИЧЕСКАЯ ИДИОТИЯ ТЕЯ – САКСА Амавротическая идиотия Тея - Сакса преимущественно встречается среди евреевашкенази. Ø Частота заболевания составляет 1: 6000 среди евреев-ашкенази и 1: 500000 среди других национальностей. Частота гетерозиготных носителей рецессивного гена среди евреев-ашкенази составляет 1: 40, среди других национальностей – 1: 380. У гетерозиготных носителей патологического гена снижена активность фермента гексозаминидазы А и содержание сфингомиелина и кефалина в эритроцитах. Ø Заболевание наследуется по аутосомнорецессивному типу. Ø

Ø КЛИНИКА. Заболевание начинает проявляться в возрасте 4 -6 месяцев. Ребенок, ранее активный, постепенно утрачивает интерес к окружающему миру, перестает смеяться, играть, узнавать родителей. Рано обнаруживается снижение зрения. Ребенок не может фиксировать взгляд. На глазном дне обнаруживается симптом «вишневой косточки» . В последующем развивается атрофия зрительного нерва и слепота. У детей наблюдается снижение интеллекта до уровня идиотии. Двигательные нарушения приводят к полной обездвиженности. Дети вздрагивают от резкого звука, могут отмечаться судороги. В конечной стадии болезни развиваются кахексия и состояние децеребрационной ригидности. Смерть в среднем наступает через 1, 5 - 2 года после начала заболевания

Ø ДИАГНОЗ. В плазме крови больных повышено содержание холестерина, снижено количество и гликолипидов. В эритроцитах больных также повышается уровень холестерина, а количество фосфолипидов снижается. У больных активность фермента глутаминщавелевоуксусной трансаминазы повышена в 3 -4 раза, активность фермента фруктозо- Iфосфатальдолазы снижена.

БОЛЕЗНЬ НИМАННА-ПИКА Эта форма сфинголипидоза представляет собой сравнительно частый и тяжелый липидоз, который встречается в 50% случаев среди евреев-ашкенази. Заболевание связано с врожденным дефицитом энзима сфингомиелинидазы. Энзимный блок приводит к накоплению сфингомиелина в тканях. При этом сфингомиелин и холестерол накапливается почти во всех органах и тканях с преимущественным поражением ЦНС, селезенки, печени, костного мозга, легких и др. Ø Заболевание наследуется по аутосомнорецессивному типу. Ø

КЛИНИКА. Заболевание начинает проявляться в первые месяцы после рождения диспепсическими нарушениями, ухудшением общего состояния, обильным потом, похуданием, частыми легочными осложнениями. Для заболевания характерна коричневатая или серо-желтоватая пигментация на коже и слизистых оболочках. На языке и деснах часто наблюдаются чернильно-синие пятна. Ведущим синдромом является гепатоспленомегалия. Часто отмечается генерализованное увеличение лимфатических узлов, остеопороз. Ø Неврологический синдром характеризуется мышечной гипертонией и исчезновением двигательной активности. Постепенно наступает психическая деградация, достигающая полной идиотии. На глазном дне отмечается ярко-красное пятно, характерное для амавротической идиотии Тея. Сакса. Слух постепенно ослабевает до полной глухоты. Болезнь непрерывно прогрессирует и заканчивается смертью через несколько лет Ø

БОЛЕЗНЬ ГОШЕ КЛИНИЧЕСКАЯ КАРТИНА. Известны 3 клинических форм этого заболевания, различающиеся временем начала и преобладанием той или иной симптоматики. При раннем начале доминируют неврологические нарушения. С рождения отмечается выраженная гипотрофия, бульбарные расстройства, беззвучный крик (афония), нарушение глотания (дисфагия), тризм, отвисание нижней челюсти. Смерть наступает от аспирации пищевых масс, пневмонии. Ø У детей более старшего возраста и у взрослых в клинической картине доминирует увеличение селезёнки, геморрагический синдром, анемия. Ø

Печень умеренно увеличена. Костные изменения проявляются в виде болей, деформаций, патологических переломов. Появляются мышечная ригидность, нарушение координации движений, судороги. Болезнь медленно прогрессирует. В терминальной стадии появляются тяжелые неврологические симптомы. Больные доживают до 20 -30 лет и умирают от кахексии, кровоизлияния. Ø Тип наследования – аутосомно-рецессивный. Ø ДИАГНОЗ основывается на клинической картине, обнаружении метаболического дефекта, обусловленного отсутствием фермента гликозидазы. Ø

Больные брат и сестры с ФКУ
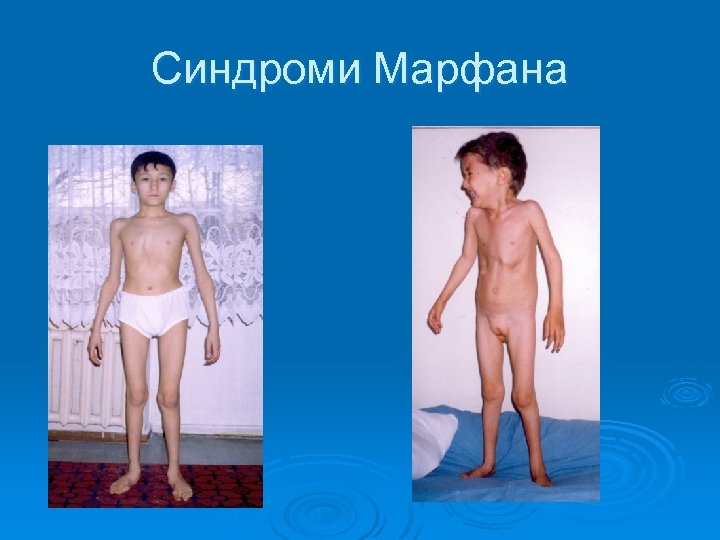
Синдроми Марфана
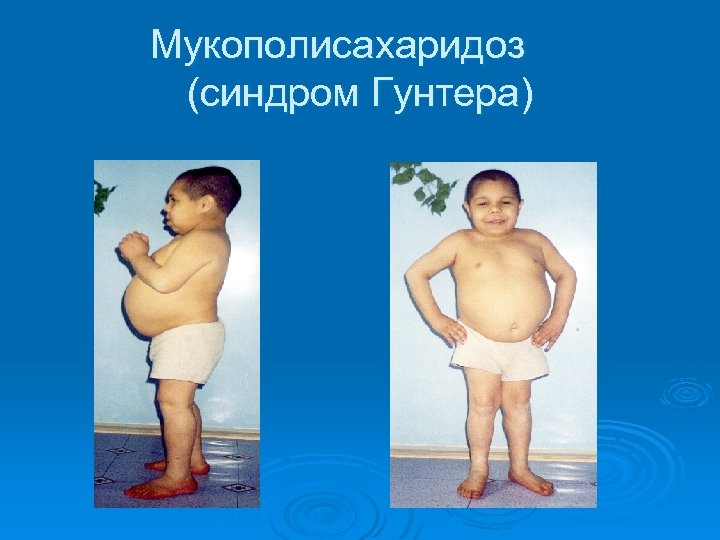
Мукополисахаридоз (синдром Гунтера)
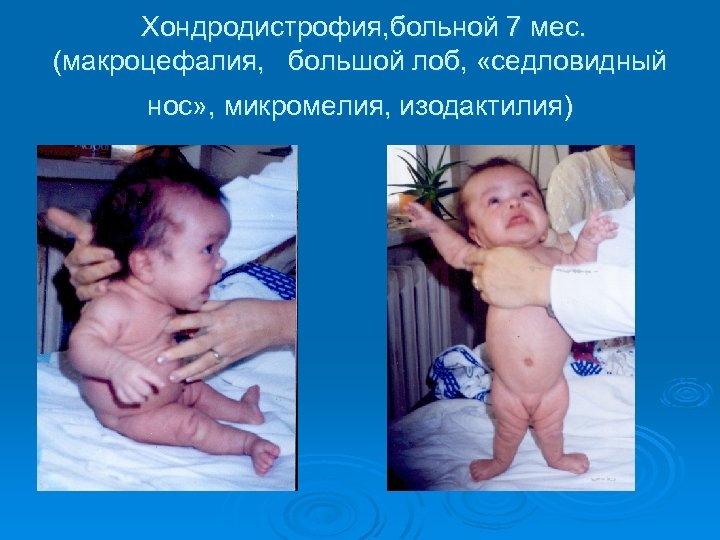
Хондродистрофия, больной 7 мес. (макроцефалия, большой лоб, «седловидный нос» , микромелия, изодактилия)

9 ёшли бемор наслий гидроцефалия.

БЛАГОДАРЮ ЗА ВНИМАНИЕ!
a4f597837a93a7524be12a94c13b6ac7.ppt