2011_inorg_medbiol_3.ppt
- Количество слайдов: 40
 Третья лекция 1
Третья лекция 1
 VII группа периодической системы 2
VII группа периодической системы 2
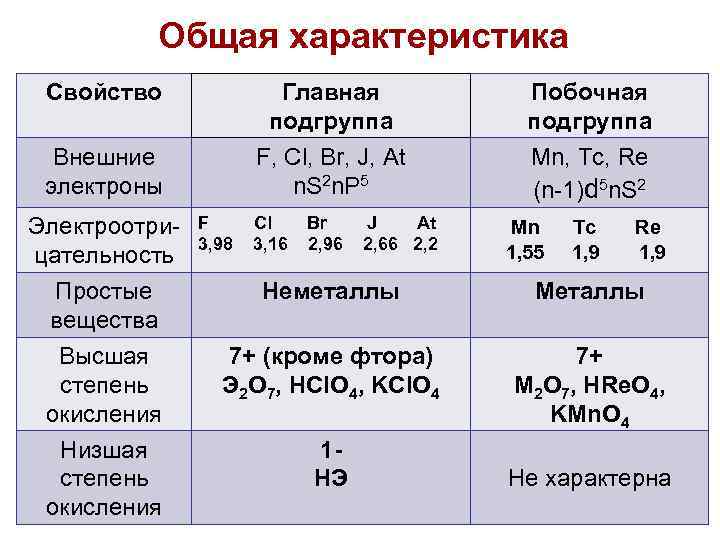 Общая характеристика Свойство Главная подгруппа F, Cl, Br, J, At n. S 2 n. P 5 Внешние электроны Электроотрицательность Простые вещества Высшая степень окисления Низшая степень окисления F 3, 98 Cl 3, 16 Br 2, 96 J At 2, 66 2, 2 Побочная подгруппа Mn, Tc, Re (n-1)d 5 n. S 2 Mn 1, 55 Tc 1, 9 Re 1, 9 Неметаллы Металлы 7+ (кроме фтора) Э 2 О 7, HCl. O 4, KCl. O 4 7+ M 2 О 7, HRe. O 4, KMn. O 4 1 НЭ Не характерна 3
Общая характеристика Свойство Главная подгруппа F, Cl, Br, J, At n. S 2 n. P 5 Внешние электроны Электроотрицательность Простые вещества Высшая степень окисления Низшая степень окисления F 3, 98 Cl 3, 16 Br 2, 96 J At 2, 66 2, 2 Побочная подгруппа Mn, Tc, Re (n-1)d 5 n. S 2 Mn 1, 55 Tc 1, 9 Re 1, 9 Неметаллы Металлы 7+ (кроме фтора) Э 2 О 7, HCl. O 4, KCl. O 4 7+ M 2 О 7, HRe. O 4, KMn. O 4 1 НЭ Не характерна 3
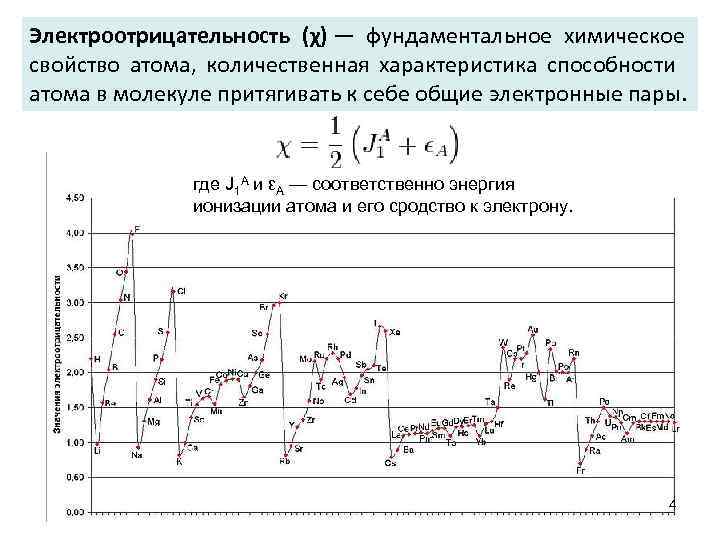 Электроотрицательность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле притягивать к себе общие электронные пары. где J 1 A и εA — соответственно энергия ионизации атома и его сродство к электрону. 4
Электроотрицательность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле притягивать к себе общие электронные пары. где J 1 A и εA — соответственно энергия ионизации атома и его сродство к электрону. 4
 ГАЛОГЕНЫ 5
ГАЛОГЕНЫ 5
 Распространенность в природе • F Cl Br J At ( 1/2 (210 At) = 8, 1 часа) • Ca. F 2 – плавиковый шпат (флюорит) • Na. Cl – галит, KCl·Na. Cl – сильвинит, KCl·Mg. Cl 2· 6 H 2 O - карналлит, Na. Br, Na. J – месторождения и природные воды • Na. JO 3 – в месторождениях нитратов щелочных металлов 6
Распространенность в природе • F Cl Br J At ( 1/2 (210 At) = 8, 1 часа) • Ca. F 2 – плавиковый шпат (флюорит) • Na. Cl – галит, KCl·Na. Cl – сильвинит, KCl·Mg. Cl 2· 6 H 2 O - карналлит, Na. Br, Na. J – месторождения и природные воды • Na. JO 3 – в месторождениях нитратов щелочных металлов 6
 Открытие элементов • F 2 - открыт в 1886 г. , Муассан (Франция) • Cl 2 - открыт в 1774 г. Шееле (Швеция) • Br 2 – открыт в 1825 г. , Левиг (Германия) или Ж. Балар (Франция) в 1826 г. • J 2 – открыт в 1811 г. , Куртуа (Франция) – фабрикант производства мыла и соды; название дал Гей-Люссак в 1813 г. • At – открыт в 1940 г. Д. Корсон, К. Мак-Кензи и Э. Сегре (США); получен в циклотроне по ядерной реакции при бомбардировке Bi мишени частицами 7
Открытие элементов • F 2 - открыт в 1886 г. , Муассан (Франция) • Cl 2 - открыт в 1774 г. Шееле (Швеция) • Br 2 – открыт в 1825 г. , Левиг (Германия) или Ж. Балар (Франция) в 1826 г. • J 2 – открыт в 1811 г. , Куртуа (Франция) – фабрикант производства мыла и соды; название дал Гей-Люссак в 1813 г. • At – открыт в 1940 г. Д. Корсон, К. Мак-Кензи и Э. Сегре (США); получен в циклотроне по ядерной реакции при бомбардировке Bi мишени частицами 7
 МУАССАН (Moissan), Анри 28 сентября 1852 г. – 20 февраля 1907 г. В 1906 г. Муассану была присуждена Нобелевская премия по химии «за большой объем проделанных им исследований, за получение элемента фтора и введение в лабораторную и промышленную практику электрической печи, названной его именем» . Поскольку фтор и его соединения высокотоксичны, они серьезно подрывали здоровье исследователей. Позднее Муассан так отозвался об этом периоде: «Фтор отнял у меня 10 лет жизни» . 8
МУАССАН (Moissan), Анри 28 сентября 1852 г. – 20 февраля 1907 г. В 1906 г. Муассану была присуждена Нобелевская премия по химии «за большой объем проделанных им исследований, за получение элемента фтора и введение в лабораторную и промышленную практику электрической печи, названной его именем» . Поскольку фтор и его соединения высокотоксичны, они серьезно подрывали здоровье исследователей. Позднее Муассан так отозвался об этом периоде: «Фтор отнял у меня 10 лет жизни» . 8
 Нобелевский диплом Муассана 9
Нобелевский диплом Муассана 9
 Происхождение названий F – греческое фторос – разрушение, гибель Cl – греческое хлорос – желто-зеленый Br - греческое бромос – зловонный J – греческое иоэдес – темно-синий At – греческое астатос – неустойчивый 10
Происхождение названий F – греческое фторос – разрушение, гибель Cl – греческое хлорос – желто-зеленый Br - греческое бромос – зловонный J – греческое иоэдес – темно-синий At – греческое астатос – неустойчивый 10
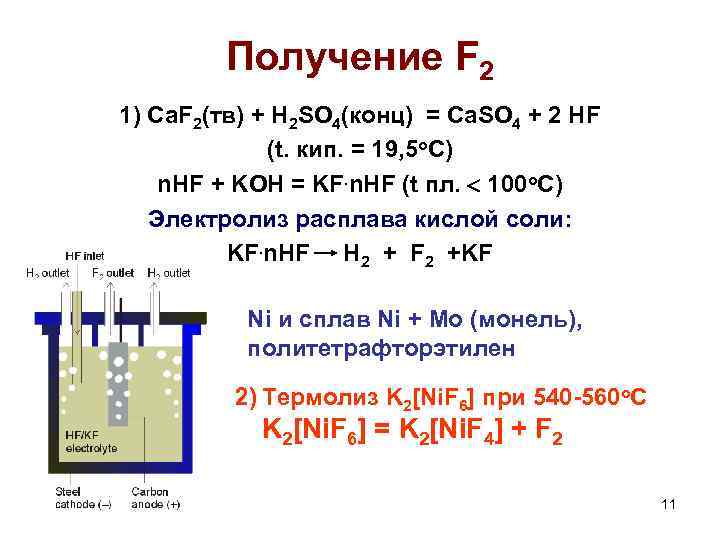 Получение F 2 1) Ca. F 2(тв) + H 2 SO 4(конц) = Ca. SO 4 + 2 HF (t. кип. = 19, 5 о. С) n. HF + KOH = KF. n. HF (t пл. 100 о. С) Электролиз расплава кислой соли: KF. n. HF H 2 + F 2 +KF Ni и сплав Ni + Mo (монель), политетрафторэтилен 2) Термолиз K 2[Ni. F 6] при 540 -560 о. С K 2[Ni. F 6] = K 2[Ni. F 4] + F 2 11
Получение F 2 1) Ca. F 2(тв) + H 2 SO 4(конц) = Ca. SO 4 + 2 HF (t. кип. = 19, 5 о. С) n. HF + KOH = KF. n. HF (t пл. 100 о. С) Электролиз расплава кислой соли: KF. n. HF H 2 + F 2 +KF Ni и сплав Ni + Mo (монель), политетрафторэтилен 2) Термолиз K 2[Ni. F 6] при 540 -560 о. С K 2[Ni. F 6] = K 2[Ni. F 4] + F 2 11
 Получение Cl 2 ЭЛЕКТРОЛИЗ Расплав: Na. Cl = Na + 1/2 Cl 2 Рассол: 2 Cl- - 2ē = Cl 2 (анод) 2 H 2 O + 2ē = + 2 OH- (катод) Анод покрывают Ru. O 2, чтобы не происходило окисление воды 12
Получение Cl 2 ЭЛЕКТРОЛИЗ Расплав: Na. Cl = Na + 1/2 Cl 2 Рассол: 2 Cl- - 2ē = Cl 2 (анод) 2 H 2 O + 2ē = + 2 OH- (катод) Анод покрывают Ru. O 2, чтобы не происходило окисление воды 12
 Лабораторные способы получения Cl 2 Взаимодействие конц. HCl с разными окислителями: KMn. O 4, K 2 Cr 2 O 7 (tºC) , Mn. O 2 (tºC), KCl. O 3, Pb. O 2. 2 KMn. O 4 + 16 HCl Ox 2 KCl + 2 Mn. Cl 2 + 5 Cl 2 + 8 H 2 O Red KCl. O 3 + 6 HCl KCl + 3 Cl 2 + 3 H 2 O 13
Лабораторные способы получения Cl 2 Взаимодействие конц. HCl с разными окислителями: KMn. O 4, K 2 Cr 2 O 7 (tºC) , Mn. O 2 (tºC), KCl. O 3, Pb. O 2. 2 KMn. O 4 + 16 HCl Ox 2 KCl + 2 Mn. Cl 2 + 5 Cl 2 + 8 H 2 O Red KCl. O 3 + 6 HCl KCl + 3 Cl 2 + 3 H 2 O 13
 Получение Br 2 • Промышленный – хлорирование рассолов, содержащих Br- (морская вода и вода некоторых озер) 2 Br- + Cl 2 = 2 Cl- + Br 2 p. H ~ 3, 5 t кипения = 58, 8 о. С (отгоняют потоком воздуха) • Лабораторный способ (редко) Mn. O 2 + 2 Br- + 4 H+ = Mn 2+ +2 H 2 O +Br 2 14
Получение Br 2 • Промышленный – хлорирование рассолов, содержащих Br- (морская вода и вода некоторых озер) 2 Br- + Cl 2 = 2 Cl- + Br 2 p. H ~ 3, 5 t кипения = 58, 8 о. С (отгоняют потоком воздуха) • Лабораторный способ (редко) Mn. O 2 + 2 Br- + 4 H+ = Mn 2+ +2 H 2 O +Br 2 14
 Получение J 2 • Лабораторный способ (редко) Mn. O 2 + 2 J- + 4 H+ = Mn 2+ +2 H 2 O + J 2 (J 2 возгоняют) • Промышленный – хлорирование растворов, содержащих J 2 J- + Cl 2 = J 2 + 2 Cl • Избыток Cl 2: J 2 + 5 Cl 2 + 6 H 2 O = 2 HJO 3 + 10 HCl • Иодаты осторожно восстанавливают: 2 JO 3 - + 5 SO 2 + 4 H 2 O = J 2 + 5 SO 42 - +8 H+ Но!!! J 2 + SO 2 + 2 H 2 O = 2 J- + SO 42 - +4 H+ 15
Получение J 2 • Лабораторный способ (редко) Mn. O 2 + 2 J- + 4 H+ = Mn 2+ +2 H 2 O + J 2 (J 2 возгоняют) • Промышленный – хлорирование растворов, содержащих J 2 J- + Cl 2 = J 2 + 2 Cl • Избыток Cl 2: J 2 + 5 Cl 2 + 6 H 2 O = 2 HJO 3 + 10 HCl • Иодаты осторожно восстанавливают: 2 JO 3 - + 5 SO 2 + 4 H 2 O = J 2 + 5 SO 42 - +8 H+ Но!!! J 2 + SO 2 + 2 H 2 O = 2 J- + SO 42 - +4 H+ 15
 Галеноводороды НХ В газовой фазе: H + X - (полярная ковалентная связь) Дипольный момент: HF HCl HBr HJ (Д) 1. 91 1. 04 0. 79 0. 38 В водных растворах: HF – слабая (Ka = 7, 2. 10 -5) HCl , HBr, и HJ (сильные кислоты) Нивелирующее влияние воды на кислотные свойства. Степень диссоциации α в 0, 1 М растворе (18 о. С): HF (10%), HCl (92, 6%), HBr (93, 5%), HJ (95%) 16
Галеноводороды НХ В газовой фазе: H + X - (полярная ковалентная связь) Дипольный момент: HF HCl HBr HJ (Д) 1. 91 1. 04 0. 79 0. 38 В водных растворах: HF – слабая (Ka = 7, 2. 10 -5) HCl , HBr, и HJ (сильные кислоты) Нивелирующее влияние воды на кислотные свойства. Степень диссоциации α в 0, 1 М растворе (18 о. С): HF (10%), HCl (92, 6%), HBr (93, 5%), HJ (95%) 16
 Особенности HF HF (жидкий) – сильная кислота HF (газ) - сильная кислота HF (в воде) - слабая кислота Самоионизация жидкого HF 3 HF = H 2 F+ + HF 2 Прочная водородная связь 165 к. Дж/моль, энергия ков. cвязи H-F равна 565 к. Дж/моль. Жидкий HF – растворитель, реагирует с металлами (если не образуется прочная защитная пленка Al. F 3, Mg. F 2, Ni. F 2) Zn + 2 HF(ж) = Zn. F 2 + H 2 17
Особенности HF HF (жидкий) – сильная кислота HF (газ) - сильная кислота HF (в воде) - слабая кислота Самоионизация жидкого HF 3 HF = H 2 F+ + HF 2 Прочная водородная связь 165 к. Дж/моль, энергия ков. cвязи H-F равна 565 к. Дж/моль. Жидкий HF – растворитель, реагирует с металлами (если не образуется прочная защитная пленка Al. F 3, Mg. F 2, Ni. F 2) Zn + 2 HF(ж) = Zn. F 2 + H 2 17
 Получение HX А) Синтез из простых веществ H 2 + X 2 = 2 HX, r. H 0 Для увеличения выхода надо снижать Т, но это снижает скорость реакции HF – Реакция идет со взрывом Степень диссоциации HX при 1000 о. С, 1 атм: HCl – 0, 014% ( можно использовать ) HBr- 0, 5% HJ – 33% 18
Получение HX А) Синтез из простых веществ H 2 + X 2 = 2 HX, r. H 0 Для увеличения выхода надо снижать Т, но это снижает скорость реакции HF – Реакция идет со взрывом Степень диссоциации HX при 1000 о. С, 1 атм: HCl – 0, 014% ( можно использовать ) HBr- 0, 5% HJ – 33% 18
 Получение HX Б) Из солей реакцией ионного обмена Ca. F 2(тв) + H 2 SO 4 (конц) = Ca. SO 4 + 2 HF (газ) 2 Na. Cl (тв) + H 2 SO 4 (конц) = Na 2 SO 4 + 2 HCl (газ) Но!!!! 2 Na. Br(тв) + 2 H 2 SO 4 (конц) = Na 2 SO 4 + Br 2 + SO 2 +2 H 2 O 8 Na. J(тв) + 5 H 2 SO 4 (конц) = 4 Na 2 SO 4 + 4 J 2 + H 2 S +4 H 2 O Na. Br + H 3 PO 4 = HBr + Na. H 2 PO 4 Аналогично получают HJ В) Гидролиз галогенидов неметаллов 2 P(тв) + 3 Br 2(ж) = 2 PBr 3 + 3 H 2 O = 3 HBr + H 3 PO 3 19
Получение HX Б) Из солей реакцией ионного обмена Ca. F 2(тв) + H 2 SO 4 (конц) = Ca. SO 4 + 2 HF (газ) 2 Na. Cl (тв) + H 2 SO 4 (конц) = Na 2 SO 4 + 2 HCl (газ) Но!!!! 2 Na. Br(тв) + 2 H 2 SO 4 (конц) = Na 2 SO 4 + Br 2 + SO 2 +2 H 2 O 8 Na. J(тв) + 5 H 2 SO 4 (конц) = 4 Na 2 SO 4 + 4 J 2 + H 2 S +4 H 2 O Na. Br + H 3 PO 4 = HBr + Na. H 2 PO 4 Аналогично получают HJ В) Гидролиз галогенидов неметаллов 2 P(тв) + 3 Br 2(ж) = 2 PBr 3 + 3 H 2 O = 3 HBr + H 3 PO 3 19
 Ox/red свойства HX HX Окислитель HF Окисление только на аноде! HCl + Mn. O 4 -, Cr 2 O 72 -, Mn. O 2, Cl. O 3 -, Pb. O 2, F 2 HBr ++ Cl 2, H 2 SO 4 (конц. ) HJ +++ Br 2, H 2 O 2, HNO 3, Fe 3+, Cu 2+ 20
Ox/red свойства HX HX Окислитель HF Окисление только на аноде! HCl + Mn. O 4 -, Cr 2 O 72 -, Mn. O 2, Cl. O 3 -, Pb. O 2, F 2 HBr ++ Cl 2, H 2 SO 4 (конц. ) HJ +++ Br 2, H 2 O 2, HNO 3, Fe 3+, Cu 2+ 20
 Галогениды металлов – твердые в-ва, ионные кристаллы, как правило, растворимы в воде. Не растворимы в воде: Ag. X, Pb. X 2, Hg 2 X 2, Cu. X (X = Cl, Br, J) Фториды почти все не растворимы, за исключением MF (M- щелочной металл), Ag. F, NH 4 F Галогениды неметаллов Газы: BF 3, Si. F 4, PF 3, PF 5 Жидкие: BCl 3, Si. Cl 4, PCl 3, POCl 3 Твердые: BJ 3, PCl 5 PCl 3 + 3 H 2 O = 3 HCl + H 3 PO 3 PCl 5 + 8 Na. OH = 5 Na. Cl + Na 3 PO 4 + 4 H 2 O 21
Галогениды металлов – твердые в-ва, ионные кристаллы, как правило, растворимы в воде. Не растворимы в воде: Ag. X, Pb. X 2, Hg 2 X 2, Cu. X (X = Cl, Br, J) Фториды почти все не растворимы, за исключением MF (M- щелочной металл), Ag. F, NH 4 F Галогениды неметаллов Газы: BF 3, Si. F 4, PF 3, PF 5 Жидкие: BCl 3, Si. Cl 4, PCl 3, POCl 3 Твердые: BJ 3, PCl 5 PCl 3 + 3 H 2 O = 3 HCl + H 3 PO 3 PCl 5 + 8 Na. OH = 5 Na. Cl + Na 3 PO 4 + 4 H 2 O 21
 Ox/red свойства HX HX Окислитель HF Окисление только на аноде! HCl + Mn. O 4 -, Cr 2 O 72 -, Mn. O 2, Cl. O 3 -, Pb. O 2, F 2 HBr ++ Cl 2, H 2 SO 4 (конц. ) HJ +++ Br 2, H 2 O 2, HNO 3, Fe 3+, Cu 2+ 22
Ox/red свойства HX HX Окислитель HF Окисление только на аноде! HCl + Mn. O 4 -, Cr 2 O 72 -, Mn. O 2, Cl. O 3 -, Pb. O 2, F 2 HBr ++ Cl 2, H 2 SO 4 (конц. ) HJ +++ Br 2, H 2 O 2, HNO 3, Fe 3+, Cu 2+ 22
 Галогениды металлов – твердые в-ва, ионные кристаллы, как правило, растворимы в воде. Не растворимы в воде: Ag. X, Pb. X 2, Hg 2 X 2, Cu. X (X = Cl, Br, J) Фториды почти все не растворимы, за исключением MF (M- щелочной металл), Ag. F, NH 4 F Галогениды неметаллов Газы: BF 3, Si. F 4, PF 3, PF 5 Жидкие: BCl 3, Si. Cl 4, PCl 3, POCl 3 Твердые: BJ 3, PCl 5 PCl 3 + 3 H 2 O = 3 HCl + H 3 PO 3 PCl 5 + 8 Na. OH = 5 Na. Cl + Na 3 PO 4 + 4 H 2 O 23
Галогениды металлов – твердые в-ва, ионные кристаллы, как правило, растворимы в воде. Не растворимы в воде: Ag. X, Pb. X 2, Hg 2 X 2, Cu. X (X = Cl, Br, J) Фториды почти все не растворимы, за исключением MF (M- щелочной металл), Ag. F, NH 4 F Галогениды неметаллов Газы: BF 3, Si. F 4, PF 3, PF 5 Жидкие: BCl 3, Si. Cl 4, PCl 3, POCl 3 Твердые: BJ 3, PCl 5 PCl 3 + 3 H 2 O = 3 HCl + H 3 PO 3 PCl 5 + 8 Na. OH = 5 Na. Cl + Na 3 PO 4 + 4 H 2 O 23
 КИСЛОРОДНЫЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ 24
КИСЛОРОДНЫЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ 24
 Оксиды фтора F 2 + O 2 – нет реакции при температурах 1001000 о. С 2 F 2 + 2 H 2 O = 4 HF + O 2 (+ получается O 3 и H 2 O 2) 2 F 2 (газ) + Na. OH (1% р-р) = OF 2 + 2 Na. F + H 2 O OF 2 – бесцветный газ, устойчив, сильный фторокислитель, но более слабый, чем F 2 (не реагирует со стеклом). F 2(ж) + O 2 (ж) = O 2 F 2 (фотолиз) Дифторид дикислорода O 2 F 2 – газ, разлагается выше -100 о. С. Pu(тв) + 3 O 2 F 2(г) = Pu. F 6 (г) + 3 O 2 (г) 25
Оксиды фтора F 2 + O 2 – нет реакции при температурах 1001000 о. С 2 F 2 + 2 H 2 O = 4 HF + O 2 (+ получается O 3 и H 2 O 2) 2 F 2 (газ) + Na. OH (1% р-р) = OF 2 + 2 Na. F + H 2 O OF 2 – бесцветный газ, устойчив, сильный фторокислитель, но более слабый, чем F 2 (не реагирует со стеклом). F 2(ж) + O 2 (ж) = O 2 F 2 (фотолиз) Дифторид дикислорода O 2 F 2 – газ, разлагается выше -100 о. С. Pu(тв) + 3 O 2 F 2(г) = Pu. F 6 (г) + 3 O 2 (г) 25
 Взаимодействие Х 2 с водой Особенности F 2 рассмотрены ранее. Физическое растворение и химические реакции. При низких температурах можно выделить гидрат Cl 2. 7, 3 H 2 O. Суммарная растворимость (с учетом всех форм) при 20 о. С. Cl 2 – 0, 73%; Br 2 – 3, 6%; J 2 – 0, 03% Увеличение растворимости: KJ + J 2 = KJ 3 26
Взаимодействие Х 2 с водой Особенности F 2 рассмотрены ранее. Физическое растворение и химические реакции. При низких температурах можно выделить гидрат Cl 2. 7, 3 H 2 O. Суммарная растворимость (с учетом всех форм) при 20 о. С. Cl 2 – 0, 73%; Br 2 – 3, 6%; J 2 – 0, 03% Увеличение растворимости: KJ + J 2 = KJ 3 26
 Химическое взаимодействие с водой X 2 + H 2 O = H+ + X- + HOX Реакция диспропорционирования обратима. К = 4. 10 -4 (X = Cl); 7. 10 -9 (X = Br); 2. 10 -13 (X = J) В щелочной среде равновесие сдвинуто вправо X 2 + 2 OH- = X- + OX- + H 2 O K = 1015 (X = Cl); 108 (X = Br); 30 (X = J) Диспропорционирование гипогалогенид- ионов 3 OX- = 2 X- + XO 3 K 1015, НО для X = Cl, Br реакция кинетически затруднена и идет только при нагревании 27
Химическое взаимодействие с водой X 2 + H 2 O = H+ + X- + HOX Реакция диспропорционирования обратима. К = 4. 10 -4 (X = Cl); 7. 10 -9 (X = Br); 2. 10 -13 (X = J) В щелочной среде равновесие сдвинуто вправо X 2 + 2 OH- = X- + OX- + H 2 O K = 1015 (X = Cl); 108 (X = Br); 30 (X = J) Диспропорционирование гипогалогенид- ионов 3 OX- = 2 X- + XO 3 K 1015, НО для X = Cl, Br реакция кинетически затруднена и идет только при нагревании 27
 Использование в промышленности «Жавелева» вода Cl 2 + 2 Na. OH = Na. Cl + Na. Cl. O Отбеливание тканей, бумаги Хлорная (белильная) известь (хлорка) Ca(OH)2 + Cl 2 = Ca. Cl(OCl) + H 2 O Ca. Cl(OCl) + CO 2 +H 2 O = Ca. CO 3 + HCl. O HCl + HCl. O = Cl 2 +H 2 O Ca. OCl 2 = Ca. Cl 2 + 1/2 O 2 28
Использование в промышленности «Жавелева» вода Cl 2 + 2 Na. OH = Na. Cl + Na. Cl. O Отбеливание тканей, бумаги Хлорная (белильная) известь (хлорка) Ca(OH)2 + Cl 2 = Ca. Cl(OCl) + H 2 O Ca. Cl(OCl) + CO 2 +H 2 O = Ca. CO 3 + HCl. O HCl + HCl. O = Cl 2 +H 2 O Ca. OCl 2 = Ca. Cl 2 + 1/2 O 2 28
 Кислородсодержащие кислоты и их соли Х=Cl Степень окисления 1+ HXO, Na. XO (оксохлорат водорода, оксохлорат натрия) Гипохлористая (хлорноватистая) кислота, гипохлориты. Степень окисления 3+ HXO 2 (диоксохлорат водорода), Na. XO 2 Хлористая кислота, хлориты. Степень окисления 5+ HXO 3 (триоксохлорат водорода), Na. XO 3 Хлорноватая кислота, хлораты. Степень окисления 7+ HXO 4 (тетраоксохлорат водорода), Na. XO 4 Хлорная кислота, перхлораты. 29
Кислородсодержащие кислоты и их соли Х=Cl Степень окисления 1+ HXO, Na. XO (оксохлорат водорода, оксохлорат натрия) Гипохлористая (хлорноватистая) кислота, гипохлориты. Степень окисления 3+ HXO 2 (диоксохлорат водорода), Na. XO 2 Хлористая кислота, хлориты. Степень окисления 5+ HXO 3 (триоксохлорат водорода), Na. XO 3 Хлорноватая кислота, хлораты. Степень окисления 7+ HXO 4 (тетраоксохлорат водорода), Na. XO 4 Хлорная кислота, перхлораты. 29
 Кислородсодержащие кислоты и их соли Степень окисления 1+ HXO: HCl. O, HBr. O, HJO Ka = 10 -8 (X = Cl), 10 -9 (X=Br), 10 -11 (X=J) Амфотерные свойства HJO = H+ + JOHJO = OH- + J+, Kb = 10 -10 Ag. NO 3 + J 2 + 2 Py = [J(Py)2]+(NO 3)- + Ag. J (тв) Растворимость J 2 в соляной кислоте увеличивается J 2 + H 2 O = HJ + HJO + HCl = H 2 O + JCl 30
Кислородсодержащие кислоты и их соли Степень окисления 1+ HXO: HCl. O, HBr. O, HJO Ka = 10 -8 (X = Cl), 10 -9 (X=Br), 10 -11 (X=J) Амфотерные свойства HJO = H+ + JOHJO = OH- + J+, Kb = 10 -10 Ag. NO 3 + J 2 + 2 Py = [J(Py)2]+(NO 3)- + Ag. J (тв) Растворимость J 2 в соляной кислоте увеличивается J 2 + H 2 O = HJ + HJO + HCl = H 2 O + JCl 30
 Получение кислот HXO X 2 + H 2 O + Ca. CO 3 (тв) = Ca. X 2 + CO 2 + HXO (X = Cl, Br) J 2 + H 2 O + Hg. O(тв) = Hg. J 2 + 2 HIO Соли подвергаются гидролизу (p. H 7) XO- + H 2 O = HXO + OHКислоты HXO являются сильными окислителями Уменьшение окислительных свойств HCl. O HBr. O HJO Уменьшение скорости ox/red реакций HCl. O HBr. O HJO 31
Получение кислот HXO X 2 + H 2 O + Ca. CO 3 (тв) = Ca. X 2 + CO 2 + HXO (X = Cl, Br) J 2 + H 2 O + Hg. O(тв) = Hg. J 2 + 2 HIO Соли подвергаются гидролизу (p. H 7) XO- + H 2 O = HXO + OHКислоты HXO являются сильными окислителями Уменьшение окислительных свойств HCl. O HBr. O HJO Уменьшение скорости ox/red реакций HCl. O HBr. O HJO 31
 Степень окисления +3 Нет HJO 2 и нет примеров солей Нет HBr. O 2, только ОДИН пример соли Ba(Br. O)2 +2 Br 2 + 4 KOH = Ba(Br. O 2)2 + 4 KBr + 4 H 2 O (0 o. C, p. H = 11, 2) Для кислоты HCl. O 2 и ее солей характерны реакции диспропорционирования (особенно быстро в кислой среде). Соли взрывают!! 4 HCl. O 2 = Cl. O 2 +HCl. O 3 +HCl +H 2 O Получение 2 Cl. O 2 +2 KOH = KCl. O 2 + KCl. O 3 + H 2 O Ba(OH)2 + H 2 O 2 + 2 Cl. O 2 = Ba(Cl. O 2)2 + 2 H 2 O + O 2 Ba(Cl. O 2)2(сусп. ) +H 2 SO 4 (разб. ) = Ba. SO 4(тв)+ HCl. O 2 32
Степень окисления +3 Нет HJO 2 и нет примеров солей Нет HBr. O 2, только ОДИН пример соли Ba(Br. O)2 +2 Br 2 + 4 KOH = Ba(Br. O 2)2 + 4 KBr + 4 H 2 O (0 o. C, p. H = 11, 2) Для кислоты HCl. O 2 и ее солей характерны реакции диспропорционирования (особенно быстро в кислой среде). Соли взрывают!! 4 HCl. O 2 = Cl. O 2 +HCl. O 3 +HCl +H 2 O Получение 2 Cl. O 2 +2 KOH = KCl. O 2 + KCl. O 3 + H 2 O Ba(OH)2 + H 2 O 2 + 2 Cl. O 2 = Ba(Cl. O 2)2 + 2 H 2 O + O 2 Ba(Cl. O 2)2(сусп. ) +H 2 SO 4 (разб. ) = Ba. SO 4(тв)+ HCl. O 2 32
 Степень окисления +5 Сильные кислоты HXO 3 (X = Cl, Br, J) HCl. O 3 и HBr. O 3 – только растворы (до 40%) HJO 3 – получена твердая и в растворах Обезвоживание (P 4 O 10) HJO 3 HJ 3 O 8 (J 2 O 5. HJO 3) J 2 O 5 Разложение при нагревании 40% р-ров: 3 HCl. O 3 = HCl. O 4 + 2 Cl. O 2 +H 2 O 8 HCl. O 3 = 4 HCl. O 4 + 2 Cl 2 + 3 O 2 +2 H 2 O 4 HBr. O 3 = 2 Br 2 + 5 O 2 + 2 H 2 O 33
Степень окисления +5 Сильные кислоты HXO 3 (X = Cl, Br, J) HCl. O 3 и HBr. O 3 – только растворы (до 40%) HJO 3 – получена твердая и в растворах Обезвоживание (P 4 O 10) HJO 3 HJ 3 O 8 (J 2 O 5. HJO 3) J 2 O 5 Разложение при нагревании 40% р-ров: 3 HCl. O 3 = HCl. O 4 + 2 Cl. O 2 +H 2 O 8 HCl. O 3 = 4 HCl. O 4 + 2 Cl 2 + 3 O 2 +2 H 2 O 4 HBr. O 3 = 2 Br 2 + 5 O 2 + 2 H 2 O 33
 Получение соединений X(+5) ХЛОРАТЫ Электрохимическое окисление хлоридов KCl +3 H 2 O = KCl. O 3 (анод) + 3 H 2(катод) Или: 6 KOH (гор. р-р) + 3 Cl 2 = KCl. O 3 + 5 KCl +3 H 2 O БРОМАТЫ Br 2 + 5 Cl 2 + 12 KOH = 2 KBr. O 3 + 10 KCl +6 H 2 O KBr + 3 Cl 2 +6 KOH = KBr. O 3 + 6 KCl + 3 H 2 O ИОДАТЫ J 2 (тв) + 10 HNO 3(конц) = 2 HJO 3 + 10 NO 2 +4 H 2 O 34
Получение соединений X(+5) ХЛОРАТЫ Электрохимическое окисление хлоридов KCl +3 H 2 O = KCl. O 3 (анод) + 3 H 2(катод) Или: 6 KOH (гор. р-р) + 3 Cl 2 = KCl. O 3 + 5 KCl +3 H 2 O БРОМАТЫ Br 2 + 5 Cl 2 + 12 KOH = 2 KBr. O 3 + 10 KCl +6 H 2 O KBr + 3 Cl 2 +6 KOH = KBr. O 3 + 6 KCl + 3 H 2 O ИОДАТЫ J 2 (тв) + 10 HNO 3(конц) = 2 HJO 3 + 10 NO 2 +4 H 2 O 34
 Бертолетова соль (хлорат калия) Впервые получена Клодом Бертолле в 1786 году при пропускании хлора через горячий концентрированный раствор гидроксида калия: 2 KOH + Cl 2 = KCl + KCl. O + H 2 O; 3 KCl. O = KCl. O 3 + 2 KCl, Смеси хлората калия с восстановителями ( фосфором, серой, органическими соединениями) взрывчаты и чувствительны к трению и ударам, чувствительность повышается в присутствии броматов и солей аммония. 35
Бертолетова соль (хлорат калия) Впервые получена Клодом Бертолле в 1786 году при пропускании хлора через горячий концентрированный раствор гидроксида калия: 2 KOH + Cl 2 = KCl + KCl. O + H 2 O; 3 KCl. O = KCl. O 3 + 2 KCl, Смеси хлората калия с восстановителями ( фосфором, серой, органическими соединениями) взрывчаты и чувствительны к трению и ударам, чувствительность повышается в присутствии броматов и солей аммония. 35
 Ox/red свойства X(+5) Все X(+5)– сильные окислители, как правило, восстанавливаются до XKCl. O 3(тв) + 6 HCl (конц) = 3 Cl 2 + 3 H 2 O + KCl 4 KCl. O 3(тв) + C 6 H 12 O 6(тв) = 4 KCl + 6 CO 2 + 6 H 2 O 10 KCl. O 3(тв) + 12 P(тв) = 10 KCl + 3 P 4 O 10 36
Ox/red свойства X(+5) Все X(+5)– сильные окислители, как правило, восстанавливаются до XKCl. O 3(тв) + 6 HCl (конц) = 3 Cl 2 + 3 H 2 O + KCl 4 KCl. O 3(тв) + C 6 H 12 O 6(тв) = 4 KCl + 6 CO 2 + 6 H 2 O 10 KCl. O 3(тв) + 12 P(тв) = 10 KCl + 3 P 4 O 10 36
 Разложение твердых солей при нагревании 4 KCl. O 3 = 3 KCl. O 4 + KCl (400 o. C) Лабораторный способ получения О 2 2 KCl. O 3 = 2 KCl + 3 O 2 (100 o. C, Mn. O 2) Нагревание до 300 – 350 о. С 2 KJO 3 = 2 KJ + 3 O 2 2 Cu(Br. O 3)2 = 2 Cu. O + Br 2 +5 O 2 37
Разложение твердых солей при нагревании 4 KCl. O 3 = 3 KCl. O 4 + KCl (400 o. C) Лабораторный способ получения О 2 2 KCl. O 3 = 2 KCl + 3 O 2 (100 o. C, Mn. O 2) Нагревание до 300 – 350 о. С 2 KJO 3 = 2 KJ + 3 O 2 2 Cu(Br. O 3)2 = 2 Cu. O + Br 2 +5 O 2 37
 Соединения Х(+7) HCl. O 4 – получены 100% растворы (взрывоопасно!), сильная кислота HBr. O 4 – получены 100% растворы (взрывоопасно!), сильная кислота HJO 4 – метаиодная кислота, Ka = 3. 10 -2 H 5 JO 6 – ортоиодная кислота, Ka 1 = 2. 10 -2; Ka 2 = 10 -9 Растворимые соли Na. XO 4, Na. H 4 JO 6, Na 2 H 3 JO 6 Нерастворимые соли KCl. O 4, Ag 5 JO 6, Ba 5(JO 6)2, 38 Na 3 H 2 JO 6
Соединения Х(+7) HCl. O 4 – получены 100% растворы (взрывоопасно!), сильная кислота HBr. O 4 – получены 100% растворы (взрывоопасно!), сильная кислота HJO 4 – метаиодная кислота, Ka = 3. 10 -2 H 5 JO 6 – ортоиодная кислота, Ka 1 = 2. 10 -2; Ka 2 = 10 -9 Растворимые соли Na. XO 4, Na. H 4 JO 6, Na 2 H 3 JO 6 Нерастворимые соли KCl. O 4, Ag 5 JO 6, Ba 5(JO 6)2, 38 Na 3 H 2 JO 6
 Получение соединений X(+7) Электролиз XO 3 - + H 2 O = XO 4 -(анод) + H 2(катод) Реакции в растворах: KBr. O 3 + O 3 = KBr. O 4 +O 2 1968 год: облучение нейтронами Rb 2 Se. O 4 82 Se + n = 83 Se = β + 83 Br Na. JO 3+ Cl 2 +4 Na. OH = Na 3 H 2 JO 6 + 2 Na. Cl + H 2 O 39
Получение соединений X(+7) Электролиз XO 3 - + H 2 O = XO 4 -(анод) + H 2(катод) Реакции в растворах: KBr. O 3 + O 3 = KBr. O 4 +O 2 1968 год: облучение нейтронами Rb 2 Se. O 4 82 Se + n = 83 Se = β + 83 Br Na. JO 3+ Cl 2 +4 Na. OH = Na 3 H 2 JO 6 + 2 Na. Cl + H 2 O 39
 Свойства соединений X(+7) Проявляют сильные окислительные свойства при нагревании (расплавы) ПЕРХЛОРАТЫ ВЗРЫВАЮТСЯ!!!!!!! KCl. O 4(тв) = KCl + 2 O 2 (выше 500 о. С) 2 NH 4 Cl. O 4(тв) = N 2 + Cl 2 + 2 O 2 + 4 H 2 O (ВЗРЫВ при 200 о. С) 40
Свойства соединений X(+7) Проявляют сильные окислительные свойства при нагревании (расплавы) ПЕРХЛОРАТЫ ВЗРЫВАЮТСЯ!!!!!!! KCl. O 4(тв) = KCl + 2 O 2 (выше 500 о. С) 2 NH 4 Cl. O 4(тв) = N 2 + Cl 2 + 2 O 2 + 4 H 2 O (ВЗРЫВ при 200 о. С) 40


