30611a550d8b237f98eb4af9e25d87ff.ppt
- Количество слайдов: 46

Требования к организации и проведению КИ в ЕС Директор Департамента доклинических исследований Государственного экспертного центра МЗ Украины к. м. н. Николаева Валентиновна

Все клинические исследования, включая исследования биодоступности и биоэквивалентности, планируются, проводят и представляют в форме отчета в соответствии с принципами Надлежащей клинической практики Директива 2001/20 ЕС, ст. 1

n. Хельсинская декларация «Рекомендации для врачей по проведению биомедицинских исследований с участием человека в качестве объекта исследования» , Всемирная Медицинская Ассоциация, 1964 с пересмотрами: Япония 1975 г. , Италия – 1984 г. , Гонконг – 1989 г. , ЮАР – 1996 г. , Шотландия – 2000 г. , Южная Корея – 2008 г. ; Медицинские исследования должны соответствовать этическим стандартам, предусматривающим уважение к испытуемым, а также защиту их прав и здоровья Ст. 8

Международная нормативно-правовая база в сфере проведения клинических испытаний Директива Европейского Парламента и Совета 2001/20/ЕС от 04. 2001 г. «О сближении законов, подзаконных актов и административных положений государств-членов касательно внедрения надлежащей клинической практики проведении КИ ЛС для применения человеком» (имплементация в законодательство европейских стран завершена в мае 2004 г. ); Директива Европейского Парламента и Совета 2001/83/ЕС от 06. 11. 2001 г. «О своде законов сообщества в отношении лекарственных препаратов для человека» ;

Международная нормативно-правовая база в сфере проведения клинических испытаний Директива Комиссии Европейских Сообществ 2005/28/ЕС от 08. 04. 2005 г. «Принципы и наставления GCP, касающиеся исследуемых ЛС предназначенных для использования человеком, а также требования к предоставлению разрешения на изготовления и импорт таких продуктов» ; Постановление Европейского Парламента и Совета 1901/2006 от 12. 2006 г. : «О лекарственных средствах для применения в педиатрии» Постановление Европейского Парламента и Совета 1902/2006 от 20. 12. 2006 г. «Изменения к Постановлению о лекарственных средствах для применения в педиатрии

Нормативная база проведения КИ в Украине Закон Украины “О лекарственных средствах”, 1996 г, с изменениями и дополнениями, ст. 7, 8 Постановление КМУ № 644 от 28. 07. 10 «О внесении изменений к перечню платных услуг, которые могут предоставляться учреждениями здравоохранения, ВУЗами и НИИ» - проведение КИ в этих учреждениях разрешается в порядке, определенном МЗ Украины (Постановление КМУ № 1138 от17. 09. 96 – р. 1 п. 33)

продолжение Нормативная база проведения КИ в Украине Руководство 42 -7. 1: 2005 (Исследования биодоступности и биоэквивалентности), приказ МЗ Украины № 191 от 25. 04. 2005 г. CPMP/EWP/QWP/ 1401/98 Руководство ICH GCP (Надлежащая клиническая практика. Руководство 42 -7. 0: 2008), Приказ МЗ Украины № 95 от 16. 02. 2009 CP/MP/ICH 135/95 (E 6)

продолжение Нормативная база проведения КИ в Украине Приказ МЗ Украины № 690 от 23. 09. 2009 «Об утверждении Порядка проведения КИ и экспертизы материалов КИ и Типового Положение о комиссии по вопросам этики» (зарегистрирован в Мин. Юсте 29. 10. 2009 № 1010/1726) В редакции Приказа МЗ Украины № 523 от 12. 07. 2012 «О внесении изменений в приказ Министерства здравоохранения Украины от 23 сентября 2009 г. № 690» (зарегистрирован в Мин. Юсте 20. 07. 2012 р. № 1235/21547 та № 1236/21548) CP/MP/ICH 135/95 (E 6) Хельсинская декларация Директива Европейского Парламента и Совета 2001/20/ЕС

продолжение Нормативная база проведения КИ в Украине Порядок ввоза на территорию Украины незарегистрированных ЛС, стандартных образцов, реагентов (Приказ МЗ Украины № 237 от 26. 04. 2011, зарегистрирован в Мин. Юсте 11. 01. 2011 № 965/19703)

продолжение Нормативная база КИ в Украине Закон Украины «О внесении изменений в некоторые законодательные акты Украины относительно усиления ответственности за фальсификацию или оборот фальсифицированных лекарственных средств» от 05. 07. 2012 г. № 5065 -VI Криминальный Кодекс дополнен статьей 3212 «Нарушение установленного порядка …клинических испытаний…»

В 1977 г. FDA предложила правила, определяющие обязанности исследователей и спонсоров, которые вскоре были внедрены в практику. Разработанную систему назвали – GCP – Good Clinical Practice. Многие страны создали свои правила GCP (США, страны ЕС, Япония…) В 1990 году в ЕС приняты единые правила Надлежащей Клинической Практики (GCP), - закреплены в последующем положении ВОЗ.

Гармонизация GCP Брюссель, 1991 Международная конференция по гармонизации технических требований к регистрации лекарственных препаратов для человека - ICH

Международная конференция по гармонизации (ICH) Основными членами ICH являются: Комиссия ЕС – Европейский Союз (EU); Европейская федерация ассоциаций фармацевтической промышленности (EFPIA); Министерство здравоохранения Японии (MHW); Ассоциация фармацевтических производителей Японии (JPMA); FDA (США); Ассоциация исследовательских и производственных фармацевтических предприятий США (Ph. RMA). Проведено 6 конференций, на которых обсуждался единый подход к вопросам качества, эффективности и безопасности ЛС

Международная конференция по гармонизации. 6 Международных конференций по гармонизации (ICH): Ø Первая (ICH 1), Брюссель (Бельгия), ноябрь 1991 г. Более 1200 участников. Ø Вторая (ICH 2), Орландо (США), октябрь 1993 г. Более 1500 участников. Ø Третья (ICH 3) Йокогама (Япония) ноябрь 1995 г. Более 2500 участников. Ø Четвертая (ICH 4), Брюссель (Бельгия), июль 1997 г. Более 1600 участников. Ø Пятая (ICH 5), Сан-Диего (США), ноябрь 2000 г. Более 1400 участников. Ø Шестая (ICH 6), Осака (Япония), ноябрь 2003 г. Более 1800 участников.

Международная конференция по гармонизации. В рамках ICH согласовано: Ø 50 отраслевых нормативов и методических рекомендаций по трем основным разделам: v «Качество» (индекс Q – “Quality”) v «Безопасность» (индекс S – “Safety”) v «Эффективность» (индекс E – “Efficacy”) Ø общий технический документ (CTD, индекс М 4) Ø терминология, касающаяся мониторинга ПР

Руководства, изданные Международной конференцией по гармонизации (ICH) технических требований к регистрации лекарственных препаратов для человека и законодательно адаптированные в ЕС (одобренные СРМР): - CPMP/ICH 135/95 (E 6) «Note for guidance on good clinical practice» , 1997 - CPMP/ICH 137/95 (E 3) «Note for guidance on structure and content of clinical study reports» , 1995; - CPMP/ICH 291/95 (E 8) «Note for guidance on general consideration for clinical trials» , 1997; - CPMP/ICH/377/95 (E 2 A) «Clinical Safety Data Management: Definitions and Standards for Expedited Reporting» , June 1995

Good Clinical Practice (GCP) Надлежащая клиническая практика стандарт планирования, проведения, выполнения, мониторинга, аудита и документального оформления клинических испытаний, а также обработки и представления их результатов, служит для общества гарантией достоверности полученных данных и защищенности прав, здоровья и анонимности испытуемых.

GCP ICH : Введение 1. Терминология 2. Принципы GCP 3. Экспертный совет/Этический комитет 4. Исследователь 5. Спонсор 6. Протокол КИ и поправки к протоколу 7. Брошюра исследователя 8. Основные документы КИ

Принципы ICH GCP 1. КИ следует проводить в соответствии с этическими принципами Хельсинской декларации, правилами GCP и действующими нормативными требованиями. 2. До начала КИ должна быть проведена оценка соотношения предполагаемого риска и пользы для испытуемого и общества. КИ может быть начато и продолжено только в том случае, если ожидаемая польза оправдывает риск.

Принципы ICH GCP 3. Права, безопасность и благополучие испытуемых важнее интересов науки и общества. 4. Данные доклинического изучения исследуемого ЛС должны быть достаточными для обоснования планируемого КИ. 5. КИ должно быть научно обосновано, подробно и ясно описано в протоколе исследования. 6. КИ следует проводить согласно протоколу, одобренному Этическим комитетом.

Принципы ICH GCP 7. Только квалифицированный врач может взять на себя ответственность за оказание испытуемым медицинской помощи и принятие решений медицинского характера. 8. Все участвующие в проведении КИ лица должны иметь образование, профессиональную подготовку и опыт, соответствующие выполняемым функциям.

Принципы ICH GCP 9. До включения испытуемого в КИ должно быть получено его добровольное информированное согласие. 10. Регистрация, обработка и хранение получаемой в ходе КИ информации должны обеспечивать корректное представление, интерпретацию и верификацию данных. 11. Необходимо обеспечить конфиденциальность документов, позволяющих установить личность испытуемого, при соблюдении прав на неприкосновенность частной жизни и конфиденциальность, гарантированные действующими нормативными требованиями.

Принципы ICH GCP 12. Производство и хранение исследуемого ЛС, а также обращение с ним осуществляется в соответствии с правилами Надлежащей производственной практики (Good Manufacturing Practice - GMP). Препарат должен использоваться согласно протоколу КИ. 13. Должна использоваться система процедур, обеспечивающих качество КИ во всех его аспектах.

Положения GCP были закреплены Директивой 2001/20 ЕС Европейского парламента и Совета от 4 апреля 2001 «О сближении законов, правил и административных норм государств-членов в отношении выполнения надлежащей клинической практики проведении клинических испытаний лекарственных препаратов для применения у человека» Приказ МЗ Украины № 95 от 16. 02. 2009 (Руководство. Лекарственные средства Надлежащая клиническая практика. СТ-Н МОЗУ 42 -7. 0: 2008)

Основные положения Директивы 2001/20/ЕС - Защита испытуемых - Рассмотрение материалов КИ Комитетом по вопросам этики - Начало проведения КИ - Проведение КИ - Обмен информацией - Приостановка КИ или нарушения - Производство и импорт исследуемого ЛС - Проверка соответствия исследуемых ЛС требованиям GCP и GMP - Уведомление о побочных явлениях и реакциях

Основные положения Директивы 2001/20/ЕС -Защита испытуемых Ø Предполагаемый риск и неудобства были сопоставимы с ожидаемой пользой для каждого испытуемого и других пациентов в будущем (гарантия физического и психического благополучия); Ø Испытуемый или его законный представитель должен подписать информированное согласие на основе его информирования о КИ; Ø Испытуемый имеет право выйти из КИ в любое время и отозвать информированное согласие; Ø Предусмотрено положение о страховании или гарантии возмещения ущерба испытуемому; Ø Медицинский уход, предоставляемый испытуемым, врачебные решения – обязанность квалифицированного врача (или стоматолога); Ø Если испытуемый неспособен писать, то в исключительных случаях, как это предусмотрено в национальном законодательстве, может быть дано устное согласие в присутствии как минимум одного свидетеля. Статья 3

Основные положения Директивы 2001/20/ЕС Клинические исследования с участием несовершеннолетних КИ с участием несовершеннолетних проводятся если: v Было получено информированное согласие родителей или законного представителя v Несовершеннолетнему предоставляется информация в соответствии с его способностью к его пониманию информации о КИ v Исследователь учитывает ясно сформулированное желание несовершеннолетнего, который способен составить свое мнение о КИ v Не используются поощрения или финансовые стимулы (кроме денежной компенсации) v Есть прямая польза, КИ имеет отношение к клиническому состоянию несовершеннолетнего или может быть выполнено только у этой категории v Минимизированы боль, дискомфорт, страх или другие риски; v ЭК имеет опыт в области педиатрии или получает консультативную помощь Интересы пациента всегда стоят выше интересов науки и общества Статья 4

Продолжение Постановление Европейского Парламента и Совета 1901/2006 от 12. 2006 г. : «О лекарственных средствах для применения в педиатрии» Предоставлять: «План исследований в педиатрии» - программа научных разработок, цель которых обеспечить получение необходимых данных, для определения показаний, согласно которым может быть одобрен тот или другой лекарственный препарат для лечения детей и подростков Доказательство эффективности, безопасности и качества (рецептура, лекарственная форма) – в соответствии с Руководством ІСН Е 11

Основные положения Директивы 2001/20/ЕС Клинические исследования с участием недееспособных Применяются все требования, перечисленные для лиц, способных дать информированное согласие, а также: Ø Получено информированное согласие законного представителя; Ø Не используются поощрения и стимулы; Ø КИ имеет отношение к опасному для жизни или истощающему организм клиническому состоянию; Ø Минимизированы боль, дискомфорт (контролируются как предел риска, так и степень дистресса); Ø ЭК имеет опыт в области лечения таких пациентов; Ø Исследуемое ЛС принесет пользу пациенту, которая будет более значительней, чем риск или оно вовсе не несет риска. Статья 5

Основные положения Директивы 2001/20/ЕС -Рассмотрение материалов КИ Комитетом по вопросам этики Ø Для проведения КИ государства – члены принимают меры, необходимые для создания и функционирования Комитетов по вопросам этики (ЭК); Ø До начала КИ ЭК, рассмотрев материалы КИ: (заявку, протокол, брошюру, СV исследователей и вспомогательного персонала, качество помещенний и оборудование, ИС, гарантия защиты персональных данных, страховку или гарантию возмещения ущерба, выплата вознаграждения или компенсации, соглашения между спонсором и клиническим центром, процедуры по набору испытуемых и др. ) и дает заключение для проведения КИ; Ø Рассмотрение материалов КИ – 60 дней; Ø Если препараты предназначены для генной терапии или содержат генетически модифицированные организмы – рассмотрение 90 дней; Ø ЭК может однократно запросить дополнительные материалы; Ø Для многоцентрового КИ, на территории одного государства-члена, независимо от числа комитетов, предусмотрено принятие единого заключения ЭК в данном государстве-члене. Статья 6, 7

Основные положения Директивы 2001/20/ЕС -Начало проведения КИ Ø Спонсор может начинать КИ при наличии положительного заключения ЭК и тогда, когда уполномоченный орган государства – члена не проинформировал спонсора КИ о наличии оснований для отказа; процедура может проводиться параллельно; Ø До начала КИ спонсор подает в регуляторный орган заявку и материалы КИ на рассмотрение; Ø Рассмотрение материалов КИ – 60 дней; Ø Если препараты предназначены для генной терапии или содержат генетически модифицированные организмы – рассмотрение 90 дней и требуется письменное разрешение уполномоченного органа; Ø Уполномоченный орган может однократно запросить дополнительные материалы. NB! Нельзя проводить любое испытание генной терапии, которое приводит к изменению генетической идентичности половых клеток Статья 9

Основные положения Директивы 2001/20/ЕС - Проведение КИ Ø Внесение существенных поправок при проведении КИ (если они могут повлиять на безопасность пациентов); ØСпонсор сообщает о внесении поправок в уполномоченный орган и ЭК; ØЭК рассматривает и составляет заключение в течении 35 дней; ØПри положительном заключении ЭК и отсутствии возражений от уполномоченного органа спонсор проводит КИ в соответствии с указанными изменениями; ØВ течении 90 дней после завершения КИ спонсор сообщает об этом в уполномоченный орган и ЭК; ØПри досрочном завершении КИ спонсор предоставляет информацию в течении 15 дней с указанием причины. Статья 10

Основные положения Директивы 2001/20/ЕС - Приостановка КИ или нарушения Ø Государство –член имеет право приостановить или запретить КИ если имеется : Øобъективная информация, которая вызывает сомнения в безопасности или научной достоверности КИ Øобъективные данные о том, что спонсор, исследователь или другое лицо, участвующее в КИ, не выполняет свои обязанности Уполномоченный орган информирует ЭК и другие уполномоченные органы, где проводится КИ Статья 12

Основные положения Директивы 2001/20/ЕС - Производство исследуемого лекарственного средства q Государства-члены принимают все соответствующие меры для гарантии того, что производство или импорт исследуемых ЛС подлежит лицензированию q Исследуемые ЛС имеют подтверждение, что каждая серия произведена и проведена в соответствии со стандартами Надлежащей производственной практики q Маркировка препарата – как минимум на официальном(ых) языке(ах) государства – члена на вторичной упаковке исследуемых ЛС или, если отсутствует вторичная, то на первичной упаковке в соответствии с руководством по Надлежащей производственной практике для исследуемых ЛС Статья 13, 14

Основные положения Директивы 2001/20/ЕС - Проверка соответствия КИ и ИЛС требованиям GCP и GMP Ø Для проверки соблюдения требований GCP и GMP государства – члены назначают инспекторов для проверки мест, имеющих отношение к проведению КИ ØПосле проведения инспекции составляется отчет, который предоставляется спонсору и может предоставляться Агентству и ЭК по их запросу Статья 15 Требования к инспекторам и порядок проведения проверок определены Директивой 2005/28/ЕС от 08. 04. 2005: «Принципы и наставления GCP, касающиеся исследуемых ЛС предназначенных для использования человеком, а также требования к предоставлению разрешения на изготовления и импорт таких продуктов»

Директива 2005/28/ЕС - Инспекция Ø Инспекторы, назначенные Государствами-членами должны иметь образование университетского уровня или эквивалентное образование в области медицины, фармацевтики, фармакологии, токсикологии, а также принципов разработки ЛС и проведения КИ; ØИнспекторы должны быть ознакомлены с процедурами и системой регистрации клинических данных, а также с регуляторной системой государств – членов и других стран; ØИнспекторы должны иметь стандартные процедуры их работы и своих обязанностей; ØИнспектор должен иметь подтверждение (расписка) об отсутствия конфликта интересов, которая учитывается при распределении инспекторов для проведения проверок; ØДля проведения инспекций могут привлекаться эксперты соответствующей квалификации. Статья 21, 22

Директива 2005/28/ЕС - Порядок проведения инспекций Ø Проверка на предмет соответствия GCP может проводиться: üдо начала, во время проведения и после завершения КИ; üв рамках проверки заявок, поданных на регистрацию препаратов; üкак контрольные мероприятия после выдачи разрешения на регистрацию ØПроверка проводится в соответствии с руководствами для проведения проверок, предназначенных для взаимного признания результатов проверок в ЕС, для проведения совместных проверок с целью обмена информацией и обучения Статья 23 Руководство EMEA/INS/GCP/197226/2005, принято СНМР 20. 09. 2007 «Процедура для уведомления об инспекции GCP, требуемая EMEA» Рабочая группа инспекторов GCP

Руководство EMEA/INS/GCP/197226/2005, принято СНМР 20. 09. 2007 «Процедура для уведомления об инспекции GCP, требуемая EMEA» Рабочая группа инспекторов GCP В Руководстве описаны: v. Форма и содержание отчетов о проведенной инспекционной проверке v. Обязанности инспекторов, которые готовят отчет v. Обмен информацией между инспекторами v. Представление и принятие отчета ЕМЕА В отчете описываются результаты проверки и проводится оценка выявленным нарушениям: ØКритические ØЗначительные ØНезначительные
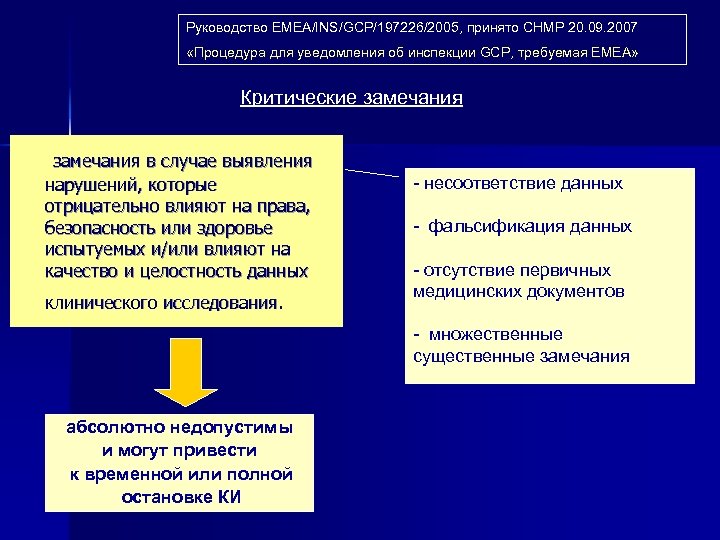
Руководство EMEA/INS/GCP/197226/2005, принято СНМР 20. 09. 2007 «Процедура для уведомления об инспекции GCP, требуемая EMEA» Критические замечания в случае выявления нарушений, которые отрицательно влияют на права, безопасность или здоровье испытуемых и/или влияют на качество и целостность данных клинического исследования. - несоответствие данных - фальсификация данных - отсутствие первичных медицинских документов - множественные существенные замечания абсолютно недопустимы и могут привести к временной или полной остановке КИ
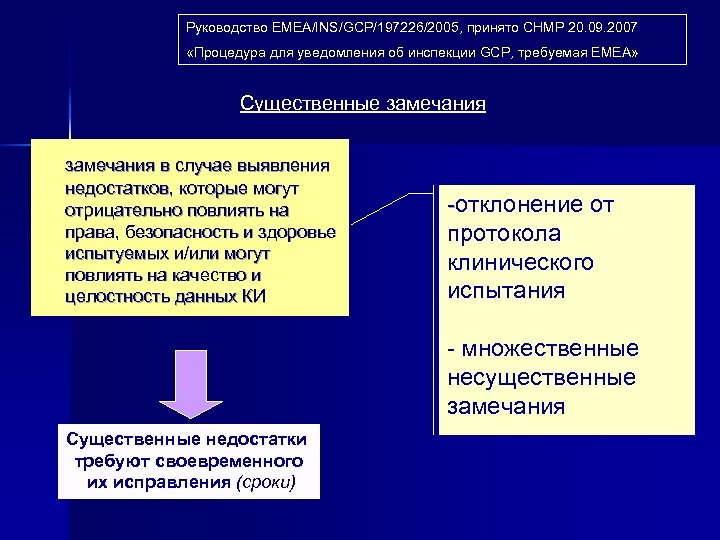
Руководство EMEA/INS/GCP/197226/2005, принято СНМР 20. 09. 2007 «Процедура для уведомления об инспекции GCP, требуемая EMEA» Существенные замечания в случае выявления недостатков, которые могут отрицательно повлиять на права, безопасность и здоровье испытуемых и/или могут повлиять на качество и целостность данных КИ -отклонение от протокола клинического испытания - множественные несущественные замечания Существенные недостатки требуют своевременного их исправления (сроки)

Руководство EMEA/INS/GCP/197226/2005, принято СНМР 20. 09. 2007 «Процедура для уведомления об инспекции GCP, требуемая EMEA» Несущественные замечания в случае выявления недостатков, которые не влияют на права, безопасность и здоровье испытуемых и/или не могут повлиять на качество и целостность данных КИ устранить недостатки в рабочем порядке
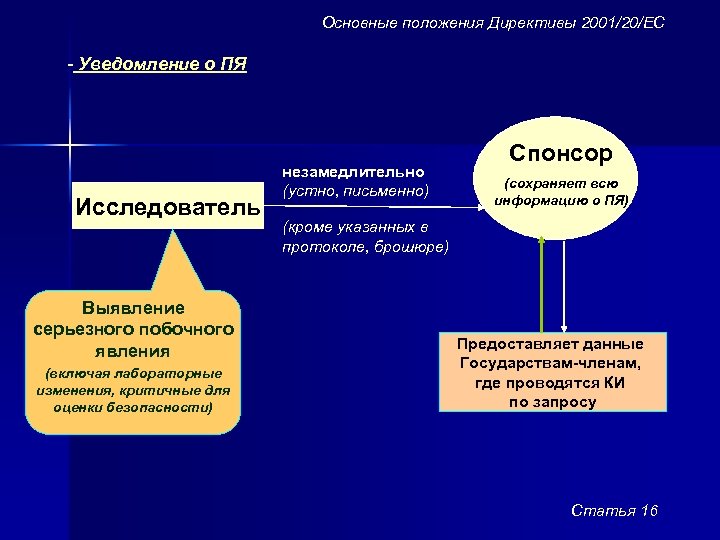
Основные положения Директивы 2001/20/ЕС - Уведомление о ПЯ Исследователь Выявление серьезного побочного явления (включая лабораторные изменения, критичные для оценки безопасности) незамедлительно (устно, письменно) Спонсор (сохраняет всю информацию о ПЯ) (кроме указанных в протоколе, брошюре) Предоставляет данные Государствам-членам, где проводятся КИ по запросу Статья 16
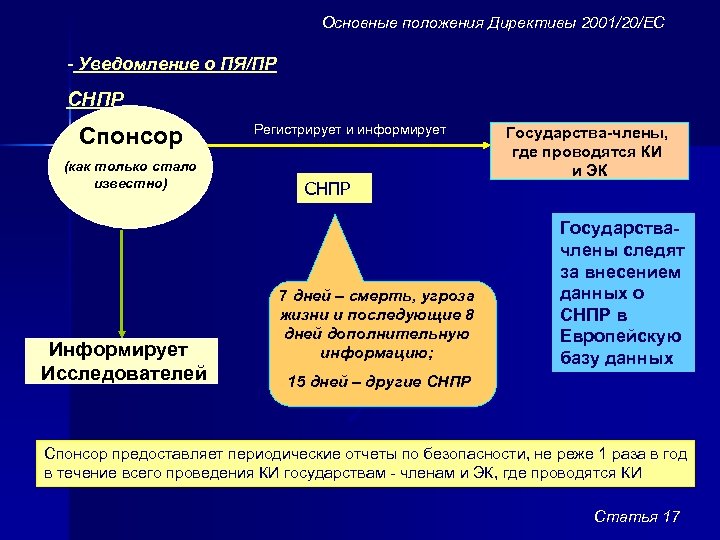
Основные положения Директивы 2001/20/ЕС - Уведомление о ПЯ/ПР СНПР Спонсор (как только стало известно) Информирует Исследователей Регистрирует и информирует СНПР 7 дней – смерть, угроза жизни и последующие 8 дней дополнительную информацию; Государства-члены, где проводятся КИ и ЭК Государствачлены следят за внесением данных о СНПР в Европейскую базу данных 15 дней – другие СНПР Спонсор предоставляет периодические отчеты по безопасности, не реже 1 раза в год в течение всего проведения КИ государствам - членам и ЭК, где проводятся КИ Статья 17

- Руководства, предназначенные для составления отчетов о ПЯ/ПР Ø ICH E 2 A «Оценка клинических данных по безопасности: определения и стандарты для экспресс-отчетности» июнь1995 г (Clinical Safety Data Management: Definitions and Standards for Expedited Reporting, CPMP/ICH/377/95) Ø ICH: E 2 F «Обновляемый отчет по безопасности ЛС, которые находяться в стадии разработки» август 2011 г. (DSUR-Development Safety Update Report, EMA/CHMP/ICH/ 309348/2008)

- Руководства, предназначенные для составления отчетов о ПЯ/ПР Основная цель DSUR Представлять всесторонний, содержательный ежегодный обзор и оценку важной информации по безопасности, собранную за отчетный период, имеющий отношение к исследуемому ЛС, находится ли он в продаже или нет, путем: (1) изучения, соответствует ли информация, полученная спонсором во время отчетного период ранее полученным знаниям о безопасности исследуемого лекарственного средства; (2) описания новых вопросов безопасности, которые могут влиять на защиту исследуемых/субъектов клинического испытания; (3) резюмирования имеющегося понимания и управления идентифицированными и потенциальными рисками; (4) предоставления обновленных данных о статусе программы клинического исследования/разработки и результатов исследования. DSUR должен быть лаконичным и предоставлять информацию, которая должна заверить регуляторные органы, что спонсоры адекватно проводят мониторинг и оценку установленного профиля безопасности исследуемого ЛС.
залог успешного проведения КИ: Строгое соблюдение действующего законодательства, конструктивное взаимодействие всех участников КИ качественные лекарственные средства с доказанной эффективностью и безопасностью
30611a550d8b237f98eb4af9e25d87ff.ppt