ТРАНСПОРТ ЖИРОВ ИЗ КИШЕЧНИКА Липиды




















ТРАНСПОРТ ЛИПИДОВ.ppt
- Количество слайдов: 21
 ТРАНСПОРТ ЖИРОВ ИЗ КИШЕЧНИКА
ТРАНСПОРТ ЖИРОВ ИЗ КИШЕЧНИКА
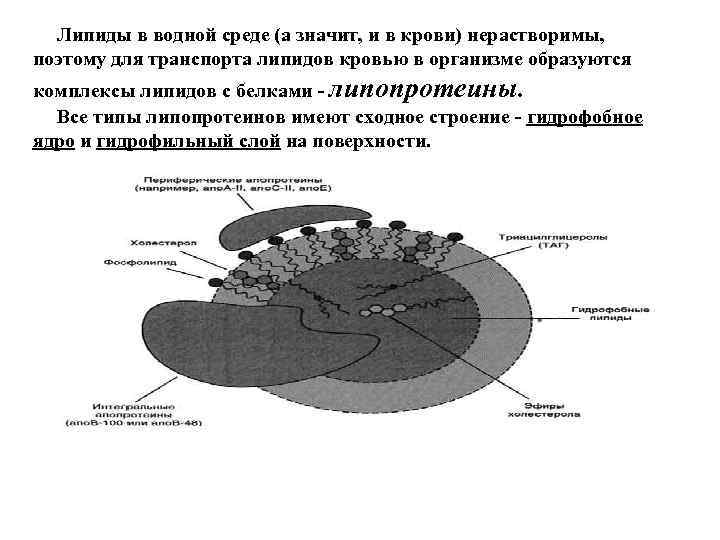
 Липиды в водной среде (а значит, и в крови) нерастворимы, поэтому для транспорта липидов кровью в организме образуются комплексы липидов с белками - липопротеины. Все типы липопротеинов имеют сходное строение - гидрофобное ядро и гидрофильный слой на поверхности.
Липиды в водной среде (а значит, и в крови) нерастворимы, поэтому для транспорта липидов кровью в организме образуются комплексы липидов с белками - липопротеины. Все типы липопротеинов имеют сходное строение - гидрофобное ядро и гидрофильный слой на поверхности.
 Гидрофильный слой образован белками, которые называют апопротеинами, и амфифильными молекулами липидов - фосфолипидами и холестеролом. Гидрофильные группы этих молекул обращены к водной фазе, а гидрофобные части - к гидрофобному ядру липопротеина, в котором находятся транспортируемые липиды.
Гидрофильный слой образован белками, которые называют апопротеинами, и амфифильными молекулами липидов - фосфолипидами и холестеролом. Гидрофильные группы этих молекул обращены к водной фазе, а гидрофобные части - к гидрофобному ядру липопротеина, в котором находятся транспортируемые липиды.
 Апопротеины выполняют несколько функций: • формируют структуру липопротеинов; • взаимодействуют с рецепторами на поверхности клеток и таким образом определяют, какими тканями будет захватываться данный тип липопротеинов; • служат ферментами или активаторами ферментов, действующих на липопротеины
Апопротеины выполняют несколько функций: • формируют структуру липопротеинов; • взаимодействуют с рецепторами на поверхности клеток и таким образом определяют, какими тканями будет захватываться данный тип липопротеинов; • служат ферментами или активаторами ферментов, действующих на липопротеины
 В организме синтезируются следующие типы липопротеинов: хиломикроны (ХМ), липопротеины очень низкой плотности (ЛПОНП), липопротеины промежуточной плотности (ЛППП), липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП).
В организме синтезируются следующие типы липопротеинов: хиломикроны (ХМ), липопротеины очень низкой плотности (ЛПОНП), липопротеины промежуточной плотности (ЛППП), липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП).
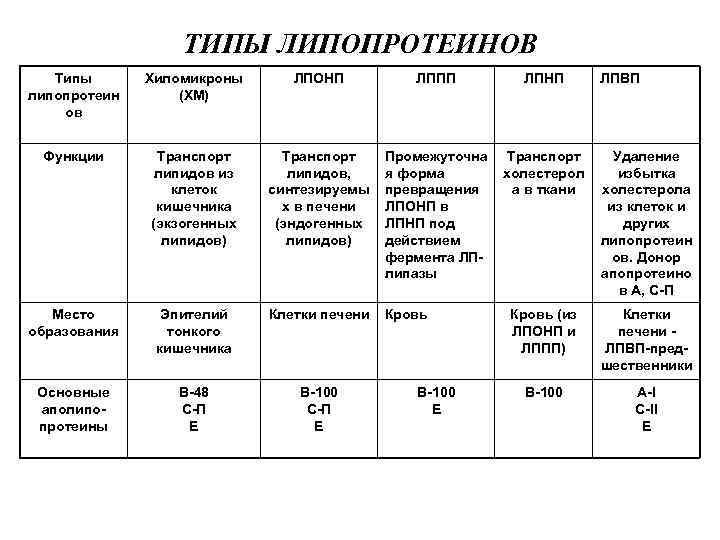
 ТИПЫ ЛИПОПРОТЕИНОВ Типы Хиломикроны ЛПОНП ЛППП ЛПНП ЛПВП липопротеин (ХМ) ов Функции Транспорт Промежуточна Транспорт Удаление липидов из липидов, я форма холестерол избытка клеток синтезируемы превращения а в ткани холестерола кишечника х в печени ЛПОНП в из клеток и (экзогенных (эндогенных ЛПНП под других липидов) действием липопротеин фермента ЛП- ов. Донор липазы апопротеино в А, С-П Место Эпителий Клетки печени Кровь (из Клетки образования тонкого ЛПОНП и печени - кишечника ЛППП) ЛПВП-пред- шественники Основные В-48 В-100 A-I аполипо- С-П Е С-II протеины Е Е
ТИПЫ ЛИПОПРОТЕИНОВ Типы Хиломикроны ЛПОНП ЛППП ЛПНП ЛПВП липопротеин (ХМ) ов Функции Транспорт Промежуточна Транспорт Удаление липидов из липидов, я форма холестерол избытка клеток синтезируемы превращения а в ткани холестерола кишечника х в печени ЛПОНП в из клеток и (экзогенных (эндогенных ЛПНП под других липидов) действием липопротеин фермента ЛП- ов. Донор липазы апопротеино в А, С-П Место Эпителий Клетки печени Кровь (из Клетки образования тонкого ЛПОНП и печени - кишечника ЛППП) ЛПВП-пред- шественники Основные В-48 В-100 A-I аполипо- С-П Е С-II протеины Е Е
 Каждый из типов ЛП образуется в разных тканях и транспортирует определённые липиды. Хиломикроны (ХМ) транспортируют экзогенные (пищевые жиры) из кишечника в ткани, поэтому триацилглицеролы составляют до 85% массы этих частиц. ЛП хорошо растворимы в крови, имеют небольшой размер и отрицательный заряд на поверхности. Некоторые ЛП легко проходят через стенки капилляров кровеносных сосудов и доставляют липиды к клеткам.
Каждый из типов ЛП образуется в разных тканях и транспортирует определённые липиды. Хиломикроны (ХМ) транспортируют экзогенные (пищевые жиры) из кишечника в ткани, поэтому триацилглицеролы составляют до 85% массы этих частиц. ЛП хорошо растворимы в крови, имеют небольшой размер и отрицательный заряд на поверхности. Некоторые ЛП легко проходят через стенки капилляров кровеносных сосудов и доставляют липиды к клеткам.
 Методы исследования Разделение липопротеинов сыворотки крови. А - метод ультрацентрифугирования. Б - метод электрофореза в полиакриламидном геле через 2 ч после еды. Метод ультрацентрифугирования позволяет разделить ЛП, используя их различие в плотности, которая зависит от соотношения количества липидов и белков в частице. Так как жир имеет меньшую, чем вода, плотность, то ХМ, содержащие более 85% жиров, располагаются на поверхности сыворотки крови, а ЛПВП, содержащие наибольшее количество белков, имеют самую большую плотность и при центрифугировании располагаются в нижней части центрифужной пробирки. Так как ЛП впервые были выделены из сыворотки крови методом ультрацентрифугирования, то в названии указывают плотность частиц.
Методы исследования Разделение липопротеинов сыворотки крови. А - метод ультрацентрифугирования. Б - метод электрофореза в полиакриламидном геле через 2 ч после еды. Метод ультрацентрифугирования позволяет разделить ЛП, используя их различие в плотности, которая зависит от соотношения количества липидов и белков в частице. Так как жир имеет меньшую, чем вода, плотность, то ХМ, содержащие более 85% жиров, располагаются на поверхности сыворотки крови, а ЛПВП, содержащие наибольшее количество белков, имеют самую большую плотность и при центрифугировании располагаются в нижней части центрифужной пробирки. Так как ЛП впервые были выделены из сыворотки крови методом ультрацентрифугирования, то в названии указывают плотность частиц.
 Методы исследования Разделение липопротеинов сыворотки крови. А - метод ультрацентрифугирования. Б - метод электрофореза в полиакриламидном геле через 2 ч после еды. В клинических лабораториях обычно применяют метод электрофореза. Скорость движения частиц при электрофорезе зависит от их заряда и размера. Заряд, в свою очередь, зависит от количества белков на поверхности ЛП. При электрофорезе в геле все типы ЛП движутся к положительному полюсу; ближе к старту располагаются ХМ, а ЛПВП, имеющие наибольшее количество белков и наименьший размер, удаляются от старта дальше других частиц.
Методы исследования Разделение липопротеинов сыворотки крови. А - метод ультрацентрифугирования. Б - метод электрофореза в полиакриламидном геле через 2 ч после еды. В клинических лабораториях обычно применяют метод электрофореза. Скорость движения частиц при электрофорезе зависит от их заряда и размера. Заряд, в свою очередь, зависит от количества белков на поверхности ЛП. При электрофорезе в геле все типы ЛП движутся к положительному полюсу; ближе к старту располагаются ХМ, а ЛПВП, имеющие наибольшее количество белков и наименьший размер, удаляются от старта дальше других частиц.
 Состав ЛП крови значительно изменяется в течение суток. В абсорбтивный период (особенно при употреблении жирной пищи) в крови появляются ХМ. ХМ Богатая углеводами пища способствует образованию ЛПОНП , так как эти ЛП транспортируют жиры, синтезированные в печени из углеводов. В постабсорбтивный период и при голодании в крови присутствуют только ЛПНП и ЛПВП , основная функция которых заключается в транспорте холестерола.
Состав ЛП крови значительно изменяется в течение суток. В абсорбтивный период (особенно при употреблении жирной пищи) в крови появляются ХМ. ХМ Богатая углеводами пища способствует образованию ЛПОНП , так как эти ЛП транспортируют жиры, синтезированные в печени из углеводов. В постабсорбтивный период и при голодании в крови присутствуют только ЛПНП и ЛПВП , основная функция которых заключается в транспорте холестерола.
 Образование хиломикронов (ХМ) Жиры, образовавшиеся в результате ресинтеза в клетках слизистой оболочки кишечника, упаковываются в ХМ. Основной апопротеин в составе ХМ - белок апо. В-48. Этот белок закодирован в том же гене, что и белок ЛПОНП - В-100, который синтезируется в печени. В-100 В кишечнике в результате посттранскрипционных превращений "считывается" последовательность м. РНК , которая кодирует только 48% от длины белка В-100 , поэтому этот белок называется апо. В-48.
Образование хиломикронов (ХМ) Жиры, образовавшиеся в результате ресинтеза в клетках слизистой оболочки кишечника, упаковываются в ХМ. Основной апопротеин в составе ХМ - белок апо. В-48. Этот белок закодирован в том же гене, что и белок ЛПОНП - В-100, который синтезируется в печени. В-100 В кишечнике в результате посттранскрипционных превращений "считывается" последовательность м. РНК , которая кодирует только 48% от длины белка В-100 , поэтому этот белок называется апо. В-48.
 Белок апо. В-48 синтезируется в шероховатом ЭР и там же гликозилируется. Затем в аппарате Гольджи происходит формирование ХМ, называемых "незрелыми". По механизму экзоцитоза они выделяются в лимфатическую систему кишечных ворсинок, и через главный грудной лимфатический проток попадают в кровь. В лимфе и крови с ЛПВП на ХМ переносятся апопротеины Е (апо. Е) и С-П (апо. С-П) и ХМ становятся «зрелыми» .
Белок апо. В-48 синтезируется в шероховатом ЭР и там же гликозилируется. Затем в аппарате Гольджи происходит формирование ХМ, называемых "незрелыми". По механизму экзоцитоза они выделяются в лимфатическую систему кишечных ворсинок, и через главный грудной лимфатический проток попадают в кровь. В лимфе и крови с ЛПВП на ХМ переносятся апопротеины Е (апо. Е) и С-П (апо. С-П) и ХМ становятся «зрелыми» .
 Функции апопротеинов • В-48 - основной белок ХМ; • В-100 - основной белок ЛПОНП, ЛППП, взаимодействует с рецепторами ЛПНП; • С-II - активатор ЛП-липазы, переносится с ЛПВП на ХМ и ЛПОНП в крови; • Е - взаимодействует с рецепторами ЛПНП; • A-I - активатор фермента лецитингхолестеролацилтрансферазы (ЛХАТ).
Функции апопротеинов • В-48 - основной белок ХМ; • В-100 - основной белок ЛПОНП, ЛППП, взаимодействует с рецепторами ЛПНП; • С-II - активатор ЛП-липазы, переносится с ЛПВП на ХМ и ЛПОНП в крови; • Е - взаимодействует с рецепторами ЛПНП; • A-I - активатор фермента лецитингхолестеролацилтрансферазы (ЛХАТ).
 ХМ имеют довольно большой размер, поэтому после приёма жирной пищи они придают плазме крови опалесцирующий, похожий на молоко, вид. ХМ транспортируют жир к различным тканям, где он утилизируется, поэтому концентрация ХМ в крови постепенно снижается, и плазма опять становится прозрачной. ХМ исчезают из крови в течение нескольких часов.
ХМ имеют довольно большой размер, поэтому после приёма жирной пищи они придают плазме крови опалесцирующий, похожий на молоко, вид. ХМ транспортируют жир к различным тканям, где он утилизируется, поэтому концентрация ХМ в крови постепенно снижается, и плазма опять становится прозрачной. ХМ исчезают из крови в течение нескольких часов.
 Жирные кислоты поступают в адипоциты и используются для синтеза жиров. В постабсорбтивном состоянии , когда количество жиров в крови снижается, ЛП-липаза сердечной мышцы продолжает гидролизовать жиры в составе ЛПОНП , которые присутствуют в крови в небольшом количестве, и жирные кислоты используются этой тканью как источники энергии, даже при низкой концентрации жиров в крови. ЛП-липазы нет в печени, на поверхности печени есть - печёночная липаза , не действующая на зрелые ХМ, но гидролизующая жиры в ЛППП , которые образуются из ЛПОНП.
Жирные кислоты поступают в адипоциты и используются для синтеза жиров. В постабсорбтивном состоянии , когда количество жиров в крови снижается, ЛП-липаза сердечной мышцы продолжает гидролизовать жиры в составе ЛПОНП , которые присутствуют в крови в небольшом количестве, и жирные кислоты используются этой тканью как источники энергии, даже при низкой концентрации жиров в крови. ЛП-липазы нет в печени, на поверхности печени есть - печёночная липаза , не действующая на зрелые ХМ, но гидролизующая жиры в ЛППП , которые образуются из ЛПОНП.
 В результате действия ЛП-липазы на жиры образуются жирные кислоты и глицерол. Основная масса жирных кислот проникает в ткани. В жировой ткани в абсорбтивный период жирные кислоты депонируются в виде триацилглицеролов , в сердечной мышце и работающих скелетных мышцах используются как источник энергии. Глицерол , растворим в крови, транспортируется в печень, где в абсорбтивный период может быть использован для синтеза жиров.
В результате действия ЛП-липазы на жиры образуются жирные кислоты и глицерол. Основная масса жирных кислот проникает в ткани. В жировой ткани в абсорбтивный период жирные кислоты депонируются в виде триацилглицеролов , в сердечной мышце и работающих скелетных мышцах используются как источник энергии. Глицерол , растворим в крови, транспортируется в печень, где в абсорбтивный период может быть использован для синтеза жиров.
 В результате действия ЛП-липазы на ХМ количество жиров в них снижается на 90%, уменьшаются размеры частиц, апопротеин С-П переносится обратно на ЛПВП. Образовавшиеся частицы называются остаточными ХМ. Они содержат в себе фосфолипиды, холестерол, жирорастворимые витамины и апопротеины В-48 и Е.
В результате действия ЛП-липазы на ХМ количество жиров в них снижается на 90%, уменьшаются размеры частиц, апопротеин С-П переносится обратно на ЛПВП. Образовавшиеся частицы называются остаточными ХМ. Они содержат в себе фосфолипиды, холестерол, жирорастворимые витамины и апопротеины В-48 и Е.
 Остаточные ХМ захватываются гепатоцитами, которые имеют рецепторы, взаимодействующие с этими апопротеинами. Путём эндоцитоза остаточные ХМ попадают внутрь клеток, ферменты лизосом гидролизуют белки и липиды, а затем ХМ утилизируются. Жирорастворимые витамины и экзогенный холестерол используются в печени или транспортируются в другие ткани.
Остаточные ХМ захватываются гепатоцитами, которые имеют рецепторы, взаимодействующие с этими апопротеинами. Путём эндоцитоза остаточные ХМ попадают внутрь клеток, ферменты лизосом гидролизуют белки и липиды, а затем ХМ утилизируются. Жирорастворимые витамины и экзогенный холестерол используются в печени или транспортируются в другие ткани.
 После приёма пищи, содержащей жиры, развивается физиологическая гипертриглицеролемия и гиперхиломикронемия, которая может продолжаться до нескольких часов. Скорость удаления ХМ из кровотока зависит от: • активности ЛП-липазы; • присутствия ЛПВП, поставляющих апопротеины С-II и Е для ХМ; • активности переноса апо С-II и апо Е на ХМ.
После приёма пищи, содержащей жиры, развивается физиологическая гипертриглицеролемия и гиперхиломикронемия, которая может продолжаться до нескольких часов. Скорость удаления ХМ из кровотока зависит от: • активности ЛП-липазы; • присутствия ЛПВП, поставляющих апопротеины С-II и Е для ХМ; • активности переноса апо С-II и апо Е на ХМ.
 Генетические дефекты любого из белков, участвующих в метаболизме ХМ, приводят к развитию семейной гиперхиломикронемии. У таких больных в постабсорбтивном периоде концентрация триацилглицеролов повышена (более 200 мг/дл), плазма крови по виду напоминает молоко и при оставлении на холоде (+4 °С) в ней всплывают белые жирные хлопья, что характерно для гипертриглицеролемии и гиперхиломикронемии.
Генетические дефекты любого из белков, участвующих в метаболизме ХМ, приводят к развитию семейной гиперхиломикронемии. У таких больных в постабсорбтивном периоде концентрация триацилглицеролов повышена (более 200 мг/дл), плазма крови по виду напоминает молоко и при оставлении на холоде (+4 °С) в ней всплывают белые жирные хлопья, что характерно для гипертриглицеролемии и гиперхиломикронемии.
 В тяжёлых случаях при этом заболевании происходит • отложение триацилглицеролов в коже и сухожилиях, • у пациентов рано нарушается память, появляются боли в животе из-за сужения просвета сосудов и уменьшения кровотока, • нарушается функция поджелудочной железы Это очень часто бывает причиной смерти больных.
В тяжёлых случаях при этом заболевании происходит • отложение триацилглицеролов в коже и сухожилиях, • у пациентов рано нарушается память, появляются боли в животе из-за сужения просвета сосудов и уменьшения кровотока, • нарушается функция поджелудочной железы Это очень часто бывает причиной смерти больных.

