трансплантация октябрь 2015-2.ppt
- Количество слайдов: 129

Трансплантация почки (ведение больных в отдаленном периоде после трансплантации почки ) СЕМЕНОВА Е. В. Доцент кафедры внутренних болезней и нефрологии Гос. мед. Университета им. И. И. Мечникова к. м. н нефролог-трансплантолог

Наиболее важные стратегические направления ведения пациентов в отдаленном периоде после трансплантации почки • • • Уменьшать объем иммуносупрессии, когда это возможно Предупреждать несоблюдение медицинских рекомендаций Строго мониторировать почечную функцию Выполнять раннюю биопсию, делать ее чаще для установления острого отторжения в отдаленном периоде Своевременное выявление и лечение инфекций (ЦМВинфекции, грибковых инфекций, реактивации вирусных гепатитов и др. ) Коррекция гиперлипидемии Коррекция АД Отказ от курения Онконастороженность (рак молочной железы, шейки матки, кожи, рак предстательной железы) Иммунизация против гриппа и пневмококковой пневмонии Профилактика и лечение остеопороза (альфакальцидол, карбонат кальция, бисфосфонаты- алендронат). Лечение сопутствующих заболеваний (заболевания сердечно-сосудистой системы, легких, ЖКТ).

Инфекции в отдаленном периоде после трансплантации почки Нокардиоз остается значимой инфекцией после трансплантации почки, хотя использование бисептола уменьшило его частоту. Факторами риска являются избыточная иммуносупрессия, лечение ранних кризов отторжения почечного трансплантата, нейтропения и уремия. Инфекция развивается остро или подостро в легких, вызывая пневмонию, но может поражаться головной мозг, кожа и подкожная клетчатка, кости и глаза. Бисептол в больших дозах (2, 5 -10 мг/кг два раза в день в зависимости от тяжести заболевания) является препаратом выбора для лечения большинства инфекций, вызванных различными видами Nocardia. Имипенем, амикацин, цефалоспорины (цефтриаксон, цефотаксим, цефуроксим), хинолоны также могут использоваться в комбинациях при тяжелых формах нокардиоза. После излечения сохраняется высокий риск рецидива заболевания, антибактериальная терапия продолжается в течение 12 месяцев.

Клостридиоз Клостридиоз выявляется у реципиентов почечного трансплантата, как и у больных в общей популяции. Синдром, характерный для клостридиоза, представлен немотивированной слабостью, диареей, кишечной обструкцией, псевдомембранозным колитом, возможно образование абсцесса малого таза. При развитии тяжелого поражения толстой кишки производят колэктомию. Антибактериальная терапия остается высокозначимым фактором риска клостридиоза. Более того, иммуносупрессия может рассматриваться как фактор, способствующий молниеносному течению инфекции. При толстокишечной дисрегуляции у пациентов развиваются водноэлектролитные нарушения и уменьшается всасывание иммуносупрессивных препаратов. При тяжелой инфекции предпочтительным антибиотиком считается ванкомицин (1 г/день. ), назначаемый перорально в течение 10 дней. В менее тяжелых случаях или при непереносимости ванкомицина применяют метронидазол, также перорально.

Туберкулез Микобактериальные инфекции: туберкулез и другие микобактериальные инфекции могут проявляться уже в раннем послеоперационном периоде (в течение 2 -х месяцев после трансплантации почки), а также в отдаленнном периоде после операции. Частота активного туберкулеза колеблется в этой популяции больных от 1 до 4% и с большой вероятностью будет увеличиваться, в связи с нарастанием заболеваемости туберкулезом в общей популяции. Легочные формы заболевания вызываются М. tuberculosis, М. kansasii, М. xenopi, М. fortuitum. При этом могут поражаться нескольких долей легкого, возникают фокальные инфильтраты и узелки, эмпиема плевры, плевриты или сочетания этих поражений. Необычная клиническая картина этих инфекций у реципиентов почечного трансплантата может отсрочить диагноз, что приводит к запущенным формам заболевания. Больные после пересадки почки, имевшие в анамнезе микобактериальные инфекции, старые гранулематозные очаги или прибывшие из стран с большой распространенностью туберкулеза, должны обследоваться на предмет реактивации инфекции.

Туберкулез У 40% больных с установленным после трансплантации диагнозом определяется диссеминация заболевания с вовлечением в процесс кожи, скелета (кости и суставы) и ЦНС. Наличие гранулемы в периферических тканях предполагает диссеминированное заболевание. Лечение туберкулеза у реципиентов почечного трансплантата обычно эффективно. Однако с увеличением полимедикаментозной устойчивости микобактерий необходимо начинать лечение как минимум 4 противотуберкулезными препаратами, пока не будет получена чувствительность возбудителя. Начальный режим должен состоять из двухмесячного приема изониазида, рифампицина, пиразинамида, этамбутола. После этого не менее двух препаратов принимаются в течение 4 -12 месяцев с учетом результатов чувствительности возбудителя (например, может быть пролонгирована терапия только изониазидом и рифампицином при положительной чувствительности микобактерий). 20

Туберкулез Лечение у больных с почечным трансплантатом должно продолжаться не менее 12 месяцев. Побочные эффекты при лечении противотуберкулезными препаратами включают: гепатит (при использовании изониазида, пиразинамида, рифампицина он возникает чаще и имеет тяжелое течение), невриты и нейропатии глазного нерва (изониазид, этамбутол), снижение слуха, азотемию (стрептомицин), дискомфорт в животе (изониазид, этамбутол, рифампицин, пиразинамид). Изониазид и рифампицин, также как и циклоспорин, взаимодействуют с системой цитохрома Р 450. Изониазид может способствовать накоплению циклоспорина, тогда как рифампицин является индуктором цитохрома Р 450 и уменьшает концентрацию ингибиторов кальциневрина в крови, увеличивая риск отторжения, развивающегося при субоптимальных концентрациях циклоспорина. Эти взаимодействия обычно определяются через 1 -3 дня от начала лечения противотуберкулезными препаратами. Доза циклоспорина подбирается индивидуально и регулярно мониторируется.

ГРИБКОВЫЕ ИНФЕКЦИИ Оппортунистическая грибковая инфекция чаще развивается в срок от 1 до 6 месяцев после трансплантации почки. Но наиболее часто через 1 месяц после трансплантации, когда объем имуносупрессивной терапии максимален. Предрасполагающими факторами развития грибковой инфекции являются: Использование кортикостероидов, особенно больших доз, для лечения отторжения. Назначение антибиотиков широкого спектра действия. Избыточная иммуносупрессия. Использование инвазивных катетеров. Длительные по времени и повторные операции. Повреждение слизистой желудочно-кишечного тракта, мочевого пузыря, сосудистые осложнения и гипергликемия. Большинство микозов являются нозокомиальной инфекцией. Кандидоз, аспергиллез, зигомикоз, криптоккоз, и эндемичные возбудители гистоплазмозов, бластомикозов вызывают реактивацию дремлющей инфекции или первичную инфекцию.

Тактика ведения больных после трансплантации почки при возникновении микозов У реципиентов почечного трансплантата возникновение микотических поражений требует изменения режима иммуносупрессии. Дозы стероидов должны быть максимально уменьшены, уровень циклоспорина и такролимуса крови предпочтительно сохранять минимально допустимых пределах, и в ряде случаев эти препараты могут быть временно отменены. При недостаточном клиническом эффекте лечения для сохранения жизни больного требуется отмена иммуносупрессивной терапии и возвращение к программному гемодиализу.

Кандидоз ДИАГНОСТИКА МИКОЗОВ Различные виды Candida часто выделяются из материала, полученного из респираторного тракта, мочи, кала, но это не всегда связано с болезнью у пациентов, получающих кортикостероиды и антибиотики широкого спектра действия. В раннем послеоперационном периоде может обнаруживаться орофарингеальный кандидоз и кандидоз пищевода, желудка. Диагностика орофарингеального кандидоза – микроскопия и посев соскоба с языка, миндалин, десен, слизистой щек; кандидоза пищевода и желудка – эндоскопия с биопсией пораженных участков, посев и гистологическое исследование биоптатов. Повторное выделение культуры грибов, полученной из одного очага или из множественных очагов, может свидетельствовать об инвазивном или диссеминированном заболевании при соответствующей клинической картине. У пациентов с установленным уретеровезикальным стентом при повторном выделении грибов из мочи необходимо удалить стент для более эффективного подавления грибковой инфекции. Кандидурия в сочетании с клиническими или инструментальными признаками инфекции мочевых путей является показанием для применения противогрибковых препаратов.

Лечение кандидоза Для профилактики кандидоза кожи и слизистых во время индукционного периода иммуносупрессии или проведении антикризовой терапии кортикостероидами используются нистатин, леворин. Нистатин и леворин не применяются для лечения микоза. При поверхностном и инвазивном кандидозе назначают флуконазол. При неосложненном течении послеоперационного периода рутинно не следует начинать лечение системными противогрибковыми препаратами. При длительной терапии бактериальных инфекций антибиотиками широкого спектра действия целесообразно применять антимикотики, несмотря на отсутствие сопутствующей грибковой инфекции. При подозрении на наличие инвазивного микоза противогрибковые препараты: вориконазол, каспофунгин, липидные формы амфотерицина B, назначаются эмпирически в течение 2 -х недель.

Аспергиллез При выделении из дыхательных путей культуры Aspergillus (особенно А. fumigatus(40 -70%), A. flavus(10 -25%), А. niger(10 -20%)) необходимо начать поиск инвазивной формы заболевания. Возбудители инвазивного аспергиллеза распространены повсеместно: в почве, на растениях, в пыли, компонентах зданий, в пищевых продуктах (чай в пакетиках), системах вентиляции. Инфицирование происходит при ингаляции конидий Aspergillus во вдыхаемом воздухе. От человека к человеку ни одна форма аспергиллеза не передается. При проведении ремонта могут наблюдаться вспышки внутрибольничного аспергиллеза особенно у пациентов, получающих иммуносупрессивную терапию. При инвазивном аспергиллезе первичное поражение легких выявляют в 80 -98%, придаточных пазух носа – у 2 -10%, а также нередко поражение центральной нервной системы (3 -20%). Прогноз заболевания зависит от величины периода времени с момента появления клинических проявлений до установки диагноза, адекватности лечения и объема иммуносупрессивной терапии. Без лечения инвазивный аспергиллез всегда заканчивается летальным исходом.

Аспергиллез Для диагностики аспергиллеза применяются: спиральная компьютерная томография грудной клетки и головного мозга, рентгенологическое исследование легких (признаки легочной формы аспергиллеза у реципиентов почечного трансплантата включают узелки, диффузные или клиновидные участки затемнений, эмпиему, полостные формы, трахеобронхит или комбинацию паренхиматозных изменений), фибробронхоскопия с исследованием промывных вод бронхов, определение галактоманнана в бронхо-альеолярном лаваже (БАЛ) и сыворотке крови, микроскопия и посев респираторных субстратов, при необходимости биопсия подозрительных участков поражения.

Лечение аспергиллеза Для лечения аспергиллеза препаратом выбора является вориконазол (вифенд): пероральный прием в первые сутки 800 мг вориконазола, в последующие дни – 400 мг/сут. Альтернативные препараты: каспофунгин (кансидос) – первое введение 75 мг (в/в), в дальнейшем по 50 мг/сут. (в/в); амфотерицин В назначается в высокой дозе (1 -1, 5 г/кг/сут), позаконазол 800 мг/сут, перорально. Комбинированная терапия – при неэффективности стартовой терапии вориконазолом: каспофунгин в сочетании с вориконазолом или липидным комплексом амфотерицина В. Длительность антимикотической терапии составляет от 3 -х до 5 -ти месяцев. После успешного лечения инвазивного аспергиллеза препаратами первой линии можно назначать итраконазол на неопределенный период в качестве поддерживающей терапии. Однако следует строго мониторировать концентрацию ингибиторов кальциневрина в крови, чтобы избежать избыточной иммуносупрессии и неблагоприятного, как следствие, исхода заболевания.

Криптококкоз Возбудителем криптококкоза является Cryptococcus neoformans/ Природный источник загрязнения — почва, загрязненная пометом голубей, гниющими овощами и фруктами. Инфицирование — при вдыхании пыли, содержащей мелкие клетки гриба. Органы мишени — легкие, головной мозг, кожа, костная ткань. Поражение ЦНС - менингит, менингоэнцефалит. Характерно повышение ВЧД. Длительное развитие болезни (иногда месяцы). Диагностика: цереброспинальная жидкость, мокрота и БАЛ, кровь, моча — микроскопия, в крови и ликворе (100%) - определение глюкуроноксиломаннана (антиген капсулы). КТ грудной и брюшной полости, МРТ головного мозга. Лечение: при легочной форме - флуконазол 400 мг/сут (длительно -6 -12 мес, иногда пожизненно), при тяжелых формах с поражением ЦНС — липосомальный амфо. В 4 мг/кг/сут — 2 недели, затем флюконазол 400800 мг/сут — 8 недель, 200 мг/сут — 6 -12 мес.

Пневмоцистоз Рneumoсуstis carinii вызывает пневмонию в первые 1 -6 месяцев после трансплантации. Клиника: лихорадка, непродуктивный кашель, артериально-альвеолярная диссоциация, диффузная интерстициальная инфильтрация или фокальные ателектазы. Диагностика осуществляется с помощью микроскопии и посева бронхоальвеолярного лаважа и выполнение трансбронхиальной биопсии, которые признаны высоко чувствительными методами идентификации возбудителя. Лечение: Для профилактики пневмоцистной пневмонии после трансплантации почки в комплексное лечение включают бисептол (480 мг х 2 р/сут. ) в течение 3 -4 месяцев. Начинают лечение пневмоцистной пневмонии с триметопримсульфаметоксазола (15 -20 мг/кг/сут) с учетом почечной функции в течение 14 -21 дня. Препаратами второй линии являются пентамидин, который вводится внутривенно (3 -4 мг/кг/сут), и дапсон/триметоприм (100 мг дапсона ежедневно и триметоприм 15 мг/кг/сут). Побочными эффектами триметоприма являются нефротоксичность, панкреатит, угнетение активности костного мозга. Дапсон способствует развитию гемолитической анемии с дефицитом глюкозо-6 -фосфат-дегидрогеназы. Легкая и средней тяжести формы пневмоцистной пневмонии могут лечиться с помощью атовакона (750 per os трижды в день в течение 21 дня) у пациентов, не переносящих бисептол. Используют также пентамидин, дапсон по отдельности или в сочетании с триметопримом.

ВИРУСНЫЕ ИНФЕКЦИИ Цитомегаловирусная инфекция (ЦМВ-инфекция) ЦМВ-инфекция первично манифестируется спустя 1 месяц после трансплантации с частотой 30 -78%, зависящей от иммунологического статуса реципиента и донора. Серонегативный реципиент, получивший трансплантат от серопозитивного донора, подвержен наибольшему риску, особенно после использования антилимфоцитарных препаратов. Различают ЦМВ статус у доноров и реципиентов почечного трансплантата: R-D-; R+D-; R-D+; R+D+. Первичная ЦМВ-инфекция развивается у серонегативного реципиента и может быть бессимптомной. ЦМВ-болезнь представляет собой ЦМВинфекцию с симптомами или органными поражениями, которые могут обуславливать тяжесть заболевания и смертность. Симптоматическая ЦМВ-инфекция может быть представлена ЦМВсиндромом (лихорадка, тромбоцитопения, лейкопения, увеличение титра антигена ЦМВ) и инвазивной ЦМВ-болезнью (т. е. с поражением органов и систем: пневмонит, гепатит, гастроинтестинальные поражения).

Цитомегаловирусная инфекция (ЦМВ-инфекция) Вторичная ЦМВ-инфекция представляет собой реактивацию латентной инфекции у ранее инфицированного серопозитивного хозяина или реинфекцию/суперинфекцию новым вирусом. Активная ЦМВ-иифекция, первичная или вторичная, может быть асимптомной или симптомной и характеризуется вирусной репликацией и специфическим иммунным ответом на ЦМВ. Латентная ЦМВ-инфекция проявляется длительной персистенцией вируса без репликации в организме здорового серопозитивного хозяина. Иммуносупрессивная терапия является мощным провокатором превращения латентной инфекции в активную. Предрасполагающими факторами к ЦМВ-инфекции считаются ЦМВположительный статус донора и реципиента, использование продуктов крови от ЦМВ-серопозитивного донора, эпизоды острого отторжения, совокупная иммуносупрессия, использование антилимфоцитарных препаратов, ретрансплантация.

Цитомегаловирусная инфекция (ЦМВ-инфекция) ЦМВ вызывает иммуномодулирующие эффекты (уменьшение соотношения Тхелперы/Т-супрессоры), что приводит к возникновению оппортунистических суперинфекций, дисфункции или отторжению трансплантата. ЦМВ-инфекция вызывает выработку провоспалительных цитокинов, а именно: фактора некроза опухоли, который связывается с латентно инфицированной клеткой, вызывая ядерную транскрипцию факторов, усиливающих репликацию ЦМВ вызывает выработку антиэндотелиальных антител, которые являются фактором риска как острого, так и хронического отторжения. ЦМВ-инфекция проявляется различными клиническими синдромами, к которым относятся лихорадка, общее недомогание, лейкопения, повышение уровня трансаминаз. При диссеминированной ЦМВ-инфекции поражаются многие органы. ЦМВ-пневмонит – наиболее тяжелое проявление инфекции – манифестируется диспноэ, гипоксемией, интерстициальными инфильтратами в легких, подтверждается определением в крови ЦМВ-антигена (ДНК-ЦМВ), наличием специфических вирусных включений в клетках бронхоальвеолярного лаважа.

Цитомегаловирусная инфекция (ЦМВ-инфекция) Проявлением болезни могут быть колит и язвенные поражения гастроинтестинального тракта, холецистит, эзофагит, дуоденит, гепатит. При диагностической эндоскопии (ФГДС, ФКС) можно обнаружить солитарные или множественные изъязвления или геморрагии. Биопсийный материал, полученный при эндоскопии, должен быть изучен методами иммуногистохимии или цитологически с целью обнаружения ЦМВ-антигена или вирусных включений. ЦМВ-гепатит подтверждается иммуногистохимически и цитологически при повышении трансаминаз. При фундоскопии диагностируется ретинит. ЦМВ-поражение центральной нервной системы (менингит, энцефалит, миелит) трудно выявить. В плане дифференциальной диагностики необходимо обследовать больного на наличие и других нейротропных оппортунистических инфекций. Рецидив ЦМВ-болезни определяется при повторном возникновении описанных симптомов после специфического лечения. Рефрактерная ЦМВ-болезнь может отражать устойчивость вируса в результате его мутации или глубокой иммуносупрессии.

Цитомегаловирусная инфекция (ЦМВ-инфекция) Проявлением болезни могут быть колит и язвенные поражения гастроинтестинального тракта, холецистит, эзофагит, дуоденит, гепатит. При диагностической эндоскопии (ФГДС, ФКС) можно обнаружить солитарные или множественные изъязвления или геморрагии. Биопсийный материал, полученный при эндоскопии, должен быть изучен методами иммуногистохимии или цитологически с целью обнаружения ЦМВ-антигена или вирусных включений. ЦМВ-гепатит подтверждается иммуногистохимически и цитологически при повышении трансаминаз. При фундоскопии диагностируется ретинит. ЦМВ-поражение центральной нервной системы (менингит, энцефалит, миелит) трудно выявить. В плане дифференциальной диагностики необходимо обследовать больного на наличие и других нейротропных оппортунистических инфекций. Рецидив ЦМВ-болезни определяется при повторном возникновении описанных симптомов после специфического лечения. Рефрактерная ЦМВ-болезнь может отражать устойчивость вируса в результате его мутации или глубокой иммуносупрессии.

Диагностика ЦМВ-инфекции Диагностика ЦМВ-инфекции осуществляется с помощью определения специфического ЦМВ-антигена или нуклеиновой кислоты в тканях или лейкоцитах, моноклональные антитела против ранних вирусных антигенов могут быть использованы для определения текущей инфекции в культуре клеток. Определение специфических циркулирующих иммуноглобулинов G и М у ранее серонегативных больных проводится с помощью иммуноферментного анализа. Метод ПЦР позволяет определить качественно и количественно присутствие ДНК ЦМВ в лейкоцитах периферической крови, исключая перекрестно-реагирующие нуклеиновые кислоты других герпес-вирусов. Отсроченное определение антигенемии ЦМВ в пробах крови может привести к значительному снижению чувствительности данного теста. Метод ПЦР в клинической практике считается высокочувствительным. Даже после эффективной терапии симптоматической ЦМВ-болезни, ЦМВ-ДНК может определяться, несмотря на исчезновение антигенемии.

Профилактика ЦМВ-инфекции В протокол лечения больных после трансплантации почки включены противовирусные средства (валганцикловир, ганцикловир). Профилактика ЦМВ: монотерапия противовирусным препаратом валганцикловир (вальцит), монотерапия ЦМВ-иммуноглобулином или сочетание противовирусных препаратов и ЦМВ-иммуноглобулина. Пероральный прием валганцикловира в дозе 900 мг/сут в течение 6 -ти месяцев может считаться эффективной профилактикой ЦМВ-болезни у реципиентов почек от серопозитивных доноров. Пациенты после трансплантации почки, когда реципиент и донор негативны по ЦМВ, получают профилактику вальцитом в течение 3 -х месяцев в дозе 900 мг при условии сохранной функции почечного трансплантата. В случае дисфунции почечного трансплантата производится коррекция дозы противовирусного средства (снижение суточной дозы в 2 раза).

Профилактика ЦМВ-инфекции ЦМВ-позитивные больные, получавшие лечение ОКТЗ или поликлональными антителами, имеют высокий риск болезни. Предупреждающая терапия ганцикловиром (2, 5 -5 мг/кг/сут), назначаемая во время лечения препаратами антител, снижает риск ЦМВ-болезни. Предупреждающая терапия ганцикловиром способна инактивировать латентный вирус, который потенциально способен к реактивации во время интенсификации иммуносупрессии. У тех больных, которые получали комбинированное лечение отторжения, должна проводиться дополнительная профилактика ЦМВболезни. Это заключается в предупреждающем назначении внутривенного ганцикловира, как описано выше, затем продолжается период менее частого введения препарата (например, 5 дней в неделю) или приема валганцикловира (вальцита) перорально (900 мг/сут, доза зависит от функции трансплантата и количества лейкоцитов в периферической крови).

Лечение ЦМВ-инфекции Лечение активной ЦМВ-болезни включает уменьшение объема иммуносупрессии (снижение вдвое дозы микофенолатов) и назначение ганцикловира (цимевена) внутривенно в дозе 5 мг/кг/сут при сохранной функции почечного трансплантата. Длительность введения цимевена составляет 21 день, с дальнейшим переходом на пероральный прием валганцикловира (вальцит) 900 мг/сут. Продолжительность периода лечения устанавливается для каждого пациента индивидуально (от 3 -х до 6 -ти месяцев). Больных с высоким риском ЦМВ, сохраняющимся после курса лечения ганцикловиром, необходимо часто проверять на наличие симптомов ЦМВ-болезни. Побочные эффекты ганцикловира представлены обратимой дозозависимой гранулоцитопенией, тромбоцитопенией, лихорадкой, кожными высыпаниями, судорогами, тошнотой, миалгиями, повышением цитолитических ферментов печени и реже панкреатитом.

Вирус простого герпеса Наиболее часто вирус простого герпеса проявляется у реципиентов почечного трансплантата высыпаниями на коже и слизистых оболочках обычно возникающими в первые 6 недель после трансплантации. Вирус простого герпеса может распространяться и на внутренние органы. Ацикловир и ганцикловир активны против вирусов герпеса и оба применяются для лечения или профилактики инфекции, но предпочтительнее использовать ацикловир (1 г/сут. ). Ацикловир назначается при поражении кожи и слизистых внутривенно. Для лечения энцефалита ацикловир назначается в больших дозах. Темп инфузии должен быть медленным, чтобы избежать образования кристаллов в канальцах почечного трансплантата. Доза вводимого препарата зависит от степени почечной недостаточности. Альтернативными лекарственными средствами являются валацикловир (в дозе 2 г/сут. ) и фамцикловир (1, 5 г/сут. ). При снижении функции почечного трансплантата необходимо снизить суточную дозу вдвое.

Варицелла зостер вирус Негрез Zoster (ВЗВ) поражает примерно 10% реципиентов органных трансплантатов, процесс может распространяться на 2 -3 соседних дерматома. Для лечения применяют валацикловир (валтрекс по 1 гр х 3 р/сут, при СКФ 25 -30 мл/мин — 1 гр х 2 р/сут — 7 дней), ацикловир, фамцикловир в стандартных дозах. Диссеминированная форма заболевания обычно развивается при первичном инфицировании и протекает с пневмонией, энцефалитом, развитием ДВС-синдрома, дисфункцией почечного трансплантата. Противовирусная терапия заключается во внутривенном введении ацикловира (12, 5 -15, 0 мг/кг трижды в день в течение 7 дней). Ганцикловир и фоскарнет также эффективны при диссеминированном процессе, вызванном ВЗВ.

Полиомавирусы ВК-вирусы относятся к семейству человеческих палиомавирусов. Реактивация вируса может приводить к формированию стриктур мочеточника, прогрессирующей мультифокальной лейкоэнцефалопатии, интерстициального нефрита и прогрессирующей дисфункции почечного трансплантата. Палиомавирус определяется методом ПЦР. Специфического лечения ВК-нефропатии нет. Производились попытки лечения лефлюномидом, но основной тактикой ведения является редукция иммуносупрессивной терапии.

Вирусы гриппа А и В Респираторные инфекции чаще проявляются симптомами поражения верхних отделов дыхательных путей, прогрессирующими общими симптомами: высокой лихорадкой, миалгиями, артралгиями, анорексией и воспалением слизистых. Может отмечаться развитие бронхиолита, пневмонии и прогрессирующей дыхательной недостаточности, что требует незамедлительных реанимационных пособий (обязательная респираторная поддержка, в т. ч. искусственная вентиляция легких). Прогрессирующая острая вирусная инфекция, которая приводит к пневмонии, может стать фатальной присоединении бактериальной флоры, нозокомиальной инфекции грамнегативными микробами или грибами, а также из-за возможной реактивации ЦМВ. Диагностика вирусной инфекции должна быть быстрой, вирус выделяется из мокроты, бронхоальвеолярных смывов, отделяемого из носа. Проводится иммунофлюоресцентный анализ проб. Иммунизация против гриппа является оптимальным способом защиты здоровых людей от гриппа, но она может быть неэффективной у больных, получающих иммуносупрессивные препараты, так как у них снижена выработка антител.

Лечение гриппа А заключается в как можно более раннем приеме осельтамивира (тамифлю). Профилактически этот препарат назначается в период эпидемии. Против вируса гриппа В нет эффективных средств профилактики и лечения. Препараты, такие, как осельтамивир, занамивир, способны укоротить длительность болезни и устранить осложнения со стороны нижних дыхательных путей, если назначаются в течение 30 -36 ч от начала заболевания. Оба препарата могут также использоваться для профилактики гриппа.

Гепатиты у больных с трансплантированной почкой

Перед трансплантацией почки потенциальный реципиент должен быть обследован на предмет инфицирования вирусами гепатитов, так как в условиях длительной иммуносупрессивной терапии оно может приводить к хроническому прогрессирующему поражению печени. Обследование HBV- или HCV-позитивных потенциальных реципиентов до трансплантации почки - Стандартные исследования. клинические и биохимические - Серологические маркеры HBV- или HCV-инфекции (исключить наличие репликации вируса). - Определение генотипа вируса гепатита «С» . - Биопсия печени (для исключения цирроза).

Наличие хронических гепатитов «В» и «С» ухудшают результаты трансплантации почки, по сравнению с неинфицированными реципиентами. У HBs. Ag-позитивных реципиентов почечного трансплантата повышается риск смерти и потери функции почечного трансплантата. HBs-Ag-негативные реципиенты почечного трансплантата имеют низкий риск увеличения вирусной репликации и прогрессирования заболевания печени. У HCV-позитивных реципиентов почечного трансплантата повышается риск осложнений, включающих прогрессирование заболевания печени, развитие сахарного диабета, HCV-ассоциированного гломерулонефрита, сердечно-сосудистых осложнений, инфекций.

Выживаемость реципиентов почечных трансплантатов с наличием HBV-, HCV-инфекции - 10 -летняя выживаемость HBs. Agпозитивных и HBs. Ag-негативных реципиентов почечного трансплантата 62% против 66%. (KDIGO, 2009). - 10 -летняя выживаемость HBs. Agпозитивных реципиентов почечного трансплантата (45%) против HCVпозитивных реципиентов почечного трансплантата (65%) (KDIGO, 2009).

- Однако при нормальных значениях трансаминаз, при отсутствии вирусологической активности болезни (ДНК HBV, Hbe. Ag, РНК HCV), а также отсутствии морфологических признаках цирроза печени трансплантация почки возможна. - При наличии цирроза печени и терминальной ХПН после выполнения трансплантации печени и почки — выживаемость реципиента хуже (смертность в раннем посттрансплантационном периоде), чем при трансплантации только почки, в отдаленном периоде — выживаемость реципиента и почечного трансплантата одинаковы в обоих случаях.

Kidney transplantation alone in ESRD patients with hepatitis C cirrhosis. Paramesh AS, Davis JY, Mallikarjun C, Zhang R, Cannon R, Shores N, Killackey MT, Mc. Gee J, Saggi BH, Slakey DP, Balart L, Buell JF. Tulane Transplant Institute, Tulane University School of Medicine, New Orleans, LA, USA. Результаты: 63 больным выполнена АТП. 2 группы: с циррозом и без цирроза печени. Не было пациентов, у которых бы развилась печеночная недостаточность. Только у одного пациента в группе (без цирроза печени) возникла гепатоцеллюлярная карцинома через 16 месяцев после трансплантации. Одно - и трех-летней выживаемости трансплантата были 75% по сравнению с 92. 1% и 75. 1% для групп с цирозом печени и без цирроза печени, соответственно (P=0, 72). Одно - и трех-летней выживаемости пациентов были на 88, 9% и 88, 9% по сравнению с 96. 3% и 77, 9% для групп с цирозом печени и без цирроза печени, соответственно (P=0, 76). Только возраст реципиента и снижение уровня альбумина достоверно ассоциируются с низкой выживаемостью почечного трансплантата и пациента. Выводы: Трансплантация почки может быть безопасна у пациентов с компенсированным гепатитом С и циррозом печени. Одновременная трансплантация печени и почек может быть не нужна. Transplantation. 2012 Aug 15; 94(3): 250 -4

У анти-НСV-позитивных реципиентов почечного трансплантата соотношение риск/польза - предпочтение трансплантации почки. Hepatitis C virus and kidney disease. Kamar N, Alric L, Izopet J, Rostaing L. Department of Nephrology, Dialysis and Organ Transplantation, CHU Rangueil, Toulouse, France; INSERM U 1043, IFR-BMT, CHU Purpan, Toulouse, France; Université Paul-Sabatier, Toulouse, France. Выводы: Выживаемость значительно ниже у HCV-позитивных, чем у HCVнегативных пациентов, находящихся на гемодиализе, в то время как выживаемость значительно выше у HCV-позитивных пациентов, перенесших трансплантацию почки по сравнению с HCV-позитивных пациентов, находящихся на гемодиализе. Таким образом, пациентам, находящимся на диализе без стойкого вирусологического ответа после анти-HCV терапии должна быть предложена трансплантация почки. Clin Res Hepatol Gastroenterol. 2013 Mar 20.

Hepatitis C and renal transplantation. Morales JM, Aguado JM. Department of Nephrology, Instituto de Investigacion Hospital, Madrid, Spain. ВГС является наиболее частой причиной заболевания печени после трансплантации. В перспективе HCV-инфекция может привести к циррозу печени, гепатоцелюллярной карциноме и смерти в некоторых случаях. Лечение интерфероном, как правило, противопоказано после трансплантации, поэтому методом выбора является лечение пациентов перед трансплантацией почки. Долгосрочная выживаемость пациента и трансплантата у HCV-позитивных пациентов ниже, чем у HCV-негативных реципиентов трансплантата. HCVинфекция является независимым фактором риска смерти и потери трансплантата. Смертность выше у данной категории больных, в результате сердечно-сосудистых осложнений, заболевания печени и инфекций, но ниже, чем у HCV-позитивных пациентов, находящихся в листе ожидания на пересадку почки. Возникновение диабета после трансплантации (NODAT), и HCVгломерулонефрит, вместе с хроническим отторжением и, в частности, посттрансплантационная гломерулопатия могут приводить к потере функции почечного трансплантата. Несмотря на это, трансплантация почки является лучшим вариантом для HCV-позитивных пациентов, находящихся на диализе. ВЫВОДЫ: Пересадка почки является терапией выбора у пациентов с HCVинфекцией на диализе. Curr Opin Organ Transplant. 2012 Dec; 17(6): 60915.

Hepatitis C and renal transplantation. Lerner SM. Mount Sinai Medical Center, New York, NY, USA. Трансплантацию почки следует рассматривать как метод выбора для лечения пациентов с терминальной почечной недостаточностью и гепатитом «С» . Биопсия печени является важным для определения степени фиброза у этих пациентов. Лечение до трансплантации должно осуществляться гепатологами, хотя имеются трудности в лечении, учитывая ограничения при почечной недостаточности. Лечение в посттрансплантационном периоде остается спорным. Одновременная почечная/печеночная трансплантация должна рассматриваться для кандидатов с признаками портальной гипертензии или декомпенсированным циррозом печени. Mt Sinai J Med. 2012 May. Jun; 79(3): 342 -50
Вирусные гепатиты В, С у больных с терминальной ХПН До трансплантации почки Не лечить? Лечить? После трансплантации почки Лечить?

Перед трансплантацией почки все пациенты с вирусными гепатитами ( «В» , «С» ) при наличии вирусологической, биохимической активности и признаками фиброза печени должны получать противовирусную терапию:

. Особенности ведения больных после трансплантации почки с хроническими гепатитами

Ведение больных с гепатитом «В» и трансплантированной почкой Иммуносупрессивная терапия может увеличивать интенсивность репликации HBV (при использовании ГКС, азатиоприна, ингибиторов кальциневрина). Поэтому следует избегать схем лечения с использованием азатиоприна, а также назначать минимально возможные дозы глюкокортикостероидов. При HBV-инфекции может быть небольшое повышение активности трансаминаз и, несмотря на это, гистологическая прогрессия заболевания. Контроль биохимических печеночных показателей ежемесячно, определение вирусной нагрузки 1 раз в 6 мес. Всем НBs-Ag позитивным пациентам с циррозом необходим скрининг для выявления гепатоцеллюлярной карциномы (альфа фетопротеин и УЗИ печени — каждые 12 мес. )

Ведение больных с гепатитом «В» и трансплантированной почкой Всем пациентам с HBV-инфекцией при ее реактивации показано проведение противовирусной терапии нуклеозидными аналогами (ламивудин, энтекавир, адефовир, телбивудин), так как во многих исследованиях доказано эффективное подавление репликативной активности HBV, регресс фиброза на фоне противовирусной терапии, что позволит избежать прогрессирования заболевания печени. - Цель терапии: элиминация ДНК HBV, исчезновение HBе. Ag, нормализация АЛТ. - Пункционная биопсия печени осуществляется через 1 год для контроля за проводимым противовирусным лечением у реципиентов почечного трансплантата. -

Изучение эффективности ламивудина при ХГВ у реципиентов почечного трансплантата (режим терапии и результаты лечения) Продолжительность посттрансплантационного периода до начала противовирусной терапии – 46, 95± 7, 1 мес. Доза препарата 50 -100 мг/сут. Длительность лечения – 15, 6 1, 9 (от 6 до 42) мес. n=14 (64%) n=9 (41%) n=8 (36%) терапевтический эффект без эффекта вирусологический ответ и биохимический ответ (+/-) биохимический ответ n=5 (23%) /Zubkin M. et al. , Int J Artif Org 2007; 30: 308 314/

Лечение гепатита «В» у реципиентов почечного трансплантата использование ламивудина приводит к развитию генотипической резистентности вируса к препарату. Эти мутации на YMDD-участке ДНК-полимеразы могут вызывать повышение уровня сывороточной HBV DNA во время терапии, что следует за появлением генотипической резистентности, затем клиническая резистентность, что проявляется повышением активности сывороточной Ал. АТ и ухудшением клинического течения болезни. - Длительное - Новые препараты (энтекавир, телбивудин, тенофовир) обладают более высокой эффективностью, чем ламивудин (КDIGO, 2009). - В течение противовирусной терапии определение ДНК HBV и АЛТ должно выполняться 1 раз в 3 мес.

Ведение больных с гепатитом «В» и трансплантированной почкой: Лечение аналогами нуклеозидов Препарат Клиренс креатинина (мл/мин) Рекомендуемая доза адефовир ≥ 50 20 -49 10 -19 10 мг/сут 10 мг через день 10 мг 1 раз в 3 дня телбивудин ≥ 50 30 -49 < 30 600 мг/сут 400 мг/сут 200 мг/сут энтекавир ≥ 50 30 -49 10 -29 0, 5 мг/сут 0, 5 мг/48 час 0, 5 мг/72 час (1 мг/сут) (1 мг/48 час) (1 мг/72 час) При резистентности к ламивудину 1 мг/сут тенофовир ≥ 50 30 -49 < 30 300 мг/сут 300 мг/48 час 300 мг/72 -96 час

A novel experience of antiviral therapy for chronic hepatitis B in renal transplant recipients. Hu TH, Tsai MC, Chien YS, Chen YT, Chen TC, Lin MT, Chang KC, Chiu KW. Division of Hepatology and Gastroenterology, Department of Internal Medicine, Kaohsiung Chang Gung Memorial Hospital and Chang Gung University College of Medicine, Kaohsiung, Taiwan. МЕТОДЫ: 27 HBs. Ag-позитивных реципиентов почечного трансплантата получали лечение энтекавиром. HBV ДНК оценивали исходно и на 12, 24, 52 и 104 неделях после лечения. Контрольная группа составила 19 пациентов, получавших в течение 2 лет терапию ламивудином. РЕЗУЛЬТАТЫ: Пациенты, которые получали лечение энтекавиром демонстрировали более высокие темпы элиминации HBV ДНК, чем в группе с ламивудином (P<0, 05). ВЫВОДЫ: Энтекавир эффективен при лечении хронического гепатита у реципиентов почечного трансплантата. Энтекавир безопасен в отношении функции почечного трансплантата, развития лактат-ацидоза, миопатии и вирусологической резистентности. Antivir Ther. 2012; 17(4): 745 - 53

Лечение гепатита «В» у больных с трансплантированной почкой Энтекавир - новое в лечении больных хроническим гепатитом В М. В. Маевская, А. О. Буеверов (Московская медицинская академия им. И. М. Сеченова) Заключение: Проведенные исследования эффективности лечения пациентов с ХГ «В» энтекавиром показали его хорошую переносимость, высокий профиль безопасности, более высокую эффективность, чем у ламивудина, и отсутствие резистентности через 2 года его приема у больных, ранее не лечившихся аналогами нуклеозидов <1%. Продемонстрирована также эффективность препарата при назначении резистентным к ламивудину больным. Таким образом, препарат энтекавир может считаться препаратом первой линии терапии HBV-инфекции у пациентов ранее не получавших аналоги нуклеозидов и вариантом терапии ламивудинрефрактерных больных.

Ведение больных с гепатитом «С» и трансплантированной почкой Исследования после трансплантации почки у HCV-позитивных реципиентов - Функциональные исследования печени и почек должны проводиться в первые 6 месяцев ежемесячно, затем каждые 3 месяца (КDIGO, 2009), а вирусная нагрузка должна оцениваться через каждые 6 месяцев. - Протеинурия должна определяться каждые 3 -6 мес. у HCVпозитивных реципиентов почечного трансплантата. При уровне протеинурии 1 г/сут – выполнение биопсии почечного трансплантата (КDIGO, 2009). - Биопсию печени следует выполнять каждые 3 года после трансплантации почки. - Всем НСV-позитивным пациентам с циррозом необходим скрининг для выявления гепатоцеллюлярной карциномы (альфа-фетопротеин и УЗИ печени — каждые 12 мес. )

Ведение больных с гепатитом «С» и трансплантированной почкой Тактика ведения анти-НСV-позитивных реципиентов почечного трансплантата заключается в использовании протоколов иммуносупрессии без применения азатиоприна, необходима оптимизация иммуносупресивной терапии (по возможности раннее уменьшение до поддерживающей). - Доказано, что in vitro лечение циклоспорином тормозит репликацию вируса гепатита «С» , а в отношении такролимуса такого действия не наблюдалось.

Ведение больных с гепатитом «С» и трансплантированной почкой Суммируя рекомендации American Association for the Study of Liver Diseases (AASLD), Infectious Diseases Society of America (IDSA), American Society of Gastroenterology (ASG)), а также результаты многих исследований: После трансплантации почки у реципиентов со стабильной функцей почек и печени требуется только тщательное наблюдение, а не противовирусная терапия. Применение интерферона после трансплантации почки не рекомендовано, в связи c возможностью развития острого отторжения трансплантата. Интерферон может вызвать экспрессию HLA-антигенов на поверхности клеток с индукцией экспрессии генов цитокинов и последующей стимуляцией выработки антител.

Ведение больных с гепатитом «С» и трансплантированной почкой По жизненным показаниям осуществляется лечение интерфероном+рибавирином при наличии фиброзирующего холестатического гепатита, криоглобулинемического нефрита в почечном трансплантате (если успех терапии превышает риск потери почечного трансплантата). Treatment of hepatitis C virus infection after kidney transplantation. Rostaing L, Weclawiak H, Izopet J, Kamar N. Department of Nephrology, Dialysis, and Organ Transplantation, CHU Rangueil, University Hospital, Toulouse, France. Contrib Nephrol. 2012; 176: 87 -96 Du L, Tang H. , 2011 г. Риск острого отторжения выше, в течение первого года после пересадки почки, поэтому рекомендуется подождать не менее 1 года после операции, чтобы начать противовирусную терапию (пегилированный интерферон + рибавирин).

Experience of fibrosing cholestatic hepatitis with hepatitis C virus in kidney transplant recipients. Siddiqui AR, Abbas Z, Luck NH, Hassan SM, Aziz T, Mubarak M, Naqvi SA, Rizvi SA. Department of Hepatogastroenterology, Sindh Institute of Urology and Transplantation, Karachi, Pakistan. Методы: У 4 реципиентов почечного трансплантата был диагностирован фиброзирующий холестатический гепатит С на основании наличия вируса гепатита С (HCV), РНК и результатов биопсии печени. Результаты: Пациенты были мужчины в возрасте от 40, 25, 20 и 27 лет. Сроки после трансплантации 1, 5 г, 10 лет, 1. 5 г, и 2. 0 г, соответственно. У 4 пациентов был 1 генотип. У первых 2 -х пациентов, которые получали интерферон и рибавирин, отмечалось улучшение в части уменьшения холестаза, но быстрого вирусологического ответа не наблюдалось. В 1 -м случае развился острый криз отторжения почечного трансплантата через 4 месяца после начала терапии интерфероном, который лечили пультерапией ГКС. Терапия интерфероном в первых 2 -х случаях была досрочно прекращена в обоих случаях из-за панцитопении. В 3 -м случае развился пиелонефрит и пациент умер, не получив лечение гепатита C. В 4 -м случае уменьшение иммуносупрессии и проведение регулярного мониторинга. ВЫВОДЫ: Фиброзирующий холестатический гепатит С трудно поддается Transplant Proc. 2012 Apr; 44(3): 721 -4
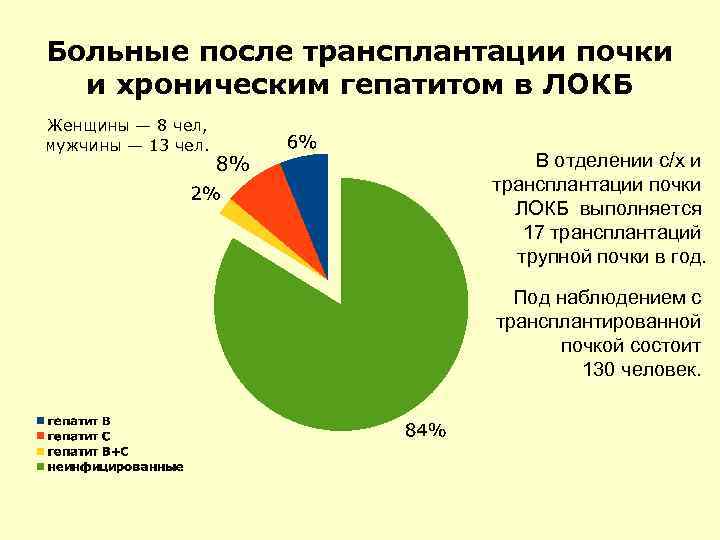
Больные после трансплантации почки и хроническим гепатитом в ЛОКБ Женщины — 8 чел, мужчины — 13 чел. В отделении с/х и трансплантации почки ЛОКБ выполняется 17 трансплантаций трупной почки в год. Под наблюдением с трансплантированной почкой состоит 130 человек.

Обследование больных с трансплантированной почкой и наличием хронического вирусного гепатита Лабораторные исследования: Биохимические показатели (АЛТ, АСТ, щелочная фосфатаза, протромбин, фибриноген, общий белок). Клинические показатели (гемоглобин, эритроциты, тромбоциты). HBs. Ag, HBc AB, Hbe. Ag; HCV AB. ДНК НВV, РНК НСV (качественный тест) - методом ПЦР. При положительном результате — количественный тест (вирусная нагрузка). Генотип вирусного гепатита «С» (определяет выбор противовирусных препаратов, длительность лечения, а также дозы препаратов) Инструментальные исследования: ФГДС. УЗИ органов брюшной полости. Эластография. Биопсия печени (перед началом ПВТ).

Фиброскан (эластография печени) Эластография может быть альтернативой биопсии печени, в случае невозможности ее проведения. Неинвазийная методика определения степени фиброза печени. В основу аппарата Фиброскан ("Fibro. Scan") положена эластометрия печени - методика определения фиброза печени с помощью упругих волн. Принцип эластографии основан на взаимосвязи эластичности ткани и степени фиброза: чем ниже эластичность (то есть плотнее ткань печени), тем более выражен фиброз. На основании скорости определяется эластичность печени. Полученный результат выражается в килопаскалях (к. Па) и позволяет четко распределять больных по стадиям заболевания от F 0 до F 4 по системе METAVIR. По результатам сравнительных исследований, информативность метода составляет при фиброзе: • F 0 -F 1 88 -90% • F 2 - F 3 90 -94% • F 4 94 -98%:

Правильный отбор на трансплантацию почки больных с наличием НВV- , HCV-инфекции позволит улучшить результаты трансплантации. Лечение вирусного гепатита должно осуществляться до трансплантации почки. Лечение хронического вирусного гепатита «В» аналогами нуклеозидов показано всем реципиентам почечного трансплантата при реактивации вирусной инфекции. Лечение хронического вирусного гепатита «С» сопряжено с высоким риском отторжения почечного трансплантата и его потери, однако, по жизненным показаниям (фиброзирующий холестатический гепатит, прогрессирующий цирроз печени) интерферонотерапия может быть назначена.

Осложнения: сердечно-сосудистая система ИБС, артериальная гипертензия • • • 60 -80% больных после трансплантации почки Контроль АД дважды в день Целевой уровень АД 120/80 мм рт ст Ограничение хлорида натрия Малые дозы тиазидных диуретиков Подбор препарата индивидуален Начало с монотерапии Ингибиторы АПФ: торможение прогрессирования дисфункции почечного трансплантата Использование БРА или сочетание и-АПФ и БРА Бета-блокаторы применяются реже, т. к. после трансплантации часто диабет, заболевания периферических сосудов, обструктивные заболевания легких Блокаторы кальциевых каналов эффективны, улучшают почечный кровоток, учитывать побочные эффекты

ИБС, артериальная гипертензия • Гиперхолестеринемия вследствие приема циклоспорина А • Гиполипидемическая диета • Отказ от курения • Физические тренировки (аэробная нагрузка) • Аспирин для длительного применения, при отсутствии противопоказаний • Статины – стратегия лечения • Госпитализация при подозрении на ОИМ, нестабильную стенокардию • Обследование у кардиолога при симптомах ИБС • Назначение препаратов должно быть согласовано с врачом-трансплантологом

Осложнения: малигнизация • Риск пропорционален срокам функционирования почечного трансплантата • Наиболее частые локализации: кожа, слизистые, половые органы, органы желудочно-кишечного тракта • Лимфопролиферативные: лимфома, саркома Капоши • Профилактика и ранняя диагностика • Ежегодная полная диспансеризация • Лечение у онколога совместно с трансплантологом

Малигнизация Протокол диспансерного обследования • Клинический анализ крови • Биохимический анализ крови (максимально возможный спектр биохимических тестов: концентрация общего белка сыворотки, альбумина, железа, кальция, фосфата, щелочной фосфатазы, парагормона, билирубина, цитолитических ферментов, глюкозы, липидов) • Общий анализ мочи • Суточная протеинурия, клубочковая фильтрация • Рентгенография легких • УЗИ брюшной полости, забрюшинного пространства, области щитовидной железы, органов малого таза • Фиброгастродуоденоскопия • Рентгенография костей скелета • Осмотр гинеколога, уролога • ФКС, КТ, МРТ, ПЭТ по показаниям

Трансплантация почки в Лениградской Областной клинической больнице

Количество трансплантаций почки, выполненных в ЛОКБ с 1992 по 2015 гг – более 400 операций Количество повторных трансплантаций почки - 7 Количество трансплантаций почки С 2011 г по 2015 г — 17 аллотрансплантаций почки в год (квоты на операции)

Характеристика больных Под наблюдением находятся 146 пациентов после трансплантации почки.
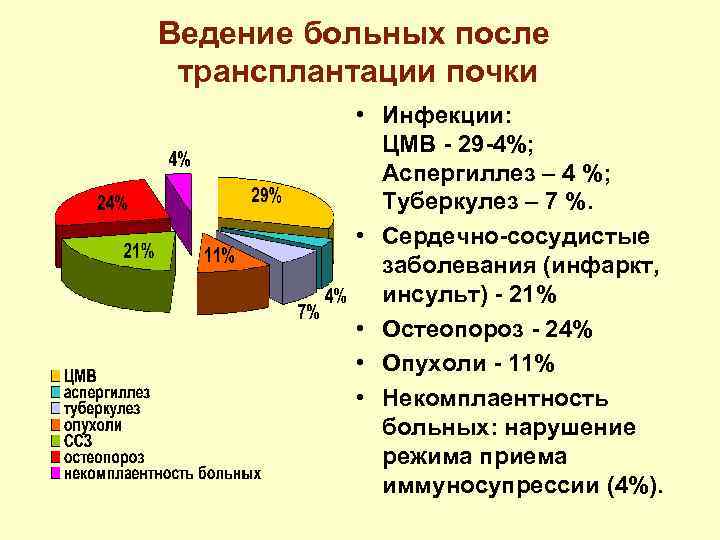
Ведение больных после трансплантации почки • Инфекции: ЦМВ - 29 -4%; Аспергиллез – 4 %; Туберкулез – 7 %. • Сердечно-сосудистые заболевания (инфаркт, инсульт) - 21% • Остеопороз - 24% • Опухоли - 11% • Некомплаентность больных: нарушение режима приема иммуносупрессии (4%).

Наблюдение за больными после трансплантации почки в ЛОКБ Амбулаторное наблюдение в ЛОКБ с кратностью 1 раз в месяц осуществляется нефрологом-трансплантологом. • Физикальное обследование(контроль артериального давления, веса, суточного диуреза, пальпаторное исследование почечного трансплантата). • Лабораторные анализы: – клинический анализ крови, – Биохимия крови – креатинин, мочевина, мочевая кислота, трансаминазы, электролиты крови (натрий, кальций, фосфор), щелочная фосфатаза, глюкоза, билирубин, общий белок, холестерин, СРБ. – Проба Реберга (расчет по формуле). – Общий анализ мочи – Посев мочи (по показаниям) – СПБ. – Концентрация сандиммуна или прографа в крови.

Наблюдение за больными после трансплантации почки в ЛОКБ • Инструментальные исследования: – Допплерография сосудов почечного трансплантата, – УЗИ почечного трансплантата, – Денситометрия – 1 раз в год.

Наблюдение терапевта • Больной после трансплантации почки должен наблюдаться врачом, имеющим опыт ведения больных данной категории. • Госпитализация при развитии осложнений осуществляется в центр, где проводилась трансплантация почки. • При возникновении осложнений после трансплантации участковый врач должен обратиться за консультацией к нефрологу-трансплантологу в центр, где проводилась операция. • Инструментальные исследования по месту ежегодно: – ФЛГ. – УЗИ брюшной полости + нативные почки. – ФГДС. жительства • Контроль общего состояния пациента с трансплантированной почкой -

Клинический случай Родственная додиализная трансплантация почки

• С 2004 г - регистрируется артериальная гипертензия (до 150/110 мм. рт. ст. ). Принимал и-АПФ. • Март 2006 г - Обследование в ДЛОКБ. Отмечалось постепенное прогрессирование ХПН (Cr 0, 4 ммоль/л, Ur 18 ммоль/л). • В июне 2006 г и марте 2007 г - госпитализация в нефрологическое отделение ЛОКБ. Диагноз: Двусторонняя нейромышечная дисплазия обоих мочеточников в стадии уретерогидронефроза. Состояние после 4 -х урологических операций: уретерокутаностомия справа и слева (1990 г), закрытие уретеростомы справа и слева (09. 1991 г), рассечение устья левого мочеточника, катетеризация левого мочеточника (10. 1991 г), бужирование мочеточников (11. 1991 г). Осл: ХБП 5 ст. Симптоматическая артериальная гипертензия. Симптоматическая анемия. Гиперурикемия. Метаболический ацидоз. Соп: Вторичный пиелонефрит, вне обострения. Хронический гастрит, вне обострения.

• • • Закономерное прогрессирование ХПН (Cr 0, 6 -0, 7 ммоль/л). Симптоматическая анемия. Метаболический ацидоз. Электролитных расстройств выявлено не было. Проведена отборочная комиссия по лечению методами ЗПТ. Консилиумно было решено выполнить родственную трансплантацию почки на додиализном этапе (донор - отец). Проведено предтрансплантационное обследование. Донор и реципиент были негативны по HBs Ag, HCV AB, HIV, ЦМВ. 22. 05. 2007. Выполнена родственная трансплантация почки на левые наружные подвздошные сосуды. Функция почечного трансплантата немедленная. СД 5 - 2 л. В течение 1 -х суток после операции развились симптоматическая гипергликемия, острый панкреатит. Пребывание в стационаре осложнилось развитием пневмоторакса, по поводу чего было выполнено дренирование грудной полости.

• 18 -е сутки. Подозрение на острый криз отторжения пт (увеличение креатинина 169 199 umol/L, повышение индексов периферического сопротивления в артериях почечного трансплантата со снижением интенсивности кровотока в периферических отделах коркового вещества) • Проведено лечение: – Иммуносупрессивная терапия: Сандиммун 10 мг/кг, майфортик 1440 мг, метипред 1 - 0, 5 мг/кг. – Ps-терапия солюмедролом (1, 5 г), на фоне чего показатели УЗДГ пт нормализовались, азотемические показатели снизились (Cr 140 µmol/L). – Дополнительная терапия: дилтиазем, диротон, гипотиазид, амоксиклав, омепразол, нистатин, бисептол, фуросемид, октреотид, инсулин актрапид, альфа-Д 3 ТЕВА. • Длительность госпитализации составила 25 к/д. • 15. 06. 07. больной был выписан на амбулаторное лечение в удовлетворительном состоянии.

Динамика лабораторных показателей в раннем посттрансплантационном периоде

Схема иммуносупрессивной терапии Cs. A - 350 -300 -200 мг/сут, Майфортик 1440 мг/селлсепт 2 г, Метипред 5 табл-1, 5 табл.

• В июле (104 - 2007 г 102 была выявлена ДНК копий ЦМВ-инфекция в 1 мл). Получал противовирусную терапию цимевеном, затем вальтрексом. • В сентябре 2007 г был госпитализирован в отделение трансплантации ЛОКБ для проведения противовирусной терапии: цимевен 500 мг № 8, дальнейшим переходом на вальцит (6 мес). с

• В декабре 2008 г перенес ОРВИ. Получал симптоматические средства, а/б препараты с (+) эффектом. Однако в январе 2009 г - рецидив лихорадки (37 -38 С). ЦМВ-инфекции не обнаружено. • 19. 01. 2009 - госпитализирован в отделение трансплантации ЛОКБ. При объективном осмотре: Жалобы: на повышение температуры тела 37 -38 С, сухой кашель. Объективно: Состояние удовлетворительное. Контактен. В сознании. Кожные покровы чистые. Периферические лимфоузлы не увеличены. Отеков нет. АД 140/100 мм. рт. ст. Ps 96 уд. мин. , тахикардия. Границы относительной сердечной тупости не изменены. Тоны сердца ритмичные, шумов нет. В легких перкуторно притупления нет. Дыхание жесткое, хрипов нет. Живот мягкий, безболезненный. Печень не увеличена, селезенка не пальпируется, перкуторно не увеличена. Почечный трансплантат пальпируется в левой подвздошной области, безболезненный, не увеличен. Мочеиспускание свободное, б/б. СД 2 л.

Лабораторные и инструментальные исследования • Клинический анализ крови 11. 02. 09: Hb – 104 г/л, Эр – 3, 53 х 1012 /л, Лейк. – 11, 1 х 109 /л, Тромб. - 196 х109/л, п/я 4, с/я – 64, л-27, м-2 %, СОЭ – 6 мм/ч. • Биохимический анализ крови (19. 01 -11. 02. 09): Общий белок – 73 г/л, креатинин – 0, 258 -0, 148 ммоль/л, мочевина – 12, 8 -8, 9 ммоль/л, глюкоза – 4, 81 ммоль/л, билирубин 10 ммоль/л, АЛТ – 18 ед/л, АСТ – 11 ед. /л, СРБ – 24, 9 -0, 65 мг/л, калий – 4, 32 моль/л, натрий – 138 ммоль/л, кальций 2, 4 ммоль/л, ЩФ – 155 U/l. Мочевая кислота – 311 ммоль/л, фосфор 1, 19 ммоль/л. • ЦМВ-инфекция от 11. 02. 09– не обнаружено. • Проба Реберга: СКФ 33 мл/мин (Cr 0, 258 ммоль/л). • Анализ мочи (30. 01. 09): р. кисл, м/м, белок нет, лейкоциты 2 -3 в поле зрения, бактерии – 0. • Посев мочи – отриц. • ФЛГ от 01. 09 - В легких без инфильтративных изменений. • УЗДГ пт - незначительное повышение индексов периферического сопротивления в артериях пт (в динамике N) 19. 01. 09. - Концентрация Cs. A - 0

19. 01. 2009 Биопсия почечного трансплантата (1) Заключение: Гистологическая картина соответствует реакции острого отторжения трансплантата I B: тубулит (t 3), диффузный острый канальцевый некроз, интерстициальная инфильтрация (i 3).

Лечение • Иммуносупрессивная терапия: – Ps-терапия р-ром солумедрола 0, 5 г № 3. – Произведена конверсия с сандиммуна на програф 3 мг/сут (Со - 11 нг/мл). – Метипред 1, 5 табл/сут. – Майфортик 1440 мг/сут. • Дополнительная терапия: – Диротон, октреотид, мезим, ультоп, альфа. Д 3 ТЕВА.

ДИАГНОЗ: ОСН: Двусторонняя нейромышечная дисплазия обоих мочеточников в стадии уретерогидронефроза. Вторичный пиелонефрит, вне обострения. Состояние после 4 -х урологических операций: уретерокутаностомия справа и слева в 1990 г. закрытие уретеростомы справа и слева в сентябре 1991 г. Бужирование мочеточников в ноябре 1991 г. Операции: Родственная трансплантация почки на левые наружные подвздошные сосуды от 22. 05. 2007 г. Острый криз отторжения почечного трансплантата (I-B) на фоне нарушения режима иммуносупрессии. Биопсия почечного трансплантата от 19. 01. 2009. ОСЛ: ХБП 5 ст (т). Вторичная анемия. Вторичная артериальная гипертензия. Сахарный диабет стероидного генеза, компенсация. Хронический панкреатит (затихающее обострение). Соп: Хронический эрозивный гастрит, вне обострения.

Повторная госпитализация через 3 месяца • Госпитализирован для выполнения контрольной биопсии почечного трансплантата. Лабораторные данные обследования: Клинический анализ крови 27. 04. 09: Hb – 107 г/л, Эр – 3, 53 х 1012 /л, Лейк. – 14, 9 х 109 /л, Тромб. - 249 х109/л, п/я 3, с/я – 63, л-23, м-5 %, СОЭ – 3 мм/ч. Биохимический анализ крови (27. 04. 09): креатинин – 0, 128 ммоль/л, мочевина – 6, 26 ммоль/л, глюкоза – 4, 81 ммоль/л, билирубин 5, 95 ммоль/л, АЛТ – 17 ед/л, АСТ – 16 ед. /л, калий – 3, 76 -4, 07 моль/л, натрий – 139, 3 ммоль/л, кальций 2+ 1, 224 ммоль/л, ЩФ – 137 U/l, фосфор 1, 21 ммоль/л, липаза - 26 U/l, амилаза – 144 U/l, железо -10, 53, глюкоза – 4, 81 ммоль/л, ферритин- 123, 8 нг/мл. Анализ мочи (27. 04. 09): р. кисл, м/м, белок следы, лейкоциты 2 -4 -5 в поле зрения, эр – единичные, бактерии – 0. • Концентрация прографа Со- 7, 1 нг/мл.

27. 04. 2009 Биопсия почечного трансплантата (2) Заключение: Подозрение на клеточное отторжение: тубулит (t 1), интерстициальное воспаление (i 1). Склеротические изменения G 1: сегментарный гломерулосклероз (11%), интерстициальный фиброз (ci 1), атрофия канальцев (ct 1); Хроническая циклоспориновая токсичность (ah 1), C 4 d (-).

Заключение • Острое отторжение почечного трансплантата у данного пациента купировано проведением Psтерапии ГКС и конверсией на програф. • Функция почечного трансплантата практически восстановилась, однако, появление фиброзных изменений в почечном трансплантате может ограничить срок его функционирования.

Беременность после трансплантации почки

Статистика беременностей у женщин после трансплантации почки, завершившихся рождением ребенка В США 16 000 трансплантаций в год • В США 7000 успешных беременностей (1998 г) • В США по данным национального регистра с 1998 г по 2008 от 700 до 1000 беременностей в год. В России 800 трансплантаций почки в год. • В России более 100 беременностей, завершившихся рождением детей. • В ЛОКБ – 2 беременности, завершившиеся рождением ребенка

Репродуктивная функция после трансплантации почки восстанавливается Мужчины • • • Фертильность улучшается в 50% • случаев по данным спермограммы; Нормализуется уровень половых • гормонов ( тестостерон, ФСГ, лютеинизирующий гормон); Число внутриутробных мальформаций плода не выше, чем в общей популяции. • Женщины После трансплантации почки способность к зачатию восстанавливается. В течение 1 -го года после трансплантации почки восстанавливается менструальный цикл, уровень пролактина нормализуется ( ). Необходимость контрацепции (предпочтительна барьерная)

Беременность у больных с почечной недостаточностью • Беременные с концентрацией креатинина более 0, 13 ммоль/л имеют высокий риск снижения функции почек. • Артериальная гипертензия является общим фактором риска для всех групп беременных с ХПН. • Задержка развития плода, преждевременные роды и неонатальная смерть также характерны для всех групп беременных с ХПН. • По мере прогрессирования почечной недостаточности способность женщин к зачатию снижается. • На фоне лечения программным гемодиализом частота беременности составляет 1: 200 в течение года S. Hou, Am J Kidney Dis, 1999, 33, 2, 235 -52 • Процент вынашивания плода на диализе крайне низкий.

Беременность после трансплантации почки • После трансплантации восстанавливается. • Беременность после подготовленной. • почки АТП способность должна быть к зачатию планируемой и

Dr. Joseph Murray Трансплантация почки от однояйцового близнеца в 1956 г. –первая успешная трансплантация. Длительность функционирования почечного трансплантата 55 лет. 2 родов после трансплантации почки.

Беременность у женщин с почечным трансплантатом • Беременность у женщин с почечным трансплантатом - состояние высокого риска. • У 2% женщин детородного возраста после АТП наступает беременность, частота спонтанных абортов – 12 -13%, внематочная беременность – 0, 5%. • Развитие осложнений беременности: преэклампсия 30%. Эпизоды отторжения пт – 2 -12%, потеря почечного трансплантата в течение 2 -х лет -2 -14%. • У 1/3 беременных с почечным трансплантатом прерывание беременности происходит из-за неправильного планирования. • Наблюдение осуществляется у нефролога-трансплантолога, гинеколога, специализирующихся на патологии беременности.

Беременность у больных с почечным трансплантатом • Беременность должна быть планируемой и подготовленной. Лечение очагов инфекции должно осуществляться до наступления беременности (кариозные зубы, ХУГИ, герпетическая инфекция в т. ч. ЦМВ-инфекция). • Беременность планируется не раньше, чем через 2 года после трансплантации. • Процент вынашивания Более 90% беременностей, заканчиваются родами плода – 70 – 100%. преодолевших I триместр, • При Cr < 0, 13 – 0, 18 ммоль/л и отсутствии артериальной гипертензии прогноз в отношении благоприятного окончания беременности хороший, а риск снижения функции трансплантата невысокий. • Беременность не влияет на длительность функционирования почечного трансплантата при изначально сохранной функции.

Критерии снижения риска осложнений беременностей после трансплантации почки • Более 1 года после трансплантации почки • Уровень креатинина в сыворотке крови < 0, 2 ммоль/л, предпочтительно < 0, 15 ммоль/л • Отсутствие эпизодов отторжения (в течение года до наступления беременности) • Нормальное артериальное давление или минимальная гипотензивная терапия • Отсутствие или минимальная протеинурия • УЗИ трансплантата без отклонений от нормы • Безопасный для беременности режим иммуносупрессии (сандиммун, програф, азатиоприн, преднизолон). Микофенолаты должен быть отменены за 3 -6 месяцев до планируемой беременности.

Неонатальные проблемы у женщин с почечным трансплантатом • Малый вес плода, досрочные роды • Цитомегаловирусная инфекция • Возможен перенос HBs антигена • Врожденные аномалии Действие лекарств на плод и новорожденного: Использование преднизолона, циклоспорина и такролимуса не увеличивает частоту врожденных аномалий, но ассоциирует с малым весом плода. Влияние азатиоприна неизвестно на развитие отклонений в последующих поколениях, Прием микофенолатов приводит к патологии лицевого скелета и другим тератогенным уродствам)

Диспансерное наблюдение за беременными после трансплантации почки • Диспансерное наблюдение нефролога-трансплантолога. • В течение беременности необходимо динамическое наблюдение с исследованием мочи (цитологическое и бактериологическое) не реже 1 раза в 14 дней, а в сроки 20 -28 недель - еженедельно. • Контроль уровня АД, массы тела, суточного диуреза. • Динамический контроль протеинурии (общий анализ мочи, СПБ), уровня креатинина, мочевины, мочевой кислоты, трансаминаз, тромбоцитов, коагулограммы (для своевременной диагностики гестоза) • УЗИ почечного трансплантата • Ограничить проведение допплерографического исследования сосудов почечного трансплантата. • Наблюдение за состоянием плода (УЗИ плода).

Основные направления ведения беременных с почечным трансплантатом • Коррекция артериальной гипертензии. • Выявление и лечение мочевой инфекции у беременной (инфекции мочевых путей возникают в 40% случаев). Необходимо лечение уросептиками (канефрон 2 табл х 3 раза в день), антибактериальными препаратами (с учетом чувствительности микрофлоры и возможности использования антибактериальных препаратов во время беременности) • Предупреждение криза отторжения почечного трансплантата (необходимо мониторировать концентрацию икальциневрина, т. к. по мере прогрессирования беременности происходит снижение уровня последних в крови за счет увеличения ОЦК, следовательно, требуется коррекция дозы сандиммуна или прографа). • Профилактика гестоза

Метилдопа (Допегит) Центральные альфаадреномиметики Клофелин (Гемитон) per os: 1 таб. (250 мг) 2 -3 р. /сут, увеличивая каждые 2 дня на 1 таб. (максимум 2 г/сут) per os : ½ таб. (75 мкг) 2 -3 р. /сут, максимально до 1 таб(150 мкг) 4 р. /сут Нифедипин Блокатор кальциевых каналов Сублингвально: 10 -20 мг однократно per os: 10 мг 3 -4 р. /сут Нормодипи н Антагонист кальция III поколения 1 таб(5 мг). максимально- 10 мг/сутки Лабеталол Неселективный бета- и в/в: 50 -100 мг в 200 мл физ. р-ра альфа-блокатор per os: 1 таб(0, 1 г) 2 -3 р. /сут, максимально до 2 т. 3 р/сут Празозин альфа-блокатор постсинаптический per os: 1 таб (0, 5 мг) 2 -3 р. /сут, увеличивая дозу каждые 3 дня максимально до 1 мг 3 р. /сут Атенолол селективный бета-блокатор per os: 25 мг 2 р. /сут, постепенно увеличивая дозу максимально до 200 мг/сут Небиволол (Небилет) селективный бета-блокатор 0 днократно (2 раза в день) по 2, 5 -5 мг макс. суточная доза 10 мг (2 таб)

Основные направления ведения беременных с почечным трансплантатом • Профилактика гестоза: Восполнение микронутриентного дефицита: – препараты кальция - кальцемин, кальций Д 3 с 20 -й недели беремености по 1 табл х 2 р/сут – препараты магния (магний оказывает эндотелиопротективное действие, проявляющееся в активации выработки простациклина и оксида азота и подавлении тромбоксана А 2) – магне В 6 по 1 табл х 3 р/сут в течение 2 недель). • Снижение гипергомоцистеинемии – При сочетанном применении вит. В 6, В 12 и фолиевой кислоты происходит естественный метаболизм гомоцистеина и нейтрализация его повреждающего действия. Поэтому профилактически включают прием поливитаминов, содержащих весь ряд витаминов группы В, фолиевой кислоты, йода, а также бета-каротина (Центрум Матерна, Теравит Прегна). • Нормализация простациклин – тромбоксанового соотношения с помощью омега 3 полиненасыщенных жирных кислот, действие которых обусловлено влиянием на метаболизм арахидоновой кислоты. – Препараты, содержащие омега-3 ПНЖК (эйконол (30%), полиен (30%), атероблок (не менее 65%)). Доза 1 -2 капс. /сут, во время еды. Курс 2 -3 месяца.

Основные направления ведения беременных с почечным трансплантатом Профилактика гестоза: • Курсовое назначение дезагрегантов: курантил 25 мг по 1 табл х 3 р/сут – 3 -4 недели в 14, 20 и 30 недель. • Назначение антикоагулянтов – низкомолекулярные гепарины (фрагмин, фраксипарин, клексан), сулодексид (80% состоит из гепариноподобной фракции и 20% дерматан сульфата) 1 капс. 450 ед. х 2 -3 р/сут. 3 -4 недели в 14, 20 и 30 недель.

Родоразрешение • Родоразрешение (35 -37 недель). • Решение вопроса о прерывание беременности присоединении гестоза: при наличии эффекта от лечения беременность может быть пролонгирована до доношенного срока, при частичном эффекте – до срока жизнеспособности плода, при отсутствии эффекта от лечения – досрочное прерывание беременности. • Способ родоразрешения - преимущественно кесарево сечение. В США, Великобритании – 40 -92%. • Профилактика криза отторжения почечного трансплантата: интраоперационно (в момент пережатия пуповины) и первые сутки после родоразрешения вводится 250 мг солюмедрола, в/в, капельно. • Производится тщательное мониторирование концентрации в крови и-кальциневрина (сандиммун, програф). • Адекватное гидратирование больной после операции (перорально или в/в введение кристаллоидных растворов). • Прекращение лактации после родоразрешения.

Почечный трансплантат и беременность (клинический случай)

1 Больная Г. , 1975 г. р. • В феврале 2006 г в нефрологическом отделении ЛОКБ установлен диагноз гипоплазии обеих почек. Вторичная артериальная гипертензия (АД 160/100 мм. рт. ст. ). Гипотензивной терапии не получала. Терминальная ХПН с 2006 г. Симтоматическая анемия. В марте 2006 г было начато лечение программным гемодиализом. C марта по октябрь 2006 г. получала ЗПТ гемодиализом. • 17. 10. 06 выполнена операция трансплантации почки на правые наружные подвздошные сосуды. Донор и реципиент были негативны по HIV, ауто-HCV, HBs-Ag, CMV. Почечный трансплантат имеет 2 артериальных и один венозный сосуд на одной площадке. • 20. 10. 2006 г. - ревизия гемолимфоцеле. • Функция почечного трансплантата отсрочена. ОПН почечного трансплантата. В связи с подозрением на острый криз отторжения почечного трансплантата (повышение индексов периферического сопротивления в артериях почечного трансплантата) была проведена пульс-терапия солю-медролом в суммарной дозе 1, 5 г. • Получала 3 -х компонентную сандиммун, селлсепт, метипред. послеоперационной раны. иммуносупрессивную Эвакуация терапию:

• 09. 11. 2006 г. - нефробиопсия почечного трансплантата (1): Гистологическое исследование № 165728 -855/06 Светооптическое исследование выполнено с использованием следующих окрасок: гематоксилин-эозин, PAS-реакция, трихром по Массону, серебрение по Джонсу, Конго-красный. В биоптате 12 клубочков (СМ – 12, ИФ – 0), полностью склерозированных нет. Клубочки не увеличены в размерах, с одноконтурной капиллярной стенкой, без признаков увеличения клеточности, сегментарного склероза и формирования полулуний. Диффузное острое повреждение эпителия канальцев в виде утраты щеточной каймы и уплощения и дегенерации клеток с участками «симплификации» эпителия. Слабовыраженная лимфо-лейкоцитарная инфильтрация интерстиция. Стенки мелких артерий и артериол незначительно утолщены за счет гипертрофии мышечного слоя. Артерии более крупного калибра в материале не представлены. Слабовыраженный очаговый периваскулярный фиброз интерстиция. Иммунофлюоресцентное исследование выполнено на парафиновых срезах с использованием антисывороток к Ig. A, Ig. G, Ig. M, C 1 q, C 3, фибриногену, lambda&kappa легким цепям. Со всеми реагентами результат отрицательный. ЗАКЛЮЧЕНИЕ: Диффузный острый канальцевый некроз с явлениями «симплификации» эпителия. Примечание: в представленном материале признаков реакции отторжения трансплантата нет. 2

3 Результаты обследования: • ФЛГ 18. 10. 06. : Легкие расправлены застойно усилен легочный рисунок. Диафрагма особенностей. контурирует. Тень средостения без • УЗИ почечного трансплантата (20. 11. 06): размеры - 11, 5 х 5, 4 см, толщина паренхимы 1, 9 -2, 0 см, пирамидки 1, 2 см, центральный эхокомплекс не расширен, чашечки нормаль-ных размеров. У верхнего полюса ПТ лоцируется гипо-эхогенное образование 4, 7 х2, 7 см. и по заднему контуру неоднородная гипоэхогенная полоска – 4, 6 х2, 7 см. , у ниж-него полюса – справа жидкостное округлое образование 5, 4 х4, 9 см. • Допплерография почечного трансплантата (17. 11. 06): Внутрипочечное сосудистое сопротивление незначительно повышено, Pi – 1, 30 -1, 31 -1, 36, Ri - 0, 72 -0, 74 -0, 75. Сосудистый рисунок почки окрашивается равномерно до капсулы. Венозный отток не нарушен.

• Лечение – Проведено 10 сеансов ГД. С 11. 2006. ОПН в полиурической стадии (суточный диурез 1, 6 -2, 4 л). – Иммуносупрессивная терапия: • Сандиммун 360 мг/сут. • Селлсепт 2 г/сут. • Метипред 4 мг – 3, 5 табл/сут. • Ps-терапия солю-медролом 1, 5 г. – Дополнительная терапия: • Дилтиазем-ретард, • Амоксиклав, азаран, нолицин, • Бисептол-480, • Фуросемид, лазикс, • Нистатин, • Омепразол. • 30. 11. 2006 г. (43 сутки) была выписана на амбулаторное лечение. К выписке почечный трансплантат функционировал удовлетворительно (Cr 0, 145 ммоль/л, Ur 9, 9 ммоль/л). Цифры артериального давления снизились до нормальных значений на фоне приема Са-блокаторов (дилтиазем). 4

Повторная госпитализация – декабрь 2006 г. • Госпитализация в отделение сосудистой хирургии и трансплантации почки ЛОКБ с 08. 12. 06. по 28. 12. 2006, в связи с развитием лихорадки до 390 С, повышением азотемических показателей (Сr 0, 154 ммоль/л, Ur 10, 9 ммоль/л), увеличением размеров лимфоцеле, изменениями в анализах мочи (бактериурия – E. coli 106 в 1 мл). Проведено обследование: УЗИ почечного трансплантата (08. 12. 06): размеры - 11, 3 х 5, 2 см, толщина паренхимы 1, 8 см, пирамидки 1, 0 см, эхогенность повышена, пирамидки 1, 1 см, чашечки нормальных размеров, лоханка 1, 5 см. ЦЭК не расширен. У нижнего полюса пт анэхогенное образование с гиперэхогенными включениями с четкими контурами (6, 0 х5, 0 см), у верхнего полюса ПТ лоцируется аналогичное образование 3, 0 х2, 0 см. Свободной жидкости в брюшной полости и малом тазу не определяется. Допплерография почечного трансплантата (12. 06): Внутрипочечное сосудистое сопротивление нормальное, Pi – 1, 13 -1, 26 -1, 28, Ri - 0, 68 -0, 70 -0, 73. Сосудистый рисунок почки окрашивается равномерно до капсулы. Венозный отток не нарушен. V max V. ren. – 0, 58 м/с. • 14. 12. 2006 г выполнена операция: фенестрация лимфоцеле почечного трансплантата правой подвздошной области. Температура тела нормализовалась, лимфоцеле уменьшилось в размерах (по данным УЗИ пт – 2, 5 х1, 5 см). Получала антибактериальную терапию (медоклав). 5

Лечение • Иммуносупрессия: – Сандиммун 360 мг, – Метипред 4 мг 3, 5 табл. , – Селлсепт 1 г/сут. • Дополнительная терапия: – – – Омез 20 мг 1 таб. в сутки. Дилтиазем-ретард 90 мг 2 таб. в сутки. Бисептол-480 1 таб. в сутки. Медоклав 625 мг х 2 р/сут. Бифидум – бактерин 5 доз (по 5 доз х 3 раза в день) – 2 недели. – Вальцит 450 мг по 1 табл х 2 раза в день (3 мес. ) (Выявлена ЦМВ-инфекция (ЦМВ-синдром) – ПЦР ДНК 6, 6 х 10 3 копий в 1 мл. Получала противовирусную терапию цимевеном (№ 6), в/в, с дальнейшим переходом на вальцит (900 мг/сут). – Сорбифер-дурулес по 1 табл х 2 р/день. 6

7 Диагноз: ХБП V ст. (т). Гипоплазия обеих почек. Нефросклероз. Аллотрансплантация трупной почки на правые наружные подвздошные сосуды от 17. 10. 2006 г. Хронический пиелонефрит почечного трансплантата.

8 Динамика показателей крови 2006 -2008 гг 17. 10. 06 -операция 23. 10. 2006 17. 11. 2006 Повторная госпитализация 22. 12. 06 06. 12. 2007 15. 12. 2008 0, 314 0, 1062 0, 145 0, 092 65, 7 0, 103 64 0, 099 67 Ur Mm/L - 39, 4 9, 9 9, 8 8, 2 7, 91 Chol mkmol/l 3, 99 - - 5, 17 4, 29 - Сахар Mm/L 2, 58 - 5, 42 4, 39 4, 94 5, 08 Hb гл 123 68 72 76 113 118 Er х 1012/л 4, 07 2, 2 2, 56 2, 74 3, 77 3, 99 Tr х 109/л 316 196 347 519 228 267 Конц. Cs. A нг/мл - Со 228 С 2 1001 Со 153, 7 С 2 831, 2 Со 186, 5 Со 107 Со- 141 ПЦР ЦМВ ДНК-копий Отриц. 8, 2 х 102 2, 2 х 103 Показатели Cr Mm/L СКФ мл/мин 6, 6 х 103

9 Динамика показателей мочи 2006 -2008 гг. 17. 10. 06 -операция 23. 10. 2006 17. 11. 2006 Повторная госпитализация 22. 12. 06 06. 12. 2007 15. 12. 2008 Относ. плотность ― 1017 1006 1016 1007 Белок г/л ― 0, 6 0, 14 0, 31 следы Лейкоциты ― 7 -9 -11 10 -15 1 -2 -3 Густо все п/зр 4 -6 -9 Эритроциты ― 10 -15 нет 15 -20 30 -40 -50 0 -2 -3 Цилиндры ― Гиалиновые ед. нет ― ― нет СПБ, г/сут ― 0, 86 ― 1, 98 0, 23 0, 128 Посев мочи ― ― ― E. Coli 10 6 ― Показатели

Иммуносупрессивная терапия и концентрация сандиммуна/прографа 17. 10. 2006 -операция 23. 10. 2006 17. 11. 2006 Повторная госпитализация Cs. A, мг ― 500 360 Концентрация и-кальциневрина, нг/мл ― Со 228 С 2 1001 ММФ, г 2 г 2 г Показатели Метипред 4 мг 500 мг, в/в, интраоперационно 6 табл 10 Госпитализация март-апрель 06. 12. 2007 15. 12. 2008 360 220 Конверсия на програф (6 мг/сут) Со 153, 7 С 2 831, 2 Со 186, 5 Со 107 Со 141 Pr 6, 4 2 г 2 -1 г (ЦМВ 103 копий) 2 г 2 г-1 г (ЦМВ 103 копий) Конверсия с ММФ на 1, 5 табл 1, 5 табл 4, 5 табл 22. 12. 06 4 табл 2009 Cr – 0, 121 Mm/L Aza (100 мг/сут) в январе 2009 1, 5 табл

• Госпитализация в отделение сосудистой хирургии и трансплантации почки в марте 2009 г, в связи с ухудшением функции почечного трансплантата (Cr 0, 115 – 0, 123 ммоль/л). • При поступлении в стационар: – Объективный статус: Состояние удовлетворительное. Кожные покровы обычной окраски. Периферические лимфоузлы не увеличены. Щитовидная железа не увеличена. Ps 80 уд. мин. АД 140/90 мм. рт. ст. (120/80 мм. рт. ст. – без гипотензивных препаратов). Границы сердца не расширены. Тоны сердца ясные чистые. ЧД 16 в 1 мин. Перкуторно ясный легочный звук. Дыхание везикулярное, хрипов нет. Живот мягкий, безболезненный. Печень не увеличена. Селезенка не пальпируется, перкуторно не увеличена. Почечный трансплантат умеренно плотный, безболезненный, не увеличен. Суточный диурез 1, 1 л. Физиологические отправления в норме. 11

12 • Инструментальные исследования: – УЗИ почечного трансплантата от 13. 03. 2009. Заключение: В правой подвздошной области лоцируется пт размерами 11, 8 х 5, 8 см, паренхима 1, 7 -1, 8 см. ЦЭК не расширен. – ФГДС от 19. 03. 09: Заключение: Хронический гастрит. – ЭХО-КГ от 17. 03. 09: Заключение: Патологии клапанов и миокарда не выявлено. – УЗДГ пт от 27. 02. 2009. : Визуально почечный трансплантат без особенностей. В зонах артериального и венозного анастомозов и по АА. Почечного трансплантата гемодинамически значимых локальных нарушений кровотока не выявлено. Скоростные показатели кровотока в диапазоне нормативных значений. Показатели периферического сопротивления умеренно повышены. Pi Ri V max м/с a. ren. 1, 41 0, 72 1, 1 aa. interlob. 1, 53 0, 77 0, 48

• 16 марта 2009 г произведена нефробиопсия (2) почечного трансплантата. Гистологическое исследование № 25871 -907/09 Светооптическое исследование выполнено с использованием следующих окрасок: гематоксилин-эозин, PAS-реакция, трихром по Массону, импрегнация солями серебра по Джонсу, Конгокрасный. В материале нефробиопсии представлен только корковый слой ткани почки; 29 клубочков (СМ-23, ИФ-6), из них полностью склерозированы 3 (10%) клубочка (СМ). Клубочки умеренно увеличены, с одноконтурной капиллярной стенкой, с незначительным расширением мезангиального пространства за счет матрикса; без признаков сегментарного склероза и формирования полулуний. В просветах отдельных капилляров клубочков – группы лимфоцитов. Цитоплазма эпителия канальцев с сохраненной щеточной каймой. Диффузно-очаговая незначительная атрофия канальцев с утолщением и сморщиванием базальной мембраны. Цилиндры отсутствуют. Стенки артериол и мелких артерий значительно утолщены за счет гипертрофии мышечного слоя и очаговых субадвентициальных инсудативных изменений. Артерии более крупного калибра в материале не представлены. В интерстиции диффузно-очаговый слабовыраженный фиброз с незначительной клеточной инфильтрацией, представленной лимфоцитами и плазматическими клетками. Иммунофлюоресцентное исследование выполнено на парафиновых срезах с использованием FITC-коньюгированных антител к человеческим Ig. A, Ig. G, Ig. M, C 1 q, C 3, фибриногену, lambda&kappa легким цепям. Со всеми реагентами результат отрицательный. Иммуногистохимическое исследование выполнено на парафиновых срезах иммунопероксидазным методом с использованием антител к C 4 d компоненту системы комплемента. Диффузная гранулярная экспрессия C 4 d (++) в мезангиальном пространстве клубочков (внутренний контроль) и вдоль базальных мембран перитубулярных капилляров. - - ЗАКЛЮЧЕНИЕ: «Подозрение» на реакцию острого отторжения трансплантата: гломерулит (g 1), интерстициальная инфильтрация (i 1); C 4 d(+); Хроническая CYA-токсичность: гиалиновая артериолопатия (ah 2). 13

• Лечение – Иммуносупрессивная терапия: • Конверсия с сандиммуна на програф 6 -5, 5 мг/сут, • Азатиоприн 50 мг 2 табл/сут, • Метипред 4 мг 1, 5 табл/сут. (1 табл/сут. с октября 2009 г. ) – Дополнительная терапия: Сорбифер-дурулес (2 табл/сут), альфа-Д 3 ТЕВА 0, 25 мкг/сут. Полное восстановление азотвыделительной функции почечного трансплантата к 09. 2009 г. 14

• 17. 03. 2010 г – 07. 04. 2010. – госпитализация в отделение патологии беременности ЛОКБ. Диагноз: Беременность 13 недель. Соп: Хроническая внутриматочная инфекция, вне обострения. Инфекция мочевых путей (бессимптомная бактериурия). Кандидозный кольпит. Хронический гастрит, вне обострения. • Гинекологический анамнез: Menses с 13 лет, регулярные, безболезненные, необильные. Б-5, Р-1 (кесарево сечение 1995 г – поздний гестоз), А-3, В-0. • • Проведено обследование: Заключение: Беременность прогрессирует, соответствует сроку гестации. Фунция почечного трансплантата сохранена. Проводилась антибактериальная терапия бссимптомной бактериурии, лечение кандидозного кольпита. ЭХО-КГ, УЗИ брюшной полости, почечного трансплантата, плода – без отклонений от нормы. Коагулограмма от 23. 03. 2010: Гиперфибриногенемия. Биохимический пренатальный скрининг: – Ассоциированный с беременностью протеин-А плазмы (РАРР-А) – 1, 45; – Хорионический гонадотропин человека (в. ХГЧ) – 1, 8. 15

• • 22. 04. – 18. 05. 2010 – госпитализация в «Научный центр акушерства, гинекологии и перинатологии им. В. И. Кулакова» Минздравсоцразвития. Проведено обследование: – Диагностика антифосфолипидного синдрома: результат отрицательный. – Определение генетической предрасположенности к тромбофилии от 27. 04. 2010: Гомозиготная мутация фактора Лейдена, гетерозиготная мутация генов гликопротеин-1 а, тробоцитарного рецептора фибриногена. – Определение полиморфизма генов фолатного цикла от 27. 04. 2010: МГТРФ, Метионинсинтаза редуктаза – гетерозиготная мутация. – Тиреоидные гормоны: ТТГ, Т 4, АТ к ТПО, АТ к ТГ – в норме. – Б/х пренатальный скрининг от 04. 05. 2010: в. ХГ – 29, 013 МЕ/л, АФП – 32 МЕ/л, эстриол – 10, 6 нмоль/л, 17 -ОН-прогестерон – 7, 7 нмоль/л. Проведена компьютерная обработка данных б/х пренатального скрининга – вычисленный риск трисомии 21 выше порога отсечки. Б/х риск > 1: 50, возрастной риск 1: 324. – УЗИ плода от 17. 05. 2010: 1 плод, размеры плода соответствуют 19 нед. 5 дням бременности. Плацента расположена по передней стенке матки, толщина 2, 5 см, «О» степени зрелости. Количество вод в норме. Патологии со стороны плода не выявлено. Длина шейки матки 3, 8 см, внутренний зев сомкнут, ц/к не расширен. 16

Динамика показателей крови 2009 -2010 гг. Показатели Госпитализация март-апрель (13 недель) 2009 Cr Mm/L СКФ мл/мин 05. 2009 07. 09. 2009 17. 03 -07. 04. 2010 18 22. 04. -18. 05. 2010. НЦ Акушерства, гинекологии и перинатологии им. В. И. Кулакова г. Москва (15 -16 недель) Отделение патологии беременности ЛОКБ 0, 121 -0, 109 0, 108 99 0, 094 0, 076 83 0, 100 -0, 078 48, 6 - 61, 9 Ur Mm/L 9, 77 -10, 2 11, 1 7, 34 4, 91 8, 0 Chol mkmol/l - - - 3, 92 - Сахар Mm/L 4, 73 5, 01 4, 89 4, 6 4, 1 Hb г/л 111 - 118 110 124 Er х 1012/л 3, 6 - 3, 42 3, 22 3, 65 Tr х 109/л 284 - 244 218 178 Конверсия на програф нг/мл 9, 1 8, 7 5, 6 5, 4 4, 3 Отриц. - - ПЦР ЦМВ ДНК-копий

19 Динамика показателей мочи 2009 -2010 гг. Госпитализация март-апрель 2009 Отделение патологии беременности ЛОКБ 1006 1019 1020 следы 0, 06 нет Лейкоциты 2 -3 -4 20 -30 -40 75 Эритроциты 0 -2 -1 0 -0 -2 нет Цилиндры нет нет СПБ, г/сут 0, 12 0, 066 нет ― E. Coli 107 - 10 5 (курс антибактериальной терапии 7 дней: E. Coli 107 - 10 5 Курс антибактериальной терапии 16 дней: амоксиклав. Показатели Относ. плотность Белок г/л Посев мочи 17. 03 -07. 04. 2010 ампициллин – возникла резистентность) 22. 04. -18. 05. 2010. НЦ Акушерства и гинекологии и перинатологии им. Кулакова г. Москва

20 Результаты обследования от 09. 06. 2010 Беременность 22 -23 недели • АД 110 -120/80 мм. рт. ст. (без гипотензиных препаратов), отеков нет. Суточный диурез 1 л. Вес 65 кг. • Клинические и биохимические показатели в норме. Функция почечного трансплантата остается сохранной (Сr 0, 077 ммоль/л ). Анализ крови на ЦМВ в работе. • В анализе мочи – лейкоцитурия (до 10 лейкоцитов в п/зр), бактериурия (+). Посев мочи в работе. • УЗИ почечного трансплантата от 09. 06. 2010. : В правой подвздошной области лоцируется пт размерами 13, 3 х 6, 6 см, паренхима 2, 0 см. ЦЭК не расширен, чашечки N.

УЗИ почечного трансплантата (ЛОКБ) 21

УЗИ почечного трансплантата и плода (плацента) 24

УЗИ почечного трансплантата и плода (плацента) УЗИ плода (23 недели)

25 • Лечение: 2 -компонентная иммуносупрессивная терапия • Програф 6 мг/сут (Концентрация 09. 06. 2010. - Со 3, 8 нг/мл). • Метипред 1 табл/сут. – Дополнительная терапия: • Канефрон 2 табл х 3 раза/сут. • Альфа Д 3 ТЕВА 0, 25 мкг/сут. • Элевит 1 драже/сут. • Йодомарин 250 мкг/сут. • Фолиевая кислота 1 табл х 3 р/сут. прографа от

• В начале сентября 2010 г – развитие гестоза легкой степени (появление отеков нижних конечностей, артериальной гипертензии – АД 140 -150/90 мм. рт. ст, протеинурии – 0, 3 -0, 4 г/л). • Госпитализация в отделение патологии беременности СПб ГУ им. акад. И. П. Павлова, где 16. 09. 2010. было произведено кесарево сечение в 37 недель беременности. • Ребенок доношен, девочка. Рост - 50 см, вес – 3, 0 кг. • В послеродовом периоде почечный трансплантат функционирует удовлетворительно: креатинин – 0, 085 ммоль/л, отеки регрессировали, артериальное давление нормализовалось. • Произведена коррекция имуносупрессивной терапии: уменьшена доза прографа (6 мг/сут) – концентрация прографа – 4, 9 нг/мл, возобновлен прием азатиоприна 100 мг/сут.

Больная Г. , 35 лет Поперечный срез почечного трансплантата Плацента

Больная, А. , 1973 г. р. • • • В анамнезе хронический пиелонефрит с исходом в ХПН. АТП в 1996 г. 2 х-компонентная ИСТ: сандиммун 200 мг/сут, метипред (15 мг/ч/д). Прерывание 1 -й беременности по мед. показаниям (1994 г). 2 -я беременность - роды в 37 недель (кесарево сечение 17. 10. 1998 г). Беременность не ухудшила функцию почечного трансплантата.

Для чего нужна трансплантация почки? • Социальная адаптация пациента. • Улучшается качество жизни – (нет ограничения водного режима, кратность посещений врача реже, возможность выезжать на пределы места проживания). • У женщин репродуктивного возраста появляется возможность родить ребенка.

Пациенты после трансплантации почки 2007 г. Трансплантация почки – 1996 г. 2009 г.
трансплантация октябрь 2015-2.ppt