транс..pptx
- Количество слайдов: 19
 Трансплантационный иммунитет Подготовила : Петриашвили И. Р. 309 леч. , фак.
Трансплантационный иммунитет Подготовила : Петриашвили И. Р. 309 леч. , фак.
 Проведение трансплантации органов и тканей стало насущной потребностью современного общества. За последнее десятилетие в развитых странах мира достигнут значительный прогресс в области трансплантации клеток, тканей и органов. Трансплантология сегодня — это наиболее развитая и высокотехнологичная направление здравоохранения. Нет той области медицины, где она не применяется: кардиология, гепатология, онкология, травматология, офтальмология, дерматология и т. д. Становление трансплантологии как науки прошло сложный путь. Проблема трансплантации требует тщательного изучения медицинских, юридических, социальных и нравственных аспектов.
Проведение трансплантации органов и тканей стало насущной потребностью современного общества. За последнее десятилетие в развитых странах мира достигнут значительный прогресс в области трансплантации клеток, тканей и органов. Трансплантология сегодня — это наиболее развитая и высокотехнологичная направление здравоохранения. Нет той области медицины, где она не применяется: кардиология, гепатология, онкология, травматология, офтальмология, дерматология и т. д. Становление трансплантологии как науки прошло сложный путь. Проблема трансплантации требует тщательного изучения медицинских, юридических, социальных и нравственных аспектов.
 Антигены HLA и типирование тканей В последнее время наряду с трансплантацией костного мозга, почки, печени и сердца стали применять трансплантацию тонкой кишки, доли и сегментов печени, легкого, костей, поджелудочной железы и клеток панкреатических островков, а также других органов и тканей. Для трансплантации используются как трупные, так и полученные от живых доноров органы и ткани. Чаще донорами служат родственники реципиента. После трансплантации в организме реципиента развивается иммунный ответ на многочисленные антигены трансплантата. Исключение составляют случаи, когда донор и реципиент — однояйцовые близнецы. Наиболее изученные антигены человека, с которым связан иммунный ответ на трансплантат, — это антигены HLA (Human Leukocyte Antygen - HLA)
Антигены HLA и типирование тканей В последнее время наряду с трансплантацией костного мозга, почки, печени и сердца стали применять трансплантацию тонкой кишки, доли и сегментов печени, легкого, костей, поджелудочной железы и клеток панкреатических островков, а также других органов и тканей. Для трансплантации используются как трупные, так и полученные от живых доноров органы и ткани. Чаще донорами служат родственники реципиента. После трансплантации в организме реципиента развивается иммунный ответ на многочисленные антигены трансплантата. Исключение составляют случаи, когда донор и реципиент — однояйцовые близнецы. Наиболее изученные антигены человека, с которым связан иммунный ответ на трансплантат, — это антигены HLA (Human Leukocyte Antygen - HLA)
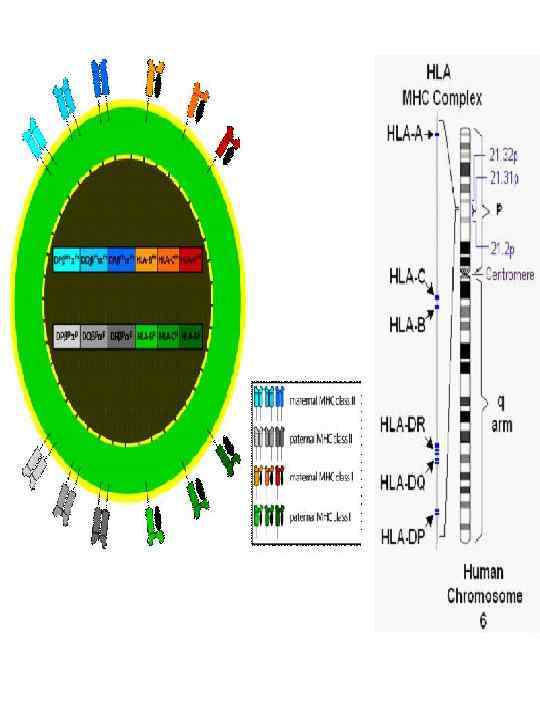
 Главный комплекс гистосовместимости человека был открыт в 1952 г. при изучении антигенов лейкоцитов. Антигены HLA (MHC) представляют собой гликопротеиды, находящиеся на поверхности клеток и кодируемые группой тесно сцепленных генов 6 -й хромосомы. Выделяют 2 класса антигенов HLA (MHC). К классу I относятся антигены A, B и C, а к классу II — антигены DR, DP и DQ. Антигены класса I присутствуют на поверхности всех ядросодержащих клеток и тромбоцитов, антигены класса II — на поверхности Bлимфоцитов, активированных T-лимфоцитов, моноцитов, макрофагов и дендритных клеток. Гены HLA обозначаются так же, как антигены HLA, но название гена пишется курсивом, а антигена — обычным шрифтом. Названия генов и антигенов HLA состоят из одной или нескольких букв и цифр, например A 3, B 45, DR 15, DQ 4. Буква обозначает ген, а цифра аллель этого гена, при этом цифровые обозначения присваиваются по мере открытия новых аллелей. Гены HLA обладают высоким полиморфизмом, определено более 100 антигенов HLA. Антигены HLA (MHC) играют важнейшую роль в регуляции иммунного ответа на чужеродные антигены и сами являются сильными антигенами.
Главный комплекс гистосовместимости человека был открыт в 1952 г. при изучении антигенов лейкоцитов. Антигены HLA (MHC) представляют собой гликопротеиды, находящиеся на поверхности клеток и кодируемые группой тесно сцепленных генов 6 -й хромосомы. Выделяют 2 класса антигенов HLA (MHC). К классу I относятся антигены A, B и C, а к классу II — антигены DR, DP и DQ. Антигены класса I присутствуют на поверхности всех ядросодержащих клеток и тромбоцитов, антигены класса II — на поверхности Bлимфоцитов, активированных T-лимфоцитов, моноцитов, макрофагов и дендритных клеток. Гены HLA обозначаются так же, как антигены HLA, но название гена пишется курсивом, а антигена — обычным шрифтом. Названия генов и антигенов HLA состоят из одной или нескольких букв и цифр, например A 3, B 45, DR 15, DQ 4. Буква обозначает ген, а цифра аллель этого гена, при этом цифровые обозначения присваиваются по мере открытия новых аллелей. Гены HLA обладают высоким полиморфизмом, определено более 100 антигенов HLA. Антигены HLA (MHC) играют важнейшую роль в регуляции иммунного ответа на чужеродные антигены и сами являются сильными антигенами.
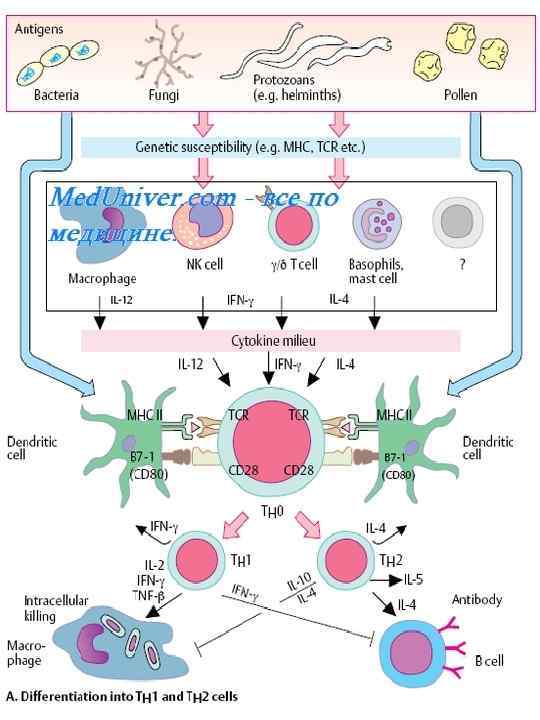
 Механизмы трансплантационного иммунитета Иммунный ответ на трансплантат обусловлен в первую очередь распознаванием антигенов HLA (MHC) донора, расположенных на поверхности мембран, пересаженного органа, лимфоцитами реципиента. Это вызывает активацию T-хелперов (Th 1, 2), которые, в свою очередь, стимулируют пролиферацию цитотоксических T-лимфоцитов и Bлимфоцитов. Антитела к чужеродным антигенам HLA могут присутствовать в сыворотке реципиента и до трансплантации. Их выявление свидетельствует о предшествующей иммунизации антигенами HLA. Она возможна при переливании цельной крови и во время беременности. Выявление в сыворотке реципиента антител к антигенам HLA донора свидетельствует о высоком риске сверхострого отторжения трансплантата. Оно обусловлено образованием комплексов, состоящих из антигенов трансплантата и антител реципиента, которые активируют свертывание крови и приводят к тромбозу сосудов трансплантата. Поскольку отторжение трансплантата вызывают чужеродные антигены HLA, лучший способ его профилактики — подбор донора, совместимого с реципиентом по антигенам HLA. Если реципиент уже иммунизирован антигенами HLA, донор должен быть полностью совместим с реципиентом.
Механизмы трансплантационного иммунитета Иммунный ответ на трансплантат обусловлен в первую очередь распознаванием антигенов HLA (MHC) донора, расположенных на поверхности мембран, пересаженного органа, лимфоцитами реципиента. Это вызывает активацию T-хелперов (Th 1, 2), которые, в свою очередь, стимулируют пролиферацию цитотоксических T-лимфоцитов и Bлимфоцитов. Антитела к чужеродным антигенам HLA могут присутствовать в сыворотке реципиента и до трансплантации. Их выявление свидетельствует о предшествующей иммунизации антигенами HLA. Она возможна при переливании цельной крови и во время беременности. Выявление в сыворотке реципиента антител к антигенам HLA донора свидетельствует о высоком риске сверхострого отторжения трансплантата. Оно обусловлено образованием комплексов, состоящих из антигенов трансплантата и антител реципиента, которые активируют свертывание крови и приводят к тромбозу сосудов трансплантата. Поскольку отторжение трансплантата вызывают чужеродные антигены HLA, лучший способ его профилактики — подбор донора, совместимого с реципиентом по антигенам HLA. Если реципиент уже иммунизирован антигенами HLA, донор должен быть полностью совместим с реципиентом.
 Подбор донора Подобрать донора, полностью совместимого с реципиентом по антигенам HLA, очень сложно, поскольку число комбинаций, составленных более чем из 100 антигенов этого семейства, чрезвычайно велико. Вероятность найти полностью совместимого донора составляет от 1: 1000 до 1: 1 000. Вероятность подбора полностью совместимого донора среди родных братьев и сестер составляет 1: 4, так как гены HLA наследуются по законам Менделя.
Подбор донора Подобрать донора, полностью совместимого с реципиентом по антигенам HLA, очень сложно, поскольку число комбинаций, составленных более чем из 100 антигенов этого семейства, чрезвычайно велико. Вероятность найти полностью совместимого донора составляет от 1: 1000 до 1: 1 000. Вероятность подбора полностью совместимого донора среди родных братьев и сестер составляет 1: 4, так как гены HLA наследуются по законам Менделя.
 Гены HLA наследуются кодоминантно и передаются потомству двумя блоками — по одному от каждого родителя. Такой блок носит название гаплотипа HLA. Частота рекомбинаций внутри гаплотипа HLA составляет около 1%, в материнской хромосоме она несколько выше. Ребенок наследует по два аллеля каждого гена HLA: один из материнского гаплотипа, другой — из отцовского. Совокупность антигенов HLA, представленных на поверхности клеток, составляет фенотип HLA, например A 1, A 24, B 35, B 44, Cw 4, Cw 5, DR 6, DR 7, DQ 1, DQ 2. По фенотипу HLA нельзя судить о составе гаплотипов. Гаплотип HLA можно установить лишь при анализе наследования генов HLA в семье. Если отцовские гаплотипы HLA обозначить буквами a и b, а материнские — c и d, у потомства возможны 4 комбинации гаплотипов. При этом вероятность совпадения и вероятность полного несовпадения генотипов HLA детей и родителей составляет 25%, а вероятность совпадения одного из гаплотипов — 50%. Типирование антигенов HLA у родственников реципиента проводят для подбора донора, совместимого с реципиентом по одному или обоим гаплотипам. Если гаплотипы HLA двух родственников совпадают хотя бы по нескольким антигенам HLA (MHC) классов I и II, с высокой вероятностью можно предположить, что остальные гены, входящие в гаплотипы HLA этих родственников, также идентичны. При совместимости донора и реципиента по антигенам HLA отторжение трансплантата можно предотвратить с помощью минимальной иммуносупрессивной терапии, необходимой для подавления иммунного ответа на слабые антигены гистосовместимости, не относящиеся к антигенам HLA. Найти донора, полностью совместимого с реципиентом по антигенам HLA, среди людей, не являющихся его родственниками, почти невозможно, поэтому доноров чаще подбирают среди братьев и сестер реципиента. Среднее время до отторжения трансплантата при трансплантации от полностью совместимого по антигенам HLA родственника составляет 22, 4 года, а при трансплантации трупного органа — 4, 6 года. Применение циклоспорина при трансплантации несовместимых по HLA органов и тканей снизило риск раннего отторжения трансплантата, но не повлияло на риск позднего отторжения.
Гены HLA наследуются кодоминантно и передаются потомству двумя блоками — по одному от каждого родителя. Такой блок носит название гаплотипа HLA. Частота рекомбинаций внутри гаплотипа HLA составляет около 1%, в материнской хромосоме она несколько выше. Ребенок наследует по два аллеля каждого гена HLA: один из материнского гаплотипа, другой — из отцовского. Совокупность антигенов HLA, представленных на поверхности клеток, составляет фенотип HLA, например A 1, A 24, B 35, B 44, Cw 4, Cw 5, DR 6, DR 7, DQ 1, DQ 2. По фенотипу HLA нельзя судить о составе гаплотипов. Гаплотип HLA можно установить лишь при анализе наследования генов HLA в семье. Если отцовские гаплотипы HLA обозначить буквами a и b, а материнские — c и d, у потомства возможны 4 комбинации гаплотипов. При этом вероятность совпадения и вероятность полного несовпадения генотипов HLA детей и родителей составляет 25%, а вероятность совпадения одного из гаплотипов — 50%. Типирование антигенов HLA у родственников реципиента проводят для подбора донора, совместимого с реципиентом по одному или обоим гаплотипам. Если гаплотипы HLA двух родственников совпадают хотя бы по нескольким антигенам HLA (MHC) классов I и II, с высокой вероятностью можно предположить, что остальные гены, входящие в гаплотипы HLA этих родственников, также идентичны. При совместимости донора и реципиента по антигенам HLA отторжение трансплантата можно предотвратить с помощью минимальной иммуносупрессивной терапии, необходимой для подавления иммунного ответа на слабые антигены гистосовместимости, не относящиеся к антигенам HLA. Найти донора, полностью совместимого с реципиентом по антигенам HLA, среди людей, не являющихся его родственниками, почти невозможно, поэтому доноров чаще подбирают среди братьев и сестер реципиента. Среднее время до отторжения трансплантата при трансплантации от полностью совместимого по антигенам HLA родственника составляет 22, 4 года, а при трансплантации трупного органа — 4, 6 года. Применение циклоспорина при трансплантации несовместимых по HLA органов и тканей снизило риск раннего отторжения трансплантата, но не повлияло на риск позднего отторжения.
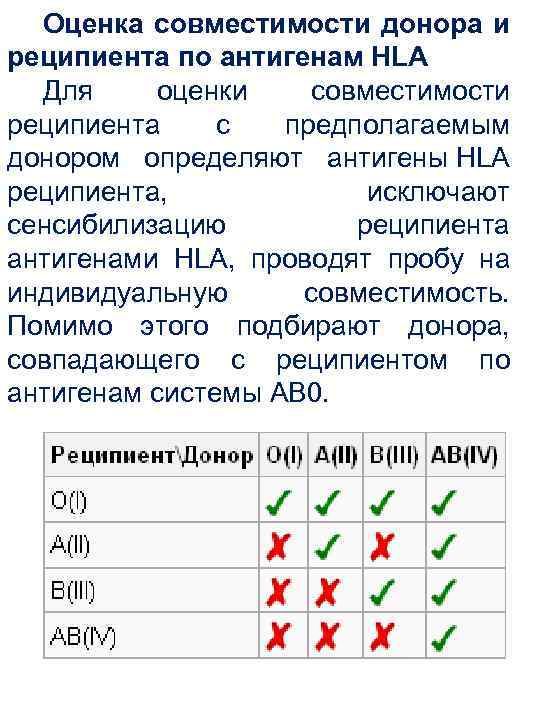 Оценка совместимости донора и реципиента по антигенам HLA Для оценки совместимости реципиента с предполагаемым донором определяют антигены HLA реципиента, исключают сенсибилизацию реципиента антигенами HLA, проводят пробу на индивидуальную совместимость. Помимо этого подбирают донора, совпадающего с реципиентом по антигенам системы AB 0.
Оценка совместимости донора и реципиента по антигенам HLA Для оценки совместимости реципиента с предполагаемым донором определяют антигены HLA реципиента, исключают сенсибилизацию реципиента антигенами HLA, проводят пробу на индивидуальную совместимость. Помимо этого подбирают донора, совпадающего с реципиентом по антигенам системы AB 0.
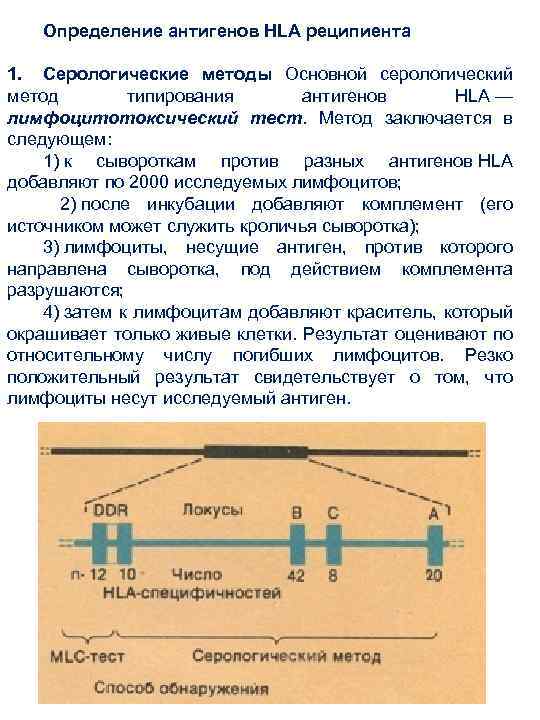 Определение антигенов HLA реципиента 1. Серологические методы Основной серологический метод типирования антигенов HLA — лимфоцитотоксический тест. Метод заключается в следующем: 1) к сывороткам против разных антигенов HLA добавляют по 2000 исследуемых лимфоцитов; 2) после инкубации добавляют комплемент (его источником может служить кроличья сыворотка); 3) лимфоциты, несущие антиген, против которого направлена сыворотка, под действием комплемента разрушаются; 4) затем к лимфоцитам добавляют краситель, который окрашивает только живые клетки. Результат оценивают по относительному числу погибших лимфоцитов. Резко положительный результат свидетельствует о том, что лимфоциты несут исследуемый антиген.
Определение антигенов HLA реципиента 1. Серологические методы Основной серологический метод типирования антигенов HLA — лимфоцитотоксический тест. Метод заключается в следующем: 1) к сывороткам против разных антигенов HLA добавляют по 2000 исследуемых лимфоцитов; 2) после инкубации добавляют комплемент (его источником может служить кроличья сыворотка); 3) лимфоциты, несущие антиген, против которого направлена сыворотка, под действием комплемента разрушаются; 4) затем к лимфоцитам добавляют краситель, который окрашивает только живые клетки. Результат оценивают по относительному числу погибших лимфоцитов. Резко положительный результат свидетельствует о том, что лимфоциты несут исследуемый антиген.
 2. Молекулярно-генетические методы Генетическое типирование стало возможным после расшифровки нуклеотидной последовательности генов HLA и выявления различий между разными аллелями этих генов. В настоящее время молекулярногенетические методы используются только для типирования генов HLA класса II. Анализ полиморфизма длин рестрикционных фрагментов В целом последовательность нуклеотидов во всех аллелях одного гена HLA класса II однотипна, уникальны лишь замены нуклеотидов в тех областях, которые отвечают за синтез вариабельных участков. Метод основан на способности бактериальных эндонуклеаз расщеплять ДНК в тех участках, в которых сосредоточены специфические для определенной эндонуклеазы последовательности нуклеотидов — сайты рестрикции. Сайты рестрикции для данной эндонуклеазы в разных аллелях одного гена располагаются на разном расстоянии друг от друга, поэтому длина рестрикционных фрагментов у разных аллелей разная. Применение эндонуклеаз позволило выявить полиморфизм длин рестрикционных фрагментов ДНК, подобный полиморфизму HLA, определяемому серологически. По длине фрагментов судят о присутствии тех или иных аллелей HLA у исследуемого. Если у донора и реципиента выявляются фрагменты одинаковой длины, считается, что они несут один и тот же аллель HLA. Определение специфических олигонуклеотидных последовательностей Аллели генов HLA иногда отличаются друг от друга лишь по одной паре нуклеотидов. Синтезированы одноцепочечные олигонуклеотидные зонды, состоящие из 19— 24 нуклеотидов, полностью комплементарные уникальным последовательностям каждого известного аллеля гена HLA. Таким образом, для определения неизвестного аллеля можно последовательно использовать серию зондов разной специфичности. ПЦР — метод, предназначенный для получения большого количества копий фрагментов ДНК с определенной нуклеотидной последовательностью. Полученные копии исследуют с помощью набора олигонуклеотидных зондов. Разрабатывается молекулярногенетическое типирование генов HLA класса I.
2. Молекулярно-генетические методы Генетическое типирование стало возможным после расшифровки нуклеотидной последовательности генов HLA и выявления различий между разными аллелями этих генов. В настоящее время молекулярногенетические методы используются только для типирования генов HLA класса II. Анализ полиморфизма длин рестрикционных фрагментов В целом последовательность нуклеотидов во всех аллелях одного гена HLA класса II однотипна, уникальны лишь замены нуклеотидов в тех областях, которые отвечают за синтез вариабельных участков. Метод основан на способности бактериальных эндонуклеаз расщеплять ДНК в тех участках, в которых сосредоточены специфические для определенной эндонуклеазы последовательности нуклеотидов — сайты рестрикции. Сайты рестрикции для данной эндонуклеазы в разных аллелях одного гена располагаются на разном расстоянии друг от друга, поэтому длина рестрикционных фрагментов у разных аллелей разная. Применение эндонуклеаз позволило выявить полиморфизм длин рестрикционных фрагментов ДНК, подобный полиморфизму HLA, определяемому серологически. По длине фрагментов судят о присутствии тех или иных аллелей HLA у исследуемого. Если у донора и реципиента выявляются фрагменты одинаковой длины, считается, что они несут один и тот же аллель HLA. Определение специфических олигонуклеотидных последовательностей Аллели генов HLA иногда отличаются друг от друга лишь по одной паре нуклеотидов. Синтезированы одноцепочечные олигонуклеотидные зонды, состоящие из 19— 24 нуклеотидов, полностью комплементарные уникальным последовательностям каждого известного аллеля гена HLA. Таким образом, для определения неизвестного аллеля можно последовательно использовать серию зондов разной специфичности. ПЦР — метод, предназначенный для получения большого количества копий фрагментов ДНК с определенной нуклеотидной последовательностью. Полученные копии исследуют с помощью набора олигонуклеотидных зондов. Разрабатывается молекулярногенетическое типирование генов HLA класса I.
 3. Клеточные методы После распознавания чужеродного антигена начинается пролиферация Tлимфоцитов. Этот процесс можно воспроизвести in vitro в смешанной культуре лимфоцитов, состоящей из лимфоцитов донора и реципиента. Если донор и реципиент несут разные антигены HLA класса II, в смешанной культуре отмечается пролиферация. Смешанная культура лимфоцитов позволяет выявить различия по антигенам HLA, которые нельзя обнаружить серологическими методами, например различия по антигенам HLA-DP и HLA-DQ. Реакция клеточной цитотоксичности При совместном культивировании лимфоцитов реципиента (отвечающих клеток) и отличающихся от них по антигенам HLA класса II стимулирующих клеток донора среди отвечающих клеток появляются цитотоксические T-лимфоциты. Они способны разрушать клеткимишени, несущие антигены, которые присутствуют и на стимулирующих клетках. Изучение клеточной цитотоксичности в смешанной культуре лимфоцитов в ряде случаев позволяет предсказать, будет трансплантат стимулировать образование цитотоксических T-лимфоцитов или нет.
3. Клеточные методы После распознавания чужеродного антигена начинается пролиферация Tлимфоцитов. Этот процесс можно воспроизвести in vitro в смешанной культуре лимфоцитов, состоящей из лимфоцитов донора и реципиента. Если донор и реципиент несут разные антигены HLA класса II, в смешанной культуре отмечается пролиферация. Смешанная культура лимфоцитов позволяет выявить различия по антигенам HLA, которые нельзя обнаружить серологическими методами, например различия по антигенам HLA-DP и HLA-DQ. Реакция клеточной цитотоксичности При совместном культивировании лимфоцитов реципиента (отвечающих клеток) и отличающихся от них по антигенам HLA класса II стимулирующих клеток донора среди отвечающих клеток появляются цитотоксические T-лимфоциты. Они способны разрушать клеткимишени, несущие антигены, которые присутствуют и на стимулирующих клетках. Изучение клеточной цитотоксичности в смешанной культуре лимфоцитов в ряде случаев позволяет предсказать, будет трансплантат стимулировать образование цитотоксических T-лимфоцитов или нет.
 Выявление сенсибилизации реципиента антигенами HLA Определение антител к антигенам HLA Антитела к антигенам HLA появляются после контакта клеток иммунной системы реципиента с этими антигенами, например во время беременности. Присутствие в сыворотке реципиента (ребенка) антител к антигенам HLA донора (матери) служит противопоказанием к трансплантации органа, полученного от данного донора. Определение антител к антигенам HLA в сыворотке больного, которому планируется трансплантация органа, проводят при первичном обращении к врачу, а также во всех случаях, когда возможен контакт с антигенами HLA: после переливания компонентов крови, трансплантации органов или во время беременности. Для выявления антител к антигенам HLA используют 30— 60 образцов лимфоцитов, типированных по наиболее распространенным антигенам HLA. Исследование проводят с помощью лимфоцитотоксического теста. Результат выражают в виде коэффициента серопозитивности. Он представляет собой отношение числа образцов лимфоцитов, вызывающих положительную реакцию, к общему числу образцов в панели, выраженное в процентах. Коэффициент серопозитивности отражает риск сверхострого отторжения трансплантата, взятого от случайного донора.
Выявление сенсибилизации реципиента антигенами HLA Определение антител к антигенам HLA Антитела к антигенам HLA появляются после контакта клеток иммунной системы реципиента с этими антигенами, например во время беременности. Присутствие в сыворотке реципиента (ребенка) антител к антигенам HLA донора (матери) служит противопоказанием к трансплантации органа, полученного от данного донора. Определение антител к антигенам HLA в сыворотке больного, которому планируется трансплантация органа, проводят при первичном обращении к врачу, а также во всех случаях, когда возможен контакт с антигенами HLA: после переливания компонентов крови, трансплантации органов или во время беременности. Для выявления антител к антигенам HLA используют 30— 60 образцов лимфоцитов, типированных по наиболее распространенным антигенам HLA. Исследование проводят с помощью лимфоцитотоксического теста. Результат выражают в виде коэффициента серопозитивности. Он представляет собой отношение числа образцов лимфоцитов, вызывающих положительную реакцию, к общему числу образцов в панели, выраженное в процентах. Коэффициент серопозитивности отражает риск сверхострого отторжения трансплантата, взятого от случайного донора.
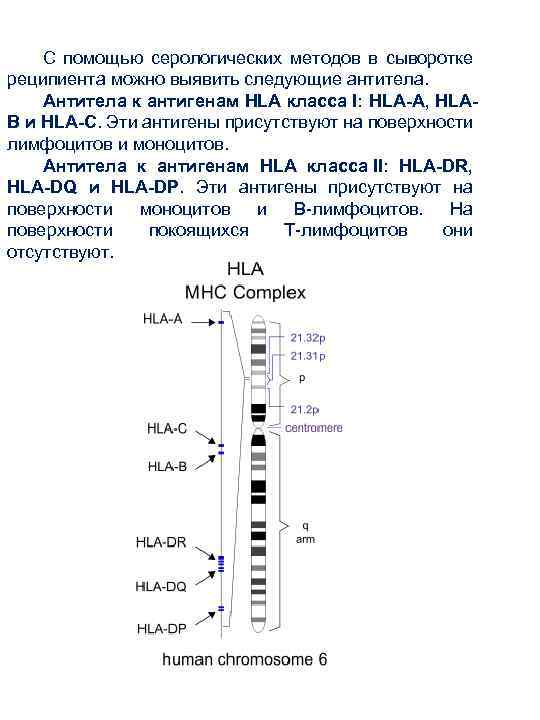 С помощью серологических методов в сыворотке реципиента можно выявить следующие антитела. Антитела к антигенам HLA класса I: HLA-A, HLAB и HLA-C. Эти антигены присутствуют на поверхности лимфоцитов и моноцитов. Антитела к антигенам HLA класса II: HLA-DR, HLA-DQ и HLA-DP. Эти антигены присутствуют на поверхности моноцитов и B-лимфоцитов. На поверхности покоящихся T-лимфоцитов они отсутствуют.
С помощью серологических методов в сыворотке реципиента можно выявить следующие антитела. Антитела к антигенам HLA класса I: HLA-A, HLAB и HLA-C. Эти антигены присутствуют на поверхности лимфоцитов и моноцитов. Антитела к антигенам HLA класса II: HLA-DR, HLA-DQ и HLA-DP. Эти антигены присутствуют на поверхности моноцитов и B-лимфоцитов. На поверхности покоящихся T-лимфоцитов они отсутствуют.
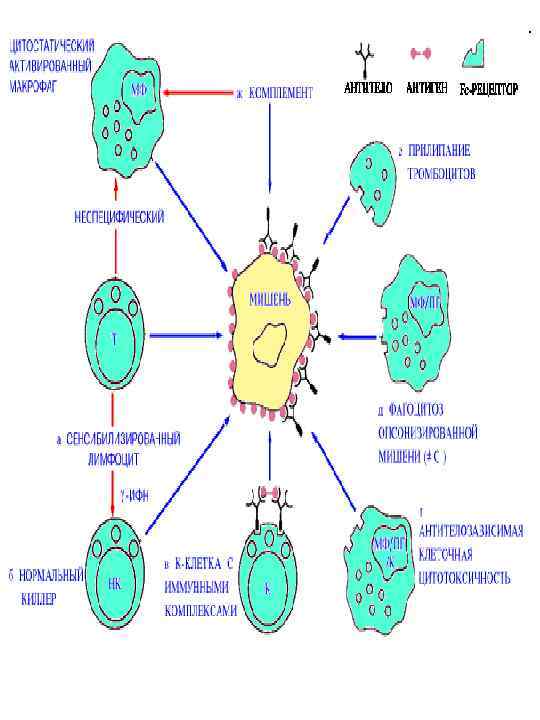
 Иммунология отторжения Существуют доказательства того, что отторжение трансплантата связано с действием Т-лимфоцитов, направленным непосредственно и специфически против антигенов донора. Это могут быть цитотоксические клетки (Т- хелперы CD 4 или Тсупрессоры CD 8) или клетки, опосредующие действие ДТН (относятся к классу Т-лимфоциты CD 4). Однако в ранних стадиях процесса отторжения в инфильтрате присутствует значительное число В-лимфоцитов, нольлимфоцитов, естественных клеток-киллеров (NK) и макрофагов; присутствуют также и клетки, способные опосредовать антителозависимую клеточноопосредуемую цитотоксичность (АЗКЦ). Многие из Влимфоцитов продуцируют иммуноглобулины. Спектры клеточного и гуморального ответов и повреждения трансплантата вариабельны и зависят от специфических генетических различий между донором и реципиентом и от степени предсенсибилизации. Чем больше степень предсенсибилизации, тем более вероятно, что будут обнаружены опосредуемые через антитела поражения сосудов. Ориентиром оценки реакции на аллотрансплантат, єфффективности лечения и прогнозирования служит биопсийное исследование трансплантата.
Иммунология отторжения Существуют доказательства того, что отторжение трансплантата связано с действием Т-лимфоцитов, направленным непосредственно и специфически против антигенов донора. Это могут быть цитотоксические клетки (Т- хелперы CD 4 или Тсупрессоры CD 8) или клетки, опосредующие действие ДТН (относятся к классу Т-лимфоциты CD 4). Однако в ранних стадиях процесса отторжения в инфильтрате присутствует значительное число В-лимфоцитов, нольлимфоцитов, естественных клеток-киллеров (NK) и макрофагов; присутствуют также и клетки, способные опосредовать антителозависимую клеточноопосредуемую цитотоксичность (АЗКЦ). Многие из Влимфоцитов продуцируют иммуноглобулины. Спектры клеточного и гуморального ответов и повреждения трансплантата вариабельны и зависят от специфических генетических различий между донором и реципиентом и от степени предсенсибилизации. Чем больше степень предсенсибилизации, тем более вероятно, что будут обнаружены опосредуемые через антитела поражения сосудов. Ориентиром оценки реакции на аллотрансплантат, єфффективности лечения и прогнозирования служит биопсийное исследование трансплантата.
 Иммуносупрессивную терапию проводят всем больным до и после трансплантации. Исключение составляют те случаи, когда донор и реципиент — однояйцовые близнецы. В случае, если между донором и реципиентом существуют различия в гистосовместимости, необходимо модифицировать или подавить иммунный ответ для того, чтобы дать возможность реципиенту принять трансплантат. Иммуносупрессивная терапия в общем подавляет все иммунные реакции, включая реакции на бактерии, грибы и даже на злокачественные опухоли. Современные подходы к иммуносупрессивной терапии предусматривают одновременное использование нескольких иммунодепрессантов и их назначение до и после трансплантации для профилактики и лечения отторжения трансплантата. В настоящее время в качестве иммунодепрессантов применяются кортикостероиды, азатиоприн, циклоспорин, монои поликлональные антитела. Эти препараты препятствуют активации иммунного ответа или блокируют эффекторные механизмы иммунитета.
Иммуносупрессивную терапию проводят всем больным до и после трансплантации. Исключение составляют те случаи, когда донор и реципиент — однояйцовые близнецы. В случае, если между донором и реципиентом существуют различия в гистосовместимости, необходимо модифицировать или подавить иммунный ответ для того, чтобы дать возможность реципиенту принять трансплантат. Иммуносупрессивная терапия в общем подавляет все иммунные реакции, включая реакции на бактерии, грибы и даже на злокачественные опухоли. Современные подходы к иммуносупрессивной терапии предусматривают одновременное использование нескольких иммунодепрессантов и их назначение до и после трансплантации для профилактики и лечения отторжения трансплантата. В настоящее время в качестве иммунодепрессантов применяются кортикостероиды, азатиоприн, циклоспорин, монои поликлональные антитела. Эти препараты препятствуют активации иммунного ответа или блокируют эффекторные механизмы иммунитета.
 Иммунологическая толерантность к трансплантату Идеальный способ, с помощью которого можно предупредить отторжение трансплантата, а также избежать иммуносупрессивной терапии, — индукция толерантности реципиента к антигенам донора. Теоретически иммунологическую толерантность можно вызвать следующими способами: 1) удалением всех клонов лимфоцитов, которые реагируют с антигенами донора; 2) активацией специфических T-супрессоров, угнетающих иммунный ответ на антигены донора; 3) индукцией синтеза антиидиотипических антител, подавляющих гуморальный иммунный ответ на антигены донора; 4) угнетением экспрессии антигенов HLA на клетках трансплантата. В настоящее время для индукции толерантности к антигенам донора перед трансплантацией применяют 1) переливание реципиенту цельной крови донора; 2) переливание лейкоцитарной массы донора и облучение лимфоидных органов реципиента (неспецифическая иммуносупрессия); 3) комбинацию этих методов с иммуносупрессивной терапией. Данные схемы лечения позволяют применять после трансплантации более щадящую иммуносупрессивную терапию.
Иммунологическая толерантность к трансплантату Идеальный способ, с помощью которого можно предупредить отторжение трансплантата, а также избежать иммуносупрессивной терапии, — индукция толерантности реципиента к антигенам донора. Теоретически иммунологическую толерантность можно вызвать следующими способами: 1) удалением всех клонов лимфоцитов, которые реагируют с антигенами донора; 2) активацией специфических T-супрессоров, угнетающих иммунный ответ на антигены донора; 3) индукцией синтеза антиидиотипических антител, подавляющих гуморальный иммунный ответ на антигены донора; 4) угнетением экспрессии антигенов HLA на клетках трансплантата. В настоящее время для индукции толерантности к антигенам донора перед трансплантацией применяют 1) переливание реципиенту цельной крови донора; 2) переливание лейкоцитарной массы донора и облучение лимфоидных органов реципиента (неспецифическая иммуносупрессия); 3) комбинацию этих методов с иммуносупрессивной терапией. Данные схемы лечения позволяют применять после трансплантации более щадящую иммуносупрессивную терапию.


