3 трансляция.ppt
- Количество слайдов: 57

Трансляция Переход от нуклеиновых кислот к белкам Генетическая информация, находящаяся в клетке в виде ДНК и воспроизводящаяся в клеточных поколениях путем редупликации ДНК, реализуется через биосинтез белка. n
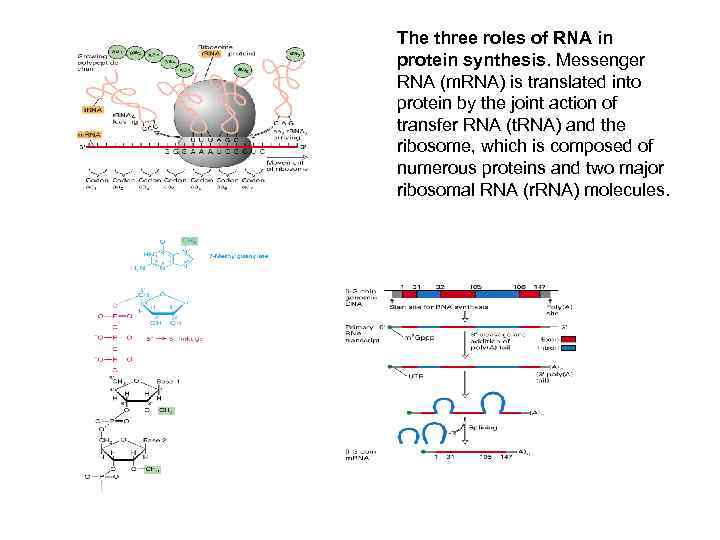
The three roles of RNA in protein synthesis. Messenger RNA (m. RNA) is translated into protein by the joint action of transfer RNA (t. RNA) and the ribosome, which is composed of numerous proteins and two major ribosomal RNA (r. RNA) molecules.
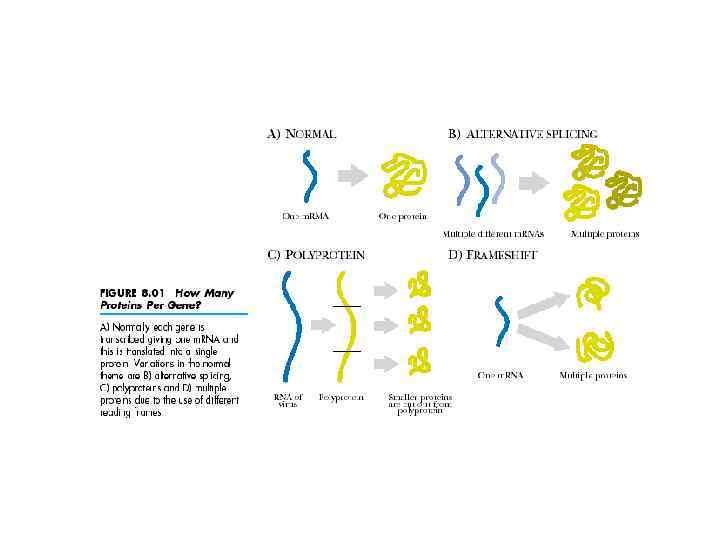

Предтрансляционный этап ГЕНЕТИЧЕСКИЙ КОД КАК СИСТЕМА
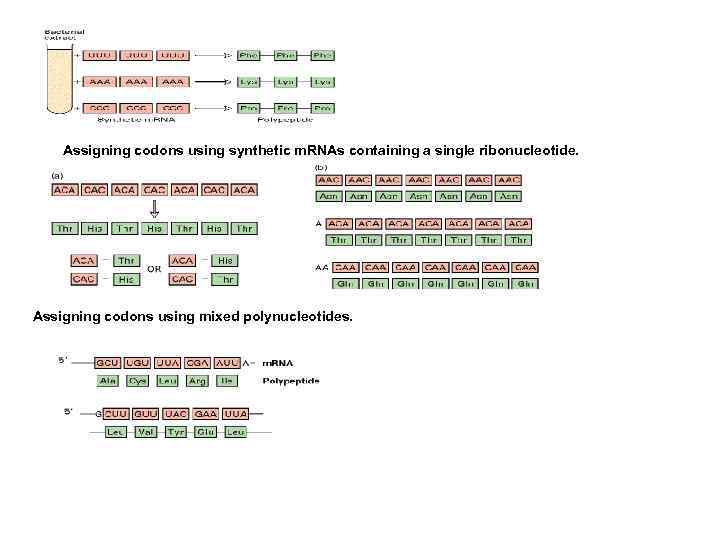
Assigning codons using synthetic m. RNAs containing a single ribonucleotide. Assigning codons using mixed polynucleotides.

Свойства генетического кода: 1. Все кодоны однозначны, то есть каждый кодирует единственную аминокислоту. Иначе говоря, в направлении кодон => аминокислота генетический код однозначен. 2. Обратное соответствие в направлении аминокислота => кодон неоднозначно, и это свойство называется вырожденностью. Отдельные аминокислоты кодируются группами (сериями) кодонов синонимов. 18 серий из 20 содержат от двух до шести кодонов, две серии (Меt и Тrр) не вырождены, содержат по одному кодону. Средняя вырожденность генетического кода приблизительно три кодона на серию.

Свойства генетического кода: 3. Генетический код содержит также знаки пунктуации (начала и конца) трансляции. – – Кодоны AUG, UUG и GUG у прокариот помимо кодирования аминокислот кодируют также инициацию трансляции. Однако однозначность кодирования при этом не нарушается, так как инициирующие знаки локализованы в определенном окружении (контексте), способном образовывать самокомплементарные "шпильки". Три "вакантных" триплета— UAA (ochre), UAG (amber) и UGA (ораl) — не кодируют аминокислот, а выполняют роль терминальных знаков трансляции (стоп кодонов, нонсенс кодонов или терминальных нонсенсов). В норме ими заканчиваются все цистроны, то есть транслируемые гены, единицы трансляции. Мутационное возникновение нонсенсов внутри гена приводит к преждевременной терминации трансляции

Неоднозначное спаривание: • Однозначность кода в направлении кодон => аминокислота обеспечивается строгой специфичностью АА-т. РНК-синтетаз. Каждая АА-т. РНК-синтетаз узнает единственную аминокислоту, поэтому неоднозначность исключена или маловероятна. • В основе систематической вырожденности лежат правила неоднозначности спаривания кодон— антикодон, установленные Ф. Криком. Один антикодон может узнавать один, два или три кодона, различающиеся по третьей позиции. • Согласно правилам неоднозначного спаривания, систематическая вырожденность в парах кодонов обеспечивается отдельными фракциями т-РНК, имеющими U, G или I (инозин) в трех позициях антикодонов. Всего генетический код требует не менее 32 фракций т-РНК.
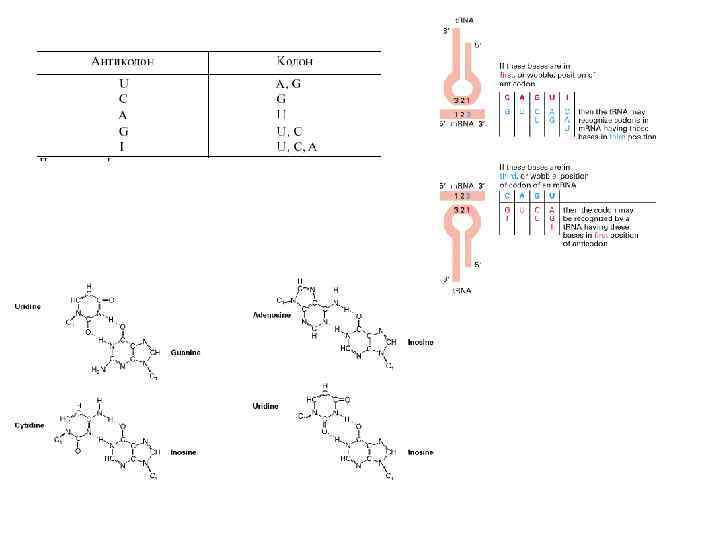
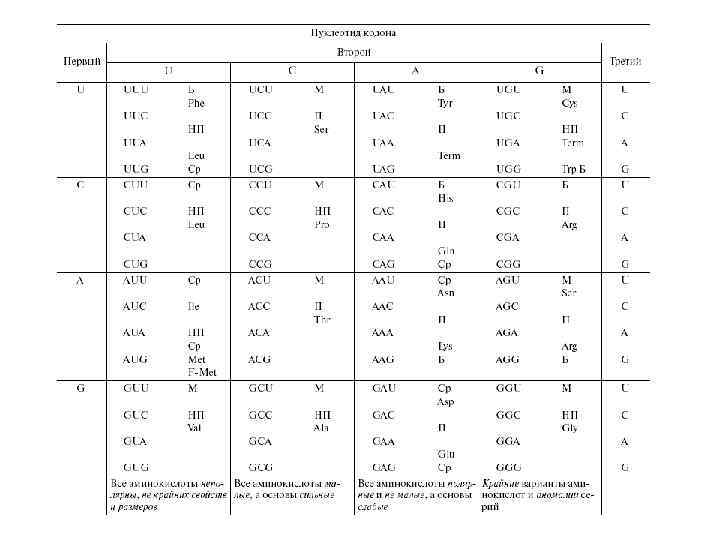

Система генетического кода: • Анализ таблицы генетического кода как целого позволяет выявить удивительные свойства его регулярности и симметрии. • Обозначим позиции нуклеотидов в кодонах (5'— 1— 2— 3— 3') через х у z, где х - приставка, у - корень, z окончание, а ху — основа кодона. • Эти термины отражают сходные понятия лингвистики. – Корни слов определяют их смысл. Все мутации, затрагивающие корень (у) кодона, также изменяют кодовую серию, то есть нарушают смысл кодона. – Приставки слов тоже участвуют в определении смысла, хотя и не так жестко, а многие их изменения меняют смысл слов. Замены в приставках (х) кодонов чаще всего изменяют их смысл, но иногда являются синонимическими. – Окончания слов обычно участвуют в словоизменении, то есть в синонимических преобразованиях. Аналогично 70% замен в окончаниях (z) кодонов синонимические. – Наконец, приставка и корень слова образуют его основу, несущую полную или доминирующую смысловую нагрузку. Основа кодона (ху) тоже играет ключевую роль в особенностях генетического кода.

Групповые свойства кода: • • • Легко заметить, что столбцы генетического кода отвечающие определенным корням кодонов, имект некоторые групповые свойства. Третий столбец (корень А) содержит полярные аминокислоты немалые по размеру, а все основы кодонов слабые. Второй столбец (корень С) содержит аминокислоты, малые по размеру, а все основы кодонов сильные. Первый столбец (корень U) включает неполярные аминокислоты разных (но не крайних) размеров, а свойства кодонов неоднозначны. Четвертый столбец (корень G) содержит все крайние и аномальные варианты аминокислот и кодовых серий: самую реактивную аминокислоту (Суs), самую большую и плоскую (Тrр), самую большую и корявую (Агg), самую маленькую (Glу), часть единственной несвязной серии (Sег) и неоднозначный терминальный нонсенс (UAG), который в ряде случаев кодирует 21 ю аминокислоту селеноцистеин (Sес). Таким образом, если групповые свойства корней (и столбцов) отвечают каким то общим правилам их возникновения, то четвертый столбец скорее напоминает свалку всего, что не попало в первые три столбца по групповым правилам их формирования.

Figure 5 -C-2. Illustration of the frameshift. m. RNA(a) and m. RNA(b) differ by only one nucleotide: m. RNA(b) has an additional nucleotide "G" at the third position in this figure. Note that the translated amino acids are entirely different after the insertion point.

Предтрансляционный этап Строение и функции т. РНК
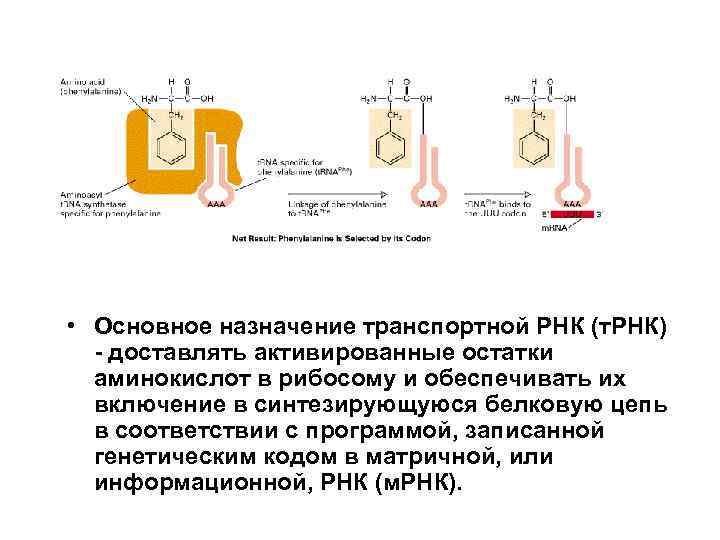
• Основное назначение транспортной РНК (т. РНК) - доставлять активированные остатки аминокислот в рибосому и обеспечивать их включение в синтезирующуюся белковую цепь в соответствии с программой, записанной генетическим кодом в матричной, или информационной, РНК (м. РНК).

Общие сведения: • Впервые нуклеотидная последовательность молекулы т. РНК — дрожжевой аланиновой т. РНК, была расшифрована в 1965 году в лаборатории Р. Холли. • С тех пор были опубликованы данные о нуклеотидной последовательности (называемой первичной структурой) более чем 1700 видов различных т. РНК из прокариотических и эукариотических организмов. • Все т. РНК имеют общие черты как в их первичной структуре, так и в способе складывания полинуклеотидной цепи во вторичную структуру за счет взаимодействий между основаниями нуклеотидных остатков. • Помимо цитоплазматических т. РНК, кодируемых ядерной ДНК, в эукариотических клетках имеются особые виды т. РНК, кодируемые автономными геномами митохондрий и хлоропластов.

Первичная структура т. РНК: • т. РНК - относительно небольшие молекулы, длина их цепей варьирует от 74 до 95 нуклеотидных остатков. • Все т. РНК имеют одинаковый З'-конец, построенный из двух остатков цитозина и одного — аденозина (ССА-конец). • Именно З'-концевой аденозин связывается с аминокислотным остатком при образовании аминоацил-т. РНК. • ССА-конец присоединяется ко многим т. РНК с помощью специального фермента. В других случаях он считывается с кодирующего данную т. РНК гена. • Нуклеотидный триплет, комплементарный кодону для аминокислоты (антикодон), находится приблизительно в середине цепи т. РНК. • В отдельных положениях последовательности практически у всех видов т. РНК встречаются одни и те же (консервативные) нуклеотидные остатки. В некоторых положениях могут находиться или только пуриновые, или только пиримидиновые основания (их называют полуконсервативными остатками).
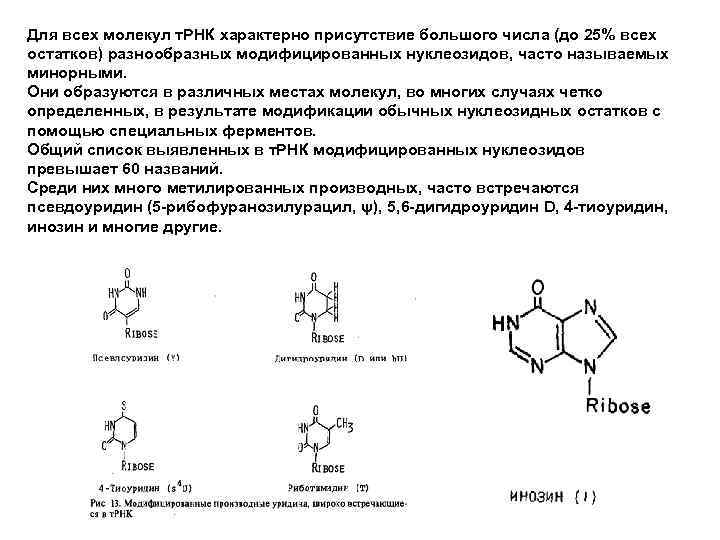
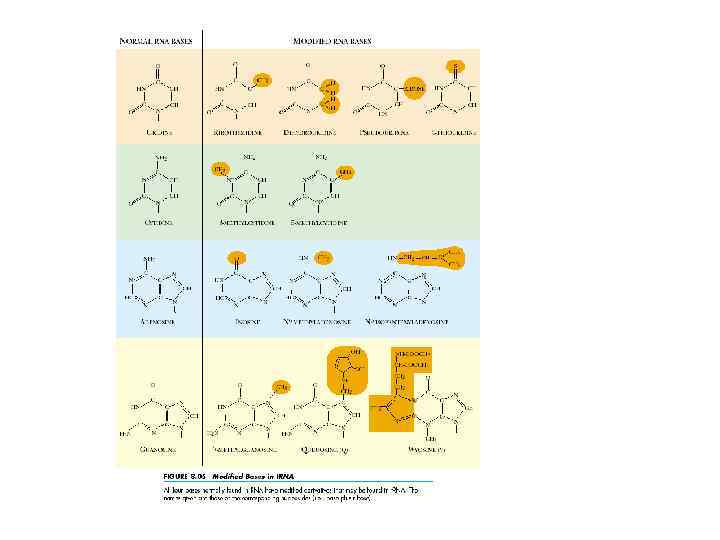
Для всех молекул т. РНК характерно присутствие большого числа (до 25% всех остатков) разнообразных модифицированных нуклеозидов, часто называемых минорными. Они образуются в различных местах молекул, во многих случаях четко определенных, в результате модификации обычных нуклеозидных остатков с помощью специальных ферментов. Общий список выявленных в т. РНК модифицированных нуклеозидов превышает 60 названий. Среди них много метилированных производных, часто встречаются псевдоуридин (5 -рибофуранозилурацил, ψ), 5, 6 -дигидроуридин D, 4 -тиоуридин, инозин и многие другие.

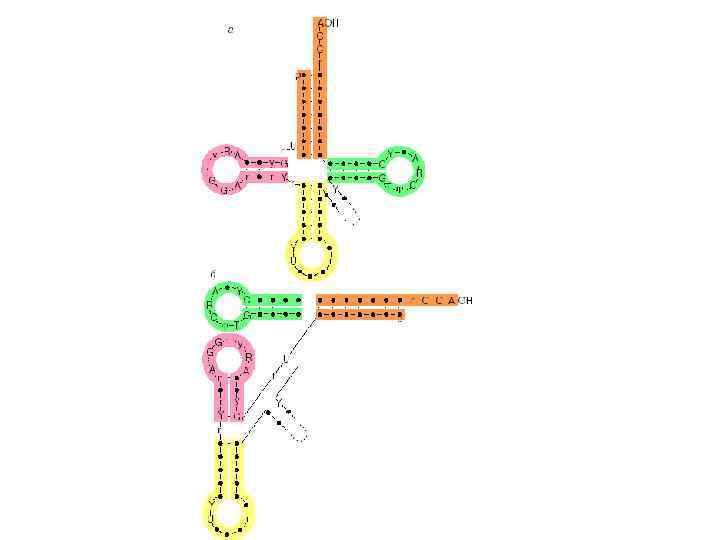
Вторичная структура т. РНК • • Анализ нуклеотидной последовательности уже первой расшифрованной дрожжевой аланиновой т. РНК выявил возможность складывания цепи во вторичную структуру за счет взаимокомплементарности участков цепи. Три фрагмента цепи оказываются комплементарными при складывании их на себя, образуя шпилькообразные структуры. Кроме того, 5' конец комплементарен участку, близкому к З' концу цепи, при их антипараллельном расположении; они формируют так называемый акцепторный стебель. В результате образуется структура, характеризующаяся наличием четырех стеблей и трех петель, которая получила название "клеверного листа". Стебель с петлей формируют ветвь. Слева и справа от антикодоновой ветви расположены D и Т ветви, соответственно названные так из за присутствия в их петлях необычных консервативных нуклеозидов дигидроуридина (D) и тимидина (Т). Нуклеотидные последовательности всех изученных т. РНК могут быть сложены в аналогичные структуры. В дополнение к трем петлям клеверного листа в структуре т. РН К выделяют также дополнительную, или вариабельную, петлю (V петлю). Ее размеры резко различаются у разных т. РНК, варьируя от 4 до 21 нуклеотида.
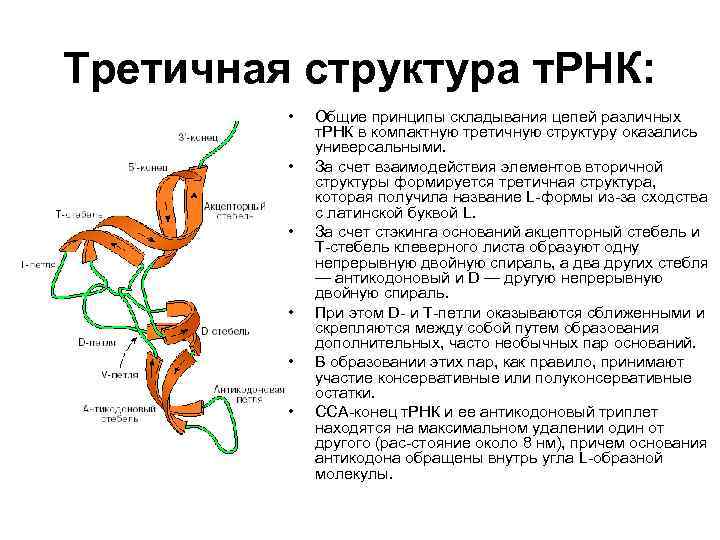
Третичная структура т. РНК: • • • Общие принципы складывания цепей различных т. РНК в компактную третичную структуру оказались универсальными. За счет взаимодействия элементов вторичной структуры формируется третичная структура, которая получила название L формы из за сходства с латинской буквой L. За счет стэкинга оснований акцепторный стебель и Т стебель клеверного листа образуют одну непрерывную двойную спираль, а два других стебля — антикодоновый и D — другую непрерывную двойную спираль. При этом D и Т петли оказываются сближенными и скрепляются между собой путем образования дополнительных, часто необычных пар оснований. В образовании этих пар, как правило, принимают участие консервативные или полуконсервативные остатки. ССА конец т. РНК и ее антикодоновый триплет находятся на максимальном удалении один от другого (рас стояние около 8 нм), причем основания антикодона обращены внутрь угла L образной молекулы.

Аминоацил т. РНК синтетазы: • Как уже указывалось, для каждой из 20 аминокислот в клетках есть специальный фермент, осуществляющий синтез соответствующей аминоацил т. РНК (общее название — аминоацил т. РНК синтетазы, для краткости будем называть их синтетазами). • Все ферменты этой группы катализируют реакции аминоацилирования т. РНК по принципиально сходному механизму. • Реакция сопряжена с расщеплением аденозин 5' трифосфата (АТР) и протекает в две стадии.
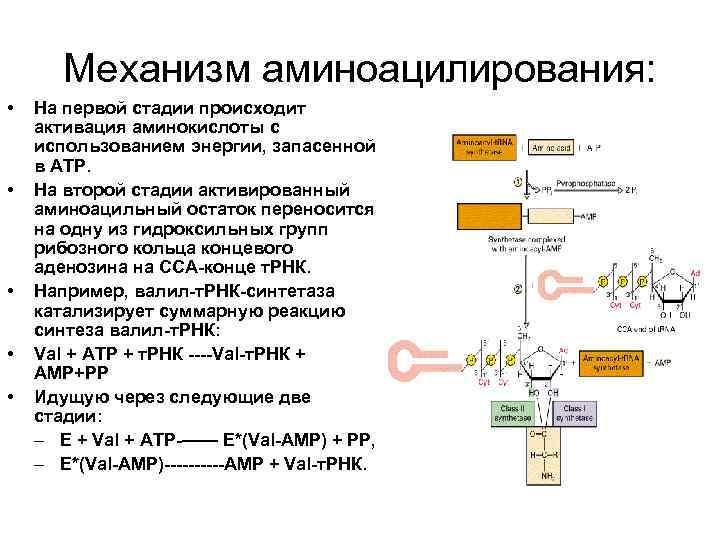
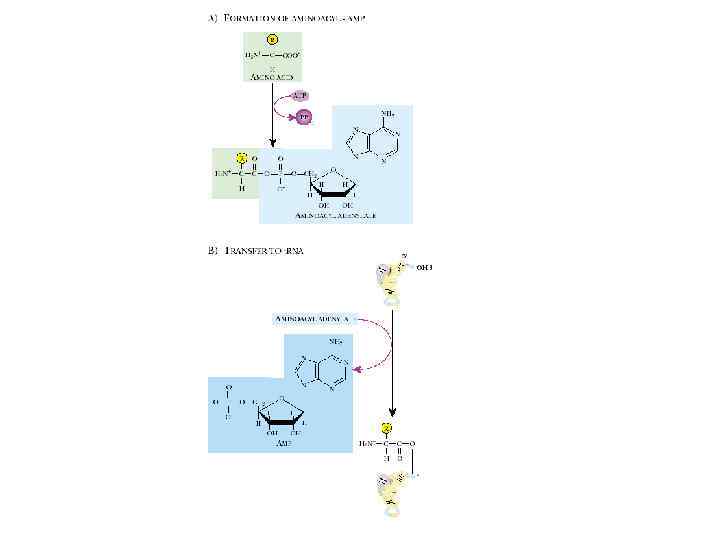
Механизм аминоацилирования: • • • На первой стадии происходит активация аминокислоты с использованием энергии, запасенной в АТР. На второй стадии активированный аминоацильный остаток переносится на одну из гидроксильных групп рибозного кольца концевого аденозина на ССА-конце т. РНК. Например, валил-т. РНК-синтетаза катализирует суммарную реакцию синтеза валил-т. РНК: Val + ATP + т. РНК ----Val-т. РНК + АМР+РР Идущую через следующие две стадии: – Е + Val + АТР-—— Е*(Val-АМР) + РР, – Е*(Val-АМР)-----АМР + Val-т. РНК.
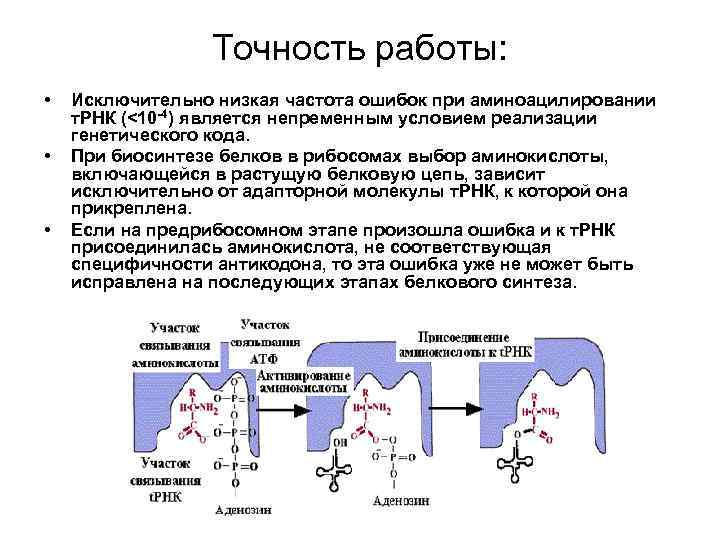
Точность работы: • • • Исключительно низкая частота ошибок при аминоацилировании т. РНК (<10 -4) является непременным условием реализации генетического кода. При биосинтезе белков в рибосомах выбор аминокислоты, включающейся в растущую белковую цепь, зависит исключительно от адапторной молекулы т. РНК, к которой она прикреплена. Если на предрибосомном этапе произошла ошибка и к т. РНК присоединилась аминокислота, не соответствующая специфичности антикодона, то эта ошибка уже не может быть исправлена на последующих этапах белкового синтеза.

Основы узнавания т. РНК аминоацил-т. РНК-синтетазами: • • Набор узнавания, естественно разный для разных пар т. РНК синтетаза, включает нуклеотиды, занимающие одни и те же положения в структуре большинства т. РНК. Это следующие участки т. РНК: – 1. Антикодон (остатки 34— 36). Участие антикодона, определяющего на рибосоме включение аминокислоты в растущую цепь белка, еще и в отборе этой аминокислоты на стадии реакции аминоацилирования т. РНК, предполагалось еще в 60 -е годы исходя из уникальности этого элемента в структуре молекулы. – 2. Нуклеотид 73, предшествующий ССА-концу. Присутствие в этом положении того или другого пуринового нуклеотида (А или G) коррелирует с типом аминокислот, присоединяемых к т. РНК. Если в этом положении находится А, то т. РНК акцептирует гидрофобные аминокислоты, а если G — то полярные. – 3. Первые три пары нуклеотидов акцепторного стебля (1 -72, 2— 71, 3 -70). В разных случаях в узнавании синтетазой может вовлекаться от одной до трех пар нуклеотидов акцепторного стебля.

Отбор аминокислот: • Аминокислоты построены из специфического радикала, аминогруппы и карбоксильной группы. • Вклад различных фрагментов молекулы аминокислоты исследовали с помощью неприродных синтетических аналогов аминокислот, в которых были изменены специфический радикал, аминогруппа или карбоксильная группа. • Было показано для различных аминоацил-т. РНК-синтетаз, что необходимым элементом узнавания всех аминокислот является аминогруппа. Модификация этой группы приводит к резкому падению сродства аминокислоты к ферменту. • Как принято считать, карбоксильная группа играет меньшую роль на стадии первичного связывания аминокислоты, однако безусловно важна на последующих каталитических этапах реакции аминоацилирования. • Специфическое распознавание аминокислот аминоацилт. РНК-синтетазами осуществляется за счет взаимодействий со специфическими радикалами аминокислот.

Аминоацил т. РНК синтетазы: • Несмотря на то что эти белки катализируют одну реакцию, они оказались чрезвычайно разнообразными по размеру, субъединичному строению и последовательности аминокислот. • Например, молекулярные массы АРСаз кишечной палочки варьируют от 51 000 до 384 000, при этом часть ферментов функционирует в виде мономеров, часть — в виде димеров, встречаются также и тетрамеры. • Оказалось, что между всеми АРСазами действительно нет сходства, но их можно разделить на два класса и внутри каждого из классов обнаруживаются характерные последовательности аминокислот (так называемые мотивы) и сходные элементы третичной структуры.
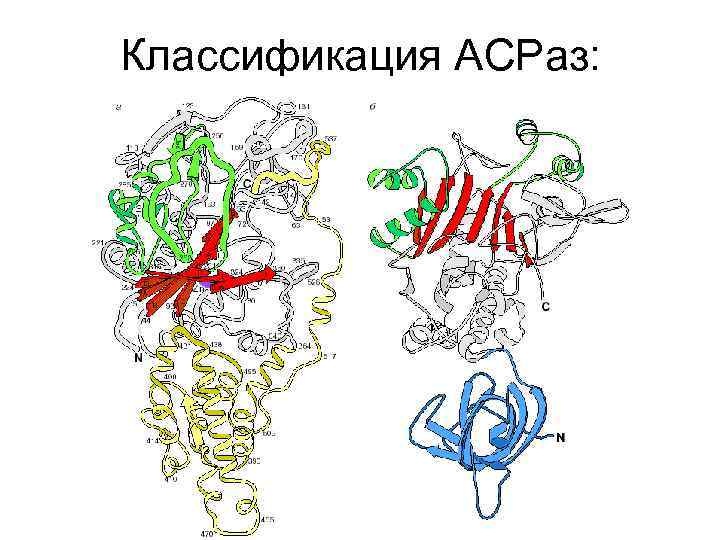
Классификация АСРаз:

ГИПОТЕЗЫ О ПРОИСХОЖДЕНИИ АРСаз: • Оказалось, что N концевой участок аланиновой АРСазы длиной 368 аминокислот способен синтезировать аминоациладенилат; фрагмент длиной 385 аминокислот связывает, но не аминоацилирует т. РНК, а фрагмент длиной в 461 аминокислоту успешно аминоацилирует не только т. РНК, но и мини и микроспирали. • При этом урезанный фермент, представляющий собой собственно центральный каталитический домен АРСазы аминоацилирует т. РНК хуже, чем полный фермент, а аминоацилирование мини спиралей осуществляется с одинаковой эффектив ностью как целой АРСазой, так и ее. N концевым доменом.
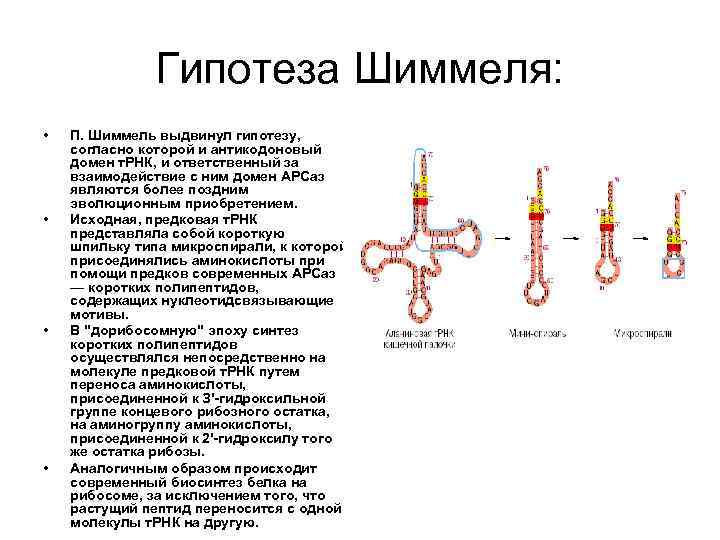
Гипотеза Шиммеля: • • П. Шиммель выдвинул гипотезу, согласно которой и антикодоновый домен т. РНК, и ответственный за взаимодействие с ним домен АРСаз являются более поздним эволюционным приобретением. Исходная, предковая т. РНК представляла собой короткую шпильку типа микроспирали, к которой присоединялись аминокислоты при помощи предков современных АРСаз — коротких полипептидов, содержащих нуклеотидсвязывающие мотивы. В "дорибосомную" эпоху синтез коротких полипептидов осуществлялся непосредственно на молекуле предковой т. РНК путем переноса аминокислоты, присоединенной к З'-гидроксильной группе концевого рибозного остатка, на аминогруппу аминокислоты, присоединенной к 2'-гидроксилу того же остатка рибозы. Аналогичным образом происходит современный биосинтез белка на рибосоме, за исключением того, что растущий пептид переносится с одной молекулы т. РНК на другую.

Гипотеза Шиммеля: • Для обеспечения такого древнего синтеза пептидов необходимы были по крайней мере два фермента, способные присоединять аминокислоты к 2'- и к З'-ОН рибозы, поскольку для этих реакций требуется совершенно различная пространственная организация субстратов в активном центре. • Эти ферменты и стали родоначальниками двух классов современных АРСаз. • В дальнейшем белоксинтезирующий аппарат стал более сложным, для хранения информации о большом количестве разнообразных белков возник генетический код, и для обеспечения запрограммированного синтеза белка на РНК-матрице к предковым т. РНК присоединился антикодоновый домен, а к АРСазам - дополнительные модули, позволяющие узнавать антикодон т. РНК и таким образом повысить специфичность и точность аминоацилирования.

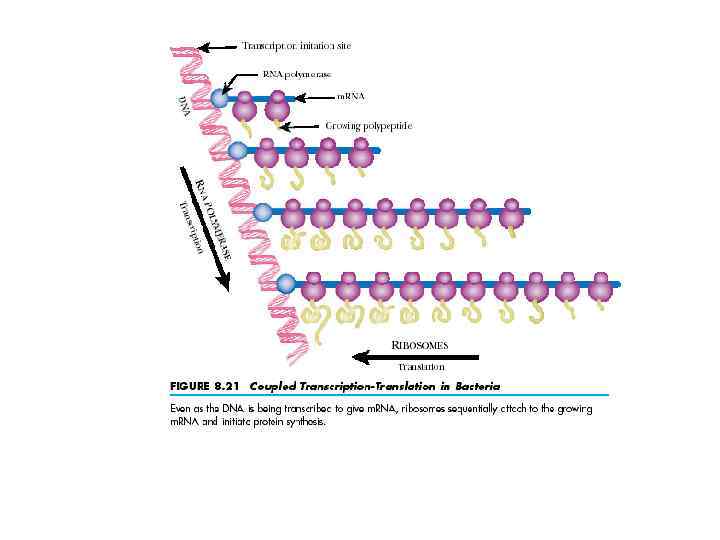
Синтез белка: общие сведения: • Процесс создания химической структуры белка (синтез полипептидной цепи) и в значительной мере ее физическое сворачивание в функционально активную белковую глобулу осуществляются рибосомой. • Количество рибосом в клетке сильно варьирует — от тысяч до десятков тысяч на клетку — в зависимости от интенсивности белкового синтеза в данном типе клеток. • Каждая рибосома полностью прочитывает одну молекулу м. РНК и в соответствии с ее программой синтезирует одну молекулу белка, после чего может быть запрограммирована другой молекулой м. РНК и произвести другую молекулу белка и т. д. • Обычно одна молекула м. РНК читается сразу несколькими рибосомами, двигающимися вдоль м. РНК друг за другом и, таким образом, независимо синтезирующими идентичные молекулы белка, но с соответствующим отставанием. Такой динамический комплекс одной м. РНК с несколькими рибосомами называется полирибосомой.
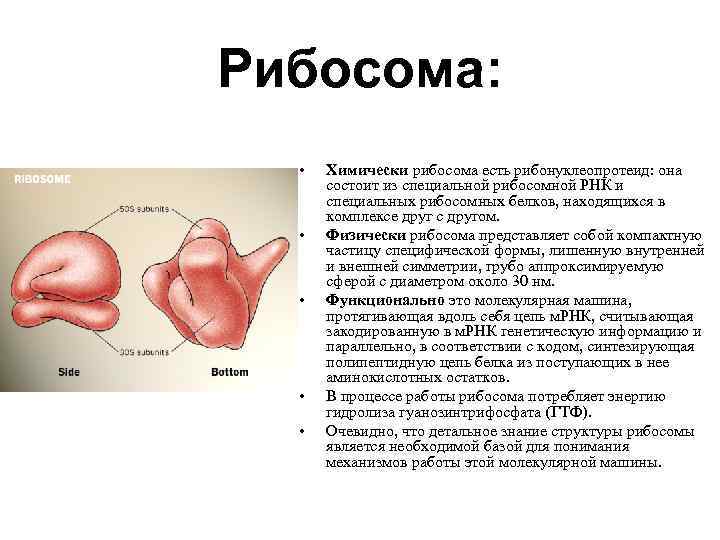
Рибосома: • • • Химически рибосома есть рибонуклеопротеид: она состоит из специальной рибосомной РНК и специальных рибосомных белков, находящихся в комплексе друг с другом. Физически рибосома представляет собой компактную частицу специфической формы, лишенную внутренней и внешней симметрии, грубо аппроксимируемую сферой с диаметром около 30 нм. Функционально это молекулярная машина, протягивающая вдоль себя цепь м. РНК, считывающая закодированную в м. РНК генетическую информацию и параллельно, в соответствии с кодом, синтезирующая полипептидную цепь белка из поступающих в нее аминокислотных остатков. В процессе работы рибосома потребляет энергию гидролиза гуанозинтрифосфата (ГТФ). Очевидно, что детальное знание структуры рибосомы является необходимой базой для понимания механизмов работы этой молекулярной машины.

ПРИНЦИП № 1: ДВЕ НЕРАВНЫЕ СУБЧАСТИЦЫ • Электронно-микроскопические изображения рибосом ясно показывают, что эти округлые частицы подразделяются на две неравные части. • Действительно, если в среде, окружающей рибосомы, понизить концентрацию ионов магния или каким-либо еще образом увеличить электростатическое отталкивание фосфатных групп рибосомной РНК, то рибосомная частица диссоциирует на две неравные субчастицы с соотношением их масс около 2: 1. • Полные рибосомные частицы и их субчастицы принято обозначать в соответствии с их коэффициентами седиментации (скоростями осаждения) в ультрацентрифуге, выражаемыми в единицах Сведберга (S). • Бактериальная рибосома с молекулярной массой около 3 • 106 имеет коэффициент седиментации 70 S и обозначается как 70 S-частица, а несколько более крупная рибосома эукариотических организмов предстает как 80 S-частица.
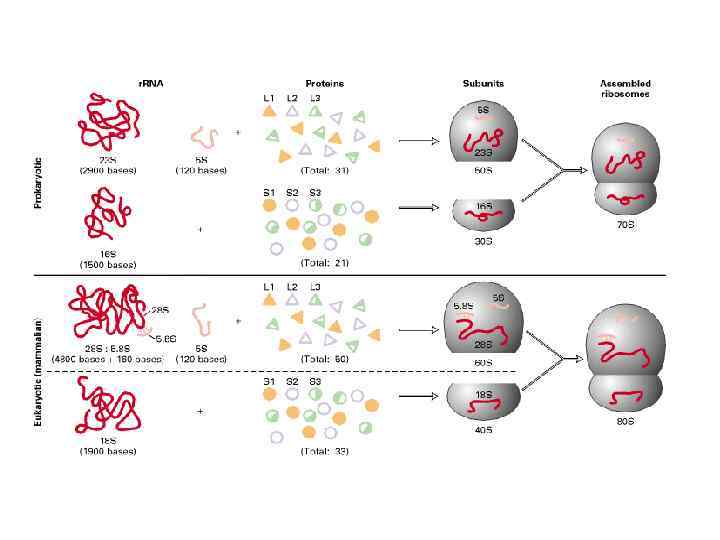
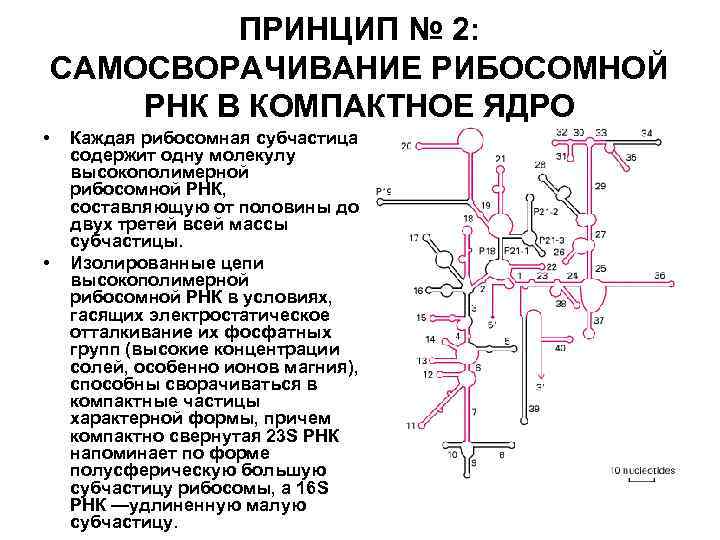
ПРИНЦИП № 2: САМОСВОРАЧИВАНИЕ РИБОСОМНОЙ РНК В КОМПАКТНОЕ ЯДРО • • Каждая рибосомная субчастица содержит одну молекулу высокополимерной рибосомной РНК, составляющую от половины до двух третей всей массы субчастицы. Изолированные цепи высокополимерной рибосомной РНК в условиях, гасящих электростатическое отталкивание их фосфатных групп (высокие концентрации солей, особенно ионов магния), способны сворачиваться в компактные частицы характерной формы, причем компактно свернутая 23 S РНК напоминает по форме полусферическую большую субчастицу рибосомы, а 16 S РНК —удлиненную малую субчастицу.

ПРИНЦИП № 3: СБОРКА РАЗНООБРАЗНЫХ БЕЛКОВ НА РНК • • • Каждая рибосомная субчастица содержит много молекул рибосомных белков, и все они разные. Многочисленные рибосомные белки могут играть двоякую роль в современной рибосоме. С одной стороны, они могут непосредственно участвовать в функциях связывания субстратов и каталитических функциях рибосомы, локализуясь в соответствующих функциональных центрах и обеспечивая их своими активными группами. С другой — рибосомные белки могут служить стабилизаторами или модификаторами определенных локальных структур рибосомной РНК и таким образом поддерживать их в функционально активном состоянии или способствовать их переключениям из одного состояния в другое. В частности, в отношении главной каталитической функции рибосомы — ее пептидил-трансферазной активности, ответственной за образование пептидных связей, имеются все основания полагать, что эта активность обеспечивается локальной структурой рибосомной РНК большой субчастицы, но некоторые рибосомные белки оказываются необходимыми для поддержания (стабилизации) этой структуры.
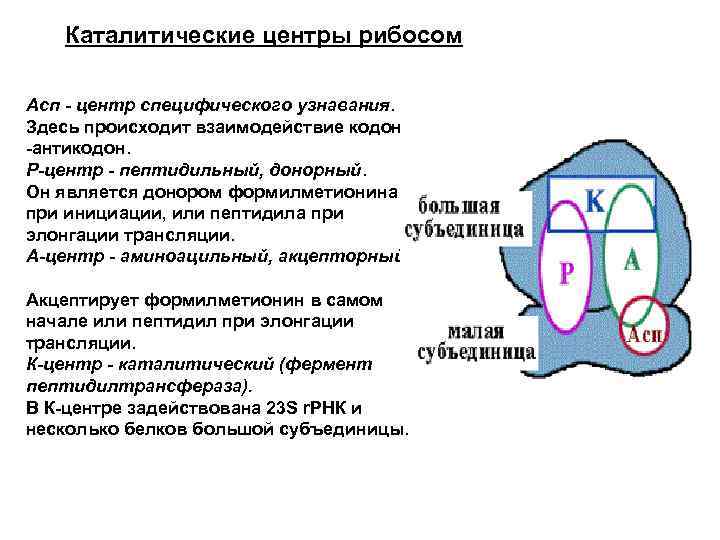
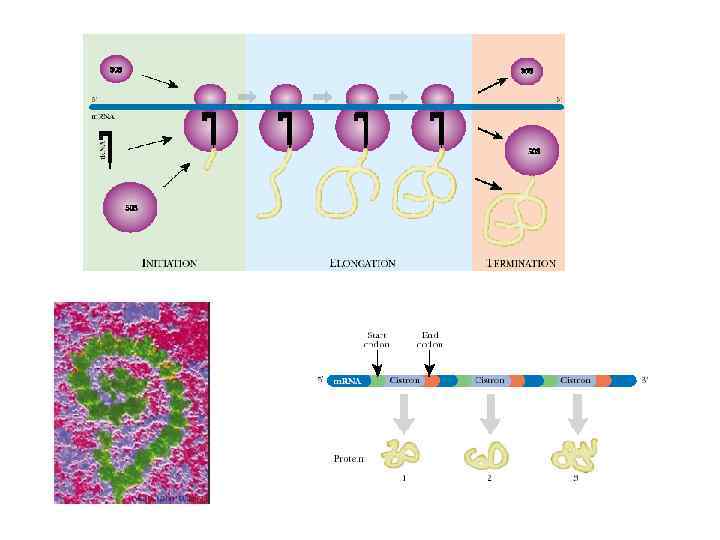
Каталитические центры рибосом Асп - центр специфического узнавания. Здесь происходит взаимодействие кодон -антикодон. Р-центр - пептидильный, донорный. Он является донором формилметионина при инициации, или пептидила при элонгации трансляции. А-центр - аминоацильный, акцепторный. Акцептирует формилметионин в самом начале или пептидил при элонгации трансляции. К-центр - каталитический (фермент пептидилтрансфераза). В К-центре задействована 23 S r. РНК и несколько белков большой субъединицы.

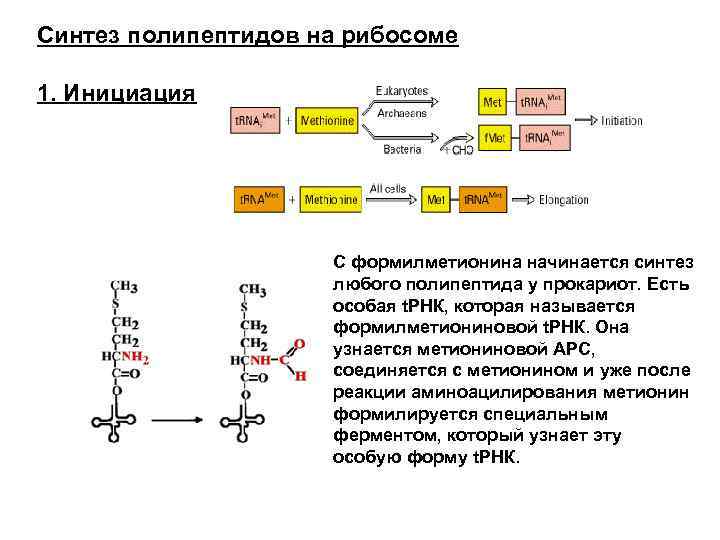
Синтез полипептидов на рибосоме 1. Инициация С формилметионина начинается синтез любого полипептида у прокариот. Есть особая t. РНК, которая называется формилметиониновой t. РНК. Она узнается метиониновой АРС, соединяется с метионином и уже после реакции аминоацилирования метионин формилируется специальным ферментом, который узнает эту особую форму t. РНК.
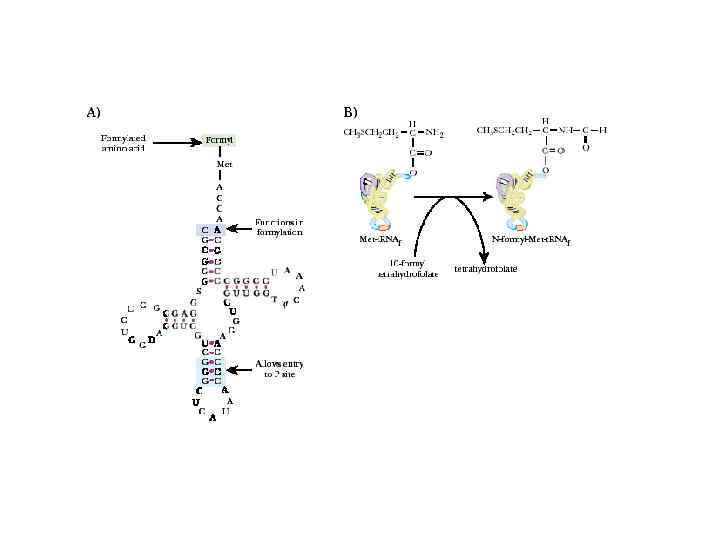
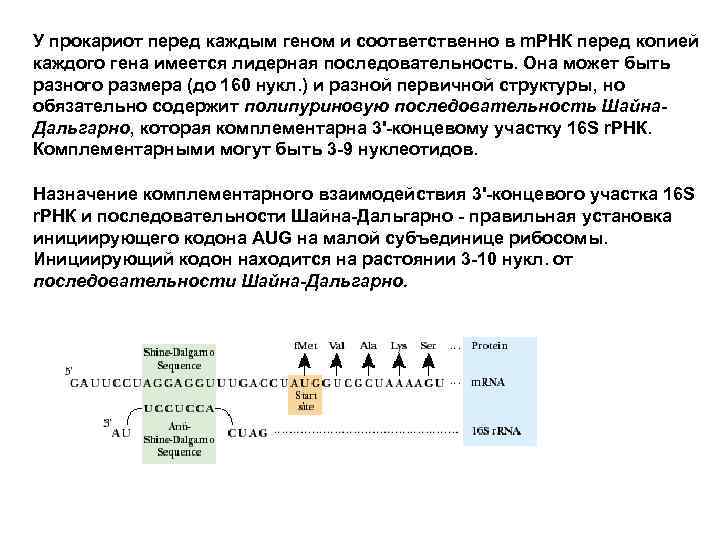
У прокариот перед каждым геном и соответственно в m. РНК перед копией каждого гена имеется лидерная последовательность. Она может быть разного размера (до 160 нукл. ) и разной первичной структуры, но обязательно содержит полипуриновую последовательность Шайна. Дальгарно, которая комплементарна 3'-концевому участку 16 S r. РНК. Комплементарными могут быть 3 -9 нуклеотидов. Назначение комплементарного взаимодействия 3'-концевого участка 16 S r. РНК и последовательности Шайна-Дальгарно - правильная установка инициирующего кодона AUG на малой субъединице рибосомы. Инициирующий кодон находится на растоянии 3 -10 нукл. от последовательности Шайна-Дальгарно.
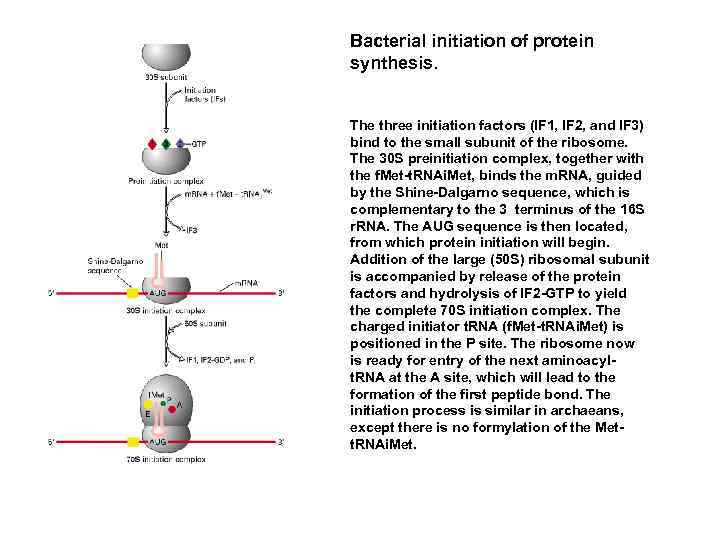
Bacterial initiation of protein synthesis. The three initiation factors (IF 1, IF 2, and IF 3) bind to the small subunit of the ribosome. The 30 S preinitiation complex, together with the f. Met-t. RNAi. Met, binds the m. RNA, guided by the Shine-Dalgarno sequence, which is complementary to the 3 terminus of the 16 S r. RNA. The AUG sequence is then located, from which protein initiation will begin. Addition of the large (50 S) ribosomal subunit is accompanied by release of the protein factors and hydrolysis of IF 2 -GTP to yield the complete 70 S initiation complex. The charged initiator t. RNA (f. Met-t. RNAi. Met) is positioned in the P site. The ribosome now is ready for entry of the next aminoacylt. RNA at the A site, which will lead to the formation of the first peptide bond. The initiation process is similar in archaeans, except there is no formylation of the Mett. RNAi. Met.
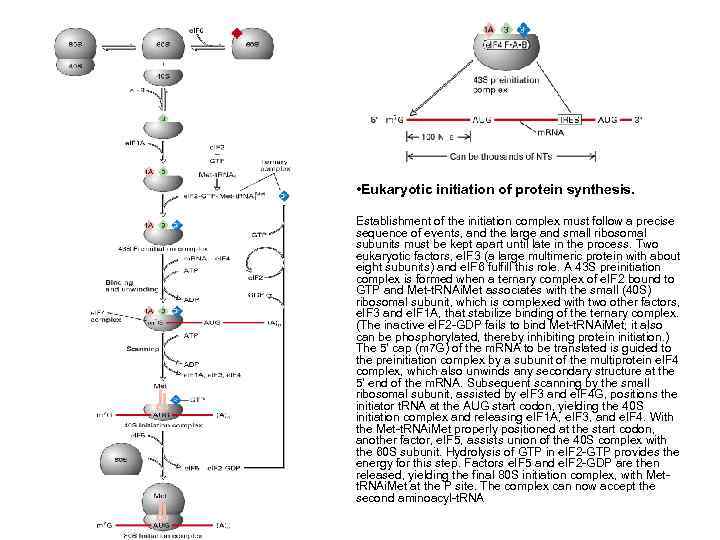
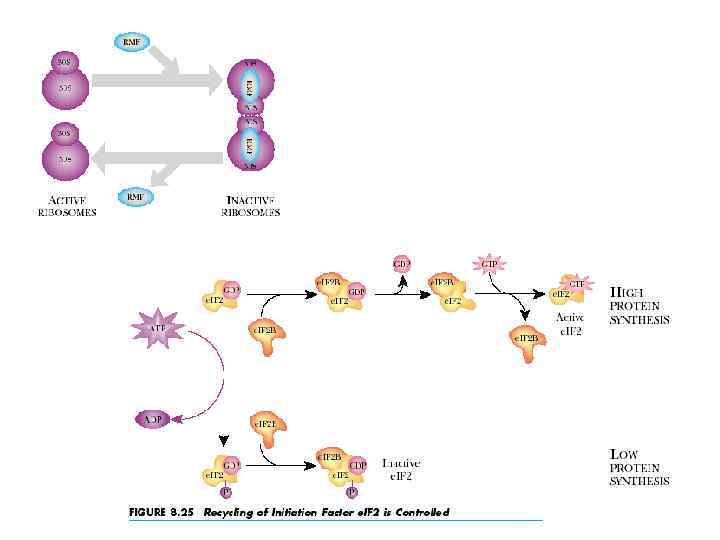
• Eukaryotic initiation of protein synthesis. Establishment of the initiation complex must follow a precise sequence of events, and the large and small ribosomal subunits must be kept apart until late in the process. Two eukaryotic factors, e. IF 3 (a large multimeric protein with about eight subunits) and e. IF 6 fulfill this role. A 43 S preinitiation complex is formed when a ternary complex of e. IF 2 bound to GTP and Met t. RNAi. Met associates with the small (40 S) ribosomal subunit, which is complexed with two other factors, e. IF 3 and e. IF 1 A, that stabilize binding of the ternary complex. (The inactive e. IF 2 GDP fails to bind Met t. RNAi. Met; it also can be phosphorylated, thereby inhibiting protein initiation. ) The 5' cap (m 7 G) of the m. RNA to be translated is guided to the preinitiation complex by a subunit of the multiprotein e. IF 4 complex, which also unwinds any secondary structure at the 5' end of the m. RNA. Subsequent scanning by the small ribosomal subunit, assisted by e. IF 3 and e. IF 4 G, positions the initiator t. RNA at the AUG start codon, yielding the 40 S initiation complex and releasing e. IF 1 A, e. IF 3, and e. IF 4. With the Met t. RNAi. Met properly positioned at the start codon, another factor, e. IF 5, assists union of the 40 S complex with the 60 S subunit. Hydrolysis of GTP in e. IF 2 GTP provides the energy for this step. Factors e. IF 5 and e. IF 2 GDP are then released, yielding the final 80 S initiation complex, with Met t. RNAi. Met at the P site. The complex can now accept the second aminoacyl t. RNA
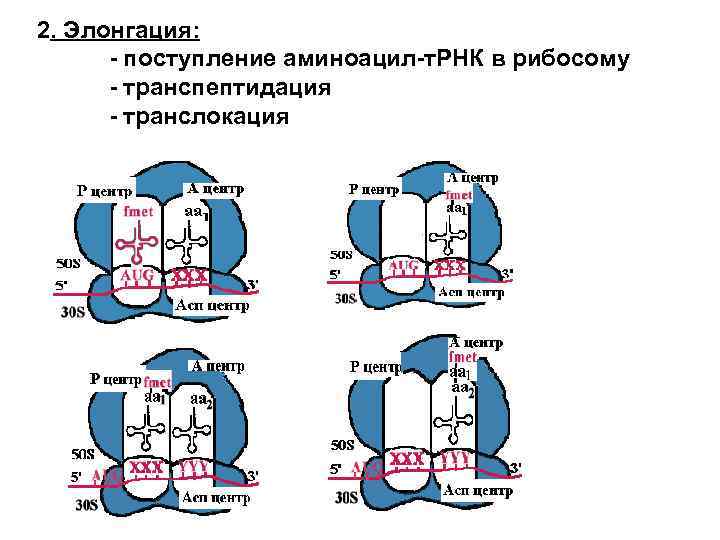
2. Элонгация: - поступление аминоацил-т. РНК в рибосому - транспептидация - транслокация
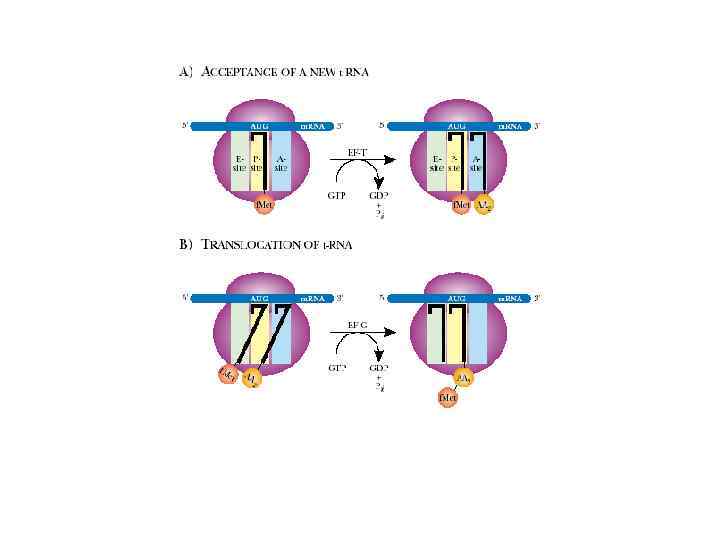
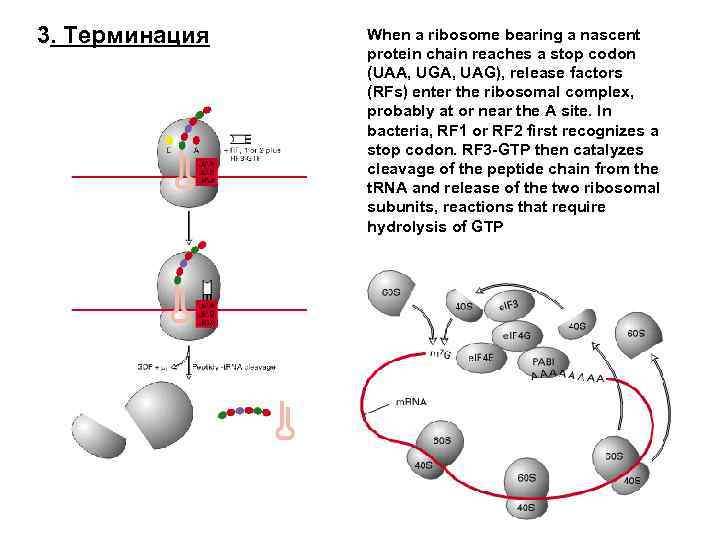
3. Терминация When a ribosome bearing a nascent protein chain reaches a stop codon (UAA, UGA, UAG), release factors (RFs) enter the ribosomal complex, probably at or near the A site. In bacteria, RF 1 or RF 2 first recognizes a stop codon. RF 3 -GTP then catalyzes cleavage of the peptide chain from the t. RNA and release of the two ribosomal subunits, reactions that require hydrolysis of GTP

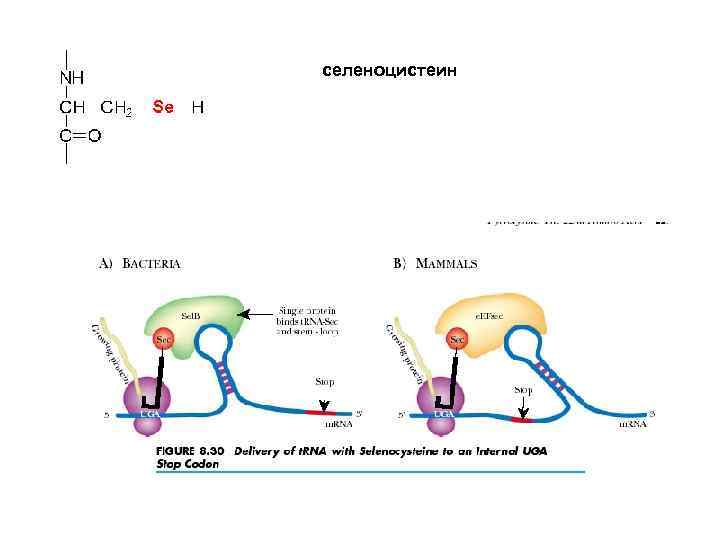
селеноцистеин
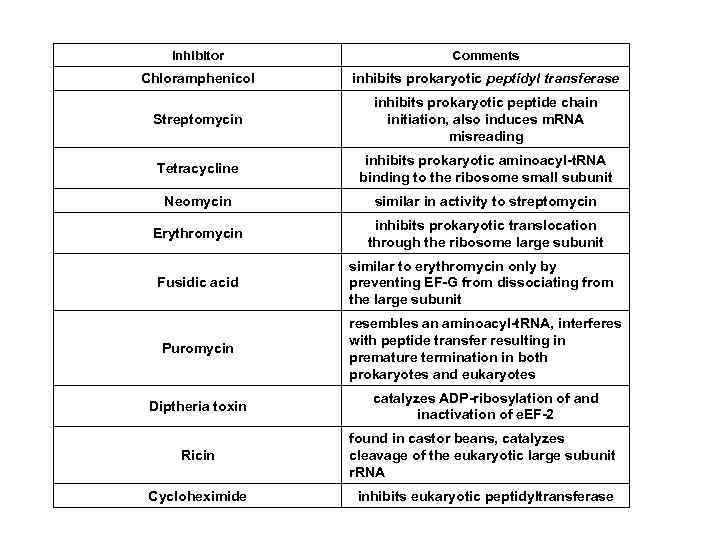
Inhibitor Comments Chloramphenicol inhibits prokaryotic peptidyl transferase Streptomycin inhibits prokaryotic peptide chain initiation, also induces m. RNA misreading Tetracycline inhibits prokaryotic aminoacyl-t. RNA binding to the ribosome small subunit Neomycin similar in activity to streptomycin Erythromycin inhibits prokaryotic translocation through the ribosome large subunit Fusidic acid similar to erythromycin only by preventing EF-G from dissociating from the large subunit Puromycin resembles an aminoacyl-t. RNA, interferes with peptide transfer resulting in premature termination in both prokaryotes and eukaryotes Diptheria toxin catalyzes ADP-ribosylation of and inactivation of e. EF-2 Ricin found in castor beans, catalyzes cleavage of the eukaryotic large subunit r. RNA Cycloheximide inhibits eukaryotic peptidyltransferase
3 трансляция.ppt