Translyatsia_i_belki.pptx
- Количество слайдов: 92

Трансляция и белки
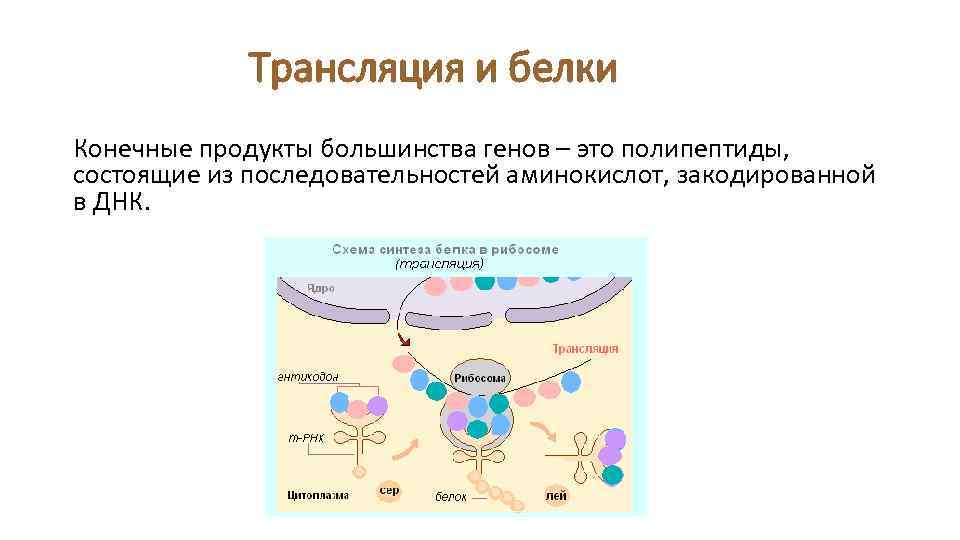
Трансляция и белки Конечные продукты большинства генов – это полипептиды, состоящие из последовательностей аминокислот, закодированной в ДНК.

Трансляция: необходимые для синтеза белков компоненты • Трансляция м. РНК – биологическая полимеризация аминокислот в полипептидную цепь. vвозможна только при ассоциации м. РНК с рибосомами. • триплеты рибонуклеотидов в м. РНК направляют специфические аминокислоты на определенные позиции в молекуле полипептида с помощью транспортных РНК (т. РНК). v. Адапторную роль т. РНК предположил в 1957 г. Фрэнсис Крик.

Трансляция: необходимые для синтеза белков компоненты • Ассоциируя с рибосомой, м. РНК презентирует специфичный для аминокислоты кодон, и молекула т. РНК с комплементарным антикодоном и ковалентно связанной аминокислотой спаривается с помощью водородных связей с м. РНК. • Затем аминокислота встраивается в полипептидную цепь.

Структура рибосом В бактериальной клетке – около 10 000 рибосом, в эукариотической – в десятки раз больше. • рибосома диаметром состоит из двух субъединиц: большой и малой. • В состав обеих субъединиц входит одна или несколько молекул р. РНК и комплекс рибосомных белков. • Когда эти субъединицы ассоциируют в одну рибосому – моносома. У прокариот моносома 70 S состоит из субъединиц 50 S и 30 S, • Большая субъединица прокариотической рибосомы содержит молекулу 23 S р. РНК и молекулу 5 S р. РНК, а также 31 рибосомный белок. • В состав малой субъединицы прокариотической рибосомы входит 16 S р. РНК и 21 белок • эукариотическая рибосома 80 S –субъединицы 60 S и 40 S. • У эукариот большая субъединица содержит молекулу 28 S р. РНК, связанную с 5, 8 S р. РНК, а также молекулу 5 S р. РНК и около 50 -ти рибосомных белков. • малая субъединица эукариотической рибосомы – 18 S р. РНК и 33 белка. Модель рибосомы Escherichia coli. Красным цветом выделена большая субъединица, синим — малая субъединица. Более светлым оттенком показаны рибосомные белки, более темным — р. РНК
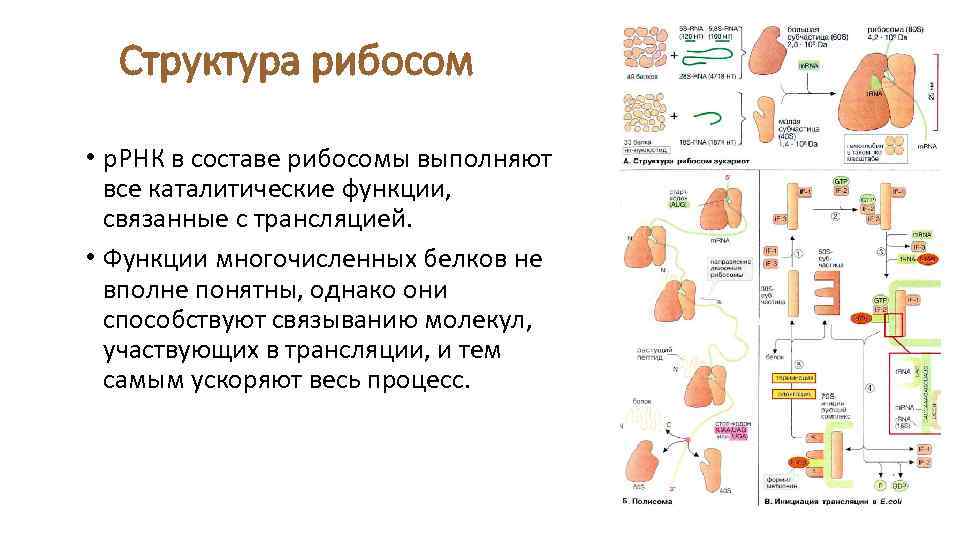
Структура рибосом • р. РНК в составе рибосомы выполняют все каталитические функции, связанные с трансляцией. • Функции многочисленных белков не вполне понятны, однако они способствуют связыванию молекул, участвующих в трансляции, и тем самым ускоряют весь процесс.
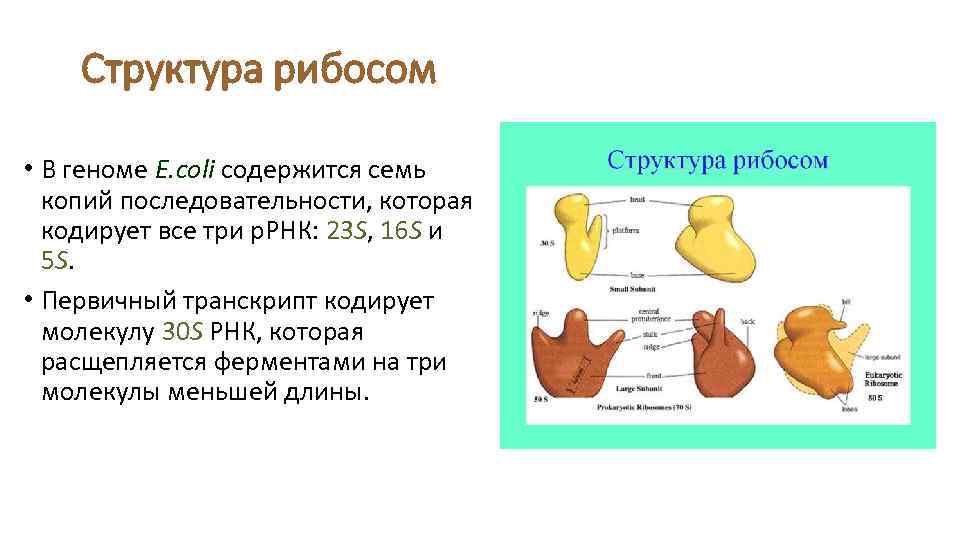
Структура рибосом • В геноме E. coli содержится семь копий последовательности, которая кодирует все три р. РНК: 23 S, 16 S и 5 S. • Первичный транскрипт кодирует молекулу 30 S РНК, которая расщепляется ферментами на три молекулы меньшей длины.

Структура рибосом • У эукариот копийность генов, кодирующих 28 S и 18 S р. РНК выше. v. В гаплоидном геноме Drosophila содержится около 120 копий гена, который транскрибируется на 34 S РНК. v. В результате процессинга этих молекул образуются молекулы 28 S, 18 S и 5, 8 S р. РНК. • В гаплоидном геноме X. laevis имеется более 500 копий генов, кодирующих р. РНК. v. Гены, кодирующие р. РНК, называются также р. ДНК и входят в состав умеренно повторяющейся фракции ДНК, локализованной на разных хромосомах в виде отдельных кластеров. v. Каждый такой кластер в геноме эукариот представлен тандемными повторами, в которых кодирующие последовательности разделены некодирующими спейсерами. У человека эти повторы локализованы в теломерных областях хромосом 13, 14, 15, 21 и 22. • Гены, кодирующие 5 S РНК локализованы по отдельности на хромосоме 1.
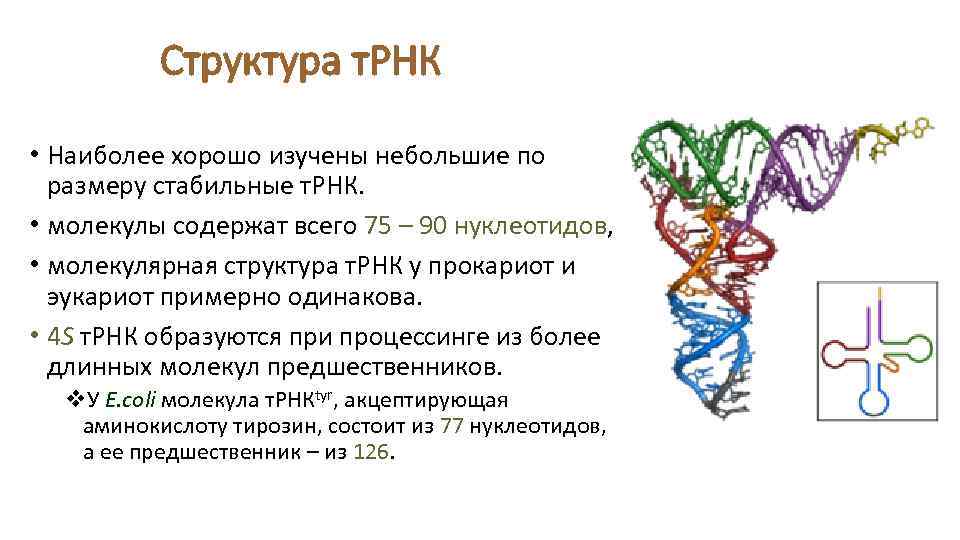
Структура т. РНК • Наиболее хорошо изучены небольшие по размеру стабильные т. РНК. • молекулы содержат всего 75 – 90 нуклеотидов, • молекулярная структура т. РНК у прокариот и эукариот примерно одинакова. • 4 S т. РНК образуются при процессинге из более длинных молекул предшественников. v. У E. coli молекула т. РНКtyr, акцептирующая аминокислоту тирозин, состоит из 77 нуклеотидов, а ее предшественник – из 126.

Структура т. РНК • В 1965 г. Роберт Холли с сутрудниками расшифровали последовательность т. РНКala, выделенной из дрожжей. vряд нуклеотидов уникален только для этого аланиновой т. РНК. v. Одно из четырех оснований (G, C, A и U) модифицировано в виде инозиновой кислоты, гипоксантина (пурина), риботимидиновой кислоты и псевдоуридина. • Эти модификации относятся к необычным, редким или непарным основаниям и появляются в ходе последующих посттранскрипционных изменений, • в процессе транскрипции в пре-т. РНК встраиваются немодифицированные основания, которые изменяются под действием ферментов. Формирование L-образной структуры и её взаимодействие с АРСазой

Структура т. РНК • В результате анализа последовательности т. РНК Холли предложил двумерную модель ее молекулы в виде клеверного листа. vвторичная структура т. РНК образуется за счет спаривания оснований. vлинейная молекула может формировать несколько протяженных участков такого спаривания. vполучается несколько спаренных «стеблей» и неспаренных петель, напоминающей клеверный лист.
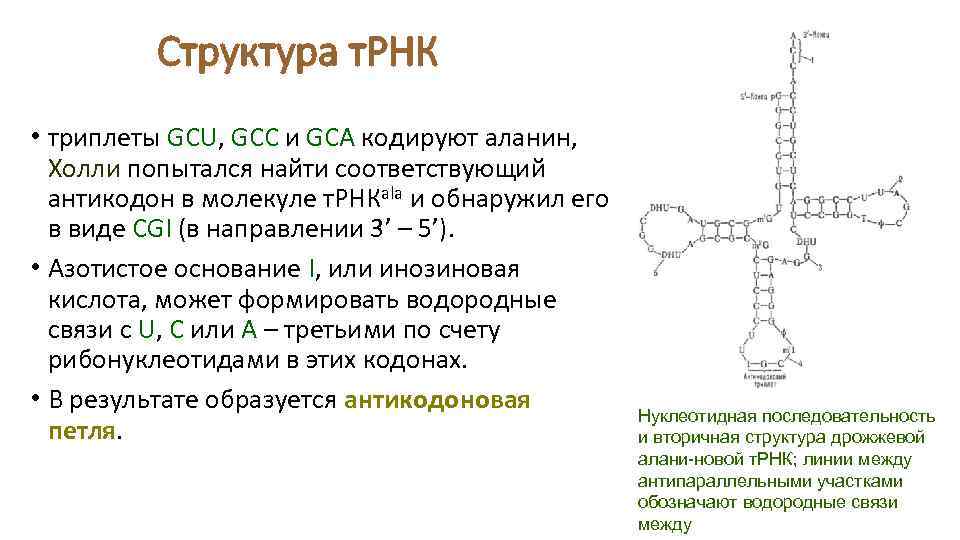
Структура т. РНК • триплеты GCU, GCC и GCA кодируют аланин, Холли попытался найти соответствующий антикодон в молекуле т. РНКala и обнаружил его в виде CGI (в направлении 3’ – 5’). • Азотистое основание I, или инозиновая кислота, может формировать водородные связи с U, C или А – третьими по счету рибонуклеотидами в этих кодонах. • В результате образуется антикодоновая петля. Нуклеотидная последовательность и вторичная структура дрожжевой алани-новой т. РНК; линии между антипараллельными участками обозначают водородные связи между
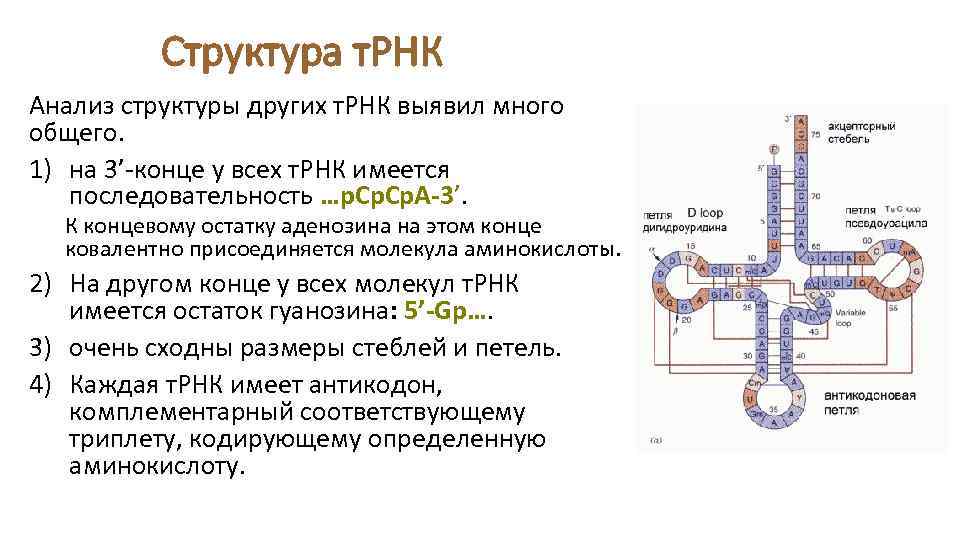
Структура т. РНК Анализ структуры других т. РНК выявил много общего. 1) на 3’-конце у всех т. РНК имеется последовательность …р. Ср. А-3’. К концевому остатку аденозина на этом конце ковалентно присоединяется молекула аминокислоты. 2) На другом конце у всех молекул т. РНК имеется остаток гуанозина: 5’-Gp…. 3) очень сходны размеры стеблей и петель. 4) Каждая т. РНК имеет антикодон, комплементарный соответствующему триплету, кодирующему определенную аминокислоту.
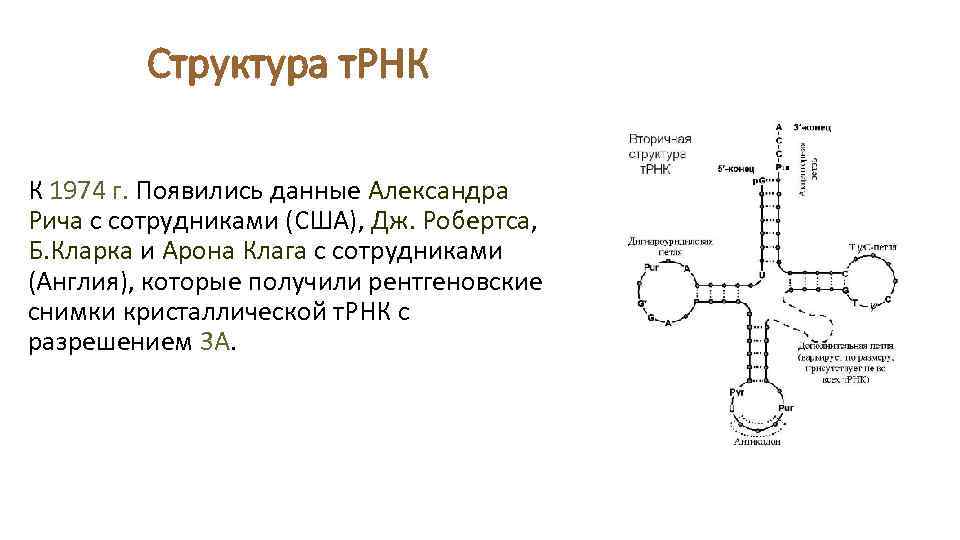
Структура т. РНК К 1974 г. Появились данные Александра Рича с сотрудниками (США), Дж. Робертса, Б. Кларка и Арона Клага с сотрудниками (Англия), которые получили рентгеновские снимки кристаллической т. РНК с разрешением 3 А.

Структура т. РНК • В результате этих исследований появилась трехмерная модель т. РНК. • На одном конце молекулы имеется антикодоновая петля и антикодоновый стебель, формирующие шпильку, а на другом конце – 3’-акцепторный участок связывания аминокислоты.
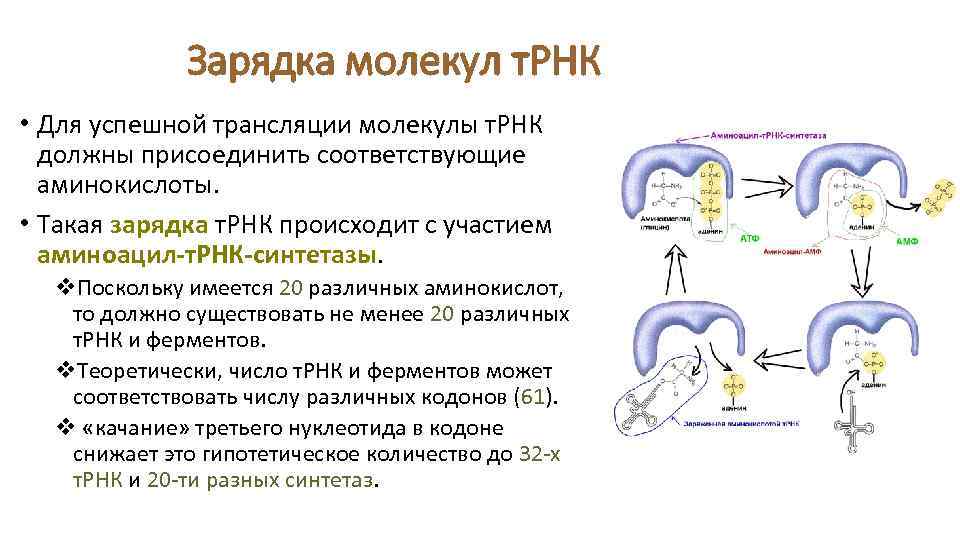
Зарядка молекул т. РНК • Для успешной трансляции молекулы т. РНК должны присоединить соответствующие аминокислоты. • Такая зарядка т. РНК происходит с участием аминоацил-т. РНК-синтетазы. v. Поскольку имеется 20 различных аминокислот, то должно существовать не менее 20 различных т. РНК и ферментов. v. Теоретически, число т. РНК и ферментов может соответствовать числу различных кодонов (61). v «качание» третьего нуклеотида в кодоне снижает это гипотетическое количество до 32 -х т. РНК и 20 -ти разных синтетаз.
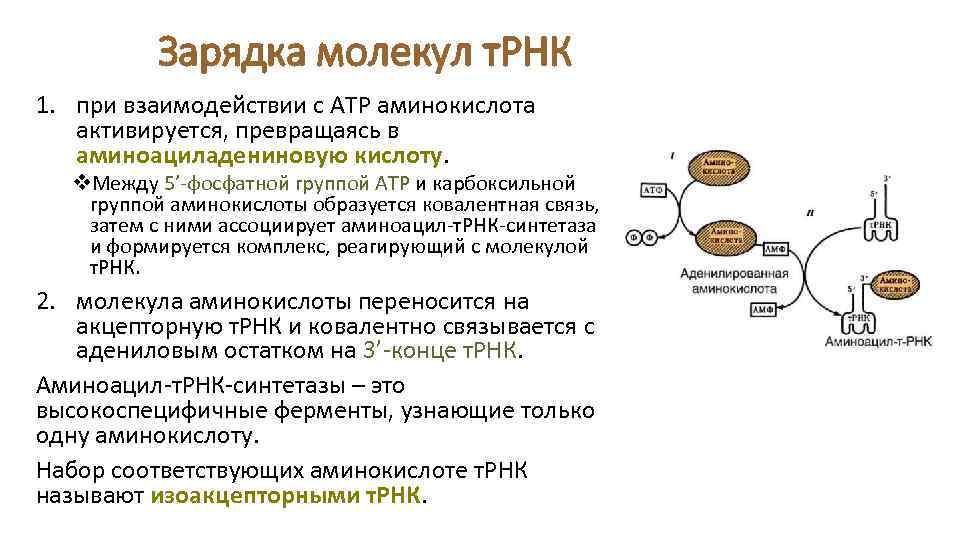
Зарядка молекул т. РНК 1. при взаимодействии с АТР аминокислота активируется, превращаясь в аминоациладениновую кислоту. v. Между 5’-фосфатной группой АТР и карбоксильной группой аминокислоты образуется ковалентная связь, затем с ними ассоциирует аминоацил-т. РНК-синтетаза и формируется комплекс, реагирующий с молекулой т. РНК. 2. молекула аминокислоты переносится на акцепторную т. РНК и ковалентно связывается с адениловым остатком на 3’-конце т. РНК. Аминоацил-т. РНК-синтетазы – это высокоспецифичные ферменты, узнающие только одну аминокислоту. Набор соответствующих аминокислоте т. РНК называют изоакцепторными т. РНК.
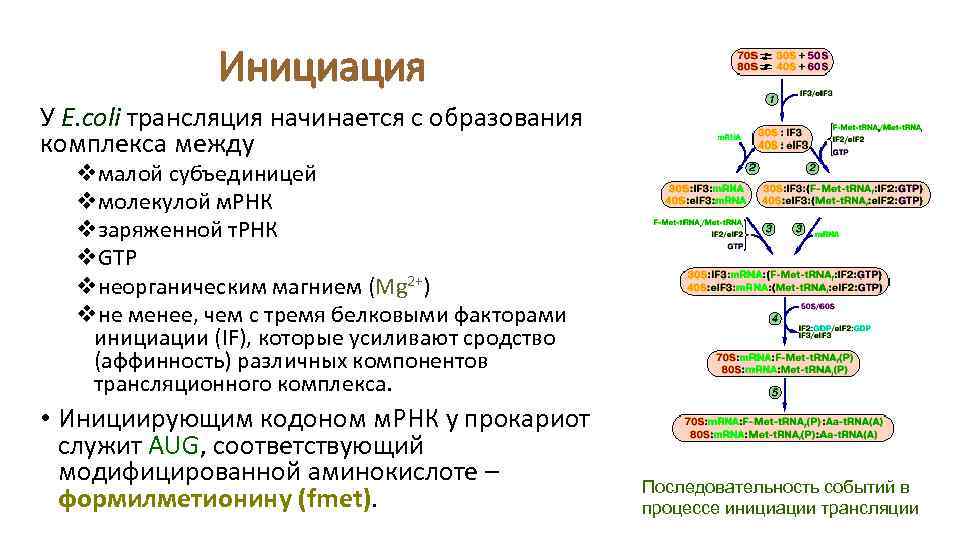
Инициация У E. coli трансляция начинается с образования комплекса между vмалой субъединицей vмолекулой м. РНК vзаряженной т. РНК v. GTP vнеорганическим магнием (Mg 2+) vне менее, чем с тремя белковыми факторами инициации (IF), которые усиливают сродство (аффинность) различных компонентов трансляционного комплекса. • Инициирующим кодоном м. РНК у прокариот служит AUG, соответствующий модифицированной аминокислоте – формилметионину (fmet). Последовательность событий в процессе инициации трансляции
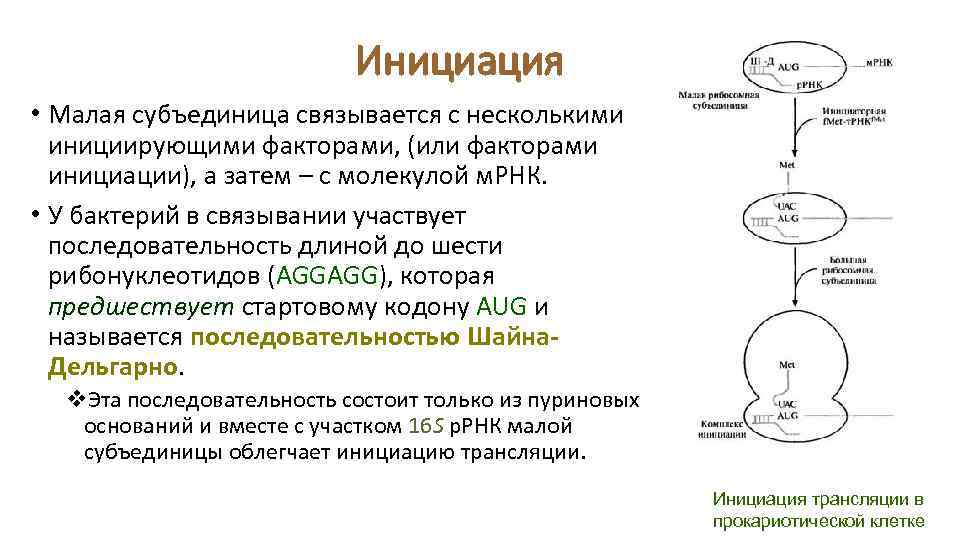
Инициация • Малая субъединица связывается с несколькими инициирующими факторами, (или факторами инициации), а затем – с молекулой м. РНК. • У бактерий в связывании участвует последовательность длиной до шести рибонуклеотидов (AGGAGG), которая предшествует стартовому кодону AUG и называется последовательностью Шайна. Дельгарно. v. Эта последовательность состоит только из пуриновых оснований и вместе с участком 16 S р. РНК малой субъединицы облегчает инициацию трансляции. Инициация трансляции в прокариотической клетке
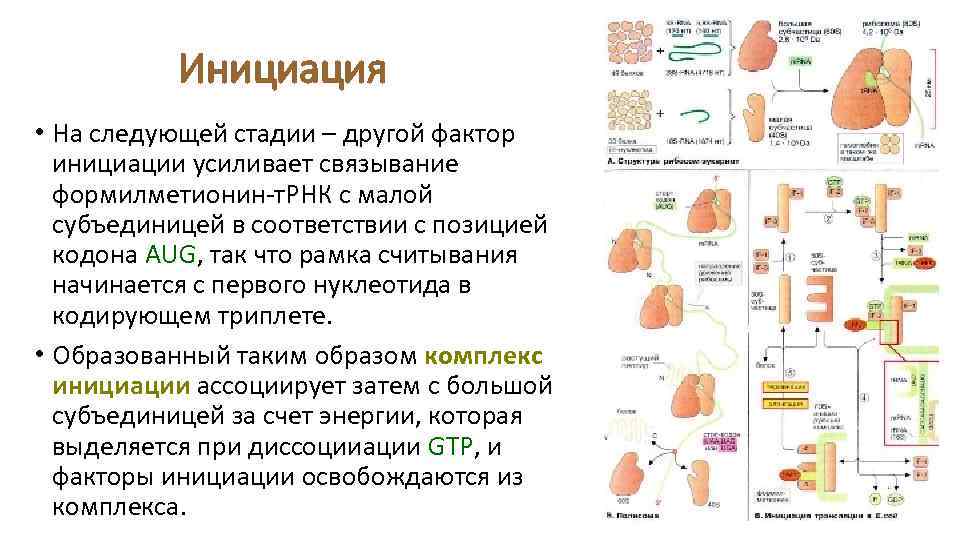
Инициация • На следующей стадии – другой фактор инициации усиливает связывание формилметионин-т. РНК с малой субъединицей в соответствии с позицией кодона AUG, так что рамка считывания начинается с первого нуклеотида в кодирующем триплете. • Образованный таким образом комплекс инициации ассоциирует затем с большой субъединицей за счет энергии, которая выделяется при диссоцииации GTP, и факторы инициации освобождаются из комплекса.
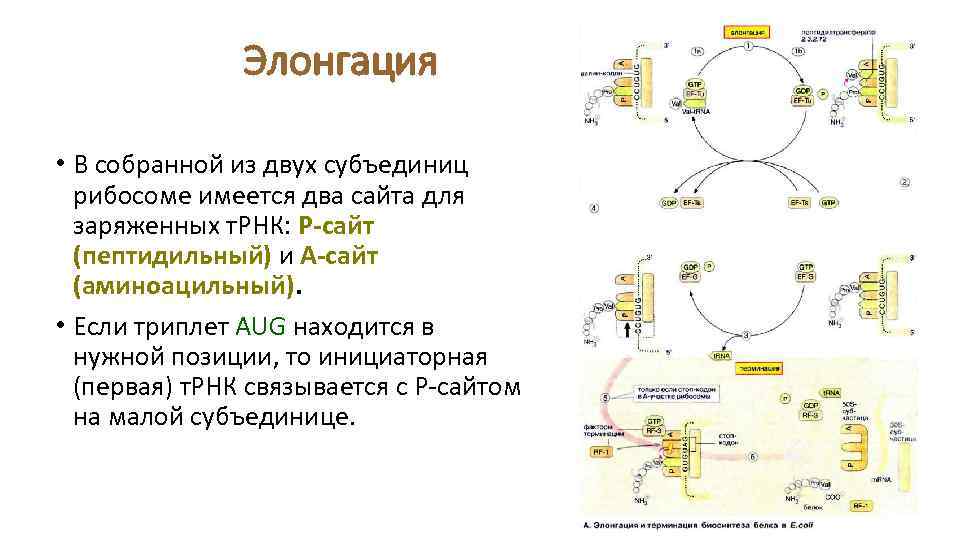
Элонгация • В собранной из двух субъединиц рибосоме имеется два сайта для заряженных т. РНК: Р-сайт (пептидильный) и А-сайт (аминоацильный). • Если триплет AUG находится в нужной позиции, то инициаторная (первая) т. РНК связывается с Р-сайтом на малой субъединице.
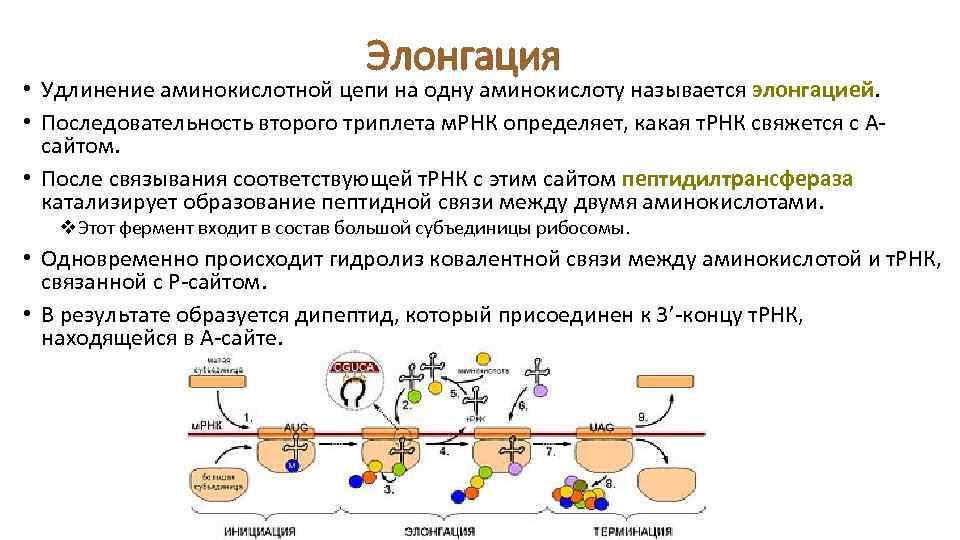
Элонгация • Удлинение аминокислотной цепи на одну аминокислоту называется элонгацией. • Последовательность второго триплета м. РНК определяет, какая т. РНК свяжется с Асайтом. • После связывания соответствующей т. РНК с этим сайтом пептидилтрансфераза катализирует образование пептидной связи между двумя аминокислотами. v. Этот фермент входит в состав большой субъединицы рибосомы. • Одновременно происходит гидролиз ковалентной связи между аминокислотой и т. РНК, связанной с Р-сайтом. • В результате образуется дипептид, который присоединен к 3’-концу т. РНК, находящейся в А-сайте.
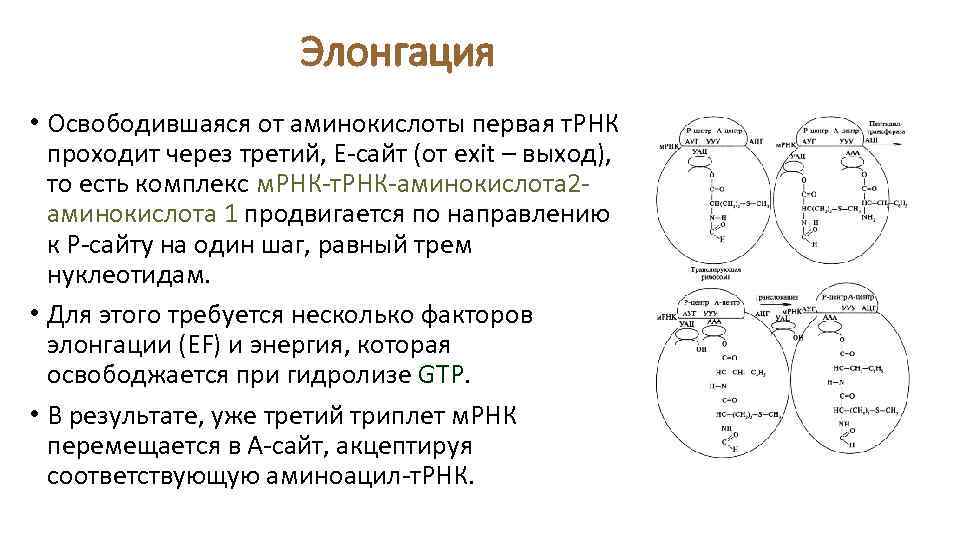
Элонгация • Освободившаяся от аминокислоты первая т. РНК проходит через третий, Е-сайт (от exit – выход), то есть комплекс м. РНК-т. РНК-аминокислота 2 аминокислота 1 продвигается по направлению к Р-сайту на один шаг, равный трем нуклеотидам. • Для этого требуется несколько факторов элонгации (EF) и энергия, которая освободжается при гидролизе GTP. • В результате, уже третий триплет м. РНК перемещается в А-сайт, акцептируя соответствующую аминоацил-т. РНК.
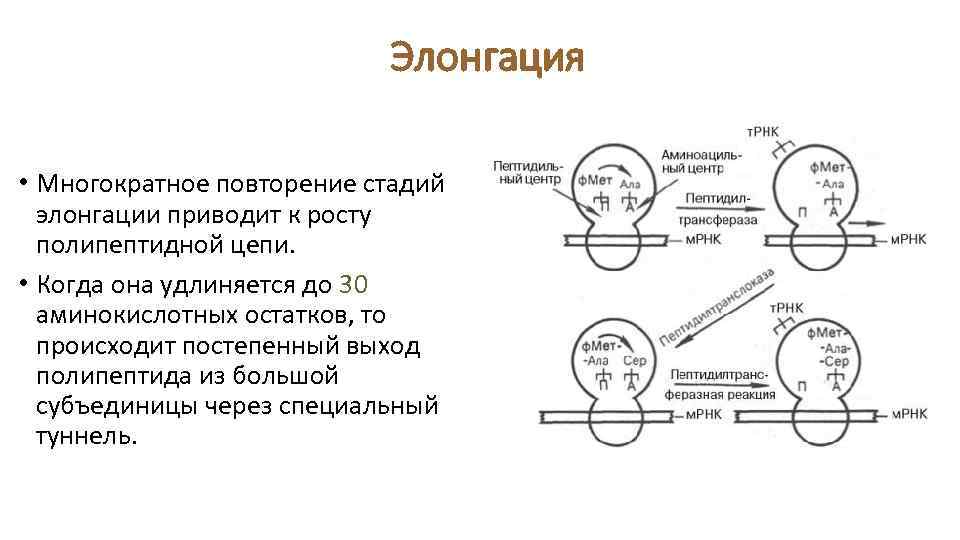
Элонгация • Многократное повторение стадий элонгации приводит к росту полипептидной цепи. • Когда она удлиняется до 30 аминокислотных остатков, то происходит постепенный выход полипептида из большой субъединицы через специальный туннель.

Элонгация • Роль малой субъединицы заключается в «расшифровке» триплетов м. РНК. • большая субъединица связывает аминокислоты в полипептидную цепь. • Скорость элонгации очень высока, а частота вероятных ошибок не превышает 10 -4. • У E. coli при 37⁰C скорость элонгации равна примерно 15 -ти аминокислотам в секунду.
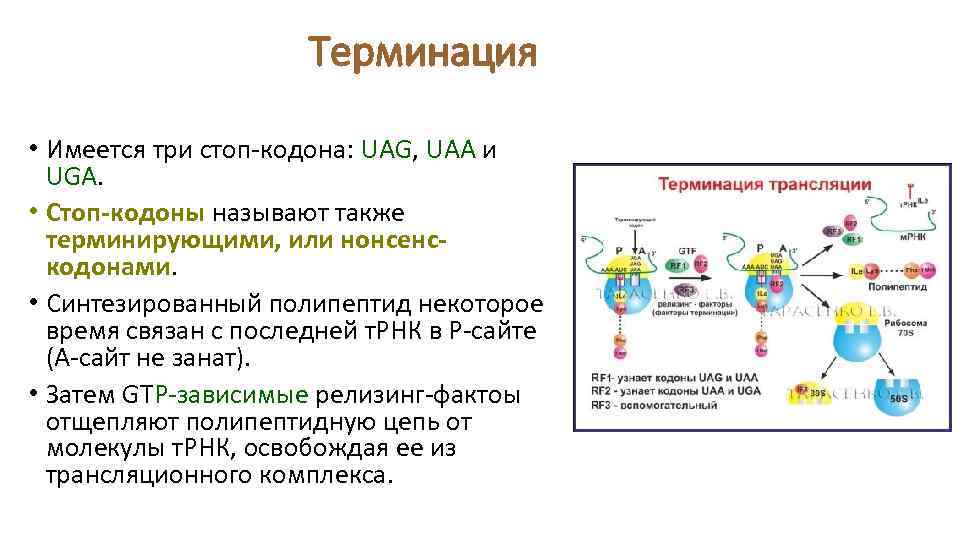
Терминация • Имеется три стоп-кодона: UAG, UAA и UGA. • Стоп-кодоны называют также терминирующими, или нонсенскодонами. • Синтезированный полипептид некоторое время связан с последней т. РНК в Р-сайте (А-сайт не занат). • Затем GTP-зависимые релизинг-фактоы отщепляют полипептидную цепь от молекулы т. РНК, освобождая ее из трансляционного комплекса.
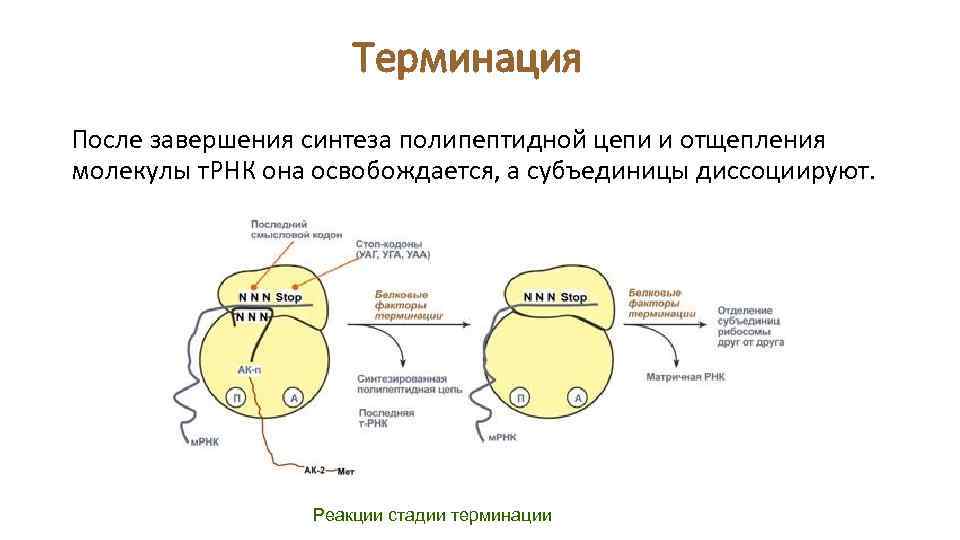
Терминация После завершения синтеза полипептидной цепи и отщепления молекулы т. РНК она освобождается, а субъединицы диссоциируют. Реакции стадии терминации

Полирибосомы • После завершения элонгации часть молекулы м. РНК проходит через рибосому и ассоциирует с малой субъединицей другой рибосомы, формируя второй инициирующий комплекс. • Этот процесс может повторяться несколько раз и в результате возникают полирибосомы, или полисомы.
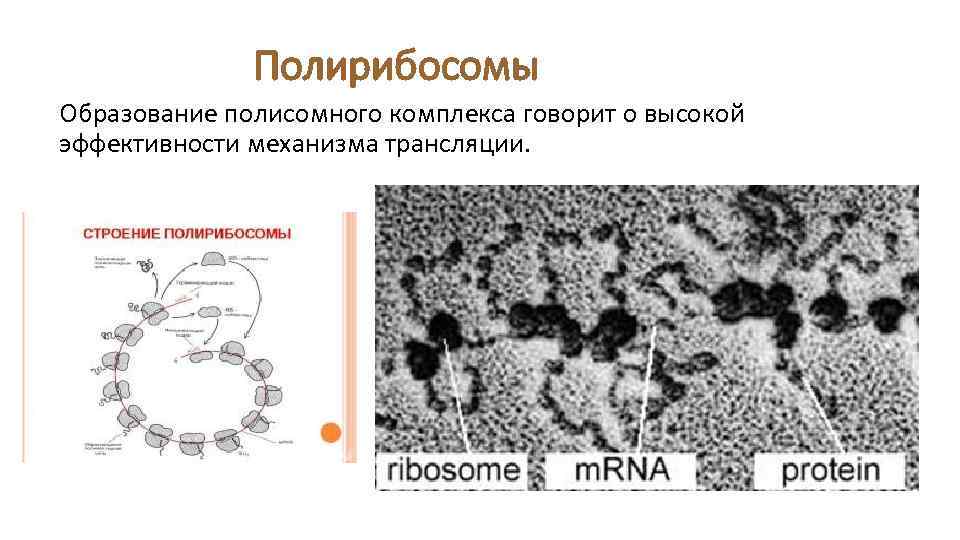
Полирибосомы Образование полисомного комплекса говорит о высокой эффективности механизма трансляции.
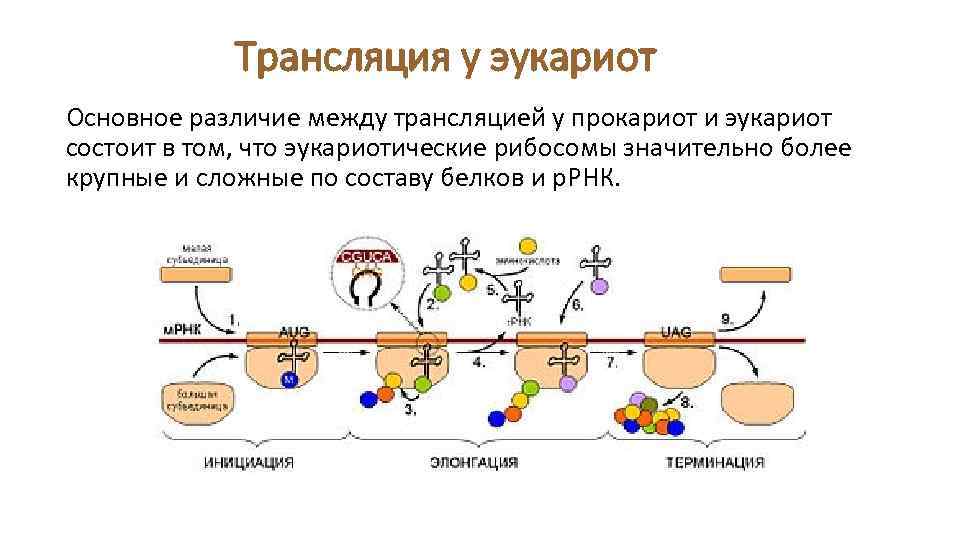
Трансляция у эукариот Основное различие между трансляцией у прокариот и эукариот состоит в том, что эукариотические рибосомы значительно более крупные и сложные по составу белков и р. РНК.

Трансляция у эукариот молекулы эукариотической м. РНК существуют в клетках значительно дольше прокариотических: большинство из них сохраняется в течение нескольких часов, а не минут, как у прокариот, то есть м. РНК достаточно долго участвует в синтезе белков, а затем деградирует под действием нуклеаз.

Трансляция у эукариот Инициация трансляции у эукариот имеет свои особенности: • за счет появления на 5’-конце зрелой м. РНК кэпа (остатка 7 метилгуанозина) эффективность трансляции эукариотических м. РНК выше, чем прокариотических, не имеющих кэпа. • Инициирующий кодон AUG в эукариотической м. РНК граничит с узнающей последовательностью Козак – 5’-ACCAUGG, названной так по имени открывшей ее Мерилин Козак. v. Эта последовательность, по-видимому, выполняет те же функции, что и последовательность Шайна-Дельгарно у прокариот: сильно ускоряет связывание м. РНК с малой субъединицей рибосомы.
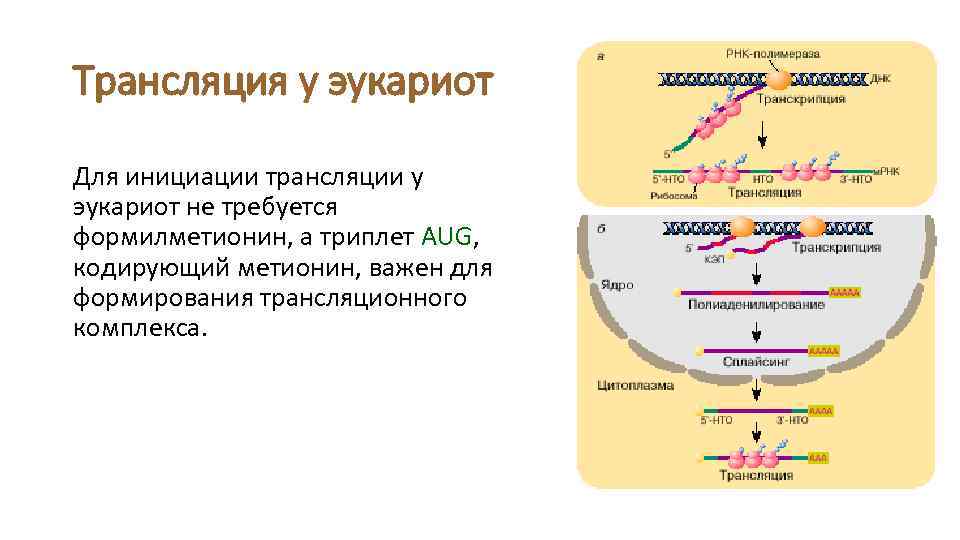
Трансляция у эукариот Для инициации трансляции у эукариот не требуется формилметионин, а триплет AUG, кодирующий метионин, важен для формирования трансляционного комплекса.

Трансляция у эукариот • В трансляции участвуют белки, сходные или гомологичные факторам инициации, элонгации и терминации прокариот. • на каждой стадии трансляции в эукариотической клетке обычно действует большее число более сложных по структуре факторов.

Трансляция у эукариот • Большинство эукариотических рибосом ассоциированно с мембранами, формируя эндоплазматический ретикулум (сеть) или ЭР, отсутствующий у прокариот. • Туннель большой субъединицы рибосомы начинается в месте соприкосновения двух субъединиц и проходит недалеко от поверхности большой субъединицы. • У дрожжей синтезированные белки входят в ЭР через его специальный мембранный канал, образованный белком Sec 61. Этот канал точно совпадает с выходом рибосомного канала.
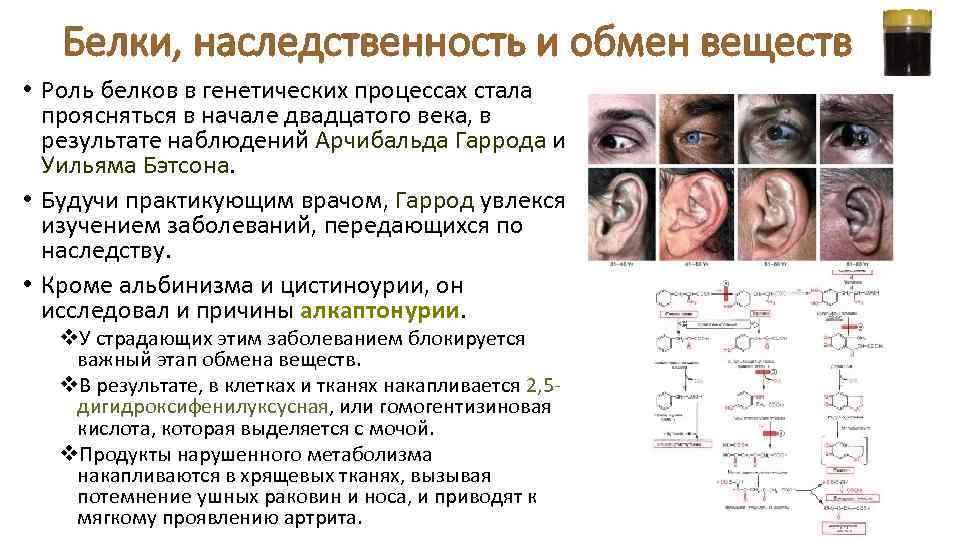
Белки, наследственность и обмен веществ • Роль белков в генетических процессах стала проясняться в начале двадцатого века, в результате наблюдений Арчибальда Гаррода и Уильяма Бэтсона. • Будучи практикующим врачом, Гаррод увлекся изучением заболеваний, передающихся по наследству. • Кроме альбинизма и цистиноурии, он исследовал и причины алкаптонурии. v. У страдающих этим заболеванием блокируется важный этап обмена веществ. v. В результате, в клетках и тканях накапливается 2, 5 дигидроксифенилуксусная, или гомогентизиновая кислота, которая выделяется с мочой. v. Продукты нарушенного метаболизма накапливаются в хрящевых тканях, вызывая потемнение ушных раковин и носа, и приводят к мягкому проявлению артрита.

Белки, наследственность и обмен веществ • Гаррод исследовал алкаптонурию, вводя в рацион больных диетический белок или аминокислоты фенилаланин и тирозин, которые химически связаны с гомогентизиновой кислотой. v. В этих условиях содержание гомогентизиновой кислоты у больных алкаптонурией повышалось, а у здоровых людей – нет. • у больных нарушен катаболизм (распад) алкаптона. v. Анализируя родословные больных алкаптонурией, он определил, что это заболевание наследуется как моногенный рецессивный признак.
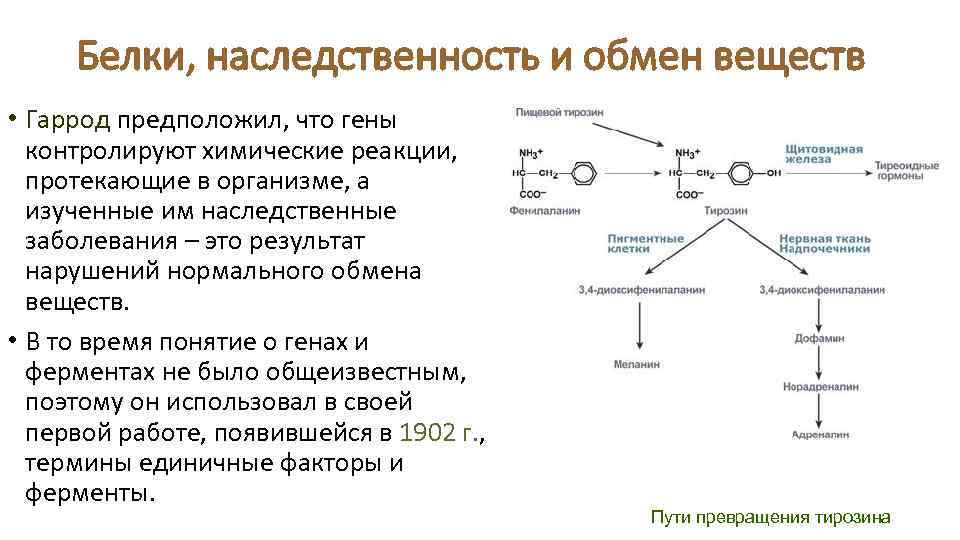
Белки, наследственность и обмен веществ • Гаррод предположил, что гены контролируют химические реакции, протекающие в организме, а изученные им наследственные заболевания – это результат нарушений нормального обмена веществ. • В то время понятие о генах и ферментах не было общеизвестным, поэтому он использовал в своей первой работе, появившейся в 1902 г. , термины единичные факторы и ферменты. Пути превращения тирозина

Белки, наследственность и обмен веществ Работами Гаррода заинтересовались несколько генетиков, включая Бэтсона, который считал, что наследственные заболевания обусловлены отсутствием в организме больных определенных критических веществ. • В 1909 г. он опубликовал работу «Менделевские принципы наследования» , в которой обосновал связь между генами и ферментами.

Фенилкетонурия • Наследственное заболевание фенилкетонурия (ФКУ) также связано с нарушением обмена веществ, - впервые его описали в 1934 г. • сопровождается умственной отсталостью, • наследуется как аутосомно-рецессивный признак. • У больных блокировано превращение фенилаланина в аминокислоту тирозин. v. Молекулы этих веществ отличаются только наличием одной гидроксильной группы у тирозина и ее отсутствием – у фенилаланина. v. Превращение фенилаланина в тирозин катализирует фермент фенилаланин-гидроксилаза, функционирующий в клетках печени. v. У гетерозигот по мутантному гену этот фермент активен на 30% от нормы, когда уровень фенилаланина в крови не более 1 мг/мл (у больных ФКУ он достигает 50 мг/мл).
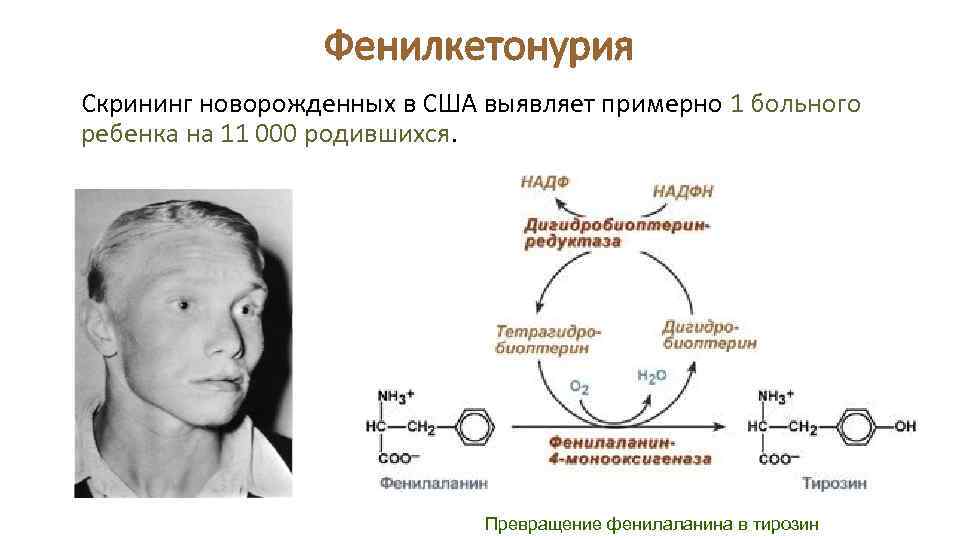
Фенилкетонурия Скрининг новорожденных в США выявляет примерно 1 больного ребенка на 11 000 родившихся. Превращение фенилаланина в тирозин

Гипотеза: один ген – один фермент • В 1933 г. Джордж Бидл эксперементально доказал прямое участие генов в синтезе ферментов. • Вместе со своим сотрудником Борисом эфрусси он исследовал пигменты, окрашивающие глаза у Drosophila. v. Оказалось, что мутации генов, вызывающих изменение окраски глаз у плодовой мушки, могут быть ассоциированны с утратой функций некоторых ферментов. • Вскоре Бидл и эдвард Татум исследовали мутации, связанные с нарушением обмена веществ у плесневого гриба Neurospora crassa. Эти работы легли в основу гипотезы один ген – один фермент.
Опыты Бидла и Татума с мутантами Neurospora В начале 40 -х годов ХХ века Бидл и Татум начали эксперименты с плесневым грибом Neurospora, биохимия которого была хорошо изучена.

Опыты Бидла и Татума с мутантами Neurospora • Используя минимальные количества углерода и азота, этот организм может синтезировать v 9 водорастворимых витаминов, v 20 аминокислот, vмножество каротиноидов, vвсе необходимые пурины и пиримидины. • Бидл и Татум облучили бесполые споры (конидии) гриба Х-лучами, что привело к резкому увеличению частоты мутаций, а затем выращивали мутанты на полной среде, содержащей витамины, аминокислоты и т. д. v. После этого все полученные культуры переносили на минимальную среду, где клетки должны синтезировать необходимые для роста вещества самостоятельно. v. Все мутанты прекращали свой рост на минимальной среде, но на различных средах можно было отобрать мутантов, у которых нарушен тот или иной путь метаболизма.

Опыты Бидла и Татума с мутантами Neurospora • С помощью таких серий минимальных сред им удалось идентифицировать различные типы мутаций, зависящие от присутствия в среде определенных витаминов, аминокислот, пуриновых или пиримидиновых оснований. • В результате, Бидл и Татум пришли к выводу, что добавленное в минимальную среду вещество, которое восстанавливает рост клеток, представляет собой субстрат, не синтезирующийся в результате мутации.

Опыты Бидла и Татума с мутантами Neurospora • Первая из выявленных ими мутаций была обнаружена в штамме, который не синтезировал витамин B 6 (пиридоксин), а вторая – штамм с нехваткой витамина B 1 (тиамина). • Вскоре Бидл и Татум выделили сотни различных мутантов нейроспоры, на способных к синтезу разных витаминов, аминокислот и других веществ.

Опыты Бидла и Татума с мутантами Neurospora • Тестирование более 80 000 спор показало взаимосвязь генетических и биохимических нарушений в клетках. • Казалось, что практически каждой ферментативной активности соответствует определенная мутация которая ведет к утрате этой активности и нарушению метаболизма. • Это позволило Бидлу и Татуму сформулировать гипотезу о том, что один ген определяет один фермент, подтверждающую высказанную на 30 лет раньше гипотезу Гэррода и Бэтсона.

Гены и ферменты: биохимический анализ Многолетняя работа с использованием различных методов проверки гипотезы один ген: один фермент значительно углубила представления о метаболизме у Neurospora, Escherichia coli и других микроорганизмов. v. Одним из первых был детально исследован метаболизм аргинина у Neurospora. v. Адриан Серб и Норман Горовиц изучили семь мутантных штаммов, для роста которых требовался аргинин (arg-). Neurospora
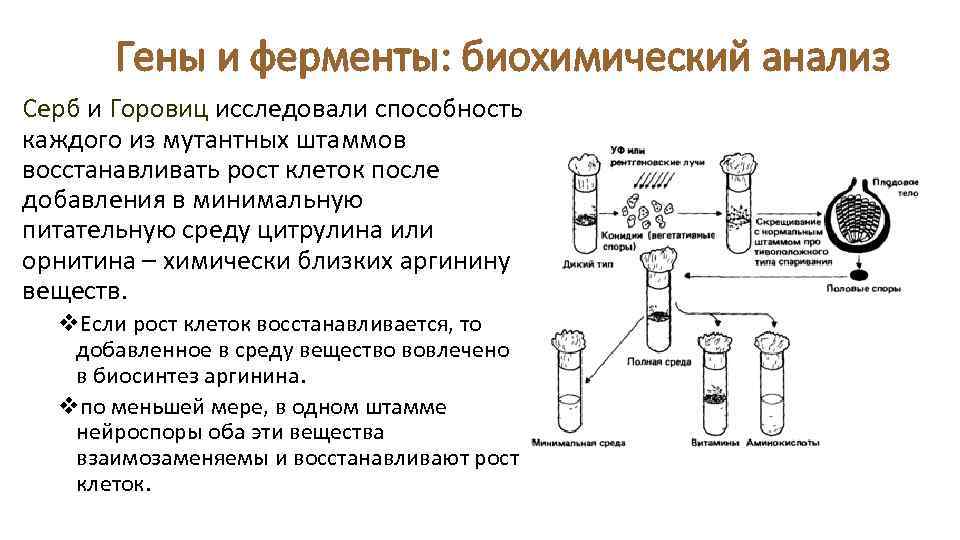
Гены и ферменты: биохимический анализ Серб и Горовиц исследовали способность каждого из мутантных штаммов восстанавливать рост клеток после добавления в минимальную питательную среду цитрулина или орнитина – химически близких аргинину веществ. v. Если рост клеток восстанавливается, то добавленное в среду вещество вовлечено в биосинтез аргинина. vпо меньшей мере, в одном штамме нейроспоры оба эти вещества взаимозаменяемы и восстанавливают рост клеток.

Гены и ферменты: биохимический анализ •

Гены и ферменты: биохимический анализ Эта схема подтверждается логически: если мутанты arg 4 -7 растут независимо от того, какое из трех веществ добавлено в минимальную среду, то соответствующие мутации затрагивают метаболизм до вовлечения в обмен веществ орнитина, цитруллина или аргинина.

Гены и ферменты: биохимический анализ При добавлении любой из этих аминокислот блок снимается, что означает вовлеченность в биосинтез аргиника как цитрулина, так и орнитина.

Гены и ферменты: биохимический анализ Если мутантные клетки из штаммов arg 2 и arg 3 растут при добавлении в среду цитруллина, следовательно, орнитин включается в биосинтез до появления блока и его присутствие в среде не компенсирует мутацию, как в случае цитрулина.

Гены и ферменты: биохимический анализ Очевидно, что мутация arg 1 блокирует превращение цитруллина в аргинин, поскольку добавление в среду орнитина или цитруллина не приводит к росту клеток.

Гены и ферменты: биохимический анализ После публикации работы Серба и Горовица в 1944 г. Были идентифицированы все ферменты, участвующие в биосинтезе аргинина.

Один ген – одна полипептидная цепь В начале 40 -х годов ХХ века концепция один ген: один фермент не привлекла особого внимания генетиков. Изменчивость раковины лунки речной вызвана модификаци ей генов окраски: пят нистый (а) и полосатый (б) фенотипы

Один ген – одна полипептидная цепь Вскоре гипотеза один ген: один фермент была модифицирована. 1) стало ясно, что почти все ферменты – это белки, но далеко не все белки – ферменты. v. Было доказано, что белки кодируются генами, поэтому эта гипотеза получила название один ген: один белок. 2) белки часто состоят из субъединиц, которые содержат две или более полипептидных цепи – основу четвертичной структуры белков. Гены кодируют отдельные полипептидные цепи, поэтому современное название гипотезы Бидла и Татума – один ген : одна полипептидная цепь.

Серповидноклеточная анемия Изучение мутантных форм гемоглобина у больных серповидноклеточной анемией послужило прямым доказательством того, что гены кодируют белки. vпри низком содержании кислорода в воздухе эритроциты больных принимают вытянутую серповидную форму. v. Это связано с полимеризацией молекул гемоглобина и приводит к скоплению клеточных агрегатов в капиллярах и венах. v. В норме эритроциты имеют форму двояковыгнутых дисков. v. Из-за «слипания» эритроцитов многие органы и ткани больных, включая почки, мышцы, суставы, мозг, желудочно-кишечный тракт и легкие плохо снабжаются кислородом и повреждаются, наступает кризис, который может привести к летальному исходу.
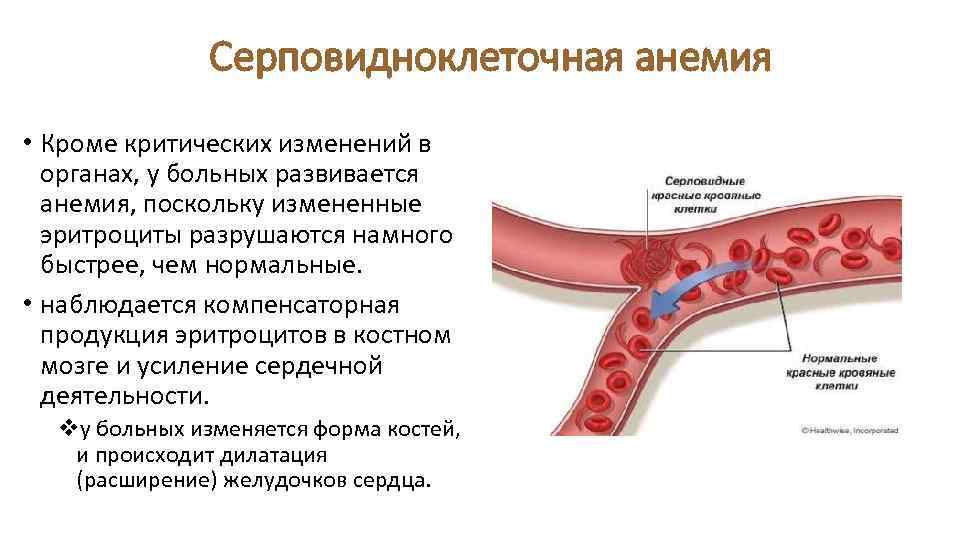
Серповидноклеточная анемия • Кроме критических изменений в органах, у больных развивается анемия, поскольку измененные эритроциты разрушаются намного быстрее, чем нормальные. • наблюдается компенсаторная продукция эритроцитов в костном мозге и усиление сердечной деятельности. vу больных изменяется форма костей, и происходит дилатация (расширение) желудочков сердца.

Серповидноклеточная анемия • В 1949 г. Джеймс Нил и Е. А. Бит показали, что серповидноклеточная анемия наследуется по Менделю. • Анализ родословных выявил три генотипа и фенотипа, контролируемые парой аллелей Hb. A и Hb. S. v. Здоровые люди имеют генотип Hb. A, vбольные серповидноклеточной анемией – генотип Hb. S. v. У гетерозигот с генотипом Hb. AHb. S половина молекул гемоглобина не изменена, поэтому признаки серповидноклеточной анемии у них выражены намного слабее.

Серповидноклеточная анемия • В 1949 г. Лайнус Полинг с сотрудниками предположили молекулярный механизм возникновения этого заболевания. • Они показали, что гемоглобин, выделенный из эритроцитов больных и здоровых доноров, имеет разную электрофоретическую подвижность. • Поллинг с сотрудниками пришли к выводу о химических различиях между молекулами гемоглобина здоровых и больных серповидноклеточной анемией. vэти формы гемоглобина были обозначены как Hb. A и Hb. S.

Серповидноклеточная анемия Из работы Поллинга следовало две возможности изменения свойств гемоглобина. • молекула гемоглобина содержит четыре небелковых железосодержащих гема и глобин, состоящий из четырех полипептидных цепей. Теоретически, изменение заряда молекулы Hb. S могло произойти за счет изменений химической структуры в любом из этих компонентов.

Серповидноклеточная анемия • В 1954 – 1957 гг. Верон Ингрэм показал, что химические изменения затрагивают первичную структуру глобиновой части молекулы гемоглобина. • При помощи фингерпринтинга он обнаружил, что аминокислотный состав молекулы Hb. S отличается от состава молекулы Hb. A. vчетвертичная структура гемоглобина у взрослых людей содержит две идентичные α-цепи по 141 аминокислоте и две одинаковые β-цепи по 146 аминокислот.

Серповидноклточная анемия • Метод фингерпринотов ( «отпечатков пальцев» ) предусматривает ферментативное расщепление белковой молекулы на отдельные пептидные фрагменты, смесь которых наносят на влажный бумажный фильтр и помещают в электрическое поле, фрагменты мигрируют на фильтре в соответствии со своим зарядом. • Затем фильтр поворачивают на 90⁰ и помещают в раствор для хроматографии, в котором фрагменты мигрируют перпендикулярно направлению их миграции в электрическом поле. Как показал Ингрэм, молекула Hb. S отличается от Hb. A только по одному пептиду. • В дальнейшем, в этом пептиде обнаружили замену единственной аминокислоты: в шестой позиции β-цепи валин замещен на глутаминовую кислоту.
Серповидноклеточная анемия Анализ структуры Hb. S подтвердил, что замещение одной аминокислоты пиводит к мутации, изменяющей фенотип.

Коллинеарность между генами и полипептидами • Когда было установлено, что гены определяют синтез полипептидных цепей, возник вопрос о том, каким образом, записанная в генах информация передается на аминокислотную последовательность полипептида. • Наиболее правдоподобно предположение о коллинеарности между молекулами ДНК и белков.

Коллинеарность между генами и полипептидами • Первые эксперементальные доказательства коллинеарности получил Чарльз Яновски, изучавший ген trp. A, кодирующий А-субъединицу триптофан-синтетазы E. coli. • Яновски изолировал множество независимых мутаций и определил локализацию мутантных сайтов в пределах одного гена. • Затем он определил аминокислотные замены в каждом из мутантных белков. • При сравнении этих данных отчетливо видна коллинеарность между геном и белком. • Локализация отдельных мутаций в гене trp. A коррелирует с соответствующими заменами в молекуле А-субъединицы триптофансинтетазы.

Структура и биологическое разнообразие белков • Полипептиды – это предшественники белков, они собираются на рибосомах в процессе трансляции. v. После выхода из рибосомы полипептид формирует более сложную складчатую структуру, а затем – трехмерную конформацию. • Обычно трехмерная конформация образована несколькими молекулами полипептидов, она функционально активна и называется протеином, или белком.

Структура и биологическое разнообразие белков • Полипептидные цепи, как и нуклеиновые кислоты, представляют собой линейные неразветвленные молекулы, построенные из 20 -ти аминокислот. • Каждая аминокислота содержит карбоксильную группу и аминогруппу, а также радикал (R), ковалентно связанный с центральным атомом углерода. • 20 радикальных групп с различной структурой можно разделить на четыре основных класса: (1) неполярные (гидрофобные), (2) полярные (гидрофильные), (3) отрицптельно заряженные (4) положительно заряженные.
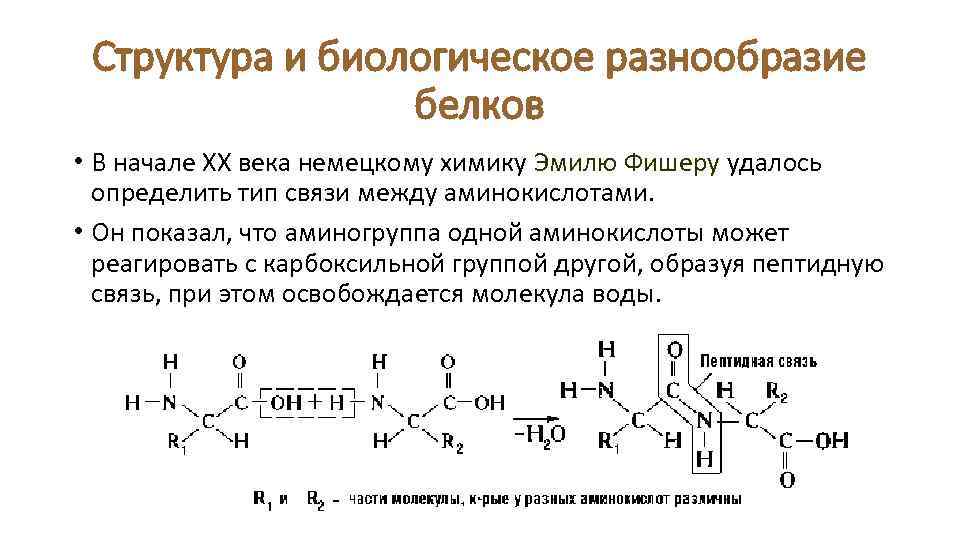
Структура и биологическое разнообразие белков • В начале ХХ века немецкому химику Эмилю Фишеру удалось определить тип связи между аминокислотами. • Он показал, что аминогруппа одной аминокислоты может реагировать с карбоксильной группой другой, образуя пептидную связь, при этом освобождается молекула воды.

Структура и биологическое разнообразие белков • Известно четыре уровня белковой структуры: vпервичная v вторичная, vтретичная vквадратичная. • Первичную структуру имеют линейные полипептиды.

Структура и биологическое разнообразие белков • Вторичная структура образуется благодаря сближению аминокислот в полипептидной цепи и появлению регулярно повторяющейся конфигурации. • В 1951 г. Лайнус Поллинг и Роберт Корей предположили, что вторичная структура белка представлена α-спиралью.

Структура и биологическое разнообразие белков • Тогда же, Полинг и Корей предположили складчатую вторичную β -структуру белка. • полипептидная цепь складывается, формируя параллельные и антипараллельные слои, которые стабилизированы благодаря водородным связям между атомами соседних цепей.

Структура и биологическое разнообразие белков большинство белков содержит смесь α-спиральных и β-складчатых структур. vфиброин – белок из желез шелкопряда – в основном, построен из складчатых полипептидов.

Структура и биологическое разнообразие белков • Третичная структура описывает трехмерную конформацию полипептидных цепей в пространстве. Для поддержания и стабилизации такой конформации молекулы белка наиболее важны три аспекта: 1. между тесно сближеными остатками цистеина образуются ковалентные дисульфидные связи, и возникает уникальная кислота цистин. 2. Практически все полярные гидрофильные радикалы локализованы на поверхности белковой молекулы, где они взаимодействуют с водой. 3. Неполярные гидрофильные группы обычно локализованы внутри молекулы белка, где они взаимодействуют друг с другом.
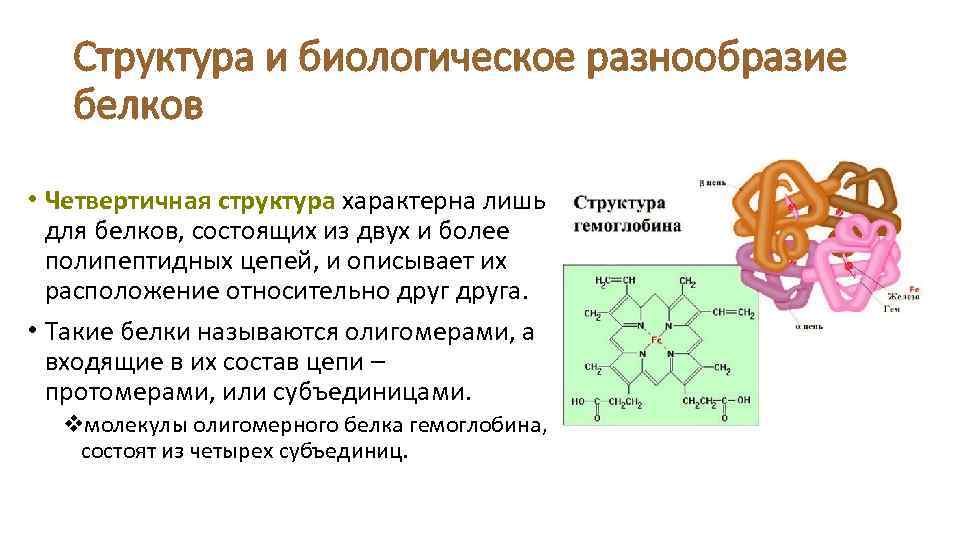
Структура и биологическое разнообразие белков • Четвертичная структура характерна лишь для белков, состоящих из двух и более полипептидных цепей, и описывает их расположение относительно друга. • Такие белки называются олигомерами, а входящие в их состав цепи – протомерами, или субъединицами. vмолекулы олигомерного белка гемоглобина, состоят из четырех субъединиц.

Посттрансляционная модификация белков 1. В молекуле полипептида обычно удаляются или модифицируются N- и С -концевые аминокислоты. • В молекулах бактериальных полипептидов ферменты часто удаляют N-концевой формилметионин. • У эукариот нередко удаляется N-концевой остаток метионина, или он химически модифицируется, подвергаясь ацетилированию. 2. Иногда модифицируются отдельные аминокислотные остатки. • к гидроксильной группе аминокислоты тирозина добавляется фосфатная группа. • В результате аминокислотный остаток несет отрицательный заряд и образует ионную связь с другими молекулами. • Фосфорилирование играет важную роль в регуляции функций ферментов, называемых киназами. • могут добавляться метильные группы. 3. Нередко к молекуле белка ковалентно присоединяются боковые цепи углеводородов. • образуются гликопротеины –класс белковых молекул, включающий многие антигенные детерминанты, например, определяющие специфичность антигенов группы кров АВ 0 у человека.

Посттрансляционная модификация белков 4. Полипептидные цепи могут укорачиваться. • инсулин транслируется в длинную молекулу, которая укорачивается ферментом до полипептида, состоящего из одной аминокислоты. 5. Удаляются сигнальные последовательности. • В N-концевой части молекул некоторых белков имеются так называемые сигнальные последовательности длиной до 30 -ти аминокислот, которые важны для локализации и функционирования белка в клетке-мишени. • молекулы белков, участвующих в секреции или входящих в состав клеточной мембраны, содержат специфические последовательности для транспорта их по эндоплазматической сети. • белки с секреторной функцией содержат на N-конце молекулы последовательность длиной до 15 -ти гидрофобных аминокислот, которая завершена положительно заряженной аминокислотой на N-конце. 6. Полипептидные цепи часто связаны с металлами. • Третичная и четвертичная структура белка часто включает атомы металлов, и функциональная активность белка зависит от комплекса полипептидных цепей, связанных с металами. • гемоглобин, содержащий четыре атома железа, связанных с четырьмя полипептидами.

Посттрансляционная модификация белков • Каким образом полипептидные цепи образуют трехмерные структуры со специфической функцией? • многочисленные исследования показывают, что это зависит от семейства белков, называемых шаперонами. • Впервые шапероны обнаружили среди белков теплового шока у Drosophila, а затем – у множества других организмов, включая бактерии, животных и растения.

Функции белков • Дыхательные пигменты гемоглобин и миоглобин переносят необходимый для клеточного метаболизма кислород. • Коллаген и кератин – структурные белки соединительной ткани, кожи и волос, • актин и миозин – сократительные белки мышечной ткани. • Иммуноглобулины функционируют в иммунной системе млекопитающих, • различные транспортные белки участвуют в прохождении молекул через мембраны. • Некоторые гормоны и их рецепторы регулируют химическую активность в клетках, • гистоны ассоциируют у эукариотов с ДНК, участвуя в организации хромосом.
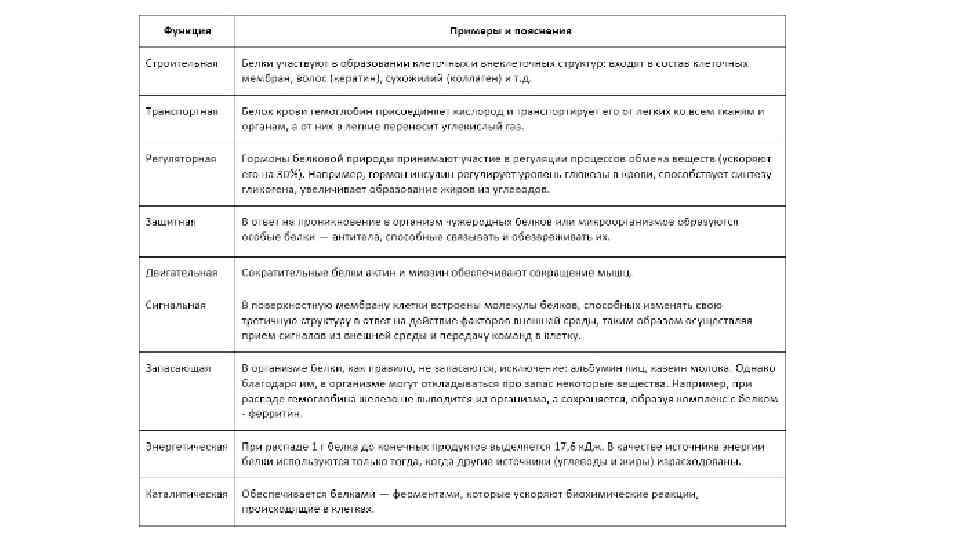
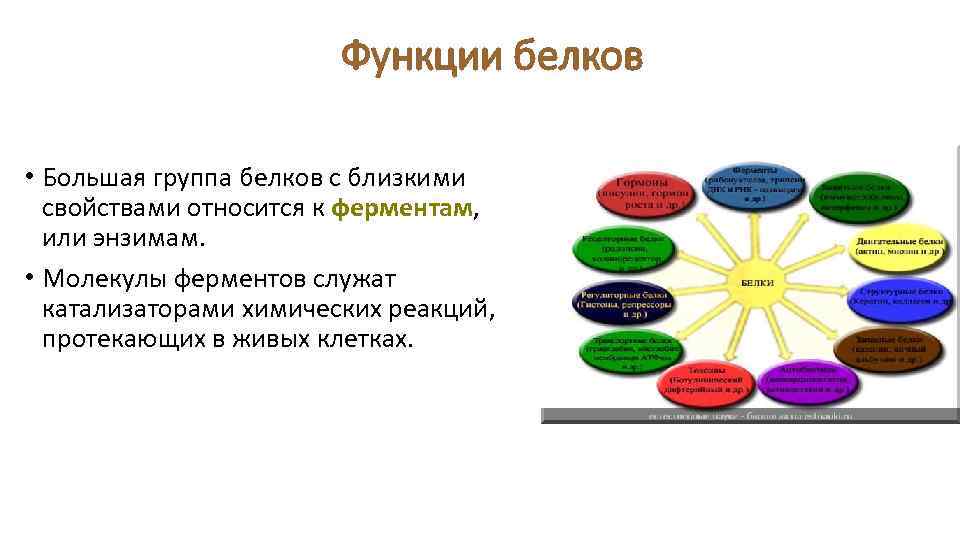
Функции белков • Большая группа белков с близкими свойствами относится к ферментам, или энзимам. • Молекулы ферментов служат катализаторами химических реакций, протекающих в живых клетках.
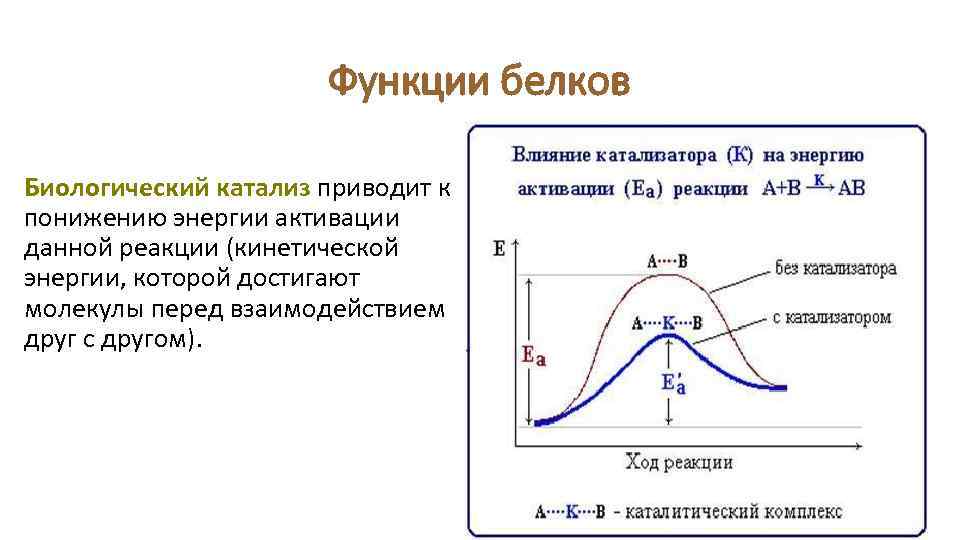
Функции белков Биологический катализ приводит к понижению энергии активации данной реакции (кинетической энергии, которой достигают молекулы перед взаимодействием друг с другом).

Функции белков Энергия активации повышается с ростом температуры, а ферментативные биологические реакции могут протекать и при более низких, физиологических температурах. Энергетическая диаграмма химической реакции без катализатора (1) и в присутствии катализатора (2).

Функции белков • Каталитические свойства ферментов и их специфичность обусловлены химической конфигурацией молекул, имеющих активные сайты. • Метаболизм клетки во многом зависит от катаболических или анаболических реакций, которые катализируют ферменты. v. Катаболизм – это распад крупных молекул на небольшие молекулы, сопровождающийся выделением энергии. v. Анаболизм – синтез различных клеточных компонентов: нуклеиновых кислот, белков, липидов и углеводов.

Белковые домены и перетасовка экзонов • Последовательности длиной от 50 до 300 аминокислот организованы в белковые домены – области белковой молекулы с уникальной стабильной конформацией, отличающейся от остальных зон этой молекулы.

Белковые домены и перетасовка экзонов • При изучении белков можно встретить такие термины, как каталитические домены, ДНК-связывающие домены и т. д. • белковая молекула состоит из отдельных структурнофункциональных модулей.

Белковые домены и перетасовка экзонов • В 1977 г. Уолтер Гильберт предложил оригинальное объяснение происхождения доменов. • Он представил функциональные области генов эукариот состоящими их серии экзонов, возникших из предковых генов путем перетасовки в ходе эволюции. • экзоны, как и белковые домены, являются модулями, которые могут рекомбинировать таким образом, что разные гены имеют сходные экзоны.

Белковые домены и перетасовка экзонов • в 1985 г. появились первые доказательства теории Гильберта. • был выделен и секвенирован человеческий ген, кодирующий мембранный рецептор липопротеинов низкой плотности (LDL). vучаствует в транспорте плазматического холетерола в клетку, служит медиатором эндоцитоза и , вероятно, содержит функционально различные домены. v. Эти домены участвуют в связывании белка с LDL-субстратами и во взаимодействии с другими белками во время транспорта липопротеинов через мембрану. • Молекула этого рецептора модифицируется после трансляции путем присоединения карбогидрата.

Белковые домены и перетасовка экзонов • Данный ген содержит 45 000 нуклеотидов и 18 экзонов, которые включают всего около 2 600 нуклеотидов. • Эти экзоны соотносятся с функциональными доменами белка и, вероятно, появились в результате рекомбинации с другими генами.

Белковые домены и перетасовка экзонов • Первый экзон кодирует сигнальную последовательность, которая удаляется до присоединения рецептора к клеточной мембране. • Следующие пять экзонов определяют специфичный сайт связывания холестерола. • Второй домен состоит из 400 аминокислот, он гомологичен эпидермальному фактору роста мышей (EGF) и кодируется 8 экзонами, содержащими три повтора по 40 аминокислот. v. Сходная последовательность найдена в экзонах, кодирующих фактор свертываемости крови. • Пятнадцатый экзон детерминирует посттрансляционное добавление карбогидратной группы, а оставшиеся экзоны служат для закрепления рецептора на особых участках клеточной мембраны.

Белковые домены и перетасовка экзонов Таким образом, структура кодирующих рецептор LDL экзонов говорит в пользу теории о перетасовке их в ходе эволюции и не противоречит тому, что специфические молекулярные взаимодействия опосредованы свойствами белковых доменов.
Translyatsia_i_belki.pptx