РХТУ_2_09.ppt
- Количество слайдов: 41

Трансгенные животные в биотехнологии Лекция 2

Что нового в 2011 г. в молекулярной генетике? 1) Проанализировали геном чумной палочки - возбудителя "Черной смерти“, эпидемии, которая произошла в XIV веке. Обнаружено, что, во- первых, за прошедшие с эпидемии 660 лет у бактерии лишь немного изменилась структура всего 12 генов (из 4200), а во-вторых, все известные сейчас штаммы чумной палочки являются потомками ныне восстановлен- ной Y. pestis. Почему же была эпидемия чумы? 2) Расшифровали геном голландки, дожившей до 115 лет без каких-либо признаков старческого слабоумия. Пока выявили у женщины ряд мутаций, связанных с пониженным риском болезни Альцгеймера, болезни Паркинсона, а также атеросклероза. Идет поиск «генов долголетия» . 3) Суицидальное поведение записано в генах человека, установили ученые, проанализировав данные, собранные в самой большой в Канаде психиатрической лечебнице. 4) Вегетарианство имеет генетическую причину и связано с наличием у человека дополнительных копий определенного гена. 5) Обнаружены «гены худых людей» .

Основные цели использования эмбриональных стволовых и i. PS клеток

Направленная дифференцировка ЭСК человека под действием различных внешних факторов

Дорзоморфин h. ESC 89% клеток дмфференциируют по нейрональному пути


Генетические модификации СК, приводящие к изменению их жизненных свойств Исходные Трансген Новые свойства Авторы клетки (продукт) ГСК СХСR 4 Увеличение длительности Brenner et al. , 2004 (рецептор культивирования, усиление хемокина) миграции в сторону стро- мального фактора МСК TERT Увеличение продолжительности Abdallah et al. , 2005 (теломераз- жизни, стабильность фенотипа ная ревертаза) ГСК HOXB 4 Усиление воспроизводства, Schmittwolf, 2005 (фактор стабилизация скорости транскрипции) пролиферации ГСК BCL-2 Повышение жизнеспособ- Orelio et al. , 2004 (антиапоптоти- ности и активности ческий фактор)

Генетически модифицированные стволовые клетки - источник для регенеративной медицины Патология Клетки/Ген Эффекты при пересадке Болезнь ЭСК мыши/bcl-XL Усиление Паркинсона (антиапоптотичекий дифференцировки в ДЭ- фактор) нейроны, увеличение выживания Рак Гемопоэтические Уменьшение размера стволовые клетки/h. RI опухоли, снижение (ингибитор рибонуклеазы) плотности кровеносных сосудов Повреждение Стромальные клетки Усиление выживаемости, спинного костного стимулирование роста мозга/BDNF аксонов нервных клеток (нейротрофный фактор) Повреждение Нейрональные Усиление выживания и

Модифицированные стволовые клетки - продуценты лекарственных средств Исходные Трансген Заболевание Авторы клетки ГСК глобиновый ген анемия Sadelain e a, 2004 ГСК аллель ГКГ кл. II диабет типа 1 Tian et al. , 2004 ЭСК ген сульфамидазы мукополисахаридоз Lau et al. , 2004 МСК ген ß-интерферона карцинома Studeny e a. , 2004 ГСК ген фактора VIII гемофилия Moayeri, 2004 ГСК ген WAS синдром Dupre et al. , 2004 Вискотт-Алдриха ГСК ген феррохелатазы протопорфирия Richard e a. , 2004

Таргетинг генов Основна методологи таргетинга генов - гомологичная рекомбинация. В результате появились возможности: 1) полностью инактивировать строго определенные гены в организме (нокаут генов), 2) вводить в гены небольшие направленные мутации и/или осуществлять коррекцию мутантных аллелей (нокин генов). Соотношение гомологичной рекомбинации к негомологичной варьирует в диапазоне 10 -3 -5

Химеры – первые «трансгенные» организмы Химера (chimera, chimaera) [греч. Chimaira — мифическое чудовище, имеющее голову льва, туловище козы и хвост дракона] — организм, состоящий из генетически неоднородных органов, тканей или клеток, которые происходят более, чем от одной оплодотворенной яйцеклетки. Термин «химера» применим к животному, полученному путем искусственного слияния эмбриональных клеток двух или более организмов, или к растению, у которого после прививки в месте срастания закладываются почки, в которых часть тканей принадлежит привою, а часть подвою. Впервые термин “Х. ” применил Г. Винклер (1907 г. ) для форм растений, полученных в результате сращивания паслёна и томата.

1 А. Тарковский, 1961 2 1 3 4 5 6 Получение агрегационных химер

Получение инъекционных химер Гарднер, 1968 г.

Что можно выяснить с помощью метода создания химер? Используя две клеточные популяции, можно проследить в онтогенезе за: - происхождением и судьбой тканей, - родословными клеток (Экспериментальная эмбриология) - как генетически различные клетки, сотрудничают и взаимодействуют между собой, создавая взрослое существо (Генетика развития). - роль отдельных генов (генный нокаут) (Молекулярная генетика)
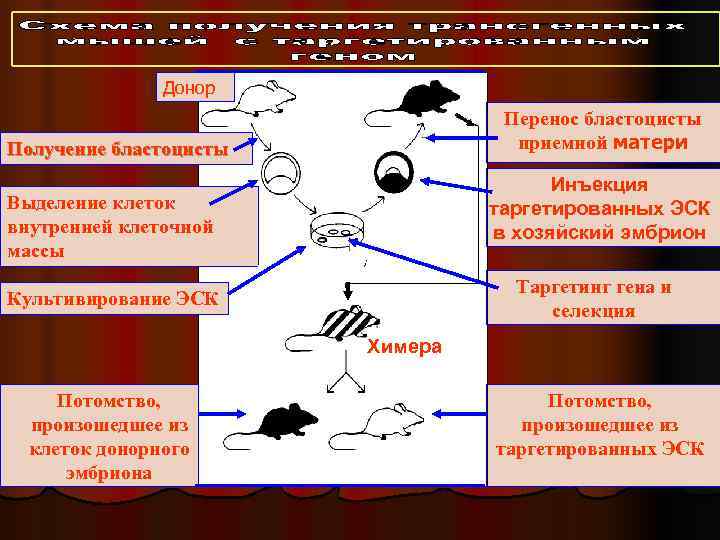
Донор Перенос бластоцисты Получение бластоцисты приемной матери Инъекция Выделение клеток таргетированных ЭСК внутренней клеточной в хозяйский эмбрион массы Таргетинг гена и Культивирование ЭСК селекция Химера мер Потомство, а Потомство, произошедшее из произошедшее из клеток донорного таргетированных ЭСК эмбриона

Два типа векторов используемых для гомологичной рекомбинации

Нокаут гена гипоксантинфосфорибозилтрансферазы (hprt) 3 4 5 6 7 8 9 Ген hprt Таргетирующий вектор neo Нокаут neo гена Селекция: Hprt- - резистентность к 6 -тиогуанину, Neo+ - резистентность к G 418

Позитивно-негативная селекция при гомологичной рекомбинации (- ) (+) (- ) трансген Вектор Хромосома Клетки, в которых не прошла гомологичная рекомбинация, выживают в присутствии G-418 и гибнут в присутствии ганцикловира Вектор Хромосома Клетки, в которых прошла гомологичная рекомбинация, выживают в присутствии G-418 и ганцикловира

Кондиционный нокут гена (Cre-lox P система) Ген Гомологичная рекомбинация Lox P Мышь № 1 Мышь № 2 с рекомбиназой Cre и + Cre Вырезание гена тканеспецифическим промотором Белок отсутствует
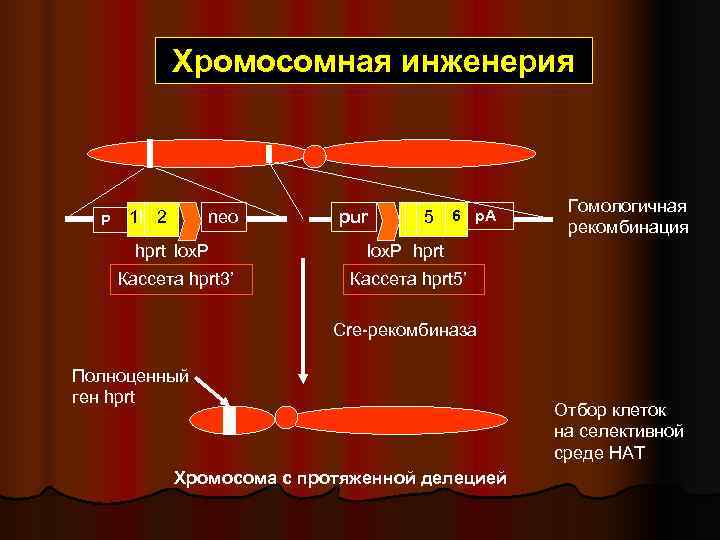
Хромосомная инженерия Гомологичная P 1 2 1 neo pur 5 6 р. А рекомбинация hprt lox. P hprt Кассета hprt 3’ Кассета hprt 5’ Cre-рекомбиназа Полноценный ген hprt Отбор клеток на селективной среде HAT Хромосома с протяженной делецией

Стратегии получения трансмитохондриальных мышей Experimental strategy used by Sligh et al Cинаптосомы Клетки без мт. ДНК Клетки с мутантной мт. ДНК Цибрид Энуклеация Цитопласт ЭСК, без митохондрий (родамин) Цибрид Трансмитохондриальные мыши
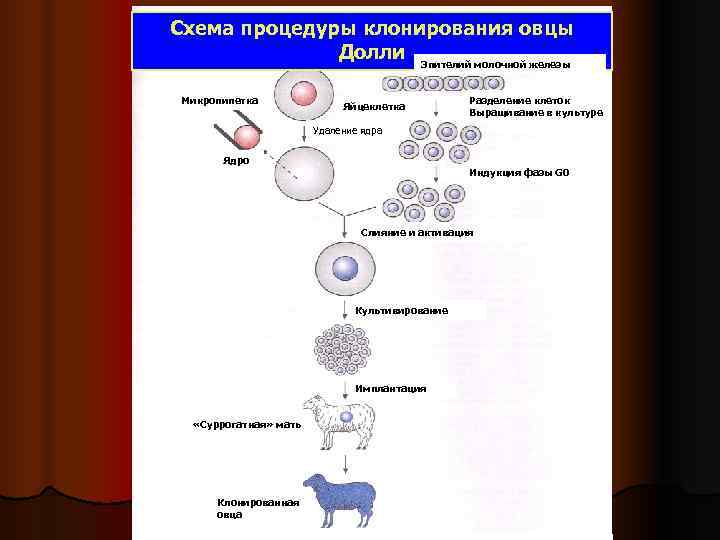
Схема процедуры клонирования овцы Долли Эпителий молочной железы Микропипетка Разделение клеток Яйцеклетка Выращивание в культуре Удаление ядра Ядро Индукция фазы G 0 Слияние и активация Культивирование Имплантация «Суррогатная» мать Клонированная овца

Создание трансгенных клонов Культура клеток Ооцит коровы 2 трансгенной коровы 1 Перенос трансгенного ядра в энуклеированный ооцит Энуклеирование Селекция клетки Перенос гена в культуру Развитие эмбриона Имплантация суррагатной матери Трансгенный клон коровы 1

Клонированные трансгенные с/х животные-биореакторы Вид Трансген Автор Кролик -гликозидаза Van den Hout e a. , 2000 Овца фактор IX Schnieke et al. , 1999 альфа 1 -антитрипсин Mc. Creath et al. , 2000 Свинья комплемент CD 59 Imaizumi et al. , 2000 N-ацетилглюкозоамин- Fujimura et al. , 2004 трансфераза III Коза антитромбин Baguisi et al. , 1999 Коза моноклональные АТ Biotherapeuticus Коза белок шолка паука Biotherapeuticus

Моделирование заболеваний человека с помощью разных вариантов трансгеноза Выявление генов, участвующих в лимфомогенезе, с помощью традиционных трансгенных мышей Cellular genes in transgenic mice accelerated lymphomas ____________________________________ Transgene Function Type of lymphoma References (promoter-gene) of protein ____________________________________ Em-c-myc Transcription factor, B cell Adams et al. , 1985 multifunctional oncoprotein CD 2 -c-my Transcription factor, T-cell Webster et al. , 1997 multifunctional oncoprotein Em-N-myc Transcription factor, B cell Sheppard et al. , 1998 apoptosis lck-bcl 2 Oncoprotein blocking T cell Linette et al. , 1995 vav-bcl 2 Oncoprotein blocking B cell, FL Egle et al. , 2003 lck-bax Protein promoting apoptosis B cell Luke et al. , 2003 MMTV-N-ras Transmembrane oncoprotein B cells Mangues et al. , 1996 Em-pim 1 Serine/threonine kinase T cell Breuer et al. , 1989 b

Синергизм действия генов в лимфомогенезе, 3. Oncogene synergy in accelerated transgenic lymphomas detected установленный с использованием двойных трансгенных by transgenic cross (double transgenic mice). мышей Transgene Synergistic gene Type of lymphoma References __________________________________ c-myc v-abl Pre-B cell Adams, Cory, 1991 c-myc pim 1 Pre-B cell Verbeek et al. , 1991 c-myc pim 2 T cell Allen et al. , 1997 c-myc N-ras Pro-B, pre-B cell Adams, Cory, 1991 c-myc bcl 2 B cell Marin et al. , 1995 c-myc cbfa 1 B cell Vaillant et al. , 1999 c- myc EBNA-1 B cell Drotar et al. , 2003 c-myc runx-2 T cell Cameron et al. , 2003 c-myc cyclin D pre-B and B cells Lovec et al. , 1994 c-myc CKIIa lymphocytic leukemia Seldin, Leder, 1995

Синергизм действия генов в лимфомогенезе, 4. Oncogene synergy in accelerated transgenic установленный с помощью инсерций провирусов в геном трансгенных мышей lymphomas detected by proviral insertions __________________________________________ Transgene Synergistic gene Type of lymphoma ____________________________________ c-myc bmi 1, pim 1 Pre-B cell c-myc p 53 B-cell c-myc til 1 T cell c-myc v-myb T cell c-myc runx 1 T cell c-myc runx 2 T cell c-myc frat 1 T cell c-myc bmi 1, gfi 1 T cell c-myc notch 1 T cell c-myc syndecan 4 T cell

2. Gene knockout inducing lymphomagenesis in mice Выявление генов, препятствующих лимфомогенезу, с помощью генного нокаута Knockout Function of protein Type of References gene lymphoma p 53 Transcriptional factor В and T cell Ward et al. , 1999 E 2 A Transcriptional factor T cell Yan et al. , 1997 N-ras Small GTPase T cell Diaz et al. , 2002 RARalpha Retinoic acid receptor В and T cell Haidar et al. , 2000 pms 2 DNA mismatch repair T cell Qin et al. , 1999 snf 5 Transcriptional factor T cell Roberts et al. , 2002 PTEN Lipid phosphatase T cell Suzuki et. , 2001 atm Phosphatidylinositol 3 -kinase T cell Xu et al. , 1996 msh 2 Mismatch repair protein T cell Zhang et al. , 2002 msh 6 Mismatch repair protein T cell de Wind et al. , 1999 53 BR 1 p 53 binding protein T cell Ward et al. , 2003 IFN-gamma Interferon gamma, cytokine B cell Street et al. , 2002

Синергизм между нокаутированными генами у дважды и трижды нокаутированных мышей

Генная терапия ex in vivo vivo Терапевтический ген Размножение клеток in vitro

Клинические испытания по генной терапии (2009 г. )

Генная терапия некоторых заболеваний человека Заболевание Вектор Ген Болезнь Паркинсона RV декарбоксилаза глутаминовой ы кислоты Гемофилия AAV фактор IX Грануломатоз RV GP 91 Острый иммунодефицит RV рецептор интерлейкина 2 Дефицит орнитинтранскарбамилазы Ad c. DNA OTC Врождённый амавроз Лебера RV RPE 65 Ишемия нижних конечностей Ad ангиогенин, VEGF

Типы генов, используемых при генной терапиии


Генная терапия опухолей с использованием клеток иммунной системы, нагруженных рекомбинантными онколитическими вирусами Опухоль Клетки с вирусами Вирусы Вирус болезни Ньюкасла, рекомбинантные аденовирусы, реовирусы, вирус простого герпеса

Принцип использования для терапии рака гена-убийцы (фермент тимидинкиназы вируса простого герпеса, HSV-tk)

Направленное подавление работы гена – другой подход к лечению. Достигается с помощью: 1) Антисмысловых РНК 2) Рибозимов 3) РНК- и ДНК-аптамеров 4) Белковых аптамеров 5) РНК-интерференции 6) Нокаута гена

Схема получения ДНК-аптамеров Комбинаторная библиотека олигонуклеотидов (1015) Обогащенная фракция Связывание ПЦР Колонка с Несколько «пришитым» циклов белком- Связавшиес мишенью я молекулы Элюция Несвязавшиеся молекулы (отбрасываются) SELEX (англ. systematic evolution of ligands by exponential enrichment – систематическая эволюция лигандов при экспоненциальном обогащении)

Схема подавления работы гена с помощью РНК-интерференции i. РНК

Генная терапия некоторых заболеваний человека Заболевание Вектор Ген Болезнь Паркинсона RV декарбоксилаза глутаминовой ы кислоты Гемофилия AAV фактор IX Грануломатоз RV GP 91 Острый иммунодефицит RV рецептор интерлейкина 2 Дефицит орнитинтранскарбамилазы Ad c. DNA OTC Врождённый амавроз Лебера RV RPE 65 Ишемия нижних конечностей Ad ангиогенин, VEGF

Генно-клеточная терапия l Стволовые нейрональные клетки, экспрессирующие VEGF, - при инсульте l Эмбриональные стволовые клетки, экспрессиирующие VEGF и L 1 CAM, – при боковом амиотрофическом склерозе l Мезенхимные стволовые клетки, экспрессирующие сурвивин, - при инсульте l Гематопоэтические стволовые клетки, экспрессирующие аденозиндеаминазу, - при остром комбинированном иммунодефиците
РХТУ_2_09.ppt