биотехнология 5.ppt
- Количество слайдов: 55
 Трансгенные растения для научных целей
Трансгенные растения для научных целей
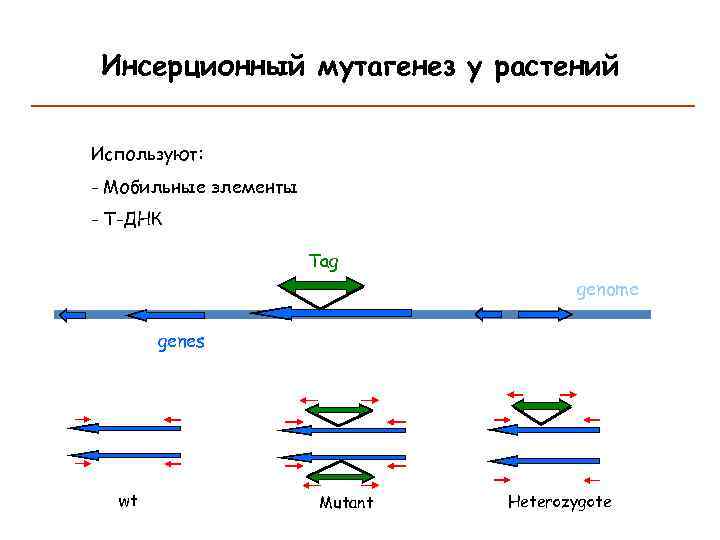 Инсерционный мутагенез у растений Используют: - Мобильные элементы - T-ДНК Tag genome genes wt Mutant Heterozygote
Инсерционный мутагенез у растений Используют: - Мобильные элементы - T-ДНК Tag genome genes wt Mutant Heterozygote
 Получение инсерционных мутантов растений на основе агробактериальной трансформации
Получение инсерционных мутантов растений на основе агробактериальной трансформации
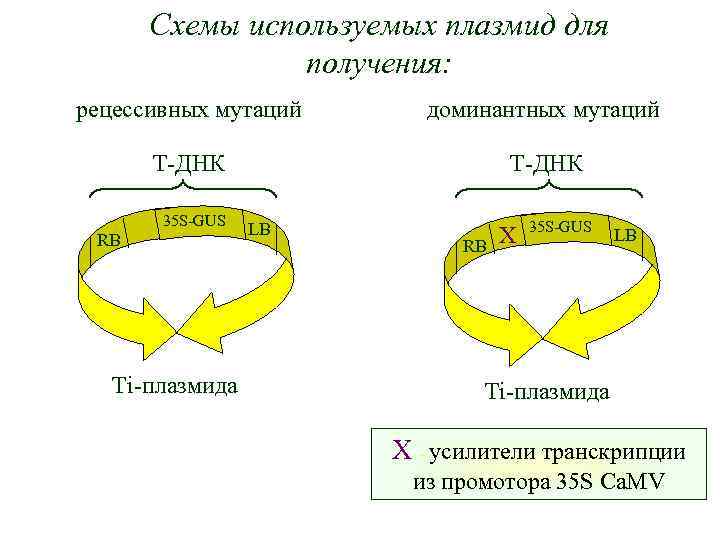 Схемы используемых плазмид для получения: рецессивных мутаций доминантных мутаций T-ДНК 35 S-GUS RB Ti-плазмида LB RB X 35 S-GUS LB Ti-плазмида X - усилители транскрипции из промотора 35 S Ca. MV
Схемы используемых плазмид для получения: рецессивных мутаций доминантных мутаций T-ДНК 35 S-GUS RB Ti-плазмида LB RB X 35 S-GUS LB Ti-плазмида X - усилители транскрипции из промотора 35 S Ca. MV
 Клонирование генов
Клонирование генов
 Т-ДНК инсерционный мутагенез интеграция Т -ДНК изменение структуры одного из генов за счет встраивания Т-ДНК… …. отбор по измененному фенотипу
Т-ДНК инсерционный мутагенез интеграция Т -ДНК изменение структуры одного из генов за счет встраивания Т-ДНК… …. отбор по измененному фенотипу
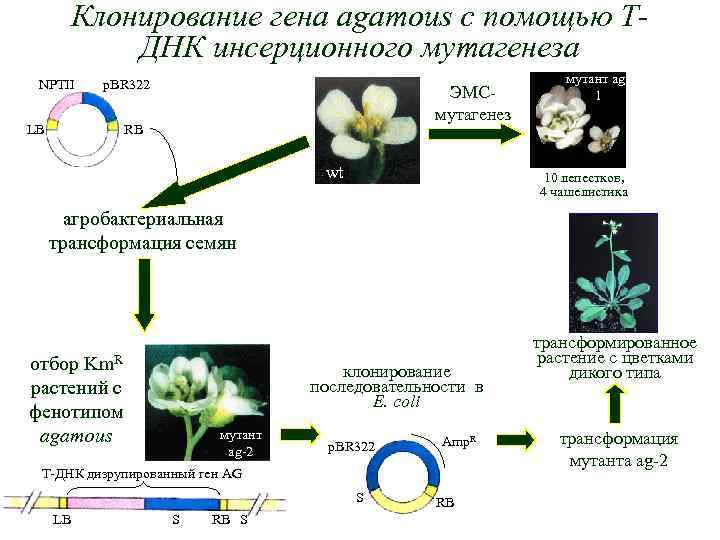 Клонирование гена agamous с помощью ТДНК инсерционного мутагенеза NPTII p. BR 322 ЭМСмутагенез RB LB wt мутант ag 1 10 лепестков, 4 чашелистика агробактериальная трансформация семян Km. R отбор растений с фенотипом agamous клонирование последовательности в E. coli мутант ag-2 p. BR 322 Amp. R T-ДНК дизрупированный ген AG S LB S RB трансформированное растение с цветками дикого типа трансформация мутанта ag-2
Клонирование гена agamous с помощью ТДНК инсерционного мутагенеза NPTII p. BR 322 ЭМСмутагенез RB LB wt мутант ag 1 10 лепестков, 4 чашелистика агробактериальная трансформация семян Km. R отбор растений с фенотипом agamous клонирование последовательности в E. coli мутант ag-2 p. BR 322 Amp. R T-ДНК дизрупированный ген AG S LB S RB трансформированное растение с цветками дикого типа трансформация мутанта ag-2
 Мобильные генетические элементы, их характеристика и применение в биотехнологии
Мобильные генетические элементы, их характеристика и применение в биотехнологии
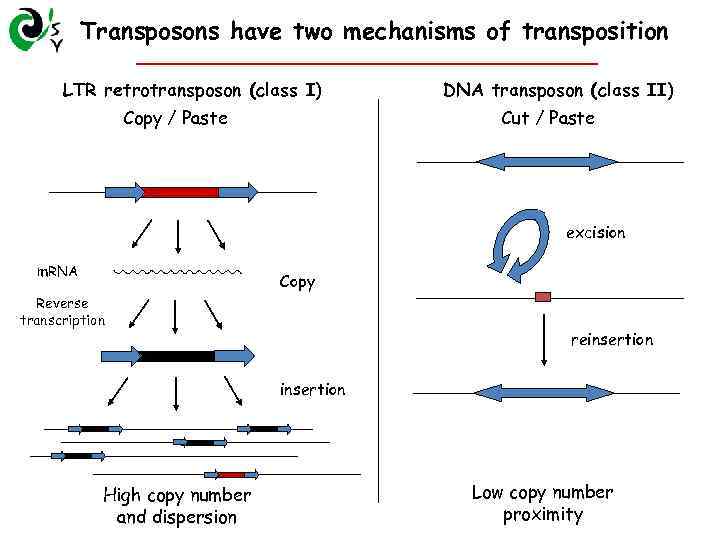 Transposons have two mechanisms of transposition LTR retrotransposon (class I) Copy / Paste DNA transposon (class II) Cut / Paste excision m. RNA Copy Reverse transcription reinsertion High copy number and dispersion Low copy number proximity
Transposons have two mechanisms of transposition LTR retrotransposon (class I) Copy / Paste DNA transposon (class II) Cut / Paste excision m. RNA Copy Reverse transcription reinsertion High copy number and dispersion Low copy number proximity
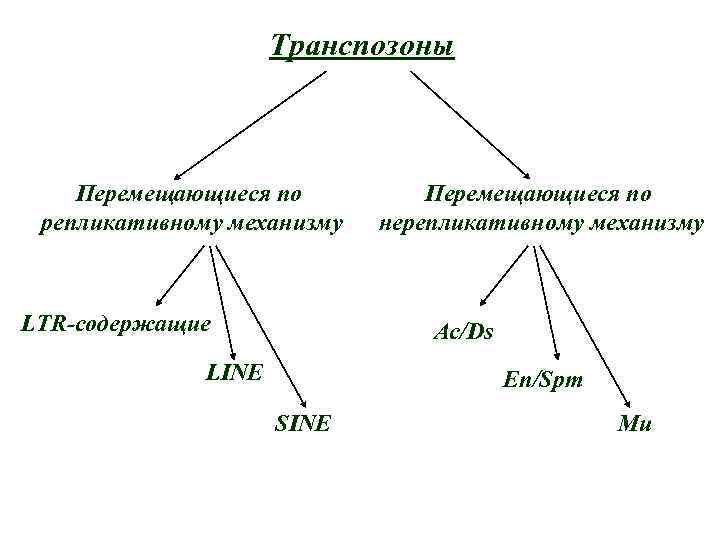 Транспозоны Перемещающиеся по репликативному механизму LTR-содержащие Перемещающиеся по нерепликативному механизму Ac/Ds LINE En/Spm SINE Mu
Транспозоны Перемещающиеся по репликативному механизму LTR-содержащие Перемещающиеся по нерепликативному механизму Ac/Ds LINE En/Spm SINE Mu
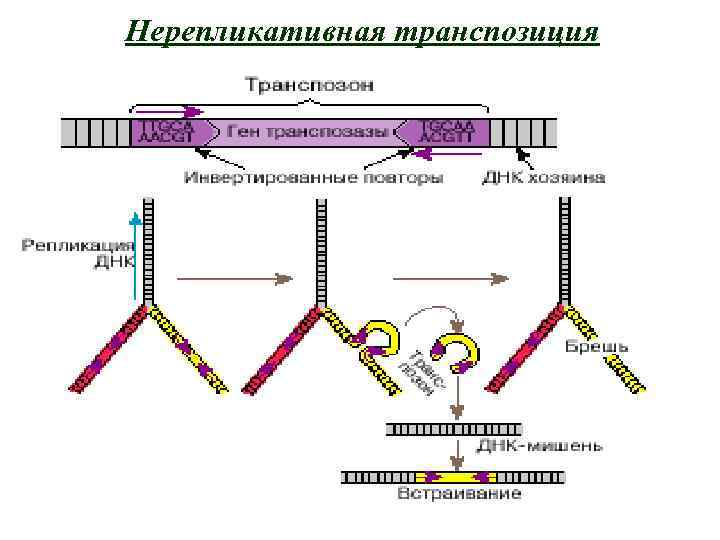 Нерепликативная транспозиция
Нерепликативная транспозиция
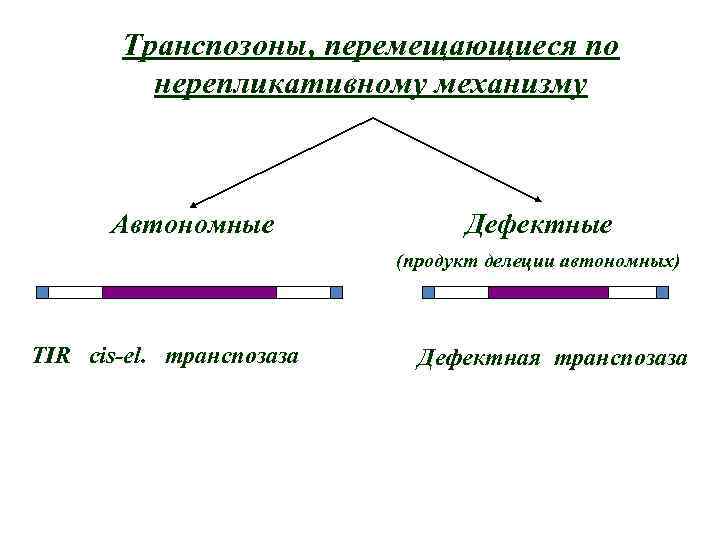 Транспозоны, перемещающиеся по нерепликативному механизму Автономные Дефектные (продукт делеции автономных) TIR cis-el. транспозаза Дефектная транспозаза
Транспозоны, перемещающиеся по нерепликативному механизму Автономные Дефектные (продукт делеции автономных) TIR cis-el. транспозаза Дефектная транспозаза
 При встраивании транспозона в кодирующую последовательность гена, наблюдается мутантный фенотип. При вырезании фенотип восстанавливается
При встраивании транспозона в кодирующую последовательность гена, наблюдается мутантный фенотип. При вырезании фенотип восстанавливается
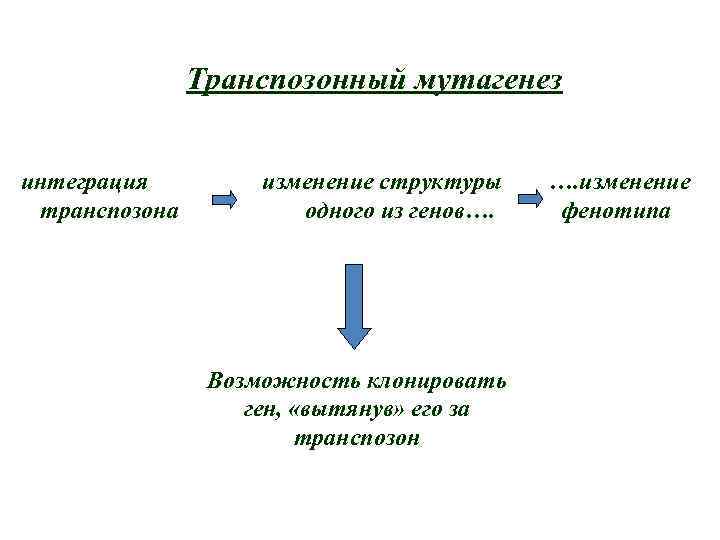 Транспозонный мутагенез интеграция транспозона изменение структуры одного из генов…. Возможность клонировать ген, «вытянув» его за транспозон …. изменение фенотипа
Транспозонный мутагенез интеграция транспозона изменение структуры одного из генов…. Возможность клонировать ген, «вытянув» его за транспозон …. изменение фенотипа
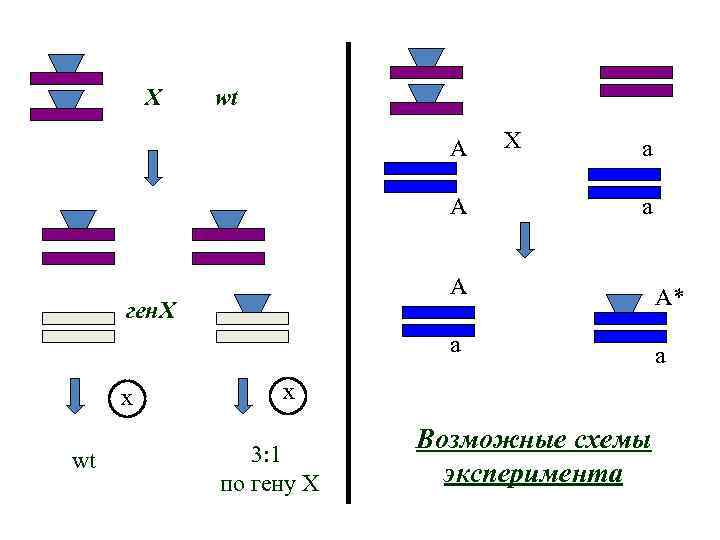 Х wt A A X a a A x wt A* a ген. Х a x 3: 1 по гену Х Возможные схемы эксперимента
Х wt A A X a a A x wt A* a ген. Х a x 3: 1 по гену Х Возможные схемы эксперимента
 Клонирование генов на основе транспозонного (инсерционного) мутагенеза Antirrhinum majus (L. ) wild type floricaula у мутанта floricaula (flo) вместо цветков развиваются побеги
Клонирование генов на основе транспозонного (инсерционного) мутагенеза Antirrhinum majus (L. ) wild type floricaula у мутанта floricaula (flo) вместо цветков развиваются побеги
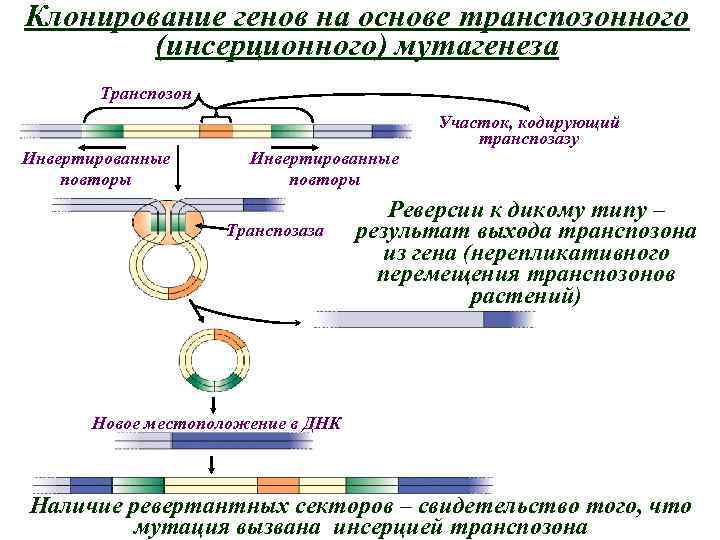 Клонирование генов на основе транспозонного (инсерционного) мутагенеза Транспозон Участок, кодирующий транспозазу Инвертированные повторы Транспозаза Реверсии к дикому типу – результат выхода транспозона из гена (нерепликативного перемещения транспозонов растений) Новое местоположение в ДНК Наличие ревертантных секторов – свидетельство того, что мутация вызвана инсерцией транспозона
Клонирование генов на основе транспозонного (инсерционного) мутагенеза Транспозон Участок, кодирующий транспозазу Инвертированные повторы Транспозаза Реверсии к дикому типу – результат выхода транспозона из гена (нерепликативного перемещения транспозонов растений) Новое местоположение в ДНК Наличие ревертантных секторов – свидетельство того, что мутация вызвана инсерцией транспозона
 Получение мутации flo 613 и клонирование гена FLORICAULA львиного зева (Coen et al. , 1990) 1. Выращивание 26 000 растений львиного зева с активным мобильным элементом Tam 3 (Transposone of Antirrhinum majus) при tº=15ºC, вызывающей наибольшую частоту транспозиций (растения М 1). 2. Самоопыление растений М 1 с целью выявления рецессивных мутаций, возникших в М 1 в результате перемещения Tam 3. 3. Выявление 15 разных гомеозисных мутаций среди 80 000 растений М 2, в том числе и flo 613. 4. Укоренение и вегетативное размножение веточек мутанта flo 613 при tº=15ºC, для выявления реверсий. Генетический анализ.
Получение мутации flo 613 и клонирование гена FLORICAULA львиного зева (Coen et al. , 1990) 1. Выращивание 26 000 растений львиного зева с активным мобильным элементом Tam 3 (Transposone of Antirrhinum majus) при tº=15ºC, вызывающей наибольшую частоту транспозиций (растения М 1). 2. Самоопыление растений М 1 с целью выявления рецессивных мутаций, возникших в М 1 в результате перемещения Tam 3. 3. Выявление 15 разных гомеозисных мутаций среди 80 000 растений М 2, в том числе и flo 613. 4. Укоренение и вегетативное размножение веточек мутанта flo 613 при tº=15ºC, для выявления реверсий. Генетический анализ.
 Ген, маркированный транспозоном (tagged gene), можно клонировать с помощью «вытягивания за транспозон»
Ген, маркированный транспозоном (tagged gene), можно клонировать с помощью «вытягивания за транспозон»
 Создание геномной библиотеки из мутанта flo 613, выращиваемого при tº=25ºC (Тam 3 не перемещается) Вставка растительной ДНК Ген для цветной селекции Изоляция ДНК Изоляция векторной ДНК Рестрикция; Комбинирование растительной и векторной ДНК; Лигирование Вставка растительной ДНК, содержащей ген интереса Amp. R (ген устойчивости к антибиотику) Рост бактерии Трансформация бактерии
Создание геномной библиотеки из мутанта flo 613, выращиваемого при tº=25ºC (Тam 3 не перемещается) Вставка растительной ДНК Ген для цветной селекции Изоляция ДНК Изоляция векторной ДНК Рестрикция; Комбинирование растительной и векторной ДНК; Лигирование Вставка растительной ДНК, содержащей ген интереса Amp. R (ген устойчивости к антибиотику) Рост бактерии Трансформация бактерии
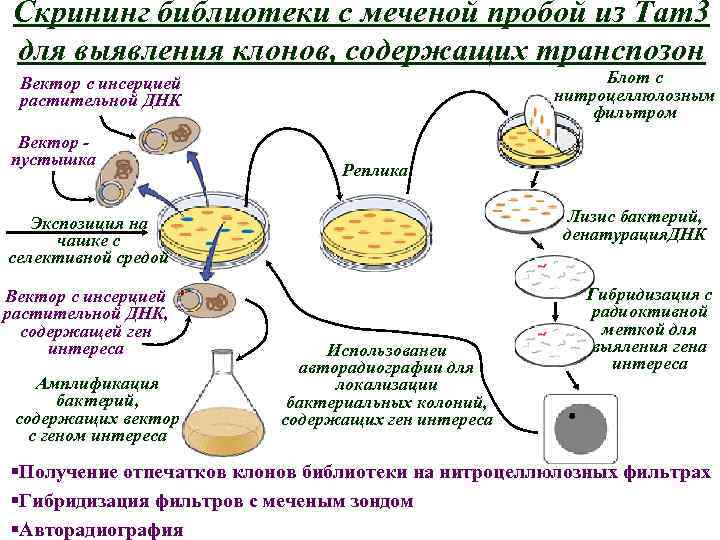 Скрининг библиотеки с меченой пробой из Tam 3 для выявления клонов, содержащих транспозон Блот с нитроцеллюлозным фильтром Вектор с инсерцией растительной ДНК Вектор пустышка Реплика Лизис бактерий, денатурация. ДНК Экспозиция на чашке с селективной средой Вектор с инсерцией растительной ДНК, содержащей ген интереса Амплификация бактерий, содержащих вектор с геном интереса Использованеи авторадиографии для локализации бактериальных колоний, содержащих ген интереса Гибридизация с радиоктивной меткой для выяления гена интереса §Получение отпечатков клонов библиотеки на нитроцеллюлозных фильтрах §Гибридизация фильтров с меченым зондом §Авторадиография
Скрининг библиотеки с меченой пробой из Tam 3 для выявления клонов, содержащих транспозон Блот с нитроцеллюлозным фильтром Вектор с инсерцией растительной ДНК Вектор пустышка Реплика Лизис бактерий, денатурация. ДНК Экспозиция на чашке с селективной средой Вектор с инсерцией растительной ДНК, содержащей ген интереса Амплификация бактерий, содержащих вектор с геном интереса Использованеи авторадиографии для локализации бактериальных колоний, содержащих ген интереса Гибридизация с радиоктивной меткой для выяления гена интереса §Получение отпечатков клонов библиотеки на нитроцеллюлозных фильтрах §Гибридизация фильтров с меченым зондом §Авторадиография
 • Выявление участков растительной фланкирующих транспозон ДНК, • Субклонирование растительной ДНК с целью дальнейшего использования в качестве зонда • Создание геномной библиотеки из растений дикого типа • Скрининг библиотеки с меченым зондом растительной ДНК, фланкирующей транспозон, для выявления клона, содержащего ген FLO • Доказательство того, что выявленные клоны содержат ген FLO
• Выявление участков растительной фланкирующих транспозон ДНК, • Субклонирование растительной ДНК с целью дальнейшего использования в качестве зонда • Создание геномной библиотеки из растений дикого типа • Скрининг библиотеки с меченым зондом растительной ДНК, фланкирующей транспозон, для выявления клона, содержащего ген FLO • Доказательство того, что выявленные клоны содержат ген FLO
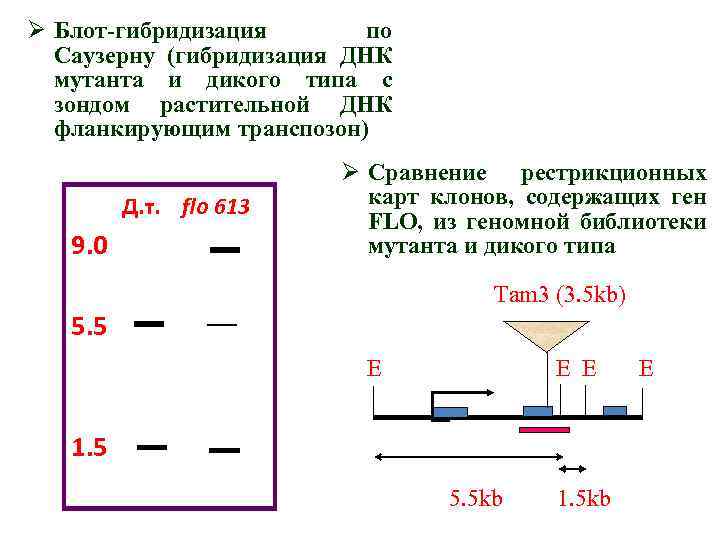 Ø Блот-гибридизация по Саузерну (гибридизация ДНК мутанта и дикого типа с зондом растительной ДНК фланкирующим транспозон) Д. т. flo 613 9. 0 Ø Сравнение рестрикционных карт клонов, содержащих ген FLO, из геномной библиотеки мутанта и дикого типа Tam 3 (3. 5 kb) 5. 5 Е Е Е 1. 5 5. 5 kb 1. 5 kb Е
Ø Блот-гибридизация по Саузерну (гибридизация ДНК мутанта и дикого типа с зондом растительной ДНК фланкирующим транспозон) Д. т. flo 613 9. 0 Ø Сравнение рестрикционных карт клонов, содержащих ген FLO, из геномной библиотеки мутанта и дикого типа Tam 3 (3. 5 kb) 5. 5 Е Е Е 1. 5 5. 5 kb 1. 5 kb Е
 Ген FLORICAULA – уникальный ген, присутствующий в геноме покрытосеменных в 1 копии. Он кодирует белок, содержащий домены, характерные для белков – активаторов транскрипции (транскрипци-онных факторов): богатый пролином домен на N-конце и кислую область в середине белка. Наиболее активная экспрессия гена FLORICAULA наблюдается в закладывающихся примордиях цветка. Клонирование гена открывает возможность для изучения роли кодируемого им белка и м. РНК во взаимодействии клеток
Ген FLORICAULA – уникальный ген, присутствующий в геноме покрытосеменных в 1 копии. Он кодирует белок, содержащий домены, характерные для белков – активаторов транскрипции (транскрипци-онных факторов): богатый пролином домен на N-конце и кислую область в середине белка. Наиболее активная экспрессия гена FLORICAULA наблюдается в закладывающихся примордиях цветка. Клонирование гена открывает возможность для изучения роли кодируемого им белка и м. РНК во взаимодействии клеток
 Гетерологичные системы 1. Изменение активности по сравнению с «родным» видом 2. Ac активен в томатах и табаке, но не в арабидопсисе 3. Эффект гетерологичного промотора на экспрессию транспозазы 4. Эффект условий культивирования
Гетерологичные системы 1. Изменение активности по сравнению с «родным» видом 2. Ac активен в томатах и табаке, но не в арабидопсисе 3. Эффект гетерологичного промотора на экспрессию транспозазы 4. Эффект условий культивирования
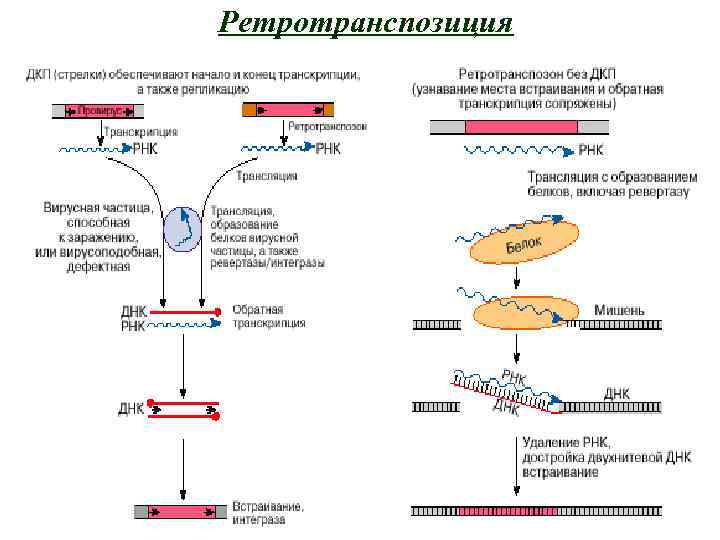 Ретротранспозиция
Ретротранспозиция
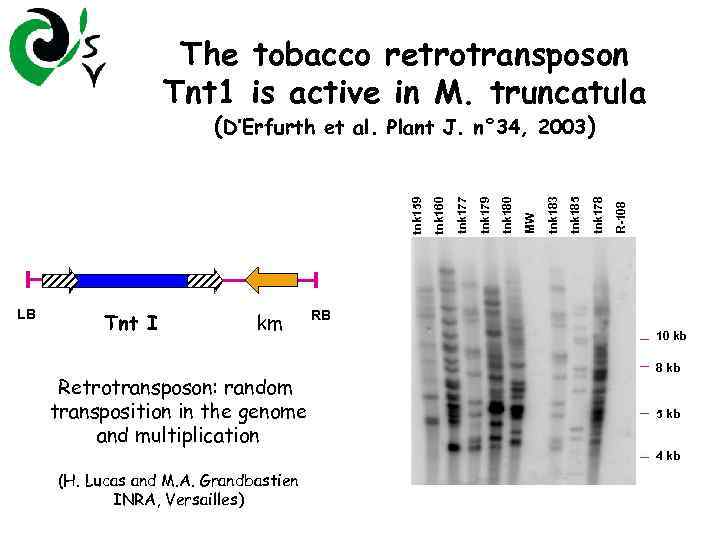 The tobacco retrotransposon Tnt 1 is active in M. truncatula LB Tnt I km Retrotransposon: random transposition in the genome and multiplication R-108 tnk 178 tnk 185 tnk 183 MW tnk 180 tnk 179 tnk 177 tnk 160 tnk 159 (D’Erfurth et al. Plant J. n° 34, 2003) RB 10 kb 8 kb 5 kb 4 kb (H. Lucas and M. A. Grandbastien INRA, Versailles)
The tobacco retrotransposon Tnt 1 is active in M. truncatula LB Tnt I km Retrotransposon: random transposition in the genome and multiplication R-108 tnk 178 tnk 185 tnk 183 MW tnk 180 tnk 179 tnk 177 tnk 160 tnk 159 (D’Erfurth et al. Plant J. n° 34, 2003) RB 10 kb 8 kb 5 kb 4 kb (H. Lucas and M. A. Grandbastien INRA, Versailles)
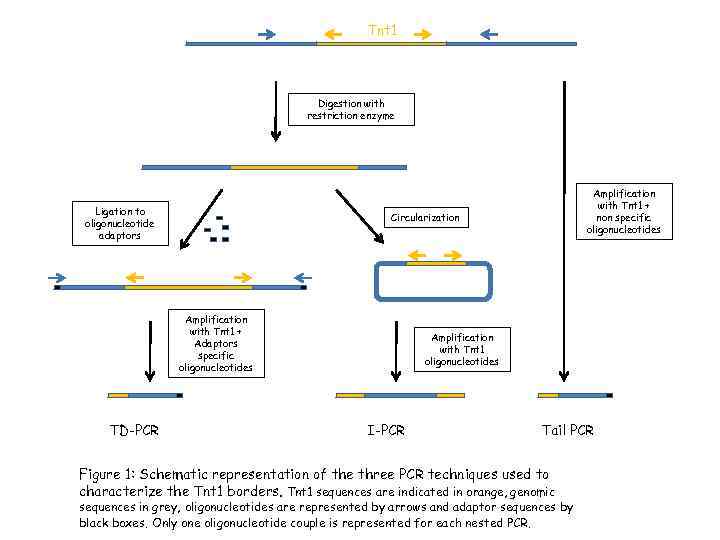 Tnt 1 Digestion with restriction enzyme Ligation to oligonucleotide adaptors Circularization Amplification with Tnt 1 + Adaptors specific oligonucleotides TD-PCR Amplification with Tnt 1 + non specific oligonucleotides Amplification with Tnt 1 oligonucleotides I-PCR Tail PCR Figure 1: Schematic representation of the three PCR techniques used to characterize the Tnt 1 borders. Tnt 1 sequences are indicated in orange, genomic sequences in grey, oligonucleotides are represented by arrows and adaptor sequences by black boxes. Only one oligonucleotide couple is represented for each nested PCR.
Tnt 1 Digestion with restriction enzyme Ligation to oligonucleotide adaptors Circularization Amplification with Tnt 1 + Adaptors specific oligonucleotides TD-PCR Amplification with Tnt 1 + non specific oligonucleotides Amplification with Tnt 1 oligonucleotides I-PCR Tail PCR Figure 1: Schematic representation of the three PCR techniques used to characterize the Tnt 1 borders. Tnt 1 sequences are indicated in orange, genomic sequences in grey, oligonucleotides are represented by arrows and adaptor sequences by black boxes. Only one oligonucleotide couple is represented for each nested PCR.

 Изучение с помощью трансгенных растений экспрессии генов и структуры растительных промоторов
Изучение с помощью трансгенных растений экспрессии генов и структуры растительных промоторов
 Изучение механизмов регуляции экспрессии генов растений с использованием репортерных (индикаторных) генов Возможности метода: 1) Выявление факторов (внешних и внутренних), определяющих особенности экспрессии исследуемого гена 2) Выявление цис-регуляторных элементов гена, отвечающих на действие внешних и внутренних факторов
Изучение механизмов регуляции экспрессии генов растений с использованием репортерных (индикаторных) генов Возможности метода: 1) Выявление факторов (внешних и внутренних), определяющих особенности экспрессии исследуемого гена 2) Выявление цис-регуляторных элементов гена, отвечающих на действие внешних и внутренних факторов
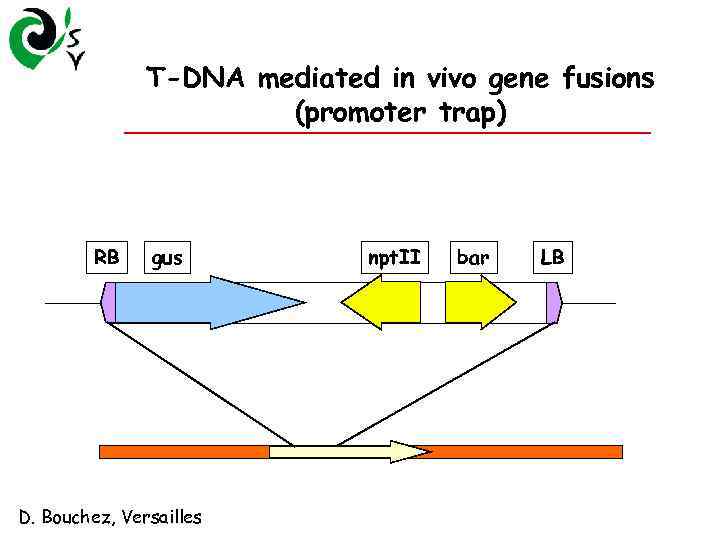 T-DNA mediated in vivo gene fusions (promoter trap) RB gus D. Bouchez, Versailles npt. II bar LB
T-DNA mediated in vivo gene fusions (promoter trap) RB gus D. Bouchez, Versailles npt. II bar LB
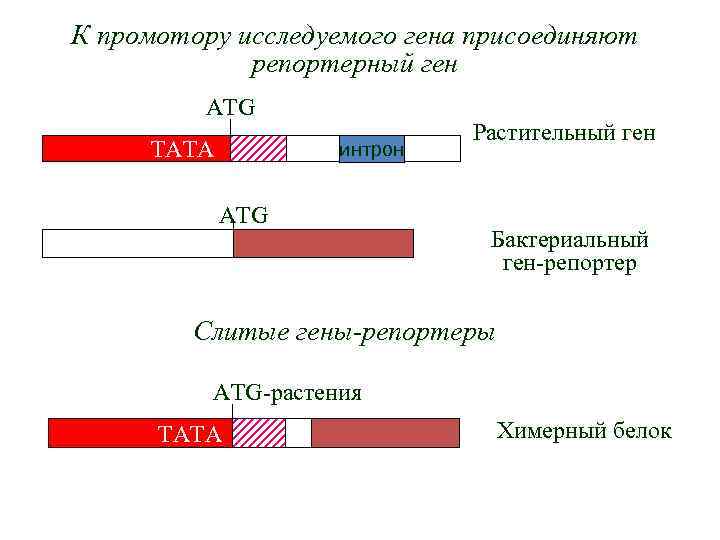 К промотору исследуемого гена присоединяют репортерный ген ATG ТАТА интрон ATG Растительный ген Бактериальный ген-репортер Слитые гены-репортеры ATG-растения ТАТА Химерный белок
К промотору исследуемого гена присоединяют репортерный ген ATG ТАТА интрон ATG Растительный ген Бактериальный ген-репортер Слитые гены-репортеры ATG-растения ТАТА Химерный белок
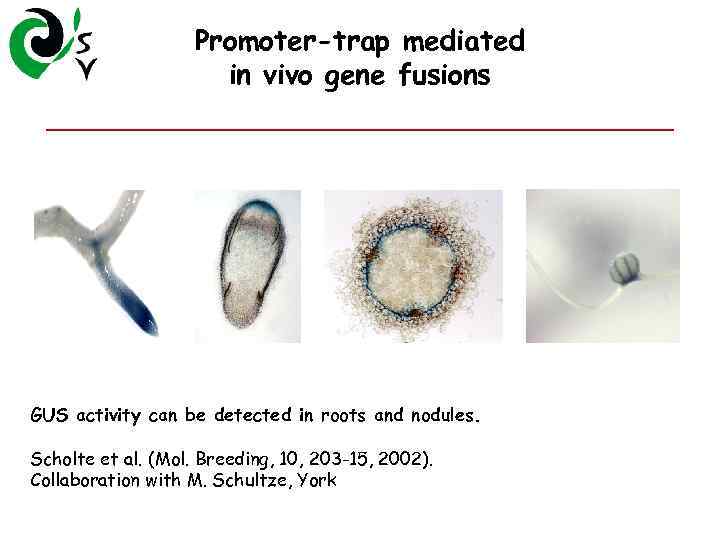 Promoter-trap mediated in vivo gene fusions GUS activity can be detected in roots and nodules. Scholte et al. (Mol. Breeding, 10, 203 -15, 2002). Collaboration with M. Schultze, York
Promoter-trap mediated in vivo gene fusions GUS activity can be detected in roots and nodules. Scholte et al. (Mol. Breeding, 10, 203 -15, 2002). Collaboration with M. Schultze, York
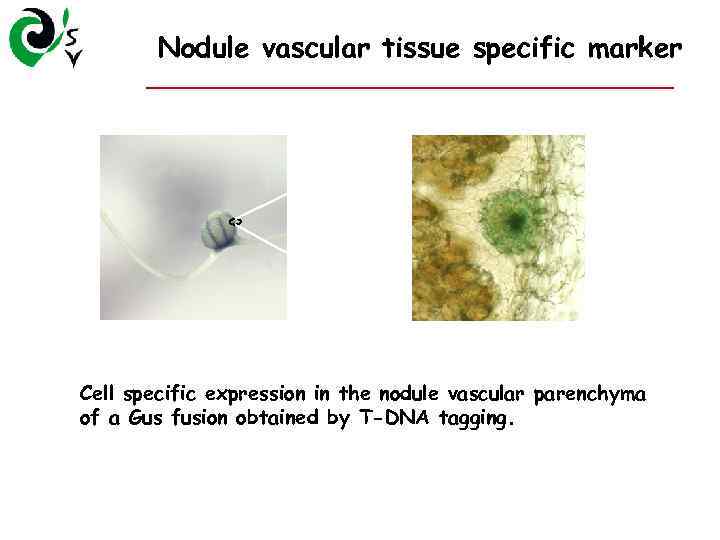 Nodule vascular tissue specific marker Cell specific expression in the nodule vascular parenchyma of a Gus fusion obtained by T-DNA tagging.
Nodule vascular tissue specific marker Cell specific expression in the nodule vascular parenchyma of a Gus fusion obtained by T-DNA tagging.
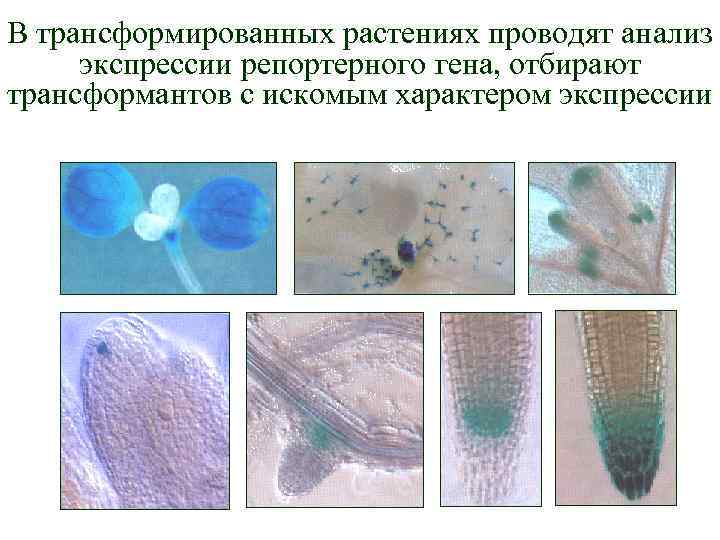 В трансформированных растениях проводят анализ экспрессии репортерного гена, отбирают трансформантов с искомым характером экспрессии
В трансформированных растениях проводят анализ экспрессии репортерного гена, отбирают трансформантов с искомым характером экспрессии
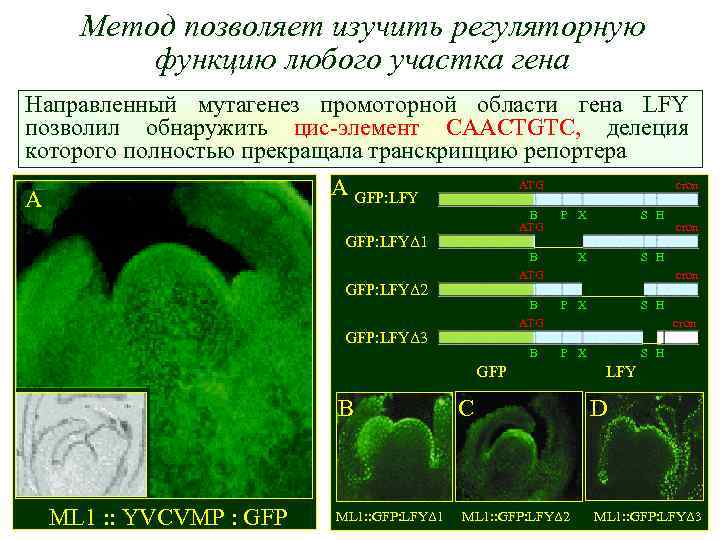 Метод позволяет изучить регуляторную функцию любого участка гена Направленный мутагенез промоторной области гена LFY позволил обнаружить цис-элемент CAACTGTC, делеция которого полностью прекращала транскрипцию репортера A GFP: LFY A ATG B ATG GFP: LFYΔ 1 стоп P X S H B ATG GFP: LFYΔ 2 стоп B ATG P X B GFP: LFYΔ 3 ML 1 : : YVCVMP : GFP ML 1: : GFP: LFYΔ 1 S H P X стоп GFP B стоп C ML 1: : GFP: LFYΔ 2 S H LFY D ML 1: : GFP: LFYΔ 3
Метод позволяет изучить регуляторную функцию любого участка гена Направленный мутагенез промоторной области гена LFY позволил обнаружить цис-элемент CAACTGTC, делеция которого полностью прекращала транскрипцию репортера A GFP: LFY A ATG B ATG GFP: LFYΔ 1 стоп P X S H B ATG GFP: LFYΔ 2 стоп B ATG P X B GFP: LFYΔ 3 ML 1 : : YVCVMP : GFP ML 1: : GFP: LFYΔ 1 S H P X стоп GFP B стоп C ML 1: : GFP: LFYΔ 2 S H LFY D ML 1: : GFP: LFYΔ 3
 Мутант арабидопсиса по гену LFY lfy-26
Мутант арабидопсиса по гену LFY lfy-26
 Получение растений со сверхэкспрессией гена с целью изучения функции гена
Получение растений со сверхэкспрессией гена с целью изучения функции гена
 Ген KNOTTED 1 был идентифи-цирован на основе доминантных мутаций kn 1, вызывающих отсутствие лигулы и появление узелков (knots) на листьях, особенно вокруг жилок. В связи с доминантностью мутаций судить о функции гена сложно
Ген KNOTTED 1 был идентифи-цирован на основе доминантных мутаций kn 1, вызывающих отсутствие лигулы и появление узелков (knots) на листьях, особенно вокруг жилок. В связи с доминантностью мутаций судить о функции гена сложно
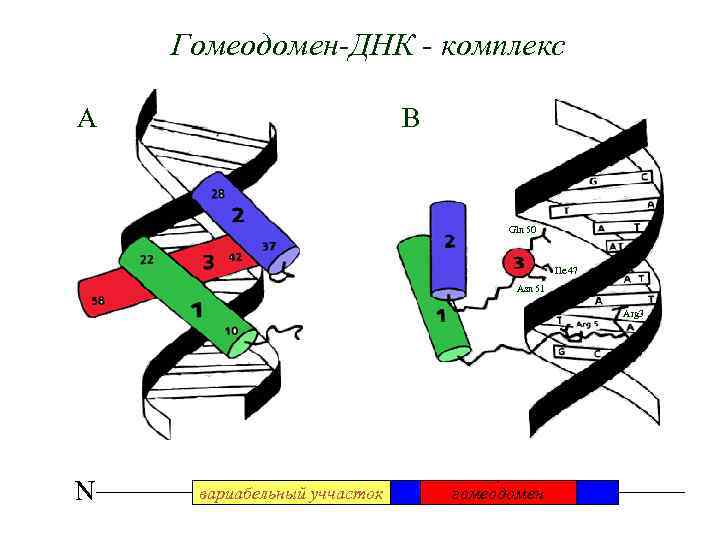 Гомеодомен-ДНК - комплекс A B Gln 50 Ile 47 Asn 51 Arg 3 N вариабельный уччасток гомеодомен
Гомеодомен-ДНК - комплекс A B Gln 50 Ile 47 Asn 51 Arg 3 N вариабельный уччасток гомеодомен
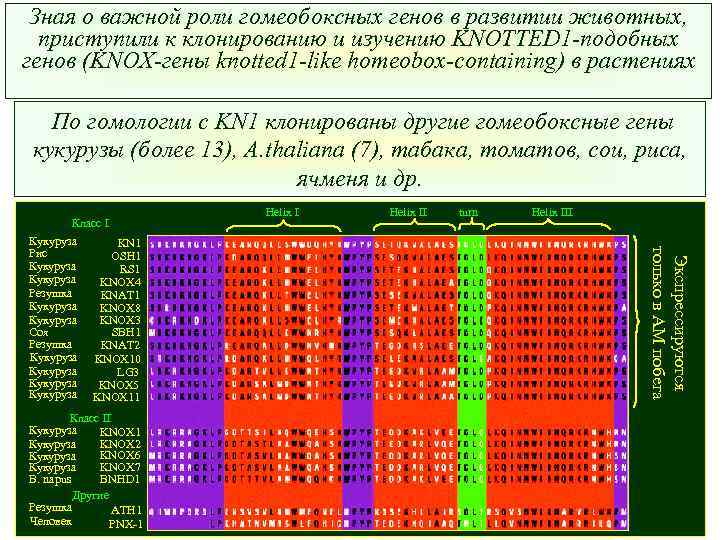 Зная о важной роли гомеобоксных генов в развитии животных, приступили к клонированию и изучению KNOTTED 1 -подобных генов (KNOX-гены knotted 1 -like homeobox-containing) в растениях По гомологии с KN 1 клонированы другие гомеобоксные гены кукурузы (более 13), A. thaliana (7), табака, томатов, сои, риса, ячменя и др. Класс II Кукуруза KNOX 1 Кукуруза KNOX 2 KNOX 6 Кукуруза KNOX 7 B. napus BNHD 1 Другие Резушка ATH 1 Человек PNX-1 Helix II turn Helix III Экспрессируются только в АМ побега Класс I Кукуруза KN 1 Рис OSH 1 Кукуруза RS 1 Кукуруза KNOX 4 Резушка KNAT 1 Кукуруза KNOX 8 Кукуруза KNOX 3 Соя SBH 1 Резушка KNAT 2 Кукуруза KNOX 10 Кукуруза LG 3 Кукуруза KNOX 5 Кукуруза KNOX 11
Зная о важной роли гомеобоксных генов в развитии животных, приступили к клонированию и изучению KNOTTED 1 -подобных генов (KNOX-гены knotted 1 -like homeobox-containing) в растениях По гомологии с KN 1 клонированы другие гомеобоксные гены кукурузы (более 13), A. thaliana (7), табака, томатов, сои, риса, ячменя и др. Класс II Кукуруза KNOX 1 Кукуруза KNOX 2 KNOX 6 Кукуруза KNOX 7 B. napus BNHD 1 Другие Резушка ATH 1 Человек PNX-1 Helix II turn Helix III Экспрессируются только в АМ побега Класс I Кукуруза KN 1 Рис OSH 1 Кукуруза RS 1 Кукуруза KNOX 4 Резушка KNAT 1 Кукуруза KNOX 8 Кукуруза KNOX 3 Соя SBH 1 Резушка KNAT 2 Кукуруза KNOX 10 Кукуруза LG 3 Кукуруза KNOX 5 Кукуруза KNOX 11
 Сверхэкспрессия гена KNAT 1 у арабидопсиса На листьях возникали дополнительные меристематические очаги, из которых могли возникать почки и побеги Листья A. thaliana 35 S: : KNAT 1 превращаются из простых в пальчаторассеченные, хотя фенотип сильно варьировал (Chuck, Linkoln, Hake, 1996)
Сверхэкспрессия гена KNAT 1 у арабидопсиса На листьях возникали дополнительные меристематические очаги, из которых могли возникать почки и побеги Листья A. thaliana 35 S: : KNAT 1 превращаются из простых в пальчаторассеченные, хотя фенотип сильно варьировал (Chuck, Linkoln, Hake, 1996)
 Сверхэкспрессия гена KNAT в листьях томатов дикий тип 35 S: : KNAT
Сверхэкспрессия гена KNAT в листьях томатов дикий тип 35 S: : KNAT
 KNOTTED-подобные гены – возможные участники морфологической эволюции растений
KNOTTED-подобные гены – возможные участники морфологической эволюции растений
 Обнаружение связи между уровнем экспрессии KNOX-генов и усложнением структуры листа позволило предположить, что эти гены могли участвовать в формировании разных типов листа Ø у видов с простым листом (арабидопсис, табак, кукуруза, рис) KNOX-гены экспрессируются только в АМ, но не в примордиях листьев; Ø у томата, имеющего сложный лист, эти гены экспрессируются и в примордиях листьев
Обнаружение связи между уровнем экспрессии KNOX-генов и усложнением структуры листа позволило предположить, что эти гены могли участвовать в формировании разных типов листа Ø у видов с простым листом (арабидопсис, табак, кукуруза, рис) KNOX-гены экспрессируются только в АМ, но не в примордиях листьев; Ø у томата, имеющего сложный лист, эти гены экспрессируются и в примордиях листьев
 Использование методов «генетической хирургии» для изучения взаимодействия клеток и тканей в процессах развития
Использование методов «генетической хирургии» для изучения взаимодействия клеток и тканей в процессах развития
 В основе «генетической хирургии» лежит метод трансформации растений химерными генами следующей конструкции: 1. Кодирующая часть гена – последовательность, кодирующая продукт, вызывающий гибель растительных клеток и не способный перемещаться в другие клетки: а) ген Corynebacterium diphtheriae, кодирующий дифтерийный токсин DT-A-белок, который катализирует АДФ-рибозилирование фактора элонгации. Это ведет к ингибированию белкового синтеза и гибели клеток. В состав DT-A-белка не входит сигнальный пептид, белок не является секреторным, поэтому вызывает гибель только тех клеток, где ген экспрессируется;
В основе «генетической хирургии» лежит метод трансформации растений химерными генами следующей конструкции: 1. Кодирующая часть гена – последовательность, кодирующая продукт, вызывающий гибель растительных клеток и не способный перемещаться в другие клетки: а) ген Corynebacterium diphtheriae, кодирующий дифтерийный токсин DT-A-белок, который катализирует АДФ-рибозилирование фактора элонгации. Это ведет к ингибированию белкового синтеза и гибели клеток. В состав DT-A-белка не входит сигнальный пептид, белок не является секреторным, поэтому вызывает гибель только тех клеток, где ген экспрессируется;
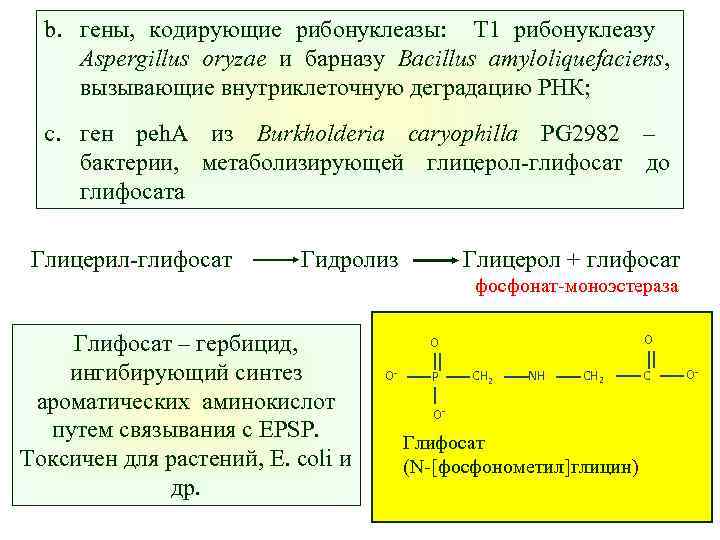 b. гены, кодирующие рибонуклеазы: Т 1 рибонуклеазу Aspergillus oryzae и барназу Bacillus amyloliquefaciens, вызывающие внутриклеточную деградацию РНК; c. ген peh. A из Burkholderia caryophilla PG 2982 – бактерии, метаболизирующей глицерол-глифосат до глифосата Глицерил-глифосат Гидролиз Глицерол + глифосат фосфонат-моноэстераза Глифосат – гербицид, ингибирующий синтез ароматических аминокислот путем связывания с EPSP. Токсичен для растений, E. сoli и др. O O O- P CH 2 NH CH 2 O- Глифосат (N-[фосфонометил]глицин) C O-
b. гены, кодирующие рибонуклеазы: Т 1 рибонуклеазу Aspergillus oryzae и барназу Bacillus amyloliquefaciens, вызывающие внутриклеточную деградацию РНК; c. ген peh. A из Burkholderia caryophilla PG 2982 – бактерии, метаболизирующей глицерол-глифосат до глифосата Глицерил-глифосат Гидролиз Глицерол + глифосат фосфонат-моноэстераза Глифосат – гербицид, ингибирующий синтез ароматических аминокислот путем связывания с EPSP. Токсичен для растений, E. сoli и др. O O O- P CH 2 NH CH 2 O- Глифосат (N-[фосфонометил]глицин) C O-
 Day, Galgoci, Irish, 1995. Генетическое удаление лепестков и тычинок для выяснения роли клеточных взаимодействий в развитии цветка Модели, описывающие процесс возникновения органов цветка: «Последовательная» модель Wardlow, 1957. Порядок возникновения органов цветка отражает последовательность индуктивных сигналов (развитие органов каждого последующего круга зависит от сигналов, поступающих из предыдущих кругов
Day, Galgoci, Irish, 1995. Генетическое удаление лепестков и тычинок для выяснения роли клеточных взаимодействий в развитии цветка Модели, описывающие процесс возникновения органов цветка: «Последовательная» модель Wardlow, 1957. Порядок возникновения органов цветка отражает последовательность индуктивных сигналов (развитие органов каждого последующего круга зависит от сигналов, поступающих из предыдущих кругов
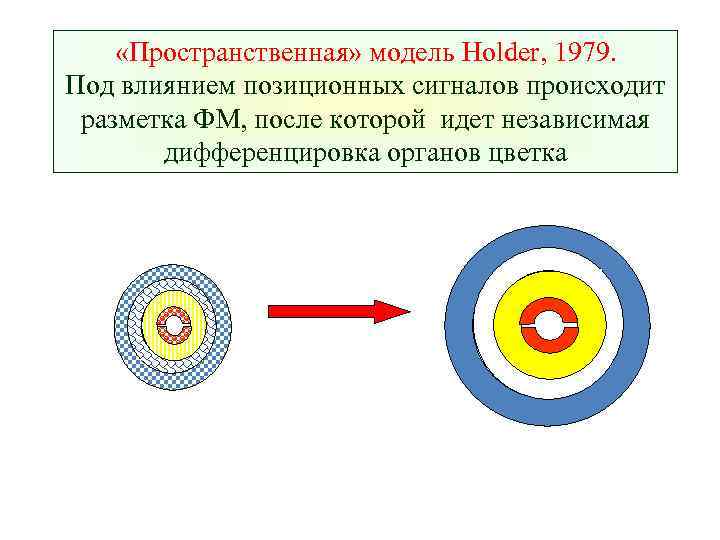 «Пространственная» модель Holder, 1979. Под влиянием позиционных сигналов происходит разметка ФМ, после которой идет независимая дифференцировка органов цветка
«Пространственная» модель Holder, 1979. Под влиянием позиционных сигналов происходит разметка ФМ, после которой идет независимая дифференцировка органов цветка
 Целью работы Day, Galgoci, Irish (1995) была проверка существующих моделей с использованием метода генетической хирургии Объекты: Arabidopsis thaliana и Nicotiana tabacum 1. 7 т. п. н. 5’ 3’ AP 3 DT-A NOS 1. 7 т. п. н. 5’ 3’ AP 3 uid. A NOS
Целью работы Day, Galgoci, Irish (1995) была проверка существующих моделей с использованием метода генетической хирургии Объекты: Arabidopsis thaliana и Nicotiana tabacum 1. 7 т. п. н. 5’ 3’ AP 3 DT-A NOS 1. 7 т. п. н. 5’ 3’ AP 3 uid. A NOS
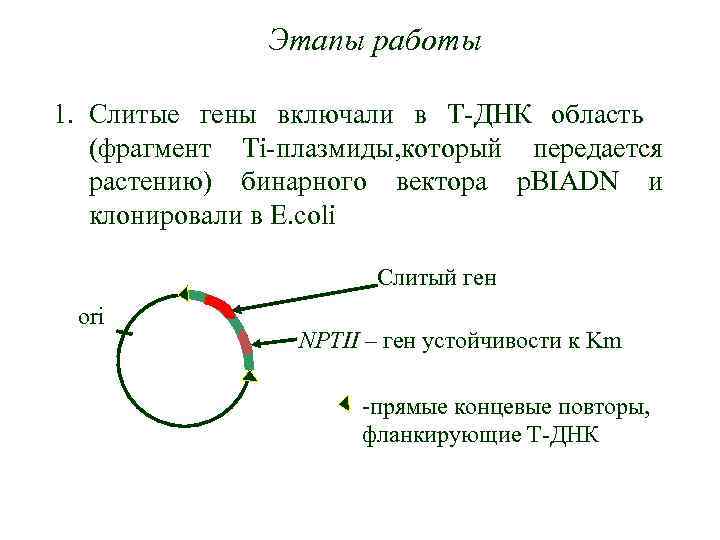 Этапы работы 1. Слитые гены включали в Т-ДНК область (фрагмент Ti-плазмиды, который передается растению) бинарного вектора p. BIADN и клонировали в E. coli Слитый ген ori NPTII – ген устойчивости к Km -прямые концевые повторы, фланкирующие Т-ДНК
Этапы работы 1. Слитые гены включали в Т-ДНК область (фрагмент Ti-плазмиды, который передается растению) бинарного вектора p. BIADN и клонировали в E. coli Слитый ген ori NPTII – ген устойчивости к Km -прямые концевые повторы, фланкирующие Т-ДНК
 РЕЗУЛЬТАТЫ: 1. У резушки получено 5 трансгенных растений, в геноме которых присутствовали от 1 до 5 копий трансгенов (Саузерн-блоттинг) 2. Все трансгенные растения имели одинаковый фенотип: органы 2 и 3 кругов (лепестки и тычинки) отсутствовали, а чашелистики и пестики имели нормальную морфологию. Следовательно, разметка кругов начинается на ранних стадиях до экспрессии трансгена во ФМ, т. е. верна пространственная модель
РЕЗУЛЬТАТЫ: 1. У резушки получено 5 трансгенных растений, в геноме которых присутствовали от 1 до 5 копий трансгенов (Саузерн-блоттинг) 2. Все трансгенные растения имели одинаковый фенотип: органы 2 и 3 кругов (лепестки и тычинки) отсутствовали, а чашелистики и пестики имели нормальную морфологию. Следовательно, разметка кругов начинается на ранних стадиях до экспрессии трансгена во ФМ, т. е. верна пространственная модель


