32b8f37e71200ebe926265b5f6c7694b.ppt
- Количество слайдов: 20

TP 1 TEPELNÉ PROCESY Pravidla hry, databáze, referáty, základní pojmy u, h, s Poznámka: folie s „černým podkladem“ při studiu klidně přeskočte, jsou tématem až poněkud teoretičtěji zaměřeného kurzu TEPELNÉ PROCESY Rudolf Žitný, Ústav procesní a zpracovatelské techniky ČVUT FS 2010

TP 1 TEPELNÉ PROCESY 3 P/2 C, zápočet/zkouška, LS 2015, posluchárna 425 • Přednáší Prof. Ing. Rudolf Žitný, CSc. (streda 13: 15 -16: 00) • Cvičí Ing. Martin Dostál, Ph. D. , Ing. Jaromír Štancl • Hodnocení 30(semestr)+40(písemná zk. )+30(ústní) bodů A B C D E F 90+ 80+ 70+ 60+ 50+ . . 49 Anotace: Provedení, principy činnosti a základy výpočtu pro výměníky tepla, chladiče, odparky, sušárny, pece, ohmický a mikrovlnný ohřev. Aplikace v potravinářském průmyslu, aseptické procesy.
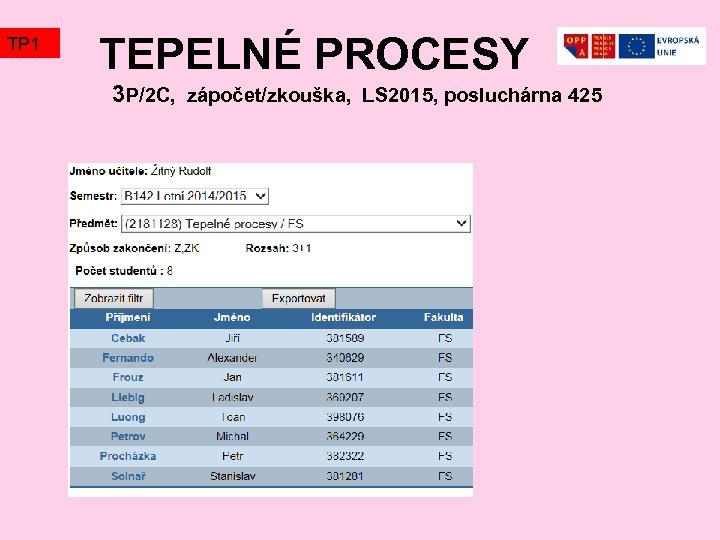
TP 1 TEPELNÉ PROCESY 3 P/2 C, zápočet/zkouška, LS 2015, posluchárna 425

TP 1 TEPELNÉ PROCESY 3 P/2 C, zápočet/zkouška, LS 2015, posluchárna 425

TP 1 LITERATURA databáze • Skripta: Šesták J. , Žitný R. : Tepelné pochody II, ČVUT Praha, 2000 • Monografie: Mc. Cabe W. L. , Smith J. C. , Harriot P. : Unit Operations of Chemical Engineering. 7 th Edition, Mc. Graw Hill, Inc. , N. Y. , 2005 Lewis M. , Heppell N. : Continuous thermal processes of foods. An ASPEN Publication, Gaithersburg, 2000 Schlünder E. Edt. VDI-Wärmeatlas. 10 -überarbeitete Auflage, Springer Verlag, Berlin, 2005 Hewitt G. F. : Heat Exchanger Design Handbook. Begell house inc. , N. Y. , 1998 • Databáze článků: Přímý přístup k počítačovým databázím článků (celé texty) jsou pouze pro vás k dispozici na adrese knihovny. cvut. cz Jméno DUPS

TP 1 VÝBĚR DATABÁZE Tady se dozvíte, čemu přednášející a cvičící alespoň trochu opravdu rozumí (možná) Databáze článků, které můžete použít jako temata referátů.
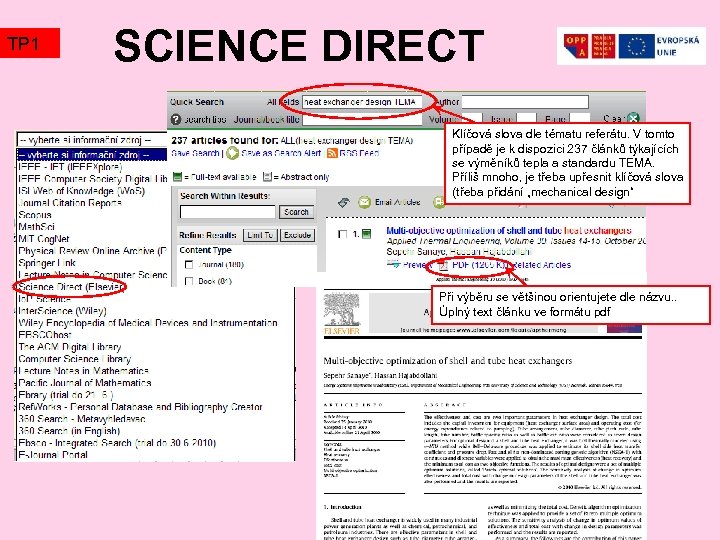
TP 1 SCIENCE DIRECT Klíčová slova dle tématu referátu. V tomto případě je k dispozici 237 článků týkajících se výměníků tepla a standardu TEMA. Příliš mnoho, je třeba upřesnit klíčová slova (třeba přidání „mechanical design“ Při výběru se většinou orientujete dle názvu. . Úplný text článku ve formátu pdf
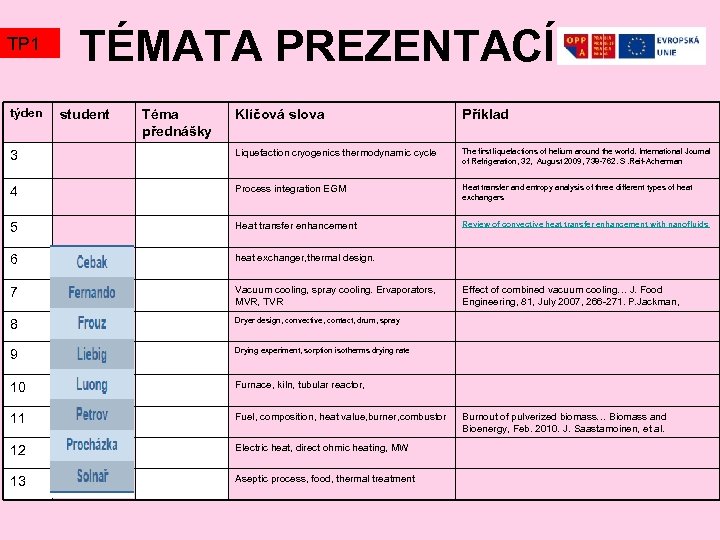
TP 1 týden TÉMATA PREZENTACÍ student Téma přednášky Klíčová slova Příklad 3 Liquefaction cryogenics thermodynamic cycle The first liquefactions of helium around the world. International Journal of Refrigeration, 32, August 2009, 738 -762. S. Reif-Acherman 4 Process integration EGM Heat transfer and entropy analysis of three different types of heat exchangers 5 Heat transfer enhancement Review of convective heat transfer enhancement with nanofluids 6 heat exchanger, thermal design. 7 Vacuum cooling, spray cooling. Ervaporators, MVR, TVR 8 Dryer design, convective, contact, drum, spray 9 Drying experiment, sorption isotherms drying rate 10 Furnace, kiln, tubular reactor, 11 Fuel, composition, heat value, burner, combustor 12 Electric heat, direct ohmic heating, MW 13 Aseptic process, food, thermal treatment Effect of combined vacuum cooling… J. Food Engineering, 81, July 2007, 266 -271. P. Jackman, Burnout of pulverized biomass… Biomass and Bioenergy, Feb. 2010. J. Saastamoinen, et al.

TP 1 OPAKOVÁNÍ TERMODYNAMIKY
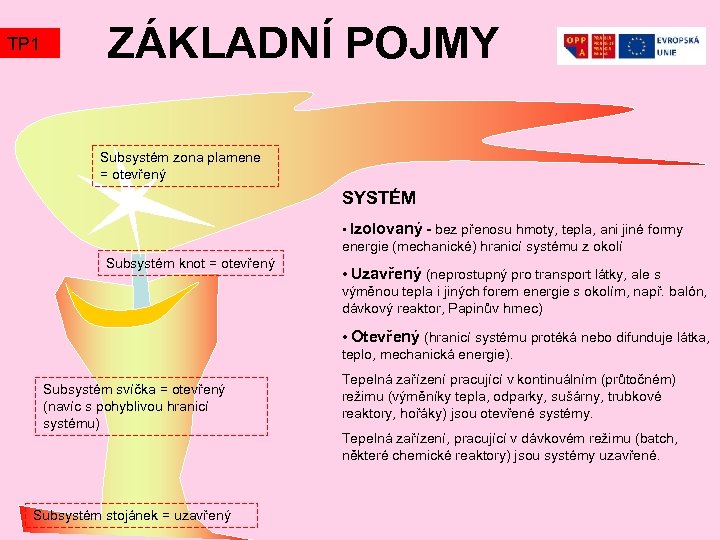
TP 1 ZÁKLADNÍ POJMY Subsystém zona plamene = otevřený SYSTÉM • Izolovaný - bez přenosu hmoty, tepla, ani jiné formy energie (mechanické) hranicí systému z okolí Subsystém knot = otevřený • Uzavřený (neprostupný pro transport látky, ale s výměnou tepla i jiných forem energie s okolím, např. balón, dávkový reaktor, Papinův hrnec) • Otevřený (hranicí systému protéká nebo difunduje látka, teplo, mechanická energie). Subsystém svíčka = otevřený (navíc s pohyblivou hranicí systému) Subsystém stojánek = uzavřený Tepelná zařízení pracující v kontinuálním (průtočném) režimu (výměníky tepla, odparky, sušárny, trubkové reaktory, hořáky) jsou otevřené systémy. Tepelná zařízení, pracující v dávkovém režimu (batch, některé chemické reaktory) jsou systémy uzavřené.

TP 1 UZAVŘENÝ SYSTÉM Stav systému charakterizují Termodynamické stavové veličiny související s mechanickými vlastnostmi (které se dají přímo měřit): Ø T [K], p[Pa], v [m 3/kg] (teplota, tlak, měrný objem) Termodynamické stavové veličiny související s energií, které se už přímo měřit nedají (musí se odvodit z T, p, v): Ø u [J/kg] měrná vnitřní energie – bilance dávkových systémů Ø s [J/kg/K] měrná entropie δq = přivedené teplo δw = p. dv mechanická práce při změně objemu systému δq = du + δw Tohle určitě znáte (zákon zachování energie, 1. zákon termodynamiky): přivedené teplo stěnou=zvýšení vnitřní energie+mechanická práce Jenže zatímto u je stavová veličina, q (teplo) a w (práce) stavové veličiny nejsou (nedají se odvodit ze změny stavu systému, pro určitou změnu stavu du existuje nekonečně mnoho různých cest, různých kombinací množství dodaného tepla a vykonané práce se stejným výsledkem).

TP 1 PRŮTOČNÝ SYSTÉM Průtočný systém nahradíme uzavřeným systémem, který obsahuje stále stejné množství hmoty m (hranice systému je pohyblivá = písty ve vstupních/výstupních proudech). Hmotnostní průtok ve vstupním proudu Hmotnostní průtok ve výstupním proudu u, V, p 1, u 1, d. V 1 d. Q Stav v čase t u+du, V, +d p 2, u 2, d. V 2 Stav v čase t+dt Změna vnitřní energie (hmotnost látky m) mechanická práce Entalpie výstupního a vstupního proudu (viz dále)

TP 1 VNITŘNÍ ENERGIE du = cv d. T. . . teplo dq přivedené do systému při konstantním objemu (přesněji, když se nekonán žádná práce)

TP 1 VNITŘNÍ ENERGIE u u-zahrnuje všechny formy energie hmoty v systému (J/kg), s výjimkou těch, které závisí na pohybu souřadného systému (tj. do vnitřní energie není zahrnuta potenciální energie polohy /gh/ a kinetická energie pohybu systému jako celku /½w 2/). Vnitřní energii lze stanovit když známe strukturu, složení a hybnost všech složek systému, tj. všech atomů a molekul). Vnitřní energie je součtem těchto energií (a dalších, např. magnetické) ØNukleární energie (vazebná energie jádra atomů) ~1017 J/kg ØChemická energie vazeb atomů v molekule ~107 J/kg ØEnergie fázových změn (mezimolekulární síly) ~106 J/kg ØTlaková energie ~105 J/kg ØTepelná energie (kinetická energie molekul) ~104 J/kg Spálením 1 kg uhlí se uvolní cca 20 MJ Kondenzací 1 kg páry se uvolní cca 2 MJ Ochlazením 1 kg vody o 1 K se uvolní 4 k. J Z praktického hlediska má smysl určovat jen změny vnitřní energie, u tepelných zařízení jen změny chemické energie (spalování), fázových změn (sušení, odpařování) a změny tepelné energie (výměníky tepla). Změna tepelné energie je svázána se změnou teploty (chápejte teplotu jako míru kinetické energie molekul) du = cv d. T, pro případ kdy objem systému je konstantní a tudíž se nekoná mechanická práce (dw = p dv = 0). cv je měrná tepelná kapacita látky při konstantním objemu. cv=4. 2 k. J. kg-1. K-1 pro vodu, =1 k. J. kg-1. K-1 pro vzduch.

TP 1 ENTROPIE dq = T ds …teplo dq přenesené do systému (ideálně, vratně)

TP 1 ENTROPIE s s-entropie je mírou pravděpodobnosti makroskopického stavu systému (makrostav je to, co se dá měřit, třeba rozložení teplot, koncentrací v systému, délky makromolekul), a tato pravděpodobnost je dána počtem mikrostavů (možných konfigurací, třeba uspořádání řetězců makromolekul, rozmístění molekul v různých místech systému apod. ), které odpovídají témuž makrostavu. Pravděpodobnost makrostavu se dá spočítat, ale není to jednoduché. Význam takto definované veličiny je v tom, že samovolně probíhající procesy probíhají ve směru od méně do více pravděpodobného stavu a tudíž jsou charakterizovány růstem entropie. To je 2. termodynamický zákon: entropie izolovaného systémy vždy roste. Analýza změn entropie umožňuje například zjistit, zda hypotetická chemická reakce bude či nebude samovolně probíhat. Pro tepelná zařízení není výše uvedená definice rozumně použitelná (rychle ji zapomeňte pokud nemáte v úmyslu se věnovat biomechanice nebo vlastnostem plastů). Vhodnější je odvozovat entropii z velikosti tepla, dodaného systému: δq < T ds teplo dodané do systému je vždy menší než součin T ds (T-musí být v Kelvinech) Všimněte si, že na rozdíl od vnitřní energie (du=cv d. T) je entropie definována nerovností. Rovnost δq=T ds platí u ideálních vratných procesů (bez tření). Zvýšení entropie ds je dáno přívodem tepla zvenčí δq/T plus vnitřním teplem, které je generováno vazkým třením třeba při proudění páry (disipací mechanické energie).

TP 1 ENTROPIE raději přeskočte Je mi celkem jasné, že souvislost entropie s mikro a makrostavy vám nemůže být pochopitelná. Pokusím se to vysvětlit na dvou příkladech: Řekněme, že systém je nádoba v níž jsou dvě molekuly. Budeme rozlišovat jen to, kolik molekul je v levé a v pravé části nádoby. Jsou jen 3 možné makrostavy: obě molekuly jsou v levé polovině, obě jsou vpravo nebo jedna je vlevo a jedna je vpravo. V prvním případě je možný jen jeden mikrostav, molekuly 1 i 2 jsou vlevo. V druhém případě jsou dva mikrostavy, molekula 1 je vlevo anebo molekula 2 je vlevo. Makrostav, kdy je v každé části právě jedna molekula, má tedy největší počet možných uspořádání (dvě), nejvyšší pravděpodobnost a tudíž největší entropii. Tak se popisuje třeba difúze: největší entropie odpovídá rovnoměrnému rozmístění složek. a b b a Druhý příklad je makromolekula elastomeru (pryže). Můžeme ji považovat za řetízek kloubově spojených monomerů. Makrostav je vzdálenost koncových bodů. Je-li makromolekula maximálně protažená (zatížená silou), existuje jediné uspořádání (poloh kloubů) a tedy jediný mikrostav. Je-li molekula nezatížená, vzdálenost koncových bodů se zmenší a způsobů uspořádání klubka (mikrostavů) bude vysoká. Entropie natahovaného polymeru tedy klesá a vlákno se ohřívá! Je to úplně obráceně než u klasických materiálů (kovový pásek při natahování chladne, kov se s rostoucí teplotou roztahuje, elastomer smrští). Praktičtější je uvažovat jak se mění entropie systému uvnitř kterého dochází k nevratnému přenosu tepla mezi teplým (T 1) a chladným (T 2) tělesem. Uvažujme dvoutělesový zvnějšku izolovaný systém T 1 δQ T 2 d. S= - δQ/T 1+ δQ/T 2 = δQ (T 1 -T 2)/(T 1 T 2) všimněte si, že d. S>0 , i když se žádné teplo zvenčí nepřivádělo, zvýšení entropie soustavy je projev nevratnosti přenosu tepla. a b

TP 1 ENTALPIE dq = cp d. T …teplo dq přenesené do systému při konstantním tlaku

TP 1 ENTALPIE Zavedení nové stavové veličiny, měrné entalpie h=u+pv výrazně zjednoduší bilanci průtočných systémů, protože není třeba explicitně počítat mechanickou práci (výkon) potřebný pro dopravu materiálu do systému a ven ze systému. V ustáleném režimu je tedy bilance systému Změna entalpie je svázána se změnou teploty du = cp d. T, pro případ kdy se objem mění, ale je konstantní tlak. cp je měrná tepelná kapacita látky při konstantním tlaku, pro nestlačitelné kapaliny je cv=cp.

TP 1 SOUHRN Měrná vnitřní energie u bilance uzavřených systémů v nestacionárním režimu Měrná entalpie h = u + pv pro bilance průtočných systémů Dodané teplo dq = T ds ds-přírůstek entropie (záporný, když se teplo odebírá) Malými písmeny označujeme měrné veličiny vztažené na 1 kg látky v systému (např. v-měrný objem). Velkými písmeny korespondující extenzivní veličiny U [J] H=U+p. V [J] S [J/K] O tom jak se dají entalpie, vnitřní energie a entropie stanovit bude pojednávat příští přednáška.
32b8f37e71200ebe926265b5f6c7694b.ppt