Топливо и основы теории горения.ppt
- Количество слайдов: 46
 Топливо и основы теории горения Проф. В. А. Широков 2012 г.
Топливо и основы теории горения Проф. В. А. Широков 2012 г.
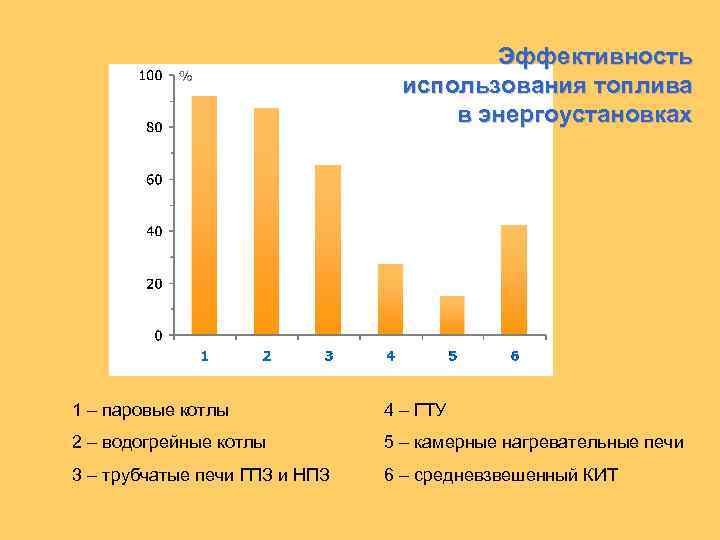 Эффективность использования топлива в энергоустановках 1 – паровые котлы 4 – ГТУ 2 – водогрейные котлы 5 – камерные нагревательные печи 3 – трубчатые печи ГПЗ и НПЗ 6 – средневзвешенный КИТ
Эффективность использования топлива в энергоустановках 1 – паровые котлы 4 – ГТУ 2 – водогрейные котлы 5 – камерные нагревательные печи 3 – трубчатые печи ГПЗ и НПЗ 6 – средневзвешенный КИТ
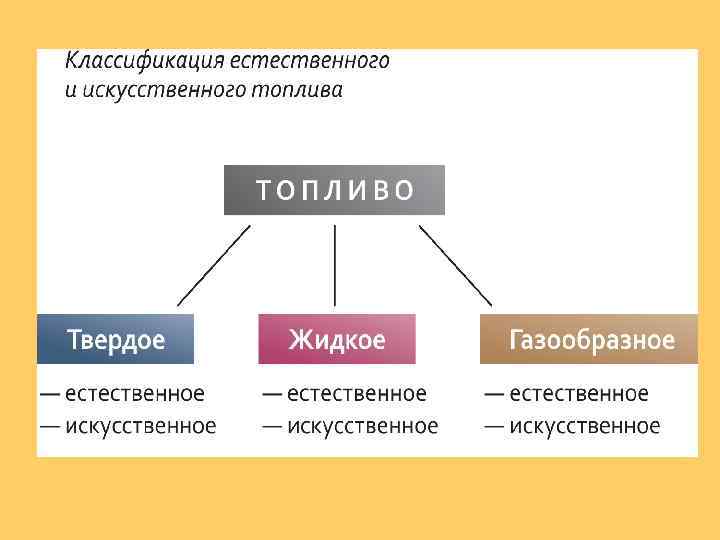

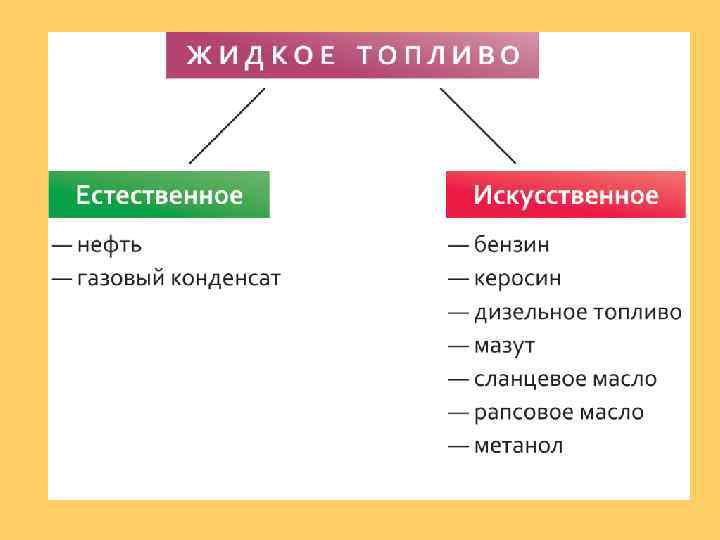
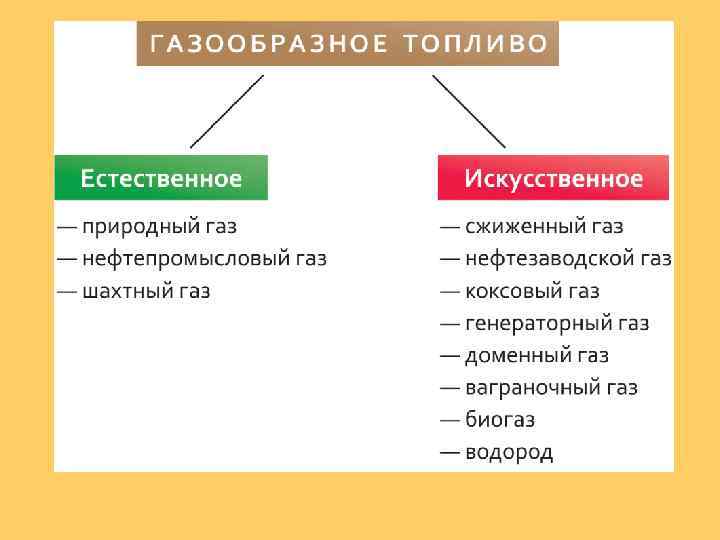
 Механизмы реакций горения Примером цепной реакции с разветвляющимися цепями является реакция горения водорода. Стехиометрическое уравнение ее имеет вид 2 Н 2 + О 2 = 2 Н 2 О
Механизмы реакций горения Примером цепной реакции с разветвляющимися цепями является реакция горения водорода. Стехиометрическое уравнение ее имеет вид 2 Н 2 + О 2 = 2 Н 2 О
 Механизмы реакций горения (продолжение) В действительности эта реакция идет через образование промежуточных активных центров - атомов водорода, кислорода и радикалов по следующей схеме: Н 2 + О 2 Н + Н 2 О — зарождение цепи Н + О 2 ОН + О — разветвление цепи О + Н 2 ОН + Н — продолжение цепи ОН + Н 2 О + Н — продолжение цепи Н + М 1/2 Н 2 — обрыв цепи на стенке Н + О 2 + М Н 2 О + М — обрыв цепи в объеме, где М — инертная молекула газа или стенки реактора.
Механизмы реакций горения (продолжение) В действительности эта реакция идет через образование промежуточных активных центров - атомов водорода, кислорода и радикалов по следующей схеме: Н 2 + О 2 Н + Н 2 О — зарождение цепи Н + О 2 ОН + О — разветвление цепи О + Н 2 ОН + Н — продолжение цепи ОН + Н 2 О + Н — продолжение цепи Н + М 1/2 Н 2 — обрыв цепи на стенке Н + О 2 + М Н 2 О + М — обрыв цепи в объеме, где М — инертная молекула газа или стенки реактора.
 Механизмы реакций горения (продолжение) Основные стадии процесса горения метана: - неполное горение метана с образованием формальдегида СН 4 + О 2 = НСНО + Н 2 О и - дожигание формальдегида НСНО + О 2 = Н 2 О + СО 2
Механизмы реакций горения (продолжение) Основные стадии процесса горения метана: - неполное горение метана с образованием формальдегида СН 4 + О 2 = НСНО + Н 2 О и - дожигание формальдегида НСНО + О 2 = Н 2 О + СО 2
 Механизмы реакций горения (продолжение) Для первой стадии характерны следующие реакции: СН 4 СН 3 + Н; СН 3 + О 2 НСНО + ОН; Н + О 2 ОН + О; СН 4 + ОН СН 3 + Н 2 О; СН 4 + О СН 3 + ОН.
Механизмы реакций горения (продолжение) Для первой стадии характерны следующие реакции: СН 4 СН 3 + Н; СН 3 + О 2 НСНО + ОН; Н + О 2 ОН + О; СН 4 + ОН СН 3 + Н 2 О; СН 4 + О СН 3 + ОН.
 Механизмы реакций горения (продолжение) При низких температурах протекают реакции с образованием метанола: СН 4 + О + М СН 3 ОН + М. С повышением температуры усиливается глубина термического разложения и метил СН 3 превращается в метилен СН 2: СН 3 СН 2 + Н. Результатом реакции обрыва цепей является образование этилена: 2 СН 2 С 2 Н 4.
Механизмы реакций горения (продолжение) При низких температурах протекают реакции с образованием метанола: СН 4 + О + М СН 3 ОН + М. С повышением температуры усиливается глубина термического разложения и метил СН 3 превращается в метилен СН 2: СН 3 СН 2 + Н. Результатом реакции обрыва цепей является образование этилена: 2 СН 2 С 2 Н 4.
 Механизмы реакций горения (продолжение) В результате термического разложения метилена СН 2 образуется метин СН: СН 2 СН + Н. Взаимодействие молекул метина приводит к образованию ацетилена: 2 СН С 2 Н 2.
Механизмы реакций горения (продолжение) В результате термического разложения метилена СН 2 образуется метин СН: СН 2 СН + Н. Взаимодействие молекул метина приводит к образованию ацетилена: 2 СН С 2 Н 2.
 Механизмы реакций горения (продолжение) Для горения формальдегида (вторая стадия) характерны следующие реакции: НСНО НСО + Н; Н + О 2 ОН + О. Образовавшийся радикал НСО может вступать в реакцию с кислородом: НСО + О 2 СО + НО 2 СО + ОН + О
Механизмы реакций горения (продолжение) Для горения формальдегида (вторая стадия) характерны следующие реакции: НСНО НСО + Н; Н + О 2 ОН + О. Образовавшийся радикал НСО может вступать в реакцию с кислородом: НСО + О 2 СО + НО 2 СО + ОН + О
 Механизмы реакций горения (продолжение) и разлагаться с образованием окиси углерода: НСО СО + Н; НСО + О СО + ОН; НСО + ОН СО + Н 2 О. Окись углерода сгорает по уравнению СО + ОН СО 2 + Н; СО + О СО 2.
Механизмы реакций горения (продолжение) и разлагаться с образованием окиси углерода: НСО СО + Н; НСО + О СО + ОН; НСО + ОН СО + Н 2 О. Окись углерода сгорает по уравнению СО + ОН СО 2 + Н; СО + О СО 2.
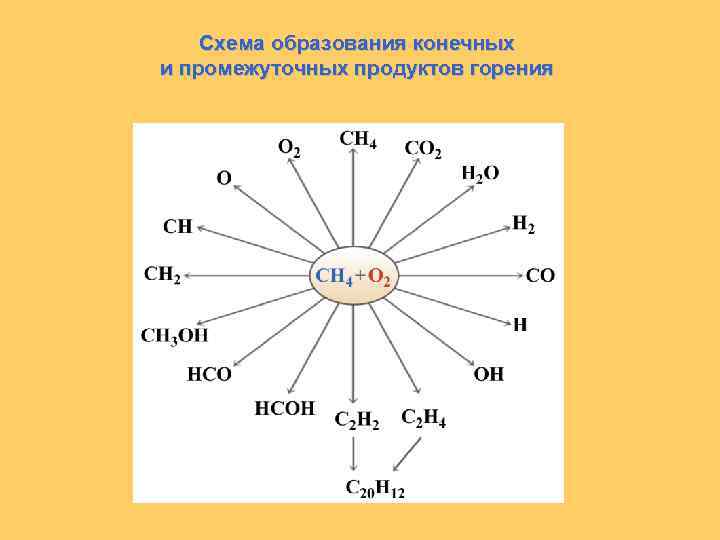 Схема образования конечных и промежуточных продуктов горения
Схема образования конечных и промежуточных продуктов горения
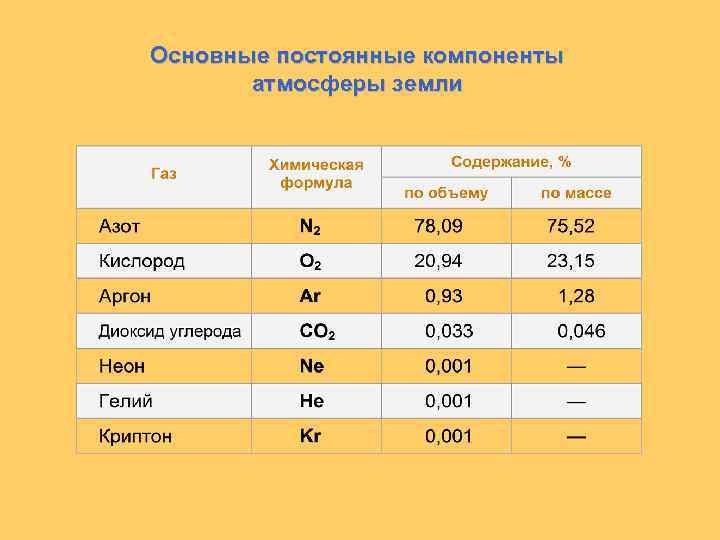 Основные постоянные компоненты атмосферы земли
Основные постоянные компоненты атмосферы земли
 ОСНОВНЫЕ ТЕПЛОТЕХНИЧЕСКИЕ И ЭКОЛОГИЧЕСКИЕ ХАРАКТЕРИСТИКИ ТОПЛИВА 1. ТЕПЛОТА СГОРАНИЯ, ккал/нм 3, ккал/кг, к. Дж/нм 3, к. Дж/кг а) низшая, Qнр б) высшая, Qвр 2. МАКСИМАЛЬНАЯ ТЕМПЕРАТУРА ГОРЕНИЯ tmax, ºС 3. МАКСИМАЛЬНОЕ СОДЕРЖАНИЕ СО 2 В ПРОДУКТАХ СГОРАНИЯ СО 2 макс. , RO 2 макс.
ОСНОВНЫЕ ТЕПЛОТЕХНИЧЕСКИЕ И ЭКОЛОГИЧЕСКИЕ ХАРАКТЕРИСТИКИ ТОПЛИВА 1. ТЕПЛОТА СГОРАНИЯ, ккал/нм 3, ккал/кг, к. Дж/нм 3, к. Дж/кг а) низшая, Qнр б) высшая, Qвр 2. МАКСИМАЛЬНАЯ ТЕМПЕРАТУРА ГОРЕНИЯ tmax, ºС 3. МАКСИМАЛЬНОЕ СОДЕРЖАНИЕ СО 2 В ПРОДУКТАХ СГОРАНИЯ СО 2 макс. , RO 2 макс.
 ОСНОВНЫЕ ТЕПЛОТЕХНИЧЕСКИЕ И ЭКОЛОГИЧЕСКИЕ ХАРАКТЕРИСТИКИ ТОПЛИВА 4. СОДЕРЖАНИЕ БАЛЛАСТА Ар, W р твердое и жидкое топливо CO 2, N 2, % газообразное топливо 5. СОДЕРЖАНИЕ ВРЕДНЫХ ПРИМЕСЕЙ Sр, H 2 S и др.
ОСНОВНЫЕ ТЕПЛОТЕХНИЧЕСКИЕ И ЭКОЛОГИЧЕСКИЕ ХАРАКТЕРИСТИКИ ТОПЛИВА 4. СОДЕРЖАНИЕ БАЛЛАСТА Ар, W р твердое и жидкое топливо CO 2, N 2, % газообразное топливо 5. СОДЕРЖАНИЕ ВРЕДНЫХ ПРИМЕСЕЙ Sр, H 2 S и др.
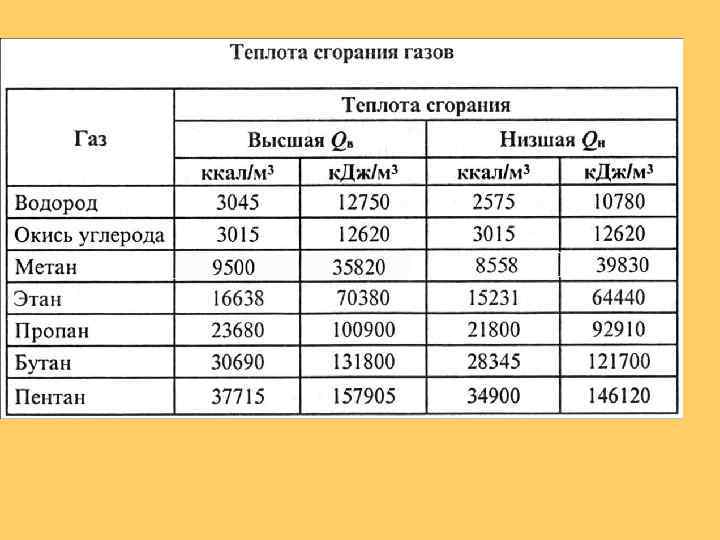
 ТЕПЛОТА СГОРАНИЯ ЖИДКОГО И ТВЕРДОГО ТОПЛИВА (Ккал/кг) ТОРФ ДРОВА БУРЫЙ УГОЛЬ КАМЕННЫЙ УГОЛЬ АНТРАЦИТ НЕФТЬ МАЗУТ БЕНЗИН ДИЗЕЛЬНОЕ ТОПЛИВО 4 600 2 400— 2 900 2 500— 6 800 4 800— 8 700 6 000— 7 200 9 500— 10 500 9 500— 9 700 10 500 10 200
ТЕПЛОТА СГОРАНИЯ ЖИДКОГО И ТВЕРДОГО ТОПЛИВА (Ккал/кг) ТОРФ ДРОВА БУРЫЙ УГОЛЬ КАМЕННЫЙ УГОЛЬ АНТРАЦИТ НЕФТЬ МАЗУТ БЕНЗИН ДИЗЕЛЬНОЕ ТОПЛИВО 4 600 2 400— 2 900 2 500— 6 800 4 800— 8 700 6 000— 7 200 9 500— 10 500 9 500— 9 700 10 500 10 200
 ТЕПЛОТА СГОРАНИЯ ЖИДКИХ И ТВЕРДЫХ ТОПЛИВ
ТЕПЛОТА СГОРАНИЯ ЖИДКИХ И ТВЕРДЫХ ТОПЛИВ
 Уравнения горения газообразных углеводородов O 2 : N 2 = 1 : 3, 76 CH 4 + 2 O 2 + 7, 52 N 2 = CO 2 + 2 H 2 O + 7, 52 N 2 C 2 H 6 + 3, 5 O 2 + 13, 16 N 2 = 2 CO 2 + 3 H 2 O + 13, 16 N 2 C 3 H 8 + 5 O 2 + 18, 8 N 2 = 3 CO 2 + 4 H 2 O + 18, 8 N 2
Уравнения горения газообразных углеводородов O 2 : N 2 = 1 : 3, 76 CH 4 + 2 O 2 + 7, 52 N 2 = CO 2 + 2 H 2 O + 7, 52 N 2 C 2 H 6 + 3, 5 O 2 + 13, 16 N 2 = 2 CO 2 + 3 H 2 O + 13, 16 N 2 C 3 H 8 + 5 O 2 + 18, 8 N 2 = 3 CO 2 + 4 H 2 O + 18, 8 N 2
 Уравнения горючих газов Н 2 + 0, 5 О 2 + 1 , 88 N 2 = Н 20 + 1 , 88 N 2 СО + 0, 5 О 2 + 1 , 88 N 2 = СО 2 + 1 , 88 N 2 H 2 S + 1, 5 О 2 + 5, 64 N 2 = SО 2 + H 2 О + 5, 64 N 2
Уравнения горючих газов Н 2 + 0, 5 О 2 + 1 , 88 N 2 = Н 20 + 1 , 88 N 2 СО + 0, 5 О 2 + 1 , 88 N 2 = СО 2 + 1 , 88 N 2 H 2 S + 1, 5 О 2 + 5, 64 N 2 = SО 2 + H 2 О + 5, 64 N 2
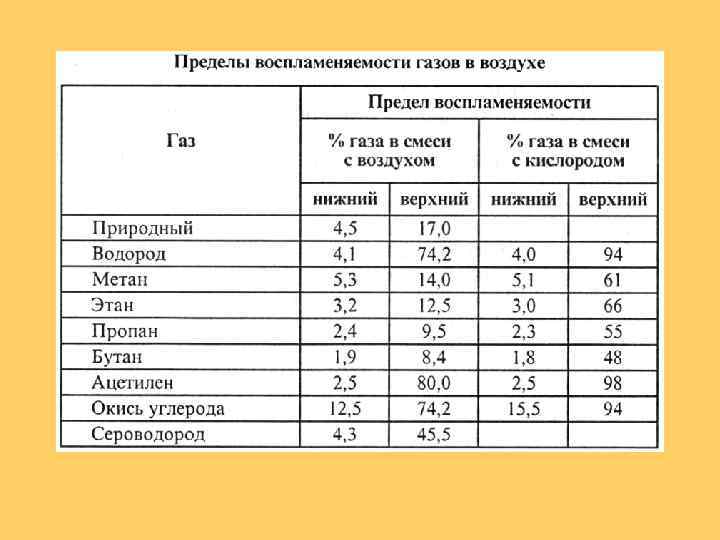
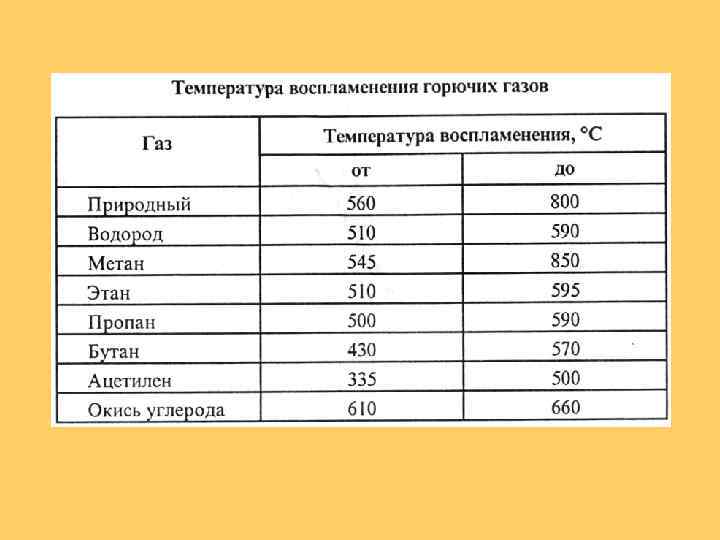
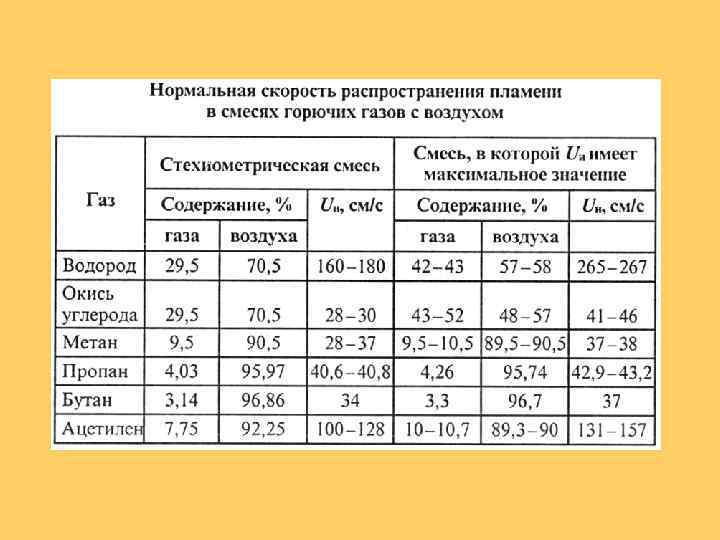
 Основные характеристики природного газа (CH 4)
Основные характеристики природного газа (CH 4)
 Основные характеристики природного газа (CH 4) (продолжение)
Основные характеристики природного газа (CH 4) (продолжение)
 Расчетные характеристики жидкого углеводородного топлива
Расчетные характеристики жидкого углеводородного топлива
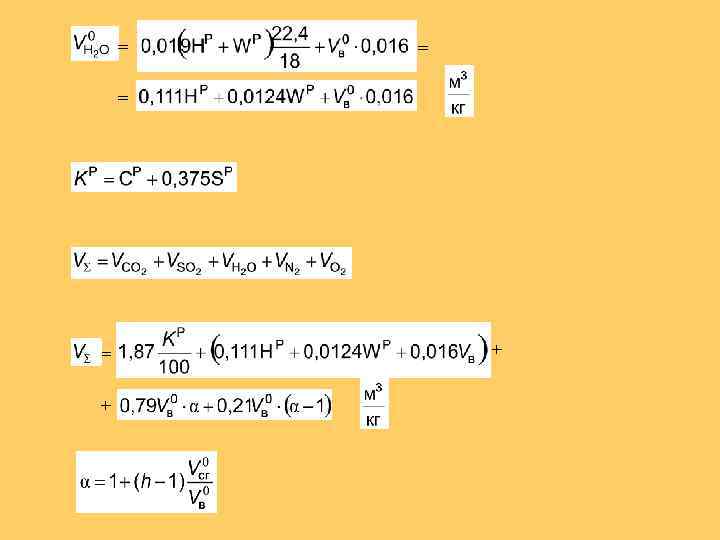 + +
+ +
 ТЕМПЕРАТУРА ГОРЕНИЯ ТОПЛИВА
ТЕМПЕРАТУРА ГОРЕНИЯ ТОПЛИВА
 ТИПЫ ГАЗОГОРЕЛОЧНЫХ УСТРОЙСТВ а) диффузионные б) инжекционные в) двухпроводные смесительные г) турбореактивные д) комбинированные
ТИПЫ ГАЗОГОРЕЛОЧНЫХ УСТРОЙСТВ а) диффузионные б) инжекционные в) двухпроводные смесительные г) турбореактивные д) комбинированные
 ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ГАЗОГОРЕЛОЧНЫХ УСТРОЙСТВ а) давление газа ( до 5 КПа; до 0, 3 МПа; более 0, 3 МПа) б) тепловая мощность (МВт) в) коэффициент избытка воздуха г) коэффициент предельного регулирования д) коэффициент рабочего регулирования
ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ГАЗОГОРЕЛОЧНЫХ УСТРОЙСТВ а) давление газа ( до 5 КПа; до 0, 3 МПа; более 0, 3 МПа) б) тепловая мощность (МВт) в) коэффициент избытка воздуха г) коэффициент предельного регулирования д) коэффициент рабочего регулирования
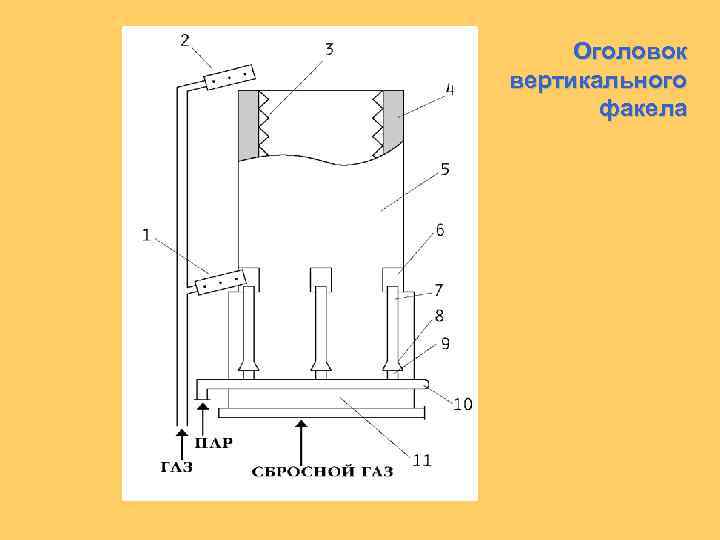 Оголовок вертикального факела
Оголовок вертикального факела
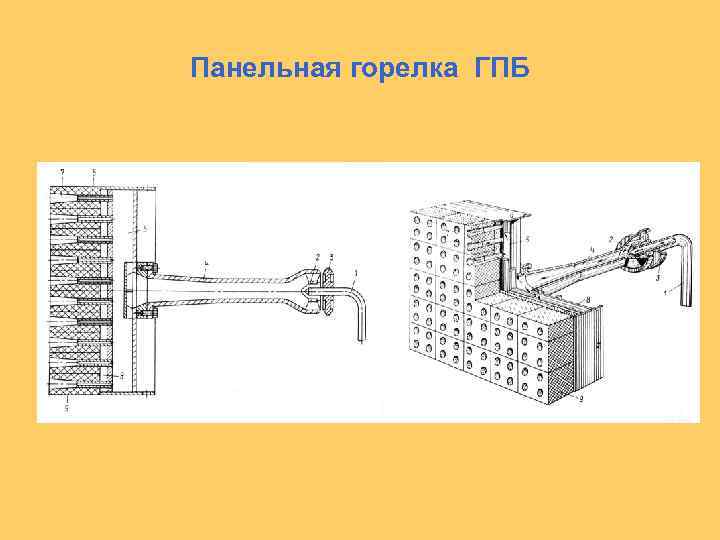 Панельная горелка ГПБ
Панельная горелка ГПБ
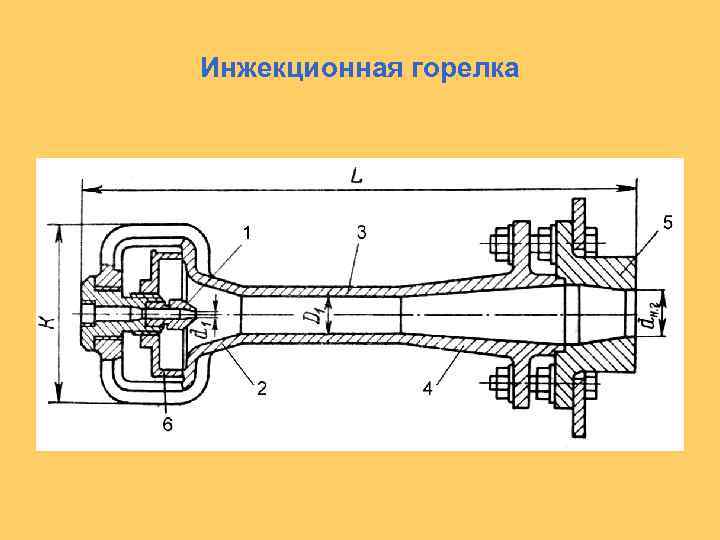 Инжекционная горелка
Инжекционная горелка
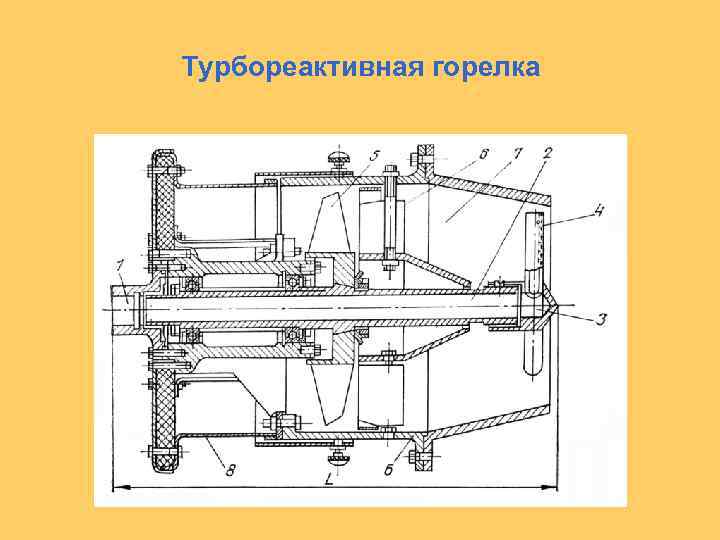 Турбореактивная горелка
Турбореактивная горелка
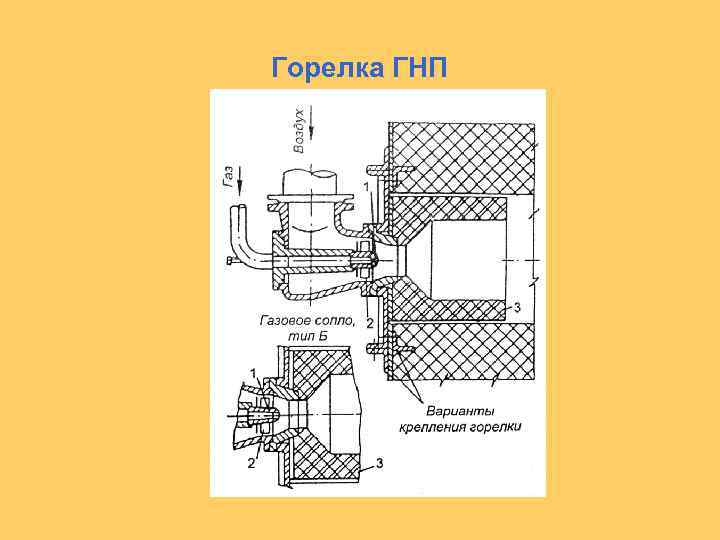 Горелка ГНП
Горелка ГНП
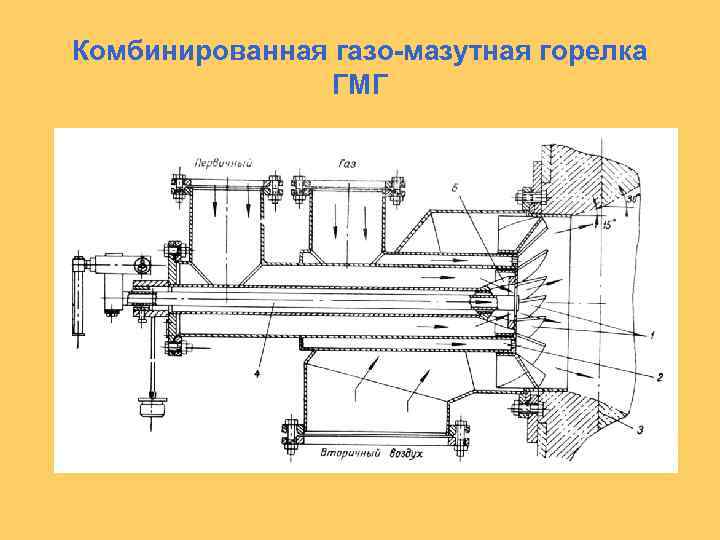 Комбинированная газо-мазутная горелка ГМГ
Комбинированная газо-мазутная горелка ГМГ
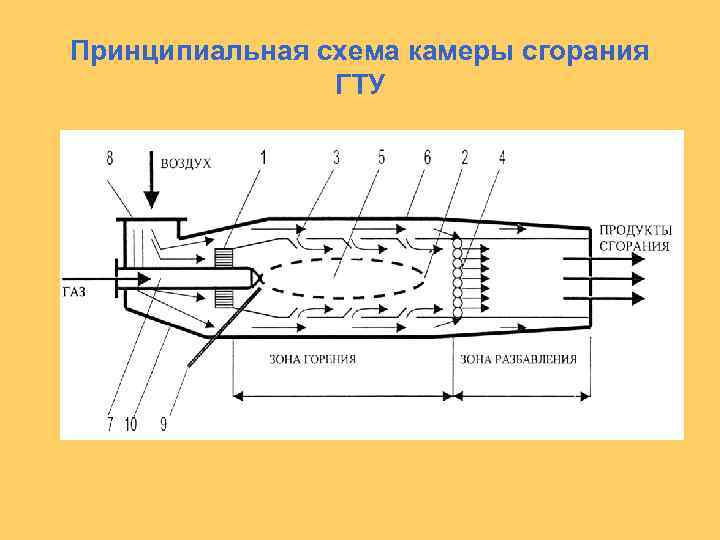 Принципиальная схема камеры сгорания ГТУ
Принципиальная схема камеры сгорания ГТУ
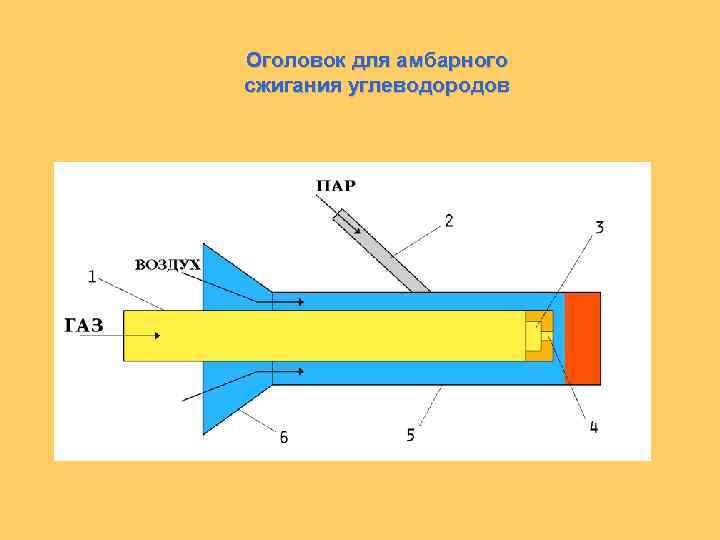 Оголовок для амбарного сжигания углеводородов
Оголовок для амбарного сжигания углеводородов
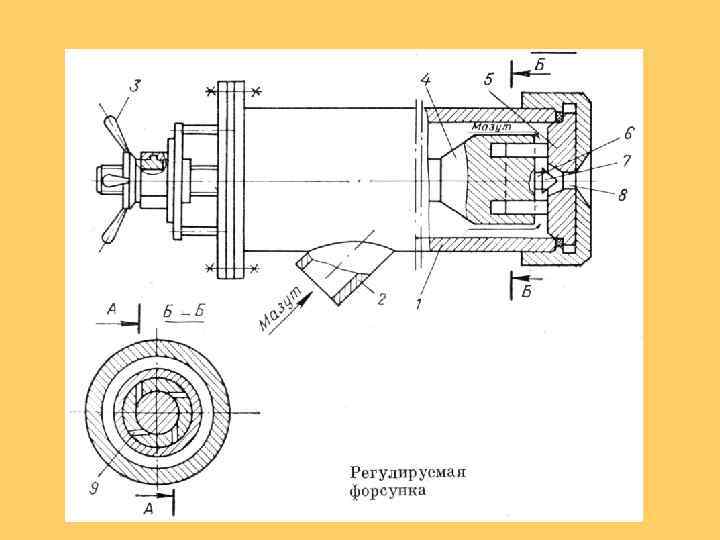
 ТИПЫ ФОРСУНОЧНЫХ УСТРОЙСТВ а) механические б) пневматические в) паровые г) комбинированные
ТИПЫ ФОРСУНОЧНЫХ УСТРОЙСТВ а) механические б) пневматические в) паровые г) комбинированные
 ВРЕМЯ ВЫГОРАНИЯ КАПЛИ ЖИДКОГО ТОПЛИВА
ВРЕМЯ ВЫГОРАНИЯ КАПЛИ ЖИДКОГО ТОПЛИВА


