Лекция 4_ткань.ppt
- Количество слайдов: 30

ТКАНИ Гистология — биологическая наука, изучающая закономерности развития, строения и жизнедеятельности тканей. Французский анатом Marie Francois Bichat (1771 -1802 гг. ) вводит в биологию термин «ТКАНЬ» и описывает 21 тип. В 1819 (от греч. histos — ткань и logos — учение) немецкий исследователь Paul Mayer вводит термин «Гистология» В 1839 г немецкий физиолог Theodore Schwann создаёт клеточную теорию Основоположник современной гистологии немецкий анатом Rudolf Kolliker в 1852 г вводит современную классификацию тканей ØЭпителиальная ØСоединительная (ткани внутренней среды) ØМышечная ØНервная
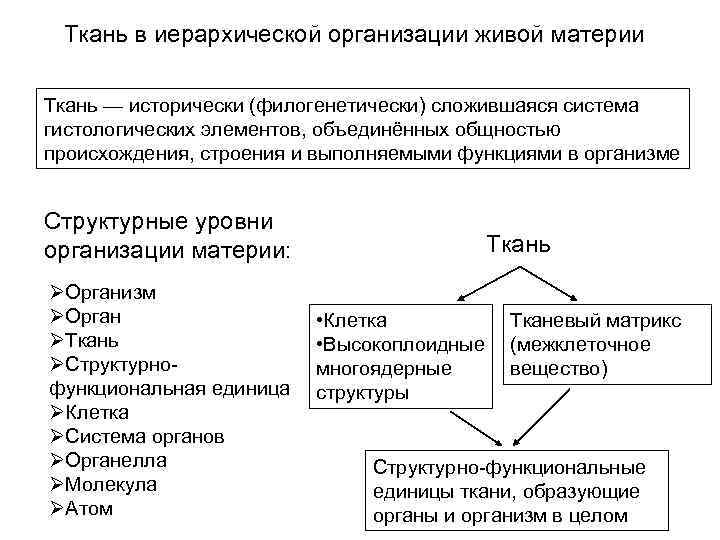
Ткань в иерархической организации живой материи Ткань — исторически (филогенетически) сложившаяся система гистологических элементов, объединённых общностью происхождения, строения и выполняемыми функциями в организме Структурные уровни организации материи: ØОрганизм ØОрган ØТкань ØСтруктурнофункциональная единица ØКлетка ØСистема органов ØОрганелла ØМолекула ØАтом Ткань • Клетка • Высокоплоидные многоядерные структуры Тканевый матрикс (межклеточное вещество) Структурно-функциональные единицы ткани, образующие органы и организм в целом

Клетка — главная тканеобразующая единица ØОднородные группы клеток образуют клеточные популяции ØПопуляции разных клеточных типов формируют разные ткани организма ØКлеточный тип включает понятие клеточные фенотипы, а также пластичность и границы нормы клеточного типа. ØКлетки с идентичным набором разрешённых к экспрессии генов относятся к одному клеточному типу. ØИзвестно более 200 клеточных типов. Каждая скелетная мышца уникальна по спектру входящих в её состав мышечных волокон. Фенотип мышцы генетически детерминирован, а экспрессия того или иного признака зависит от активности специфических генов, регулируемых нервной и гуморальной системами. При различных функциональных и патологических состояниях организма структурно-функциональные характеристики мышцы изменяются в широких пределах, что является проявлением мышечной пластичности. Типы мышечных волокон Миозин Митохонд рии Миогло бин Утомля емость Гликоген быстрые красные быстрый IIa много высокое медленно высокое быстрые белые IIb быстрый немного низкое утомля емые медленные медленны много высокое медленно низкое высокое
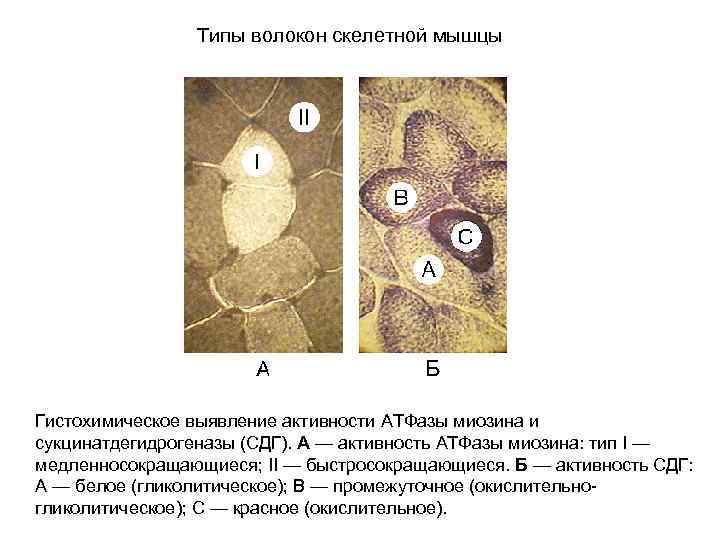
Типы волокон скелетной мышцы Гистохимическое выявление активности АТФазы миозина и сукцинатдегидрогеназы (СДГ). A — активность АТФазы миозина: тип I — медленносокращающиеся; II — быстросокращающиеся. Б — активность СДГ: А — белое (гликолитическое); B — промежуточное (окислительногликолитическое); C — красное (окислительное).
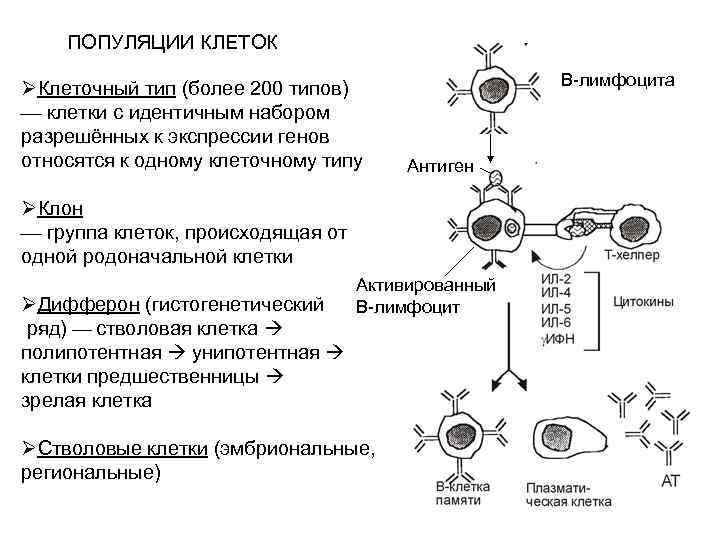
ПОПУЛЯЦИИ КЛЕТОК ØКлеточный тип (более 200 типов) клетки с идентичным набором разрешённых к экспрессии генов относятся к одному клеточному типу В-лимфоцита Антиген ØКлон группа клеток, происходящая от одной родоначальной клетки ØДифферон (гистогенетический ряд) стволовая клетка полипотентная унипотентная клетки предшественницы зрелая клетка Активированный В-лимфоцит ØСтволовые клетки (эмбриональные, региональные)

Гистогенез Миграция клеток. Конец адгезии начало адресной миграции клеток конец миграции начало адгезии. Межклеточные информационные взаимодействия. Клетки, занявшие определённое положение в системе развивающегося зародыша (морфогенетическое поле), получают позиционную информацию и приступают к выполнению программы детерминации и дифференцировки. Детерминация последовательное снижение проспективных потенций клетки. Дифференцировка реализация программы намеченной в ходе детерминации. Предифференцировка (строится система синтеза белка) протодифференцировка (начало синтеза специфического продукта) собственно дифференцировка (утрачивается способность к пролиферации) терминальная дифференцировка (выход на пик синтеза специфического продукта). Апоптоз генетически запрограммированное самоубийство клеток
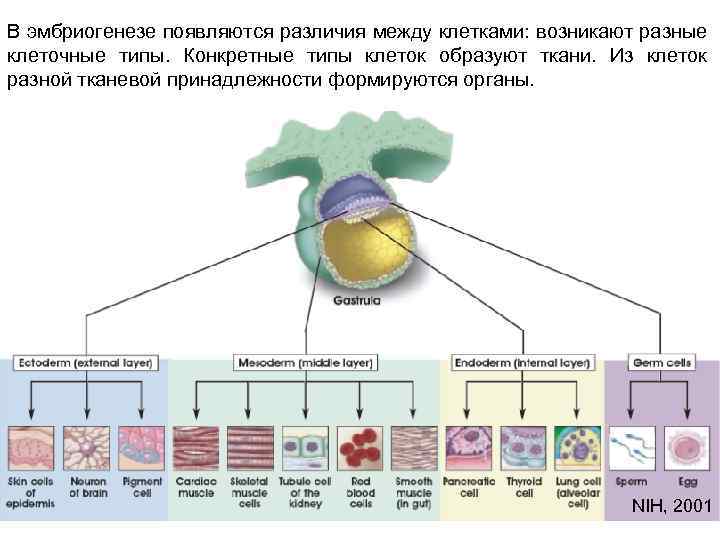
В эмбриогенезе появляются различия между клетками: возникают разные клеточные типы. Конкретные типы клеток образуют ткани. Из клеток разной тканевой принадлежности формируются органы. NIH, 2001

Миграция клеток 1. (1) Конец адгезии начало миграции. Исчезновение молекул адгезии из плазматических мембран и разборка адгезионных контактов позволяет клеткам начать миграцию. В эмбриогенезе клетки нервного гребня связаны при помощи трансмембранных гликопротеинов — молекул адгезии нервных клеток (N-CAM) и N-кадгерина. Момент исчезновения этих молекул адгезии совпадает с началом активного выселения клеток из нервного гребня. (2) Адресная миграция клеток. Узнавание мигрирующими клетками молекул адгезии на поверхности других клеток или во внеклеточном матриксе обеспечивает не случайную, а направленную миграцию клеток. Миграция клеток включает адгезию клеток к субстрату (межклеточному матриксу), образование цитоплазматических выростов (псевдоподий) по ходу движения и ретракцию заднего края клетки. Подвижность клеток обеспечивает актомиозиновый хемомеханический преобразователь, в том числе циклы полимеризации и деполимеризации актина. (3) Конец миграции начало адгезии. Миграция части клеток нервного гребня заканчивается в зачатке ганглиев, где клетки оказываются связанными при помощи молекул адгезии нервных клеток (N-CAM) и дифференцируются в нейроны.
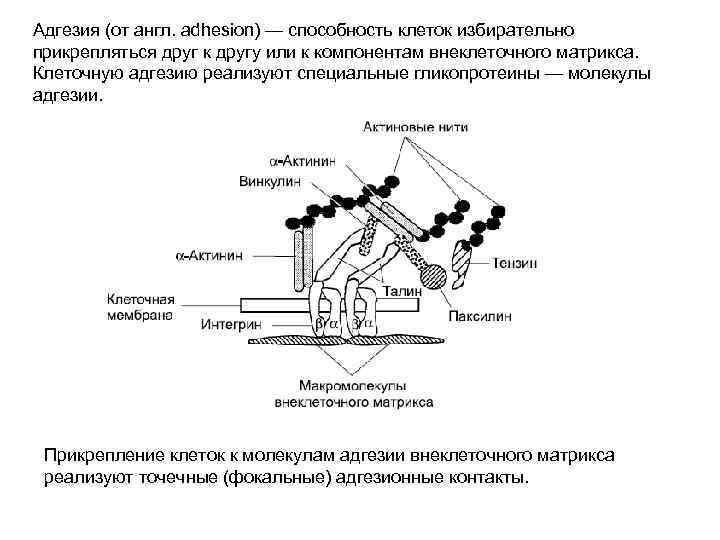
Адгезия (от англ. adhesion) — способность клеток избирательно прикрепляться друг к другу или к компонентам внеклеточного матрикса. Клеточную адгезию реализуют специальные гликопротеины — молекулы адгезии. Прикрепление клеток к молекулам адгезии внеклеточного матрикса реализуют точечные (фокальные) адгезионные контакты.
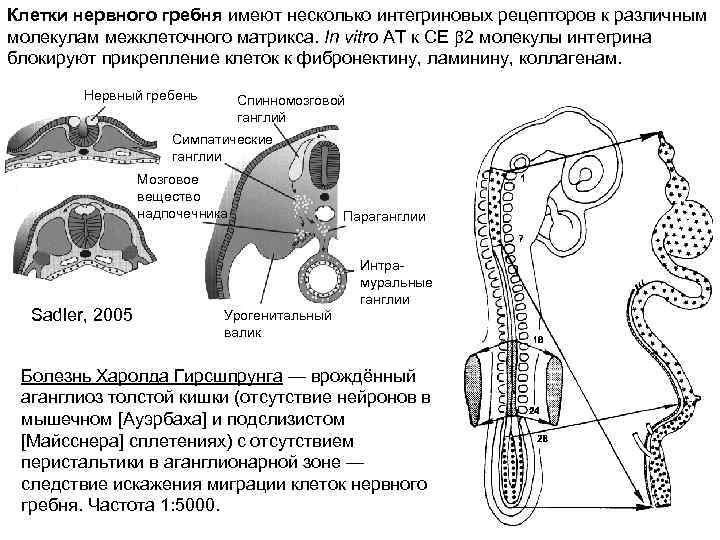
Клетки нервного гребня имеют несколько интегриновых рецепторов к различным молекулам межклеточного матрикса. In vitro АТ к СЕ 2 молекулы интегрина блокируют прикрепление клеток к фибронектину, ламинину, коллагенам. Нервный гребень Спинномозговой ганглий Симпатические ганглии Мозговое вещество надпочечника Sadler, 2005 Параганглии Интрамуральные ганглии Урогенитальный валик Болезнь Харолда Гирсшпрунга — врождённый аганглиоз толстой кишки (отсутствие нейронов в мышечном [Ауэрбаха] и подслизистом [Майсснера] сплетениях) с отсутствием перистальтики в аганглионарной зоне — следствие искажения миграции клеток нервного гребня. Частота 1: 5000.
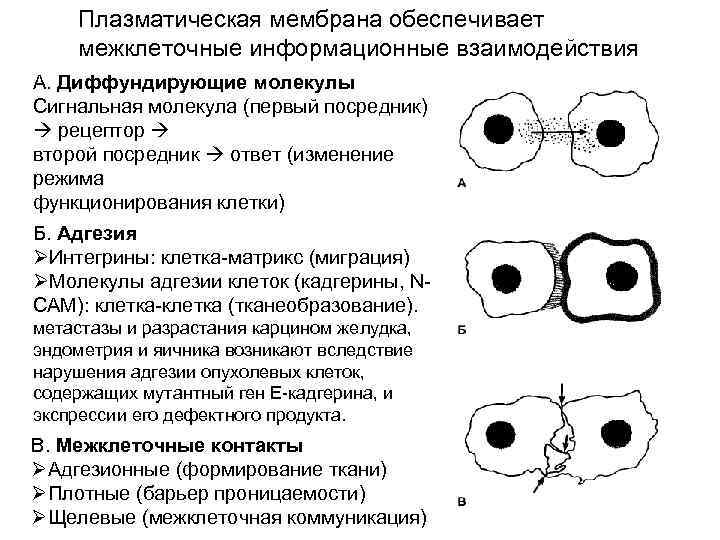
Плазматическая мембрана обеспечивает межклеточные информационные взаимодействия А. Диффундирующие молекулы Сигнальная молекула (первый посредник) рецептор второй посредник ответ (изменение режима функционирования клетки) Б. Адгезия ØИнтегрины: клетка-матрикс (миграция) ØМолекулы адгезии клеток (кадгерины, NCAM): клетка-клетка (тканеобразование). метастазы и разрастания карцином желудка, эндометрия и яичника возникают вследствие нарушения адгезии опухолевых клеток, содержащих мутантный ген E-кадгерина, и экспрессии его дефектного продукта. В. Межклеточные контакты ØАдгезионные (формирование ткани) ØПлотные (барьер проницаемости) ØЩелевые (межклеточная коммуникация)
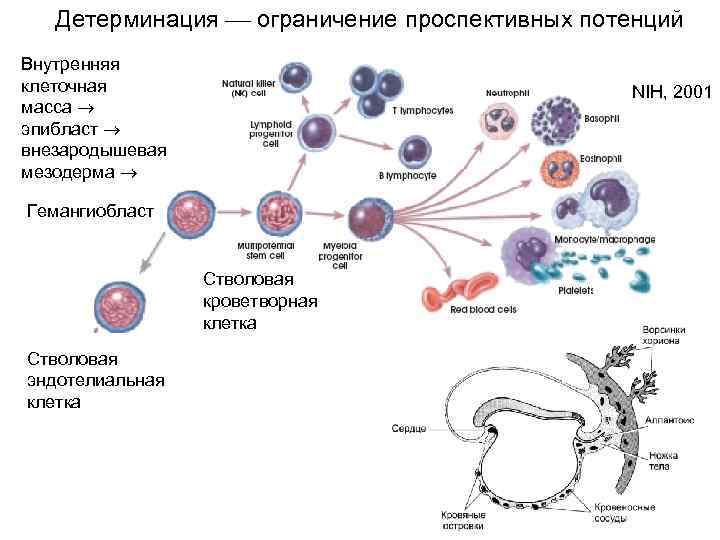
Детерминация ограничение проспективных потенций Внутренняя клеточная масса эпибласт внезародышевая мезодерма NIH, 2001 Гемангиобласт Стволовая кроветворная клетка Стволовая эндотелиальная клетка
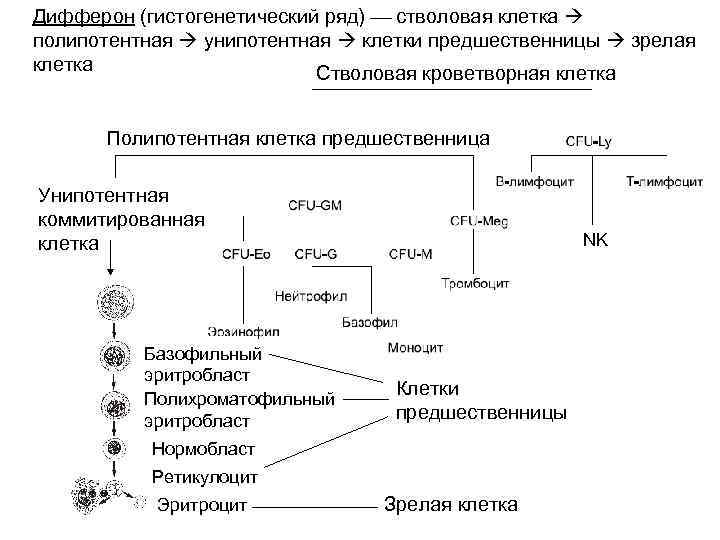
Дифферон (гистогенетический ряд) стволовая клетка полипотентная унипотентная клетки предшественницы зрелая клетка Стволовая кроветворная клетка Полипотентная клетка предшественница Унипотентная коммитированная клетка Базофильный эритробласт Полихроматофильный эритробласт NK Клетки предшественницы Нормобласт Ретикулоцит Эритроцит Зрелая клетка
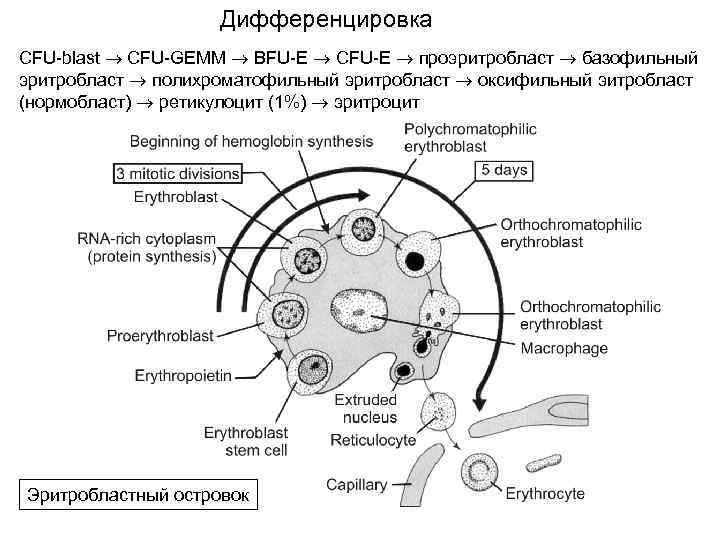
Дифференцировка CFU-blast CFU-GEMM BFU-E CFU-E проэритробласт базофильный эритробласт полихроматофильный эритробласт оксифильный эитробласт (нормобласт) ретикулоцит (1%) эритроцит Эритробластный островок
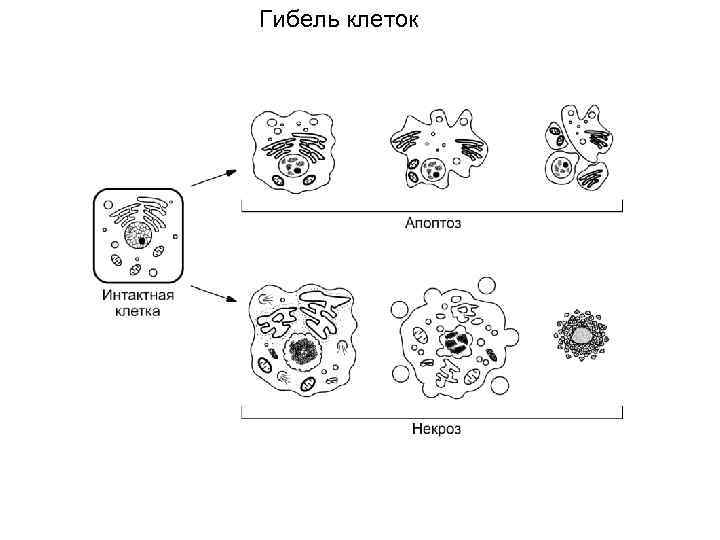
Гибель клеток

Программа апоптоза консервативна и универсальна от червя до человека Феноменология: Øактивация эндогенных протеаз Øконденсация клеточного ядра и деградация ядерной ДНК Благодаря апоптозу осуществляются: Øэмбриогенез Øгормон-зависимая инволюция клеток в менструальном цикле Øудаление лишних или потенциально опасных клеток (лимфоциты) Øудаление опухолевых клеток Øудаление инфицированных вирусом клеток (Т киллерами) Гены, контролирующие апоптоз: Øгены смерти (ICE – interleukin-1β-converting enzyme) Øанти-апоптозный ген (bcl-2) Апоптоз и болезни: ØМногие опухоли используют BCL-2 для подавления клеточной гибели ØЭкспрессия bcl-2 плохой прогноз рака кишечника, рака предстательной железы ØИнгибиторы апоптоза ограничивают размеры инфаркта (сердца, мозга)
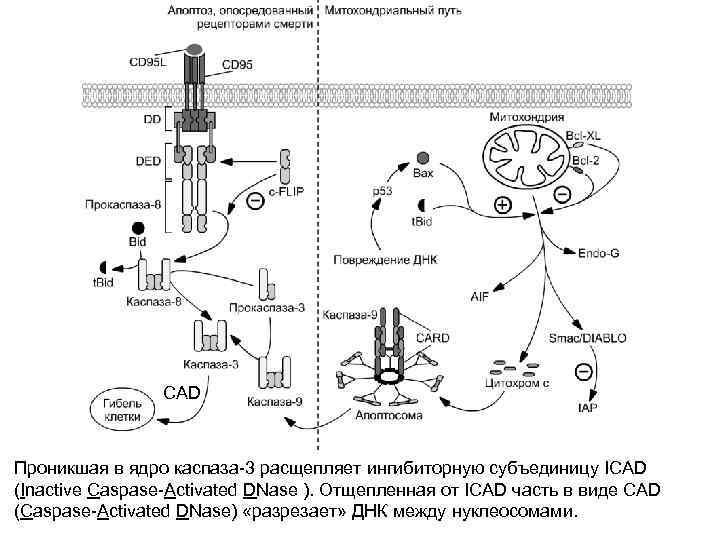
CAD Проникшая в ядро каспаза-3 расщепляет ингибиторную субъединицу ICAD (Inactive Caspase-Activated DNase ). Отщепленная от ICAD часть в виде CAD (Caspase-Activated DNase) «разрезает» ДНК между нуклеосомами.
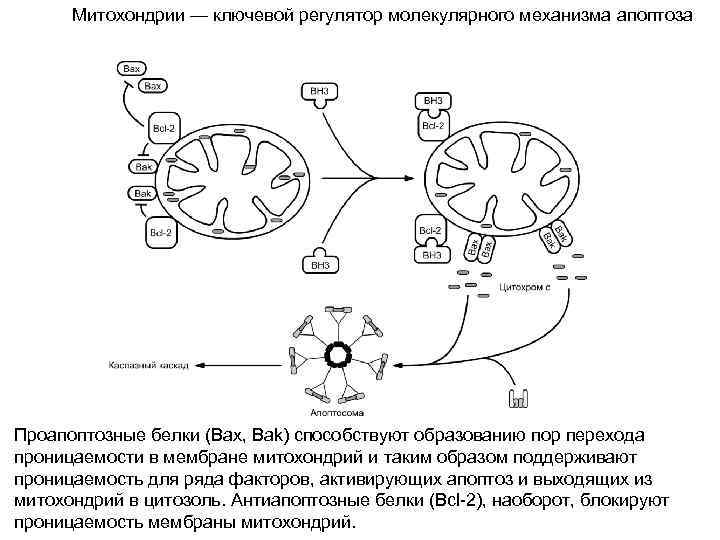
Митохондрии — ключевой регулятор молекулярного механизма апоптоза Проапоптозные белки (Bax, Bak) способствуют образованию пор перехода проницаемости в мембране митохондрий и таким образом поддерживают проницаемость для ряда факторов, активирующих апоптоз и выходящих из митохондрий в цитозоль. Антиапоптозные белки (Bcl-2), наоборот, блокируют проницаемость мембраны митохондрий.
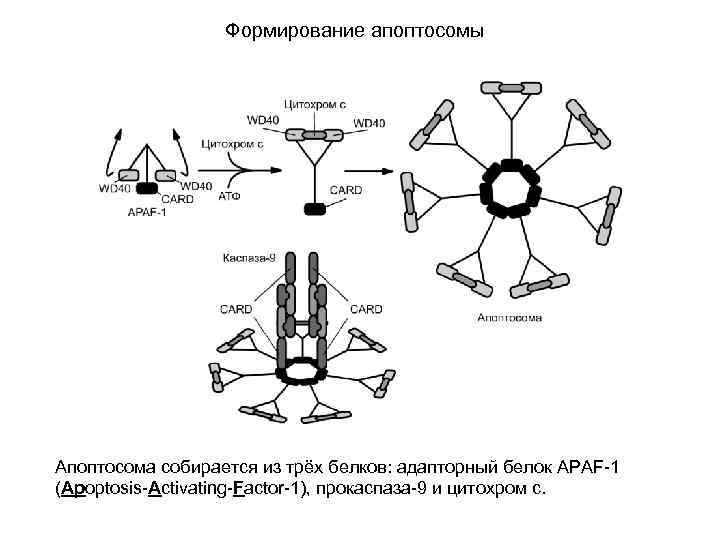
Формирование апоптосомы Апоптосома собирается из трёх белков: адапторный белок APAF-1 (Apoptosis-Activating-Factor-1), прокаспаза-9 и цитохром c.

Методы выявления апоптозных клеток Под действием каспаз в клетке, вступившей в апоптоз, появляются метки для последующего их распознавания и фагоцитоза. Подобной меткой служит принадлежащий к фосфолипидам внутреннего слоя плазматической мембраны фосфатидилсерин. В результате действия каспазы этот сигнал «выставляется» на поверхности клетки и распознаётся фагоцитом при участии молекулы CD 14. TUNEL-метод (Transferase mediated d. UTP Nick End Labeling) основан на выявлении 3’-ОН концов в молекуле ядерной ДНК, образующихся при её фрагментации в клетках, вступивших в апоптоз. 3'-Урацил, конъюгированный с биотином, с помощью терминальной дезоксинуклеотидил трансферазы (Td. T) включается в фрагменты ДНК. Далее биотинилированный нуклеотид выявляют с помощью стрептавидина, меченного пероксидазой хрена [стрептавидинбиотиновый метод, основанный на высокой аффинности (сродстве) биотина к стрептавидину].

Стволовые клетки Стволовыми клетками эмбриона, плода, или взрослого организма считаются клетки, способные длительное время воспроизводить себе подобные клетки и в течение жизни давать начало специализированным клеткам, образующих разные ткани организма. Тотипотентная (лат. totus — целый, полный) клетка обладает потенциалом дать начало всем специализированным клеткам, формирующих ткани эмбриона и обеспечивающих его развитие. Например, зигота и бластомеры по всем признакам относится к тотипотентным клеткам. Плюрипотентные (лат. plures — несколько, много) клетки дифференцируются в разные полипотентные клетки всех трёх зародышевых листков — экто-, энто- и мезодермы. Клетки внутренней клеточной массы бластоцисты относятся к плюрипотентным клеткам. Стволовые клетки эмбриона ØЭмбриональная стволовая клетка ØЭмбриональная клетка зародышевого пути Стволовые клетки взрослого организма
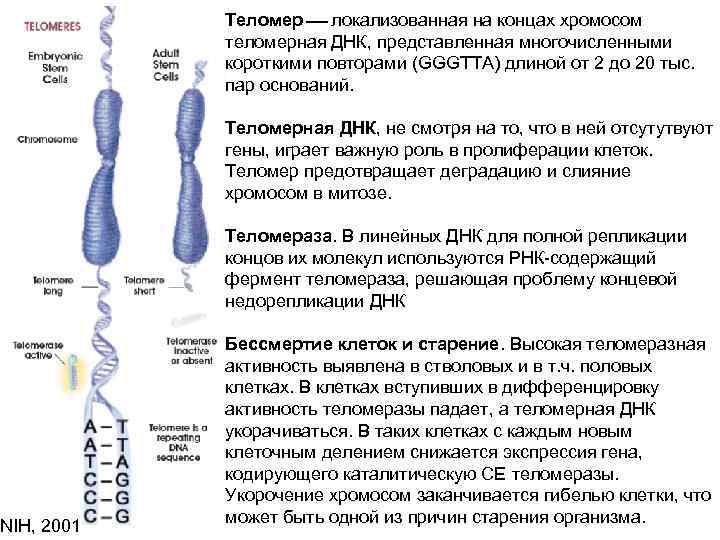
NIH, 2001 Теломер локализованная на концах хромосом теломерная ДНК, представленная многочисленными короткими повторами (GGGTTA) длиной от 2 до 20 тыс. пар оснований. Теломерная ДНК, не смотря на то, что в ней отсутутвуют гены, играет важную роль в пролиферации клеток. Теломер предотвращает деградацию и слияние хромосом в митозе. Теломераза. В линейных ДНК для полной репликации концов их молекул используются РНК-содержащий фермент теломераза, решающая проблему концевой недорепликации ДНК Бессмертие клеток и старение. Высокая теломеразная активность выявлена в стволовых и в т. ч. половых клетках. В клетках вступивших в дифференцировку активность теломеразы падает, а теломерная ДНК укорачиваться. В таких клетках с каждым новым клеточным делением снижается экспрессия гена, кодирующего каталитическую СЕ теломеразы. Укорочение хромосом заканчивается гибелью клетки, что может быть одной из причин старения организма.
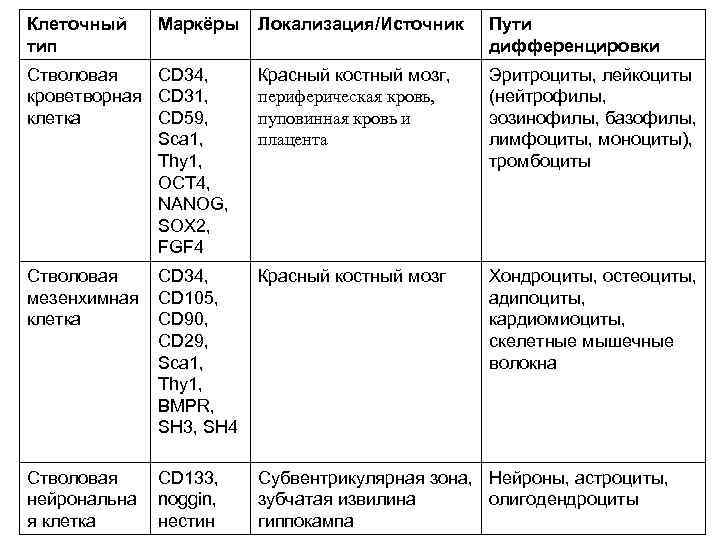
Клеточный тип Маркёры Локализация/Источник Пути дифференцировки Стволовая CD 34, кроветворная CD 31, клетка CD 59, Sca 1, Thy 1, OCT 4, NANOG, SOX 2, FGF 4 Красный костный мозг, периферическая кровь, пуповинная кровь и плацента Эритроциты, лейкоциты (нейтрофилы, эозинофилы, базофилы, лимфоциты, моноциты), тромбоциты Стволовая CD 34, мезенхимная CD 105, клетка CD 90, CD 29, Sca 1, Thy 1, BMPR, SH 3, SH 4 Красный костный мозг Хондроциты, остеоциты, адипоциты, кардиомиоциты, скелетные мышечные волокна Стволовая нейрональна я клетка Субвентрикулярная зона, Нейроны, астроциты, зубчатая извилина олигодендроциты гиппокампа CD 133, noggin, нестин
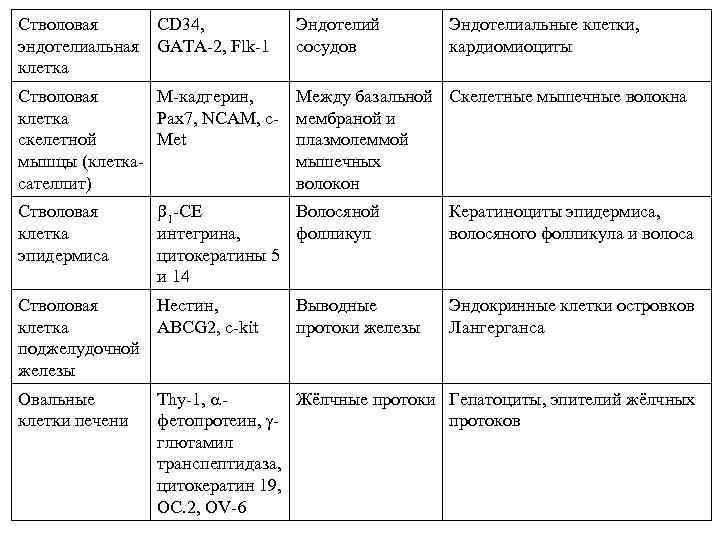
Стволовая эндотелиальная клетка CD 34, GATA-2, Flk-1 Эндотелий сосудов Эндотелиальные клетки, кардиомиоциты Стволовая М-кадгерин, Между базальной Скелетные мышечные волокна клетка Pax 7, NCAM, c- мембраной и скелетной Met плазмолеммой мышцы (клеткамышечных сателлит) волокон Стволовая клетка эпидермиса 1 -СЕ Волосяной интегрина, фолликул цитокератины 5 и 14 Стволовая Нестин, клетка ABCG 2, c-kit поджелудочной железы Овальные клетки печени Выводные протоки железы Кератиноциты эпидермиса, волосяного фолликула и волоса Эндокринные клетки островков Лангерганса Thy-1, Жёлчные протоки Гепатоциты, эпителий жёлчных фетопротеин, протоков глютамил транспептидаза, цитокератин 19, OC. 2, OV-6
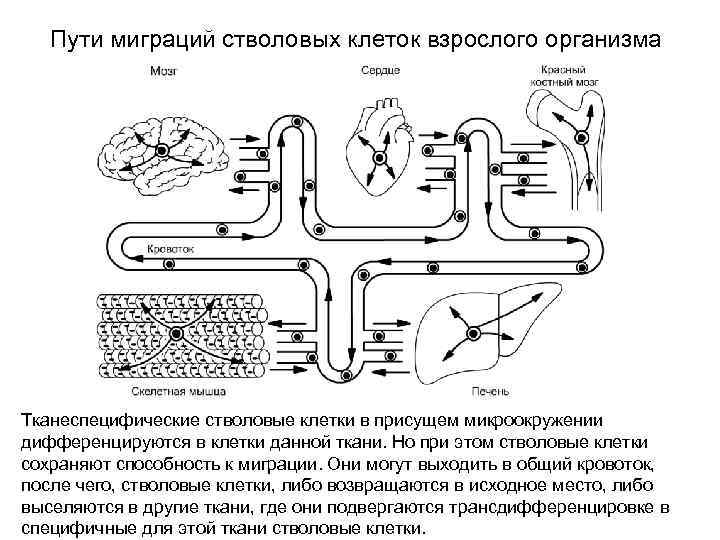
Пути миграций стволовых клеток взрослого организма Тканеспецифические стволовые клетки в присущем микроокружении дифференцируются в клетки данной ткани. Но при этом стволовые клетки сохраняют способность к миграции. Они могут выходить в общий кровоток, после чего, стволовые клетки, либо возвращаются в исходное место, либо выселяются в другие ткани, где они подвергаются трансдифференцировке в специфичные для этой ткани стволовые клетки.
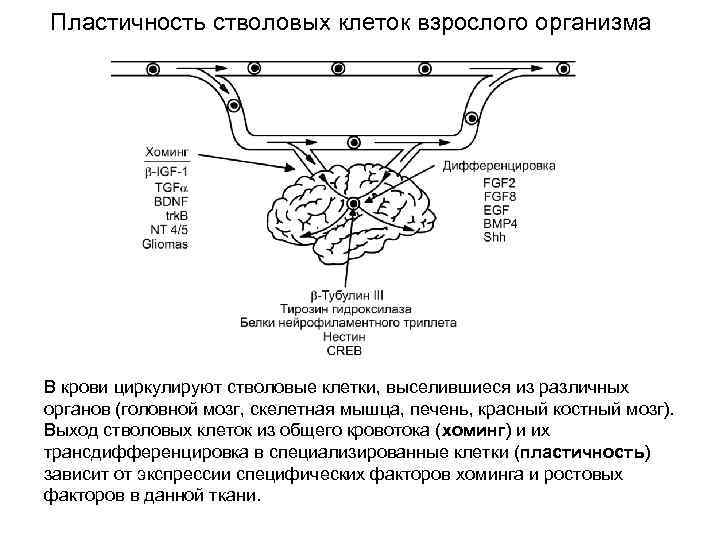
Пластичность стволовых клеток взрослого организма В крови циркулируют стволовые клетки, выселившиеся из различных органов (головной мозг, скелетная мышца, печень, красный костный мозг). Выход стволовых клеток из общего кровотока (хоминг) и их трансдифференцировка в специализированные клетки (пластичность) зависит от экспрессии специфических факторов хоминга и ростовых факторов в данной ткани.

Получение стволовых кроветворных клеток Красный костный мозг. В среднем удаётся выделить одну стволовую кроветворную клетку на каждые 100 000 полученных аспирацией клеток. Периферическая кровь. Инъекция колониестимулирующего фактора гранулоцитов за несколько дней до забора крови стимулирует выход стволовых кроветворная клеток из красного костного мозга в кровь. Пуповинная кровь и плацента. Возможно получить несколько миллионов стволовых кроветворных клеток, что недостаточно для трансплантации взрослому (требуется от 7 до 10 миллионов клеток на 1 кг массы тела), но может быть адекватным для трансплантации детям. Клиническое применение стволовых кроветворных клеток Трансплантация стволовых кроветворных клеток производится при лечении ряда врождённых заболеваний крови (апластическая анемия, -талассемия, серповидноклеточная анемия, лимфопролиферативный синдром, связанный с Х-хромосомой и др. ) и гемобластозов (лимфом и лейкемий), при химиотерапии рака для поддержания пула полипотентных кроветворных клеток красного костного мозга.

Сортировка клеток методом проточной цитометрии В культуральной среде специфические АТ, конъюгированные с флуоресцентным зондом, связываются с Аг на поверхности клеток, например, с CD 34+ на мембране стволовой кроветворной клетки. Под давлением клетки проходят по капилляру, где меченые CD 34+ клетки под действием лучей лазера получают отрицательный электрический заряд. В электрическом поле происходит разделение клеток, несущих положительный или отрицательный заряд.
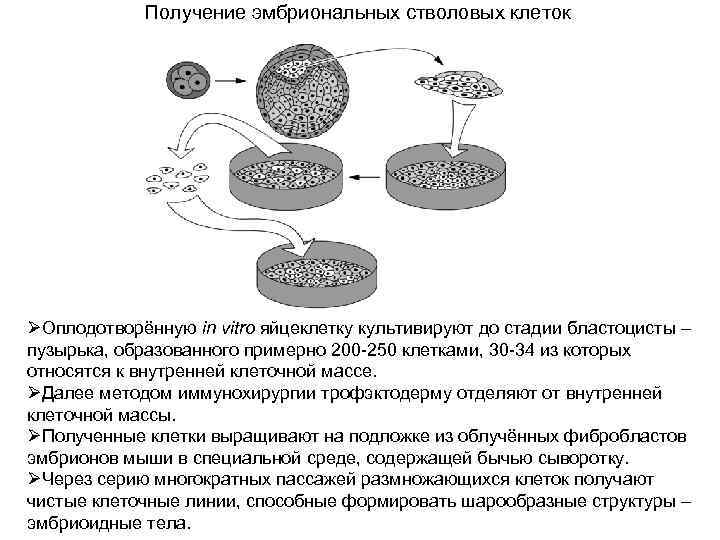
Получение эмбриональных стволовых клеток ØОплодотворённую in vitro яйцеклетку культивируют до стадии бластоцисты – пузырька, образованного примерно 200 -250 клетками, 30 -34 из которых относятся к внутренней клеточной массе. ØДалее методом иммунохирургии трофэктодерму отделяют от внутренней клеточной массы. ØПолученные клетки выращивают на подложке из облучённых фибробластов эмбрионов мыши в специальной среде, содержащей бычью сыворотку. ØЧерез серию многократных пассажей размножающихся клеток получают чистые клеточные линии, способные формировать шарообразные структуры – эмбриоидные тела.

Клиническое применение эмбриональных стволовых клеток Подготовленные для трансплантации стволовые клетки должны иметь предсказуемые и воспроизводимые характеристики: Øактивно размножаться с образованием достаточного количества клеток для восстановления утраченной ткани; Øдифференцироваться в требуемые клеточные типы; Øсохранять жизнеспособность; Øинтегрироваться с клетками органа-реципиента; Øвыполнять свойственные для органа-реципиента функции. Для безопасной трансплантации стволовых клеток необходимо исключить любое возможное негативное воздействие трансплантированных клеток на организм реципиента. В будущем технология эмбриональных стволовых клеток может быть применена для лечения таких заболеваний, как инсулин-зависимый сахарный диабет (тип I, юношеский диабет), болезнь Паркинсона, несовершенный остеогенез, мышечная дистрофия Дюшенна, повреждения спинного мозга, сердечная недостаточность и др.
Лекция 4_ткань.ppt