Титан Лисова М..ppt
- Количество слайдов: 13
 Титан Выполнила: Лисова Мария 11 ФМ Учитель: И. П. Сухарцова
Титан Выполнила: Лисова Мария 11 ФМ Учитель: И. П. Сухарцова
 Положение титана в периодической системе химических элементов и строение атома. u u u Титан — элемент главной подгруппы IV группы. Его электронная формула следующая: +22 Тi 1 s 2|2 s 22 p 6|3 s 23 p 63 d 2|4 s 2 Как и у многих других d элементов, в атоме титана Тi подвижными являются не только электроны наружного энергетического уровня, но и два электрона d подуровня. Поэтому титан в соединениях проявляет степени окисления + 2 и +4 (реже +3): Ti. SO 4 , Ti. O 2, Ca. Ti. O 3.
Положение титана в периодической системе химических элементов и строение атома. u u u Титан — элемент главной подгруппы IV группы. Его электронная формула следующая: +22 Тi 1 s 2|2 s 22 p 6|3 s 23 p 63 d 2|4 s 2 Как и у многих других d элементов, в атоме титана Тi подвижными являются не только электроны наружного энергетического уровня, но и два электрона d подуровня. Поэтому титан в соединениях проявляет степени окисления + 2 и +4 (реже +3): Ti. SO 4 , Ti. O 2, Ca. Ti. O 3.
 Нахождение u u в природе Важнейшими минералами, содержащими титан, являются: титаномагнетиты Fe. Ti. O 3 *n. Fe 3 O 4, ильменит Fe. Ti. O 3, рутил Ti. O 2 и др. Титановые руды распространены относительно широко, но содержание в них титана небольшое.
Нахождение u u в природе Важнейшими минералами, содержащими титан, являются: титаномагнетиты Fe. Ti. O 3 *n. Fe 3 O 4, ильменит Fe. Ti. O 3, рутил Ti. O 2 и др. Титановые руды распространены относительно широко, но содержание в них титана небольшое.
 Физические свойства u Титан — серебристо белый металл. Сравнительно легкий — немного тяжелее алюминия, но примерно в три раза прочнее его. Тугоплавкий (1665°С). В обычных условиях отличается высокой прочностью и вязкостью. Поддается различным видам обработки.
Физические свойства u Титан — серебристо белый металл. Сравнительно легкий — немного тяжелее алюминия, но примерно в три раза прочнее его. Тугоплавкий (1665°С). В обычных условиях отличается высокой прочностью и вязкостью. Поддается различным видам обработки.
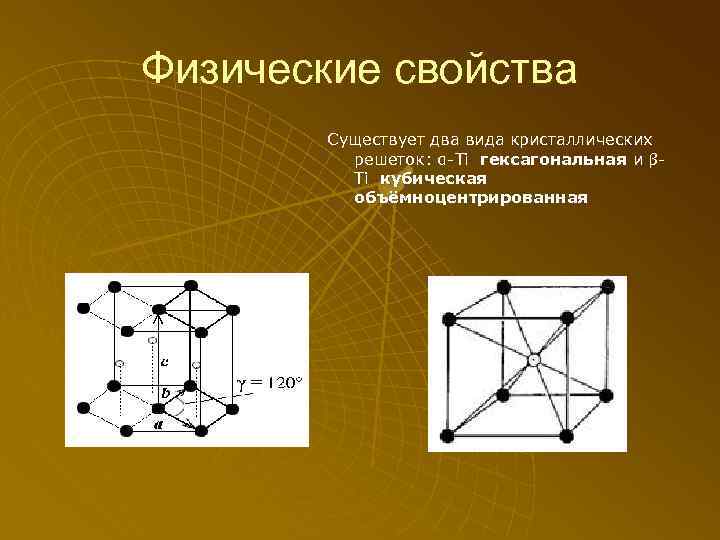 Физические свойства Существует два вида кристаллических решеток: α Ti гексагональная и β Ti кубическая объёмноцентрированная
Физические свойства Существует два вида кристаллических решеток: α Ti гексагональная и β Ti кубическая объёмноцентрированная
 Химические свойства u Титан, как и алюминий, довольно активный металл. Однако благодаря образованию на поверхности металла плотной защитной оксидной пленки он обладает исключительно высокой стойкостью против коррозии превышающей стойкость нержавеющей стали. При обычных условиях на титан не действуют ни кислород воздуха, ни морская вода, ни даже царская водка. При повышенной температуре его химическая активность повы шается. Так, например, титан реагирует с хлором:
Химические свойства u Титан, как и алюминий, довольно активный металл. Однако благодаря образованию на поверхности металла плотной защитной оксидной пленки он обладает исключительно высокой стойкостью против коррозии превышающей стойкость нержавеющей стали. При обычных условиях на титан не действуют ни кислород воздуха, ни морская вода, ни даже царская водка. При повышенной температуре его химическая активность повы шается. Так, например, титан реагирует с хлором:
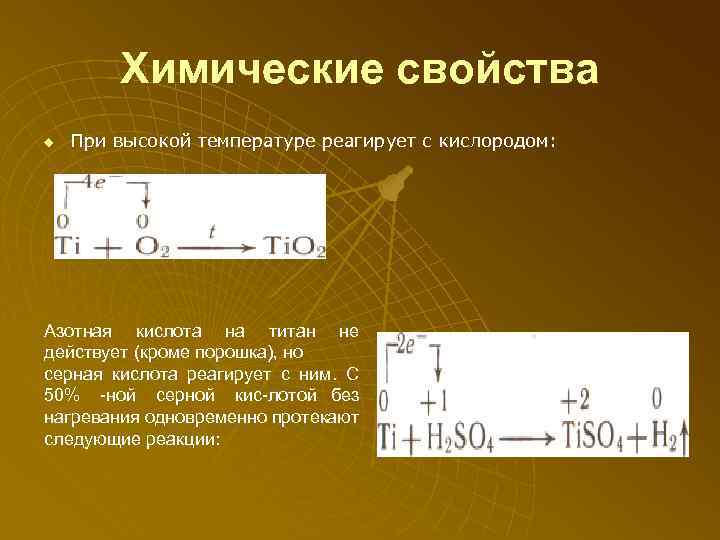 Химические свойства u При высокой температуре реагирует с кислородом: Азотная кислота на титан не действует (кроме порошка), но серная кислота реагирует с ним. С 50% ной серной кис лотой без нагревания одновременно протекают следующие реакции:
Химические свойства u При высокой температуре реагирует с кислородом: Азотная кислота на титан не действует (кроме порошка), но серная кислота реагирует с ним. С 50% ной серной кис лотой без нагревания одновременно протекают следующие реакции:
 Химические свойства 1)Свойства оксида. Диоксид титана амфотерен, то есть проявляет как осно вные, так и кислотные свойства (хотя реагирует главным образом с концентрированными кислотами). Медленно растворяется в концентрированной серной кислоте, образуя соответствующие соли четырёхвалентного титана: Ti. O 2 + 2 H 2 SO 4 → Ti(SO 4)2 + 2 H 2 O В концентрированных растворах щелочей или при сплавлении с ними образуются титанаты — соли титановой кислоты (амфотерного гидроксида титана Ti. O(OH)2) Ti. O 2 + 2 Na. OH → Na 2 Ti. O 3 + H 2 O
Химические свойства 1)Свойства оксида. Диоксид титана амфотерен, то есть проявляет как осно вные, так и кислотные свойства (хотя реагирует главным образом с концентрированными кислотами). Медленно растворяется в концентрированной серной кислоте, образуя соответствующие соли четырёхвалентного титана: Ti. O 2 + 2 H 2 SO 4 → Ti(SO 4)2 + 2 H 2 O В концентрированных растворах щелочей или при сплавлении с ними образуются титанаты — соли титановой кислоты (амфотерного гидроксида титана Ti. O(OH)2) Ti. O 2 + 2 Na. OH → Na 2 Ti. O 3 + H 2 O
 2)Свойства гидроксида. Оксид Ti (IV) с водой не взаимодействует , поэтому гидроксид Ti (OH)4 получают косвенным путём , например: Ti. Cl 4 + 4 Na. OH = Ti (OH)4 + 4 Na. Cl Гидроксид титана (IV) окрашен в белый цвет. Он амфотерен, причём и основные и кислотные его свойства выражены очень слабо. Свежеосаждённый Ti (OH)4, α–форма, растворяется в кислотах (например, в H 2 SO 4) с образованием титанил–иона Ti. O 2+: Ti (OH)4 + H 2 SO 4 = Ti. OSO 4 + 3 H 2 O Если концентрированная серная кислота берётся в избытке, образуется комплексные соединения состава [Ti. O(SO 4)2]2– или [Ti (SO 4)3]2–: Ti (OH)4 + 2 H 2 SO 4 = H 2[Ti. O(SO 4)2] + 2 H 2 O Ti (OH)4 + 3 H 2 SO 4 = H 2[Ti (SO 4)3] + 4 H 2 O
2)Свойства гидроксида. Оксид Ti (IV) с водой не взаимодействует , поэтому гидроксид Ti (OH)4 получают косвенным путём , например: Ti. Cl 4 + 4 Na. OH = Ti (OH)4 + 4 Na. Cl Гидроксид титана (IV) окрашен в белый цвет. Он амфотерен, причём и основные и кислотные его свойства выражены очень слабо. Свежеосаждённый Ti (OH)4, α–форма, растворяется в кислотах (например, в H 2 SO 4) с образованием титанил–иона Ti. O 2+: Ti (OH)4 + H 2 SO 4 = Ti. OSO 4 + 3 H 2 O Если концентрированная серная кислота берётся в избытке, образуется комплексные соединения состава [Ti. O(SO 4)2]2– или [Ti (SO 4)3]2–: Ti (OH)4 + 2 H 2 SO 4 = H 2[Ti. O(SO 4)2] + 2 H 2 O Ti (OH)4 + 3 H 2 SO 4 = H 2[Ti (SO 4)3] + 4 H 2 O
 u Оксид титана (III) Ti 2 O 3 не взаимодействует с водой, поэтому соответствующий гидроксид получают косвенным путём: Ti. Cl 3 + 3 Na. OH = Ti (OH)3↓ + 3 Na. Cl Ti (OH)3 представляет собой осадок серо–фиолетового цвета. Гидроксид титана (III) обладает только основными свойствами. Он взаимодействует с кислотами, образуя соответствующие соли: 2 Ti (OH)3 + 3 H 2 SO 4 = Ti 2(SO 4)3 + 6 H 2 O
u Оксид титана (III) Ti 2 O 3 не взаимодействует с водой, поэтому соответствующий гидроксид получают косвенным путём: Ti. Cl 3 + 3 Na. OH = Ti (OH)3↓ + 3 Na. Cl Ti (OH)3 представляет собой осадок серо–фиолетового цвета. Гидроксид титана (III) обладает только основными свойствами. Он взаимодействует с кислотами, образуя соответствующие соли: 2 Ti (OH)3 + 3 H 2 SO 4 = Ti 2(SO 4)3 + 6 H 2 O
 Применение u Титан и его сплавы в связи с их легкостью, прочностью, термической и коррозионной стойкостью при меняются для изготовления деталей самолетов, космиче ских кораблей, ракет, подводных лодок, трубопроводов, котлов высокого давления, различных аппаратов для хи мической промышленности. Титан широко используется в виде листов для обшивки корпусов судов, обеспечивающих высокую прочность и стойкость в морской воде.
Применение u Титан и его сплавы в связи с их легкостью, прочностью, термической и коррозионной стойкостью при меняются для изготовления деталей самолетов, космиче ских кораблей, ракет, подводных лодок, трубопроводов, котлов высокого давления, различных аппаратов для хи мической промышленности. Титан широко используется в виде листов для обшивки корпусов судов, обеспечивающих высокую прочность и стойкость в морской воде.
 u u Титан, как и тантал, не действует на живые ткани организма, поэтому он применяется в хирургии для скрепления костей при переломах. Высокой кроющей способностью обладают титановые белила, основной составной частью которых является оксид титана (IV) Тi. O 2.
u u Титан, как и тантал, не действует на живые ткани организма, поэтому он применяется в хирургии для скрепления костей при переломах. Высокой кроющей способностью обладают титановые белила, основной составной частью которых является оксид титана (IV) Тi. O 2.
 Источники информации u u http: //ru. wikipedia. org/wiki/%D 0%A 2%D 0%B 8%D 1%82%D 0%B 0%D 0% BD_%28%D 1%8 D%D 0%BB%D 0%B 5%D 0%BC%D 0%B 5%D 0%BD%D 1% 82%29 http: //chem 100. ru/elem. php? n=22
Источники информации u u http: //ru. wikipedia. org/wiki/%D 0%A 2%D 0%B 8%D 1%82%D 0%B 0%D 0% BD_%28%D 1%8 D%D 0%BB%D 0%B 5%D 0%BC%D 0%B 5%D 0%BD%D 1% 82%29 http: //chem 100. ru/elem. php? n=22


