типы химических реакций 8 класс.pptx
- Количество слайдов: 23
 Типы химических реакций Вострецов Олег Игоревич Учитель химии 30. 12
Типы химических реакций Вострецов Олег Игоревич Учитель химии 30. 12
 • Химическая реакция — превращение одного или нескольких исходных веществ в отличающиеся от них по химическому составу или строению вещества (продукты реакции). • Ca. O+H 2 O=Ca(OH)2 • 4 HNO 3=2 H 2 O+4 NO 2+O 2 • Cu. SO 4+Fe=Fe. SO 4+Cu • Ag. NO 3+KBr=Ag. Br +КNO 3 • SO 2+O 2 SO 3 • 4 Fe(OH)2+2 H 2 O+O 2=4 Fe(OH)3 • Что объединяет все эти реакции? • В чём их отличие? • Как мы можем назвать процесс, который протекает?
• Химическая реакция — превращение одного или нескольких исходных веществ в отличающиеся от них по химическому составу или строению вещества (продукты реакции). • Ca. O+H 2 O=Ca(OH)2 • 4 HNO 3=2 H 2 O+4 NO 2+O 2 • Cu. SO 4+Fe=Fe. SO 4+Cu • Ag. NO 3+KBr=Ag. Br +КNO 3 • SO 2+O 2 SO 3 • 4 Fe(OH)2+2 H 2 O+O 2=4 Fe(OH)3 • Что объединяет все эти реакции? • В чём их отличие? • Как мы можем назвать процесс, который протекает?
 q. Химические реакции происходят: Ø при смешении или физическом контакте реагентов самопроизвольно Ø при нагревании Ø при участии катализаторов Ø действии света Ø электрического тока Ø механического воздействия и т. п.
q. Химические реакции происходят: Ø при смешении или физическом контакте реагентов самопроизвольно Ø при нагревании Ø при участии катализаторов Ø действии света Ø электрического тока Ø механического воздействия и т. п.
 • Все реакции сопровождаются тепловыми эффектами. • При разрыве химических связей в реагентах выделяется энергия, которая, в основном, идет на образование новых химических связей.
• Все реакции сопровождаются тепловыми эффектами. • При разрыве химических связей в реагентах выделяется энергия, которая, в основном, идет на образование новых химических связей.
 • Реакции, протекающие с выделением теплоты и света называются - РЕАКЦИЯМИ ГОРЕНИЯ • Реакции, протекающие с выделением теплоты, называются – ЭКЗОТЕРМИЧЕСКИМИ (+Q) (от греч. «экзо» – наружу) 4 Al+3 O 2=2 Al 2 O 3+Q • Протекающие с поглощением теплоты – ЭНДОТЕРМИЧЕСКИМИ (-Q) (от греч. «эндо» – внутрь) N 2+O 2 2 NO-Q
• Реакции, протекающие с выделением теплоты и света называются - РЕАКЦИЯМИ ГОРЕНИЯ • Реакции, протекающие с выделением теплоты, называются – ЭКЗОТЕРМИЧЕСКИМИ (+Q) (от греч. «экзо» – наружу) 4 Al+3 O 2=2 Al 2 O 3+Q • Протекающие с поглощением теплоты – ЭНДОТЕРМИЧЕСКИМИ (-Q) (от греч. «эндо» – внутрь) N 2+O 2 2 NO-Q
 Какие условия должны выполняться, чтобы произошла химическая реакция? 1. Необходимо, чтобы реагирующие вещества соприкоснулись и чем больше площадь их соприкосновения, тем быстрее произойдет химическая реакция. 2. Некоторые реакции идут без нагревания, и только для некоторых реакций оно необходимо. 3. Некоторые реакции протекают под действием электрического тока и света.
Какие условия должны выполняться, чтобы произошла химическая реакция? 1. Необходимо, чтобы реагирующие вещества соприкоснулись и чем больше площадь их соприкосновения, тем быстрее произойдет химическая реакция. 2. Некоторые реакции идут без нагревания, и только для некоторых реакций оно необходимо. 3. Некоторые реакции протекают под действием электрического тока и света.
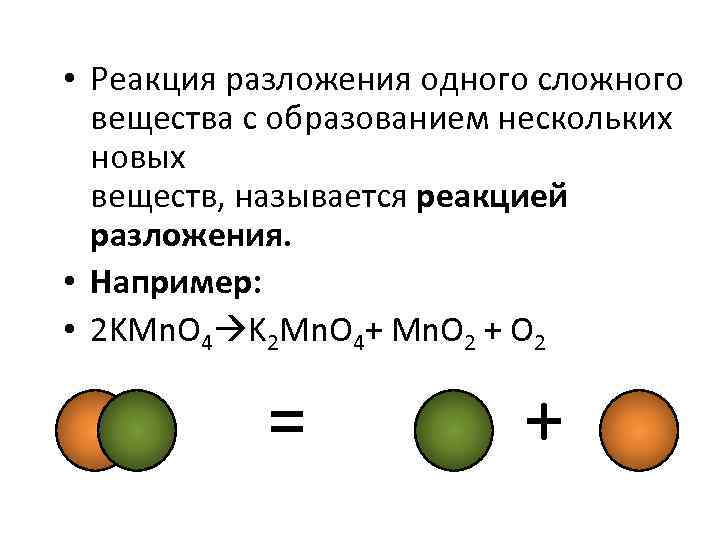 • Реакция разложения одного сложного вещества с образованием нескольких новых веществ, называется реакцией разложения. • Например: • 2 KMn. O 4 K 2 Mn. O 4+ Mn. O 2 + O 2 = +
• Реакция разложения одного сложного вещества с образованием нескольких новых веществ, называется реакцией разложения. • Например: • 2 KMn. O 4 K 2 Mn. O 4+ Mn. O 2 + O 2 = +
 Подавляющее большинство реакций разложения эндотермичны и требуют для своего проведения повышенной температуры. Например: 2 Hg. O – 2 Hg + O 2 Ca. CO 3 – Ca. O + CO 2 Cu(OH)2 – Cu. O + H 2 O 2 Al(OH)3 – Al 2 O 3 + 3 H 2 O
Подавляющее большинство реакций разложения эндотермичны и требуют для своего проведения повышенной температуры. Например: 2 Hg. O – 2 Hg + O 2 Ca. CO 3 – Ca. O + CO 2 Cu(OH)2 – Cu. O + H 2 O 2 Al(OH)3 – Al 2 O 3 + 3 H 2 O
 Выберите уравнения реакций разложения: 1) 2) 3) 4) 5) 6) 7) 8) Ca. O + CO 2 = Ca. CO 3 CO 2 + 2 Na. OH = Na 2 CO 3 + H 2 O Fe + S = Fe. S 2 H 2 O = 2 H 2 + O 2↑ Cu. O + H 2 = Cu + H 2 O Zn + 2 HCl = Zn. Cl 2 + H 2↑ Zn. O + H 2 SO 4 = Zn. SO 4 + H 2 O Cu(OH)2 = Cu. O + H 2 O
Выберите уравнения реакций разложения: 1) 2) 3) 4) 5) 6) 7) 8) Ca. O + CO 2 = Ca. CO 3 CO 2 + 2 Na. OH = Na 2 CO 3 + H 2 O Fe + S = Fe. S 2 H 2 O = 2 H 2 + O 2↑ Cu. O + H 2 = Cu + H 2 O Zn + 2 HCl = Zn. Cl 2 + H 2↑ Zn. O + H 2 SO 4 = Zn. SO 4 + H 2 O Cu(OH)2 = Cu. O + H 2 O
 Реакции соединения – химические реакции, в которых из двух или нескольких менее сложных по элементному составу веществ получается более сложное вещество Например: NH 3 + CO 2 + H 2 O = NH 4 HCO 3 Подавляющее большинство реакций соединения экзотермичны. + =
Реакции соединения – химические реакции, в которых из двух или нескольких менее сложных по элементному составу веществ получается более сложное вещество Например: NH 3 + CO 2 + H 2 O = NH 4 HCO 3 Подавляющее большинство реакций соединения экзотермичны. + =
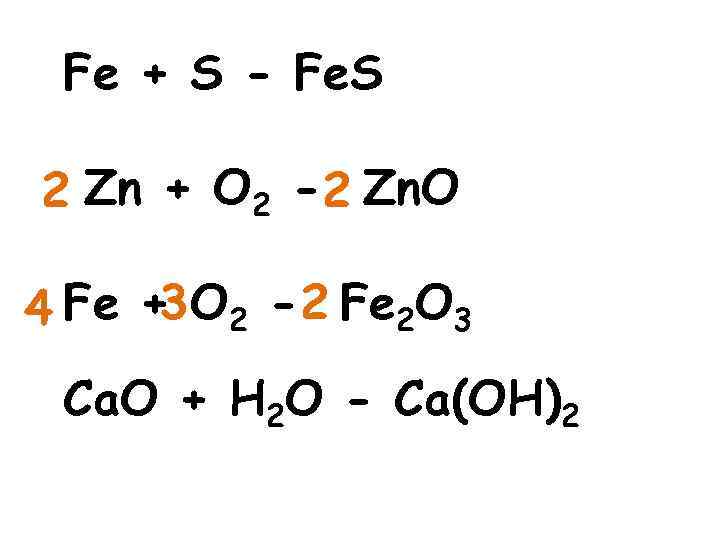 Fe + S - Fe. S 2 Zn + O 2 -2 Zn. O 3 4 Fe + O 2 - 2 Fe 2 O 3 Ca. O + H 2 O - Ca(OH)2
Fe + S - Fe. S 2 Zn + O 2 -2 Zn. O 3 4 Fe + O 2 - 2 Fe 2 O 3 Ca. O + H 2 O - Ca(OH)2
 Выберите уравнения реакций соединения: 1) 2) 3) 4) 5) 6) 7) 2 Hg. O = 2 Hg + O 2 Ca. CO 3 = Ca. O + CO 2 Cu. SO 4 + Fe = Cu + Fe. SO 4 Cu. O + H 2 = Cu + H 2 O 2 H 2 + O 2 = 2 H 2 O H 2 SO 4 + 2 KOH = K 2 SO 4 + 2 H 2 O Ba. O + SO 2 = Ba. SO 3
Выберите уравнения реакций соединения: 1) 2) 3) 4) 5) 6) 7) 2 Hg. O = 2 Hg + O 2 Ca. CO 3 = Ca. O + CO 2 Cu. SO 4 + Fe = Cu + Fe. SO 4 Cu. O + H 2 = Cu + H 2 O 2 H 2 + O 2 = 2 H 2 O H 2 SO 4 + 2 KOH = K 2 SO 4 + 2 H 2 O Ba. O + SO 2 = Ba. SO 3
 Реакция, протекающая между простыми и сложными веществами, при которой атомы простого вещества замещают атомы одного из элементов в сложном веществе, называется реакцией замещения. Zn + 2 HCl = Zn. Cl 2 + H 2 2 Fe +3 H 2 O = Fe 2 O 3 +3 H 2 + = +
Реакция, протекающая между простыми и сложными веществами, при которой атомы простого вещества замещают атомы одного из элементов в сложном веществе, называется реакцией замещения. Zn + 2 HCl = Zn. Cl 2 + H 2 2 Fe +3 H 2 O = Fe 2 O 3 +3 H 2 + = +
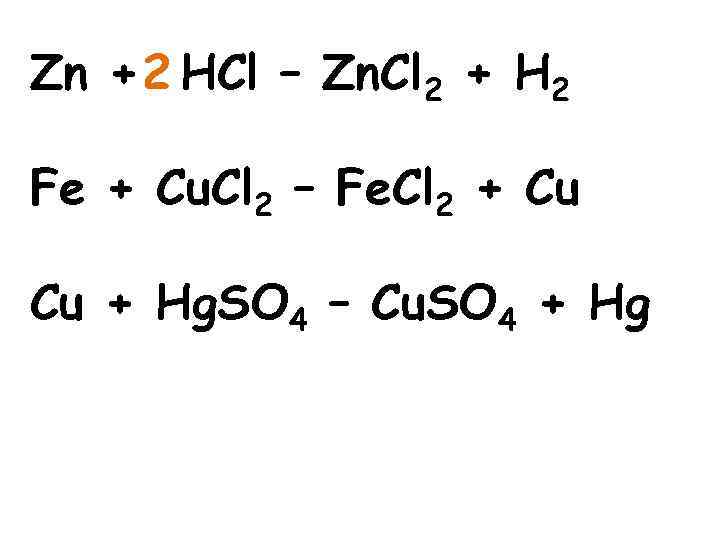 Zn + 2 HCl – Zn. Cl 2 + H 2 Fe + Cu. Cl 2 – Fe. Cl 2 + Cu Cu + Hg. SO 4 – Cu. SO 4 + Hg
Zn + 2 HCl – Zn. Cl 2 + H 2 Fe + Cu. Cl 2 – Fe. Cl 2 + Cu Cu + Hg. SO 4 – Cu. SO 4 + Hg
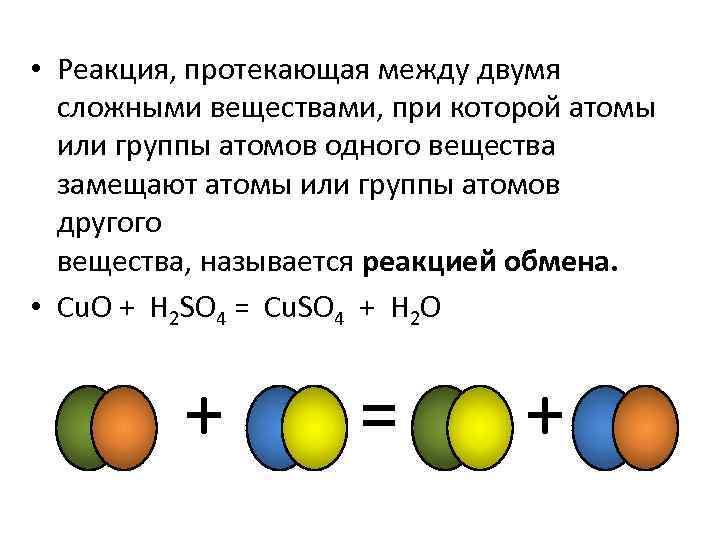 • Реакция, протекающая между двумя сложными веществами, при которой атомы или группы атомов одного вещества замещают атомы или группы атомов другого вещества, называется реакцией обмена. • Cu. O + H 2 SO 4 = Cu. SO 4 + H 2 O + = +
• Реакция, протекающая между двумя сложными веществами, при которой атомы или группы атомов одного вещества замещают атомы или группы атомов другого вещества, называется реакцией обмена. • Cu. O + H 2 SO 4 = Cu. SO 4 + H 2 O + = +
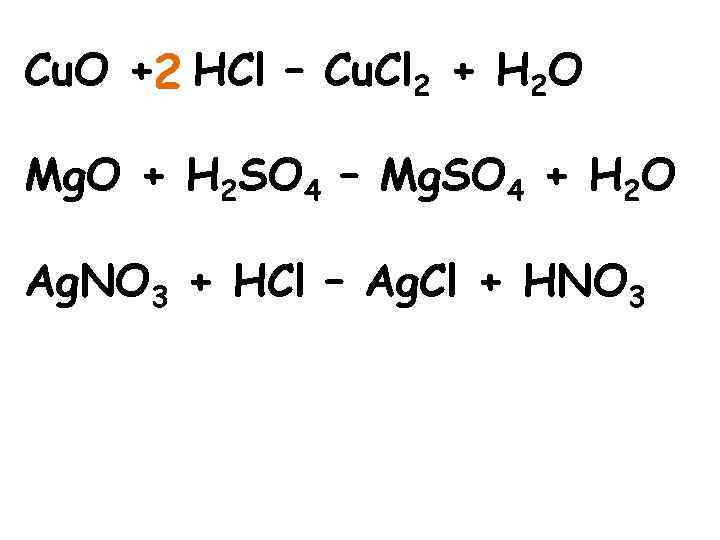 Cu. O +2 HCl – Cu. Cl 2 + H 2 O Mg. O + H 2 SO 4 – Mg. SO 4 + H 2 O Ag. NO 3 + HCl – Ag. Cl + HNO 3
Cu. O +2 HCl – Cu. Cl 2 + H 2 O Mg. O + H 2 SO 4 – Mg. SO 4 + H 2 O Ag. NO 3 + HCl – Ag. Cl + HNO 3
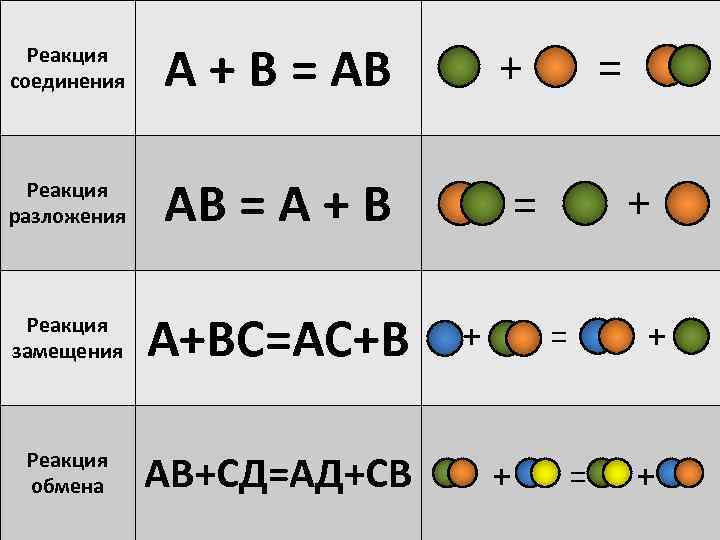 Реакция соединения А + В = АВ Реакция разложения АВ = А + В Реакция замещения А+ВС=АС+В Реакция обмена АВ+СД=АД+СВ = + + = = + + + = +
Реакция соединения А + В = АВ Реакция разложения АВ = А + В Реакция замещения А+ВС=АС+В Реакция обмена АВ+СД=АД+СВ = + + = = + + + = +
 Домашнее задание • Учебник с. 40 -41, выполнить упражнения 56 (с. 47). • Повторить учебный материал о химической формуле (параграф 10). • Творческое задание из тетради.
Домашнее задание • Учебник с. 40 -41, выполнить упражнения 56 (с. 47). • Повторить учебный материал о химической формуле (параграф 10). • Творческое задание из тетради.
 Домашнее задание: Оформить на альбомном листе работу, где необходимо привести примеры разных типов реакций и нарисовать рисунки, иллюстрирующие эти типы. Примеры таких работ приведены на следующих слайдах.
Домашнее задание: Оформить на альбомном листе работу, где необходимо привести примеры разных типов реакций и нарисовать рисунки, иллюстрирующие эти типы. Примеры таких работ приведены на следующих слайдах.






