Типы химических реакций на примере свойств воды.ppt
- Количество слайдов: 17
 Типы химических реакций на примере свойств воды.
Типы химических реакций на примере свойств воды.
 Нахождение в природе Физические свойства Н 2 О Мr(Н 2 О)=18 Химические свойства Применение
Нахождение в природе Физические свойства Н 2 О Мr(Н 2 О)=18 Химические свойства Применение
 Нахождение природе Нахождение вв природе 1. Атмосфера 2. Гидросфера 3. Литосфера 4. Биосфера 5. Космос Физические свойства Н 2 О Мr(Н 2 О)=18 Химические свойства Применение
Нахождение природе Нахождение вв природе 1. Атмосфера 2. Гидросфера 3. Литосфера 4. Биосфера 5. Космос Физические свойства Н 2 О Мr(Н 2 О)=18 Химические свойства Применение
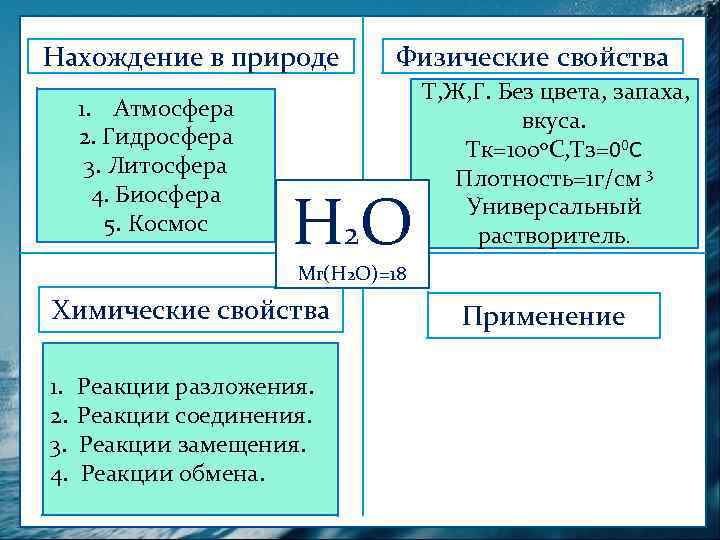 Нахождение природе Нахождение вв природе 1. Атмосфера 2. Гидросфера 3. Литосфера 4. Биосфера 5. Космос Физические свойства Н 2 О Т, Ж, Г. Без цвета, запаха, вкуса. Тк=1000 С, Тз=00 С Плотность=1 г/см 3 Универсальный растворитель. Мr(Н 2 О)=18 Химические свойства 1. 2. 3. 4. Реакции разложения. Реакции соединения. Реакции замещения. Реакции обмена. Применение
Нахождение природе Нахождение вв природе 1. Атмосфера 2. Гидросфера 3. Литосфера 4. Биосфера 5. Космос Физические свойства Н 2 О Т, Ж, Г. Без цвета, запаха, вкуса. Тк=1000 С, Тз=00 С Плотность=1 г/см 3 Универсальный растворитель. Мr(Н 2 О)=18 Химические свойства 1. 2. 3. 4. Реакции разложения. Реакции соединения. Реакции замещения. Реакции обмена. Применение
 1) Реакции разложения: Электролиз воды: 2 H 2 O ϟ 2 H 2 + O 2
1) Реакции разложения: Электролиз воды: 2 H 2 O ϟ 2 H 2 + O 2
 Реакции соединения: А) С оксидами металлов: - С оксидами щелочных металлов ( Li , K, Na); - C оксидами щелочноземельных металлов (Ca, Sr, Ba) Me. O + H 2 O → Me+n(OH)n Пример: Са. О + H 2 O → Са+2(OH)2 негашеная известь Na 2 O гашеная известь + H 2 O → Na+1 OH
Реакции соединения: А) С оксидами металлов: - С оксидами щелочных металлов ( Li , K, Na); - C оксидами щелочноземельных металлов (Ca, Sr, Ba) Me. O + H 2 O → Me+n(OH)n Пример: Са. О + H 2 O → Са+2(OH)2 негашеная известь Na 2 O гашеная известь + H 2 O → Na+1 OH
 Реакции соединения: А) С оксидами металлов: - С оксидами щелочных металлов ( Li , K, Na); - C оксидами щелочноземельных металлов (Ca, Sr, Ba) Me. O + H 2 O → Me+n(OH)n Пример: Са. О + H 2 O → Са+2(OH)2 негашеная известь Na 2 O гашеная известь + H 2 O → 2 Na+1 OH
Реакции соединения: А) С оксидами металлов: - С оксидами щелочных металлов ( Li , K, Na); - C оксидами щелочноземельных металлов (Ca, Sr, Ba) Me. O + H 2 O → Me+n(OH)n Пример: Са. О + H 2 O → Са+2(OH)2 негашеная известь Na 2 O гашеная известь + H 2 O → 2 Na+1 OH
 Реакции соединения: Б) С оксидами неметаллов: Не. Ме. О + Н 2 О → Нn(КО)-n (кислородсодержащая кислота) N 2 O 3 + H 2 O → 2 HNO 2 N 2 O 5 + H 2 O → 2 HNO 3 Ст. ок. элемента, образующего оксид остается неизменной. Основания и кислородсодержащие кислоты называются общим словом – гидроксиды.
Реакции соединения: Б) С оксидами неметаллов: Не. Ме. О + Н 2 О → Нn(КО)-n (кислородсодержащая кислота) N 2 O 3 + H 2 O → 2 HNO 2 N 2 O 5 + H 2 O → 2 HNO 3 Ст. ок. элемента, образующего оксид остается неизменной. Основания и кислородсодержащие кислоты называются общим словом – гидроксиды.
 Правило: Вода реагирует с оксидами металлов и оксидами неметаллов в том случае, если образуется растворимый гидроксид (щелочь или кислородсодержащая кислота).
Правило: Вода реагирует с оксидами металлов и оксидами неметаллов в том случае, если образуется растворимый гидроксид (щелочь или кислородсодержащая кислота).
 Реакции замещения: Щелочные и щелочноземельные металлы реагируют с водой по схеме: Me + H 2 O → Me+n(OH)n+ H 2↑ K + H 2 O → K+OH+ H 2↑ Ca + H 2 O → Ca+2(OH)2+ H 2↑
Реакции замещения: Щелочные и щелочноземельные металлы реагируют с водой по схеме: Me + H 2 O → Me+n(OH)n+ H 2↑ K + H 2 O → K+OH+ H 2↑ Ca + H 2 O → Ca+2(OH)2+ H 2↑
 Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + HOH → Al(OH)3↓ + H 2 S↑ Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + HOH → Al(OH)3↓ + H 2 S↑ Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
 Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + HOH → 2 Al(OH)3 + H 2 S Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + HOH → 2 Al(OH)3 + H 2 S Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
 Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + HOH → 2 Al(OH)3 + 3 H 2 S Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + HOH → 2 Al(OH)3 + 3 H 2 S Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
 Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + 6 HOH → 2 Al(OH)3 + 3 H 2 S Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
Реакции обмена: Обменное взаимодействие веществ с водой, приводящее к их разложению, называют гидролизом. Al 2 S 3 + 6 HOH → 2 Al(OH)3 + 3 H 2 S Са. С 2 + Н 2 О → Са(ОН)2 + С 2 Н 2
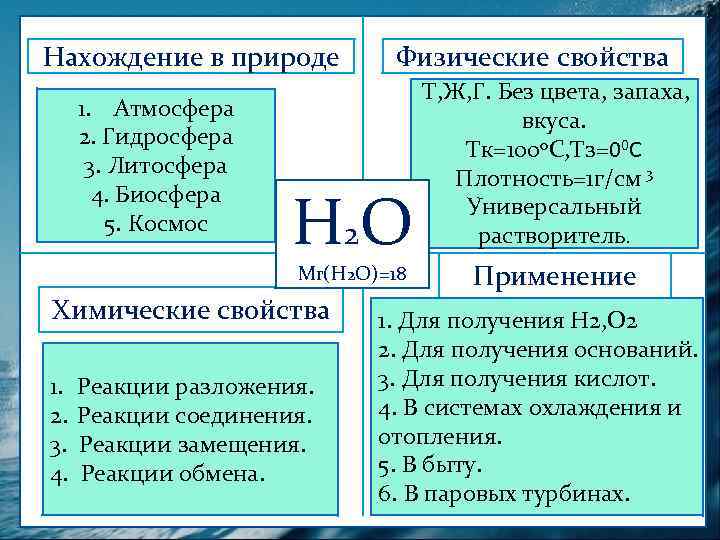 Нахождение природе Нахождение вв природе 1. Атмосфера 2. Гидросфера 3. Литосфера 4. Биосфера 5. Космос Физические свойства Н 2 О Мr(Н 2 О)=18 Химические свойства 1. 2. 3. 4. Реакции разложения. Реакции соединения. Реакции замещения. Реакции обмена. Т, Ж, Г. Без цвета, запаха, вкуса. Тк=1000 С, Тз=00 С Плотность=1 г/см 3 Универсальный растворитель. Применение 1. Для получения Н 2, О 2 2. Для получения оснований. 3. Для получения кислот. 4. В системах охлаждения и отопления. 5. В быту. 6. В паровых турбинах.
Нахождение природе Нахождение вв природе 1. Атмосфера 2. Гидросфера 3. Литосфера 4. Биосфера 5. Космос Физические свойства Н 2 О Мr(Н 2 О)=18 Химические свойства 1. 2. 3. 4. Реакции разложения. Реакции соединения. Реакции замещения. Реакции обмена. Т, Ж, Г. Без цвета, запаха, вкуса. Тк=1000 С, Тз=00 С Плотность=1 г/см 3 Универсальный растворитель. Применение 1. Для получения Н 2, О 2 2. Для получения оснований. 3. Для получения кислот. 4. В системах охлаждения и отопления. 5. В быту. 6. В паровых турбинах.
 Вариант № 1 1) 2) Напишите уравнение реакции взаимодействия кальция с кислородом и водой. 3) Вариант № 2 1) 2) Напишите уравнение реакции взаимодействия железа с хлором и лития с водой. 3)
Вариант № 1 1) 2) Напишите уравнение реакции взаимодействия кальция с кислородом и водой. 3) Вариант № 2 1) 2) Напишите уравнение реакции взаимодействия железа с хлором и лития с водой. 3)
 Домашнее задание: § 33, № 1 (б - д), 2, 4, с. 173
Домашнее задание: § 33, № 1 (б - д), 2, 4, с. 173


