лекция 3 химия.ppt
- Количество слайдов: 43
 ТИПЫ ХИМИЧЕСКИХ РАВНОВЕСИЙ И ПРОЦЕССОВ, ПРОТЕКАЮЩИХ В ЖИВЫХ СИСТЕМАХ
ТИПЫ ХИМИЧЕСКИХ РАВНОВЕСИЙ И ПРОЦЕССОВ, ПРОТЕКАЮЩИХ В ЖИВЫХ СИСТЕМАХ
 Типы химических процессов, протекающих в организме Протолитические реакции Гетерогенные реакции Реакции замещения лигандов Окислительно-восстановительные (редокс) реакции • Совмещенные равновесия и конкурирующие процессы • •
Типы химических процессов, протекающих в организме Протолитические реакции Гетерогенные реакции Реакции замещения лигандов Окислительно-восстановительные (редокс) реакции • Совмещенные равновесия и конкурирующие процессы • •
 • Химическое равновесие — состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости прямой и обратной реакций равны между собой. Для системы, находящейся в химическом равновесии, концентрации реагентов, температура и другие параметры системы не изменяются со временем
• Химическое равновесие — состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости прямой и обратной реакций равны между собой. Для системы, находящейся в химическом равновесии, концентрации реагентов, температура и другие параметры системы не изменяются со временем
 • Термодинамически химическое равновесие определяется как соотношение концентраций исходных веществ и продуктов реакции, при котором энтропия системы имеет максимальное, а изобарно-изотермический потенциал – минимальное значение
• Термодинамически химическое равновесие определяется как соотношение концентраций исходных веществ и продуктов реакции, при котором энтропия системы имеет максимальное, а изобарно-изотермический потенциал – минимальное значение
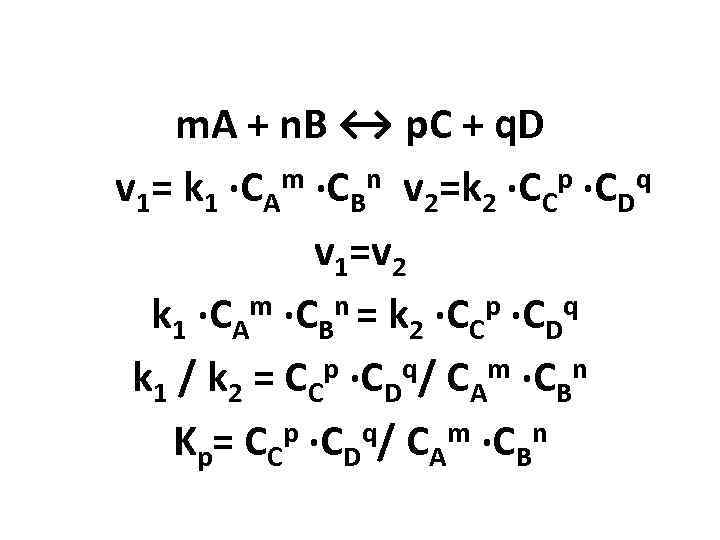 m. A + n. B ↔ p. C + q. D v 1= k 1 ·CАm ·CBn v 2=k 2 ·CCp ·CDq v 1=v 2 k 1 ·CАm ·CBn = k 2 ·CCp ·CDq k 1 / k 2 = CCp ·CDq/ CАm ·CBn Kp= CCp ·CDq/ CАm ·CBn
m. A + n. B ↔ p. C + q. D v 1= k 1 ·CАm ·CBn v 2=k 2 ·CCp ·CDq v 1=v 2 k 1 ·CАm ·CBn = k 2 ·CCp ·CDq k 1 / k 2 = CCp ·CDq/ CАm ·CBn Kp= CCp ·CDq/ CАm ·CBn
 Протолитические реакции. Ионизация воды. Н 2 О ↔ Н++ОН- К = С(Н )·С(ОН ) /С(Н 0) К(Н О)= С(Н )·С (ОН ) =Кw С(Н ) = С(ОН ) = 55, 5 · 1, 8· 10 -9 = 10 -7 моль/л Кw = С(Н )·С (ОН ) =10 -7· 10 -7=10 -14 С(Н )=С(ОН ) — раствор нейтрален; С(Н )>С(ОН ) - среда кислая; С(Н )<С(ОН )— среда щелочная + 2 • • • + - + - + - - + 2 -
Протолитические реакции. Ионизация воды. Н 2 О ↔ Н++ОН- К = С(Н )·С(ОН ) /С(Н 0) К(Н О)= С(Н )·С (ОН ) =Кw С(Н ) = С(ОН ) = 55, 5 · 1, 8· 10 -9 = 10 -7 моль/л Кw = С(Н )·С (ОН ) =10 -7· 10 -7=10 -14 С(Н )=С(ОН ) — раствор нейтрален; С(Н )>С(ОН ) - среда кислая; С(Н )<С(ОН )— среда щелочная + 2 • • • + - + - + - - + 2 -
 Водородный показатель • Отрицательный десятичный логарифм концентрации водородных ионов называется водородным показателем и обозначается р. Н = - lg С(Н ) р. Н = - lg (10 -7) = 7 • При увеличении С(Н ) р. Н уменьшается (<7); при увеличении С(ОН ) р. Н увеличивается (>7) + + -
Водородный показатель • Отрицательный десятичный логарифм концентрации водородных ионов называется водородным показателем и обозначается р. Н = - lg С(Н ) р. Н = - lg (10 -7) = 7 • При увеличении С(Н ) р. Н уменьшается (<7); при увеличении С(ОН ) р. Н увеличивается (>7) + + -
 Кислоты и основания по Аррениусу Кислотой следует считать электролиты, которые при диссоциации образуют ионы водорода, а основанием — вещества, образующие в водном растворе ионы ОН-. Вещества, которые в водных растворах способны в зависимости от условий высвобождать как Н+, так и ионы ОН-, называются амфотерными.
Кислоты и основания по Аррениусу Кислотой следует считать электролиты, которые при диссоциации образуют ионы водорода, а основанием — вещества, образующие в водном растворе ионы ОН-. Вещества, которые в водных растворах способны в зависимости от условий высвобождать как Н+, так и ионы ОН-, называются амфотерными.
 Определение Бренстеда — Лоури Кислоты - вещества, высвобождающие протоны (доноры протонов), а основания — вещества, способные соединяться с протонами (акцепторы протонов) А 1↔В 1+ Н+ к о п В 2 + Н+ ↔ А 2 о п к А 1 + B 2 ↔ А 2 + В 1 к о
Определение Бренстеда — Лоури Кислоты - вещества, высвобождающие протоны (доноры протонов), а основания — вещества, способные соединяться с протонами (акцепторы протонов) А 1↔В 1+ Н+ к о п В 2 + Н+ ↔ А 2 о п к А 1 + B 2 ↔ А 2 + В 1 к о
 Определение Бренстеда — Лоури Реакция нейтрализации может рассматриваться как процесс, в котором осуществляется конкуренция за обладание протоном
Определение Бренстеда — Лоури Реакция нейтрализации может рассматриваться как процесс, в котором осуществляется конкуренция за обладание протоном
 Определение Бренстеда — Лоури Сила кислоты определяется константой кислотности Ка. Исходя из равновесия HA↔Н+ + А- Ка=С(Н )·С(А )/С(НА) + - • Для осуществления этого равновесия в растворе необходимо присутствие акцептора протона, благодаря которому осуществляется переход протона от кислоты к основанию: НА + В- ↔ НВ + Ак о
Определение Бренстеда — Лоури Сила кислоты определяется константой кислотности Ка. Исходя из равновесия HA↔Н+ + А- Ка=С(Н )·С(А )/С(НА) + - • Для осуществления этого равновесия в растворе необходимо присутствие акцептора протона, благодаря которому осуществляется переход протона от кислоты к основанию: НА + В- ↔ НВ + Ак о
 Определение Бренстеда — Лоури Реакции данного типа называются протолитическими, количественная сторона которых характеризуется константой равновесия (константой протолиза): Кп = С(НВ) ·С(А )/С(В )·С(НА) - - Значения Кп для НА и НВ можно определить следующим путем: К 1= С(Н+)·С(А-)/С(НА), К 2 = С(Н+)·С(B-)/С(НB) Тогда Кп = К 1/К 2
Определение Бренстеда — Лоури Реакции данного типа называются протолитическими, количественная сторона которых характеризуется константой равновесия (константой протолиза): Кп = С(НВ) ·С(А )/С(В )·С(НА) - - Значения Кп для НА и НВ можно определить следующим путем: К 1= С(Н+)·С(А-)/С(НА), К 2 = С(Н+)·С(B-)/С(НB) Тогда Кп = К 1/К 2
 Определение Бренстеда — Лоури Сила основания определяется константой основности Кb, которая соответствует равновесию ВОН↔В++ОНКb=С(OН )·С(B )/С (BOН) - +
Определение Бренстеда — Лоури Сила основания определяется константой основности Кb, которая соответствует равновесию ВОН↔В++ОНКb=С(OН )·С(B )/С (BOН) - +
 Определение Льюиса Кислота — это вещество, которое акцептирует электронную пару; основание — это вещество, которое предоставляет электронную пару Взаимодействие между кислотой и основанием, согласно этому определению, заключается в возникновении ковалентной связи по донорно-акцепторному механизму: H 3 N: + A 1 C 13 → H 3 N+ + Al. Cl 3 -
Определение Льюиса Кислота — это вещество, которое акцептирует электронную пару; основание — это вещество, которое предоставляет электронную пару Взаимодействие между кислотой и основанием, согласно этому определению, заключается в возникновении ковалентной связи по донорно-акцепторному механизму: H 3 N: + A 1 C 13 → H 3 N+ + Al. Cl 3 -
 1) расчет р. Н раствора слабой кислоты 2) расчет р. Н раствора слабого основания
1) расчет р. Н раствора слабой кислоты 2) расчет р. Н раствора слабого основания
 ГИДРОЛИЗ Гидролиз представляет собой обменное взаимодействие ионов соли с молекулами воды, в результате которого смещается равновесие электролитической диссоциации воды. Сущность этого процесса заключается в том, что катион соли (слабое основание) или ее анион (слабая кислота) связывает соответственно ОН- или Н+ с образованием слабого электролита (основания или кислоты).
ГИДРОЛИЗ Гидролиз представляет собой обменное взаимодействие ионов соли с молекулами воды, в результате которого смещается равновесие электролитической диссоциации воды. Сущность этого процесса заключается в том, что катион соли (слабое основание) или ее анион (слабая кислота) связывает соответственно ОН- или Н+ с образованием слабого электролита (основания или кислоты).
 ГИДРОЛИЗ 1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону): Na 2 CO 3+HOH 1)2 Na+ +CO 32 - + HOH↔Na++НCO 3 - + ОН- (I ступень) СО 32 - + НОН ↔ HCO 3 - + OН 2)Na++HCO 3 - +H 2 O↔H 2 CO 3+Na++OH- (II ступень) HCO 3 - + НОН ↔ Н 2 СО 3+ОН(раствор имеет слабощелочную среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
ГИДРОЛИЗ 1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону): Na 2 CO 3+HOH 1)2 Na+ +CO 32 - + HOH↔Na++НCO 3 - + ОН- (I ступень) СО 32 - + НОН ↔ HCO 3 - + OН 2)Na++HCO 3 - +H 2 O↔H 2 CO 3+Na++OH- (II ступень) HCO 3 - + НОН ↔ Н 2 СО 3+ОН(раствор имеет слабощелочную среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
 ГИДРОЛИЗ 2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону): Cu. Cl 2+HOH 1) Сu 2++2 С 1 -+Н 2 О↔Сu(ОН)++С 1 - + Н++С 1 - (I ступень) Сu 2+ + Н 2 О = Сu(ОН)+ + Н+ 2) Сu(0 Н)++С 1 -+Н 2 О↔Сu(ОН)2 + H++ С 1 - (II ступень) Сu(ОН)+ + Н 2 О ↔ Cu(OH)2 + H+ (раствор имеет слабокислую среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
ГИДРОЛИЗ 2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону): Cu. Cl 2+HOH 1) Сu 2++2 С 1 -+Н 2 О↔Сu(ОН)++С 1 - + Н++С 1 - (I ступень) Сu 2+ + Н 2 О = Сu(ОН)+ + Н+ 2) Сu(0 Н)++С 1 -+Н 2 О↔Сu(ОН)2 + H++ С 1 - (II ступень) Сu(ОН)+ + Н 2 О ↔ Cu(OH)2 + H+ (раствор имеет слабокислую среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
 ГИДРОЛИЗ 3. Гидролиз соли слабой кислоты и слабого основания: Аl 2(CO 3)3+HOH 2 А 13+ + ЗСО 32 - + 6 Н 0 Н ↔ 2 А 1(ОН)з +ЗСО 2 +3 Н 2 О (равновесие смещено в сторону продуктов, гидролиз протекает практически полностью, так как оба продукта реакции уходят из зоны реакции в виде осадка или газа). 4. Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор нейтрален
ГИДРОЛИЗ 3. Гидролиз соли слабой кислоты и слабого основания: Аl 2(CO 3)3+HOH 2 А 13+ + ЗСО 32 - + 6 Н 0 Н ↔ 2 А 1(ОН)з +ЗСО 2 +3 Н 2 О (равновесие смещено в сторону продуктов, гидролиз протекает практически полностью, так как оба продукта реакции уходят из зоны реакции в виде осадка или газа). 4. Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор нейтрален
 ГИДРОЛИЗ Количественно гидролиз характеризуется степенью гидролиза αГ и константой гидролиза Кг. Доля вещества, подвергающаяся гидролизу, называется степенью гидролиза: αг = Сг/С, где Сг — концентрация гидролизованной части вещества; С — общая концентрация растворенного вещества.
ГИДРОЛИЗ Количественно гидролиз характеризуется степенью гидролиза αГ и константой гидролиза Кг. Доля вещества, подвергающаяся гидролизу, называется степенью гидролиза: αг = Сг/С, где Сг — концентрация гидролизованной части вещества; С — общая концентрация растворенного вещества.
 ГИДРОЛИЗ • Для соли, образованной слабой кислотой и сильным основанием: где Ка— константа диссоциации слабой кислоты, образующейся при гидролизе • Для соли, образованной сильной кислотой и слабым основанием: • где Кb— константа диссоциации слабого основания, образующегося при гидролизе • для соли, образованной слабой кислотой и слабым основанием:
ГИДРОЛИЗ • Для соли, образованной слабой кислотой и сильным основанием: где Ка— константа диссоциации слабой кислоты, образующейся при гидролизе • Для соли, образованной сильной кислотой и слабым основанием: • где Кb— константа диссоциации слабого основания, образующегося при гидролизе • для соли, образованной слабой кислотой и слабым основанием:
 Гетерогенные реакции • Гетерогенные равновесия в водных растворах характеризуются тем, что перенос частиц происходит через поверхность раздела по крайней мере двух сосуществующих фаз
Гетерогенные реакции • Гетерогенные равновесия в водных растворах характеризуются тем, что перенос частиц происходит через поверхность раздела по крайней мере двух сосуществующих фаз
 Гетерогенные реакции • Равновесие, устанавливающееся между осадком малорастворимого вещества и его насыщенным раствором описывается уравнением Аа. Вв(т) ↔
Гетерогенные реакции • Равновесие, устанавливающееся между осадком малорастворимого вещества и его насыщенным раствором описывается уравнением Аа. Вв(т) ↔
 Гетерогенные реакции • Константа равновесия этого процесса называется произведением растворимости малорастворимого соединения при постоянной температуре является величиной постоянной
Гетерогенные реакции • Константа равновесия этого процесса называется произведением растворимости малорастворимого соединения при постоянной температуре является величиной постоянной
 Растворимость солей Для бинарного электролита МВ(т) ↔ М 2+(р) +В 2 -(р)
Растворимость солей Для бинарного электролита МВ(т) ↔ М 2+(р) +В 2 -(р)
 Гетерогенные реакции Изоморфизм - явление замены в кристаллической решетке минерала одних химических элементов другими (при патологических состояниях - замещение в гидроксидфосфате кальция гидроксид-ионов на ионы фтора, ионов кальция на ионы стронция) При изоморфной замене одного атома другим существенного изменения кристаллической решетки не происходит. Поэтому для явления изоморфизма необходимы следующие условия: 1. Ионные радиусы изоморфно замещающихся элементов должны быть близки. 2. Близость химических свойств элементов, замещающих друга. 3. Сохранение электронейтральности кристаллической структуры минерала
Гетерогенные реакции Изоморфизм - явление замены в кристаллической решетке минерала одних химических элементов другими (при патологических состояниях - замещение в гидроксидфосфате кальция гидроксид-ионов на ионы фтора, ионов кальция на ионы стронция) При изоморфной замене одного атома другим существенного изменения кристаллической решетки не происходит. Поэтому для явления изоморфизма необходимы следующие условия: 1. Ионные радиусы изоморфно замещающихся элементов должны быть близки. 2. Близость химических свойств элементов, замещающих друга. 3. Сохранение электронейтральности кристаллической структуры минерала
 Гетерогенные реакции Около 60 элементов могут быть отнесены к группе остеотропных элементов. Остеотропные элементы можно разделить на три группы: 1. Элементы, являющиеся или заменяющие физиологические составляющие кости. Двадцать подобных элементов присутствуют в больших количествах. Другие отмечаются в следовых количествах. В условиях хронического воздействия такие металлы как свинец, алюминий и ртуть могут внедряться в минеральную матрицу клеток кости. 2. Щелочно-земельные и другие элементы, образующие катионы с диаметром ионов равным диаметру ионов кальция могут заменять его в минерале кости. Некоторые анионы также могут заменять анионы (фосфаты, гидроксилы) минерала кости. 3. Элементы, образующие микроколлоиды (редкоземельные) могут абсорбироваться на поверхности минерала кости.
Гетерогенные реакции Около 60 элементов могут быть отнесены к группе остеотропных элементов. Остеотропные элементы можно разделить на три группы: 1. Элементы, являющиеся или заменяющие физиологические составляющие кости. Двадцать подобных элементов присутствуют в больших количествах. Другие отмечаются в следовых количествах. В условиях хронического воздействия такие металлы как свинец, алюминий и ртуть могут внедряться в минеральную матрицу клеток кости. 2. Щелочно-земельные и другие элементы, образующие катионы с диаметром ионов равным диаметру ионов кальция могут заменять его в минерале кости. Некоторые анионы также могут заменять анионы (фосфаты, гидроксилы) минерала кости. 3. Элементы, образующие микроколлоиды (редкоземельные) могут абсорбироваться на поверхности минерала кости.
 Гетерогенные реакции Скелет стандартного человека составляет 10 -15% общего веса тела, являясь крупным потенциальным хранилищем остеотропных токсикантов. Кость - это высокоспецифичная ткань, состоящая по объему на 54% из минералов и на 38% из органической матрицы. Минеральная матрица кости является гидроксиапатитом , в котором соотношение Ca и P составляет примерно 1, 5 к одному. Площадь поверхности минерала, участвующего в абсорбции, составляет примерно 100 на 1 г кости.
Гетерогенные реакции Скелет стандартного человека составляет 10 -15% общего веса тела, являясь крупным потенциальным хранилищем остеотропных токсикантов. Кость - это высокоспецифичная ткань, состоящая по объему на 54% из минералов и на 38% из органической матрицы. Минеральная матрица кости является гидроксиапатитом , в котором соотношение Ca и P составляет примерно 1, 5 к одному. Площадь поверхности минерала, участвующего в абсорбции, составляет примерно 100 на 1 г кости.
 Гетерогенные реакции • Конкремент (от лат. concrementum — скопление, срастание) — камни, плотные образования, встречающиеся в полостных органах и выводных протоках желез человека • Химический состав конкрементов зависит от места их образования и состава жидкости, в которой происходит камнеобразование • Мочевые конкременты образуются в мочевыводящих путях и по кислотным остаткам делятся на ураты (самый частый вид мочевых конкрементов), оксалаты, карбонаты.
Гетерогенные реакции • Конкремент (от лат. concrementum — скопление, срастание) — камни, плотные образования, встречающиеся в полостных органах и выводных протоках желез человека • Химический состав конкрементов зависит от места их образования и состава жидкости, в которой происходит камнеобразование • Мочевые конкременты образуются в мочевыводящих путях и по кислотным остаткам делятся на ураты (самый частый вид мочевых конкрементов), оксалаты, карбонаты.
 Гетерогенные реакции • Хлорид кальция применяется как антидот при отравлениях солями магния, щавелевой кислотой и ее растворимыми солями, а также растворимыми солями фтористой кислоты • Сульфат магния является антидотом при отравлениях солями тяжелых металлов
Гетерогенные реакции • Хлорид кальция применяется как антидот при отравлениях солями магния, щавелевой кислотой и ее растворимыми солями, а также растворимыми солями фтористой кислоты • Сульфат магния является антидотом при отравлениях солями тяжелых металлов
 Реакции замещения лигандов • Комплексное соединение — вещество, в состав которого входят комплексные частицы (определение не используется). • Комплексная частица — сложная частица, способная к самостоятельному существованию в кристалле или растворе, образованная из других, более простых частиц, также способных к самостоятельному существованию.
Реакции замещения лигандов • Комплексное соединение — вещество, в состав которого входят комплексные частицы (определение не используется). • Комплексная частица — сложная частица, способная к самостоятельному существованию в кристалле или растворе, образованная из других, более простых частиц, также способных к самостоятельному существованию.
 Общие положения теории координационных соединений Комплексные ионы - ионы, которые образуются путем присоединения к данному иону нейтральных молекул или ионов противоположного знака [Cu(NH 3)4]2+ [Pt. Cl 6]2 -
Общие положения теории координационных соединений Комплексные ионы - ионы, которые образуются путем присоединения к данному иону нейтральных молекул или ионов противоположного знака [Cu(NH 3)4]2+ [Pt. Cl 6]2 -
 Общие положения теории координационных соединений • Комплексные соединения - соединения, в состав которых входят комплексные ионы [Pt(NH 3)6]Cl 4 [Pt(NH 3)4 Cl 2]Cl 2 [Pt(NH 3)2 Cl 4] K 2[Pt. Cl 6]
Общие положения теории координационных соединений • Комплексные соединения - соединения, в состав которых входят комплексные ионы [Pt(NH 3)6]Cl 4 [Pt(NH 3)4 Cl 2]Cl 2 [Pt(NH 3)2 Cl 4] K 2[Pt. Cl 6]
 Общие положения теории координационных соединений 1. В молекуле любого КС один из ионов (обычно катион) занимает центральное место и называется комплексообразователем или центральным ионом 2. Вокруг него координировано некоторое число противоположно заряженных ионов или электронейтральных молекул – лигандов или аддендов
Общие положения теории координационных соединений 1. В молекуле любого КС один из ионов (обычно катион) занимает центральное место и называется комплексообразователем или центральным ионом 2. Вокруг него координировано некоторое число противоположно заряженных ионов или электронейтральных молекул – лигандов или аддендов
 Общие положения теории координационных соединений 3. Лиганды образуют внутреннюю координационную сферу соединения 4. Ионы, находящиеся на более далеком расстоянии от центрального иона, составляют внешнюю координационную сферу
Общие положения теории координационных соединений 3. Лиганды образуют внутреннюю координационную сферу соединения 4. Ионы, находящиеся на более далеком расстоянии от центрального иона, составляют внешнюю координационную сферу
 Общие положения теории координационных соединений 5. Число лигандов, окружающих центральный ион, - координационное число 6. Во внутренней сфере ионы связаны неионогенно, а во внешней - ионогенно
Общие положения теории координационных соединений 5. Число лигандов, окружающих центральный ион, - координационное число 6. Во внутренней сфере ионы связаны неионогенно, а во внешней - ионогенно
![Пример K 2[Pt. Cl 6] Внутренняя сфера Комплексообразователь ион Pt+4 Лиганды ионы Cl. Внешняя Пример K 2[Pt. Cl 6] Внутренняя сфера Комплексообразователь ион Pt+4 Лиганды ионы Cl. Внешняя](https://present5.com/presentation/3/-43229180_132929146.pdf-img/-43229180_132929146.pdf-37.jpg) Пример K 2[Pt. Cl 6] Внутренняя сфера Комплексообразователь ион Pt+4 Лиганды ионы Cl. Внешняя сфера ион К+
Пример K 2[Pt. Cl 6] Внутренняя сфера Комплексообразователь ион Pt+4 Лиганды ионы Cl. Внешняя сфера ион К+
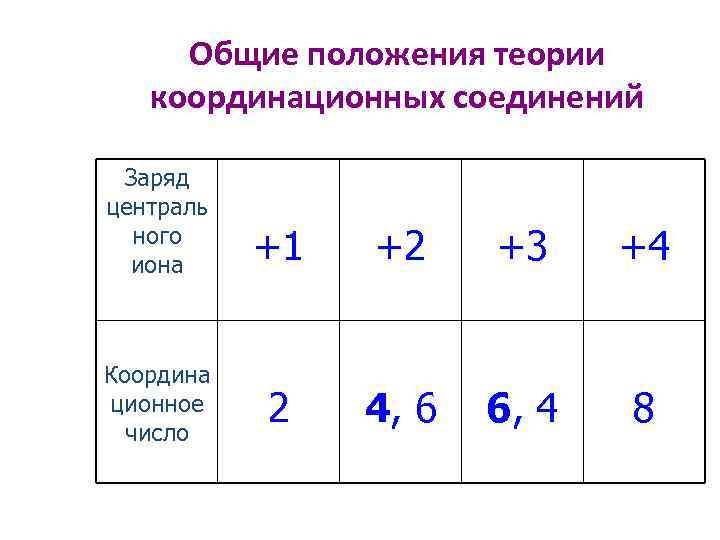 Общие положения теории координационных соединений Заряд централь ного иона Координа ционное число +1 +2 +3 +4 2 4, 6 6, 4 8
Общие положения теории координационных соединений Заряд централь ного иона Координа ционное число +1 +2 +3 +4 2 4, 6 6, 4 8
 • Лиганды, занимающие во внутренней координационной сфере 1 место, - монодентатные • Лиганды, занимающие во внутренней координационной сфере 2 и более мест, - би- и полидентатные
• Лиганды, занимающие во внутренней координационной сфере 1 место, - монодентатные • Лиганды, занимающие во внутренней координационной сфере 2 и более мест, - би- и полидентатные
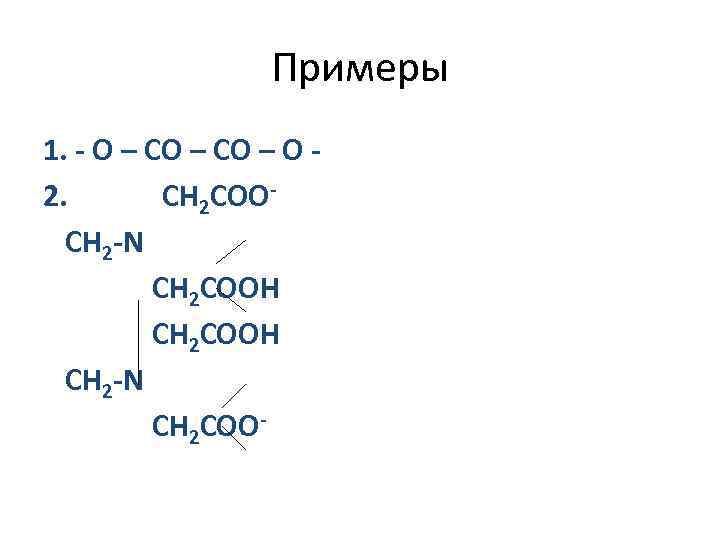 Примеры 1. - О – СО – О 2. CH 2 COOСН 2 -N CH 2 COOH СН 2 -N CH 2 COO-
Примеры 1. - О – СО – О 2. CH 2 COOСН 2 -N CH 2 COOH СН 2 -N CH 2 COO-
 Общие положения теории координационных соединений • Заряд комплексного иона равен алгебраической сумме зарядов составляющих его простых ионов Ag+ + 2 CN[Ag(CN)2](+1 – 2 = - 1) Электронейтральные молекулы, входящие в состав комплекса, не влияют на величину его заряда
Общие положения теории координационных соединений • Заряд комплексного иона равен алгебраической сумме зарядов составляющих его простых ионов Ag+ + 2 CN[Ag(CN)2](+1 – 2 = - 1) Электронейтральные молекулы, входящие в состав комплекса, не влияют на величину его заряда
 Номенклатура КС 1. Число лигандов (ди- (бис-), три- (трис-), тетра(тетраксис-) и т. п. ) 2. Названия лигандов (для анионов добавляется гласная -о- , исключения – меркапто-, тио-; для нейтральных лигандов названия не модифицируются, исключения вода - аква-, аммиак - аммин-, СО – карбонил-, NO – нитрозил) 3. Центральный атом (в анионных КС - лат. корень + -ат, в остальных - как в ПСЭМ)
Номенклатура КС 1. Число лигандов (ди- (бис-), три- (трис-), тетра(тетраксис-) и т. п. ) 2. Названия лигандов (для анионов добавляется гласная -о- , исключения – меркапто-, тио-; для нейтральных лигандов названия не модифицируются, исключения вода - аква-, аммиак - аммин-, СО – карбонил-, NO – нитрозил) 3. Центральный атом (в анионных КС - лат. корень + -ат, в остальных - как в ПСЭМ)
![Номенклатура КС • [Fe(CO)5] пентакарбонилжелезо • [Zn(NH 3)4](OH)2 гидроксид тетраамминцинка • [Co(NH 3)3(NO 2)2 Номенклатура КС • [Fe(CO)5] пентакарбонилжелезо • [Zn(NH 3)4](OH)2 гидроксид тетраамминцинка • [Co(NH 3)3(NO 2)2](https://present5.com/presentation/3/-43229180_132929146.pdf-img/-43229180_132929146.pdf-43.jpg) Номенклатура КС • [Fe(CO)5] пентакарбонилжелезо • [Zn(NH 3)4](OH)2 гидроксид тетраамминцинка • [Co(NH 3)3(NO 2)2 Cl] хлородинитритотриамминкобальт • K[Fe(NH 3)2(CN)4] тетрацианодиамминферрат (III) калия
Номенклатура КС • [Fe(CO)5] пентакарбонилжелезо • [Zn(NH 3)4](OH)2 гидроксид тетраамминцинка • [Co(NH 3)3(NO 2)2 Cl] хлородинитритотриамминкобальт • K[Fe(NH 3)2(CN)4] тетрацианодиамминферрат (III) калия


