Tiospirti-.ppt
- Количество слайдов: 4
 ТІОСПИРТИ, ТІОЕТЕРИ. Сульфур є аналогом Оксигену. Тому органічні сполуки, молекули яких містять Сульфур, хімічно подібні до аналогічних оксигеновмісних сполук. Тіоспирти (тіоли, або меркаптани) – це органічні сполуки, молекули яких містять сульфгідрильну групу –SH. Загальна формула тіоспиртів R–S–Н. Тіоспирти можна розглядати як похідні гідрогенсульфіду, в молекулі якого один атом гідрогену заміщений на вуглеводневий радикал. Тіоспирти називають за історичною та систематичною номенклатурами. За систематичною – з назви відповідного вуглеводню, до якої додають суфікс -тіол і вказують номер карбонового атома, біля якого знаходиться група –S–Н. (Н 3 С—SH – метилмеркаптан, або метантіол; Н 3 С–СН 2–SH – етилмеркаптан, або етантіол. Тіоспирти одержують з галогеналканів, діючи на них натрій гідросульфідом, або взаємодією спиртів з гідрогенсульфідом при наявності каталізатора: H 3 C–CH 2–I + Na–SH → H 3 C–CH 2–SH + Na I Фізичні та хімічні властивості тіоспиртів. Тіоспирти киплять при значно нижчих температурах, ніж відповідні спирти. Вони важко розчиняються у воді і легко – у багатьох органічних розчинниках. Нижчі тіоспирти – рідини, вищі – тверді речовини. Хімічні властивості тіоспиртів визначаються наявністю в їх молекулах SH–груп. За хімічними властивостями тіоспирти наближаються до слабких кислот, але завдяки +І ефекту групи R→S–Н кислотні властивості тіоспиртів слабкіші, ніж гідрогенсульфуру. Вони легко реагують з лугами, оксидами металів і утворюють солеподібні сполуки – тіоляти, або меркаптиди: Н 3 С–CH 2–SH + Na. OH → Н 3 С–CH 2–SNa + HOH. Тіоспирти порівняно легко окиснюються до дисульфідів або сульфокислот: 2 Н 3 С–CH 2–SH + І2 → Н 3 С–CH 2–S–S–CH 2–CH 3 + 2 HI.
ТІОСПИРТИ, ТІОЕТЕРИ. Сульфур є аналогом Оксигену. Тому органічні сполуки, молекули яких містять Сульфур, хімічно подібні до аналогічних оксигеновмісних сполук. Тіоспирти (тіоли, або меркаптани) – це органічні сполуки, молекули яких містять сульфгідрильну групу –SH. Загальна формула тіоспиртів R–S–Н. Тіоспирти можна розглядати як похідні гідрогенсульфіду, в молекулі якого один атом гідрогену заміщений на вуглеводневий радикал. Тіоспирти називають за історичною та систематичною номенклатурами. За систематичною – з назви відповідного вуглеводню, до якої додають суфікс -тіол і вказують номер карбонового атома, біля якого знаходиться група –S–Н. (Н 3 С—SH – метилмеркаптан, або метантіол; Н 3 С–СН 2–SH – етилмеркаптан, або етантіол. Тіоспирти одержують з галогеналканів, діючи на них натрій гідросульфідом, або взаємодією спиртів з гідрогенсульфідом при наявності каталізатора: H 3 C–CH 2–I + Na–SH → H 3 C–CH 2–SH + Na I Фізичні та хімічні властивості тіоспиртів. Тіоспирти киплять при значно нижчих температурах, ніж відповідні спирти. Вони важко розчиняються у воді і легко – у багатьох органічних розчинниках. Нижчі тіоспирти – рідини, вищі – тверді речовини. Хімічні властивості тіоспиртів визначаються наявністю в їх молекулах SH–груп. За хімічними властивостями тіоспирти наближаються до слабких кислот, але завдяки +І ефекту групи R→S–Н кислотні властивості тіоспиртів слабкіші, ніж гідрогенсульфуру. Вони легко реагують з лугами, оксидами металів і утворюють солеподібні сполуки – тіоляти, або меркаптиди: Н 3 С–CH 2–SH + Na. OH → Н 3 С–CH 2–SNa + HOH. Тіоспирти порівняно легко окиснюються до дисульфідів або сульфокислот: 2 Н 3 С–CH 2–SH + І2 → Н 3 С–CH 2–S–S–CH 2–CH 3 + 2 HI.
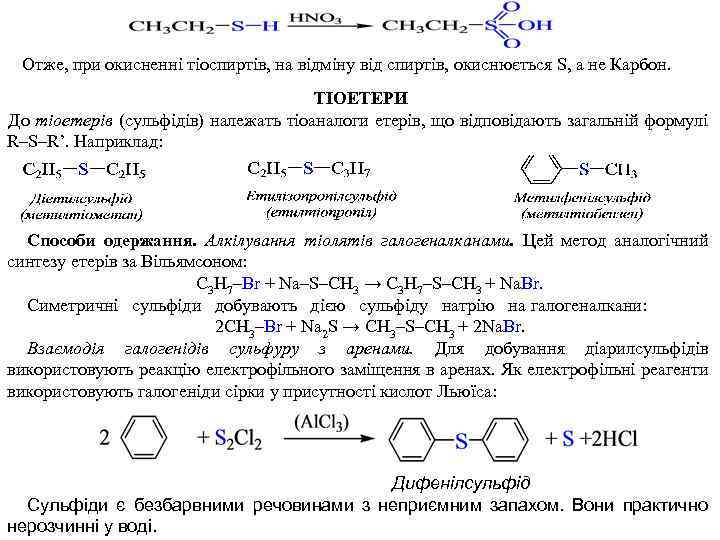 Отже, при окисненні тіоспиртів, на відміну від спиртів, окиснюється S, а не Карбон. ТІОЕТЕРИ До тіоетерів (сульфідів) належать тіоаналоги етерів, що відповідають загальній формулі R–S–R’. Наприклад: Способи одержання. Алкілування тіолятів галогеналканами. Цей метод аналогічний синтезу етерів за Вільямсоном: С 3 H 7–Br + Na–S–CH 3 → С 3 H 7–S–CH 3 + Na. Br. Симетричні сульфіди добувають дією сульфіду натрію на галогеналкани: 2 СH 3–Br + Na 2 S → СH 3–S–CH 3 + 2 Na. Br. Взаємодія галогенідів сульфуру з аренами. Для добування діарилсульфідів використовують реакцію електрофільного заміщення в аренах. Як електрофільні реагенти використовують галогеніди сірки у присутності кислот Льюїса: Дифенілсульфід Сульфіди є безбарвними речовинами з неприємним запахом. Вони практично нерозчинні у воді.
Отже, при окисненні тіоспиртів, на відміну від спиртів, окиснюється S, а не Карбон. ТІОЕТЕРИ До тіоетерів (сульфідів) належать тіоаналоги етерів, що відповідають загальній формулі R–S–R’. Наприклад: Способи одержання. Алкілування тіолятів галогеналканами. Цей метод аналогічний синтезу етерів за Вільямсоном: С 3 H 7–Br + Na–S–CH 3 → С 3 H 7–S–CH 3 + Na. Br. Симетричні сульфіди добувають дією сульфіду натрію на галогеналкани: 2 СH 3–Br + Na 2 S → СH 3–S–CH 3 + 2 Na. Br. Взаємодія галогенідів сульфуру з аренами. Для добування діарилсульфідів використовують реакцію електрофільного заміщення в аренах. Як електрофільні реагенти використовують галогеніди сірки у присутності кислот Льюїса: Дифенілсульфід Сульфіди є безбарвними речовинами з неприємним запахом. Вони практично нерозчинні у воді.
 Тіоетери – рідини з Ткип. , близькою до тіоспиртів з такою самою молекулярною масою. За хімічними властивостями вони є нейтральними речовинами, які не взаємодіють з кислотами. За рахунок вільних електронних пар атома Сульфуру тіоетери виявляють нуклеофільні властивості, реагуючи з галогеналканами з утворенням сульфонієвих (тіоніевих) солей: Триметилтіоній іодид Гідроген пероксид окиснює тіоетери до сульфоксидів: Сильні окисники (KMn. O 4, HNO 3) окиснюють тіоетери і сульфоксиди до сульфонів: Диметилсульфон Диметилсульфоксид Алкілування сульфідів. Сульфіди порівняно легко реагують з галогеналканами з утворенням досить стабільних галогенідів триалкілсульфонію: Диетилсульфід Іодид триетилсульфонію.
Тіоетери – рідини з Ткип. , близькою до тіоспиртів з такою самою молекулярною масою. За хімічними властивостями вони є нейтральними речовинами, які не взаємодіють з кислотами. За рахунок вільних електронних пар атома Сульфуру тіоетери виявляють нуклеофільні властивості, реагуючи з галогеналканами з утворенням сульфонієвих (тіоніевих) солей: Триметилтіоній іодид Гідроген пероксид окиснює тіоетери до сульфоксидів: Сильні окисники (KMn. O 4, HNO 3) окиснюють тіоетери і сульфоксиди до сульфонів: Диметилсульфон Диметилсульфоксид Алкілування сульфідів. Сульфіди порівняно легко реагують з галогеналканами з утворенням досить стабільних галогенідів триалкілсульфонію: Диетилсульфід Іодид триетилсульфонію.
 Реакція з солями важких металів. Сульфіди легко реагують з солями важких металів з утворенням комплексів, наприклад: R 2 S + Hg. Cl 2 → R 2 S · Hg. Cl 2 Ця реакція застосовується в аналізі для ідентифікації сульфідів. На цій реакції ґрунтується і використання деяких сульфідів як антидотів при отруєнні солями важких металів. Окремі представники. Застосування. Диметилсульфід СН 3–S–СН 3. Являє собою без барвну летку рідину з неприємним запахом. Добувають у при сутності каталізатора з метанолу та сірководню. Використовують для виробництва диметилсульфоксиду. Іприт (β, β’ диxлopдieтилcyльфiд) СІСН 2–S–СН 2 С 1. Безбарвна кристалічна речовина, погано розчинна у воді, добре – в органічних розчинниках (Т. кип. 157 °С). Технічний іприт являє собою бурувату рідину з запахом гірчиці. Надзви чайноотруйний. Це бойова отруйна речовина (БОР) шкірно наривної та загальнотоксичної дії, протиплазматична отрута. Як БОР іприт був уперше застосований Німеччиною у 1917 р. біля бельгійського міста Іпр (звідки і назва – іприт) проти англо французьких військ. Смертельна концентрація іприту при потраплянні на шкіру 70 мг/кг. Як захисні засоби застосовують протигаз і спецодяг. Для дегазації використовують хлоруючі та окиснюючі агенти. Діафенілсульфон (NH 2–C 6 H 4–SO 2–C 6 H 4–NH 2– 4, 4 діамінодифенілсульфон). Застосовується у медицині як лікарський препарат для лікування лепри (прокази). Диметилсульфоксид (димексид, ДМСО) (CH 3)2 S=О. Без барвна рідина, ефективний органічний розчинник. ДМСО широко використовується в органіч ному синтезі, промисло вості. Застосовується як лікарський препарат з проти запальними, знеболюючими й антимікробними властивостями. Головним чином використовується для зовнішнього застосування (примочки, мазі, розчини та ін. ). Дигідрохлорид цистаміну (дигідрохлорид біс β аміноетил)дисульфіду) – NH –CH –S–S–CH –NH · 2 HCl. Він знайшов застосування як лікарський
Реакція з солями важких металів. Сульфіди легко реагують з солями важких металів з утворенням комплексів, наприклад: R 2 S + Hg. Cl 2 → R 2 S · Hg. Cl 2 Ця реакція застосовується в аналізі для ідентифікації сульфідів. На цій реакції ґрунтується і використання деяких сульфідів як антидотів при отруєнні солями важких металів. Окремі представники. Застосування. Диметилсульфід СН 3–S–СН 3. Являє собою без барвну летку рідину з неприємним запахом. Добувають у при сутності каталізатора з метанолу та сірководню. Використовують для виробництва диметилсульфоксиду. Іприт (β, β’ диxлopдieтилcyльфiд) СІСН 2–S–СН 2 С 1. Безбарвна кристалічна речовина, погано розчинна у воді, добре – в органічних розчинниках (Т. кип. 157 °С). Технічний іприт являє собою бурувату рідину з запахом гірчиці. Надзви чайноотруйний. Це бойова отруйна речовина (БОР) шкірно наривної та загальнотоксичної дії, протиплазматична отрута. Як БОР іприт був уперше застосований Німеччиною у 1917 р. біля бельгійського міста Іпр (звідки і назва – іприт) проти англо французьких військ. Смертельна концентрація іприту при потраплянні на шкіру 70 мг/кг. Як захисні засоби застосовують протигаз і спецодяг. Для дегазації використовують хлоруючі та окиснюючі агенти. Діафенілсульфон (NH 2–C 6 H 4–SO 2–C 6 H 4–NH 2– 4, 4 діамінодифенілсульфон). Застосовується у медицині як лікарський препарат для лікування лепри (прокази). Диметилсульфоксид (димексид, ДМСО) (CH 3)2 S=О. Без барвна рідина, ефективний органічний розчинник. ДМСО широко використовується в органіч ному синтезі, промисло вості. Застосовується як лікарський препарат з проти запальними, знеболюючими й антимікробними властивостями. Головним чином використовується для зовнішнього застосування (примочки, мазі, розчини та ін. ). Дигідрохлорид цистаміну (дигідрохлорид біс β аміноетил)дисульфіду) – NH –CH –S–S–CH –NH · 2 HCl. Він знайшов застосування як лікарський


