Лекция серная кислота1.ppt
- Количество слайдов: 55
 Технология серной кислоты • Среди минеральных кислот, производимых химической промышленностью, серная кислота по объему производства и потребления занимает первое место. Объясняется это и тем, что она самая дешевая из всех кислот, а также ее свойствами. Серная кислота не дымит, в концентри рованном виде не разрушает черные металлы, в то же время является одной из самых сильных кислот, в широком диапазоне температур (от 40. . . 20 до +260 336, 5 °С) находится в жидком состоянии.
Технология серной кислоты • Среди минеральных кислот, производимых химической промышленностью, серная кислота по объему производства и потребления занимает первое место. Объясняется это и тем, что она самая дешевая из всех кислот, а также ее свойствами. Серная кислота не дымит, в концентри рованном виде не разрушает черные металлы, в то же время является одной из самых сильных кислот, в широком диапазоне температур (от 40. . . 20 до +260 336, 5 °С) находится в жидком состоянии.
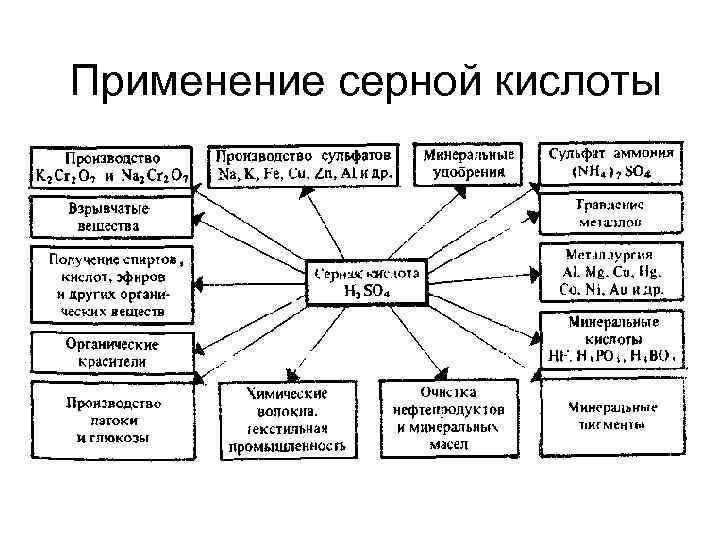 Применение серной кислоты
Применение серной кислоты
 Температура кристаллизации серной кислоты
Температура кристаллизации серной кислоты
 • Серная кислота может существовать как самостоятельное химическое соединение H 2 SO 4, а также в виде соединений с водой H 2 SO 4 • 2 Н 2 О, H 2 SO 4 • 4 Н 2 О и с триоксидом серы H 2 SO 4 • SO 3, H 2 SO 4 • 2 SO 3. • В технике серной кислотой называют и безводную H 2 SO 4 и ее водные растворы (по сути дела, это смесь Н 2 О, H 2 SO 4 и соединений H 2 SO 4 • n. Н 2 О), и растворы триоксида серы в безводной H 2 SO 4 олеум (смесь H 2 SO 4 и соединений H 2 SO 4 • n SO 3).
• Серная кислота может существовать как самостоятельное химическое соединение H 2 SO 4, а также в виде соединений с водой H 2 SO 4 • 2 Н 2 О, H 2 SO 4 • 4 Н 2 О и с триоксидом серы H 2 SO 4 • SO 3, H 2 SO 4 • 2 SO 3. • В технике серной кислотой называют и безводную H 2 SO 4 и ее водные растворы (по сути дела, это смесь Н 2 О, H 2 SO 4 и соединений H 2 SO 4 • n. Н 2 О), и растворы триоксида серы в безводной H 2 SO 4 олеум (смесь H 2 SO 4 и соединений H 2 SO 4 • n SO 3).
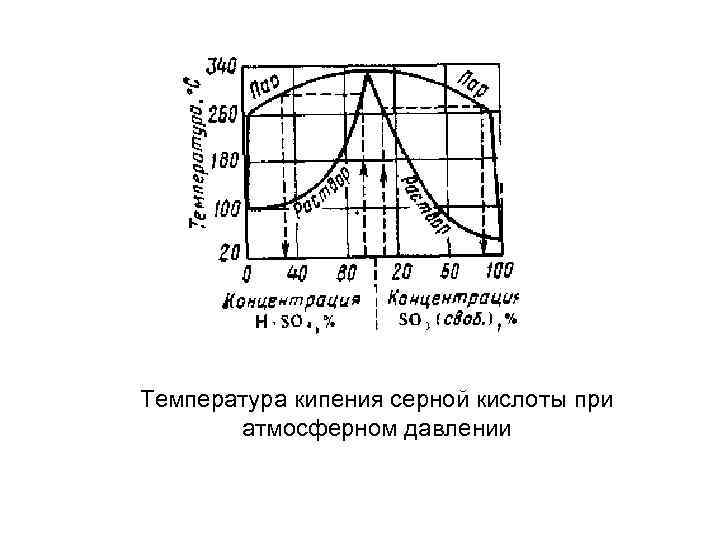 Температура кипения серной кислоты при атмосферном давлении
Температура кипения серной кислоты при атмосферном давлении
 • Нижняя кривая этой диаграммы фазового равновесия отвечает составу жидкой фазы, верхняя составу паровой фазы, находящейся в равновесии с кипящей жидкой. Из диаграммы следует, что серная кислота и вода образуют азеотропную смесь состава 98, 3% H 2 SO 4 и 1, 7°С Н 2 О с максималь ной температурой кипения (336, 5 °С). Состав находящихся в равновесии жидкой и паровой фаз для кислоты азеотропной концентрации одинаков: у более разбавленных растворов кислоты в паровой фазе преобладают пары воды, в паровой фазе над олеумом высока равновесная концентрация SO 3.
• Нижняя кривая этой диаграммы фазового равновесия отвечает составу жидкой фазы, верхняя составу паровой фазы, находящейся в равновесии с кипящей жидкой. Из диаграммы следует, что серная кислота и вода образуют азеотропную смесь состава 98, 3% H 2 SO 4 и 1, 7°С Н 2 О с максималь ной температурой кипения (336, 5 °С). Состав находящихся в равновесии жидкой и паровой фаз для кислоты азеотропной концентрации одинаков: у более разбавленных растворов кислоты в паровой фазе преобладают пары воды, в паровой фазе над олеумом высока равновесная концентрация SO 3.
 • Рассмотренные свойства серной кислоты необходимо учитывать как при выборе технологического режима процесса, так и проектировании отдельных аппаратов, трубопроводов и т. д. Например, при размещении цеха на открытой площадке необходимо предусмотреть теплоизоляцию трубопроводов, по которым циркулируют растворы серной кислоты, имеющие достаточно высокие температуры кристаллизации. Учет диаграммы фазового равновесия паров и жидкости позволяет правильно выбрать условия проведения стадии абсорбции триоксида серы, обеспечивающие высокую степень абсорбции и предупреждающие побочные явления, такие, например, как образование сернокислотного тумана.
• Рассмотренные свойства серной кислоты необходимо учитывать как при выборе технологического режима процесса, так и проектировании отдельных аппаратов, трубопроводов и т. д. Например, при размещении цеха на открытой площадке необходимо предусмотреть теплоизоляцию трубопроводов, по которым циркулируют растворы серной кислоты, имеющие достаточно высокие температуры кристаллизации. Учет диаграммы фазового равновесия паров и жидкости позволяет правильно выбрать условия проведения стадии абсорбции триоксида серы, обеспечивающие высокую степень абсорбции и предупреждающие побочные явления, такие, например, как образование сернокислотного тумана.
 Получение серной кислоты • Получение серной кислоты включает несколько этапов. Первым этапом является получение диоксида серы окислением (обжигом) серосодержащего сырья. Следующий этап — превращение оксида серы в оксид серы. Этот окислительный процесс характеризуется очень высоким значением энергии активации, для понижения которой необходимо, как правило, применение катализаторов. В зависимости от того, как осуществляется процесс окисления SO 2 в SO 3, различают два основных метода получения серной кислоты. • В контактном методе получения серной кислоты процесс окисления SO 2 и SO 3 проводят на твердых катализаторах.
Получение серной кислоты • Получение серной кислоты включает несколько этапов. Первым этапом является получение диоксида серы окислением (обжигом) серосодержащего сырья. Следующий этап — превращение оксида серы в оксид серы. Этот окислительный процесс характеризуется очень высоким значением энергии активации, для понижения которой необходимо, как правило, применение катализаторов. В зависимости от того, как осуществляется процесс окисления SO 2 в SO 3, различают два основных метода получения серной кислоты. • В контактном методе получения серной кислоты процесс окисления SO 2 и SO 3 проводят на твердых катализаторах.
 • Триоксид серы переводят в серную кислоту на последней стадии процесса — абсорбции триоксида серы, которую упрощенно можно представить уравнением реакции • SO 3+Н 2 О= H 2 SO 4
• Триоксид серы переводят в серную кислоту на последней стадии процесса — абсорбции триоксида серы, которую упрощенно можно представить уравнением реакции • SO 3+Н 2 О= H 2 SO 4
 Башенный метод • При проведении процесса по нитрозному (башенному) методу в качестве переносчика кислорода используют оксиды азота. • Окисление диоксида серы осуществляется в жидкой фазе и конечным продуктом является серная кислота: • 5 SО 2 + N 203 +Н 2 О = H 2 S 04+2 NO • В настоящее время в промышленности в основном применяют контактный метод получения серной кислоты, позволяющий использовать аппараты с большей интенсивностью.
Башенный метод • При проведении процесса по нитрозному (башенному) методу в качестве переносчика кислорода используют оксиды азота. • Окисление диоксида серы осуществляется в жидкой фазе и конечным продуктом является серная кислота: • 5 SО 2 + N 203 +Н 2 О = H 2 S 04+2 NO • В настоящее время в промышленности в основном применяют контактный метод получения серной кислоты, позволяющий использовать аппараты с большей интенсивностью.
 Контактный метод получения серной кислоты. • Рассмотрим процесс получения серной кислоты контактным методом из двух видов сырья: серного (железного) колчедана и серы. Первой стадией процесса является окисление сырья с получением обжигового газа, содержащего диоксид серы. В зависимости от вида сырья протекают экзотермические химические реакции обжига: • 4 Fe. S 2 + 1102 — 2 Fе 2 О 3 +8 SO 2 • S +02 = S 02
Контактный метод получения серной кислоты. • Рассмотрим процесс получения серной кислоты контактным методом из двух видов сырья: серного (железного) колчедана и серы. Первой стадией процесса является окисление сырья с получением обжигового газа, содержащего диоксид серы. В зависимости от вида сырья протекают экзотермические химические реакции обжига: • 4 Fe. S 2 + 1102 — 2 Fе 2 О 3 +8 SO 2 • S +02 = S 02
 • При протекании реакции помимо газообразного продукта реакции SO 2 образуется твердый продукт Fe 2 O 3, который может присутствовать в газовой фазе в виде пыли. Колчедан содержит различные примеси, в частности соединения мышьяка и фтора, которые и процессе обжига переходят в газовую фазу. Присутствие этих соединений на стадии контактного окисления диоксида серы может вызвать отравление катализатора. Поэтому реакционный газ после стадии обжига колчедана должен быть предварительно направлен настадию подготовки к контактному окислению (вторая стадия), которая помимо очистки от каталитических ядов включает выделение паров воды (осушку), а также получение побочных продуктов (Se и Те).
• При протекании реакции помимо газообразного продукта реакции SO 2 образуется твердый продукт Fe 2 O 3, который может присутствовать в газовой фазе в виде пыли. Колчедан содержит различные примеси, в частности соединения мышьяка и фтора, которые и процессе обжига переходят в газовую фазу. Присутствие этих соединений на стадии контактного окисления диоксида серы может вызвать отравление катализатора. Поэтому реакционный газ после стадии обжига колчедана должен быть предварительно направлен настадию подготовки к контактному окислению (вторая стадия), которая помимо очистки от каталитических ядов включает выделение паров воды (осушку), а также получение побочных продуктов (Se и Те).
 • На третьей стадии протекает обратимая экзотермическая химичес кая реакция контактного окисления диоксида серы: • S 02+1/202 = S 03 • Последняя стадия процесса — абсорбция триоксида серы концентрированной серной кислотой или олеумом. • Повышение степени превращения SO 2 может быть достигнуто разными путями. Наиболее распространенный из них — создание схем двойного контактирования и двойной абсорбции (ДКДА).
• На третьей стадии протекает обратимая экзотермическая химичес кая реакция контактного окисления диоксида серы: • S 02+1/202 = S 03 • Последняя стадия процесса — абсорбция триоксида серы концентрированной серной кислотой или олеумом. • Повышение степени превращения SO 2 может быть достигнуто разными путями. Наиболее распространенный из них — создание схем двойного контактирования и двойной абсорбции (ДКДА).
 Получение обжигового газа из колчедана. • Суммарную реакцию обжига колчедана можно представить в виде реакции, где Δ Н = • — 853, 8 к. Дж/моль Fe. S 2, или 7117 к. Дж/кг. Фактически она протекает через несколько последовательно параллельных стадий. Сначала происходит медленная эндотермическая реакция термического разложения дисульфида железа, а затем начинаются сильно экзотермические реакции горения паров серы и окисления сульфида железа Fe. S
Получение обжигового газа из колчедана. • Суммарную реакцию обжига колчедана можно представить в виде реакции, где Δ Н = • — 853, 8 к. Дж/моль Fe. S 2, или 7117 к. Дж/кг. Фактически она протекает через несколько последовательно параллельных стадий. Сначала происходит медленная эндотермическая реакция термического разложения дисульфида железа, а затем начинаются сильно экзотермические реакции горения паров серы и окисления сульфида железа Fe. S
 • Колчедан, применяемый для обжига, предварительно обогащают флотацией. Флотационный колчедан кроме пирита Fe. S 2 содержит ряд примесей (в частности, соединения мышьяка, селена, теллура, фтора), которые при обжиге переходят в состав обжигового газа в виде оксидов As 2 O 3, Se. O 2, Te. O 2 и фторсодержащих газообразных соединений HF, Si. F 4. Наличие этих соединений обусловливает необходимость последующей очистки газа.
• Колчедан, применяемый для обжига, предварительно обогащают флотацией. Флотационный колчедан кроме пирита Fe. S 2 содержит ряд примесей (в частности, соединения мышьяка, селена, теллура, фтора), которые при обжиге переходят в состав обжигового газа в виде оксидов As 2 O 3, Se. O 2, Te. O 2 и фторсодержащих газообразных соединений HF, Si. F 4. Наличие этих соединений обусловливает необходимость последующей очистки газа.
 Функциональные схемы производства серной кислоты
Функциональные схемы производства серной кислоты
 Циклонная печь для сжигания серы: 1 — форкамера; 2, 3 — камеры дожигания; 4 — воздушный короб: 5, 6 — пережимные кольца: 7, 9 — сопла для подачи воздуха; 8, 10 — форсунки для подачи серы
Циклонная печь для сжигания серы: 1 — форкамера; 2, 3 — камеры дожигания; 4 — воздушный короб: 5, 6 — пережимные кольца: 7, 9 — сопла для подачи воздуха; 8, 10 — форсунки для подачи серы
 Получение обжигового газа из серы. • При сжигании серы протекает необратимая экзотермическая реакция с выделением очень большого количества теплоты: ΔН— 362, 4 к. Дж/моль, или в пересчете на единицу массы 362, 4/32 = 11 325 к. Дж/кг S. • Расплавленная жидкая сера, подаваемая на сжигание, испаряется (кипит) при температуре 444, 6 o. С; теплота испарения составляет 288 к. Дж/кг. Как видно из приведенных данных, теплоты реакции го рения серы вполне достаточно для испарения исходного сырья, поэто му взаимодействие серы и кислорода происходит в газовой фазе (гомогенная реакция).
Получение обжигового газа из серы. • При сжигании серы протекает необратимая экзотермическая реакция с выделением очень большого количества теплоты: ΔН— 362, 4 к. Дж/моль, или в пересчете на единицу массы 362, 4/32 = 11 325 к. Дж/кг S. • Расплавленная жидкая сера, подаваемая на сжигание, испаряется (кипит) при температуре 444, 6 o. С; теплота испарения составляет 288 к. Дж/кг. Как видно из приведенных данных, теплоты реакции го рения серы вполне достаточно для испарения исходного сырья, поэто му взаимодействие серы и кислорода происходит в газовой фазе (гомогенная реакция).
 Сравнительные характеристики печей КС и механических (подовых) Печь Интенсивность, кг/(м 3 -сут) КС Механическая 1000 200 Содер. Запылен. Содержание ность газа. жание S в SO 3 на г/м 8 огарке, % выходе из печи, % 13— 15 8 — 9 Печь КС для обжига колчедана: 1 корпус; 2 - разгрузочная камера; колчедана 3 — бункер для огарка; 4 — подовая плита (решетка); 5 — охлаждающие элементы; 6 — коллектор для подачи 300 - 10 0, 5— 1, 2
Сравнительные характеристики печей КС и механических (подовых) Печь Интенсивность, кг/(м 3 -сут) КС Механическая 1000 200 Содер. Запылен. Содержание ность газа. жание S в SO 3 на г/м 8 огарке, % выходе из печи, % 13— 15 8 — 9 Печь КС для обжига колчедана: 1 корпус; 2 - разгрузочная камера; колчедана 3 — бункер для огарка; 4 — подовая плита (решетка); 5 — охлаждающие элементы; 6 — коллектор для подачи 300 - 10 0, 5— 1, 2
 • Так как реакция окисления SO 2 относится к типу экзотермических, температурный режим ее проведения должен приближаться к линии оптимальных температур. На выбор температурного режима дополнительно накладываются два ограничения, связанные со свойствами катализатора. Нижним температурным пределом является температура зажигания ванадиевых катализаторов, составляющая в зависимости от конкретного вида катализатора и состава газа 400— 440 °С. Верхний температурный предел составляет 600— 650 °С и оп ределяется тем, что выше этих температур происходит перестройка структуры катализатора и он теряет свою активность. • В диапазоне 400— 600 °С процесс стремятся провести так, чтобы по мере увеличения степени превращения температура уменьшалась.
• Так как реакция окисления SO 2 относится к типу экзотермических, температурный режим ее проведения должен приближаться к линии оптимальных температур. На выбор температурного режима дополнительно накладываются два ограничения, связанные со свойствами катализатора. Нижним температурным пределом является температура зажигания ванадиевых катализаторов, составляющая в зависимости от конкретного вида катализатора и состава газа 400— 440 °С. Верхний температурный предел составляет 600— 650 °С и оп ределяется тем, что выше этих температур происходит перестройка структуры катализатора и он теряет свою активность. • В диапазоне 400— 600 °С процесс стремятся провести так, чтобы по мере увеличения степени превращения температура уменьшалась.
 • Мокрая очистка обжигового газа заключается в промывке его разбавленной серной кислотой. При этом происходит ряд физических процессов: конденсация, абсорбция и т. п. • Основные примеси обжигового газа (As 2 O 3, Se. O 2 и др. ), находящиеся в газо и парообразном состоянии, выделяются при промывке серной кислотой, имеющей более низкую температуру, чем очищаемый газ. Примеси частично растворяются в серной кислоте, но большая их часть переходит в состав сернокислотного тумана. Появление тумана объясняют тем, что кроме SO 2, обжиговый газ содержит небольшое количество триоксида серы и паров воды, которые при охлаждении газа взаимодействуют с образованием паров серной кислоты. В первой промывной башне газ очень быстро охлаждается; при этом пары серной кислоты конденсируются в объеме в виде тумана мелких взвешенных в газе капель.
• Мокрая очистка обжигового газа заключается в промывке его разбавленной серной кислотой. При этом происходит ряд физических процессов: конденсация, абсорбция и т. п. • Основные примеси обжигового газа (As 2 O 3, Se. O 2 и др. ), находящиеся в газо и парообразном состоянии, выделяются при промывке серной кислотой, имеющей более низкую температуру, чем очищаемый газ. Примеси частично растворяются в серной кислоте, но большая их часть переходит в состав сернокислотного тумана. Появление тумана объясняют тем, что кроме SO 2, обжиговый газ содержит небольшое количество триоксида серы и паров воды, которые при охлаждении газа взаимодействуют с образованием паров серной кислоты. В первой промывной башне газ очень быстро охлаждается; при этом пары серной кислоты конденсируются в объеме в виде тумана мелких взвешенных в газе капель.
 Устройство трубчатого, как наиболее простого, электрофильтра изображе но на рис. 1. Он состоит из осадительного (1) и коронирующего (2) электродов, 4 изолятор для подключения коронирующегоэлектрода, 5 фланец, 6, 7 коллектор, емкость для сбора пыли соответственно.
Устройство трубчатого, как наиболее простого, электрофильтра изображе но на рис. 1. Он состоит из осадительного (1) и коронирующего (2) электродов, 4 изолятор для подключения коронирующегоэлектрода, 5 фланец, 6, 7 коллектор, емкость для сбора пыли соответственно.
 Осадительный электрод, как правило, представляет собой металлическую трубу, а коронирующий тонкую проволоку или стержень с острыми краями. Под действием высокого напряжения между осадительным и коронирующим электродом возникает коронный разряд. Твердые или жидкие частицы, находящиеся в газе, заряжаются и под действием электрического поля осаждаются, образуя компактнуюоднородную массу (3). Далее после того как эта масса сформируется в некоторое подобие материала, она при помощи вибрации удаляется вниз в контейнер.
Осадительный электрод, как правило, представляет собой металлическую трубу, а коронирующий тонкую проволоку или стержень с острыми краями. Под действием высокого напряжения между осадительным и коронирующим электродом возникает коронный разряд. Твердые или жидкие частицы, находящиеся в газе, заряжаются и под действием электрического поля осаждаются, образуя компактнуюоднородную массу (3). Далее после того как эта масса сформируется в некоторое подобие материала, она при помощи вибрации удаляется вниз в контейнер.
 Степень улавливания пыли электрофильтром в зависимости от приложенного напряжения. Т температура газа; v – скорость газа; q запыленность очищаемого газа.
Степень улавливания пыли электрофильтром в зависимости от приложенного напряжения. Т температура газа; v – скорость газа; q запыленность очищаемого газа.
 Теоретические основы улавливания пыли электрофильтрами. • Для расчета степени улавливания пыли трубчатым электрофильтром Дейчем была выведена следующая формула: • • • где L длина осадительного электрода; υ линейная скорость газа в электрофильтре; R радиус осадительного электрода; ω скорость дрейфа частицы к электроду. При выводе формулы были сделаны следующие допущения:
Теоретические основы улавливания пыли электрофильтрами. • Для расчета степени улавливания пыли трубчатым электрофильтром Дейчем была выведена следующая формула: • • • где L длина осадительного электрода; υ линейная скорость газа в электрофильтре; R радиус осадительного электрода; ω скорость дрейфа частицы к электроду. При выводе формулы были сделаны следующие допущения:
 • 1. Шарообразная частица пыли движется в однородном электрическом поле. • 2. Заряд частицы не изменяется во времени и равен максимально возможному, полученному по ударному механизму. • 3. Интенсивность турбулентности потока в любом сечении канала достаточна для полного выравнивания концентрации перемешивающихся частиц. • Скорость дрейфа рассчитывается из предположения, что на частицу пыли действует две силы: сила электрического поля (Fэ) и сила сопротивления среды (Fс). • Fэ = Fс , • QE=6πμrω , • где Е напряженность электрического поля. • Движение частицы считается установившимся.
• 1. Шарообразная частица пыли движется в однородном электрическом поле. • 2. Заряд частицы не изменяется во времени и равен максимально возможному, полученному по ударному механизму. • 3. Интенсивность турбулентности потока в любом сечении канала достаточна для полного выравнивания концентрации перемешивающихся частиц. • Скорость дрейфа рассчитывается из предположения, что на частицу пыли действует две силы: сила электрического поля (Fэ) и сила сопротивления среды (Fс). • Fэ = Fс , • QE=6πμrω , • где Е напряженность электрического поля. • Движение частицы считается установившимся.
 Было установлено, что частицы пыли могут заряжаться по ударному и диффузионному механизмам, причем процесс зарядки протекает во времени. По ударному механизму заряжаются частицы размером более 1 мкм в сильных электрических полях: Первый сомножитель уравнения выражает величину максимально возможного заряда, получаемого по ударному механизму. По формуле рассчитывается заряд частиц размером менее 1 мкм, получаемый по диффузионному механизму в слабых электрических полях и в отсутствии электрического поля для частиц всех размеров.
Было установлено, что частицы пыли могут заряжаться по ударному и диффузионному механизмам, причем процесс зарядки протекает во времени. По ударному механизму заряжаются частицы размером более 1 мкм в сильных электрических полях: Первый сомножитель уравнения выражает величину максимально возможного заряда, получаемого по ударному механизму. По формуле рассчитывается заряд частиц размером менее 1 мкм, получаемый по диффузионному механизму в слабых электрических полях и в отсутствии электрического поля для частиц всех размеров.
 Зависимость равновесной степени превращения SO 2: а — от температуры при разных давлениях: 1 — 0, 1 МПа; 2 — 1 МПа, 3 — 10 Мпа Состав исходной реакционной смеси: 7 % SO 2, 11% 02, 82% N 2; б—от молярного отношения О 2 : SO 2 (температура 475 о. С: давление 0. 1 МПа)
Зависимость равновесной степени превращения SO 2: а — от температуры при разных давлениях: 1 — 0, 1 МПа; 2 — 1 МПа, 3 — 10 Мпа Состав исходной реакционной смеси: 7 % SO 2, 11% 02, 82% N 2; б—от молярного отношения О 2 : SO 2 (температура 475 о. С: давление 0. 1 МПа)
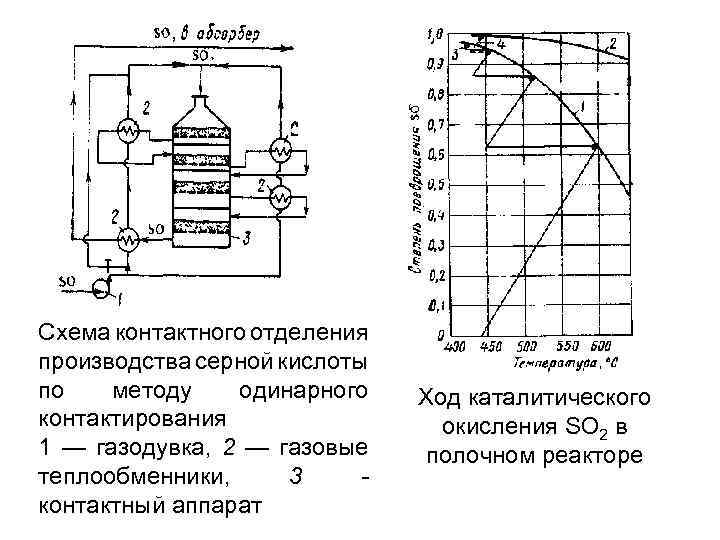 Схема контактного отделения производства серной кислоты по методу одинарного контактирования 1 — газодувка, 2 — газовые теплообменники, 3 контактный аппарат Ход каталитического окисления SO 2 в полочном реакторе
Схема контактного отделения производства серной кислоты по методу одинарного контактирования 1 — газодувка, 2 — газовые теплообменники, 3 контактный аппарат Ход каталитического окисления SO 2 в полочном реакторе
 Абсорбция триоксида серы. • Диаграмма фазового равновесия пар — жидкость для системы Н 2 О—H 2 SO 4—SO 3 показывает, что оптимальным абсорбентом является 98, 3% ная серная кислота (техническое название — моногидрат), соответствующая азеотропному составу. Действительно, над этой кислотой практически нет ни паров воды, ни паров SO 3. Протекающий при этом процесс можно условно описать уравнением реакции: • S 03 + n. H 2 S 04+H 20 = (n 1) H 2 S 04
Абсорбция триоксида серы. • Диаграмма фазового равновесия пар — жидкость для системы Н 2 О—H 2 SO 4—SO 3 показывает, что оптимальным абсорбентом является 98, 3% ная серная кислота (техническое название — моногидрат), соответствующая азеотропному составу. Действительно, над этой кислотой практически нет ни паров воды, ни паров SO 3. Протекающий при этом процесс можно условно описать уравнением реакции: • S 03 + n. H 2 S 04+H 20 = (n 1) H 2 S 04
 • Использование в качестве поглотителя менее концентрированной серной кислоты может привести к образованию сернокислотного тумана, а над 100% ной серной кислотой или олеумом в паровой фазе довольно велико равновесное парциальное давление SO 3, поэтому он будет абсорбироваться не полностью. Однако если в качестве одного из продуктов процесса необходимо получить олеум, можно совместить абсорбцию олеумом (1 й абсорбер) и абсорбцию 98. 3% ной кислотой 2 й абсорбер).
• Использование в качестве поглотителя менее концентрированной серной кислоты может привести к образованию сернокислотного тумана, а над 100% ной серной кислотой или олеумом в паровой фазе довольно велико равновесное парциальное давление SO 3, поэтому он будет абсорбироваться не полностью. Однако если в качестве одного из продуктов процесса необходимо получить олеум, можно совместить абсорбцию олеумом (1 й абсорбер) и абсорбцию 98. 3% ной кислотой 2 й абсорбер).
 Степень абсорбции SO 3 в моногидратном абсорбере при различных температурах: 1 — при 60 °С. 2 — при 80°С; 3 — при 100 о. С; 4 — при 120 °С. 95 96 97 98 99 96 Концентрация серной кислоты, %
Степень абсорбции SO 3 в моногидратном абсорбере при различных температурах: 1 — при 60 °С. 2 — при 80°С; 3 — при 100 о. С; 4 — при 120 °С. 95 96 97 98 99 96 Концентрация серной кислоты, %
 Контактное отделение произ водсгва серной кислоты по схеме ДКДА: 1 газодувка; 2 - газовые теплообменники; 3 контактный аппарат
Контактное отделение произ водсгва серной кислоты по схеме ДКДА: 1 газодувка; 2 - газовые теплообменники; 3 контактный аппарат
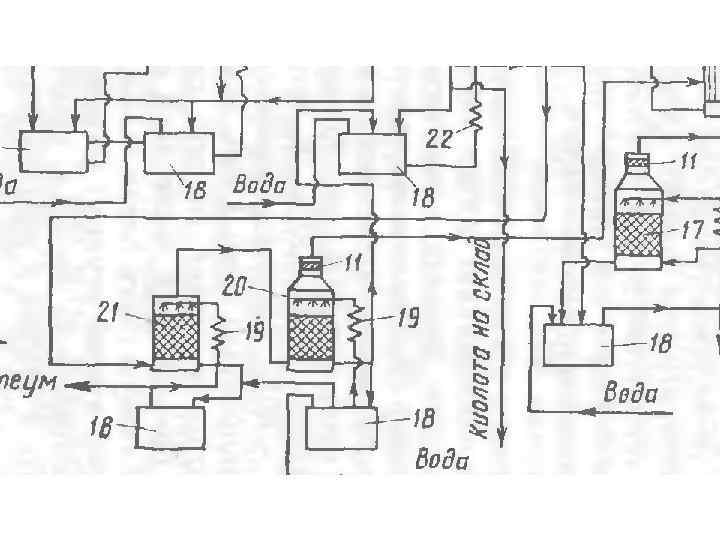
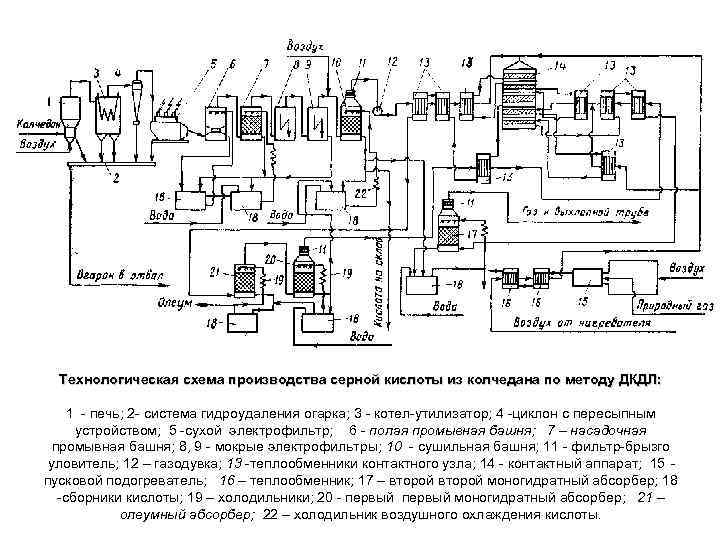 Технологическая схема производства серной кислоты из колчедана по методу ДКДЛ: 1 печь; 2 система гидроудаления огарка; 3 котел утилизатор; 4 циклон с пересыпным устройством; 5 сухой электрофильтр; 6 полая промывная башня; 7 – насадочная промывная башня; 8, 9 мокрые электрофильтры; 10 сушильная башня; 11 фильтр брызго уловитель; 12 – газодувка; 13 теплообменники контактного узла; 14 контактный аппарат; 15 пусковой подогреватель; 16 – теплообменник; 17 – второй моногидратный абсорбер; 18 сборники кислоты; 19 – холодильники; 20 первый моногидратный абсорбер; 21 – олеумный абсорбер; 22 – холодильник воздушного охлаждения кислоты.
Технологическая схема производства серной кислоты из колчедана по методу ДКДЛ: 1 печь; 2 система гидроудаления огарка; 3 котел утилизатор; 4 циклон с пересыпным устройством; 5 сухой электрофильтр; 6 полая промывная башня; 7 – насадочная промывная башня; 8, 9 мокрые электрофильтры; 10 сушильная башня; 11 фильтр брызго уловитель; 12 – газодувка; 13 теплообменники контактного узла; 14 контактный аппарат; 15 пусковой подогреватель; 16 – теплообменник; 17 – второй моногидратный абсорбер; 18 сборники кислоты; 19 – холодильники; 20 первый моногидратный абсорбер; 21 – олеумный абсорбер; 22 – холодильник воздушного охлаждения кислоты.





 Основные виды конструкций циклонов (по подводу газов): а спиральный; б-тангенциальный; в-винтообразный; г розеточный (циклон с возвратом газов); д-розеточный Схема работы циклона: 1 -входной патрубок; 2 -выхлопная труба; 3 -цилиндрическая камера; 4 -коническая камера; 5 -пылеосадительная камера.
Основные виды конструкций циклонов (по подводу газов): а спиральный; б-тангенциальный; в-винтообразный; г розеточный (циклон с возвратом газов); д-розеточный Схема работы циклона: 1 -входной патрубок; 2 -выхлопная труба; 3 -цилиндрическая камера; 4 -коническая камера; 5 -пылеосадительная камера.
 ЦЕНТРОБЕЖНЫЕ ПЫЛЕУЛОВИТЕЛИ (ЦИКЛОНЫ) Центробежные силы, возникающие при вращении газового потока, широко используются в технике пылеулавливания. На этом принципе основана работа наиболее многочисленной группы пылеуловителей циклонов. Вследствие дешевизны и простоты устройства и обслуживания,
ЦЕНТРОБЕЖНЫЕ ПЫЛЕУЛОВИТЕЛИ (ЦИКЛОНЫ) Центробежные силы, возникающие при вращении газового потока, широко используются в технике пылеулавливания. На этом принципе основана работа наиболее многочисленной группы пылеуловителей циклонов. Вследствие дешевизны и простоты устройства и обслуживания,
 сравнительно небольшого сопротивления и высокой производительности циклоны имеют преимущество перед другими аппаратами, применяемыми для очистки газов.
сравнительно небольшого сопротивления и высокой производительности циклоны имеют преимущество перед другими аппаратами, применяемыми для очистки газов.
 Башенный скруббер с оросительным устройством, расположенным по: а)окружности (б) оси
Башенный скруббер с оросительным устройством, расположенным по: а)окружности (б) оси


 виды насадок: 1 -кольца Рашига; 2 -кольца с перегородкой; 3 -кольца с крестообразной перегородкой; 4 -кольца Палля (с вырезами в стенках и перегородками); 5 -седла Берля; 6 -седло “Инталокс”; 7 -розетка Теллера;
виды насадок: 1 -кольца Рашига; 2 -кольца с перегородкой; 3 -кольца с крестообразной перегородкой; 4 -кольца Палля (с вырезами в стенках и перегородками); 5 -седла Берля; 6 -седло “Инталокс”; 7 -розетка Теллера;
 • Так как реакция окисления SO 2 относится к типу экзотермических, температурный режим ее проведения должен приближаться к линии оптимальных температур. На выбор температурного режима дополнительно накладываются два ограничения, связанные со свойствами катализатора. Нижним температурным пределом является температура зажигания ванадиевых катализаторов, составляющая в зависимости от конкретного вида катализатора и состава газа 400— 440 °С. Верхний температурный предел составляет 600— 650 °С и оп ределяется тем, что выше этих температур происходит перестройка структуры катализатора и он теряет свою активность. • В диапазоне 400— 600 °С процесс стремятся провести так, чтобы по мере увеличения степени превращения температура уменьшалась.
• Так как реакция окисления SO 2 относится к типу экзотермических, температурный режим ее проведения должен приближаться к линии оптимальных температур. На выбор температурного режима дополнительно накладываются два ограничения, связанные со свойствами катализатора. Нижним температурным пределом является температура зажигания ванадиевых катализаторов, составляющая в зависимости от конкретного вида катализатора и состава газа 400— 440 °С. Верхний температурный предел составляет 600— 650 °С и оп ределяется тем, что выше этих температур происходит перестройка структуры катализатора и он теряет свою активность. • В диапазоне 400— 600 °С процесс стремятся провести так, чтобы по мере увеличения степени превращения температура уменьшалась.
 Технологическая схема производства серной кислоты из колчедана методом двойного контактирования. • Колчедан через дозатор подают в печь кипящего слоя. Полученный запыленный обжиговый газ, содержащий 13% SO 2 и имеющий на выходе из печи температуру ~ 700 °С, подают сначала в котел утилизатор 3, а затем на стадию сухой очистки от огарковой пыли (в циклоны 4 и в сухой электрофильтр 5). В котле утилизаторе происходит охлаждение газа с одновременным получением энергетического водяного пара (давление 4 МПа и температура 450 °С), который может быть использован как в самой установке для компенсации затрат энергии на работу компрессоров и насосов, так и в других цехах завода.
Технологическая схема производства серной кислоты из колчедана методом двойного контактирования. • Колчедан через дозатор подают в печь кипящего слоя. Полученный запыленный обжиговый газ, содержащий 13% SO 2 и имеющий на выходе из печи температуру ~ 700 °С, подают сначала в котел утилизатор 3, а затем на стадию сухой очистки от огарковой пыли (в циклоны 4 и в сухой электрофильтр 5). В котле утилизаторе происходит охлаждение газа с одновременным получением энергетического водяного пара (давление 4 МПа и температура 450 °С), который может быть использован как в самой установке для компенсации затрат энергии на работу компрессоров и насосов, так и в других цехах завода.
 В очистном отделении, состоящем из двух промывных башен 6 и 7, двух пар мокрых электрофильтров 8 и 9 и сушильной башни 10, происходит очистка газа от соединений мышьяка, селена, фтора и его осушка. Первая полая промывная башня 6 работает в испарительном режиме: циркулирующая кислота охлаждает газ, при этом теплота затрачивается на испарение воды из кислоты, поступающей на орошение. Концентрацию орошающей кислоты в первой башне, равную 40— 50% H 2 SO 4, поддерживают постоянной за счет разбавления 10 15% ной кислотой из второй промывной башни 7. Кислота из второй башни поступает в сборник 18 и после охлаждения возвращается на орошение.
В очистном отделении, состоящем из двух промывных башен 6 и 7, двух пар мокрых электрофильтров 8 и 9 и сушильной башни 10, происходит очистка газа от соединений мышьяка, селена, фтора и его осушка. Первая полая промывная башня 6 работает в испарительном режиме: циркулирующая кислота охлаждает газ, при этом теплота затрачивается на испарение воды из кислоты, поступающей на орошение. Концентрацию орошающей кислоты в первой башне, равную 40— 50% H 2 SO 4, поддерживают постоянной за счет разбавления 10 15% ной кислотой из второй промывной башни 7. Кислота из второй башни поступает в сборник 18 и после охлаждения возвращается на орошение.
 • После второй промывной башни газ проходит последовательно две пары электрофильтров 8 и 9, затем насадочную сушильную башню 10, орошаемую 93— 94% ной серной кислотой при температуре 28— 30 о. C. Кислота циркулирует между сушильной башней 10 и сборни ком 18; часть кислоты отводится как готовая продукция на склад. Для поддержания постоянной концентрации H 2 SO 4 в сборник 18 вводят 98— 99% ную кислоту из моногидратных абсорберов 17 и 20. Для поддержания постоянной температуры на стадии осушки циркулирующую кислоту охлаждают в воздушном холодильнике 22.
• После второй промывной башни газ проходит последовательно две пары электрофильтров 8 и 9, затем насадочную сушильную башню 10, орошаемую 93— 94% ной серной кислотой при температуре 28— 30 о. C. Кислота циркулирует между сушильной башней 10 и сборни ком 18; часть кислоты отводится как готовая продукция на склад. Для поддержания постоянной концентрации H 2 SO 4 в сборник 18 вводят 98— 99% ную кислоту из моногидратных абсорберов 17 и 20. Для поддержания постоянной температуры на стадии осушки циркулирующую кислоту охлаждают в воздушном холодильнике 22.
 • Перед сушильной башней обжиговый газ разбавляют воздухом с целью снижения в нем концентрации SO 2 до 9% и увеличения избытка кислорода в соответствии с оптимальными условиями окисления диоксида серы. • После сушильной башни обжиговый газ проходит через фильтр брызгоуловитель 11 и поступает в турбогазодувку 12. В теплообменниках 13 газ нагревается за счет теплоты продуктов реакции до температуры зажигания катализатора (420— 440 °С) и поступает на первый слой контактного аппарата. В первом слое катализатора происходит окисление SO 2 на 74% с одновременным повышением температуры до 600 0 С.
• Перед сушильной башней обжиговый газ разбавляют воздухом с целью снижения в нем концентрации SO 2 до 9% и увеличения избытка кислорода в соответствии с оптимальными условиями окисления диоксида серы. • После сушильной башни обжиговый газ проходит через фильтр брызгоуловитель 11 и поступает в турбогазодувку 12. В теплообменниках 13 газ нагревается за счет теплоты продуктов реакции до температуры зажигания катализатора (420— 440 °С) и поступает на первый слой контактного аппарата. В первом слое катализатора происходит окисление SO 2 на 74% с одновременным повышением температуры до 600 0 С.
 • После охлаждения до 465 o. С газ поступает на второй слой контактного аппарата, где степень превращения достигает 86 96, а температура газа возрастает до 514 °С. После охлаждения до 450 °С газ поступает на третий слой контактного аппарата, где степень превращения SO 2, увеличивается до 94— 94, 5 %, а температура повышается до 470 0 С. • Затем в соответствии с требованиями метода ДКДА реакционный газ охлаждают в теплообменниках 13 до 100 °С и направляют на абсорбцию первой ступени: сначала в олеумный абсорбер 21, затем в моногидратный абсорбер 20.
• После охлаждения до 465 o. С газ поступает на второй слой контактного аппарата, где степень превращения достигает 86 96, а температура газа возрастает до 514 °С. После охлаждения до 450 °С газ поступает на третий слой контактного аппарата, где степень превращения SO 2, увеличивается до 94— 94, 5 %, а температура повышается до 470 0 С. • Затем в соответствии с требованиями метода ДКДА реакционный газ охлаждают в теплообменниках 13 до 100 °С и направляют на абсорбцию первой ступени: сначала в олеумный абсорбер 21, затем в моногидратный абсорбер 20.
 • После моногидратного абсорбера и фильт рабрызгоуловителя газ вновь нагревают до температуры 430 °С и по дают на четвертый слой катализатора. Концентрация диоксида серы в газе составляет теперь 0, 75— 0, 85%. В четвертом слое происходит окисление SO 2 на ~80%, сопровождающееся повышением темпера туры до 449 °С. Реакционную смесь вновь охлаждают до температуры 409 OС и направляют на последний (пятый) слой контактного аппара та. Общая степень превращения после пяти стадий контактирования составляет 99, 9%. Газовую смесь после охлаждения направляют в моногидратный абсорбер второй ступени абсорбции 17.
• После моногидратного абсорбера и фильт рабрызгоуловителя газ вновь нагревают до температуры 430 °С и по дают на четвертый слой катализатора. Концентрация диоксида серы в газе составляет теперь 0, 75— 0, 85%. В четвертом слое происходит окисление SO 2 на ~80%, сопровождающееся повышением темпера туры до 449 °С. Реакционную смесь вновь охлаждают до температуры 409 OС и направляют на последний (пятый) слой контактного аппара та. Общая степень превращения после пяти стадий контактирования составляет 99, 9%. Газовую смесь после охлаждения направляют в моногидратный абсорбер второй ступени абсорбции 17.
 Непоглощенный газ, состоящий в основном из воздуха, пропускают через фильтр 11 для выделения брызг и тумана и выбрасывают в атмосферу через выхлопную трубу. КОНЕЦ ЛЕКЦИИ
Непоглощенный газ, состоящий в основном из воздуха, пропускают через фильтр 11 для выделения брызг и тумана и выбрасывают в атмосферу через выхлопную трубу. КОНЕЦ ЛЕКЦИИ


