Лекция-15_pres.ppt
- Количество слайдов: 22

Технология нефтегазопереработки и нефтехимического синтеза Лекция 15: Термокаталитические процессы переработки нефти и газа (8) Газовый риформинг и родственные процессы Производство серы и водорода 15. 1. Газовый риформинг и сопряженные процессы 15. 1. 1. Конверсия метана: целевая и побочные реакции 15. 1. 2. Синтез аммиака 15. 1. 3. Синтез Ф. Фишера Г. Тропша 15. 1. 4. Производство метанола и формальдегида 15. 1. 5 Производство метиламинов и метилхлорида 15. 1. 6. Производство уксусной кислоты из метанола 15. 1. 7. Получение углеводоролов из метанола 15. 2. Производство серы по методу Клауса 15. 2. 1. Технологическая схема 15. 3. Производство водорода

Газовый риформинг и родственные процессы (1) 15. 1. Газовый риформинг и связанные с ним процессы составляют третий основной блок нефтехимического производства. Газовый риформинг в настоящее время лежит в основе промышленного синтеза аммиака, метанола, уксусной кислоты, уксусного ангидрида, алканов по Фишеру Тропшу, гидроформилирования алкенов (оксо синтез) и ряда других процессов. Термин нефтехимический газовый риформинг описывает группу родственных реакций, в результате которых природный газ или фракция нафта превращается в смесь СО и Н 2, называемую "синтез-газ". Получение "синтез газа" из природного газа может быть выражено уравнением: Эта реакция носит название конверсии метана, она эндотермична и обратима. Положение равновесия зависит от температуры, оптимальной является температура 800 С в присутствии никелевого катализатора. Образование синтез газа в результате конверсии метана осложняется рядом побочных процессов, сопровождающихся отложением кокса на катализаторе:
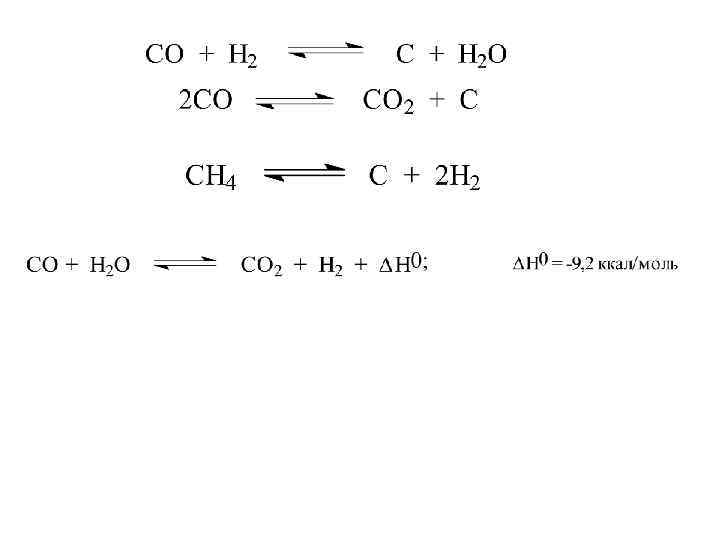

При 800° константа равновесия этой экзотермической реакции очень мала и концентрация СО 2 также ничтожно мала. Если для получения синтез газа вместо природного газа использовать фракцию нафта, то помимо синтез газа всегда получается значительное количество углерода и это осложняет процесс выделения продуктов реакции. Получение "синтез газа" конверсией метана осуществляется примерно с 1955 1960 годов. До этого его получали при взаимодействии кокса с водяным паром в очень жестких условиях при 1200°С. Необходимую для этой эндотермической реакции высокую температуру можно поддерживать за счет сжигания части кокса до СО 2. Через слой раскаленного угля поочередно продувают воздух и перегретый водяной пар. Процесс чрезвычайно энергоемок и требует затраты большого количества кокса. Более эффективна подземная газификация угля, где уголь в пластах обрабатывается смесью кислорода и водяного пара. Себестоимость синтез газа, водорода и СО, полученного газификацией каменного и бурого угля в настоящее время гораздо выше, чем при конверсии метана. Поэтому более 90% оксида углерода и водорода сейчас получают газовым риформингом природного газа и нафты. В ближайшее время, по крайней мере до 2012 года, ситуация принципиально не изменится. Однако такой прогноз не вечен.

15. 1. 2. Синтез аммиака Синтез-газ как исходное сырье используется во многих крупномасштабных химических производствах. Самым важным из них является синтез аммиака из азота и водорода. Необходимый для этого водород получают конверсией СО и последующим связыванием СО 2 раствором гидроксида калия или этаноламина. Синтез аммиака стал в настоящее время самым крупнотоннажным из всех химических производств. Мировое производство аммиака превышает 70 млн. тонн в год и продолжает расти. Лидирующее место здесь занимают СССР и США. Аммиак используется главным образом для получения азотных удобрений нитрата и сульфата аммония, мочевины и др. , а также для производства азотной кислоты. Мочевину получают при взаимодействии NH 3 и СО 2 в газовой фазе.

15. 1. 3. Синтез Фишера-Тропша Синтез Ф. Фишера Г. Тропша можно рассматривать как восстановительную олигомеризацию оксида углерода на гетерогенных катализаторах, ведущую к образованию смеси различных алкенов и алканов. В качестве катализаторов используются Co, Fe, Ru с различными добавками. Состав продуктов зависит от природы катализатора и условий реакции. Его можно изменять в очень широких пределах. При взаимодействии СО и Н 2 на Co, осажденном на кизельгуре и содержащем в качестве промоторов диоксид тория Тh. О 2 и Мg. O, при 200°С и давлении 1 1, 5 МПА получается около 80% парафинов нормального строения, 15% неразветвленных алкенов и около 5% разветвленных алканов. Получающаяся смесь углеводородов состоит из 45% низкого качества бензина, 23% дизельного топлива, 3% машинного масла и 27% высших твердых парафинов. Общая мощность производства в 1943 1944 годах достигала 1 млн тонн в год. Более дешевые и доступные Fe катализаторы активны и стабильны в широком интервале температур и давлений. На осажденных Fe-катализаторах, содержащих Si. O 2, К 2 О и медь, получают смесь бензина (32%), дизельного топлива (20%) и высших парафинов (48%), причем их соотношение меняется с изменением температуры. Бензин, получаемый на железных катализаторах, имеет лучшие моторные характеристики, чем бензин, производимый на кобальтовых катализаторах. Для получения высокомолекулярных парафинов ("полиметилена") линейных алканов с молярной массой до 10(6) эффективным оказался мелкодисперсный Ru.

15. 1. 4. Производство метанола и формальдегида Производство метанола на основе синтез-газа впервые было осуществлено в Германии в начале 1920 х годов. Первоначально в качестве катализатора использовали смесь Zn. O и Cr 2 O 3, а саму реакцию проводили при 350 400° и высоком давлении до 300 атм. Это обеспечивало 10 15% ную конверсию синтез газа в метанол, при рециркуляции выход может быть повышен до 85%. Условия проведения процесса и аппаратура в этом случае такие же, как и при синтезе аммиака, и производства метанола и аммиака часто объединяют. В настоящее время основное количество метанола получают каталитическим гидрированием СО при низком давлении на медно цинковом катализаторе. В 1960 году фирма ICI разработала процесс, где в качестве катализатора используется смесь Cu. O и Zn. O, нанесенная на глинозем. Традиционные, давно сформировавшиеся направления использования метанола заключаются в получении формальдегида, метиламинов, метилхлорида, метил трет бутилового эфира, диметилтерефталата. Около 40% производимого метанола превращают в формальдегид в результате дегидрирования или окисления.

15. 1. 5 Производство метиламинов и метилхлорида При взаимодействии метанола с аммиаком при 350 -500 С и давлении 20 атм в присутствии Аl 2 O 3 происходит образование смеси метил , диметил и триметиламина. Метилхлорид образуется при взаимодействии метанола и хлороводорода в газовой фазе при 300 С в присутствии Zn. Cl 2 или Cu. Cl 2 в качестве катализатора. В последние двадцать лет отчетливо проявляется большой и все возрастающий интерес к метанолу как исходному реагенту для самых разнообразных химических превращений. Этот интерес вызван тем, что 1) Метанол очень дешев; 2) он может быть получен практически из любого углеродсодержащего источника нефти, газа, угля, торфа и даже бытового мусора, которые можно превратить в смесь СО и Н 2; 3) из него в промышленных условиях может быть получено большое число практически важных веществ с применением как гетерогенного, так и в особенности гомогенного катализа. Некоторые наиболее перспективные направления производства на основе метанола: Это производства уксусной кислоты, уксусного ангидрида, этанола, этиленгликоля, метилметакрилата, метилформиата, диметилформамида, некоторых видов топлива и т. д. Часть из них уже эксплуатируются в промышленном масштабе, другие находятся в стадии внедрения, а остальные разрабатываются и найдут применение в недалеком будущем. Возможно, в XXI столетии метанол, наряду с этиленом, станет одним из главных полупродуктов крупнотоннажного органического синтеза.

15. 1. 6. Производство уксусной кислоты из метанола В результате роста цен на нефть (1 энергетический кризис) экономически более выгодным стал новый метод производства уксусной кислоты, основанный на карбонилировании метанола. Этот метод был разработан фирмой "Моnsantо" в 1970 г. . Это гомогенный процесс, катализируемый комплексами родия и промотируемый метилиодидом и иодидом калия. Реакция характеризуется двумя важными особенностями: 1) высокой скоростью и 2) чрезвычайно высокой селективностью (99% по метанолу и 90% по СО). Установлен механизм этого сложного превращения, который включает образование метилродиевого комплекса в результате окислительного присоединения к комплексу родия: На самом деле карбонилированию подвергается не метанол, а получающийся из него в ходе реакции метилиодид. Предшественником истинного катализатора для этой реакции может быть практически любое растворимое соединение родия (III), но обычно используют Rh. Cl 3. 3 H 2 O, а промоторами КI и СН 3 I. По этому способу в ряде стран, в том числе и в России, налажено производство СН 3 СООН объемом до 2 млн тонн в год. Мировое производство уксусной кислоты различными способами составляет примерно 5 млн тонн.

Если карбонилирование метанола, каталитизируемое соединениями кобальта, проводить в присутствии водорода, то в результате гидроформилирования метанола получается этанол. Впервые эта реакция была осуществлена в 40 х годах и получила название гомологизации метанола. Первоначально в качестве катализатора использовался карбонил кобаль та Со(СО)8, более подходящими оказались бромид 2 или иодид кобальта (II) в присутствии фосфиновых лигандов. Процесс характеризуется недостаточно высокой селективностью и наряду с этанолом образуются уксусный альдегид, ацеталь уксусного альдегида, метилацетат, этилацетат и другие соединения. Для промышленного освоения этого процесса требуется подобрать более активную и более селективную гомогенную каталитическую систему. Интерес к нему вызван тем, что при дегидратации этанола получается этилен наиболее значительный по объему производства продукт. Таким образом, открывается заманчивая перспектива получения этилена на основе каменного угля по схеме: уголь синтез-газ метанол этилен Есть все основания полагать, что эта задача будет успешно решена в начале ХXI столетия. Это же следует отнести к высокоселективному синтезу этиленгликоля из синтез газа СО и Н 2, который пока не в состоянии конкурировать с процессом окисления этилена до окиси этилена с последующим гидролизом в этиленгликоль.

15. 1. 7. Получение углеводородов из метанола Самостоятельной и актуальной проблемой является переработка метанола в углеводороды. Пионерское исследование в этой области было выполнено сотрудниками фирмы "Mobil" в 1976 1980 годах, которые впервые применили для каталитического крекинга метанола высокопористые цеолиты, названные ими ZSМ-5. На цеолитных катализаторах при 370 С и давлении 15 атм осуществляется селективное превращение метанола в смесь ароматических углеводородов и алканов, содержащих от пяти до двенадцати атомов углерода. Бензин, получаемый в этом процессе, имеет октановое число 90 -95 без добавки тетраэтилсвинца и содержит 30 -40% ароматических углеводородов, главным образом, бензол, толуол и ксилолы. Установлено, что каталитический крекинг метанола на цеолитах включает три стадии: 1) дегидратация метанола в диметиловый эфир, 2) дегидратация диметилового эфира в смесь низших алкенов (этилен, пропилен и др. ) и 3) превращение этих алкенов в смесь ароматических углеводородов и алканов. Превращение метанола в моторное топливо уже реализовано на промышленной основе в Новой Зеландии и Австралии, богатых природным газом, но не имеющих собственных источников нефти. Несомненно, что превращение метанола в бензин имеет большое будущее, и дальнейшее развитие этого метода в значительной степени будет определяться соотношением цен на нефть, газ и уголь на мировом рынке.

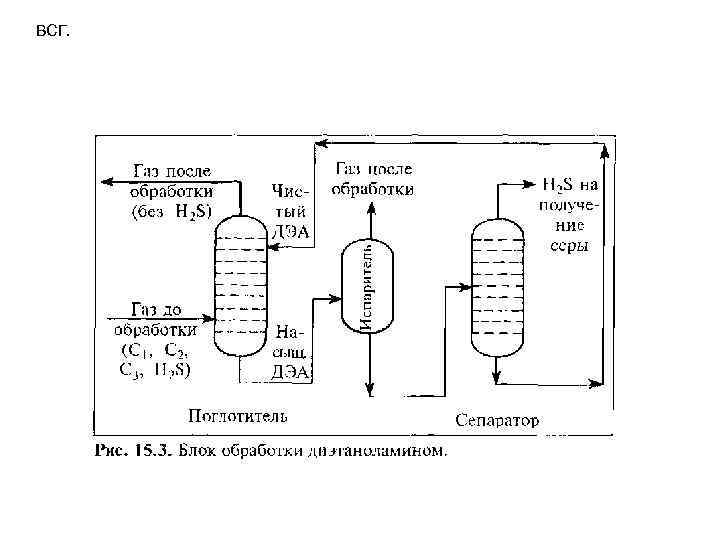
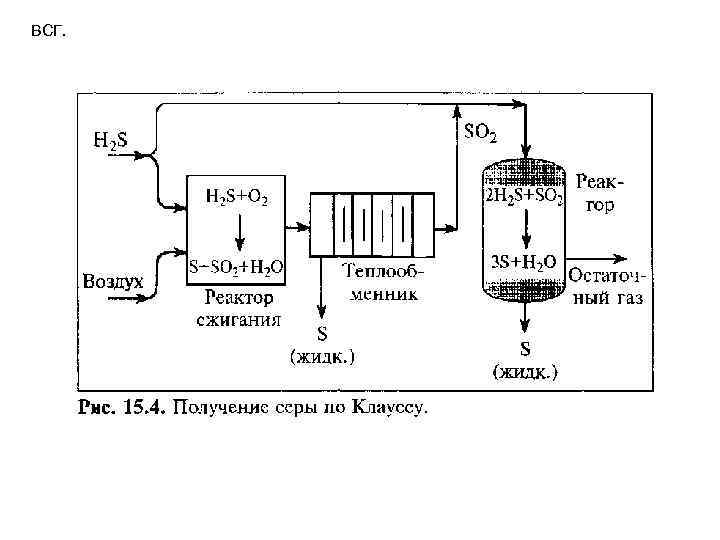
15. 2. Производство серы Сероводород, выделяемый из технологических газов термогидрокаталитических процессов нефтепереработки, обычнло перерабатывают на НПЗ в элементную серу. Самый распространенный промышленный способ получения серы из технологических и природных газов процесс Клауса, осуществляемый в две стадии. ХИМИЯ ПРОЦЕССА И УПРАВЛЕНИЕ 1) Термическая стадия высокотемпературное сжигание сероводорода в топочной части реактора при подаче стехиометрического количества воздуха. В ходе реакций H 2 S + 3/2*02 -> S 02 + Н 20 + Q; 2*H 2 S + S 02 -> 3/2*S 2 + 2*Н 20 + Q выделяется значительное количество теплоты, которое необходимо утилизировать перед второй стадией процесса, и расходуется до 70% сероводорода. 2) Каталитическая стадия, проводимая на активном оксиде алюминия при 200 300°С в две ступени, позволяет довести конверсию сероводорода до 95%: 2*H 2 S + S 02 ->3/6*S 6 + 2*H 20; 2*H 2 S + S 02 -> 3/8*S 8 + 2*H 20 Кроме оксида алюминия, бокситов в качестве катализатора используют диоксид титана. В ходе процесса Клауса образуются три модификации серы – S 2, S 6 и S 8. Жидкая сера представлена в основном модификацией S 8. На эффективность процесса Клауса влияют: 1) состав кислого газа, 2) температура процесса, 3) давление, 4) время контакта, 5)эффективность катализаторов и 6) работа конденсаторов серы.
ВСГ.

15. 2. 1. Технологическая схема процесса Клауса При концентрации сероводорода в кислом газе выше 50% (об. ) используют прямоточный процесс Клауса пламенный способ. По этому способу весь кислый газ подается на сжигание в печь реактор термической ступени установки Клауса, выполненную в одном корпусе с котлом утилизатором. В топке печи реактора температура достигает 1100 1300°С, и выход серы – 70 75%. Дальнейшее превращение сероводорода в серу осуществляется в две три ступени на катализаторах при температуре 220 260°С. После каждой ступени пары образовавшейся серы конденсируются в поверхностных конденсаторах. Теплота, выделяющаяся при горении сероводорода и конденсации паров серы, используется для получения пара среднего и низкого давления. Выход серы в этом процессе достигает 96 97%. Установка прямоточного процесса Клауса состоит из двух ступеней получения серы термической и каталитической (Рис. 15. 1). Кислый газ сжигается в печи реакторе 5, причем кислород воздуха подается в топку в количестве, необходимом для протекания окисления сероводорода до серы. На термической ступени установок Клауса применяют цилиндрические реакторы, состоящие из топочной камеры и трубчатого теплообменника. В торцевой части топочной камеры расположены горелочные устройства. Основная часть сероводородного газа и воздуха обычно подается по тангенциальным каналам. В зоне смешения горение происходит в закрученном потоке. Проходя решетку из расположенного в шахматном порядке огнеупорного кирпича, продукты сгорания поступают в основной топочный объем также цилиндрической формы, но большего диаметра.

Оптимальная температура, способствующая максимальной степени конверсии на термической ступени - 1100 -1300°С. На каталитической ступени имеет место обратная зависимость степени конверсии от температуры: конверсия повышается с понижением температуры; нижний температурный предел ограничен точкой росы серы (188°С). На практике с целью исключения конденсации серы в порах катализатора температуру каталитической ступени процесса поддерживают на уровне 210 -220°С. На каждой из вышеперечисленных ступеней процесса влияние давления другое: на термической снижение давления повышает степень конверсии сероводорода в серу, а на каталитической наоборот. На современных установках давление поддерживают на уровне 0, 12 -0, 17 МПа. Повышение времени контакта увеличивает выход серы на обеих ступенях процесса. Эффективно работающие конденсаторы коагуляторы снижают потери серы с хвостовыми газами, что способствует росту конверсии. Активность катализатора, его устойчивость к сульфатации и способность ускорять реакции гидролиза COS и CS 2 также определяют эффективность процесса. На установках используют альфа и гамма Аl 203 со средним сроком службы 4 года.
ВСГ.
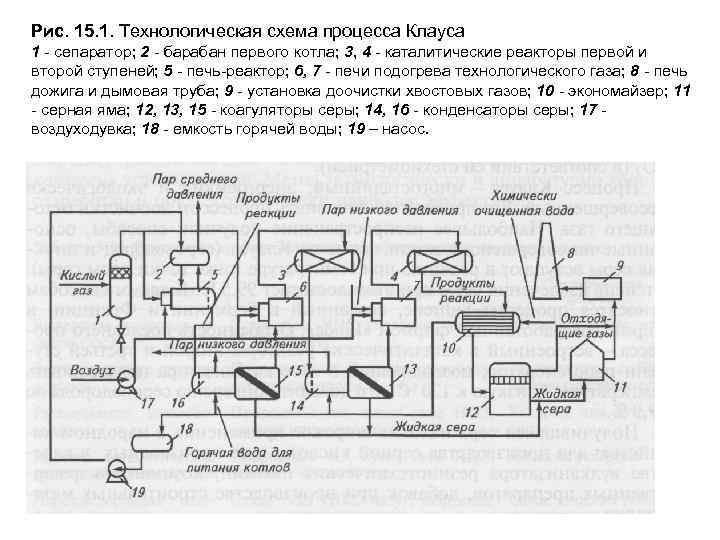
Рис. 15. 1. Технологическая схема процесса Клауса 1 сепаратор; 2 барабан первого котла; 3, 4 каталитические реакторы первой и второй ступеней; 5 печь реактор; 6, 7 печи подогрева технологического газа; 8 печь дожига и дымовая труба; 9 установка доочистки хвостовых газов; 10 экономайзер; 11 серная яма; 12, 13, 15 коагуляторы серы; 14, 16 конденсаторы серы; 17 воздуходувка; 18 емкость горячей воды; 19 – насос.

Затем продукты сгорания охлаждаются водой, проходя по трубному пространству трубчатого теплообменника, и поступают в конденсатор, откуда полученная в термической ступени сера выводится в хранилище. Технологический газ после термической ступени, содержащий непрореагировавший сероводород, сернистый ангидрид, образовавшийся одновременно с серой при пламенном сжигании сероводорода, а также сульфидоксид углерода и сероуглерод (продукты побочных реакций, протекающих в реакторе), вновь подогревается в подогревателе до 220 300°С и поступает на каталитическую ступень. В слое катализатора происходит основная реакция: 2*H 2 S + S 02 = 3/n. Sn + 2 Н 20 Каталитических ступеней бывает обычно две или три. На выход серы большое влияние оказывает число ступеней конверсии, способ подогрева газов перед ступенями и соотношение компонентов H 2 S и S 02 (в соответствии со стехиометрией). Процесс Клауса - многостадийный, энергоемкий и экологически несовершенный. Его приходится дополнять процессом доочистки отходящего газа. Наибольшее распространение получили способы, основанные на совершенствовании процесса Клауса (сероводород и диоксид серы вступают в реакцию при температуре ниже точки росы серы). Степень извлечения серы при этом достигает 99, 5%. К таким способам относятся процессы Sulfrene, созданный в Германии и Франции, и Clipsulf, разработанный фирмой «Linde» . Особенность последнего процесса встроенный в каталитические реакторы второй и третьей ступени парогенератор, позволяющий в слое катализатора поддерживать температуру, близкую к 120°С, что доводит конверсию сероводорода до 99, 9%.

Сера процесса Клауса находит широкое применение в народном хозяйстве: 1) для производства серной кислоты и ее производных, 2) в качестве вулканизатора резинотехнических изделий, 3) компонента лекарственных препаратов, 4) добавок при производстве строительных материалов. Следует отметить, что процесс получения серы больше экологический процесс (цена на серу значительно меньше цены любого нефтепродукта), с учетом цен на транспорт сбыт для производителя не приносит доходов, как правило, имеют место только убытки и трудности.
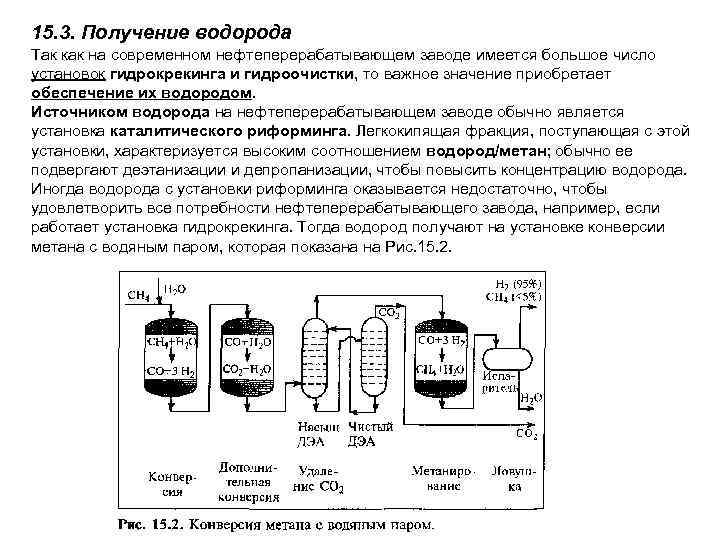
15. 3. Получение водорода Так как на современном нефтеперерабатывающем заводе имеется большое число установок гидрокрекинга и гидроочистки, то важное значение приобретает обеспечение их водородом. Источником водорода на нефтеперерабатывающем заводе обычно является установка каталитического риформинга. Легкокипящая фракция, поступающая с этой установки, характеризуется высоким соотношением водород/метан; обычно ее подвергают деэтанизации и депропанизации, чтобы повысить концентрацию водорода. Иногда водорода с установки риформинга оказывается недостаточно, чтобы удовлетворить все потребности нефтеперерабатывающего завода, например, если работает установка гидрокрекинга. Тогда водород получают на установке конверсии метана с водяным паром, которая показана на Рис. 15. 2.

Этот процесс осуществляется в четыре стадии (каталитические). 1. Конверсия. Метан и водяной пар (Н 2 О) смешивают и пропускают над Ni катализатором при 800°С, в результате чего образуется монооксид углерода и водород. СН 4 + Н 2 О -> СО + 3 Н 2 2. Дополнительная конверсия. Не удовлетворившись водородом, который уже образовался, его дополнительно получают и из монооксида углерода. К смеси прибавляют дополнительное количество водяного пара и пропускают над другим катализатором при 340°С. В результате образуется диоксид углерода и водород. 3. Разделение газов. Чтобы получить поток с высоким содержанием водорода, его отделяют от диоксида углерода с помощью процесса жидкостной экстракции диэтаноламином (ДЭА). 4. Метанирование. Поскольку присутствие даже небольших количеств оксидов углерода в потоке водорода может оказаться вредным, на следующей стадии процесса эти примеси превращаются в метан. Процесс идет на катализаторе при 420°С. СО + 3 Н 2 -> СН 4 + Н 2 О СО 2 + 4 Н 2 -> СН 4 + 2 Н 2 О В некоторых случаях в распоряжении не оказывается метана, не содержащего серы. В этом случае вместо метана можно использовать более тяжелые углеводороды, например пропан или нафту. Такой процесс требует другого оборудования и других катализаторов. Кроме того, он менее энергетически эффективен, но все же работает.

сбыт
Лекция-15_pres.ppt