Лекция 1 Основные понятия и определения тд.ppt
- Количество слайдов: 24
 ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА И ТЕПЛОТЕХНИКА ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ
ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА И ТЕПЛОТЕХНИКА ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ
 ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ Термодинамика – наука изучающая законы превращения энергии и особенности этих превращений. l Изучает закономерности преобразования энергии в различных процессах, сопровождающихся тепловыми явлениями, а также свойства тел, участвующих в этих преобразованиях. l Термодинамика базируется на двух основных, опытных законах (началах), которые являются обобщением закономерностей, существующих в природе. l
ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ Термодинамика – наука изучающая законы превращения энергии и особенности этих превращений. l Изучает закономерности преобразования энергии в различных процессах, сопровождающихся тепловыми явлениями, а также свойства тел, участвующих в этих преобразованиях. l Термодинамика базируется на двух основных, опытных законах (началах), которые являются обобщением закономерностей, существующих в природе. l
 Основные законы термодинамики Первое начало термодинамики устанавливает количественные отношения в процессах взаимного преобразования теплоты и работы и является частным случаем всеобщего закона сохранения и превращения энергии. l Второе начало термодинамики характеризует направление естественных (необратимых) процессов и отмечает качественное отличие теплоты от других форм передачи энергии. l
Основные законы термодинамики Первое начало термодинамики устанавливает количественные отношения в процессах взаимного преобразования теплоты и работы и является частным случаем всеобщего закона сохранения и превращения энергии. l Второе начало термодинамики характеризует направление естественных (необратимых) процессов и отмечает качественное отличие теплоты от других форм передачи энергии. l
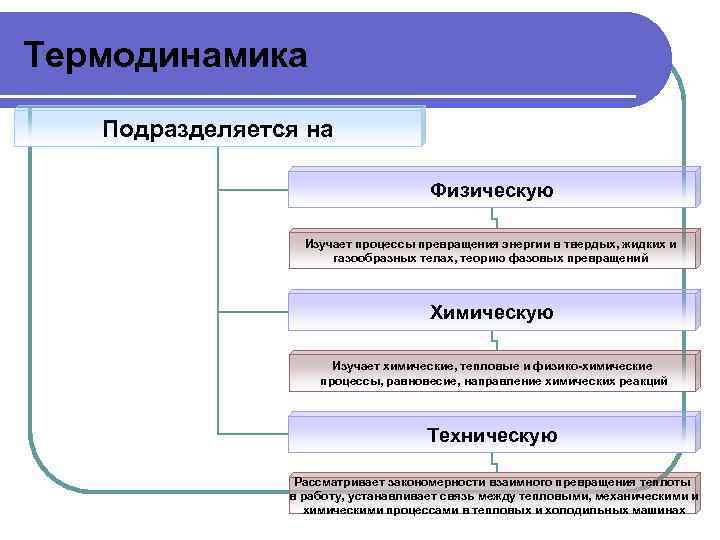 Термодинамика Подразделяется на Физическую Изучает процессы превращения энергии в твердых, жидких и газообразных телах, теорию фазовых превращений Химическую Изучает химические, тепловые и физико-химические процессы, равновесие, направление химических реакций Техническую Рассматривает закономерности взаимного превращения теплоты в работу, устанавливает связь между тепловыми, механическими и химическими процессами в тепловых и холодильных машинах
Термодинамика Подразделяется на Физическую Изучает процессы превращения энергии в твердых, жидких и газообразных телах, теорию фазовых превращений Химическую Изучает химические, тепловые и физико-химические процессы, равновесие, направление химических реакций Техническую Рассматривает закономерности взаимного превращения теплоты в работу, устанавливает связь между тепловыми, механическими и химическими процессами в тепловых и холодильных машинах
 Термодинамика Техническая термодинамика изучает процессы взаимного превращения теплоты и работы, а также свойства рабочих тел, с помощью которых происходя эти преобразования. l Наука, которая изучает методы получения, преобразования, передачи и использования теплоты, а также принципы действия и конструктивные особенности тепло- и парогенераторов, тепловых и холодильных машин, аппаратов и устройств, называется теплотехникой. l
Термодинамика Техническая термодинамика изучает процессы взаимного превращения теплоты и работы, а также свойства рабочих тел, с помощью которых происходя эти преобразования. l Наука, которая изучает методы получения, преобразования, передачи и использования теплоты, а также принципы действия и конструктивные особенности тепло- и парогенераторов, тепловых и холодильных машин, аппаратов и устройств, называется теплотехникой. l
 Основные задачи термодинамики l Разработка теории течения и истечения паров и газов l Исследование термодинамических свойств паров, жидкостей, твердых тел l Изучение уравнений состояния вещества, фазового равновесия, фазовых превращений и др.
Основные задачи термодинамики l Разработка теории течения и истечения паров и газов l Исследование термодинамических свойств паров, жидкостей, твердых тел l Изучение уравнений состояния вещества, фазового равновесия, фазовых превращений и др.
 Параметры состояния l Величины, которые характеризуют состояние любого вещества или тела называются параметрами состояния а) масса , кг - мера инертности; б) плотность - масса вещества в единице объема: или удельный объем
Параметры состояния l Величины, которые характеризуют состояние любого вещества или тела называются параметрами состояния а) масса , кг - мера инертности; б) плотность - масса вещества в единице объема: или удельный объем
![Параметры состояния в) давление [Па = Н/м 2], [к. Па], [МПа]: Различают: - абсолютное Параметры состояния в) давление [Па = Н/м 2], [к. Па], [МПа]: Различают: - абсолютное](https://present5.com/presentation/23623665_64910193/image-8.jpg) Параметры состояния в) давление [Па = Н/м 2], [к. Па], [МПа]: Различают: - абсолютное давление - Ра - барометрическое (атмосферное) давление - Рб; - вакуумметрическое давление (Ра < Pб) - Рв ; - избыточное (Ра > Pб) - Риз.
Параметры состояния в) давление [Па = Н/м 2], [к. Па], [МПа]: Различают: - абсолютное давление - Ра - барометрическое (атмосферное) давление - Рб; - вакуумметрическое давление (Ра < Pб) - Рв ; - избыточное (Ра > Pб) - Риз.
 Параметры состояния г) температура – степень нагретости тела, мера интенсивности движения молекул, определяет направление теплообмена - шкала Цельсия (предложил в 1742 году шведский астроном Андерс Цельсий) - термодинамическая шкала Кельвина - Т, К (предложил в 1848 году английский ученый Уильям Томсон (он же лорд Кельвин) t =T-273, 15 (о. С) Т = t + 273, 15 (К) 1 о С= 1 К
Параметры состояния г) температура – степень нагретости тела, мера интенсивности движения молекул, определяет направление теплообмена - шкала Цельсия (предложил в 1742 году шведский астроном Андерс Цельсий) - термодинамическая шкала Кельвина - Т, К (предложил в 1848 году английский ученый Уильям Томсон (он же лорд Кельвин) t =T-273, 15 (о. С) Т = t + 273, 15 (К) 1 о С= 1 К
 Температура l - Шкала Фаренгейта (предложена зимой 1709 года немецким учёным Габриэлем Фаренгейтом) точка замерзания воды на уровне моря оказалась равной +32º (в один холодный день), а точка кипения воды +212º. Шкала популярна в США и Великобритании. о. С=5/9(о. F-32) Шкала Реомюра ( предложил в 1731 году французский учёный Рене де Реомюр) - температурная шкала, основанна на использовании спирта, обладающего свойством расширяться. - за нижнюю реперную точку была принята точка замерзания воды. При нормальных условиях точка кипения воды по этой шкале составляет 80º. Шкала Реомюра ныне повсеместно вышла из употребления. о. С=5/4 о. R l
Температура l - Шкала Фаренгейта (предложена зимой 1709 года немецким учёным Габриэлем Фаренгейтом) точка замерзания воды на уровне моря оказалась равной +32º (в один холодный день), а точка кипения воды +212º. Шкала популярна в США и Великобритании. о. С=5/9(о. F-32) Шкала Реомюра ( предложил в 1731 году французский учёный Рене де Реомюр) - температурная шкала, основанна на использовании спирта, обладающего свойством расширяться. - за нижнюю реперную точку была принята точка замерзания воды. При нормальных условиях точка кипения воды по этой шкале составляет 80º. Шкала Реомюра ныне повсеместно вышла из употребления. о. С=5/4 о. R l
 Температура l - Шкала Ранкина (Ренкина)(предложена шотландским инженером и физиком Уильямом Ранкином) ноль совпадает с нулём термодинамической температуры размер 1ºRa равен 5/9 К. по размерности шкала Ранкина совпадает не со шкалой Цельсия, а со шкалой Фаренгейта. Данная система измерения температуры распространения не получила. о. С=5/9 Ra
Температура l - Шкала Ранкина (Ренкина)(предложена шотландским инженером и физиком Уильямом Ранкином) ноль совпадает с нулём термодинамической температуры размер 1ºRa равен 5/9 К. по размерности шкала Ранкина совпадает не со шкалой Цельсия, а со шкалой Фаренгейта. Данная система измерения температуры распространения не получила. о. С=5/9 Ra
 Термодинамическая система l Совокупность тел, находящихся в механическом и тепловом взаимодействии или равновесии называется термодинамической системой Различают: - открытую систему – существует обмен между веществом и энергией; - закрытую систему - нет обмена веществом; - изолированную систему - нет обмена ни веществом, ни энергией; - адиабатную систему (теплоизолированную) - нет обмена энергией; - гомогенную систему - когда вещества, составляющую систему, состоят в одинаковом агрегатном состоянии; - гетерогенную систему - когда вещества, составляющую систему, имеют различное агрегатное состояние.
Термодинамическая система l Совокупность тел, находящихся в механическом и тепловом взаимодействии или равновесии называется термодинамической системой Различают: - открытую систему – существует обмен между веществом и энергией; - закрытую систему - нет обмена веществом; - изолированную систему - нет обмена ни веществом, ни энергией; - адиабатную систему (теплоизолированную) - нет обмена энергией; - гомогенную систему - когда вещества, составляющую систему, состоят в одинаковом агрегатном состоянии; - гетерогенную систему - когда вещества, составляющую систему, имеют различное агрегатное состояние.
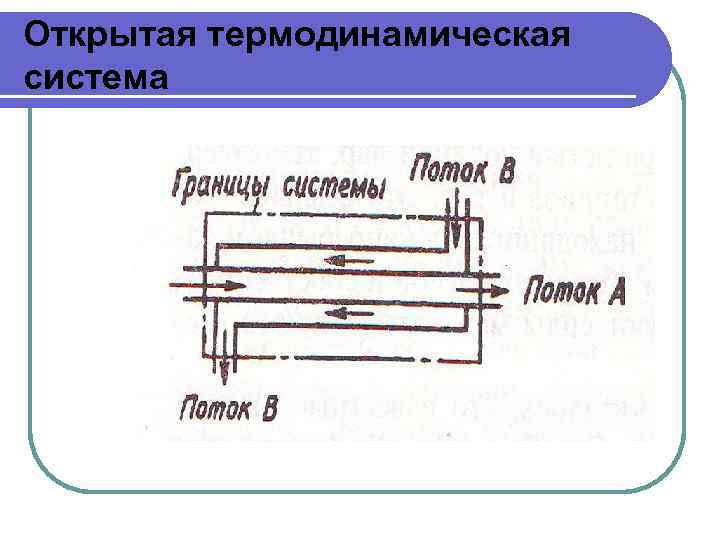 Открытая термодинамическая система
Открытая термодинамическая система
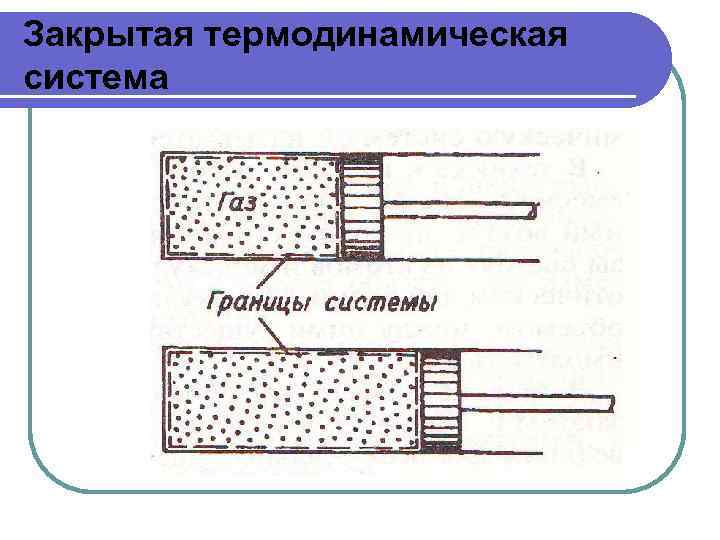 Закрытая термодинамическая система
Закрытая термодинамическая система
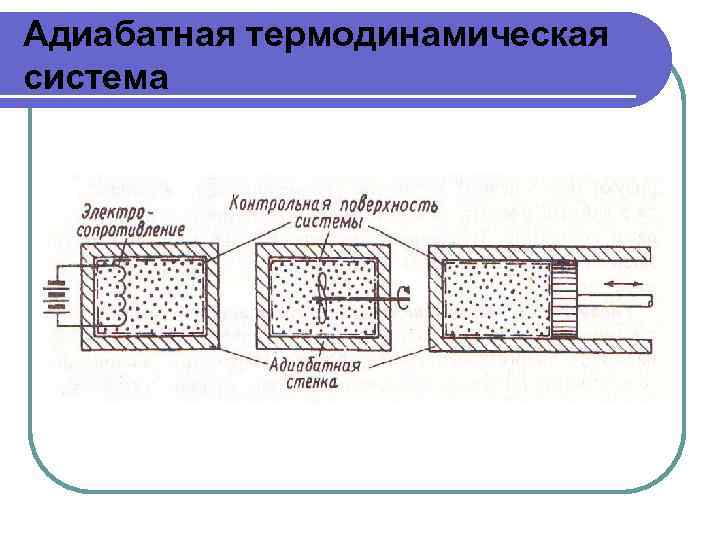 Адиабатная термодинамическая система
Адиабатная термодинамическая система
 Рабочее тело Тело, с помощью которого происходит взаимное превращение тепла и работы называется рабочим телом l Рабочее тело обладает - интенсивными свойствами, не зависящими от массы (давление, температура, удельная теплоемкость) - экстенсивными свойствами, зависящие от массы вещества. l Примеры рабочего тела: в гидроэлектростанциях – вода, в ТЭЦ – водяной пар, в ДВС – продукты сгорания. l
Рабочее тело Тело, с помощью которого происходит взаимное превращение тепла и работы называется рабочим телом l Рабочее тело обладает - интенсивными свойствами, не зависящими от массы (давление, температура, удельная теплоемкость) - экстенсивными свойствами, зависящие от массы вещества. l Примеры рабочего тела: в гидроэлектростанциях – вода, в ТЭЦ – водяной пар, в ДВС – продукты сгорания. l
 Термодинамический процесс - есть изменение состояния системы, возникающее под влиянием внешних воздействий l Бывают равновесные и неравновесные термодинамические процессы. Равновесный процесс – непрерывная последовательность равновесных состояний системы, все части системы имеют одинаковые параметры (p, v, T) в данный момент времени. Неравновесный процесс – непрерывная последовательность равновесных состояний системы когда в данный момент времени все части системы имеют различные параметры (p, v, T). l
Термодинамический процесс - есть изменение состояния системы, возникающее под влиянием внешних воздействий l Бывают равновесные и неравновесные термодинамические процессы. Равновесный процесс – непрерывная последовательность равновесных состояний системы, все части системы имеют одинаковые параметры (p, v, T) в данный момент времени. Неравновесный процесс – непрерывная последовательность равновесных состояний системы когда в данный момент времени все части системы имеют различные параметры (p, v, T). l
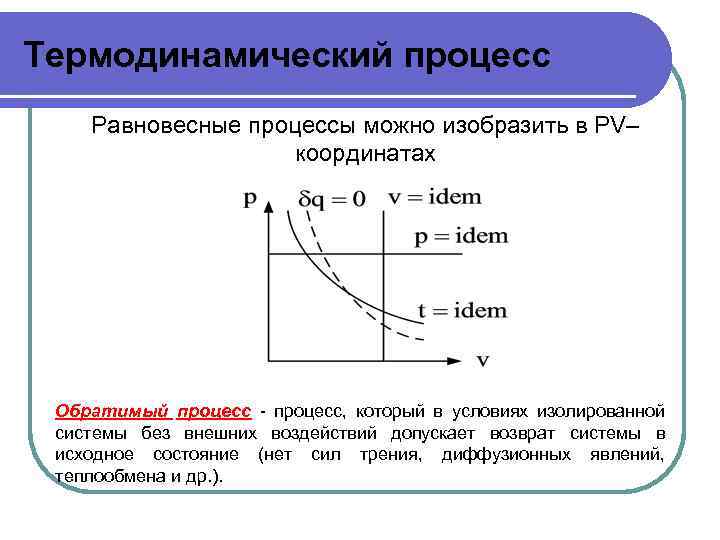 Термодинамический процесс Равновесные процессы можно изобразить в РV– координатах Обратимый процесс - процесс, который в условиях изолированной системы без внешних воздействий допускает возврат системы в исходное состояние (нет сил трения, диффузионных явлений, теплообмена и др. ).
Термодинамический процесс Равновесные процессы можно изобразить в РV– координатах Обратимый процесс - процесс, который в условиях изолированной системы без внешних воздействий допускает возврат системы в исходное состояние (нет сил трения, диффузионных явлений, теплообмена и др. ).
 Внутренняя энергия l Внутренняя энергия - представляет собой полный запас энергии тела и состоит из: а) энергии поступательного и вращательного движения молекул; б) энергии внутримолекулярных колебаний; в) потенциальной энергии сил сцепления между молекулами; г) внутримолекулярной, внутриатомной и внутриядерной энергий. l Полная внутренняя энергия является функцией состояния - U [Дж] l Удельная внутренняя энергия:
Внутренняя энергия l Внутренняя энергия - представляет собой полный запас энергии тела и состоит из: а) энергии поступательного и вращательного движения молекул; б) энергии внутримолекулярных колебаний; в) потенциальной энергии сил сцепления между молекулами; г) внутримолекулярной, внутриатомной и внутриядерной энергий. l Полная внутренняя энергия является функцией состояния - U [Дж] l Удельная внутренняя энергия:
 Теплота l Теплота - это энергия, передаваемая более нагретым l Удельная теплота: телом менее нагретому, не связанная с переносом вещества и совершением работы. l Полное количество теплоты: Формы передачи теплоты: - теплопроводность - Уравнение Фурье где λ - коэффициент теплопроводности; - конвекция (теплоотдача) - уравнение Ньютона – Рихмана - излучение (лучистый теплообмен) - закон Стефана-Больцмана
Теплота l Теплота - это энергия, передаваемая более нагретым l Удельная теплота: телом менее нагретому, не связанная с переносом вещества и совершением работы. l Полное количество теплоты: Формы передачи теплоты: - теплопроводность - Уравнение Фурье где λ - коэффициент теплопроводности; - конвекция (теплоотдача) - уравнение Ньютона – Рихмана - излучение (лучистый теплообмен) - закон Стефана-Больцмана
 Работа l Термодинамическая работа - работа по изменению объема системы l Полная термодинамическая работа: l Удельная термодинамическая работа:
Работа l Термодинамическая работа - работа по изменению объема системы l Полная термодинамическая работа: l Удельная термодинамическая работа:
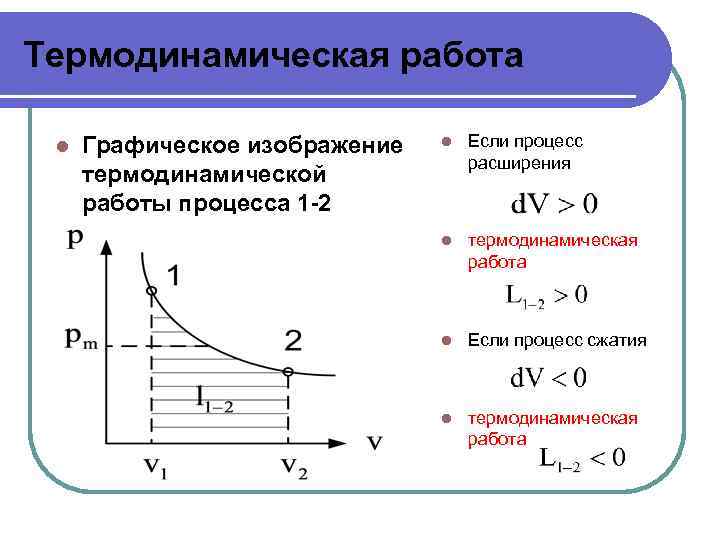 Термодинамическая работа l Графическое изображение термодинамической работы процесса 1 -2 l Если процесс расширения l термодинамическая работа l Если процесс сжатия l термодинамическая работа
Термодинамическая работа l Графическое изображение термодинамической работы процесса 1 -2 l Если процесс расширения l термодинамическая работа l Если процесс сжатия l термодинамическая работа
 Работа Потенциальная работа - работа по обратимому перемещению паров, газов, жидкостей из области одного давления в область другого. l Полная потенциальная работа: l l Удельная потенциальная работа:
Работа Потенциальная работа - работа по обратимому перемещению паров, газов, жидкостей из области одного давления в область другого. l Полная потенциальная работа: l l Удельная потенциальная работа:
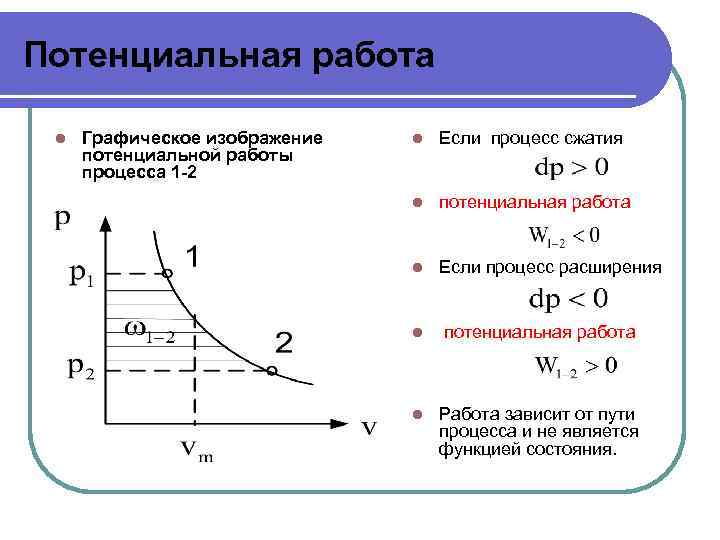 Потенциальная работа l Графическое изображение потенциальной работы процесса 1 -2 l Если процесс сжатия l потенциальная работа l Если процесс расширения l потенциальная работа l Работа зависит от пути процесса и не является функцией состояния.
Потенциальная работа l Графическое изображение потенциальной работы процесса 1 -2 l Если процесс сжатия l потенциальная работа l Если процесс расширения l потенциальная работа l Работа зависит от пути процесса и не является функцией состояния.


