Лекция 1 ТД часть 1 (2).ppt
- Количество слайдов: 44
 Техническая термодинамика часть 1 Доцент кафедры ТСУ и ТД ЗЛОБИН Владимир Германович
Техническая термодинамика часть 1 Доцент кафедры ТСУ и ТД ЗЛОБИН Владимир Германович
 Рекомендованная литература: 1. Техническая термодинамика и теплотехника: учебное пособие для вузов/ 2. 3. 4. 5. 6. 7. 8. 9. под ред. проф. А. А. Захаровой. – 2 -е изд. испр. -М: Издат. центр «Академия» , 2008. -272 с. Техническая термодинамика. Кирилин В. А. , Сычев В. В. , Шейдулин А. Е. Учебник для вузов. 5 -е изд. , перераб. и доп. –М: ИД МЭИ, 2008. -496 с. Основы теории тепловых процессов и машин. Учебное пособие для вузов. Доп. МО РФ ч. 1/ под ред. Н. И. Прокопенко. -3 -е изд. испр. – М: БИНОМ. Лаборатория знаний, 2009. – 560 с. Основы теории тепловых процессов и машин. Учебное пособие для вузов. Доп. МО РФ ч. 2/ под ред. Н. И. Прокопенко. -3 -е изд. испр. – М: БИНОМ. Лаборатория знаний, 2009. – 571 с. Техническая термодинамика и теплотехника. Учебное пособие для вузов/ под ред. проф. А. А. Захаровой. –М: Издат. центр «Академия» , 2006. -272 с. Расчет процесса истечения идеального газа и водяного пара. Французов В. И. , Гладышев Н. Н. , Короткова Т. Ю. , Часовских О. Н. , Рудаков С. Н. Ротапринт. СПб. : ГТУ РП, 2001. Лекции по термодинамике Лоренц Г. А. . Ижевск. : НИЦ «Регулярная и хаотическая динамика» , 2001. -176 с. Расчет политропного процесса изменения состояния смеси идеальных газов. Французов В. И. , Гладышев Н. Н. , Часовских О. Н. , Рудаков С. Н. Ротапринт. СПб. : ГТУ РП, 1999. Определение отношения теплоемкостей воздуха Ср/Сv. Злобин В. Г. , Горбай С. В. , Короткова Т. Ю. , Алиев Э. Р. Методические указания к лабораторным работам по курсу «Техническая термодинамика» для студентов дневного и вечернего отделения. СПб. : ГОУВПО СПб. ГТУРП, 2010, -14 с.
Рекомендованная литература: 1. Техническая термодинамика и теплотехника: учебное пособие для вузов/ 2. 3. 4. 5. 6. 7. 8. 9. под ред. проф. А. А. Захаровой. – 2 -е изд. испр. -М: Издат. центр «Академия» , 2008. -272 с. Техническая термодинамика. Кирилин В. А. , Сычев В. В. , Шейдулин А. Е. Учебник для вузов. 5 -е изд. , перераб. и доп. –М: ИД МЭИ, 2008. -496 с. Основы теории тепловых процессов и машин. Учебное пособие для вузов. Доп. МО РФ ч. 1/ под ред. Н. И. Прокопенко. -3 -е изд. испр. – М: БИНОМ. Лаборатория знаний, 2009. – 560 с. Основы теории тепловых процессов и машин. Учебное пособие для вузов. Доп. МО РФ ч. 2/ под ред. Н. И. Прокопенко. -3 -е изд. испр. – М: БИНОМ. Лаборатория знаний, 2009. – 571 с. Техническая термодинамика и теплотехника. Учебное пособие для вузов/ под ред. проф. А. А. Захаровой. –М: Издат. центр «Академия» , 2006. -272 с. Расчет процесса истечения идеального газа и водяного пара. Французов В. И. , Гладышев Н. Н. , Короткова Т. Ю. , Часовских О. Н. , Рудаков С. Н. Ротапринт. СПб. : ГТУ РП, 2001. Лекции по термодинамике Лоренц Г. А. . Ижевск. : НИЦ «Регулярная и хаотическая динамика» , 2001. -176 с. Расчет политропного процесса изменения состояния смеси идеальных газов. Французов В. И. , Гладышев Н. Н. , Часовских О. Н. , Рудаков С. Н. Ротапринт. СПб. : ГТУ РП, 1999. Определение отношения теплоемкостей воздуха Ср/Сv. Злобин В. Г. , Горбай С. В. , Короткова Т. Ю. , Алиев Э. Р. Методические указания к лабораторным работам по курсу «Техническая термодинамика» для студентов дневного и вечернего отделения. СПб. : ГОУВПО СПб. ГТУРП, 2010, -14 с.
 Лекция 1. Основные понятия и определения. Предмет и метод технической термодинамики 1. Введение. Международная система 2. 3. 4. единиц (СИ) Основные термодинамические параметры состояния Термодинамическая система и термодинамический процесс Теплота и работа. Термодинамическое равновесие
Лекция 1. Основные понятия и определения. Предмет и метод технической термодинамики 1. Введение. Международная система 2. 3. 4. единиц (СИ) Основные термодинамические параметры состояния Термодинамическая система и термодинамический процесс Теплота и работа. Термодинамическое равновесие
 1. Введение • Термодинамика — наука о превращениях различных видов энергии друг в друга.
1. Введение • Термодинамика — наука о превращениях различных видов энергии друг в друга.
 Термодинамика 1) рассматривает закономерности взаимного превращения теплоты в работу; Общая 2) устанавливает. Химическая взаимосвязь между Техническая (физическая) тепловыми, механическими и химическими процессами, которые процессы превращения на основе законов совершаются общей в тепловых и холодильных энергии в твердых, жидких и газообразных телах, термодинамики машинах; излучение различных тел, изучает химические, магнитные и электрические явления, а также устанавливающую математические зависимости между термодинамическими величинами тепловые, физикохимические процессы, равновесие и влияние на равновесие внешних условий 3) 3) изучает процессы, происходящие в газах и парах, а также свойства этих тел при различных физических условиях
Термодинамика 1) рассматривает закономерности взаимного превращения теплоты в работу; Общая 2) устанавливает. Химическая взаимосвязь между Техническая (физическая) тепловыми, механическими и химическими процессами, которые процессы превращения на основе законов совершаются общей в тепловых и холодильных энергии в твердых, жидких и газообразных телах, термодинамики машинах; излучение различных тел, изучает химические, магнитные и электрические явления, а также устанавливающую математические зависимости между термодинамическими величинами тепловые, физикохимические процессы, равновесие и влияние на равновесие внешних условий 3) 3) изучает процессы, происходящие в газах и парах, а также свойства этих тел при различных физических условиях
 Основные законы термодинамики • Первое начало термодинамики — закон • превращения и сохранения энергии Второе начало термодинамики устанавливает условия протекания и направленность макроскопических процессов в системах, состоящих из большого количества частиц • Третье начало термодинамики (тепловая теорема Нернста). Позволяет определить свойства тел при очень низких температурах
Основные законы термодинамики • Первое начало термодинамики — закон • превращения и сохранения энергии Второе начало термодинамики устанавливает условия протекания и направленность макроскопических процессов в системах, состоящих из большого количества частиц • Третье начало термодинамики (тепловая теорема Нернста). Позволяет определить свойства тел при очень низких температурах
 • В теоретической части техническая термодинамика является общим отделом науки об энергии • в прикладной части представляет собой теоретический фундамент всей теплотехники, изучающей процессы, протекающие в тепловых двигателях.
• В теоретической части техническая термодинамика является общим отделом науки об энергии • в прикладной части представляет собой теоретический фундамент всей теплотехники, изучающей процессы, протекающие в тепловых двигателях.
 Методы исследования в термодинамике • Метод круговых процессов (циклов) • Метод термодинамических функций и геометрических построений (метод Гиббса)
Методы исследования в термодинамике • Метод круговых процессов (циклов) • Метод термодинамических функций и геометрических построений (метод Гиббса)
 МЕЖДУНАРОДНАЯ СИСТЕМА ЕДИНИЦ (СИ) • единица длины — метр (м); • единица массы — килограмм (кг); • единица времени — секунда (с); • температура термодинамическая — кельвин (К); • количество вещества — моль (моль).
МЕЖДУНАРОДНАЯ СИСТЕМА ЕДИНИЦ (СИ) • единица длины — метр (м); • единица массы — килограмм (кг); • единица времени — секунда (с); • температура термодинамическая — кельвин (К); • количество вещества — моль (моль).
 • Единица количества энергии (в том числе • теплоты и работы) - Джоуль (Дж) - равный работе постоянной силы в 1 Н на пути в 1 м при совпадении направлений силы и перемещения точки приложения силы (1 Дж = 1 Н· 1 м = 1 кг·м 2/с2). Единица мощности - Ватт (Вт) соответствует работе 1 Дж в 1 с (Дж/с)
• Единица количества энергии (в том числе • теплоты и работы) - Джоуль (Дж) - равный работе постоянной силы в 1 Н на пути в 1 м при совпадении направлений силы и перемещения точки приложения силы (1 Дж = 1 Н· 1 м = 1 кг·м 2/с2). Единица мощности - Ватт (Вт) соответствует работе 1 Дж в 1 с (Дж/с)
 Вывод по 1 -ому вопросу: • Техническая термодинамика, применяя основные законы к процессам превращения теплоты в механическую работу и механической работы в теплоту, дает возможность : 1) разрабатывать теорию тепловых двигателей; 2) исследовать процессы, протекающие в тепловых двигателях; 3) выявлять экономичность процессов для каждого типа тепловых двигателей.
Вывод по 1 -ому вопросу: • Техническая термодинамика, применяя основные законы к процессам превращения теплоты в механическую работу и механической работы в теплоту, дает возможность : 1) разрабатывать теорию тепловых двигателей; 2) исследовать процессы, протекающие в тепловых двигателях; 3) выявлять экономичность процессов для каждого типа тепловых двигателей.
 2. Основные термодинамические параметры состояния Предметом технической термодинамики является – изучение процессов взаимного преобразования теплоты и работы в различных тепловых машинах
2. Основные термодинамические параметры состояния Предметом технической термодинамики является – изучение процессов взаимного преобразования теплоты и работы в различных тепловых машинах
 • Физическое состояние тела определяется некоторыми величинами, характеризующими данное состояние, которые в термодинамике называют параметрами состояния Параметрами состояния могут быть целый ряд величин: удельный объем; абсолютное давление; абсолютная температура; внутренняя энергия; энтальпия; энтропия; концентрация; изохорноизотёрмный потенциал и др.
• Физическое состояние тела определяется некоторыми величинами, характеризующими данное состояние, которые в термодинамике называют параметрами состояния Параметрами состояния могут быть целый ряд величин: удельный объем; абсолютное давление; абсолютная температура; внутренняя энергия; энтальпия; энтропия; концентрация; изохорноизотёрмный потенциал и др.
 Состояние однородного тела может быть однозначно определено тремя параметрами: • удельный объем; • абсолютная температура; • давление. Основные параметры не являются независимыми величинами
Состояние однородного тела может быть однозначно определено тремя параметрами: • удельный объем; • абсолютная температура; • давление. Основные параметры не являются независимыми величинами
 Удельный объем однородного вещества: обозначается v, а единица удельного объема — кубический метр на килограмм (м 3/кг)]: (1. 1)
Удельный объем однородного вещества: обозначается v, а единица удельного объема — кубический метр на килограмм (м 3/кг)]: (1. 1)
![Плотность вещества: [единица плотности — килограмм на кубический метр (кг/м 3)]: (1. 2) Плотность вещества: [единица плотности — килограмм на кубический метр (кг/м 3)]: (1. 2)](https://present5.com/presentation/5636354_26376847/image-16.jpg) Плотность вещества: [единица плотности — килограмм на кубический метр (кг/м 3)]: (1. 2)
Плотность вещества: [единица плотности — килограмм на кубический метр (кг/м 3)]: (1. 2)
 Давление: Давление с точки зрения молекулярнокинетической теории : (1. 3)
Давление: Давление с точки зрения молекулярнокинетической теории : (1. 3)
 Единицей давления в СИ является паскаль — давление, вызываемое силой в 1 Н, равномерно распределенной по поверхности площадью в 1 м 2, обозначается Па (1 Па = 1 Н/м 2). В практических расчетах используют килопаскали [103 ×Па] (к. Па), мегапаскали [106 ×Па] (МПа); часто давление выражают во внесистемных единицах — барах (1 бар = 105 Па).
Единицей давления в СИ является паскаль — давление, вызываемое силой в 1 Н, равномерно распределенной по поверхности площадью в 1 м 2, обозначается Па (1 Па = 1 Н/м 2). В практических расчетах используют килопаскали [103 ×Па] (к. Па), мегапаскали [106 ×Па] (МПа); часто давление выражают во внесистемных единицах — барах (1 бар = 105 Па).
 Высота столба жидкости h прямо пропорциональна разности давлений в сосуде и наружной среды и обратно пропорциональна плотности жидкости мм рт. ст. м
Высота столба жидкости h прямо пропорциональна разности давлений в сосуде и наружной среды и обратно пропорциональна плотности жидкости мм рт. ст. м
 Давление измеряют: • Атмосферное – барометрами – р0 • Выше атмосферного (избыточное) – манометрами - ри • Ниже атмосферного (разрежение) – вакууметрами - рв
Давление измеряют: • Атмосферное – барометрами – р0 • Выше атмосферного (избыточное) – манометрами - ри • Ниже атмосферного (разрежение) – вакууметрами - рв
 Абсолютным давлением (ра) называют давление, отсчитываемое от абсолютного нуля давления или от Избыточное давление и абсолютного вакуума. разрежение не являются При определении абсолютного давления параметрами состояния, так как различают два случая: они при одном и том же 1) когда давление в сосуде больше абсолютном давлении могут атмосферного: (1. 4) принимать различные значения в 2) когда оно меньше величины зависимости от атмосферного давления (1. 5)
Абсолютным давлением (ра) называют давление, отсчитываемое от абсолютного нуля давления или от Избыточное давление и абсолютного вакуума. разрежение не являются При определении абсолютного давления параметрами состояния, так как различают два случая: они при одном и том же 1) когда давление в сосуде больше абсолютном давлении могут атмосферного: (1. 4) принимать различные значения в 2) когда оно меньше величины зависимости от атмосферного давления (1. 5)
 Температура, характеризуя степень нагретости тел, представляет собой меру средней кинетической энергии поступательного движения его молекул (1. 6) k — постоянная Больцмана, равная 1, 38· 10 -23 Дж/К
Температура, характеризуя степень нагретости тел, представляет собой меру средней кинетической энергии поступательного движения его молекул (1. 6) k — постоянная Больцмана, равная 1, 38· 10 -23 Дж/К
 Абсолютная температура • Абсолютная температура всегда величина положительная. При температуре абсолютного нуля (Т = 0) прекращается тепловое движение молекул ( ). Эта предельная минимальная температура и является началом для отсчета абсолютных температур.
Абсолютная температура • Абсолютная температура всегда величина положительная. При температуре абсолютного нуля (Т = 0) прекращается тепловое движение молекул ( ). Эта предельная минимальная температура и является началом для отсчета абсолютных температур.
 Температура измеряется: • расширение тел от нагревания в жидкостных термометрах; • изменение объема при постоянном давлении или • • • изменение давления при постоянном объеме в газовых термометрах; изменение электрического сопротивления проводника при нагревании в термометрах сопротивления; изменение электродвижущей силы в цепи термопары при нагревании или охлаждении ее спая. При измерении высоких температур оптическими пирометрами используются законы излучения твердых тел и методы сравнения раскаленной нити с исследуемым материалом.
Температура измеряется: • расширение тел от нагревания в жидкостных термометрах; • изменение объема при постоянном давлении или • • • изменение давления при постоянном объеме в газовых термометрах; изменение электрического сопротивления проводника при нагревании в термометрах сопротивления; изменение электродвижущей силы в цепи термопары при нагревании или охлаждении ее спая. При измерении высоких температур оптическими пирометрами используются законы излучения твердых тел и методы сравнения раскаленной нити с исследуемым материалом.
 Температурные шкалы: 1) термодинамическая температурная шкала, основанная на втором законе термодинамики; 2) международной практической температурной шкалы, которая является практическим осуществлением термодинамической температурной шкалы, полученной с помощью реперных (опорных) точек и интерполяционных уравнений
Температурные шкалы: 1) термодинамическая температурная шкала, основанная на втором законе термодинамики; 2) международной практической температурной шкалы, которая является практическим осуществлением термодинамической температурной шкалы, полученной с помощью реперных (опорных) точек и интерполяционных уравнений
 Тройная точка воды: • Точка, где жидкая, газообразная и твердая фазы находятся в устойчивом равновесии - температура 273, 16 К или 0, 01 °С Параметром состояния является абсолютная температура, выражаемая в Кельвинах. Градус абсолютной шкалы численно равен градусу шкалы Цельсия, так что
Тройная точка воды: • Точка, где жидкая, газообразная и твердая фазы находятся в устойчивом равновесии - температура 273, 16 К или 0, 01 °С Параметром состояния является абсолютная температура, выражаемая в Кельвинах. Градус абсолютной шкалы численно равен градусу шкалы Цельсия, так что
 3. Термодинамическая система и термодинамический процесс Термодинамической системой называется совокупность макроскопических тел, обменивающихся энергией как друг с другом, так и с окружающей (внешней) средой. Если термодинамическая система не имеет никаких взаимодействий с окружающей средой, то ее называют изолированной (или замкнутой) системой.
3. Термодинамическая система и термодинамический процесс Термодинамической системой называется совокупность макроскопических тел, обменивающихся энергией как друг с другом, так и с окружающей (внешней) средой. Если термодинамическая система не имеет никаких взаимодействий с окружающей средой, то ее называют изолированной (или замкнутой) системой.
 Система, окруженная так называемой адиабатной оболочкой, исключающей теплообмен с окружающей средой, называется теплоизолированной (или адиабатной) системой. Система, имеющая во всех своих частях одинаковый состав и физические свойства, называется физически однородной. Однородная термодинамическая система (как по составу, так и по физическому строению), внутри которой нет поверхностей раздела, называется гомогенной (например, лед, вода, газы).
Система, окруженная так называемой адиабатной оболочкой, исключающей теплообмен с окружающей средой, называется теплоизолированной (или адиабатной) системой. Система, имеющая во всех своих частях одинаковый состав и физические свойства, называется физически однородной. Однородная термодинамическая система (как по составу, так и по физическому строению), внутри которой нет поверхностей раздела, называется гомогенной (например, лед, вода, газы).
 Система, состоящая из нескольких макроскопических частей с различными физическими свойствами, отделенных одна от другой видимыми поверхностями раздела, называется гетерогенной (например, лед и вода, вода и пар и др. ). Гомогенные части системы, отделенные от остальных частей видимыми поверхностями раздела, называются фазами. Компонентом термодинамической системы называют всякую химически однородную систему.
Система, состоящая из нескольких макроскопических частей с различными физическими свойствами, отделенных одна от другой видимыми поверхностями раздела, называется гетерогенной (например, лед и вода, вода и пар и др. ). Гомогенные части системы, отделенные от остальных частей видимыми поверхностями раздела, называются фазами. Компонентом термодинамической системы называют всякую химически однородную систему.
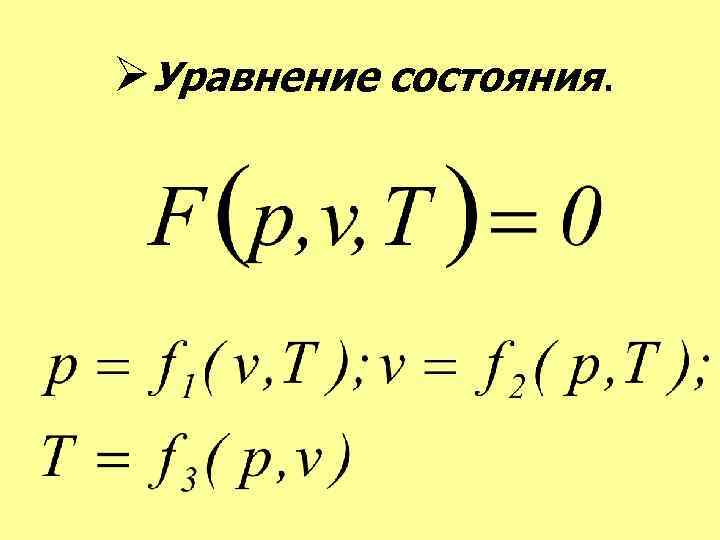 ØУравнение состояния.
ØУравнение состояния.
 • Термодинамический процесс Совокупность изменений состояния термодинамической системы при переходе из одного равновесного состояния в другое называют термодинамическим процессом. • Равновесное состояние тела Под равновесным состоянием тела понимают такое, при котором во всех точках его объема давление, температура, удельный объем и все другие физические свойства одинаковы. • Если процесс проходит через равновесные состояния, то его называют равновесным.
• Термодинамический процесс Совокупность изменений состояния термодинамической системы при переходе из одного равновесного состояния в другое называют термодинамическим процессом. • Равновесное состояние тела Под равновесным состоянием тела понимают такое, при котором во всех точках его объема давление, температура, удельный объем и все другие физические свойства одинаковы. • Если процесс проходит через равновесные состояния, то его называют равновесным.
 • С математической точки зрения уравнение состояния в трехосной системе координат р, v и Т выражает некоторую поверхность, которая называется термодинамической поверхностью.
• С математической точки зрения уравнение состояния в трехосной системе координат р, v и Т выражает некоторую поверхность, которая называется термодинамической поверхностью.
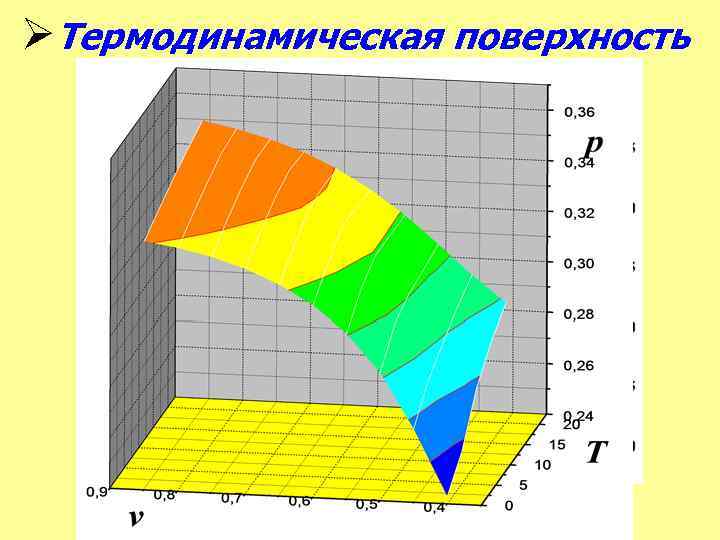 ØТермодинамическая поверхность
ØТермодинамическая поверхность
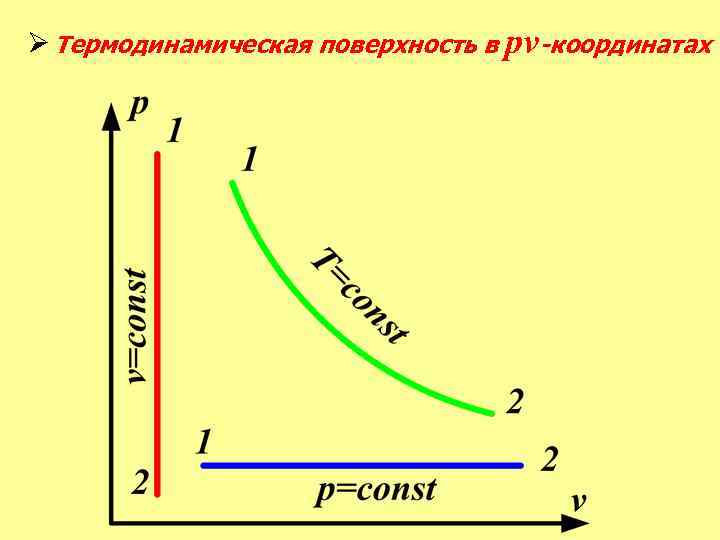 Ø Термодинамическая поверхность в pv-координатах
Ø Термодинамическая поверхность в pv-координатах
 Замкнутые (или круговые) процессы – при которых система, проходя через ряд последовательных состояний, возвращается к начальному состоянию Круговой процесс называют циклом Интенсивные параметры Аддитивные (или экстенсивные) параметры
Замкнутые (или круговые) процессы – при которых система, проходя через ряд последовательных состояний, возвращается к начальному состоянию Круговой процесс называют циклом Интенсивные параметры Аддитивные (или экстенсивные) параметры
 4. Теплота и работа. Термодинамическое равновесие • Мерой движения материи является энергия • Передача энергии в процессе от одного тела к другому может происходить двумя способами
4. Теплота и работа. Термодинамическое равновесие • Мерой движения материи является энергия • Передача энергии в процессе от одного тела к другому может происходить двумя способами
 Первый способ передачи энергии • при непосредственном контакте тел, • • имеющих различную температуру путем обмена кинетической энергией между молекулами или лучистым переносом внутренней энергии. Количество энергии – количество теплоты; Способ - передача энергии в виде теплоты; Подведенная (сообщенная) теплота; Отведенная (отнятая) теплота
Первый способ передачи энергии • при непосредственном контакте тел, • • имеющих различную температуру путем обмена кинетической энергией между молекулами или лучистым переносом внутренней энергии. Количество энергии – количество теплоты; Способ - передача энергии в виде теплоты; Подведенная (сообщенная) теплота; Отведенная (отнятая) теплота
 • Теплота, так же как и любая энергия, выражается в джоулях (Дж) или килоджоулях (к. Дж). • Подведенная теплота считается положительной, отведенная — отрицательной. • Произвольное количество теплоты Q, а удельное (отнесенное к 1 кг) — q.
• Теплота, так же как и любая энергия, выражается в джоулях (Дж) или килоджоулях (к. Дж). • Подведенная теплота считается положительной, отведенная — отрицательной. • Произвольное количество теплоты Q, а удельное (отнесенное к 1 кг) — q.
 Второй способ передачи энергии • тело должно либо передвигаться в силовом поле, либо изменять свой объем под действием внешнего давления. Иначе говоря, передача энергии в этом случае происходит при условии перемещения всего тела или его части в пространстве.
Второй способ передачи энергии • тело должно либо передвигаться в силовом поле, либо изменять свой объем под действием внешнего давления. Иначе говоря, передача энергии в этом случае происходит при условии перемещения всего тела или его части в пространстве.
 • Способ - передача энергии в форме работы; • Количество энергии - работа; • Совершенная над телом работа; • Затраченная телом работа • Работа также выражается в джоулях (Дж) или килоджоулях (к. Дж). Затраченная телом работа считается положительной, а совершенная над телом работа — отрицательной. • Произвольное количество энергии, переданное в форме работы - L, а удельное — l.
• Способ - передача энергии в форме работы; • Количество энергии - работа; • Совершенная над телом работа; • Затраченная телом работа • Работа также выражается в джоулях (Дж) или килоджоулях (к. Дж). Затраченная телом работа считается положительной, а совершенная над телом работа — отрицательной. • Произвольное количество энергии, переданное в форме работы - L, а удельное — l.
 • В общем случае передача энергии в форме теплоты и в форме работы может происходить одновременно. • При этом важно отметить, что в различных термодинамических процессах в зависимости от условий их протекания количество теплоты и работа различны.
• В общем случае передача энергии в форме теплоты и в форме работы может происходить одновременно. • При этом важно отметить, что в различных термодинамических процессах в зависимости от условий их протекания количество теплоты и работа различны.
 • Теплота и работа характеризуют качественно и количественно две различные формы передачи движения от одних тел материального мира к другим. • Работа представляет собой макрофизическую форму передачи • энергии, а теплота есть совокупность микрофизических процессов, поскольку передача энергии этим способом происходит на молекулярном уровне без видимого движения тел Количество теплоты, полученное телом, и работа, произведенная телом, зависят от условий перехода тела из начального в конечное состояние, т. е. зависят от характера процесса.
• Теплота и работа характеризуют качественно и количественно две различные формы передачи движения от одних тел материального мира к другим. • Работа представляет собой макрофизическую форму передачи • энергии, а теплота есть совокупность микрофизических процессов, поскольку передача энергии этим способом происходит на молекулярном уровне без видимого движения тел Количество теплоты, полученное телом, и работа, произведенная телом, зависят от условий перехода тела из начального в конечное состояние, т. е. зависят от характера процесса.
 Теплота и работа представляют собой два единственно возможных способа передачи энергии от одного тела к другому.
Теплота и работа представляют собой два единственно возможных способа передачи энергии от одного тела к другому.
 ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ • истечении некоторого времени (рано или Если состояние всех тел, входящих в По термодинамическую систему, длительное время системе наступит состояние поздно) в не изменяется, то говорят, что система находится в термодинамическом устойчивого термодинамического равновесия равновесии. • При термодинамической равновесии передача С изменением внешних условий окружающей среды будет теплоты от одних тел системы к другим изменяться и состояние системы, и это изменение и механическое перемещение отдельных частей наблюдается до тех пор, пока не наступит равенство системы относительно друга давлений и температур е. имеет место тепловое ит. е. отсутствуют, т. окружающей среды и системы, не наступит устойчивое равновесие. . механическое равновесие • Без внешнего влияния (самопроизвольно) выйти из состояния равновесия система не может.
ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ • истечении некоторого времени (рано или Если состояние всех тел, входящих в По термодинамическую систему, длительное время системе наступит состояние поздно) в не изменяется, то говорят, что система находится в термодинамическом устойчивого термодинамического равновесия равновесии. • При термодинамической равновесии передача С изменением внешних условий окружающей среды будет теплоты от одних тел системы к другим изменяться и состояние системы, и это изменение и механическое перемещение отдельных частей наблюдается до тех пор, пока не наступит равенство системы относительно друга давлений и температур е. имеет место тепловое ит. е. отсутствуют, т. окружающей среды и системы, не наступит устойчивое равновесие. . механическое равновесие • Без внешнего влияния (самопроизвольно) выйти из состояния равновесия система не может.


