Подготовка.ppt
- Количество слайдов: 22
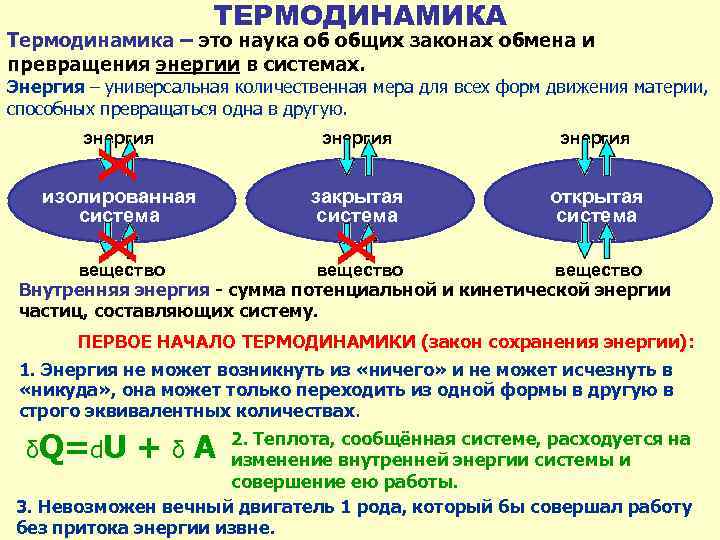
ТЕРМОДИНАМИКА Термодинамика – это наука об общих законах обмена и превращения энергии в системах. Энергия – универсальная количественная мера для всех форм движения материи, способных превращаться одна в другую. энергия изолированная система закрытая система открытая система х х х энергия вещество Внутренняя энергия - сумма потенциальной и кинетической энергии частиц, составляющих систему. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ (закон сохранения энергии): 1. Энергия не может возникнуть из «ничего» и не может исчезнуть в «никуда» , она может только переходить из одной формы в другую в строго эквивалентных количествах. δQ=d. U + δ A 2. Теплота, сообщённая системе, расходуется на изменение внутренней энергии системы и совершение ею работы. 3. Невозможен вечный двигатель 1 рода, который бы совершал работу без притока энергии извне.
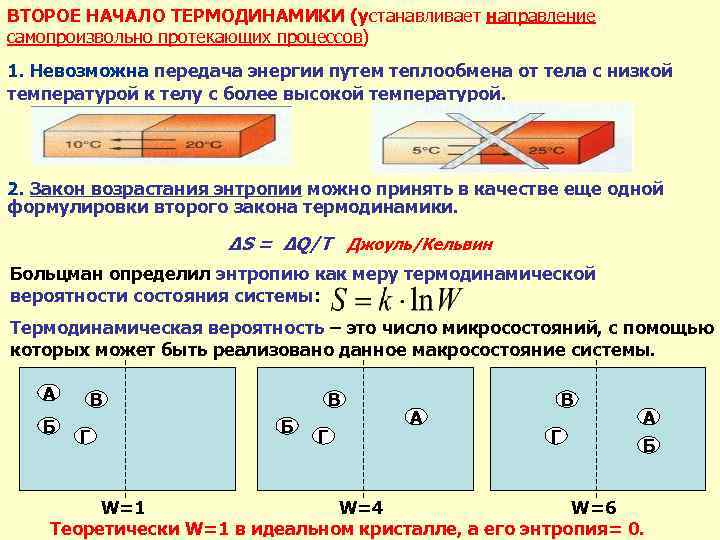
ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ (устанавливает направление самопроизвольно протекающих процессов) 1. Невозможна передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой. 2. Закон возрастания энтропии можно принять в качестве еще одной формулировки второго закона термодинамики. ΔS = ΔQ/T Джоуль/Кельвин Больцман определил энтропию как меру термодинамической вероятности состояния системы: Термодинамическая вероятность – это число микросостояний, с помощью которых может быть реализовано данное макросостояние системы. А Б В В Г Б Г А В Г А Б W=1 W=4 W=6 Теоретически W=1 в идеальном кристалле, а его энтропия= 0.

Любая система стремится в равновесное состояние, но живые организмы находятся в стационарных состояниях. Общее между состояниями – устойчивость во времени. В стационарном состоянии: 1. осуществляются различные термодинамические процессы 2. существуют градиенты В равновесном состоянии 1. отсутствуют градиенты физических величин 2. прекращаются все термодинамические процессы 3. энтропия максимальна 4. термодинамические потенциалы минимальны 3. энтропия имеет определённое, но не максимальное значение 4. термодинамические потенциалы поддерживаются на постоянном, но не минимальном уровне Уравнение Пригожина d. S = d. Se + d. Sі Si - всегда положителен, а член d. Se отрицателен, сумма d. S может иметь любой знак. В стационарном состоянии d. S = 0, т. е. d нарастание энтропии уравновешено её удалением. Теорема Пригожина

Клетка получает энергию, в основном, при окислении глюкозы и жирных кислот. Этот процесс проходит в митохондриях. (принцип Гесса – в результате многоэтапного процесса выделяется столько же энергии, сколько бы выделилось, если бы реакция шла в одну стадию). Полимеры до Освобождает 1 этап Полностью мономеров до 1% энергии рассеивается (гидролитический, в (углеводы до сахаров, жиры до глицерина и жирных кислот, веществ ЖКТ и лизосомах) белки до аминокислот) 2 этап Освобождает до Из них Образование (бескислородный, в 30% энергии рассеивается ацетилцитозоле) веществ 56% коэнзима А Из них 3 этап До 70% рассеивается Углекислый (кислородный, в энергии до 34% газ и вода митохондриях) энергии БИОЛОГИЧЕСКАЯ РАБОТА (в покое): Первично –рассеянное тепло Часть энергии окисления запасается в форме АТФ - аденозинтрифосфорной кислоты (АТФ). – универсального (не единственного) источника энергии для всех видов биологической работы. - 2 АТФ 36 АТФ 1. Электрохимическая работа - поддержание градиентов на мембранах клеток и органоидов (до 30% энерготрат в покое). 2. Сердечная деятельность, дыхание, перистальтика кишечника, анаболизм, терморегуляция и т. д. Поскольку в любом процессе не может быть гидролизовано меньше 1 молекулы АТФ, то неиспользованная часть её энергии всегда превращается в теплоту (вторично-рассеянную).
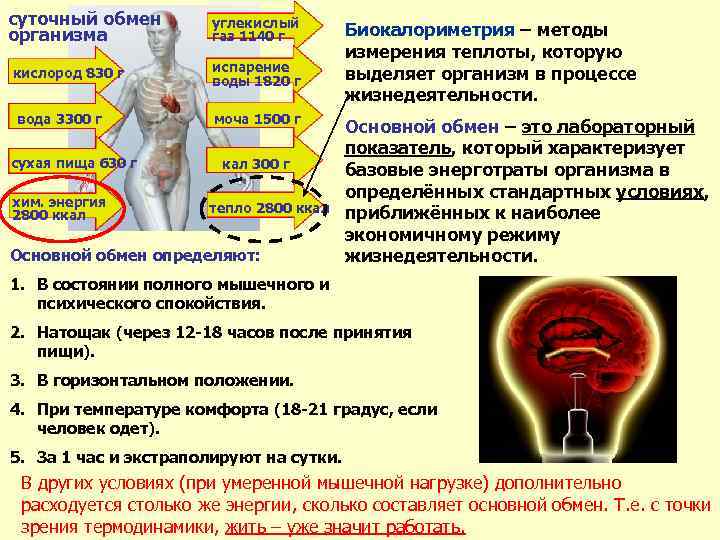
суточный обмен организма кислород 830 г вода 3300 г сухая пища 630 г хим. энергия 2800 ккал углекислый газ 1140 г испарение воды 1820 г моча 1500 г кал 300 г тепло 2800 ккал Основной обмен определяют: Биокалориметрия – методы измерения теплоты, которую выделяет организм в процессе жизнедеятельности. Основной обмен – это лабораторный показатель, который характеризует базовые энерготраты организма в определённых стандартных условиях, приближённых к наиболее экономичному режиму жизнедеятельности. 1. В состоянии полного мышечного и психического спокойствия. 2. Натощак (через 12 -18 часов после принятия пищи). 3. В горизонтальном положении. 4. При температуре комфорта (18 -21 градус, если человек одет). 5. За 1 час и экстраполируют на сутки. В других условиях (при умеренной мышечной нагрузке) дополнительно расходуется столько же энергии, сколько составляет основной обмен. Т. е. с точки зрения термодинамики, жить – уже значит работать.
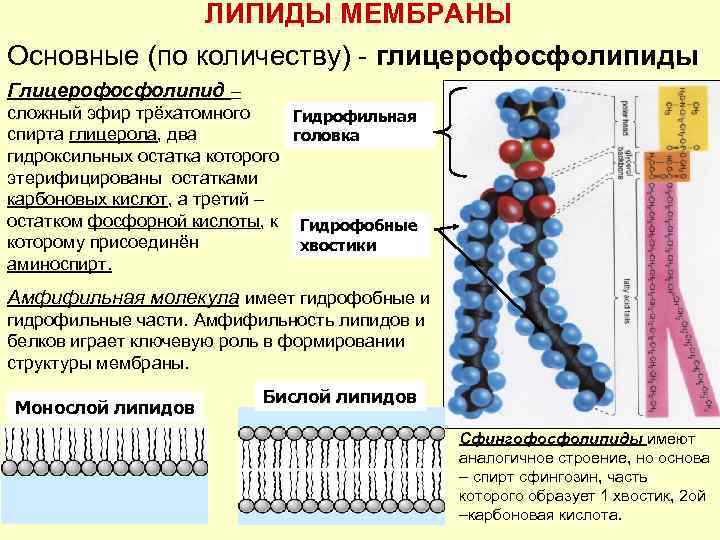
ЛИПИДЫ МЕМБРАНЫ Основные (по количеству) - глицерофосфолипиды Глицерофосфолипид – сложный эфир трёхатомного Гидрофильная спирта глицерола, два головка гидроксильных остатка которого этерифицированы остатками карбоновых кислот, а третий – остатком фосфорной кислоты, к Гидрофобные которому присоединён хвостики аминоспирт. Амфифильная молекула имеет гидрофобные и гидрофильные части. Амфифильность липидов и белков играет ключевую роль в формировании структуры мембраны. Монослой липидов Бислой липидов Сфингофосфолипиды имеют аналогичное строение, но основа – спирт сфингозин, часть которого образует 1 хвостик, 2 ой –карбоновая кислота.
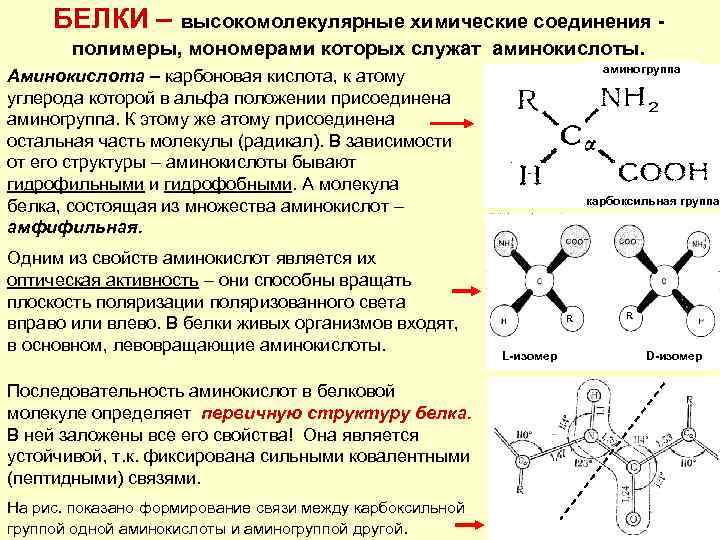
БЕЛКИ – высокомолекулярные химические соединения полимеры, мономерами которых служат аминокислоты. аминогруппа Аминокислота – карбоновая кислота, к атому углерода которой в альфа положении присоединена аминогруппа. К этому же атому присоединена остальная часть молекулы (радикал). В зависимости от его структуры – аминокислоты бывают гидрофильными и гидрофобными. А молекула белка, состоящая из множества аминокислот – амфифильная. Одним из свойств аминокислот является их оптическая активность – они способны вращать плоскость поляризации поляризованного света вправо или влево. В белки живых организмов входят, в основном, левовращающие аминокислоты. Последовательность аминокислот в белковой молекуле определяет первичную структуру белка. В ней заложены все его свойства! Она является устойчивой, т. к. фиксирована сильными ковалентными (пептидными) связями. На рис. показано формирование связи между карбоксильной группой одной аминокислоты и аминогруппой другой. карбоксильная группа R L-изомер R D-изомер
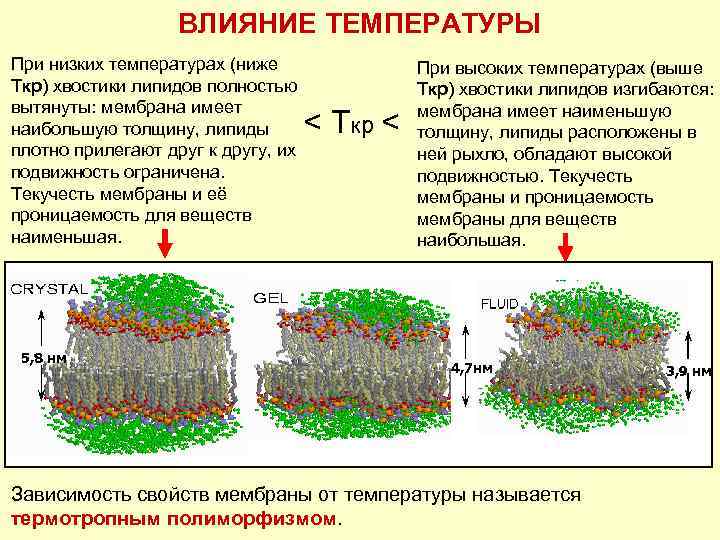
ВЛИЯНИЕ ТЕМПЕРАТУРЫ При низких температурах (ниже Ткр) хвостики липидов полностью вытянуты: мембрана имеет наибольшую толщину, липиды плотно прилегают друг к другу, их подвижность ограничена. Текучесть мембраны и её проницаемость для веществ наименьшая. 5, 8 нм < Ткр < При высоких температурах (выше Ткр) хвостики липидов изгибаются: мембрана имеет наименьшую толщину, липиды расположены в ней рыхло, обладают высокой подвижностью. Текучесть мембраны и проницаемость мембраны для веществ наибольшая. 4, 7 нм Зависимость свойств мембраны от температуры называется термотропным полиморфизмом. 3, 9 нм
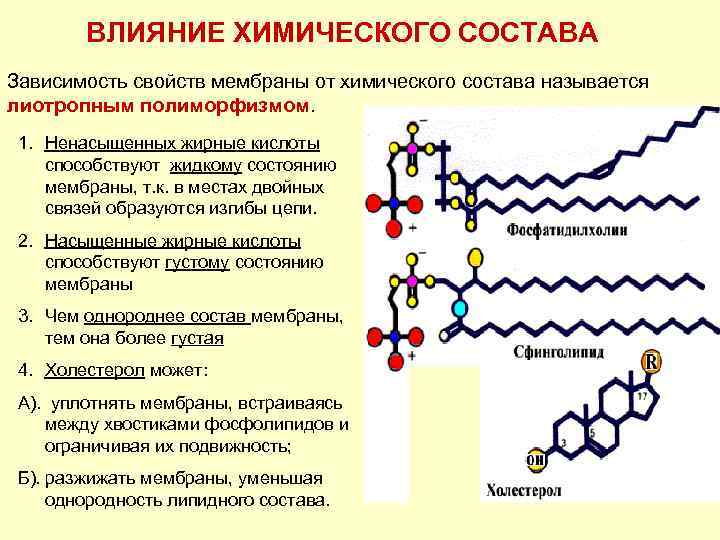
ВЛИЯНИЕ ХИМИЧЕСКОГО СОСТАВА Зависимость свойств мембраны от химического состава называется лиотропным полиморфизмом. 1. Ненасыщенных жирные кислоты способствуют жидкому состоянию мембраны, т. к. в местах двойных связей образуются изгибы цепи. 2. Насыщенные жирные кислоты способствуют густому состоянию мембраны 3. Чем однороднее состав мембраны, тем она более густая 4. Холестерол может: А). уплотнять мембраны, встраиваясь между хвостиками фосфолипидов и ограничивая их подвижность; Б). разжижать мембраны, уменьшая однородность липидного состава.
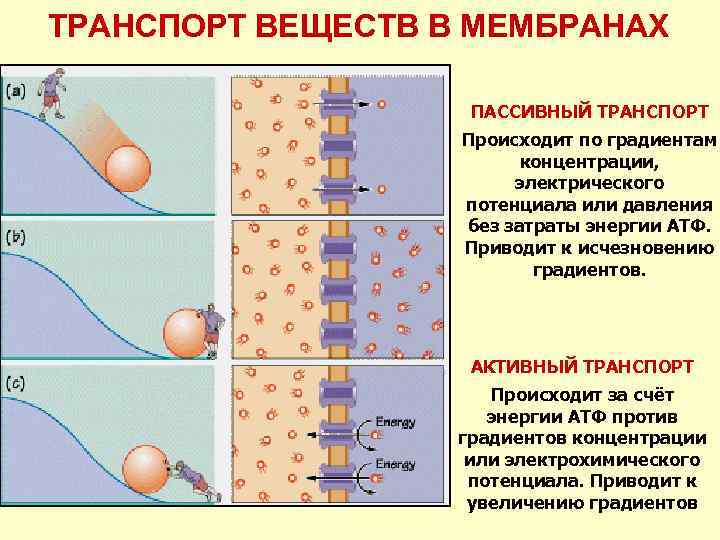
ТРАНСПОРТ ВЕЩЕСТВ В МЕМБРАНАХ ПАССИВНЫЙ ТРАНСПОРТ Происходит по градиентам концентрации, электрического потенциала или давления без затраты энергии АТФ. Приводит к исчезновению градиентов. АКТИВНЫЙ ТРАНСПОРТ Происходит за счёт энергии АТФ против градиентов концентрации или электрохимического потенциала. Приводит к увеличению градиентов
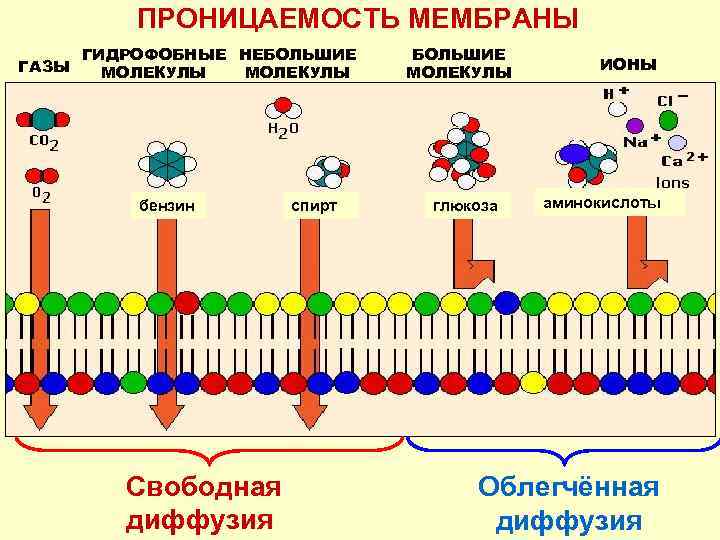
ПРОНИЦАЕМОСТЬ МЕМБРАНЫ ГАЗЫ ГИДРОФОБНЫЕ НЕБОЛЬШИЕ МОЛЕКУЛЫ бензин Свободная диффузия спирт БОЛЬШИЕ МОЛЕКУЛЫ глюкоза ИОНЫ аминокислоты Облегчённая диффузия

СВОБОДНАЯ ДИФФУЗИЯ Плотность потока вещества (I) – число молей (dn) вещества переносимого через единицу поверхности (S) за единицу времени (dt): Уравнение Фика показывает, что плотность потока диффундирующего вещества пропорциональна градиенту концентрации: Уравнение Фика, если на пути диффундирующего вещества находится мембрана, в связи с её неодинаковой проницаемостью для различных веществ приобретает вид: где Р- проницаемость мембраны коэффициент диффузии проницаемость мембраны коэффициент распределения вещества, показывающий его растворимость в липидах толщина мембраны для вещества, С 2 и С 1 – концентрации вещества внутри и снаружи клетки
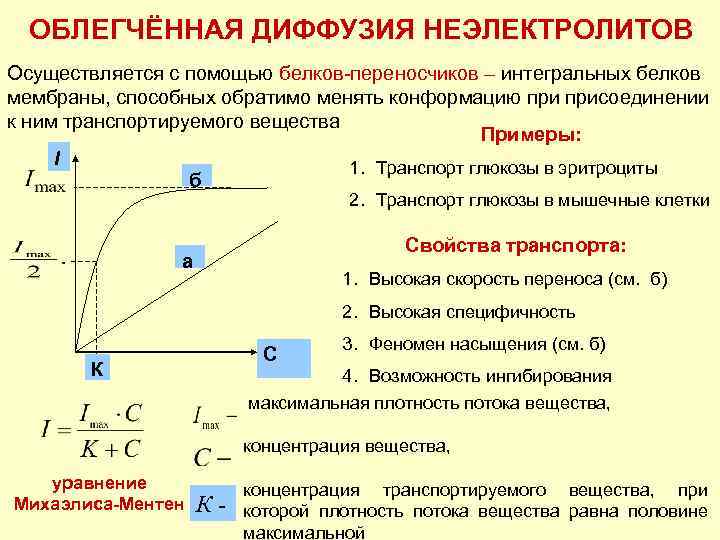
ОБЛЕГЧЁННАЯ ДИФФУЗИЯ НЕЭЛЕКТРОЛИТОВ Осуществляется с помощью белков-переносчиков – интегральных белков мембраны, способных обратимо менять конформацию присоединении к ним транспортируемого вещества Примеры: I 1. Транспорт глюкозы в эритроциты б 2. Транспорт глюкозы в мышечные клетки Свойства транспорта: а 1. Высокая скорость переноса (см. б) 2. Высокая специфичность С К 3. Феномен насыщения (см. б) 4. Возможность ингибирования максимальная плотность потока вещества, концентрация вещества, уравнение Михаэлиса-Ментен К- концентрация транспортируемого вещества, при которой плотность потока вещества равна половине максимальной
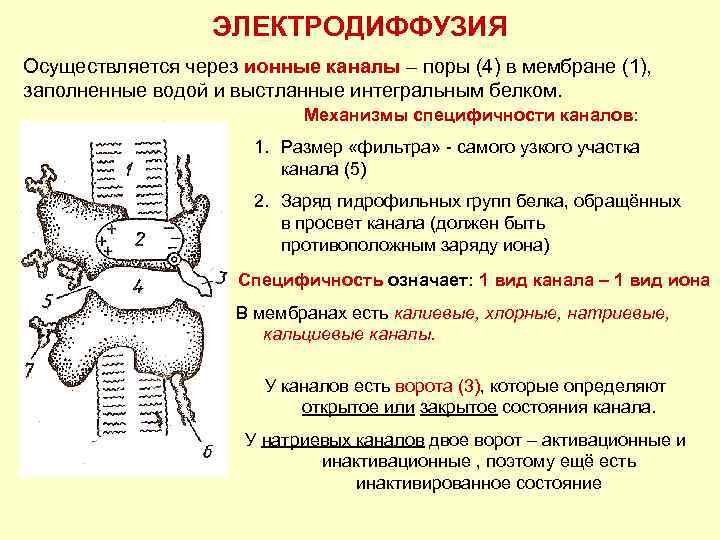
ЭЛЕКТРОДИФФУЗИЯ Осуществляется через ионные каналы – поры (4) в мембране (1), заполненные водой и выстланные интегральным белком. Механизмы специфичности каналов: 1. Размер «фильтра» - самого узкого участка канала (5) 2. Заряд гидрофильных групп белка, обращённых в просвет канала (должен быть противоположным заряду иона) Специфичность означает: 1 вид канала – 1 вид иона В мембранах есть калиевые, хлорные, натриевые, кальциевые каналы. У каналов есть ворота (3), которые определяют открытое или закрытое состояния канала. У натриевых каналов двое ворот – активационные и инактивационные , поэтому ещё есть инактивированное состояние

ЭЛЕКТРОДИФФУЗИЯ Уравнение Нернста. Планка Уравнение Теорелла плотность потока иона подвижность иона в растворе; ТД температура градиент электрохимического потенциала иона концентрация иона, универсальная газовая постоянная градиент концентрации иона градиент электрического потенциала иона число Фарадея заряд иона Уравнение Теорелла и уравнение Нернста-Планка описывают один и тот же вид транспорта – ЭЛЕКТРОДИФФУЗИЮ! Не путать уравнение Нернста. Планка с уравнением Нернста.
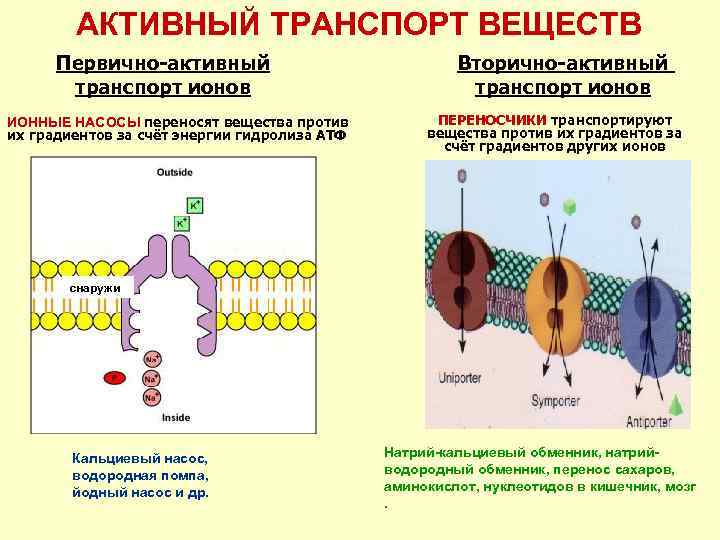
АКТИВНЫЙ ТРАНСПОРТ ВЕЩЕСТВ Первично-активный транспорт ионов ИОННЫЕ НАСОСЫ переносят вещества против их градиентов за счёт энергии гидролиза АТФ Вторично-активный транспорт ионов ПЕРЕНОСЧИКИ транспортируют вещества против их градиентов за счёт градиентов других ионов снаружи Кальциевый насос, водородная помпа, йодный насос и др. Натрий-кальциевый обменник, натрийводородный обменник, перенос сахаров, аминокислот, нуклеотидов в кишечник, мозг.

МЕМБРАННЫЙ ПОТЕНЦИАЛ ПОКОЯ И ЕГО ИОННЫЕ МЕХАНИЗМЫ В покое мембранный потенциал клеток отрицательный. В нервной клетке его величина составляет около -70 м. В. Благодаря тому, что клетка имеет МП, говорят, что мембрана электрически поляризована. Деполяризация – состояние мембраны, при котором МП смещается в положительную сторону (МП по модулю становится меньшим). Гиперполяризация – состояние мембраны, при котором МП смещается в отрицательную сторону, то есть увеличивается по модулю. ПРИЧИНЫ МЕМБРАННОГО ПОТЕНЦИАЛА ПОКОЯ: 1. Неодинаковая концентрация различных ионов внутри и снаружи клетки. Внутри клетки много катионов калия и мало натрия, тогда как снаружи наоборот - много катионов натрия и мало калия. Такое распределение ионов создаётся работой натрий-калиевого насоса. В результате – имеются градиенты концентрации обоих катионов: калий стремится покинуть клетку, а натрий – попасть в неё. Заряд катионов калия внутри клетки компенсируют органические анионы, для которых мембрана непроницаема, заряд натрия снаружи компенсируют хлор.

ПРИЧИНЫ МЕМБРАННОГО ПОТЕНЦИАЛА ПОКОЯ: 2. Неодинаковая проницаемость мембраны для различных ионов. В покое мембрана нервного волокна проницаема для ионов калия, но мало проницаема для других ионов. Поэтому в покое постоянно происходит диффузия ионов калия изнутри клетки наружу. Концентрация ионов калия практически не меняется. Но электрический потенциал внутри клетки оказывается сниженным по отношению к электрическому потенциалу наружной среды, а мембранный потенциал покоя имеет отрицательное значение. 3. Электрогенность натрий-калиевого насоса Натрий-калиевый насос выводит за один цикл 3 иона натрия из клетки, а вводит только два иона калия. Т. е. за один цикл на 3 выведенных положительных иона приходится 2 введённых положительных иона. На долю этого механизма приходится около 10% мембранного потенциала покоя
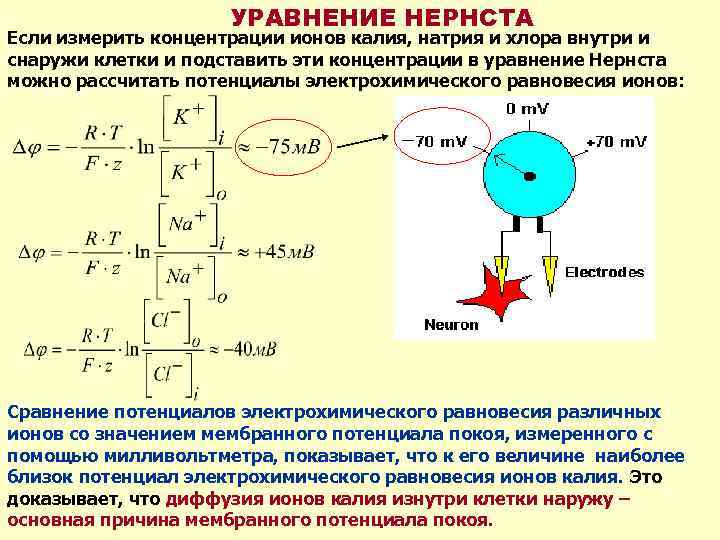
УРАВНЕНИЕ НЕРНСТА Если измерить концентрации ионов калия, натрия и хлора внутри и снаружи клетки и подставить эти концентрации в уравнение Нернста можно рассчитать потенциалы электрохимического равновесия ионов: Сравнение потенциалов электрохимического равновесия различных ионов со значением мембранного потенциала покоя, измеренного с помощью милливольтметра, показывает, что к его величине наиболее близок потенциал электрохимического равновесия ионов калия. Это доказывает, что диффузия ионов калия изнутри клетки наружу – основная причина мембранного потенциала покоя.

УРАВНЕНИЕ ГОЛЬДМАНА-ХОДЖКИНА Рассчитанный по уравнению Нернста для ионов калия мембранный потенциал покоя сдвинут в отрицательную стороны по отношению к реальной (измеряемой) величине. Это связано с тем, что мембрана также немного проницаема в покое для ионов натрия и хлора. Более точный расчёт мембранного потенциала покоя возможен на основе уравнения Гольдмана-Ходжкина, в котором учтены концентрации всех ионов, способных диффундировать через мембрану, и её проницаемость для различных ионов. Таким образом, мембранный потенциал покоя может быть рассчитан: 1. на основе отношения концентраций калия внутри и снаружи клетки с помощью уравнения Нернста для ионов калия (приблизительно), 2. На основе отношения концентраций всех потенциалобразующих ионов и проницаемостей в покое для них мембраны по уравнению Гольдмана-Ходжкина (более точно)
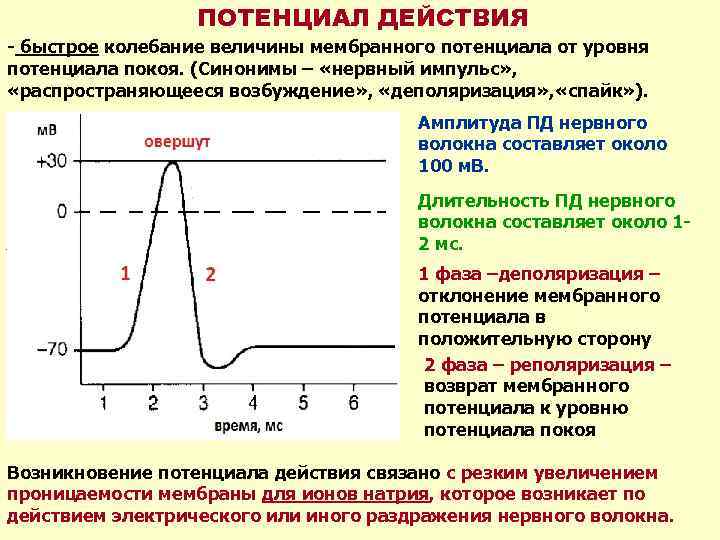
ПОТЕНЦИАЛ ДЕЙСТВИЯ - быстрое колебание величины мембранного потенциала от уровня потенциала покоя. (Синонимы – «нервный импульс» , «распространяющееся возбуждение» , «деполяризация» , «спайк» ). Амплитуда ПД нервного волокна составляет около 100 м. В. Длительность ПД нервного волокна составляет около 12 мс. 1 фаза –деполяризация – отклонение мембранного потенциала в положительную сторону 2 фаза – реполяризация – возврат мембранного потенциала к уровню потенциала покоя Возникновение потенциала действия связано с резким увеличением проницаемости мембраны для ионов натрия, которое возникает по действием электрического или иного раздражения нервного волокна.
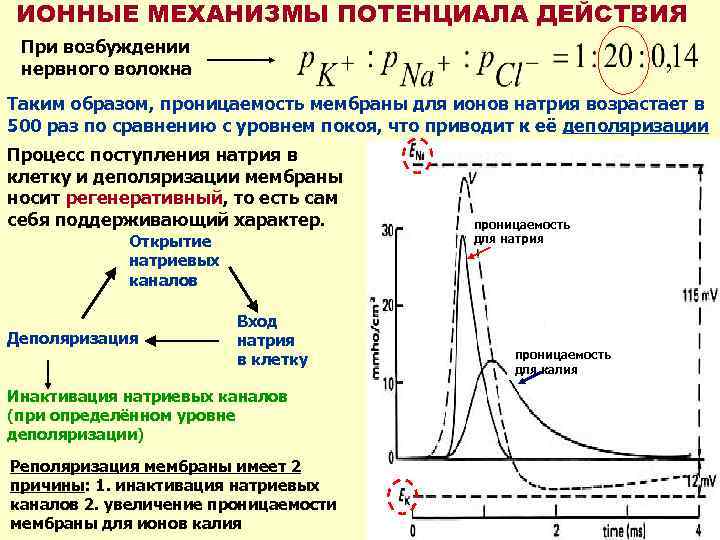
ИОННЫЕ МЕХАНИЗМЫ ПОТЕНЦИАЛА ДЕЙСТВИЯ При возбуждении нервного волокна Таким образом, проницаемость мембраны для ионов натрия возрастает в 500 раз по сравнению с уровнем покоя, что приводит к её деполяризации Процесс поступления натрия в клетку и деполяризации мембраны носит регенеративный, то есть сам себя поддерживающий характер. Открытие натриевых каналов Деполяризация проницаемость для натрия Вход натрия проницаемость в клетку для калия Инактивация натриевых каналов (при определённом уровне деполяризации) Реполяризация мембраны имеет 2 причины: 1. инактивация натриевых каналов 2. увеличение проницаемости мембраны для ионов калия
Подготовка.ppt