Физика.Веб 8.термодинамика.ppt
- Количество слайдов: 60

 Термодинамика. Основные понятия. Термодинамика – это наука о тепловых явлениях. Термодинамика рассматривает изолированные системы тел, находящиеся в состоянии термодинамического равновеси. В таких системах прекратились все наблюдаемые макроскопические процессы. Основное свойство термодинамически равновесной системы - выравнивание температуры всех ее частей; Термодинамический процесс - переход из одного в другое равновесное состояние. Процессы, состоящие из последовательности равновесных состояний, называются квазистатическими.
Термодинамика. Основные понятия. Термодинамика – это наука о тепловых явлениях. Термодинамика рассматривает изолированные системы тел, находящиеся в состоянии термодинамического равновеси. В таких системах прекратились все наблюдаемые макроскопические процессы. Основное свойство термодинамически равновесной системы - выравнивание температуры всех ее частей; Термодинамический процесс - переход из одного в другое равновесное состояние. Процессы, состоящие из последовательности равновесных состояний, называются квазистатическими.
 ОСНОВЫ ТЕРМОДИНАМИКИ. • Это теория о наиболее общих свойствах макроскопических тел. • На первый план выступают тепловые процессы и энергетические преобразования • Ядром являются три начала (закона) термодинамики.
ОСНОВЫ ТЕРМОДИНАМИКИ. • Это теория о наиболее общих свойствах макроскопических тел. • На первый план выступают тепловые процессы и энергетические преобразования • Ядром являются три начала (закона) термодинамики.
 ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИ АВТОР СУТЬ ВВЕДЕННЫХ ПРЕДСТАВЛЕНИЙ Д. Фаренгейт (1685 -1736) В 1710 – 1714 годах предложил шкалу и термометр: 0° температура смеси воды, льда и поваренной соли, 32° температура смеси воды и льда, 212° температура кипения воды, 96° температура тела человека. А. Цельсий (1701 – 1744), В 1742 году предложил стоградусную шкалу температур: 0° температура таяния льда, 100° температура кипение воды голливудский физик, мастер стеклодув шведский физик и астроном. Ж. Понселе (1788 – 1867), В 1826 году ввел понятие работы и единицы её французский физик и инженер. измерения. С. Карно (1796 – 1832), французский физик и инженер. Ввел представление об идеальной тепловой машине, а в 1824 году фактически дал формулировку второго начала термодинамики, связал тепло с движение частиц тела. Б. Клапейрон (1799 – 1864), французский физик и В 1834 году вывел уравнение состояния идеального газа, обобщенное в дальнейшем Д. И. Менделеевым. инженер.
ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИ АВТОР СУТЬ ВВЕДЕННЫХ ПРЕДСТАВЛЕНИЙ Д. Фаренгейт (1685 -1736) В 1710 – 1714 годах предложил шкалу и термометр: 0° температура смеси воды, льда и поваренной соли, 32° температура смеси воды и льда, 212° температура кипения воды, 96° температура тела человека. А. Цельсий (1701 – 1744), В 1742 году предложил стоградусную шкалу температур: 0° температура таяния льда, 100° температура кипение воды голливудский физик, мастер стеклодув шведский физик и астроном. Ж. Понселе (1788 – 1867), В 1826 году ввел понятие работы и единицы её французский физик и инженер. измерения. С. Карно (1796 – 1832), французский физик и инженер. Ввел представление об идеальной тепловой машине, а в 1824 году фактически дал формулировку второго начала термодинамики, связал тепло с движение частиц тела. Б. Клапейрон (1799 – 1864), французский физик и В 1834 году вывел уравнение состояния идеального газа, обобщенное в дальнейшем Д. И. Менделеевым. инженер.
 ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИ АВТОР СУТЬ ВВЕДЕННЫХ ПРЕДСТАВЛЕНИЙ Р. Майер (1818 – 1878), В 1842 году одним из первых сформулировал закон сохранения и превращения энергии. Дж. Джоуль (1818 – 1889), В 1843 году первый вычислил механический эквивалент теплоты и пришел к закону сохранения энергии. немецкий врач и естествоиспытатель. английский физик Г. Гельмгольц (1821 – 1894), В 1847 году дополнив идеи Майера и опыты Джоуля, немецкий физик и естествоиспытатель сформулировал и математически обосновал закон сохранения и превращения энергии. Р. Клаузиус (1822 – 1888), немецкий физик теоретик. В 1850 году сформулировал второе начало термодинамики, а в 1854 г. дал математическую формулировку первого начала. У. Томсон (Кельвин) (1824 – 1907), английский физик. В 1848 году ввел понятие абсолютной температуры, в 1851 году сформулировал второе начало термодинамики.
ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИ АВТОР СУТЬ ВВЕДЕННЫХ ПРЕДСТАВЛЕНИЙ Р. Майер (1818 – 1878), В 1842 году одним из первых сформулировал закон сохранения и превращения энергии. Дж. Джоуль (1818 – 1889), В 1843 году первый вычислил механический эквивалент теплоты и пришел к закону сохранения энергии. немецкий врач и естествоиспытатель. английский физик Г. Гельмгольц (1821 – 1894), В 1847 году дополнив идеи Майера и опыты Джоуля, немецкий физик и естествоиспытатель сформулировал и математически обосновал закон сохранения и превращения энергии. Р. Клаузиус (1822 – 1888), немецкий физик теоретик. В 1850 году сформулировал второе начало термодинамики, а в 1854 г. дал математическую формулировку первого начала. У. Томсон (Кельвин) (1824 – 1907), английский физик. В 1848 году ввел понятие абсолютной температуры, в 1851 году сформулировал второе начало термодинамики.
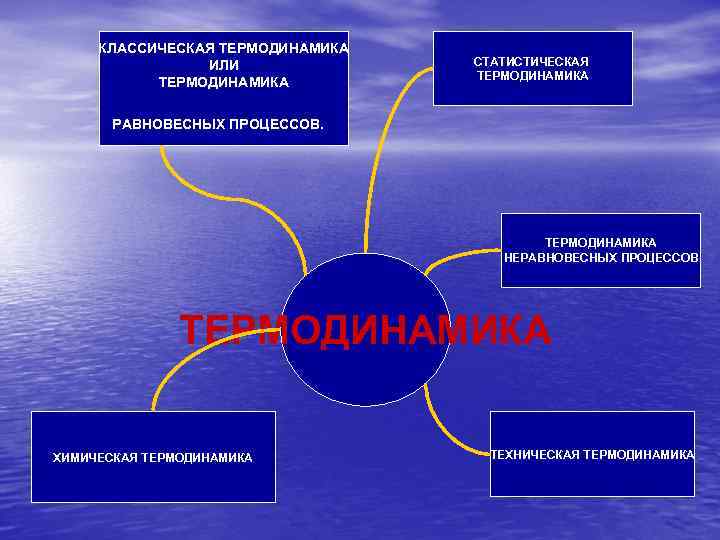 КЛАССИЧЕСКАЯ ТЕРМОДИНАМИКА ИЛИ ТЕРМОДИНАМИКА СТАТИСТИЧЕСКАЯ ТЕРМОДИНАМИКА РАВНОВЕСНЫХ ПРОЦЕССОВ. ТЕРМОДИНАМИКА НЕРАВНОВЕСНЫХ ПРОЦЕССОВ ТЕРМОДИНАМИКА ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА
КЛАССИЧЕСКАЯ ТЕРМОДИНАМИКА ИЛИ ТЕРМОДИНАМИКА СТАТИСТИЧЕСКАЯ ТЕРМОДИНАМИКА РАВНОВЕСНЫХ ПРОЦЕССОВ. ТЕРМОДИНАМИКА НЕРАВНОВЕСНЫХ ПРОЦЕССОВ ТЕРМОДИНАМИКА ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА
 ОСНОВЫ ТЕРМОДИНАМИКИ. • Это теория о наиболее общих свойствах макроскопических тел. • На первый план выступают тепловые процессы и энергетические преобразования • Ядром являются два начала (закона) термодинамики
ОСНОВЫ ТЕРМОДИНАМИКИ. • Это теория о наиболее общих свойствах макроскопических тел. • На первый план выступают тепловые процессы и энергетические преобразования • Ядром являются два начала (закона) термодинамики
 ЧТО ИЗУЧАЕТ ТЕРМОДИНАМИКА? Возникла как наука тепловых процессов, рассматриваемых с точки зрения энергетических преобразований. Не рассматривает явления с точки зрения движения молекул. Изучает наиболее общие свойства макроскопических систем, находящихся в равновесном состоянии, и процессы их перехода из одного состояния в другое. Термодинамический метод широко используется в других разделах физики, химии, биологии. Как и любая физическая теория или раздел физики, имеет свои границы применимости.
ЧТО ИЗУЧАЕТ ТЕРМОДИНАМИКА? Возникла как наука тепловых процессов, рассматриваемых с точки зрения энергетических преобразований. Не рассматривает явления с точки зрения движения молекул. Изучает наиболее общие свойства макроскопических систем, находящихся в равновесном состоянии, и процессы их перехода из одного состояния в другое. Термодинамический метод широко используется в других разделах физики, химии, биологии. Как и любая физическая теория или раздел физики, имеет свои границы применимости.
 ГРАНИЦЫ ПРИМЕНИМОСТИ ТЕРМОДИНАМИКИ • Неприменима к системе из нескольких молекул. • Не может быть применима ко всей Вселенной, слишком сложной и неопределенной физической системе.
ГРАНИЦЫ ПРИМЕНИМОСТИ ТЕРМОДИНАМИКИ • Неприменима к системе из нескольких молекул. • Не может быть применима ко всей Вселенной, слишком сложной и неопределенной физической системе.
 Термодинамические системы. Термодинамическими системами обычно называют не всякие , а только те макроскопические системы , которые находятся в термодинамическом равновесии. По способу передачи энергии , вещества и информации между рассматриваемой системы и окружающей средой термодинамические системы классифицируются : 1. Замкнутая ( изолированная ) система это система в которой нет обмена с внешними телами ни энергией , ни веществом ( в том числе и излучением ) , ни информацией . 2. Закрытая система в которой есть обмен только с энергией.
Термодинамические системы. Термодинамическими системами обычно называют не всякие , а только те макроскопические системы , которые находятся в термодинамическом равновесии. По способу передачи энергии , вещества и информации между рассматриваемой системы и окружающей средой термодинамические системы классифицируются : 1. Замкнутая ( изолированная ) система это система в которой нет обмена с внешними телами ни энергией , ни веществом ( в том числе и излучением ) , ни информацией . 2. Закрытая система в которой есть обмен только с энергией.
 Термодинамические системы. • 3. Адиабатно изолированная система это система в • которой есть обмен энергией только в форме теплоты . 4. Открытая система это система , которая обменивается и энергией , и веществом , и информацией.
Термодинамические системы. • 3. Адиабатно изолированная система это система в • которой есть обмен энергией только в форме теплоты . 4. Открытая система это система , которая обменивается и энергией , и веществом , и информацией.
 ТЕРМОДИНАМИКА ИЗОПРОЦЕССОВ. Процессы, происходящие при постоянном значении одного из параметров состояния (T, V или P) с данной массой газа называются изопроцессами. ИЗОТЕРМИЧЕСКИЙ ИЗОХОРНЫЙ ИЗОБАРНЫЙ АДИАБАТНЫЙ
ТЕРМОДИНАМИКА ИЗОПРОЦЕССОВ. Процессы, происходящие при постоянном значении одного из параметров состояния (T, V или P) с данной массой газа называются изопроцессами. ИЗОТЕРМИЧЕСКИЙ ИЗОХОРНЫЙ ИЗОБАРНЫЙ АДИАБАТНЫЙ
 • Внутренняя энергия и энтальпия Известно, что • • • протекание реакции Zn + H 2 SO 4 = Zn. SO 4 + H 2↑ сопрово ждается выделением тепла, которое, видимо, содержалось внутри данных веществ. Внутренняя энергия U – это энергия, скрытая в веществах и высвобо ждающаяся при химических реакциях или физических превращениях (вода лед пар). Внутренняя энергия равна сумме энергий: U = U 1 + U 2 + U 3 + U 4 + U 5, где U 1 – энергия поступательного движения молекул; U 2 – энергия враща тельного движения молекул; 3 – энергия U внутримолекулярного колебания электронов; U 4 – энергия движения электронов; U 5 – внутриядерная энергия; ΔU = U 2 U 1, • здесь ΔU – изменение внутренней энергии, равное разности между значения ми внутренней энергии конечного состояния системы 2 и U начального со стояния 1. U
• Внутренняя энергия и энтальпия Известно, что • • • протекание реакции Zn + H 2 SO 4 = Zn. SO 4 + H 2↑ сопрово ждается выделением тепла, которое, видимо, содержалось внутри данных веществ. Внутренняя энергия U – это энергия, скрытая в веществах и высвобо ждающаяся при химических реакциях или физических превращениях (вода лед пар). Внутренняя энергия равна сумме энергий: U = U 1 + U 2 + U 3 + U 4 + U 5, где U 1 – энергия поступательного движения молекул; U 2 – энергия враща тельного движения молекул; 3 – энергия U внутримолекулярного колебания электронов; U 4 – энергия движения электронов; U 5 – внутриядерная энергия; ΔU = U 2 U 1, • здесь ΔU – изменение внутренней энергии, равное разности между значения ми внутренней энергии конечного состояния системы 2 и U начального со стояния 1. U
 • Энтальпия – это свойство вещества, характеризующее • теплосодержа ние системы подобно тому, как свойствами вещества являются объем V, дав ление Р, температура и T внутренняя энергия U. Измеряется энтальпия в ккал/моль или к. Дж/моль (1 ккал = 4, 1840 к. Дж). На приведены графики изменения энтальпии в эндо и экзо термических реакциях, из которых видно, что в экзотермических реакциях энтальпия (теплосодержание) убывает, т. е. ∆Н < 0, а в эндотермических ре акциях энтальпия возрастает, т. е. ∆Н > 0.
• Энтальпия – это свойство вещества, характеризующее • теплосодержа ние системы подобно тому, как свойствами вещества являются объем V, дав ление Р, температура и T внутренняя энергия U. Измеряется энтальпия в ккал/моль или к. Дж/моль (1 ккал = 4, 1840 к. Дж). На приведены графики изменения энтальпии в эндо и экзо термических реакциях, из которых видно, что в экзотермических реакциях энтальпия (теплосодержание) убывает, т. е. ∆Н < 0, а в эндотермических ре акциях энтальпия возрастает, т. е. ∆Н > 0.
 • • Энтропия Частицам (молекулам, атомам, ионам) присуще стремление к беспоря дочному движению, поэтому система стремится перейти из более упорядо ченного состояния Wi в менее упорядоченное W 2. Количественной мерой беспорядка системы является энтропия Энтропия возрастает при следующих условиях: увеличении темпера туры, плавлении, кипении, расширении газов, растворении веществ. Зна чит, во всех случаях, когда вещество переходит из состояния с меньшей энергией в состояние с большей энергией, неупорядоченность частиц рас тет. И наоборот, все • процессы, связанные с увеличением упорядоченно сти, сопровождаются уменьшением энтропии (охлаждение, затвердевание, сжатие, кристаллизация). Изменение энтропии в химической реакции ΔSх. р в общем виде можно выразить уравнением в соответствии со следствием из закона Гесса: ΔSх. р = Σ Sкон. в в Σ Sисх. в в. • • Об изменении энтропии в ходе реакции можно судить по изменению объема газообразных веществ в ходе процесса. Например, при реакции • С(графит) + ½О 2(г) = СО(г) • объем газообразных продуктов реакции (1 моль) больше, чем исходных ве ществ (½ моль), т. е. реакция идет с увеличением объема. Следовательно, эн тропия возрастает, Δ S > 0. Если реакция идет без изменения объема, то энтропия практически не изменяется
• • Энтропия Частицам (молекулам, атомам, ионам) присуще стремление к беспоря дочному движению, поэтому система стремится перейти из более упорядо ченного состояния Wi в менее упорядоченное W 2. Количественной мерой беспорядка системы является энтропия Энтропия возрастает при следующих условиях: увеличении темпера туры, плавлении, кипении, расширении газов, растворении веществ. Зна чит, во всех случаях, когда вещество переходит из состояния с меньшей энергией в состояние с большей энергией, неупорядоченность частиц рас тет. И наоборот, все • процессы, связанные с увеличением упорядоченно сти, сопровождаются уменьшением энтропии (охлаждение, затвердевание, сжатие, кристаллизация). Изменение энтропии в химической реакции ΔSх. р в общем виде можно выразить уравнением в соответствии со следствием из закона Гесса: ΔSх. р = Σ Sкон. в в Σ Sисх. в в. • • Об изменении энтропии в ходе реакции можно судить по изменению объема газообразных веществ в ходе процесса. Например, при реакции • С(графит) + ½О 2(г) = СО(г) • объем газообразных продуктов реакции (1 моль) больше, чем исходных ве ществ (½ моль), т. е. реакция идет с увеличением объема. Следовательно, эн тропия возрастает, Δ S > 0. Если реакция идет без изменения объема, то энтропия практически не изменяется
 • • Энергия Гиббса В химических процессах одно временно действуют две тенденции: стремление частиц объединяться в более сложные, что уменьшает энтальпию; стремление частиц разъединиться, уве личить беспорядок, что увеличивает энтропию. Суммарный эффект этих двух противоположных тенденций в процес сах, протекающих при постоянной температуре и постоянном давлении, от ражает изменение нергии Гиббса ΔG: ΔG = ΔН TΔS, э где ΔН – изменение эптальпии (теплосодержания системы), к. Дж/моль; ΔS – изменение энтропии (меры беспорядка системы), Дж/(моль·К); T – темпера тура, К. Энергия Гиббса измеряется в килоджоулях на моль (к. Дж/моль). Характер изменений ΔG позволяет судить о принципиальной возмож ности или невозможности протекания процесса: если ΔG < 0, т. е. энергия Гиббса в ходе реакции уменьшается, то про цесс возможен и, начавшись, он протекает самопроизвольно (спонтанно); если ΔG > 0, то невозможно осуществить прямую реакцию в данных условиях, но возможно протекание обратной реакции; если ΔG = 0, наблюдается состояние химического равновесия, т. е. ΔН = TΔS.
• • Энергия Гиббса В химических процессах одно временно действуют две тенденции: стремление частиц объединяться в более сложные, что уменьшает энтальпию; стремление частиц разъединиться, уве личить беспорядок, что увеличивает энтропию. Суммарный эффект этих двух противоположных тенденций в процес сах, протекающих при постоянной температуре и постоянном давлении, от ражает изменение нергии Гиббса ΔG: ΔG = ΔН TΔS, э где ΔН – изменение эптальпии (теплосодержания системы), к. Дж/моль; ΔS – изменение энтропии (меры беспорядка системы), Дж/(моль·К); T – темпера тура, К. Энергия Гиббса измеряется в килоджоулях на моль (к. Дж/моль). Характер изменений ΔG позволяет судить о принципиальной возмож ности или невозможности протекания процесса: если ΔG < 0, т. е. энергия Гиббса в ходе реакции уменьшается, то про цесс возможен и, начавшись, он протекает самопроизвольно (спонтанно); если ΔG > 0, то невозможно осуществить прямую реакцию в данных условиях, но возможно протекание обратной реакции; если ΔG = 0, наблюдается состояние химического равновесия, т. е. ΔН = TΔS.
 • Процессы, протекающие с уменьшением энтальпии и увеличением эн тропии, необратимы. • Самопроизвольному протеканию реакции, т. е. чтобы было значение ΔG • • < 0, способствует уменьшение ΔН и увеличение ΔS. Итак, ΔG < 0, если ΔН < 0 и ΔS > 0. При других сочетаниях характера изменения ΔН и ΔS возможность протекания процесса определяет один из этих факторов: либо ΔН, либо ΔS. Если ΔН > 0 и ΔS > 0, то независимо от абсолютных величин ΔН, ΔS и Т реакция может протекать только в обратном направлении. Влияние температуры определяется знаком и величиной изменения энтропии ΔS в ходе реакции. При значениях ΔS > 0 и ΔН > 0 реакция будет протекать в прямом на правлении в том случае, если │ТΔ S│> │ΔН│. Самопроизвольному протека нию реакции должно способствовать повышение температуры. Если ΔН < 0 и ΔS < 0, то будет │ΔН│ > │ТΔS│. Поэтому для протека ния реакции в прямом направлении необходимо понижение температуры. Например, для реакции, протекающей с увеличением энтропии, т. е. ΔS > 0, 2 С(графит) + О 2(г) = 2 СО(г) (реакция экзотермическая, ΔН < 0), повыше ние температуры приводит к увеличению отрицательного значения ΔG, т. к. │ТΔS│< 0. Следовательно, при высоких
• Процессы, протекающие с уменьшением энтальпии и увеличением эн тропии, необратимы. • Самопроизвольному протеканию реакции, т. е. чтобы было значение ΔG • • < 0, способствует уменьшение ΔН и увеличение ΔS. Итак, ΔG < 0, если ΔН < 0 и ΔS > 0. При других сочетаниях характера изменения ΔН и ΔS возможность протекания процесса определяет один из этих факторов: либо ΔН, либо ΔS. Если ΔН > 0 и ΔS > 0, то независимо от абсолютных величин ΔН, ΔS и Т реакция может протекать только в обратном направлении. Влияние температуры определяется знаком и величиной изменения энтропии ΔS в ходе реакции. При значениях ΔS > 0 и ΔН > 0 реакция будет протекать в прямом на правлении в том случае, если │ТΔ S│> │ΔН│. Самопроизвольному протека нию реакции должно способствовать повышение температуры. Если ΔН < 0 и ΔS < 0, то будет │ΔН│ > │ТΔS│. Поэтому для протека ния реакции в прямом направлении необходимо понижение температуры. Например, для реакции, протекающей с увеличением энтропии, т. е. ΔS > 0, 2 С(графит) + О 2(г) = 2 СО(г) (реакция экзотермическая, ΔН < 0), повыше ние температуры приводит к увеличению отрицательного значения ΔG, т. к. │ТΔS│< 0. Следовательно, при высоких
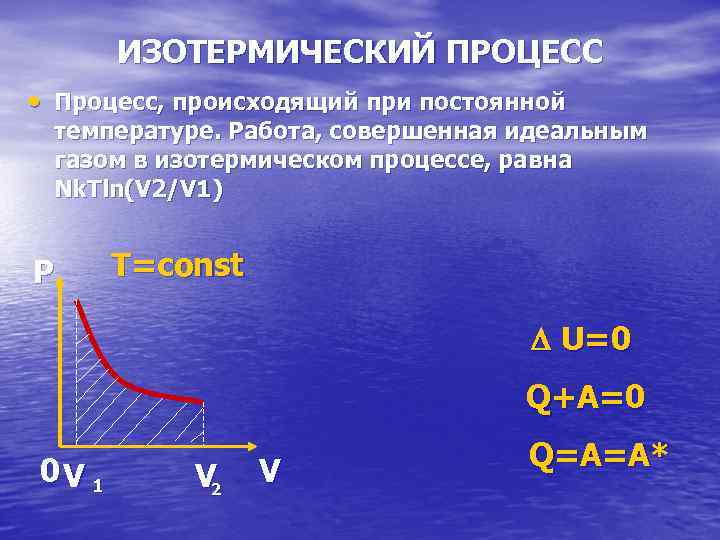 ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС • Процесс, происходящий при постоянной температуре. Работа, совершенная идеальным газом в изотермическом процессе, равна Nk. Tln(V 2/V 1) P T=const U=0 Q+A=0 0 V 1 V 2 V Q=A=A*
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС • Процесс, происходящий при постоянной температуре. Работа, совершенная идеальным газом в изотермическом процессе, равна Nk. Tln(V 2/V 1) P T=const U=0 Q+A=0 0 V 1 V 2 V Q=A=A*
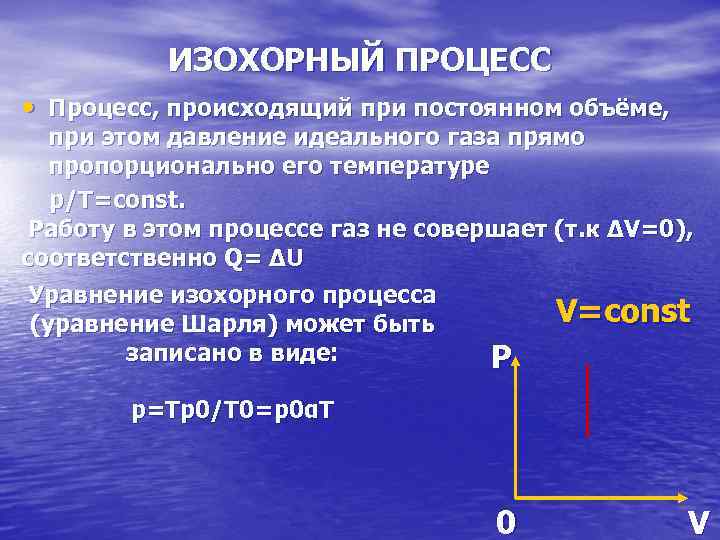 ИЗОХОРНЫЙ ПРОЦЕСС • Процесс, происходящий при постоянном объёме, при этом давление идеального газа прямо пропорционально его температуре p/T=const. Работу в этом процессе газ не совершает (т. к ΔV=0), соответственно Q= ΔU Уравнение изохорного процесса (уравнение Шарля) может быть записано в виде: V=const P p=Tp 0/T 0=p 0αT 0 V
ИЗОХОРНЫЙ ПРОЦЕСС • Процесс, происходящий при постоянном объёме, при этом давление идеального газа прямо пропорционально его температуре p/T=const. Работу в этом процессе газ не совершает (т. к ΔV=0), соответственно Q= ΔU Уравнение изохорного процесса (уравнение Шарля) может быть записано в виде: V=const P p=Tp 0/T 0=p 0αT 0 V
 ИЗОБАРНЫЙ ПРОЦЕСС • Процесс, происходящий при постоянном • • • давлении. Объем идеального газа при изобарном процессе пропорционален температуре V/T=const. Изобарный процесс можно описать уравнением: V = VoαT. Работа, совершаемая газом при расширении или сжатии газа, равна A = PΔV. P 0 V 1 2 V V
ИЗОБАРНЫЙ ПРОЦЕСС • Процесс, происходящий при постоянном • • • давлении. Объем идеального газа при изобарном процессе пропорционален температуре V/T=const. Изобарный процесс можно описать уравнением: V = VoαT. Работа, совершаемая газом при расширении или сжатии газа, равна A = PΔV. P 0 V 1 2 V V
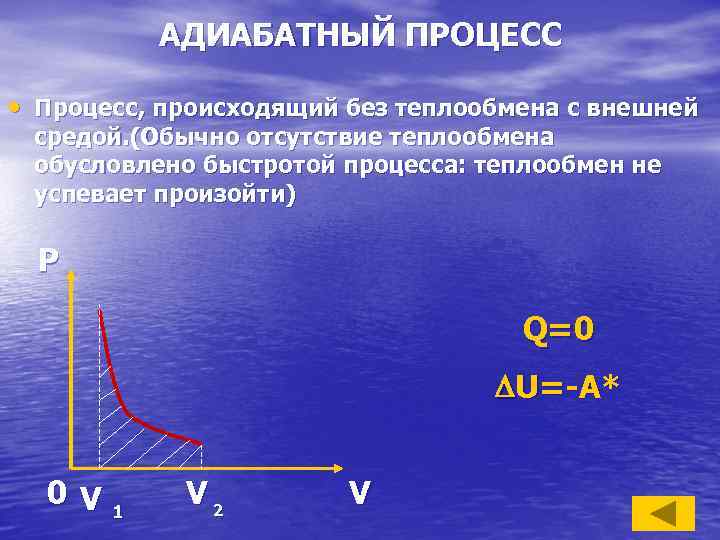 АДИАБАТНЫЙ ПРОЦЕСС • Процесс, происходящий без теплообмена с внешней средой. (Обычно отсутствие теплообмена обусловлено быстротой процесса: теплообмен не успевает произойти) P Q=0 U=-A* 0 V 1 V 2 V
АДИАБАТНЫЙ ПРОЦЕСС • Процесс, происходящий без теплообмена с внешней средой. (Обычно отсутствие теплообмена обусловлено быстротой процесса: теплообмен не успевает произойти) P Q=0 U=-A* 0 V 1 V 2 V
 ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ Совокупность физических величин, характеризующих свойства термодинамической системы. V - объём Р - давление T - температура U - внутренняя энергия
ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ Совокупность физических величин, характеризующих свойства термодинамической системы. V - объём Р - давление T - температура U - внутренняя энергия
 Законы термодинамики Термодинамика основывается на трёх законах, которые сформулированы на основе экспериментальных данных и поэтому могут быть приняты как постулаты.
Законы термодинамики Термодинамика основывается на трёх законах, которые сформулированы на основе экспериментальных данных и поэтому могут быть приняты как постулаты.
 Первое начало термодинамики – представляет собой закон сохранения энергии. Оно было сформулировано в середине 19 века в результате работ немецкого учёного Ю. Р. Майера, английского физика Дж. П. Джоуля и немецкого физика Г. Гельмгольца. Согласно первому началу термодинамики, термодинамическая система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника.
Первое начало термодинамики – представляет собой закон сохранения энергии. Оно было сформулировано в середине 19 века в результате работ немецкого учёного Ю. Р. Майера, английского физика Дж. П. Джоуля и немецкого физика Г. Гельмгольца. Согласно первому началу термодинамики, термодинамическая система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника.
 I ЗАКОН ТЕРМОДИНАМИКИ (Закон сохранения и превращения энергии в применении к тепловым процессам) Первый закон термодинамики U 2 -U 1=A+Q, где А-работа, совершаемая внешними силами над системой, Q-количество теплоты, переданное системе внешней силы, U 2 -U 1 -приращение энергии.
I ЗАКОН ТЕРМОДИНАМИКИ (Закон сохранения и превращения энергии в применении к тепловым процессам) Первый закон термодинамики U 2 -U 1=A+Q, где А-работа, совершаемая внешними силами над системой, Q-количество теплоты, переданное системе внешней силы, U 2 -U 1 -приращение энергии.
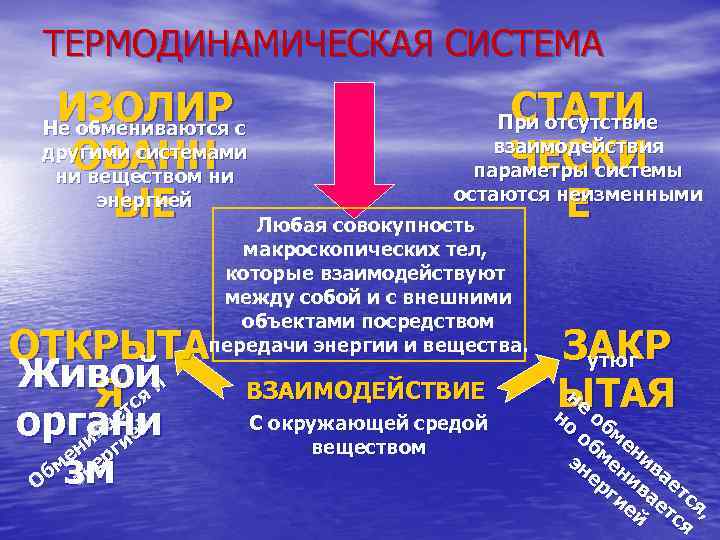 ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА ИЗОЛИР ОВАНН ЫЕ Не обмениваются с другими системами ни веществом ни энергией СТАТИ ЧЕСКИ Е При отсутствие взаимодействия параметры системы остаются неизменными Любая совокупность макроскопических тел, которые взаимодействуют между собой и с внешними объектами посредством передачи энергии и вещества. ОТКРЫТА Живойи Яется органи ва ей ни рги ме не э Об зм ВЗАИМОДЕЙСТВИЕ С окружающей средой веществом ЗАКР утюг не ЫТАЯ но об б об ме н эн мен ив ер и ае ги ва тс ей ет я, ся о
ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА ИЗОЛИР ОВАНН ЫЕ Не обмениваются с другими системами ни веществом ни энергией СТАТИ ЧЕСКИ Е При отсутствие взаимодействия параметры системы остаются неизменными Любая совокупность макроскопических тел, которые взаимодействуют между собой и с внешними объектами посредством передачи энергии и вещества. ОТКРЫТА Живойи Яется органи ва ей ни рги ме не э Об зм ВЗАИМОДЕЙСТВИЕ С окружающей средой веществом ЗАКР утюг не ЫТАЯ но об б об ме н эн мен ив ер и ае ги ва тс ей ет я, ся о
 ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ Совокупность физических величин, характеризующих свойства термодинамической системы. V - объём Р - давление T - температура U - внутренняя энергия
ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ Совокупность физических величин, характеризующих свойства термодинамической системы. V - объём Р - давление T - температура U - внутренняя энергия
 I ЗАКОН ТЕРМОДИНАМИКИ (Закон сохранения и превращения энергии в применении к тепловым процессам) Изменение внутренней энергии U системы равно сумме работы A совершенной внешними телами над системой, и сообщенного ей количества теплоты Q. U=A+Q A*=-A Q=A*+ U Количество теплоты Q, переданное системе, расходуется на увеличение её внутренней энергии U и совершение системой работы A* над внешними телами.
I ЗАКОН ТЕРМОДИНАМИКИ (Закон сохранения и превращения энергии в применении к тепловым процессам) Изменение внутренней энергии U системы равно сумме работы A совершенной внешними телами над системой, и сообщенного ей количества теплоты Q. U=A+Q A*=-A Q=A*+ U Количество теплоты Q, переданное системе, расходуется на увеличение её внутренней энергии U и совершение системой работы A* над внешними телами.
 ТЕРМОДИНАМИКА ИЗОПРОЦЕССОВ. Процессы, происходящие при постоянном значении одного из параметров состояния (T, V или P) с данной массой газа называются изопроцессами. ИЗОТЕРМИЧЕСКИЙ ИЗОХОРНЫЙ ИЗОБАРНЫЙ АДИАБАТНЫЙ
ТЕРМОДИНАМИКА ИЗОПРОЦЕССОВ. Процессы, происходящие при постоянном значении одного из параметров состояния (T, V или P) с данной массой газа называются изопроцессами. ИЗОТЕРМИЧЕСКИЙ ИЗОХОРНЫЙ ИЗОБАРНЫЙ АДИАБАТНЫЙ
 II ЗАКОН ТЕРМОДИНАМИКИ Невозможно перевести теплоту от более холодной системы к более горячей при отсутствии других одновременных изменений в обеих системах или окружающих телах. Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара. Невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела более нагретому. Тепловые процессы необратимы.
II ЗАКОН ТЕРМОДИНАМИКИ Невозможно перевести теплоту от более холодной системы к более горячей при отсутствии других одновременных изменений в обеих системах или окружающих телах. Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара. Невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела более нагретому. Тепловые процессы необратимы.
 ТЕПЛОВОЙ ДВИГАТЕЛЬ – ГЛАВНЫЙ ДВИГАТЕЛЬ СОВРЕМЕННОЙ ЭНЕРГЕТИКИ • Периодически действующий двигатель, совершающий работу за счет полученной извне теплоты. НАГРЕВАТЕЛЬ (Т 1) Q 1 РАБОЧЕЕ ТЕЛА Q 2 ХОЛОДИЛЬНИК (Т 2) A* A*=Q 1 – Q 2 Виды двигателей: 1. Паровая и газовая турбины 2. Карбюраторный двс 3. Дизель двс 4. Ракетный двигатель
ТЕПЛОВОЙ ДВИГАТЕЛЬ – ГЛАВНЫЙ ДВИГАТЕЛЬ СОВРЕМЕННОЙ ЭНЕРГЕТИКИ • Периодически действующий двигатель, совершающий работу за счет полученной извне теплоты. НАГРЕВАТЕЛЬ (Т 1) Q 1 РАБОЧЕЕ ТЕЛА Q 2 ХОЛОДИЛЬНИК (Т 2) A* A*=Q 1 – Q 2 Виды двигателей: 1. Паровая и газовая турбины 2. Карбюраторный двс 3. Дизель двс 4. Ракетный двигатель
 ВЕЧНЫЙ ДВИГАТЕЛЬ Первого рода Второго рода Будучи раз пущен в ход, совершал бы работу неограниченно долгое время, не заимствуя энергию извне Целиком превращал бы в работу теплоту, извлекаемою из окружающих тел НЕВОЗМОЖНЫ Противоречит закону сохранения и превращения энергии Противоречит второму началу термодинамики
ВЕЧНЫЙ ДВИГАТЕЛЬ Первого рода Второго рода Будучи раз пущен в ход, совершал бы работу неограниченно долгое время, не заимствуя энергию извне Целиком превращал бы в работу теплоту, извлекаемою из окружающих тел НЕВОЗМОЖНЫ Противоречит закону сохранения и превращения энергии Противоречит второму началу термодинамики
 Фазовые равновесия Правило фаз Гиббса: С = k – f + n, где k – число независимых компонентов; f – число фаз; n – число внешних параметров, влияющих на состояние фазового равновесия; С – число степеней свободы, т. е. число параметров, которые можно менять, не изменяя число фаз в системе. 33
Фазовые равновесия Правило фаз Гиббса: С = k – f + n, где k – число независимых компонентов; f – число фаз; n – число внешних параметров, влияющих на состояние фазового равновесия; С – число степеней свободы, т. е. число параметров, которые можно менять, не изменяя число фаз в системе. 33
 ТЕРМОДИНАМИКА И ПРИРОДА В окружающей нас природе термодинамически обратимых процессов нет. Энтропия в термодинамически не обратимых процессах, протекающих в изолированной системе, возрастает. По определению А. Эддингтона, возрастание энтропии, определяющей необратимые процессы есть «стрела времени» : чем выше энтропия системы, тем больше временной промежуток прошла система в своей эволюции. Возрастание энтропии вселенной должно привести к тому, что температура всех тел сравняется т. е. наступит тепловое равновесие и все процессы прекратятся, наступит «тепловая смерть Вселенной» . (Выводы второго закона термодинамики не всегда имеют место в природе и его нельзя применить ко всем существующим процессам).
ТЕРМОДИНАМИКА И ПРИРОДА В окружающей нас природе термодинамически обратимых процессов нет. Энтропия в термодинамически не обратимых процессах, протекающих в изолированной системе, возрастает. По определению А. Эддингтона, возрастание энтропии, определяющей необратимые процессы есть «стрела времени» : чем выше энтропия системы, тем больше временной промежуток прошла система в своей эволюции. Возрастание энтропии вселенной должно привести к тому, что температура всех тел сравняется т. е. наступит тепловое равновесие и все процессы прекратятся, наступит «тепловая смерть Вселенной» . (Выводы второго закона термодинамики не всегда имеют место в природе и его нельзя применить ко всем существующим процессам).
 Второе начало термодинамики - физический принцип, накладывающий ограничение на направление процессов передачи тепла между телами. Постулат Клаузиуса: «Невозможен процесс, единственным результатом которого являлась бы передача тепла от более холодного тела к более горячему» Не возможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара. Не возможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела более нагретому. Тепловые процессы необратимы
Второе начало термодинамики - физический принцип, накладывающий ограничение на направление процессов передачи тепла между телами. Постулат Клаузиуса: «Невозможен процесс, единственным результатом которого являлась бы передача тепла от более холодного тела к более горячему» Не возможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара. Не возможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела более нагретому. Тепловые процессы необратимы
 Третье начало термодинамики. • Это физический принцип, определяющий • поведение энтропии приближении температуры к абсолютному нулю. Является одним из постулатов термодинамики, принимаемым на основе обобщения значительного количества экспериментальных данных. В 1911 году Макс Планк сформулировал третье начало, как условие обращения в нуль энтропии всех тел при стремлении температуры к абсолютному нулю.
Третье начало термодинамики. • Это физический принцип, определяющий • поведение энтропии приближении температуры к абсолютному нулю. Является одним из постулатов термодинамики, принимаемым на основе обобщения значительного количества экспериментальных данных. В 1911 году Макс Планк сформулировал третье начало, как условие обращения в нуль энтропии всех тел при стремлении температуры к абсолютному нулю.
 Энергия Гиббса ( G) (изобарно-изотермический потенциал) – стандартная энергия Гиббса образования вещества. 37
Энергия Гиббса ( G) (изобарно-изотермический потенциал) – стандартная энергия Гиббса образования вещества. 37
 Энтальпия ( Н), к. Дж/моль . 38
Энтальпия ( Н), к. Дж/моль . 38
 Изменение энтальпии в экзо- и эндотермических реакциях 39
Изменение энтальпии в экзо- и эндотермических реакциях 39
 Внутренняя энергия (U) U=U 1+U 2+U 3+U 4+U 5, где U 1 – энергия поступательного движения молекул; U 2 – энергия вращательного движения молекул; U 3 – энергия движения электронов; U 4 – внутриядерная энергия; U 5 – энергия внутримолекулярных колебаний электронов. 40
Внутренняя энергия (U) U=U 1+U 2+U 3+U 4+U 5, где U 1 – энергия поступательного движения молекул; U 2 – энергия вращательного движения молекул; U 3 – энергия движения электронов; U 4 – внутриядерная энергия; U 5 – энергия внутримолекулярных колебаний электронов. 40
 Внутренняя энергия. • Внутренняя энергия вещества складывается из • • • кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом; Внутренняя энергия U тела однозначно определяется макроскопическими параметрами, характеризующими состояние тела; Внутренняя энергия U тела зависит наряду с температурой T также и от объема V; Внутренняя энергия является функцией состояния; U = U(T, V) Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную).
Внутренняя энергия. • Внутренняя энергия вещества складывается из • • • кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом; Внутренняя энергия U тела однозначно определяется макроскопическими параметрами, характеризующими состояние тела; Внутренняя энергия U тела зависит наряду с температурой T также и от объема V; Внутренняя энергия является функцией состояния; U = U(T, V) Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную).
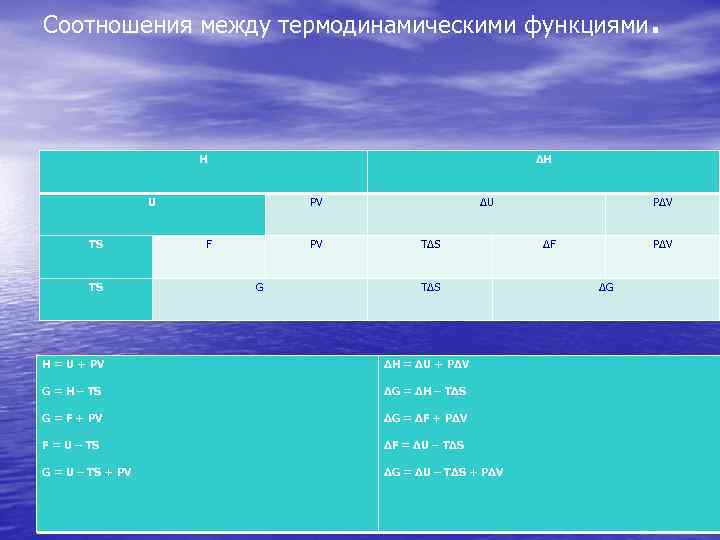 Соотношения между термодинамическими функциями H ΔH U TS TS . PV F PV G ΔU TΔS H = U + PV ΔH = ΔU + PΔV G = H – TS ΔG = ΔH – TΔS G = F + PV ΔG = ΔF + PΔV F = U – TS ΔF = ΔU – TΔS G = U – TS + PV ΔG = ΔU – TΔS + PΔV ΔF PΔV ΔG
Соотношения между термодинамическими функциями H ΔH U TS TS . PV F PV G ΔU TΔS H = U + PV ΔH = ΔU + PΔV G = H – TS ΔG = ΔH – TΔS G = F + PV ΔG = ΔF + PΔV F = U – TS ΔF = ΔU – TΔS G = U – TS + PV ΔG = ΔU – TΔS + PΔV ΔF PΔV ΔG
 Третий закон термодинамики. • Постулат Планка • Энтропия любого вещества находится в • • термодинамическом равновесии при абсолютном нуле равна нулю. S = 0, при Т = 0 К. Абсолютный ноль температуры недостижим. Т = 10 5 К. При абсолютном нуле, энтропия правильно построенного кристалла любого химически чистого соединения равна нулю. Sок = 0; . Тепловая теорема Нернста. По мере приближения к абсолютному нулю, значение энтропии и энергии Гиббса сближается друг с другом.
Третий закон термодинамики. • Постулат Планка • Энтропия любого вещества находится в • • термодинамическом равновесии при абсолютном нуле равна нулю. S = 0, при Т = 0 К. Абсолютный ноль температуры недостижим. Т = 10 5 К. При абсолютном нуле, энтропия правильно построенного кристалла любого химически чистого соединения равна нулю. Sок = 0; . Тепловая теорема Нернста. По мере приближения к абсолютному нулю, значение энтропии и энергии Гиббса сближается друг с другом.
 • • • • Процессы, протекающие с возрастанием энтропии (ΔS > 0): Кипение Плавление Испарение Растворение Диссоциация Процессы, протекающие с уменьшением энтропии (S → min): Сжатие Конденсация паров Кристаллизация вещества Диссоциативные процессы
• • • • Процессы, протекающие с возрастанием энтропии (ΔS > 0): Кипение Плавление Испарение Растворение Диссоциация Процессы, протекающие с уменьшением энтропии (S → min): Сжатие Конденсация паров Кристаллизация вещества Диссоциативные процессы
 • F (свободная энергия Гельмгольца, или изохорно изотермический потенциал) – количество энергии, которое можно перевести в любую полезную работу • G (свободная энергия Гиббса, или изобарно изотермический потенциал) – количество тепла, которое можно перевести в другую работу.
• F (свободная энергия Гельмгольца, или изохорно изотермический потенциал) – количество энергии, которое можно перевести в любую полезную работу • G (свободная энергия Гиббса, или изобарно изотермический потенциал) – количество тепла, которое можно перевести в другую работу.
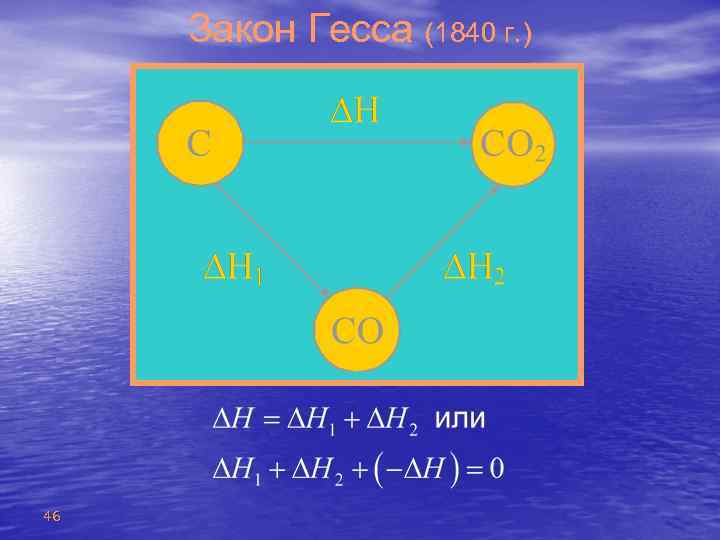 Закон Гесса (1840 г. ) 46
Закон Гесса (1840 г. ) 46
 Следствие из закона Гесса 47
Следствие из закона Гесса 47
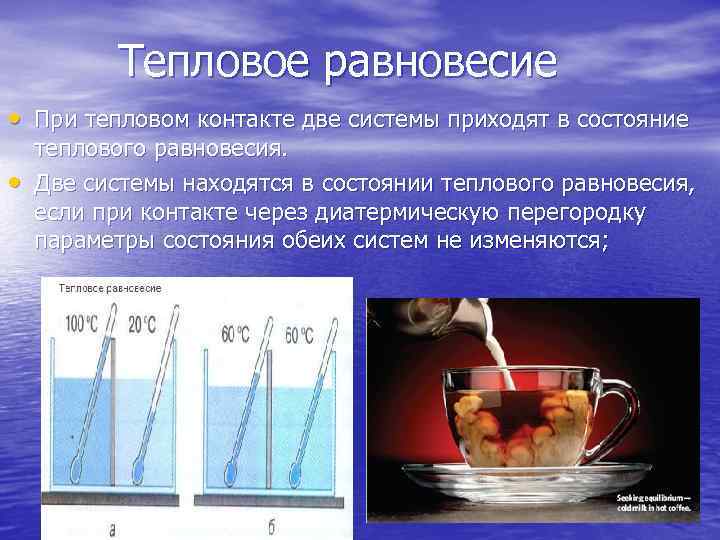 Тепловое равновесие • При тепловом контакте две системы приходят в состояние • теплового равновесия. Две системы находятся в состоянии теплового равновесия, если при контакте через диатермическую перегородку параметры состояния обеих систем не изменяются;
Тепловое равновесие • При тепловом контакте две системы приходят в состояние • теплового равновесия. Две системы находятся в состоянии теплового равновесия, если при контакте через диатермическую перегородку параметры состояния обеих систем не изменяются;
 Теплопередача. • ТЕПЛОПЕРЕДАЧА (или теплообмен) один из способов • • изменения внутренней энергии тела (или системы тел), при этом внутренняя энергия одного тела переходит во внутреннюю энергию другого тела без совершения механической работы. Теплота способна переходить только от тела с более высокой температурой к телу менее нагретому Теплообмен всегда протекает так, что убыль внутренней энергии одних тел всегда сопровождается таким же приращением внутренней энергии других тел, участвующих в теплообмене. Это является частным случаем закона сохранения энергии.
Теплопередача. • ТЕПЛОПЕРЕДАЧА (или теплообмен) один из способов • • изменения внутренней энергии тела (или системы тел), при этом внутренняя энергия одного тела переходит во внутреннюю энергию другого тела без совершения механической работы. Теплота способна переходить только от тела с более высокой температурой к телу менее нагретому Теплообмен всегда протекает так, что убыль внутренней энергии одних тел всегда сопровождается таким же приращением внутренней энергии других тел, участвующих в теплообмене. Это является частным случаем закона сохранения энергии.
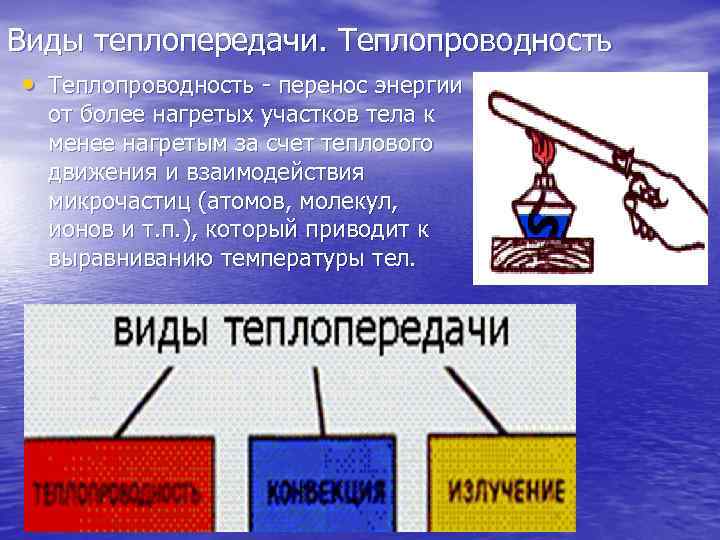 Виды теплопередачи. Теплопроводность • Теплопроводность перенос энергии от более нагретых участков тела к менее нагретым за счет теплового движения и взаимодействия микрочастиц (атомов, молекул, ионов и т. п. ), который приводит к выравниванию температуры тел.
Виды теплопередачи. Теплопроводность • Теплопроводность перенос энергии от более нагретых участков тела к менее нагретым за счет теплового движения и взаимодействия микрочастиц (атомов, молекул, ионов и т. п. ), который приводит к выравниванию температуры тел.
 Виды теплопередачи. Теплопроводность • Этот вид передачи внутренней энергии характерен как • • • для твердых веществ, так и для жидкостей и газов. Теплопроводность различных веществ разная. Металлы обладают самой высокой теплопроводностью, причем у разных металлов теплопроводность отличается. Жидкости обладают меньшей теплопроводностью, чем твердые тела, а газы меньшей, чем жидкости.
Виды теплопередачи. Теплопроводность • Этот вид передачи внутренней энергии характерен как • • • для твердых веществ, так и для жидкостей и газов. Теплопроводность различных веществ разная. Металлы обладают самой высокой теплопроводностью, причем у разных металлов теплопроводность отличается. Жидкости обладают меньшей теплопроводностью, чем твердые тела, а газы меньшей, чем жидкости.
 Виды теплопередачи. Конвекция. Естественная конвекция возникает при неравномерном нагреве (нагреве снизу) текучих или сыпучих веществ, находящихся в поле силы тяжести (или в системе, движущейся с ускорением). При вынужденной конвекция перемещение вещества происходит главным образом под воздействием какого либо устройства (насоса, мешалки и т. п. )
Виды теплопередачи. Конвекция. Естественная конвекция возникает при неравномерном нагреве (нагреве снизу) текучих или сыпучих веществ, находящихся в поле силы тяжести (или в системе, движущейся с ускорением). При вынужденной конвекция перемещение вещества происходит главным образом под воздействием какого либо устройства (насоса, мешалки и т. п. )
 Виды теплопередачи. Излучение. • Излучение вид теплопередачи, • при котором энергия передается с помощью электромагнитных волн (преимущественно инфракрасного диапазона). Может происходить в вакууме
Виды теплопередачи. Излучение. • Излучение вид теплопередачи, • при котором энергия передается с помощью электромагнитных волн (преимущественно инфракрасного диапазона). Может происходить в вакууме
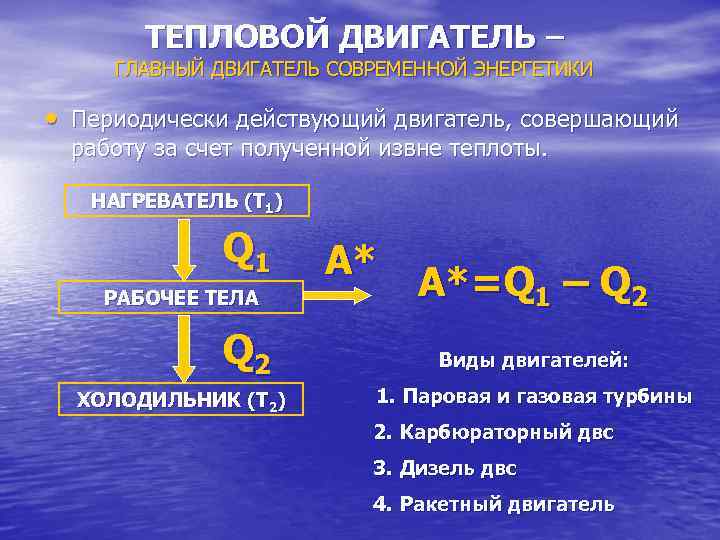 ТЕПЛОВОЙ ДВИГАТЕЛЬ – ГЛАВНЫЙ ДВИГАТЕЛЬ СОВРЕМЕННОЙ ЭНЕРГЕТИКИ • Периодически действующий двигатель, совершающий работу за счет полученной извне теплоты. НАГРЕВАТЕЛЬ (Т 1) Q 1 РАБОЧЕЕ ТЕЛА Q 2 ХОЛОДИЛЬНИК (Т 2) A* A*=Q 1 – Q 2 Виды двигателей: 1. Паровая и газовая турбины 2. Карбюраторный двс 3. Дизель двс 4. Ракетный двигатель
ТЕПЛОВОЙ ДВИГАТЕЛЬ – ГЛАВНЫЙ ДВИГАТЕЛЬ СОВРЕМЕННОЙ ЭНЕРГЕТИКИ • Периодически действующий двигатель, совершающий работу за счет полученной извне теплоты. НАГРЕВАТЕЛЬ (Т 1) Q 1 РАБОЧЕЕ ТЕЛА Q 2 ХОЛОДИЛЬНИК (Т 2) A* A*=Q 1 – Q 2 Виды двигателей: 1. Паровая и газовая турбины 2. Карбюраторный двс 3. Дизель двс 4. Ракетный двигатель
 Принципы действия тепловых машин. • Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. • Механическая работа в тепловых двигателях • • производится в процессе расширения некоторого вещества, которое называется рабочим телом. Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние.
Принципы действия тепловых машин. • Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. • Механическая работа в тепловых двигателях • • производится в процессе расширения некоторого вещества, которое называется рабочим телом. Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние.
 КПД тепловой машины. • В 1824 году французский инженер Карно изобрёл (на бумаге) идеальную тепловую машину с идеальным газом в качестве рабочего тела. Важная роль двигателя Карно заключается не только в его возможном практическом применении, но и в том, что он позволяет объяснить принципы действия тепловых машин вообще. Все процессы в машине Карно рассматриваются как равновесные (обратимые).
КПД тепловой машины. • В 1824 году французский инженер Карно изобрёл (на бумаге) идеальную тепловую машину с идеальным газом в качестве рабочего тела. Важная роль двигателя Карно заключается не только в его возможном практическом применении, но и в том, что он позволяет объяснить принципы действия тепловых машин вообще. Все процессы в машине Карно рассматриваются как равновесные (обратимые).
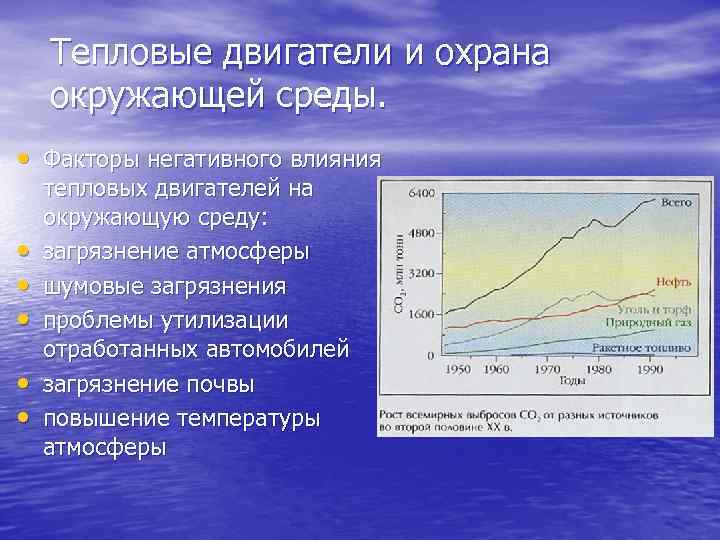 Тепловые двигатели и охрана окружающей среды. • Факторы негативного влияния • • • тепловых двигателей на окружающую среду: загрязнение атмосферы шумовые загрязнения проблемы утилизации отработанных автомобилей загрязнение почвы повышение температуры атмосферы
Тепловые двигатели и охрана окружающей среды. • Факторы негативного влияния • • • тепловых двигателей на окружающую среду: загрязнение атмосферы шумовые загрязнения проблемы утилизации отработанных автомобилей загрязнение почвы повышение температуры атмосферы
 Отрицательное влияние тепловых машин на окружающую среду связано с действием различных факторов. при сжигании топлива используется кислород из атмосферы, вследствие чего содержание кислорода в воздухе постепенно уменьшается. сжигание топлива сопровождается выделением в атмосферу углекислого газа. при сжигании угля и нефти атмосфера загрязняется азотными и серными соединениями, вредными для здоровья человека. Автомобильные двигатели ежегодно выбрасывают в атмосферу два три тонн свинца.
Отрицательное влияние тепловых машин на окружающую среду связано с действием различных факторов. при сжигании топлива используется кислород из атмосферы, вследствие чего содержание кислорода в воздухе постепенно уменьшается. сжигание топлива сопровождается выделением в атмосферу углекислого газа. при сжигании угля и нефти атмосфера загрязняется азотными и серными соединениями, вредными для здоровья человека. Автомобильные двигатели ежегодно выбрасывают в атмосферу два три тонн свинца.
 Тепловые двигатели и охрана окружающей среды. • Один из путей уменьшения путей загрязнения окружающей • • среды использованием в автомобилях вместо карбюраторных бензиновых двигателей дизелей, в топливо которых не добавляют соединения свинца. Перспективными являются разработки автомобилей, в которых вместо бензиновых двигателей применяются электродвигатели или двигатели, использующие в качестве топлива водород. Согласно законам термодинамики производство электрической и механической энергии в принципе не может быть осуществлено без отвода в окружающую среду значительных количеств теплоты. Это не может не приводить к постепенному повышению средней температуры на земле.
Тепловые двигатели и охрана окружающей среды. • Один из путей уменьшения путей загрязнения окружающей • • среды использованием в автомобилях вместо карбюраторных бензиновых двигателей дизелей, в топливо которых не добавляют соединения свинца. Перспективными являются разработки автомобилей, в которых вместо бензиновых двигателей применяются электродвигатели или двигатели, использующие в качестве топлива водород. Согласно законам термодинамики производство электрической и механической энергии в принципе не может быть осуществлено без отвода в окружающую среду значительных количеств теплоты. Это не может не приводить к постепенному повышению средней температуры на земле.
 Заключение. • Термодинамика исторически возникла как эмпирическая наука об основных способах преобразования внутренней энергии тел для совершения механической работы. Однако в процессе своего развития термодинамика проникла во все разделы физики, где возможно ввести понятие "температура" и позволила теоретически предсказать многие явления задолго до появления строгой теории этих явлений.
Заключение. • Термодинамика исторически возникла как эмпирическая наука об основных способах преобразования внутренней энергии тел для совершения механической работы. Однако в процессе своего развития термодинамика проникла во все разделы физики, где возможно ввести понятие "температура" и позволила теоретически предсказать многие явления задолго до появления строгой теории этих явлений.


