биофизика 004-005.ppt
- Количество слайдов: 18

Термодинамика неравновесных процессов • Биологические объекты не находятся в состоянии равновесия. • Процессы, проходящие в биологических системах, являются необратимыми. «Термодинамика необратимых процессов вблизи состояния равновесия» «Нелинейная термодинамика»

Работоспособность биологических систем Биологические системы характеризуются наличием разнообразных градиентов: • концентрационный • осмотический • электрический Работа в биологических системах связана с реализацией энергии каких-либо градиентов

Свободная энергия (Гиббса G) биологической системы определяется наличием и величиной градиента: G = RT ln Ф 1/Ф 2 • R – универсальная газовая постоянная, • Т – термодинамическая температура по Кельвину • Ф 1 и Ф 2 – значения параметра, определяющего градиенты.
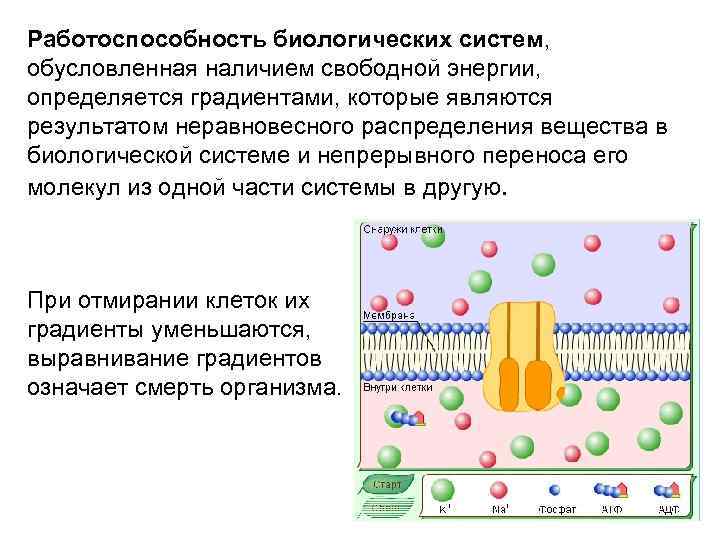
Работоспособность биологических систем, обусловленная наличием свободной энергии, определяется градиентами, которые являются результатом неравновесного распределения вещества в биологической системе и непрерывного переноса его молекул из одной части системы в другую. При отмирании клеток их градиенты уменьшаются, выравнивание градиентов означает смерть организма.

Термодинамические потоки Процесс жизнедеятельности определяют потоки: осмотический, электрический, тепловой, диффузионный…которые характеризуются градиентами соответствующих величин. Н-р: интенсивность диффузионного потока , согласно закону Фика, пропорциональна градиенту концентрации вещества: • Ig = - D dc/dx, где D – коэффициент диффузии, • dc/dx – концентрационный градиент .

В живых организмах градиенты определяют потоки • Градиенты, вызывающие в системе потоки веществ, теплоты, зарядов, называются термодинамическими силами, обозначаются символом х. Соответствующие потоки обозначаются буквой J (значение потока, или суммарная скорость соответствующего потока).
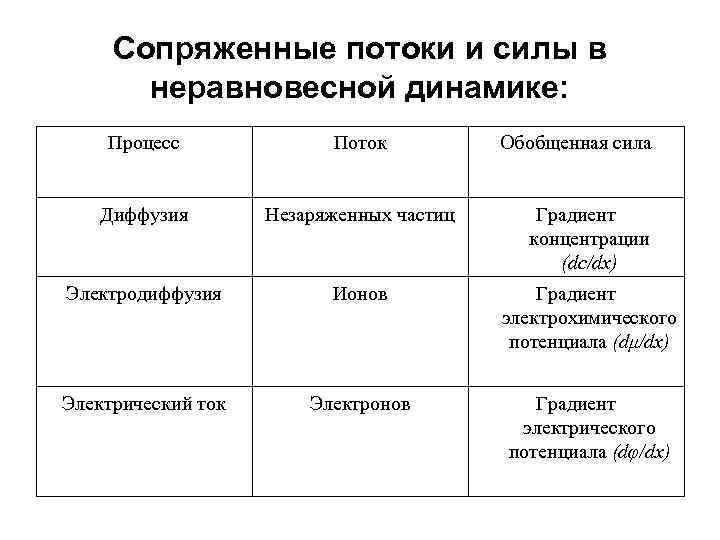
Сопряженные потоки и силы в неравновесной динамике: Процесс Поток Обобщенная сила Диффузия Незаряженных частиц Градиент концентрации (dc/dx) Электродиффузия Ионов Градиент электрохимического потенциала (dμ/dx) Электрический ток Электронов Градиент электрического потенциала (dφ/dx)

Соотношение между значениями движущих сил и скоростей процессов Ларс Онзагер (1903 — 1976) — норвежскоамериканский химик и физик, Лауреат Нобелевской премии по химии (1968). Известен благодаря своей теории необратимых реакций

di. S / dt = (1/Т)Х J > 0 • Х – термодинамические силы, действующие в системе интенсивные факторы, представляющие собой разнообразные градиенты (температуры, давления, концентрации, электрического потенциала, химического потенциала и др. ) • J – обобщенные потоки, вызываемые этими силами, это могут быть потоки тепла, вещества, электрических зарядов и т. д. Произведение Х J имеет размерность работы
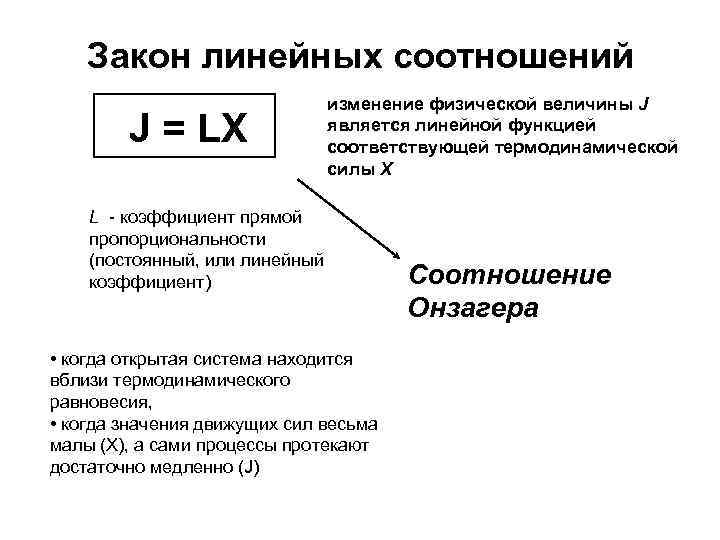
Закон линейных соотношений J = LX изменение физической величины J является линейной функцией соответствующей термодинамической силы X L - коэффициент прямой пропорциональности (постоянный, или линейный коэффициент) • когда открытая система находится вблизи термодинамического равновесия, • когда значения движущих сил весьма малы (Х), а сами процессы протекают достаточно медленно (J) Соотношение Онзагера

Например, закон Ома: • поток электричества I • движущая сила – разность потенциалов U • L = 1/R – линейный коэффициент пропорциональности I = U/R • I — сила тока (А, ампер) , • U — напряжение или разность потенциалов (В, вольт), • R — сопротивление (Ом).

в живой системе одновременно протекает несколько процессов, каждый из которых характеризуется собственными значениями скорости и движущей силы каждый поток зависит не только от «своей силы» , но и от всех других сил Два взаимодействующих процесса : J 1, X 1 поток тепла Линейный градиент температуры коэффициент J 2, X 2 взаимности L 12. поток массы концентрационный градиент L 12 и L 21 соответствуют возможной взаимосвязи двух потоков коэффициенты взаимности Онзагера L 12 = L 21 J 1 = L 11 X 1 + L 12 X 2 J 2 = L 21 X 1 + L 22 X 2 Каждый из потоков влияет на величину других потоков системы! Сопряжение потоков различных процессов означает, что потоки, сами по себе невозможные с ТД точки зрения, которые сопровождаются повышением свободной энергии, - могут осуществляться за счет других обобщенных сил.

Стационарное состояние открытой системы • Состояние системы, при котором ее параметры не изменяются в течении длительного времени, но происходит обмен веществом и энергией с окружающей средой, называют стационарным. • Состояние системы называется стационарным, если величина энтропии не изменяется во времени d. S = 0 (di. S = - de. S). Энтропия системы в стационарном состоянии - стабильная, но не максимальная. • Градиенты и потоки сохраняются в системе.
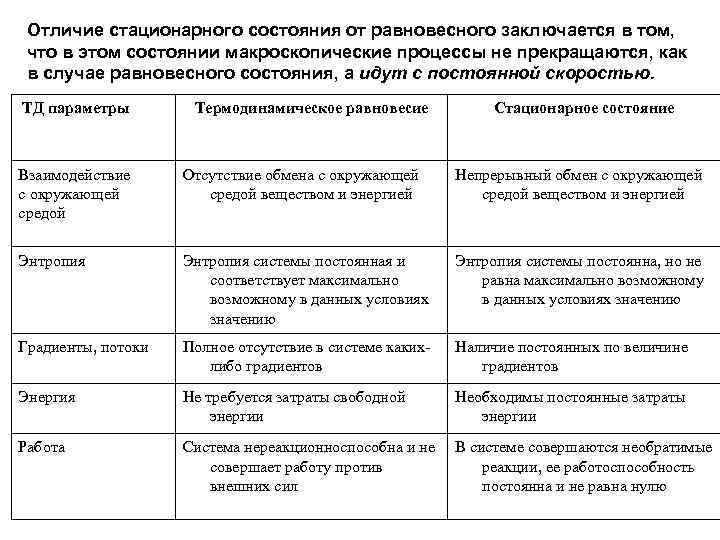
Отличие стационарного состояния от равновесного заключается в том, что в этом состоянии макроскопические процессы не прекращаются, как в случае равновесного состояния, а идут с постоянной скоростью. ТД параметры Термодинамическое равновесие Стационарное состояние Взаимодействие с окружающей средой Отсутствие обмена с окружающей средой веществом и энергией Непрерывный обмен с окружающей средой веществом и энергией Энтропия системы постоянная и соответствует максимально возможному в данных условиях значению Энтропия системы постоянна, но не равна максимально возможному в данных условиях значению Градиенты, потоки Полное отсутствие в системе какихлибо градиентов Наличие постоянных по величине градиентов Энергия Не требуется затраты свободной энергии Необходимы постоянные затраты энергии Работа Система нереакционноспособна и не совершает работу против внешних сил В системе совершаются необратимые реакции, ее работоспособность постоянна и не равна нулю
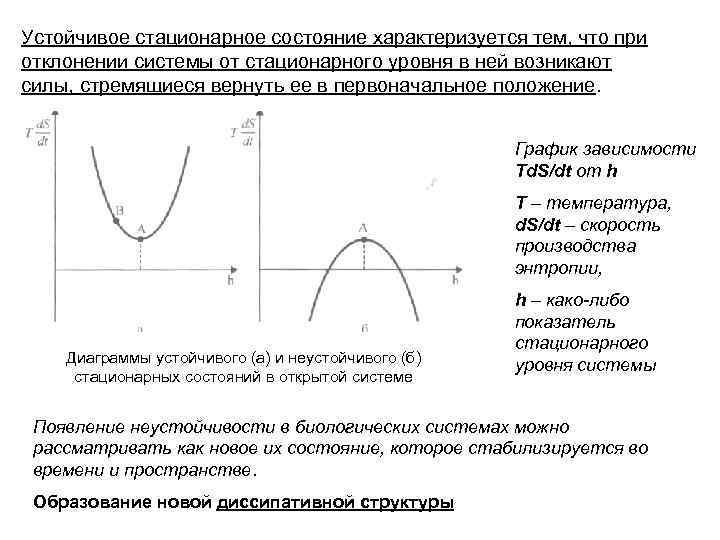
Устойчивое стационарное состояние характеризуется тем, что при отклонении системы от стационарного уровня в ней возникают силы, стремящиеся вернуть ее в первоначальное положение. График зависимости Тd. S/dt от h Т – температура, d. S/dt – скорость производства энтропии, Диаграммы устойчивого (а) и неустойчивого (б) стационарных состояний в открытой системе h – како-либо показатель стационарного уровня системы Появление неустойчивости в биологических системах можно рассматривать как новое их состояние, которое стабилизируется во времени и пространстве. Образование новой диссипативной структуры

Теорема Пригожин Илья Романович 25 января 1917 г. – 28 мая 2003 г. Нобелевская премия по химии, 1977 г. ( «за работы по термодинамике необратимых процессов, особенно за теорию диссипативных структур» ) « В стационарном состоянии при фиксированных внешних параметрах скорость продукции энтропии в системе постоянна во времени и минимальна по величине»

• Условия стационарного процесса оказываются эквивалентными условиям минимума прироста энтропии. • Живые организмы поставлены природой в весьма выгодные условия, с точки зрения энергообеспечения: поддержание гомеостаза требует минимального потребления энергии. • Принцип минимума прироста энтропии представляет собой критерий эволюции открытых систем.

Эволюция открытой системы стремящейся к стационарному состоянию или равновесному состоянию описывается неравенством: dβ / dt ≤ 0, β= T/V * di. S/dt β – удельная диссипативная функция системы Диссипация энергии системы – это переход части энергии упорядоченного процесса в энергию неупорядоченного процесса, в конечном счете – тепловую. Если система выходит из стационарного состояния самопроизвольно, происходит увеличение энтропии. В результате в системе возникают процессы, которые стремятся возвратить её в стационарное состояние. Если изменения не превышают определенных пределов, то стационарное состояние может восстановится, т. е. небольшие отклонения от стационарного состояния не ведут к необратимым изменениям.
биофизика 004-005.ppt