 Термодинамика и теплопередача Лекция 2
Термодинамика и теплопередача Лекция 2
 Внутренняя энергия: l l Кинетическая энергия Потенциальная энергия Энергия электронных оболочек атомов Внутриядерная энергия Две последние в большинстве теплоэнергетических процессах остаются неизменными.
Внутренняя энергия: l l Кинетическая энергия Потенциальная энергия Энергия электронных оболочек атомов Внутриядерная энергия Две последние в большинстве теплоэнергетических процессах остаются неизменными.
![Внутренняя энергия, U [Дж] энергия хаотического движения молекул и атомов, включающую энергию поступательного, вращательного Внутренняя энергия, U [Дж] энергия хаотического движения молекул и атомов, включающую энергию поступательного, вращательного](https://present5.com/presentation/307036297_445379576/image-3.jpg) Внутренняя энергия, U [Дж] энергия хаотического движения молекул и атомов, включающую энергию поступательного, вращательного и колебательного движений как молекулярного, так и внутримолекулярного, а так же потенциальную энергию сил взаимодействия между молекулами
Внутренняя энергия, U [Дж] энергия хаотического движения молекул и атомов, включающую энергию поступательного, вращательного и колебательного движений как молекулярного, так и внутримолекулярного, а так же потенциальную энергию сил взаимодействия между молекулами
![Удельная внутренняя энергия, u [Дж/кг] Внутренняя энергия функция состояния тела и может быть представлена Удельная внутренняя энергия, u [Дж/кг] Внутренняя энергия функция состояния тела и может быть представлена](https://present5.com/presentation/307036297_445379576/image-4.jpg) Удельная внутренняя энергия, u [Дж/кг] Внутренняя энергия функция состояния тела и может быть представлена в виде функции двух любых независимых параметров: Изменение внутренней энергии:
Удельная внутренняя энергия, u [Дж/кг] Внутренняя энергия функция состояния тела и может быть представлена в виде функции двух любых независимых параметров: Изменение внутренней энергии:
 Теплота l l l Теплота, Q – представляет собой переданное от одного тела к другому определенное количество энергии хаотического молекулярного и внутримолекулярного движения + Q – подводимая теплота - Q – отводимая теплота
Теплота l l l Теплота, Q – представляет собой переданное от одного тела к другому определенное количество энергии хаотического молекулярного и внутримолекулярного движения + Q – подводимая теплота - Q – отводимая теплота
![Работа l Работа, L [Дж] – в термодинамике называется процесс превращения одного вида энергии Работа l Работа, L [Дж] – в термодинамике называется процесс превращения одного вида энергии](https://present5.com/presentation/307036297_445379576/image-6.jpg) Работа l Работа, L [Дж] – в термодинамике называется процесс превращения одного вида энергии в другой, при котором энергия одного вида уменьшается, а энергия другого вида увеличивается.
Работа l Работа, L [Дж] – в термодинамике называется процесс превращения одного вида энергии в другой, при котором энергия одного вида уменьшается, а энергия другого вида увеличивается.
 Работа расширения l l l Масса М Объем V Площадь поверхности F Элементарный элемент оболочки d. F Сила pd. F Элементарная работа pd. Fdn
Работа расширения l l l Масса М Объем V Площадь поверхности F Элементарный элемент оболочки d. F Сила pd. F Элементарная работа pd. Fdn
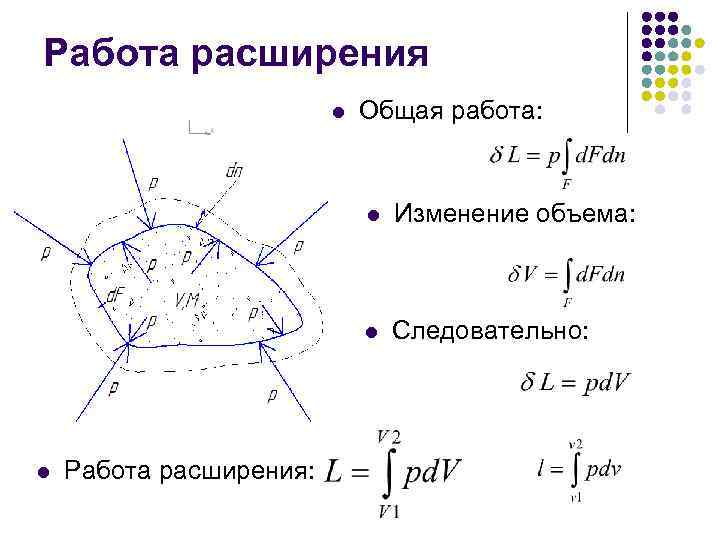 Работа расширения l Общая работа: l l l Работа расширения: Изменение объема: Следовательно:
Работа расширения l Общая работа: l l l Работа расширения: Изменение объема: Следовательно:
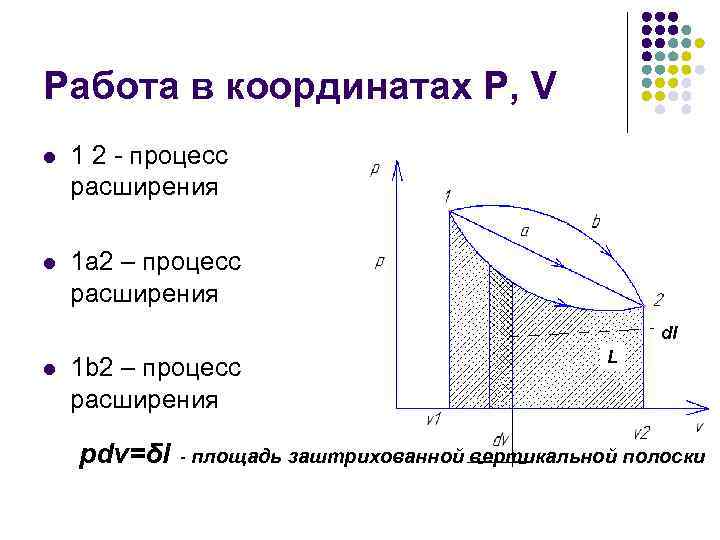 Работа в координатах Р, V l 1 2 - процесс расширения l 1 а 2 – процесс расширения dl l 1 b 2 – процесс расширения pdv=δl L - площадь заштрихованной вертикальной полоски
Работа в координатах Р, V l 1 2 - процесс расширения l 1 а 2 – процесс расширения dl l 1 b 2 – процесс расширения pdv=δl L - площадь заштрихованной вертикальной полоски
![Энтальпия l l Энтальпия, Н [Дж] - термодинамический потенциал, характеризующий состояние термодинамической системы. Энергия, Энтальпия l l Энтальпия, Н [Дж] - термодинамический потенциал, характеризующий состояние термодинамической системы. Энергия,](https://present5.com/presentation/307036297_445379576/image-10.jpg) Энтальпия l l Энтальпия, Н [Дж] - термодинамический потенциал, характеризующий состояние термодинамической системы. Энергия, которая доступна для преобразования в теплоту при постоянном давлении. Энтальпия – функция состояния:
Энтальпия l l Энтальпия, Н [Дж] - термодинамический потенциал, характеризующий состояние термодинамической системы. Энергия, которая доступна для преобразования в теплоту при постоянном давлении. Энтальпия – функция состояния:
![Энтальпия l Удельная энтальпия – энтальпия системы содержащий 1 кг вещества h [Дж/кг]: Изменение Энтальпия l Удельная энтальпия – энтальпия системы содержащий 1 кг вещества h [Дж/кг]: Изменение](https://present5.com/presentation/307036297_445379576/image-11.jpg) Энтальпия l Удельная энтальпия – энтальпия системы содержащий 1 кг вещества h [Дж/кг]: Изменение энтальпии в любом процессе определяется только начальным и конечным состояниями тела и не зависит от характера процесса
Энтальпия l Удельная энтальпия – энтальпия системы содержащий 1 кг вещества h [Дж/кг]: Изменение энтальпии в любом процессе определяется только начальным и конечным состояниями тела и не зависит от характера процесса
 Уравнение первого начала термодинамики: С учетом очевидного соотношения: Может быть записано в виде: или Если давление системы сохраняется неизменным: или
Уравнение первого начала термодинамики: С учетом очевидного соотношения: Может быть записано в виде: или Если давление системы сохраняется неизменным: или
![Теплоемкость l Теплоемкость, с [Дж/кг*град] – количество тепла, которое нужно повести единице тела для Теплоемкость l Теплоемкость, с [Дж/кг*град] – количество тепла, которое нужно повести единице тела для](https://present5.com/presentation/307036297_445379576/image-13.jpg) Теплоемкость l Теплоемкость, с [Дж/кг*град] – количество тепла, которое нужно повести единице тела для повышения его температуры на 10 С в данном процессе.
Теплоемкость l Теплоемкость, с [Дж/кг*град] – количество тепла, которое нужно повести единице тела для повышения его температуры на 10 С в данном процессе.
 Теплоемкость в зависимости от единицы количества вещества: l l l Удельная массовая теплоемкость, с [Дж/кг*К]; Удельная объемная теплоемкость, с/ [Дж/м 3*К]; Удельная мольная теплоемкость, см, [Дж/кмоль*К]
Теплоемкость в зависимости от единицы количества вещества: l l l Удельная массовая теплоемкость, с [Дж/кг*К]; Удельная объемная теплоемкость, с/ [Дж/м 3*К]; Удельная мольная теплоемкость, см, [Дж/кмоль*К]
 Массовая теплоемкость l Изобарная теплоемкость: l Изохорная теплоемкость: l Отношение теплоемкостей: l Уравнение Майера:
Массовая теплоемкость l Изобарная теплоемкость: l Изохорная теплоемкость: l Отношение теплоемкостей: l Уравнение Майера:
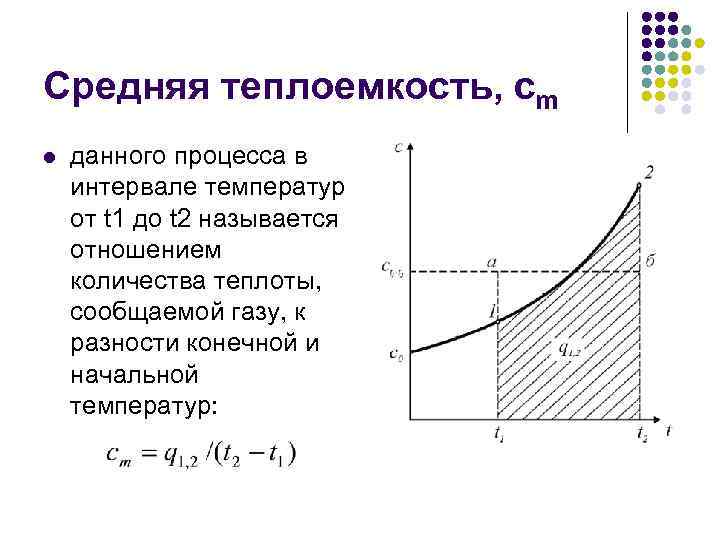 Средняя теплоемкость, сm l данного процесса в интервале температур от t 1 до t 2 называется отношением количества теплоты, сообщаемой газу, к разности конечной и начальной температур:
Средняя теплоемкость, сm l данного процесса в интервале температур от t 1 до t 2 называется отношением количества теплоты, сообщаемой газу, к разности конечной и начальной температур:
 Истинная теплоемкость l Истинная теплоемкость соответствует бесконечно малому интервалу температур.
Истинная теплоемкость l Истинная теплоемкость соответствует бесконечно малому интервалу температур.