ТЕРМОДИНАМИКА БИОЛОГИЧЕСКИХ СИСТЕМ.ppt
- Количество слайдов: 103

ТЕРМОДИНАМИКА БИОЛОГИЧЕСКИХ СИСТЕМ

План лекции n n n n n 1. Введение 2. Основные термины термодинамики 3. Свободная и связанная энергии 4. Первый закон термодинамики 5. Применение первого начала термодинамики к живым системам 6. Закон Гесса 7. Второй закон термодинамики 8. Второй закон термодинамики и живой организм 9. Стационарное состояние 10. Теорема Пригожина

1. Введение n Жизненные процессы при всём своём многообразии имеют и общие черты – любой из них требует затрат энергии. Поэтому важным направлением биофизических исследований является термодинамика – наука о преобразовании энергии в системах.

n Основная цель термодинамики – изучение трансформации энергии при переходе системы из одного энергетического состояния в другое.

n Термодинамические методы в основе своей являются методами статистическими. Нельзя представить себе, например, температуру или давление одной какой-либо молекулы, потому что эти термодинамические параметры отражают взаимодействие огромного количества молекул, образующих макросистему.

n . Термодинамика не дает ответа на вопрос – какова природа или механизм того или иного явления. Она может только показать, возможно ли протекание данного процесса, реален ли он с точки зрения баланса энергии и энтропии

2. Осносные термины термодинамики n С учетом стохастической природы основных законов термодинамики вводится понятие системы. n Система – это совокупность материальных объектов (тел), ограниченных каким-либо образом от окружающей среды.

n. В зависимости от характера взаимодействия с окружающей средой термодинамические системы делятся на три типа:

n 1) изолированная – система, которая не обменивается с окружающей средой ни веществом, ни энергией;

n 2) замкнутая – система, которая может обмениваться с окружающей средой лишь энергией и не может обмениваться веществом;

n 3) открытая – система, которая обменивается с окружающей средой и энергией и веществом

n Живые организмы являются открытыми термодинамическими системами.

n Состояние любой термодинамической системы характеризуется некоторыми параметрами

n Одни из них не зависят от массы или числа частиц в системе (иначе говоря, от размеров системы), получили название интенсивные термодинамические параметры (давление Р, температура Т и т. п. ).

n Другие пропорциональны этим параметрам ( m, V), называются экстенсивными (энергия W или U, энтропия S, свободная энергия G, F).

n Изменение параметров термодинамической системы называется термодинамическим процессом.

Энергия системы n n Энергию системы (W) можно представить как совокупность двух частей: зависящую от движения и положения системы как целого (Wц) и не зависящую от этих факторов (U) W = Wц + U

n Вторую составляющую этой совокупности U называют внутренней энергией системы. Она включает энергию теплового движения частиц, а также химическую и ядерную. Энергию поступательного, колебательного и вращательного движения молекул, внутримолекулярного взаимодействия и колебания атомов, энергию вращения электронов и т. д. .

3. Свободная и связанная энергии n Внутренняя энергия тела в значительной мере связана с неупорядоченным тепловым движением молекул. В то же время совершение работы всегда требует упорядоченного переноса вещества, т. е. (направленного) движения. Поэтому невозможно всю внутреннюю энергию тела использовать для совершения работы

n . Та часть внутренней энергии системы, которую в принципе можно использовать для совершения работы, называется свободной энергией (G). Остальную часть внутренней энергии системы, которую даже в принципе нельзя превратить в работу называют связанной энергией (Wсв). n n U = G + Wсв

n Те процессы, в которых n n A=∆G называются обратимыми; если направить такой процесс обратно, то, затратив работу А , можно полностью вернуть систему в исходное состояние

n Таких процессов в природе не существует – все реальные процессы необратимы. Иными словами, свободная энергия системы не может быть полностью преобразована в работу. При таком преобразовании часть свободной энергии обязательно превратится в тепло

n В биологии нас интересует в первую очередь работа, совершенная системой. Поэтому важно знать не столько полную внутреннюю энергию системы, сколько её свободную энергию.

n Характеризуя это явление, говорят о диссипации (рассеянии) свободной энергии. Следовательно n n А ≤ ∆ G, т. е. работа не может быть больше свободной энергии.

4. Первое начало термодинамики n Термодинамика базируется на первом и втором началах (законах).

n Первое начало термодинамики представляет собой одну из форм записи закона сохранения энергии. Оно было сформулировано независимо друг от друга Ю. Р. Майером (1842 г. ), Д. П. Джоулем (1843 г. ) и Г. Л. Гельмгольцем (1847 г. ). Двое из них (Майер и Гельмгольц) были врачами и закладывали основы термодинамики, рассматривая преобразования энергии как в живой, так и в неживой природе.

n Смысл первого начала термодинамики сводится к тому, что изменение внутренней энергии системы может произойти только при обмене энергией с окружающей средой.

n Энергетический обмен между системой и средой осуществляется двумя способами – посредством передачи тепла и путём совершения работы. ∆U = Q -A ; Q = ∆U + A Этот вид формул и выражает I начало термодинамики. n Q – количество теплоты, переданное системе; n ∆ U – изменение внутренней энергии системы; n А – работа, совершаемая системой.

n n В живых организмах формы совершения работы очень разнообразны (Аi). Остановимся на способах совершения работы:

n n механическая работа : d. A(l) =Fd. L, где : F – сила, d. L – перемещение;

n n работа расширения газа : d. A(V) =Pd. V, где : P – давление, d. V – изменение объёма;

n n работа переноса заряда, при разности потенциалов φ: d. A(q) = φdq, где : φ - потенциал, dq – электрический заряд;

X датчик XX f(x ) n команда задание Σ=f i i анализатор ---------- У. О. Y=φ(f ) Канал прямой связи канал обратной связи результат И. О.

n работа переноса вещества за счёт осмотического давления: d. A(C) = pосмdc, n n где pосм -осмотическое давление, nс – концентрация вещества;

n работа, совершаемая при химической реакции: d A ( ν) = μ d ν , n где: μ - химический потенциал , n ν - число молей вещества, вступающих в реакцию;

n n n Все эти формулы имеют сходную структуру d. A(x) =Xdx ИЛИ A=∫Xdx где: х – величина, характеризующая перенос ( L, V, q, c, ν ), а Х – сила, характеризующая причину переноса (F, p, pосм, φ, μ ).

n Используя принятые обозначения, основной закон термодинамики можно записать в виде Q = ∆ U + Σ Аi ИЛИ Q = ∆U + Σ Xidxi n n То есть количество тепла (Q), полученное системой, определяется изменениями внутренней энергии ( U), а также суммой всех видов работы (Σ Аi ), совершаемой системой. Эту формулу можно считать наиболее общим выражением первого начала термодинамики

5. Применение первого начала термодинамики к живым системам ( организмам ) n Различие термодинамических процессов в живой и неживой системах

n Классическая форма первого начала термодинамики отображает запросы теплотехники, интенсивно развивающиеся в эпоху открытия этого основного закона. Поэтому эта форма не вполне удобна для биологии, т. к. не отображает сути термодинамических процессов, происходящих в живых системах

n n В отличие от тепловых машин, живые организмы производят работу не за счёт тепловой энергии, а посредством использования химической энергии пищевых продуктов, усвоенных ими (Wпищи).

n n n Поэтому для живой системы ∆ U = WПИЩИ– Q – A (перед Q стоит знак «–» , т. к. биологическая система отдаёт тепло окружающей среде).

n Организм гомойотермных животных имеет постоянную температуру, химический состав его в среднем не изменяется, поэтому U=const и U=0. Учитывая это, предыдущую формулу можно записать так: 0 = Wпищи – Q – A или Wпищи = Q + A, если при этом помнить, что совершаемая работа (А) и теплообмен (Q) могут иметь разнообразные формы, то получаем, что Wпищи =ΣQi + ΣAi

n n Wпищи =ΣQi + ΣAi Эта форма наиболее точно отображает первое начало термодинамики для биологических систем.

n термодинамические n процессы в тепловой машине можно представить схемой (источник энергии на Земле – Солнце) неживая система : n n Wc Wтоплива ΣQi U+ΣAi в биологическ. ОЙ ( ЖИВАЯ систем. А ) : Wc WПИЩИ ΣQi + U+ ΣAi

n В живой системе между Wc и последним значением A отсутствует промежуточное звено в форме тепловой энергии, следовательно, КПД живой системы выше, чем у неживой и достигает значения 20 -60 %.

n Таким образом, обмен веществ в организме сопровождается процессами превращения энергии. Обмен энергии и вещества представляет собой единый процесс, лежащий в основе жизнедеятельности. Живой организм расходует химическую энергию всех рабочих процессов, выполняемых в организме, и выделяет избыточное количество тепла (тепловой эффект).

6. Закон Гесса n Следствием I закона термодинамики является з-н Гесса. Тепловой эффект химического процесса не зависит от промежуточных стадий и определяется лишь начальным и конечным состояниями термодинамической системы.
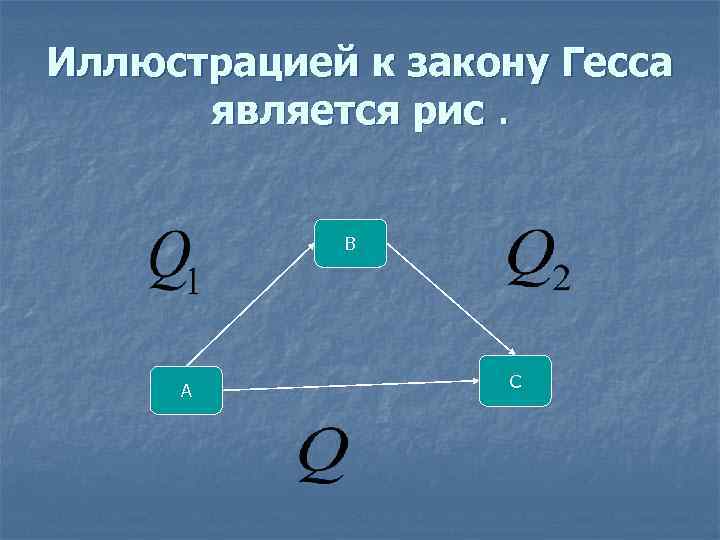
Иллюстрацией к закону Гесса является рис. B A C

Q C + O 2 = CO 2 + 97 ккал/моль n Q 2 CO +1/2 O 2 = CO 2 +68 ккал/моль n Произведём вычисления Q – Q 2 = Q 1 , Q 1 = (97 - 68)=29 ккал/моль n то есть C + 1/2 O 2 = CO + 29 ккал/моль , n величина теплового эффекта этой реакции равна 29 ккал/моль.

n Закон Гесса позволяет вычислить тепловые эффекты таких реакций, которые совсем не протекают в условиях опыта, а также таких, для которых невозможно измерить тепловой эффект.

Биохимические реакции организма очень сложные и имеют много промежуточных стадий, которые не всегда известны. Однако, на основании закона Гесса, зная начальный и конечный продукты реакции, можно рассчитать тепловой эффект сложной биохимической реакции

n Закон Гесса используется также для вычисления калорийности пищевых продуктов. Хотя питательные вещества претерпевают в организме сложные превращения, энергетический эффект их равен тепловому эффекту непосредственного сжигания этого продукта в калориметрической бомбе, поскольку в обоих случаях начальные и конечные состояния реагирующих веществ одинаковы (т. е. , грубо говоря, можно определить калориметрическую стоимость пищи). Энергозатраты организма определяются с помощью прямой или непрямой калориметрии

7. Второй закон термодинамики n Первый закон термодинамики позволяет определить количественные соотношения между различными формами энергии, которые принимают участие в данном процессе. Но этот закон ничего не говорит о возможности протекания данного процесса и о направлении, в котором он будет развиваться. Ответ на этот вопрос дает второе начало термодинамики.

n Мы уже знаем, что тепловая энергия, образуясь в организме, представляет конкретную форму связанной энергии биологических систем, т. к. в условиях жизнедеятельности она не может быть преобразована ни в одну из форм работы, совершаемой организмами. Чем же определяется эта энергия? .

n Вспомним, что Wсвяз. зависит от степени неупорядоченности молекулярного движения, а ее количественной мерой является температура, поэтому Wсвяз. пропорциональна Т. Однако величина связанной энергии в разных системах, имеющих одинаковую температуру, не всегда одинакова. Следовательно, степень неупорядоченности молекулярного движения зависит не только от температуры, но и еще от каких-то свойств системы

n n Эти свойства Клаузиус (1865) выразил в виде коэффициента, который однозначно определяет значение Wсвяз и Т. Коэффициент принято обозначать буквой S и называть ЭНТРОПИЕЙ. С вводом энтропии зависимость связанной энергии системы от ее температуры выглядит так : Wсвяз= ST откуда S=Wсвяз/T Размерность энтропии – [Дж/К].

n Энтропия – это физическая величина, характеризующая значение связанной энергии данной системы, приходящаяся на единицу температуры (1 К).

n Говоря о запасе энергии в какойлибо системе, интересуются прежде всего тем, какую работу она может совершить. Ясно, что при этом следует учитывать не полную, а только свободную энергию.

n Пищевые продукты важны для человека потому, что он получает при их усвоении свободную энергию для совершения работы.

n В ванне горячей воды содержится больший запас энергии, чем в килограмме хлеба, но за счет нее человек, погруженный в ванну, не способен совершить работу, т. к. почти вся энергия является связанной. Следовательно, энергия в различных формах имеет разную практическую ценность, которая тем выше, чем большую часть этой энергии можно преобразовать в работу, т. е. чем меньше доля связанной энергии, мерой которой служит энтропия.

n Следовательно, чем ниже энтропия системы, тем выше ценность свойственной ей внутренней энергии. Мы помним, что превращение свободной энергии в связанную называется диссипацией (рассеянием) энергии.

n n Необходимо понять, что такими превращениями сопровождаются любые преобразования более ценной формы энергии в менее ценную. Например, преобразования химической энергии, заключенной в биологических макромолекулах, в тепловую есть диссипация энергии.

n n В природе (в биофизике и биохимии) часто трудно предвидеть, как будут происходить те или иные явления в интересующих нас условиях. Поэтому необходим алгоритм, который дал бы возможность достоверно предсказать направление процессов в любом случае. Термодинамика позволяет сформулировать такой алгоритм, – он получил название второго начала

n Проще всего он формулируется для изолированных систем: «в изолированной системе общее изменение энтропии всегда положительно» n n Sобщ > 0

n Рассмотрим простой пример: пусть изолированная система состоит из двух тел « 1» и « 2» , обладающих неодинаковой температурой Т 1>Т 2. Тело « 1» отдает некоторое количество тепла Q, а тело “ 2” его получит (т. к. система изолирована, то никаких потерь тепла нет). Изменение энтропии « 1 -го» тела составит S 1= - Q/T 1, а для « 2 -го» тела S 2= + Q/T 2. Общее изменение энтропии Sобщ = S 1 + S 2, Sобщ= - Q/T 1 + Q/T 2= Q(1/T 2 – 1/T 1), т. к. Т 1>Т 2, то выражение в скобках положительно, и Sобщ > 0. Такой процесс соответствует второму началу термодинамики и происходит самопроизвольно.

5. Применение первого начала термодинамики к живым системам ( организмам ) n Различие термодинамических процессов в живой и неживой системах

n n n Итак: энтропия – это функция состояния системы; S – это физическая величина, количественно характеризующая особенности молекулярного строения системы, от которых зависят энергетические преобразования в ней, в частности направление; S – это мера неупорядоченности системы.

n n n Эту связь энтропии с молекулярным строением системы первым объяснил Л. Больцман в 1887 году. Он установил статистический смысл энтропии. Согласно Больцману (высокая упорядоченность имеет относительно низкую вероятность)

n n S = k ln W , n где k – постоянная Больцмана n n n -23 k=R/Na= 1, 37*10 Дж/К, W – термодинамическая вероятность состояния системы. S = k ln W , n где k – постоянная Больцмана k=R/Na= 1, 37*10 -23 Дж/К, W – термодинамическая вероятность состояния системы.

n n Термодинамической вероятностью называется число способов размещения частиц, т. е. число микросостояний, реализующих данное макросостояние. Из формулы Больцмана видно, что при повышении термодинамической вероятности возрастает и энтропия.

n n n Значит, всякая система, если на нее не действует внешняя сила, будет переходить из менее вероятного в более вероятное состояние (из порядка в хаос), т. е. направление всех реальных процессов в изолированной системе соответствует повышению термодинамической вероятности, а следовательно энтропия d. S=d. Q/T≥ 0 в необратимых процессах >0, в обратимых = 0.

n Итак: в результате самопроизвольности процессов любая изолированная система стремится достичь состояния, обеспечивающего наибольший беспорядок, который обладает наибольшей вероятностью, т. е. состояния с максимальным значением энтропии S max.

n Между S и W существует явная функциональная зависимость, то есть S=f(W). Найдём вид этой функции:

n n Допустим имеются две термодинамических системы. Энтропия и термодинамическая вероятность первой – S 1 и W 1 Энтропия и термодинамическая вероятность второй – S 2 и W 2 Вероятность и энтропия сложной системы, состоящей из этих двух систем – Sи. W

n n Общая энтропия равна S=S 1+S 2 , поскольку S=f(W), запишем это равенство таким образом f(W)=f(W 1)+f(W 2).

n Общая вероятность сложной системы, в соответствии с теорией вероятности, равна произведению вероятностей, n то есть W=W 1 W 2, n а значит f(W 1 W 2)= f(W 1)+f(W 2). n

n n Такому равенству удовлетворяет логарифмическая функция ln(W 1 W 2)=ln(W 1)+ln(W 2) Таким образом и окончательно S ln. W S=kln. W.

8. Второй закон термодинамики и живой организм. n В течение длительного времени считали, что второй закон термодинамики неприменим к биологическим системам, т. к. согласно этому закону в системах могут происходить лишь процессы, связанные с рассеянием энергии

n Живые же организмы способны накапливать богатые энергией соединения, т. е. создавать более упорядоченную структуру и энтропию не увеличивать. Это несоответствие объясняется тем, что закон классической термодинамики справедлив для изолированных систем, а живые организмы являются открытыми системами. Живые структуры непрерывно разрушаются и вновь восстанавливаются, их постоянство заключается только в том, что процессы распада и обновления точно компенсируют друга. Состояние, при котором распад уравновешивается синтезом, называется динамическим равновесным состоянием.

n С точки зрения термодинамики жизнь – невероятное состояние (феномен). И опять здесь нет противоречия, т. к. организм неизолированная система! Если изолировать биологический объект, лишить его пищи, воздуха, то энтропия такой системы возросла бы, и все закончилось смертью.

n В процессе прекращения связи системы с окружающей средой резко возрастает неупорядоченность системы и увеличивается энтропия. Таким образом, обмен веществ позволяет сохранить или даже повысить упорядоченность организма и, соответственно, сохранять или уменьшать его энтропию.

n n n . Поэтому общее изменение системы можно представить в виде двух составляющих: d. S=d. Si+ d. Se, где d. Si – изменение энтропии вследствие необратимости процессов в биохимической системе; d. Se – изменение энтропии, обусловленное взаимодействием биологической системы с окружающей средой (т. е. получение продуктов питания и выведения продуктов жизнедеятельности).

n n Если внутри биологических систем протекают обратимые процессы, то они не сопровождаются возникновением энтропии d. Si=0. Для всех случаев необратимых изменений d. S>0.

n n В изолированной системе обмен со средой не происходит, то есть d. Se=0. И потому d. S=d. Si>0, что соответствует классической формулировке второго закона термодинамики для изолированных систем.

n n В открытых системах в разные промежутки времени изменение полной энтропии может быть различным, т. к. постоянно изменяются величины d. Si и d. Se. В связи с этим в термодинамике открытых систем был введен новый параметр – время …

n n и тогда d. S/dt=d. Si/dt+d. Se/dt, член d. Si/dt – называется продукция энтропии, а d. Se/dt – потоком энтропии. Это уравнение является математическим выражением второго закона термодинамики для живых организмов

n n Он гласит : «Скорость изменения энтропии организме d. S/dt равна алгебраической сумме скорости возникновения энтропии внутри системы (продукция энтропии d. Si/dt) и скорости обмена энтропии между организмом и окружающей средой (поток энтропии d. Se/dt)» .

9. Стационарное состояние n Стационарным состоянием называется такое состояние системы, при котором параметры системы не меняются со временем на фоне протекающих процессов обмена с окружающей средой.

n n В таком состоянии и энтропия S постоянна, а следовательно d. S=d. Si+d. Se=0, n n n то есть d. Si=-d. Se и d. Si/dt=-d. Se/dt является уравнением стационарного состояния

n Сходство стационарного состояния и термодинамического равновесия заключается в том, что параметры системы не меняются во времени как в одном, так и в другом случае.

n Но постоянство параметров при стационарном состоянии достигается не в результате отсутствия всяких направленных процессов, как при термодинамическом равновесии, а в результате того, что процессы протекают, но скорость направления этих процессов постоянна и взаимно уравновешивается

n. В состоянии равновесия в системе прекращаются все процессы, кроме теплового движения молекул; соответственно, выравниваются все градиенты

n. В стационарном состоянии идут химические реакции, диффузии, перенос ионов и др. процессы, но они так сбалансированы, что состояние системы в целом не изменяется

n. Способность сохранять постоянство внутренней среды называется гомеостазисом или просто гомеостазом

n Гомеостаз представляет собой стационарное состояние организма высших животных.

n Характерным свойством живого организма помимо постоянства параметров являются также совершенно определённые реакции на внешнее воздействие, которые выводят организм из стационарного состояния.

n Такие явления, как возбуждение, мышечное сокращение, генерация нервного импульса и другие, являются примерами переходных процессов между стационарными уровнями. При этом все уровни лежат в пределах биологических норм.

n Если система выведена из стационарного состояния, то к новому стационарному состоянию она может переходить по-разному. Можно выделить три основных типа переходов.
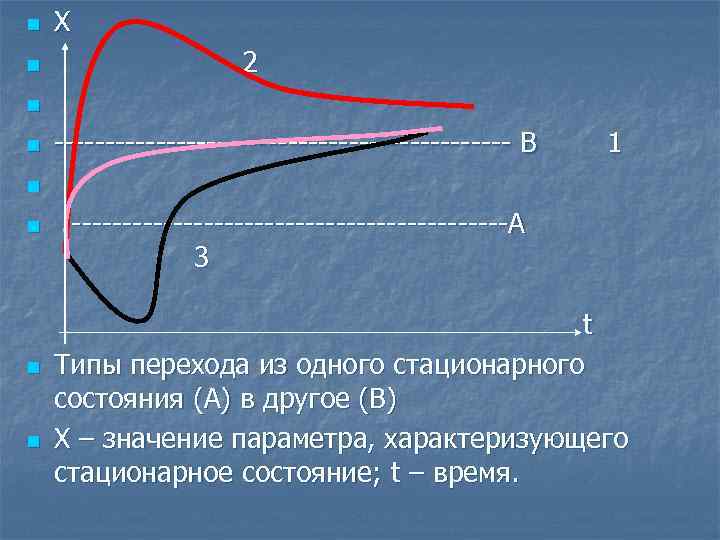
n n Х 2 n n ----------------------- B 1 n n ----------------------А 3 t Типы перехода из одного стационарного состояния (А) в другое (В) Х – значение параметра, характеризующего стационарное состояние; t – время.

n Кривая 1 изображает простой экспоненциальный переход от одного уровня стационарного состояния к другому. Такой переход характерен например для частоты дыхания и сердцебиения при равномерном изменении интенсивности физической работы (нагрузки)

n Кривая 2 называется кривой с избыточными отклонениями (овершут), когда промежуточный уровень выше конечного. Такая кривая может характеризовать, например, изменения артериального давления крови человека при резком увеличении интенсивности физической работы

n Кривая 3 отражает такие изменения, когда уровень сначала понижается, а затем возрастает до конечного стационарного состояния. Этот тип называют «ложным стартом»

n Приведённые кривые отражают переходные процессы только в первом приближении. Строго говоря, и переходные и стационарные процессы имеют колебательный характер.
ТЕРМОДИНАМИКА БИОЛОГИЧЕСКИХ СИСТЕМ.ppt