ТЕРМОДИНАМИКА 1 Пусть газ заключен
















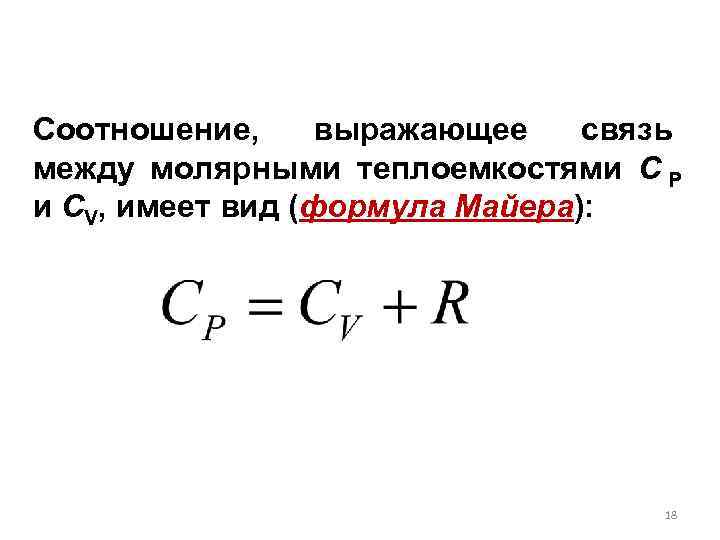






































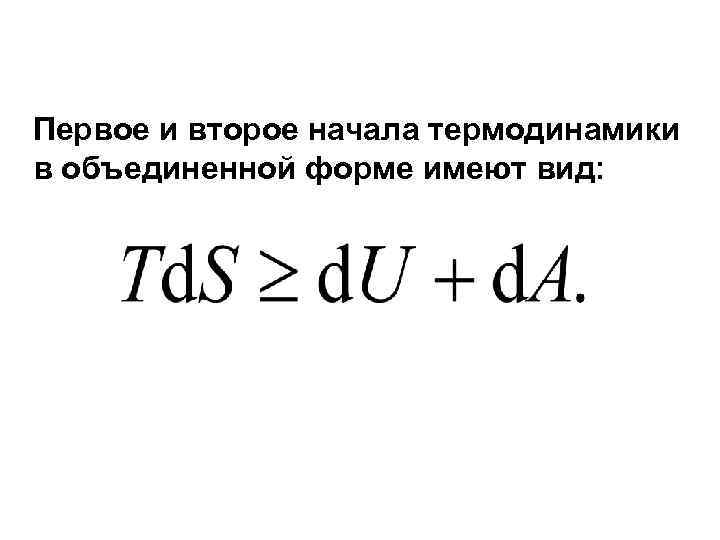








 ТЕРМОДИНАМИКА 1
ТЕРМОДИНАМИКА 1
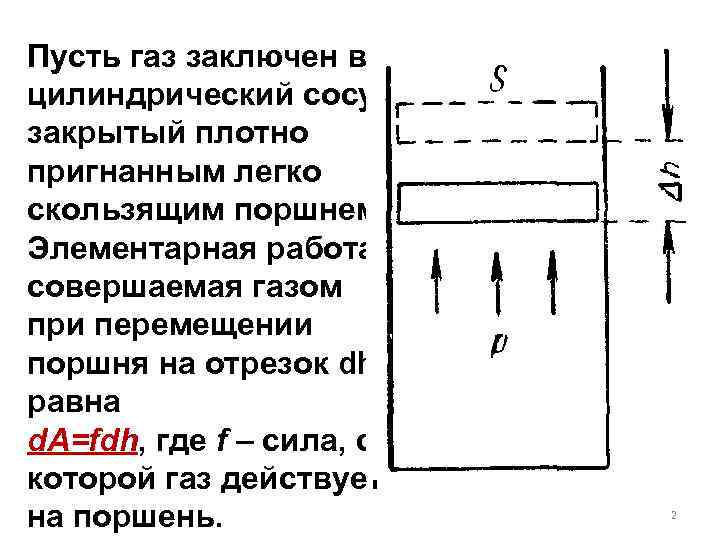
 Пусть газ заключен в цилиндрический сосуд, закрытый плотно пригнанным легко скользящим поршнем. Элементарная работа, совершаемая газом при перемещении поршня на отрезок dh, равна d. A=fdh, где f – сила, с которой газ действует на поршень. 2
Пусть газ заключен в цилиндрический сосуд, закрытый плотно пригнанным легко скользящим поршнем. Элементарная работа, совершаемая газом при перемещении поршня на отрезок dh, равна d. A=fdh, где f – сила, с которой газ действует на поршень. 2
 Заменяя эту силу произведением давления газа P на площадь поршня S, получаем: Sdh представляет собой приращение объема газа d. V. Поэтому выражение для элементарной работы можно записать следующим образом: 3
Заменяя эту силу произведением давления газа P на площадь поршня S, получаем: Sdh представляет собой приращение объема газа d. V. Поэтому выражение для элементарной работы можно записать следующим образом: 3
 При сжатии газа направления перемещения dh и силы f , с которой газ действует на поршень, противоположны, вследствие чего элементарная работа d. A будет отрицательна. Приращение объема d. V в этом случае также будет отрицательным. Если при изменении объема давление не остается постоянным, работа должна вычисляться путем интегрирования: 4
При сжатии газа направления перемещения dh и силы f , с которой газ действует на поршень, противоположны, вследствие чего элементарная работа d. A будет отрицательна. Приращение объема d. V в этом случае также будет отрицательным. Если при изменении объема давление не остается постоянным, работа должна вычисляться путем интегрирования: 4
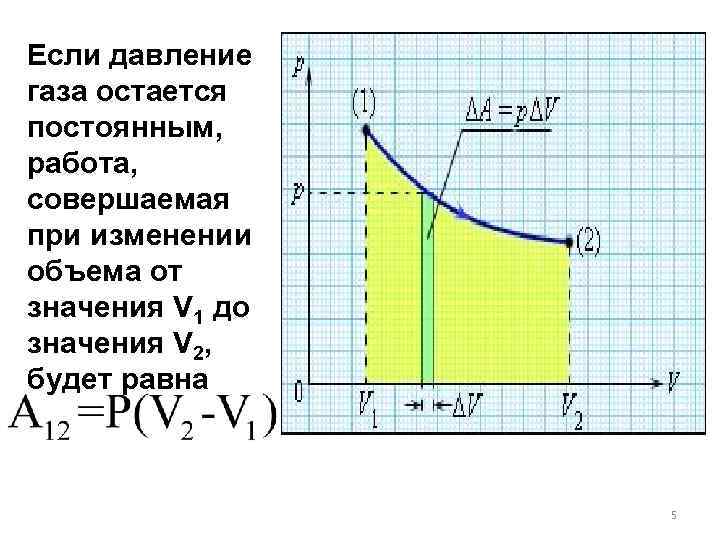
 Если давление газа остается постоянным, работа, совершаемая при изменении объема от значения V 1 до значения V 2, будет равна 5
Если давление газа остается постоянным, работа, совершаемая при изменении объема от значения V 1 до значения V 2, будет равна 5
 Первое начало термодинамики • Формулировка первого начала термодинамики: Количество тепла, сообщённое системе, идёт на приращение внутренней энергии системы и совершение системой работы над внешними телами Q= U+A • Здесь А>0 если система совершает работу над внешними телами • Приращение энергии U находится как разность энергий конечного и начального состояний U 2 -U 1 • Q>0 если тепло сообщается системе 6
Первое начало термодинамики • Формулировка первого начала термодинамики: Количество тепла, сообщённое системе, идёт на приращение внутренней энергии системы и совершение системой работы над внешними телами Q= U+A • Здесь А>0 если система совершает работу над внешними телами • Приращение энергии U находится как разность энергий конечного и начального состояний U 2 -U 1 • Q>0 если тепло сообщается системе 6
 • Другая формулировка первого начала термодинамики: Невозможен вечный двигатель (перпетуум мобиле) первого рода, т. е. такой периодически действующий двигатель, который совершал бы работу в большем количестве, чем получаемая им извне энергия 7
• Другая формулировка первого начала термодинамики: Невозможен вечный двигатель (перпетуум мобиле) первого рода, т. е. такой периодически действующий двигатель, который совершал бы работу в большем количестве, чем получаемая им извне энергия 7
 Первое начало Т. Д. выражает закон сохранения энергии применительно к тепловым процессам Первым к формулировке закона сохранения энергии пришел Роберт Майер Кроме Майера вопросами превращения разных форм энергии друг в друга занимались Джеймс П. Джоуль, открывший в 1843 г. эквивалентность теплоты и механической работы, и Герман Гельмгольц, исследовавший закон сохранения энергии в различных 8
Первое начало Т. Д. выражает закон сохранения энергии применительно к тепловым процессам Первым к формулировке закона сохранения энергии пришел Роберт Майер Кроме Майера вопросами превращения разных форм энергии друг в друга занимались Джеймс П. Джоуль, открывший в 1843 г. эквивалентность теплоты и механической работы, и Герман Гельмгольц, исследовавший закон сохранения энергии в различных 8
 Внутренняя энергия термодинамической системы включает в себя энергию микроскопического движения и взаимодействия частиц системы, а так же их внутримолекулярную и внутриядерную энергии. Внутренняя энергия произвольной массы идеального газа m будет равна произведению числа молекул в данной массе газа на энергию одной молекулы 9
Внутренняя энергия термодинамической системы включает в себя энергию микроскопического движения и взаимодействия частиц системы, а так же их внутримолекулярную и внутриядерную энергии. Внутренняя энергия произвольной массы идеального газа m будет равна произведению числа молекул в данной массе газа на энергию одной молекулы 9
 Приращение температуры тела прямо пропорционально количеству теплоты, сообщенного ему. Для количественного описания этого соотношения вводится коэффициент пропорциональности Стела между количеством теплоты, сообщаемого телу, и изменением его температуры, называемый теплоемкостью: 10
Приращение температуры тела прямо пропорционально количеству теплоты, сообщенного ему. Для количественного описания этого соотношения вводится коэффициент пропорциональности Стела между количеством теплоты, сообщаемого телу, и изменением его температуры, называемый теплоемкостью: 10
 Теплоемкость позволяет определить количество теплоты d. Q ’, которое необходимо сообщить телу для повышения его температуры на величину d. T. Теплоемкость термодинамической системы изменяется при изменении количества вещества в ней. 11
Теплоемкость позволяет определить количество теплоты d. Q ’, которое необходимо сообщить телу для повышения его температуры на величину d. T. Теплоемкость термодинамической системы изменяется при изменении количества вещества в ней. 11
 Это позволяет ввести для описания свойств тела удельную теплоемкость: Молярную теплоемкость: Эти теплоемкости связаны между собой через молярную массу μ следующим соотношением: 12
Это позволяет ввести для описания свойств тела удельную теплоемкость: Молярную теплоемкость: Эти теплоемкости связаны между собой через молярную массу μ следующим соотношением: 12
 Теплоемкость, так же как и количество переданной телу теплоты, зависит от того, каким образом, а точнее при осуществлении какого процесса, теплота передавалась этому телу. Обычно рассматриваются два значения теплоемкости газов: C V – молярная теплоемкость в изохорном процессе ( V = const) и C p – молярная теплоемкость в изобарном процессе (p = const). 13
Теплоемкость, так же как и количество переданной телу теплоты, зависит от того, каким образом, а точнее при осуществлении какого процесса, теплота передавалась этому телу. Обычно рассматриваются два значения теплоемкости газов: C V – молярная теплоемкость в изохорном процессе ( V = const) и C p – молярная теплоемкость в изобарном процессе (p = const). 13
 Если нагревание происходит при постоянном объеме, тело не совершает работы над внешними телами и, следовательно, все тепло идет на приращение внутренней энергии тела: Отсюда следует, что теплоемкость любого тела при постоянном объеме равна: 14
Если нагревание происходит при постоянном объеме, тело не совершает работы над внешними телами и, следовательно, все тепло идет на приращение внутренней энергии тела: Отсюда следует, что теплоемкость любого тела при постоянном объеме равна: 14
 Продифференцируе м по температуре выражение для одного моля ( =1) внутренней энергии идеального газа. Получим: 15
Продифференцируе м по температуре выражение для одного моля ( =1) внутренней энергии идеального газа. Получим: 15
 При изменении объема газ совершает работу, то есть подведенная теплота и изменение внутренней энергии становятся не равными другу. При постоянном давлении из первого начала термодинамики получаем: 16
При изменении объема газ совершает работу, то есть подведенная теплота и изменение внутренней энергии становятся не равными другу. При постоянном давлении из первого начала термодинамики получаем: 16
 Отношение ΔV / ΔT найдем из уравнения состояния идеального газа, записанного для 1 моля: При Р = const 17
Отношение ΔV / ΔT найдем из уравнения состояния идеального газа, записанного для 1 моля: При Р = const 17
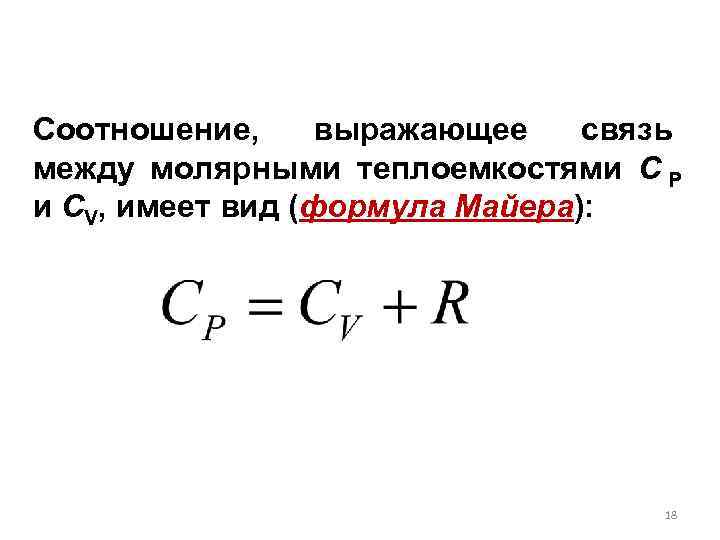 Соотношение, выражающее связь между молярными теплоемкостями C Р и CV, имеет вид (формула Майера): 18
Соотношение, выражающее связь между молярными теплоемкостями C Р и CV, имеет вид (формула Майера): 18
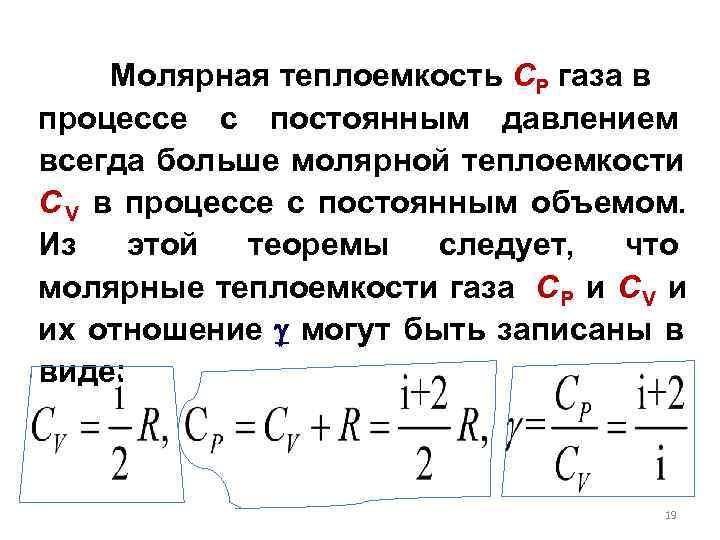
 Молярная теплоемкость CР газа в процессе с постоянным давлением всегда больше молярной теплоемкости C V в процессе с постоянным объемом. Из этой теоремы следует, что молярные теплоемкости газа C Р и C V и их отношение могут быть записаны в виде: 19
Молярная теплоемкость CР газа в процессе с постоянным давлением всегда больше молярной теплоемкости C V в процессе с постоянным объемом. Из этой теоремы следует, что молярные теплоемкости газа C Р и C V и их отношение могут быть записаны в виде: 19
 § Теплота Q и работа А не являются функциями состояния потому, что они описывают процесс обмена энергией, а не являются какими либо видами энергии § Работа описывает макроскопический процесс обмена механической энергией между Т. Д. системой и внешней средой § Теплота описывает микроскопический процесс обмена энергией, протекающий при непосредственном соударении молекул 20
§ Теплота Q и работа А не являются функциями состояния потому, что они описывают процесс обмена энергией, а не являются какими либо видами энергии § Работа описывает макроскопический процесс обмена механической энергией между Т. Д. системой и внешней средой § Теплота описывает микроскопический процесс обмена энергией, протекающий при непосредственном соударении молекул 20
 Метод получения и анализа зависимостей c(T) или Q(T) называется калориметрией. С его помощью можно определить частоты колебаний и моменты инерции молекул, температуры и теплоты фазовых переходов 21
Метод получения и анализа зависимостей c(T) или Q(T) называется калориметрией. С его помощью можно определить частоты колебаний и моменты инерции молекул, температуры и теплоты фазовых переходов 21
 Адиабатический процесс в идеальном газе d. Q=0 d. U=-d. A Имеем: c. V d. T+P d. V=0 Обозначив (c. V+R)/c. V= , получим: P d. V+V d. P=0 Можно убедиться, что это выражение получается при дифференцировании уравнения: P V =const и C=d. Q/d. T=0 22
Адиабатический процесс в идеальном газе d. Q=0 d. U=-d. A Имеем: c. V d. T+P d. V=0 Обозначив (c. V+R)/c. V= , получим: P d. V+V d. P=0 Можно убедиться, что это выражение получается при дифференцировании уравнения: P V =const и C=d. Q/d. T=0 22
 Второе начало термодинамики • Второе начало термодинамики констатирует неэквивалентность различных видов энергии. Оно постулирует направление протекания тепловых процессов • Формулировка Клаузиуса: Теплота не может самопроизвольно переходить от тела менее нагретого к более нагретому 23
Второе начало термодинамики • Второе начало термодинамики констатирует неэквивалентность различных видов энергии. Оно постулирует направление протекания тепловых процессов • Формулировка Клаузиуса: Теплота не может самопроизвольно переходить от тела менее нагретого к более нагретому 23
 • Формулировка Томсона. Невозможен круговой процесс, единственным результатом которого было бы совершение работы за счёт охлаждения теплового резервуара • Устройство, которое позволяло бы осуществлять этот процесс, называется вечным двигателем второго рода 24
• Формулировка Томсона. Невозможен круговой процесс, единственным результатом которого было бы совершение работы за счёт охлаждения теплового резервуара • Устройство, которое позволяло бы осуществлять этот процесс, называется вечным двигателем второго рода 24
 • Второе начало Т. Д. накладывает запрет на вечный двигатель второго рода • Из второго начала Т. Д. можно получить множество конкретных результатов с помощью метода циклов и метода термодинамических функций 25
• Второе начало Т. Д. накладывает запрет на вечный двигатель второго рода • Из второго начала Т. Д. можно получить множество конкретных результатов с помощью метода циклов и метода термодинамических функций 25
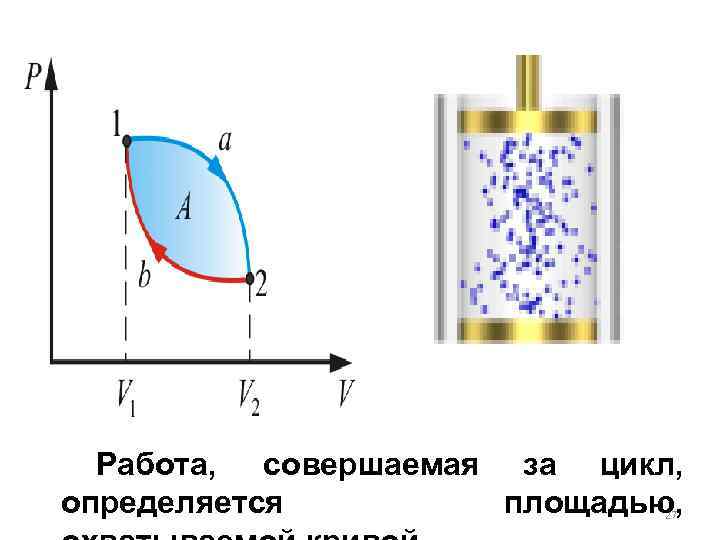
 Круговым процессом, или циклом, называется такой процесс, в результате которого термодинамическое тело возвращается в исходное состояние. В диаграммах состояния P, V и других круговые процессы изображается в виде замкнутых кривых. Это связано с тем, что в любой диаграмме два тождественных состояния (начало и конец кругового процесса) изображаются одной и той же точкой на плоскости. 26
Круговым процессом, или циклом, называется такой процесс, в результате которого термодинамическое тело возвращается в исходное состояние. В диаграммах состояния P, V и других круговые процессы изображается в виде замкнутых кривых. Это связано с тем, что в любой диаграмме два тождественных состояния (начало и конец кругового процесса) изображаются одной и той же точкой на плоскости. 26
 Работа, совершаемая за цикл, определяется площадью, 27
Работа, совершаемая за цикл, определяется площадью, 27
 Если за цикл совершается положительная работа (цикл протекает по часовой стрелке), то он называется прямым. Если за цикл совершается отрицательная работа (цикл протекает против часовой стрелки), то он называется обратным.
Если за цикл совершается положительная работа (цикл протекает по часовой стрелке), то он называется прямым. Если за цикл совершается отрицательная работа (цикл протекает против часовой стрелки), то он называется обратным.
 В результате кругового процесса система может теплоту как получать, так и отдавать, поэтому Q 1 – количество теплоты, полученное системой; Q 2 – количество теплоты, отданное 29
В результате кругового процесса система может теплоту как получать, так и отдавать, поэтому Q 1 – количество теплоты, полученное системой; Q 2 – количество теплоты, отданное 29
 Термический коэффициент полезного действия для кругового процесса 30
Термический коэффициент полезного действия для кругового процесса 30
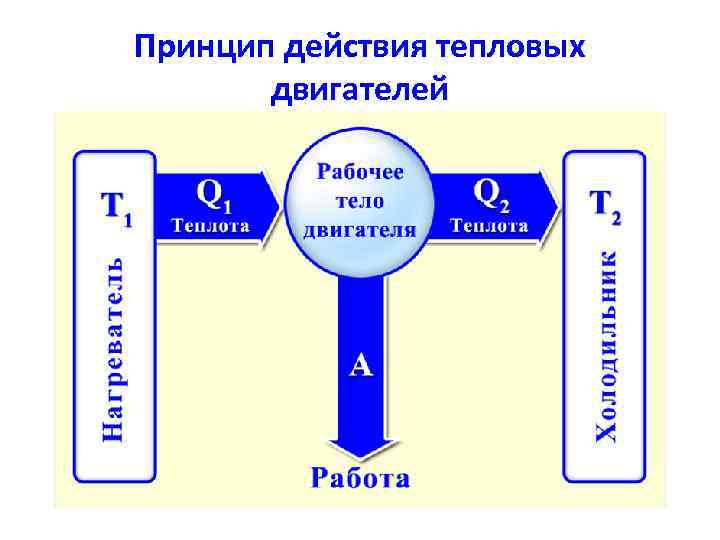
 • Тепловой двигатель – это устройство, в котором совершается циклический Т. Д. процесс • В любом тепловом двигателе тепло передаётся от нагревателя к рабочему телу, а затем к холодильнику. При этом совершается полезная работа 31
• Тепловой двигатель – это устройство, в котором совершается циклический Т. Д. процесс • В любом тепловом двигателе тепло передаётся от нагревателя к рабочему телу, а затем к холодильнику. При этом совершается полезная работа 31
 Принцип действия тепловых двигателей
Принцип действия тепловых двигателей
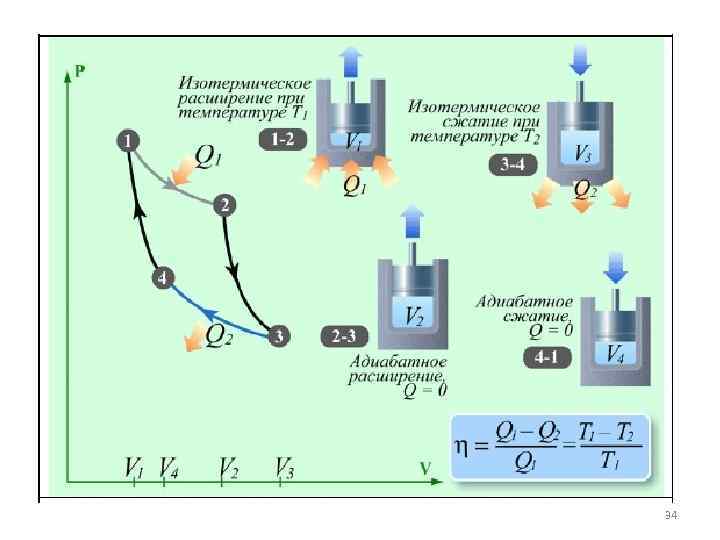
 Наибольшим КПД при заданных температурах нагревателя T 1 и холодильника T 2 обладает тепловой двигатель, где рабочее тело расширяется и сжимается по циклу Карно график которого состоит из двух изотерм и двух адиабат. Теплоёмкости в адиабатическом и изотермическом процессах не зависят от рабочего тела, поэтому их рассмотрение позволяет выявить ряд общих закономерностей
Наибольшим КПД при заданных температурах нагревателя T 1 и холодильника T 2 обладает тепловой двигатель, где рабочее тело расширяется и сжимается по циклу Карно график которого состоит из двух изотерм и двух адиабат. Теплоёмкости в адиабатическом и изотермическом процессах не зависят от рабочего тела, поэтому их рассмотрение позволяет выявить ряд общих закономерностей
 34
34
 Цикл Карно • Первая теорема Карно: Коэффициент полезного действия тепловой машины, работающей по циклу Карно, зависит только от температур нагревателя и холодильника и не зависит от устройства машины и типа рабочего тела 35
Цикл Карно • Первая теорема Карно: Коэффициент полезного действия тепловой машины, работающей по циклу Карно, зависит только от температур нагревателя и холодильника и не зависит от устройства машины и типа рабочего тела 35
 Для повышения КПД надо повышать температуру нагревателя и понижать температуру холодильника =(Q 1 -Q 2)/Q 1=(T 1 -T 2)/T 1 Q 1/T 1=Q 2/T 2 Величина Q/T называется приведённой теплотой
Для повышения КПД надо повышать температуру нагревателя и понижать температуру холодильника =(Q 1 -Q 2)/Q 1=(T 1 -T 2)/T 1 Q 1/T 1=Q 2/T 2 Величина Q/T называется приведённой теплотой
 Вторая теорема Карно: КПД любого цикла не может быть больше, чем КПД цикла Карно - =1 -Т 2 /Т 1 , где под Т 1 понимается максимальная, а под Т 2 минимальная температура
Вторая теорема Карно: КПД любого цикла не может быть больше, чем КПД цикла Карно - =1 -Т 2 /Т 1 , где под Т 1 понимается максимальная, а под Т 2 минимальная температура
 На всех стадиях кругового процесса - цикла Карно - нигде не допускается соприкосновенность тел с разной температурой, т. е. нет необратимых процессов теплопроводности. Весь цикл проводится обратимо (бесконечно медленно).
На всех стадиях кругового процесса - цикла Карно - нигде не допускается соприкосновенность тел с разной температурой, т. е. нет необратимых процессов теплопроводности. Весь цикл проводится обратимо (бесконечно медленно).
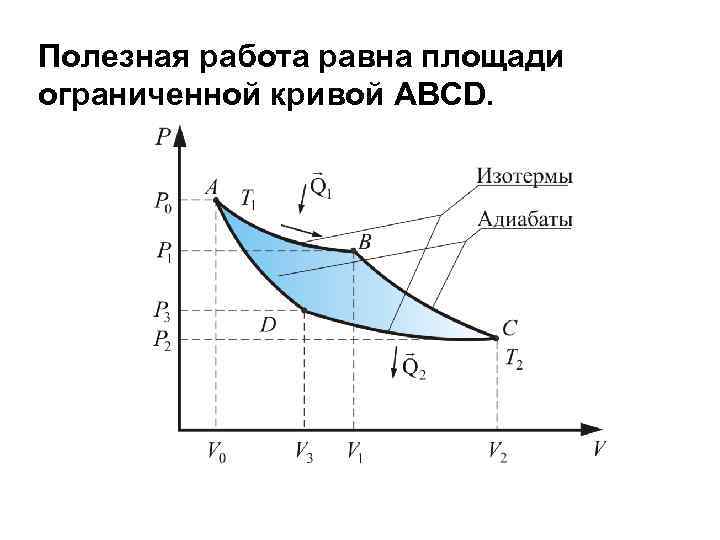
 Полезная работа равна площади ограниченной кривой ABCD.
Полезная работа равна площади ограниченной кривой ABCD.
 А = А 1 + А 2 + А 3 + А 4 Работа совершаемая газом больше работы внешних сил
А = А 1 + А 2 + А 3 + А 4 Работа совершаемая газом больше работы внешних сил
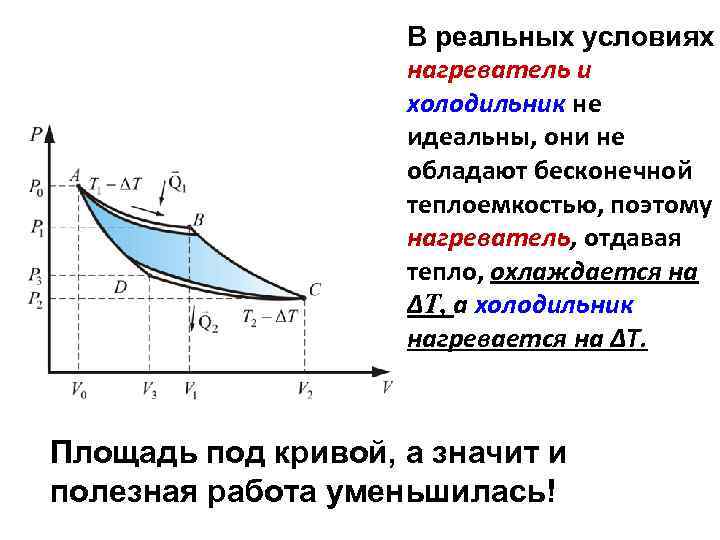
 В реальных условиях нагреватель и холодильник не идеальны, они не обладают бесконечной теплоемкостью, поэтому нагреватель, отдавая тепло, охлаждается на ΔT, а холодильник нагревается на ΔТ. Площадь под кривой, а значит и полезная работа уменьшилась!
В реальных условиях нагреватель и холодильник не идеальны, они не обладают бесконечной теплоемкостью, поэтому нагреватель, отдавая тепло, охлаждается на ΔT, а холодильник нагревается на ΔТ. Площадь под кривой, а значит и полезная работа уменьшилась!
 Для обратимого цикла Карно Для необратимого цикла Всегда – этот вывод справедлив независимо от причин необратимости цикла Карно.
Для обратимого цикла Карно Для необратимого цикла Всегда – этот вывод справедлив независимо от причин необратимости цикла Карно.
 Холодильная машина, работает по обратному циклу Карно. Если проводить цикл в обратном направлении, тепло будет забираться у холодильника и передаваться нагревателю (за счет работы внешних сил).
Холодильная машина, работает по обратному циклу Карно. Если проводить цикл в обратном направлении, тепло будет забираться у холодильника и передаваться нагревателю (за счет работы внешних сил).
 В этом цикле ра бота, совершаемая над газом – отрицательна, т. е. Если рабочее тело совершает обратный цикл, то при этом можно переносить энергию в форме тепла от холодного тела к горячему за счет совершения внешними силами работы.
В этом цикле ра бота, совершаемая над газом – отрицательна, т. е. Если рабочее тело совершает обратный цикл, то при этом можно переносить энергию в форме тепла от холодного тела к горячему за счет совершения внешними силами работы.
 Из рассмотренного цикла Карно видно, что равны между собой отношения теплот к температурам, при которых они были получены или отданы в изотермическом процессе:
Из рассмотренного цикла Карно видно, что равны между собой отношения теплот к температурам, при которых они были получены или отданы в изотермическом процессе:
 Отношение теплоты Q в изотермическом процессе к температуре, при которой происходила передача теплоты, называется приведенной теплотой :
Отношение теплоты Q в изотермическом процессе к температуре, при которой происходила передача теплоты, называется приведенной теплотой :
 Для подсчета приведенной теплоты в произвольном процессе необходимо разбить этот процесс на бесконечно малые участки, где Т можно считать константой. Приведенная теплота на таком участке будет равна : Суммируя приведенную теплоту на всех участках процесса, получим:
Для подсчета приведенной теплоты в произвольном процессе необходимо разбить этот процесс на бесконечно малые участки, где Т можно считать константой. Приведенная теплота на таком участке будет равна : Суммируя приведенную теплоту на всех участках процесса, получим:
 Для процесса, происходящего по замкнутому циклу Из равенства нулю интеграла, взятого по замкнутому контуру, следует, что подынтегральное выражение - есть полный дифференциал некоторой функции, которая определяется только состоянием системы и не зависит от пути, каким система пришла в это состояние.
Для процесса, происходящего по замкнутому циклу Из равенства нулю интеграла, взятого по замкнутому контуру, следует, что подынтегральное выражение - есть полный дифференциал некоторой функции, которая определяется только состоянием системы и не зависит от пути, каким система пришла в это состояние.
 Это позволяет ввести новую функцию состояния S: Функция состояния, полный дифференциал которой равен , называется энтропией.
Это позволяет ввести новую функцию состояния S: Функция состояния, полный дифференциал которой равен , называется энтропией.
 Энтропия S – это отношение полученной или отданной теплоты к температуре, при которой происходил этот процесс. Понятие энтропии было впервые введено Рудольфом Клаузиусом. Для обратимых процессов изменение энтропии: - это выражение называется равенство Клаузиуса.
Энтропия S – это отношение полученной или отданной теплоты к температуре, при которой происходил этот процесс. Понятие энтропии было впервые введено Рудольфом Клаузиусом. Для обратимых процессов изменение энтропии: - это выражение называется равенство Клаузиуса.
 Энтропия системы является функцией ее состояния, определенная с точностью до произвольной постоянной. Если система совершает равновесный переход из состояния 1 в состояние 2, то изменение энтропии: Физический смысл имеет лишь разность энтропий. Исходя из этого, найдем изменения энтропии в процессах идеального газа.
Энтропия системы является функцией ее состояния, определенная с точностью до произвольной постоянной. Если система совершает равновесный переход из состояния 1 в состояние 2, то изменение энтропии: Физический смысл имеет лишь разность энтропий. Исходя из этого, найдем изменения энтропии в процессах идеального газа.
 Изменение энтропии S 1 2 идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида перехода 1 2. Изохорический т. к. процесс: Изобаричес- т. к. P 1 = P 2 кий процесс: Изотермичес- т. к. Т 1 = Т 2 кий процесс: Адиабатичес- то кий процесс: изоэнтропийный процесс
Изменение энтропии S 1 2 идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида перехода 1 2. Изохорический т. к. процесс: Изобаричес- т. к. P 1 = P 2 кий процесс: Изотермичес- т. к. Т 1 = Т 2 кий процесс: Адиабатичес- то кий процесс: изоэнтропийный процесс
 Рассмотрим фазовый переход «твердое тело – жидкость» Коэффициент пропорциональности λ есть константа, зависящая только от вещества системы и называемая удельной теплотой плавления.
Рассмотрим фазовый переход «твердое тело – жидкость» Коэффициент пропорциональности λ есть константа, зависящая только от вещества системы и называемая удельной теплотой плавления.
 Изменение энтропии в процессе этого фазового перехода можно найти просто, если считать процесс равновесным. Это вполне допустимое приближение, если считать, что разность температур между системой и тем объектом, который поставляет системе тепло, не слишком велика, намного меньше температуры плавления. Тогда:
Изменение энтропии в процессе этого фазового перехода можно найти просто, если считать процесс равновесным. Это вполне допустимое приближение, если считать, что разность температур между системой и тем объектом, который поставляет системе тепло, не слишком велика, намного меньше температуры плавления. Тогда:
 Так как температура системы в данном фазовом переходе не меняется и равна температуре плавления, то подынтегральное выражение это величина, которая в ходе процесса не меняется, поэтому она от массы m вещества не зависит. Тогда:
Так как температура системы в данном фазовом переходе не меняется и равна температуре плавления, то подынтегральное выражение это величина, которая в ходе процесса не меняется, поэтому она от массы m вещества не зависит. Тогда:
 Из этой формулы следует, что при плавлении энтропия возрастает, а при кристаллизации уменьшается. Физический смысл этого результата достаточно ясен: фазовая область молекулы в твердом теле гораздо меньше, чем в жидкости, так как в твердом теле каждой молекуле доступна только малая область пространства между соседними узлами кристаллической решетки, а в жидкости молекулы занимают всю область пространства.
Из этой формулы следует, что при плавлении энтропия возрастает, а при кристаллизации уменьшается. Физический смысл этого результата достаточно ясен: фазовая область молекулы в твердом теле гораздо меньше, чем в жидкости, так как в твердом теле каждой молекуле доступна только малая область пространства между соседними узлами кристаллической решетки, а в жидкости молекулы занимают всю область пространства.
 Поэтому при равной температуре энтропия твердого тела меньше энтропии жидкости. Это означает, что твердое тело представляет собой более упорядоченную, и менее хаотичную систему, поэтому и энтропия его меньше, чем у жидкости.
Поэтому при равной температуре энтропия твердого тела меньше энтропии жидкости. Это означает, что твердое тело представляет собой более упорядоченную, и менее хаотичную систему, поэтому и энтропия его меньше, чем у жидкости.
 Рассмотрим фазовый переход «жидкость знак плюс относится к испарению, а знак минус – к конденсации. Коэффициент пропорциональности r в этом выражении, есть константа, зависящая от вещества системы, называемая удельной теплотой испарения.
Рассмотрим фазовый переход «жидкость знак плюс относится к испарению, а знак минус – к конденсации. Коэффициент пропорциональности r в этом выражении, есть константа, зависящая от вещества системы, называемая удельной теплотой испарения.
 Изменение энтропии в этом процессе можно найти, считая процесс равновесным. Это вполне допустимое приближение, при условии, что разность температур между системой и «поставщиком» тепла невелика, т. е. намного меньше температуры кипения. Тогда изменение энтропии:
Изменение энтропии в этом процессе можно найти, считая процесс равновесным. Это вполне допустимое приближение, при условии, что разность температур между системой и «поставщиком» тепла невелика, т. е. намного меньше температуры кипения. Тогда изменение энтропии:
 Из формулы следует, что при испарении энтропия возрастает, а при конденсации уменьшается. При равных температурах фазовая область молекул газа значительно больше фазовой области молекул жидкости. Газ, по сравнению с жидкостью, гораздо менее упорядоченная, более хаотичная система и энтропия газа
Из формулы следует, что при испарении энтропия возрастает, а при конденсации уменьшается. При равных температурах фазовая область молекул газа значительно больше фазовой области молекул жидкости. Газ, по сравнению с жидкостью, гораздо менее упорядоченная, более хаотичная система и энтропия газа
 При любом необратимом процессе в замкнутой системе энтропия возрастает (d. S > 0) или Это неравенство Клаузиуса. Таким образом, для произвольного процесса, где, знак равенства – для обратимого процесса; знак больше для
При любом необратимом процессе в замкнутой системе энтропия возрастает (d. S > 0) или Это неравенство Клаузиуса. Таким образом, для произвольного процесса, где, знак равенства – для обратимого процесса; знак больше для
 Тогда для замкнутой системы – математическая запись второго начала термодинамики. Энтропия замкнутой системы при любых происходивших в ней процессах не может убывать (или увеличивается или остается неизменной).
Тогда для замкнутой системы – математическая запись второго начала термодинамики. Энтропия замкнутой системы при любых происходивших в ней процессах не может убывать (или увеличивается или остается неизменной).
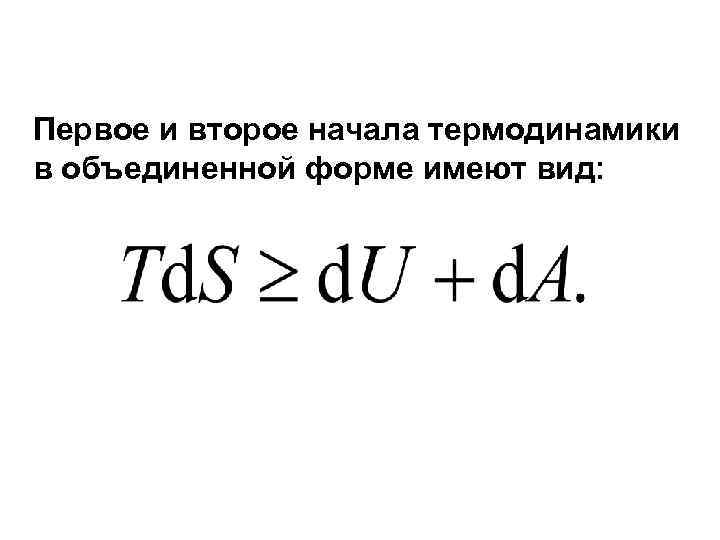 Первое и второе начала термодинамики в объединенной форме имеют вид:
Первое и второе начала термодинамики в объединенной форме имеют вид:
 Свободная энергия есть та работа, которую могло бы совершить тело в обратимом изотермическом процессе или, свободная энергия – есть максимальная возможная работа, которую может совершить система, обладая каким-то запасом внутренней энергии.
Свободная энергия есть та работа, которую могло бы совершить тело в обратимом изотермическом процессе или, свободная энергия – есть максимальная возможная работа, которую может совершить система, обладая каким-то запасом внутренней энергии.
 При любом необратимом процессе энтропия увеличивается до того, пока не прекратятся какие-либо процессы. Это произойдет, при достижении замкнутой системы равновесного состояния, т. е. когда все параметры состояния системы (Р, Т) во всех точках системы станут одинаковыми. Вывести систему из этого равновесного состояния можно только затратив энергию извне.
При любом необратимом процессе энтропия увеличивается до того, пока не прекратятся какие-либо процессы. Это произойдет, при достижении замкнутой системы равновесного состояния, т. е. когда все параметры состояния системы (Р, Т) во всех точках системы станут одинаковыми. Вывести систему из этого равновесного состояния можно только затратив энергию извне.
 Макросостояние – это состояние вещества, характеризуемое его термодинамическими параметрами. Состояние системы, характеризуемое состоянием каждой входящей в систему молекулы, называют микросостоянием. Так как молекулы движутся хаотически, то имеется много микросостояний, соответствующих одному макросостоянию. Обозначим W число микросостояний соответствующее
Макросостояние – это состояние вещества, характеризуемое его термодинамическими параметрами. Состояние системы, характеризуемое состоянием каждой входящей в систему молекулы, называют микросостоянием. Так как молекулы движутся хаотически, то имеется много микросостояний, соответствующих одному макросостоянию. Обозначим W число микросостояний соответствующее
 Термодинамической вероятностью макросостояния W называется число микросостояний, осуществляющих данное макросостояние Термодинамическая вероятность W максимальна, когда система находится в равновесном состоянии.
Термодинамической вероятностью макросостояния W называется число микросостояний, осуществляющих данное макросостояние Термодинамическая вероятность W максимальна, когда система находится в равновесном состоянии.
 Больцман предложил, что где k – коэффициент Больцмана. С этой точки зрения энтропия выступает, как мера беспорядочности, хаотичности состояния. Связь между S и W позволяет несколько иначе сформулировать второе начало термодинамики: наиболее вероятным изменением энтропии является ее возрастание. Энтропия системы – максимальна, при
Больцман предложил, что где k – коэффициент Больцмана. С этой точки зрения энтропия выступает, как мера беспорядочности, хаотичности состояния. Связь между S и W позволяет несколько иначе сформулировать второе начало термодинамики: наиболее вероятным изменением энтропии является ее возрастание. Энтропия системы – максимальна, при
 Третье начало термодинамики или закон Нернста: изменение энтропии S стремится к нулю при любых обратимых изотермических процессах, совершаемых между двумя равновесными состояниями при температурах, приближающихся к абсолютному нулю Объяснение теоремы Нернста можно дать ( S → 0 при Т → 0). только на основании квантово- механических представлений.
Третье начало термодинамики или закон Нернста: изменение энтропии S стремится к нулю при любых обратимых изотермических процессах, совершаемых между двумя равновесными состояниями при температурах, приближающихся к абсолютному нулю Объяснение теоремы Нернста можно дать ( S → 0 при Т → 0). только на основании квантово- механических представлений.
 Следствием Третьего начала является то что, невозможно охладить тело до абсолютного нуля (принцип недостижимости абсолютного нуля температуры).
Следствием Третьего начала является то что, невозможно охладить тело до абсолютного нуля (принцип недостижимости абсолютного нуля температуры).
 Контрольные вопросы 1. Теплоемкость: удельная, при постоянном объеме и при постоянном давлении. 2. Адиабатический процесс 3. Работа газа. Внутренняя энергия газа. 4. Перове начало термодинамики. 5. Второе начало термодинамики. 6. Циклические процессы. 7. Энтропия и ее изменения 8. Третье начало термодинамики.
Контрольные вопросы 1. Теплоемкость: удельная, при постоянном объеме и при постоянном давлении. 2. Адиабатический процесс 3. Работа газа. Внутренняя энергия газа. 4. Перове начало термодинамики. 5. Второе начало термодинамики. 6. Циклические процессы. 7. Энтропия и ее изменения 8. Третье начало термодинамики.

