Термохимия.ppt
- Количество слайдов: 21
 Термодинамические расчеты. Закон Гесса. • 1840 год. Академик Гесс • Тепловой эффект реакции не зависит от пути реакции, т. е. от ее промежуточных стадий и определяется только природой и состоянием исходных веществ и продуктов реакции.
Термодинамические расчеты. Закон Гесса. • 1840 год. Академик Гесс • Тепловой эффект реакции не зависит от пути реакции, т. е. от ее промежуточных стадий и определяется только природой и состоянием исходных веществ и продуктов реакции.
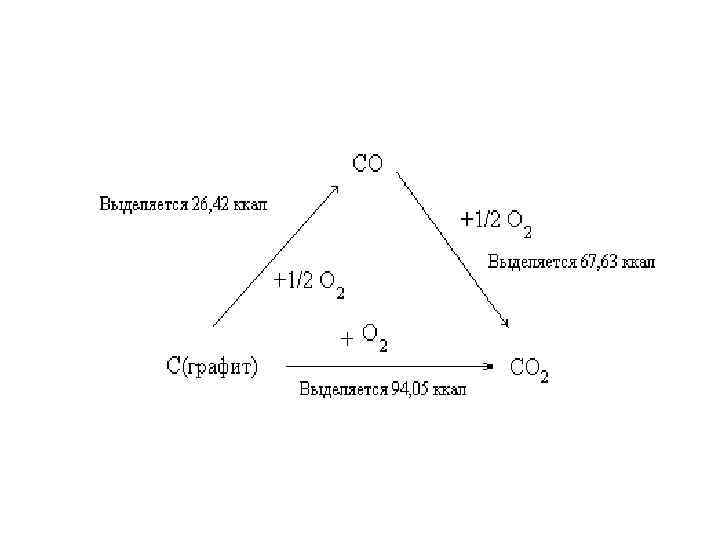
 CO 2 можно получить сжиганием углерода в кислороде непосредственно до двуокиси углерода: С+О 2=СО 2+Q 1 или получая сначала СО, а затем сжигая ее до двуокиси: С+1/2 О 2=СО+Q 2 CO+1/2 О 2=СО 2+Q 3 Q 1=Q 2+Q 3
CO 2 можно получить сжиганием углерода в кислороде непосредственно до двуокиси углерода: С+О 2=СО 2+Q 1 или получая сначала СО, а затем сжигая ее до двуокиси: С+1/2 О 2=СО+Q 2 CO+1/2 О 2=СО 2+Q 3 Q 1=Q 2+Q 3
 • Первое следствие: тепловой эффект разложения какого либо химического соединения точно равен по абсолютной величине и противоположен по знаку тепловому эффекту образования этого соединения.
• Первое следствие: тепловой эффект разложения какого либо химического соединения точно равен по абсолютной величине и противоположен по знаку тепловому эффекту образования этого соединения.
 • Второе следствие: если совершаются две реакции, приводящие из различных начальных состояний к одинаковым конечным, то разница между тепловыми эффектами представляет собой тепловой эффект перехода из одного начального состояния в другое.
• Второе следствие: если совершаются две реакции, приводящие из различных начальных состояний к одинаковым конечным, то разница между тепловыми эффектами представляет собой тепловой эффект перехода из одного начального состояния в другое.
 • Третье следствие: если совершаются две реакции, приводящие из одинаковых начальных состояний к различным конечным, то разница между их тепловыми эффектами представляет собой тепловой эффект перехода из одного конечного состояния в другое.
• Третье следствие: если совершаются две реакции, приводящие из одинаковых начальных состояний к различным конечным, то разница между их тепловыми эффектами представляет собой тепловой эффект перехода из одного конечного состояния в другое.
 • Теплота образования: тепловой эффект реакции образования одного моля данного соединения из простых веществ, взятых в наиболее устойчивой модификации. • Стандартная теплота образования: теплота образования соединения, отнесенная к температуре 25 С (298 К) и давлению 1 атм (760 мм рт. ст. )
• Теплота образования: тепловой эффект реакции образования одного моля данного соединения из простых веществ, взятых в наиболее устойчивой модификации. • Стандартная теплота образования: теплота образования соединения, отнесенная к температуре 25 С (298 К) и давлению 1 атм (760 мм рт. ст. )
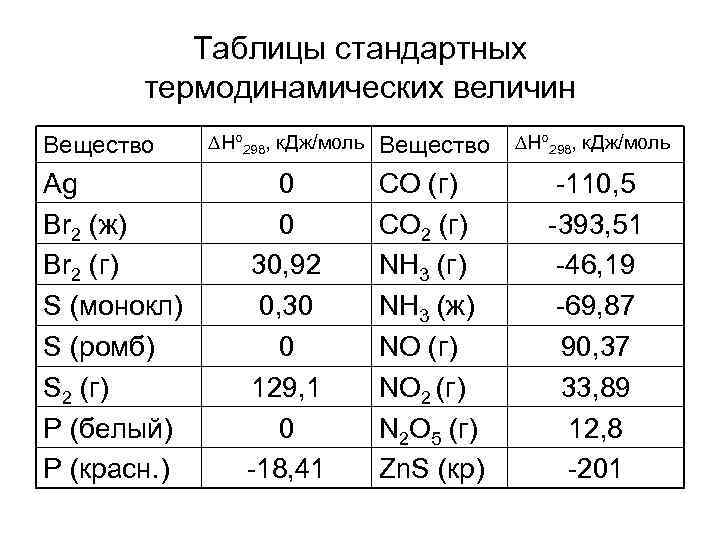 Таблицы стандартных термодинамических величин Вещество Ag Br 2 (ж) Br 2 (г) S (монокл) S (ромб) S 2 (г) Р (белый) Р (красн. ) Н 298, к. Дж/моль Вещество Н 298, к. Дж/моль 0 0 30, 92 0, 30 0 129, 1 0 -18, 41 СО (г) СО 2 (г) NH 3 (ж) NO (г) NO 2 (г) N 2 O 5 (г) Zn. S (кр) -110, 5 -393, 51 -46, 19 -69, 87 90, 37 33, 89 12, 8 -201
Таблицы стандартных термодинамических величин Вещество Ag Br 2 (ж) Br 2 (г) S (монокл) S (ромб) S 2 (г) Р (белый) Р (красн. ) Н 298, к. Дж/моль Вещество Н 298, к. Дж/моль 0 0 30, 92 0, 30 0 129, 1 0 -18, 41 СО (г) СО 2 (г) NH 3 (ж) NO (г) NO 2 (г) N 2 O 5 (г) Zn. S (кр) -110, 5 -393, 51 -46, 19 -69, 87 90, 37 33, 89 12, 8 -201
 Н 298
Н 298
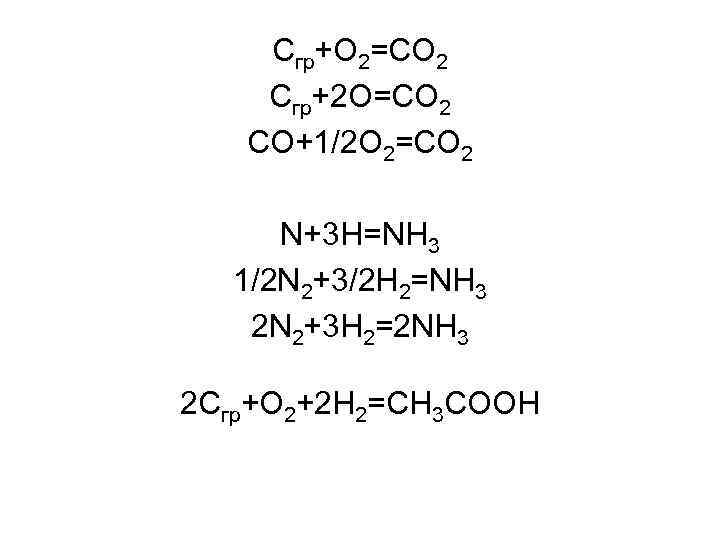 Сгр+О 2=СО 2 Сгр+2 О=СО 2 СО+1/2 О 2=СО 2 N+3 H=NH 3 1/2 N 2+3/2 H 2=NH 3 2 N 2+3 H 2=2 NH 3 2 Cгр+О 2+2 Н 2=СН 3 СООН
Сгр+О 2=СО 2 Сгр+2 О=СО 2 СО+1/2 О 2=СО 2 N+3 H=NH 3 1/2 N 2+3/2 H 2=NH 3 2 N 2+3 H 2=2 NH 3 2 Cгр+О 2+2 Н 2=СН 3 СООН
 • Четвертое следствие: тепловой эффект реакции равен разности между суммой теплот образования продуктов и суммой теплот образования исходных веществ с учетом стехиометрических коэффициентов.
• Четвертое следствие: тепловой эффект реакции равен разности между суммой теплот образования продуктов и суммой теплот образования исходных веществ с учетом стехиометрических коэффициентов.
 • Пример. (1) S+O 2=SO 2 -70, 94 ккал (2) 2 Cu+S=Cu 2 S-19, 0 ккал (3) 2 Cu+1/2 O 2=Cu 2 O-39, 89 ккал Найти тепловой эффект реакции 2 Сu 2 O+Cu 2 S=6 Cu+SO 2+ H р-ции Н р-ции= Н (SO 2)+6 Н (Сu)- Н (Cu 2 S)-2 Н (Cu 2 O)= =1. (-70, 94)+ 6. 0 -1. (-19, 0)-2. (-39, 8)= =27, 66 ккал
• Пример. (1) S+O 2=SO 2 -70, 94 ккал (2) 2 Cu+S=Cu 2 S-19, 0 ккал (3) 2 Cu+1/2 O 2=Cu 2 O-39, 89 ккал Найти тепловой эффект реакции 2 Сu 2 O+Cu 2 S=6 Cu+SO 2+ H р-ции Н р-ции= Н (SO 2)+6 Н (Сu)- Н (Cu 2 S)-2 Н (Cu 2 O)= =1. (-70, 94)+ 6. 0 -1. (-19, 0)-2. (-39, 8)= =27, 66 ккал
 • Теплота сгорания: тепловой эффект реакции полного сгорания одного моля данного вещества до образования высших оксидов. • Стандартная теплота сгорания: теплота сгорания, отнесенная к стандартным условиям, т. е. 25 С (298 К) и 1 атм (760 мм рт. ст) CH 4+2 O 2=CO 2+2 H 2 O
• Теплота сгорания: тепловой эффект реакции полного сгорания одного моля данного вещества до образования высших оксидов. • Стандартная теплота сгорания: теплота сгорания, отнесенная к стандартным условиям, т. е. 25 С (298 К) и 1 атм (760 мм рт. ст) CH 4+2 O 2=CO 2+2 H 2 O
 • Пятое следствие: тепловой эффект реакции равен разности между суммой теплот сгорания исходных веществ и суммой теплот сгорания продуктов с учетом стехиометрических коэффициентов.
• Пятое следствие: тепловой эффект реакции равен разности между суммой теплот сгорания исходных веществ и суммой теплот сгорания продуктов с учетом стехиометрических коэффициентов.
 Пример. Необходимо определить теплоту образования метана С+2 Н 2=СН 4+ Н обр (1) С+О 2=СО 2 -94, 05 ккал (2) Н 2+1/2 О 2=Н 2 О-68, 32 ккал (3) СН 4+2 О 2=СО 2+2 Н 2 О-211, 93 ккал Н обр= Н сгор(С)+2 Н сгор(Н 2)- Н сгор(СН 4)=1. (-94, 05)+ 2. (-68, 32)-1. (-211, 93)=-18, 76 ккал
Пример. Необходимо определить теплоту образования метана С+2 Н 2=СН 4+ Н обр (1) С+О 2=СО 2 -94, 05 ккал (2) Н 2+1/2 О 2=Н 2 О-68, 32 ккал (3) СН 4+2 О 2=СО 2+2 Н 2 О-211, 93 ккал Н обр= Н сгор(С)+2 Н сгор(Н 2)- Н сгор(СН 4)=1. (-94, 05)+ 2. (-68, 32)-1. (-211, 93)=-18, 76 ккал
 Зависимость теплового эффекта реакции от температуры • Уравнение зависимости энтальпии индивидуального вещества от температуры • Ср>0 энтальпия вещества растет с ростом температуры (всегда!!!!)
Зависимость теплового эффекта реакции от температуры • Уравнение зависимости энтальпии индивидуального вещества от температуры • Ср>0 энтальпия вещества растет с ростом температуры (всегда!!!!)
 • Уравнение зависимости энтальпии химической реакции от температуры (уравнение Кирхгофа) • Ср>0 H растет с ростом температуры • Ср<0 H уменьшается с ростом т-ры
• Уравнение зависимости энтальпии химической реакции от температуры (уравнение Кирхгофа) • Ср>0 H растет с ростом температуры • Ср<0 H уменьшается с ростом т-ры
 • Уравнение зависимости внутренней энергии индивидуального вещества от температуры • СV>0 внутренняя энергия вещества растет с ростом температуры (всегда!!!!)
• Уравнение зависимости внутренней энергии индивидуального вещества от температуры • СV>0 внутренняя энергия вещества растет с ростом температуры (всегда!!!!)
 • Уравнение зависимости изменения внутренней энергии химической реакции от температуры (уравнение Кирхгофа) • СV>0 U растет с ростом температуры • СV<0 U уменьшается с ростом т-ры
• Уравнение зависимости изменения внутренней энергии химической реакции от температуры (уравнение Кирхгофа) • СV>0 U растет с ростом температуры • СV<0 U уменьшается с ростом т-ры
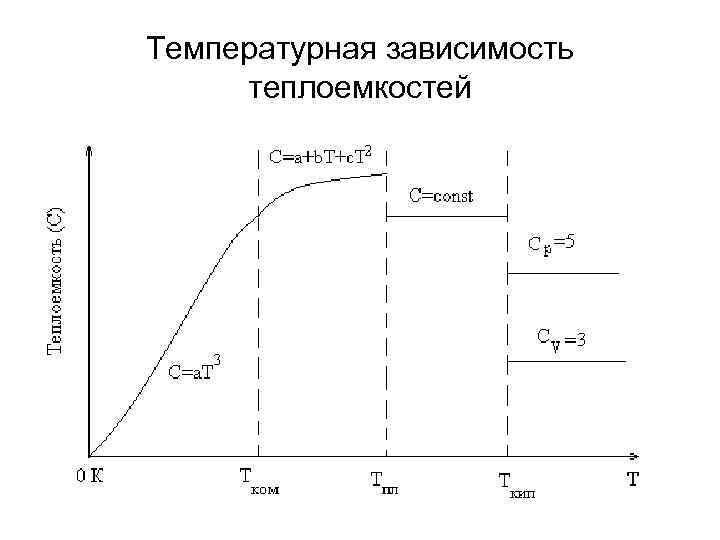 Температурная зависимость теплоемкостей
Температурная зависимость теплоемкостей
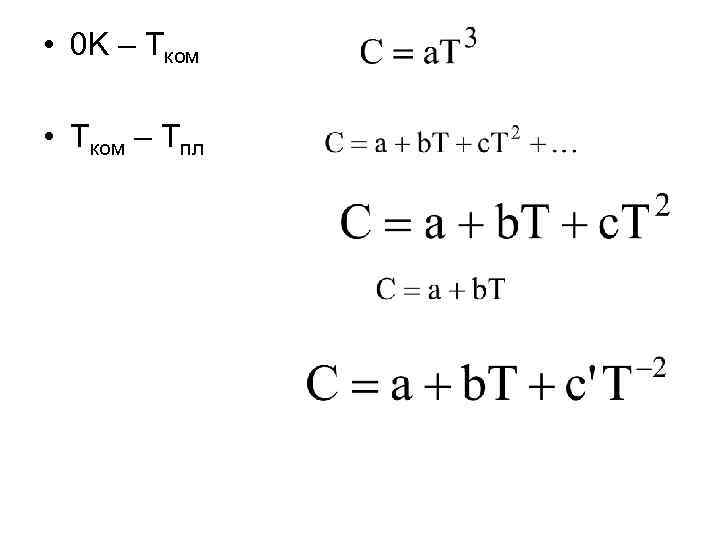 • 0 K – Tком • Tком – Тпл
• 0 K – Tком • Tком – Тпл


