Термодинамическая теория растворов.ppt
- Количество слайдов: 34
 Термодинамическая теория растворов • Раствором называется однородная смесь, состоящая из двух или большего числа веществ, состав которой в известных пределах может непрерывно изменяться. • • Газообразные растворы Твердые растворы -твердые растворы замещения -твердые растворы внедрения -твердые растворы вычитания Жидкие растворы •
Термодинамическая теория растворов • Раствором называется однородная смесь, состоящая из двух или большего числа веществ, состав которой в известных пределах может непрерывно изменяться. • • Газообразные растворы Твердые растворы -твердые растворы замещения -твердые растворы внедрения -твердые растворы вычитания Жидкие растворы •
 Способы выражения концентраций растворов • Мольная доля (Хi) или мольный процент (мол. %) Мольная доля – отношение числа молей данного компонента к сумме чисел молей всех компонентов раствора
Способы выражения концентраций растворов • Мольная доля (Хi) или мольный процент (мол. %) Мольная доля – отношение числа молей данного компонента к сумме чисел молей всех компонентов раствора
 • Массовая доля (Wi) или массовый (весовой) процент (вес. %, масс. %) Массовая (весовая) доля – отношение массы данного компонента к массе раствора. • Массовый (весовой) процент – массовая доля выраженная в процентах или количество граммов растворенного вещества в 100 г. раствора. • Молярность (Сi) – число молей растворенного вещества в одном литре раствора.
• Массовая доля (Wi) или массовый (весовой) процент (вес. %, масс. %) Массовая (весовая) доля – отношение массы данного компонента к массе раствора. • Массовый (весовой) процент – массовая доля выраженная в процентах или количество граммов растворенного вещества в 100 г. раствора. • Молярность (Сi) – число молей растворенного вещества в одном литре раствора.
 • Моляльность (m) – число молей растворенного вещества в 1000 г. растворителя. • Нормальность (Ni) – количество граммэквивалент растворенного вещества, содержащееся в 1 л. раствора.
• Моляльность (m) – число молей растворенного вещества в 1000 г. растворителя. • Нормальность (Ni) – количество граммэквивалент растворенного вещества, содержащееся в 1 л. раствора.
 • Раствор KCl содержит 250 г. KCl в 1000 г воды. Выразить состав раствора через молярность, моляльность, весовой процент, мольные доли. МKCl=39+35, 5=74, 5 г/моль а) Масса раствора mр-ра=250+1000=1250 г Объем раствора см 3
• Раствор KCl содержит 250 г. KCl в 1000 г воды. Выразить состав раствора через молярность, моляльность, весовой процент, мольные доли. МKCl=39+35, 5=74, 5 г/моль а) Масса раствора mр-ра=250+1000=1250 г Объем раствора см 3
 3, 36 моля KCl содержится в 1103, 3 см 3 С содержится в 1000 см 3 моль/л б) 3, 36 моля KCl содержится в 1000 г воды m=3, 36 моль/1 кг воды в) mр-ра=1250 г
3, 36 моля KCl содержится в 1103, 3 см 3 С содержится в 1000 см 3 моль/л б) 3, 36 моля KCl содержится в 1000 г воды m=3, 36 моль/1 кг воды в) mр-ра=1250 г
 г) n. KCl=3, 36 моль
г) n. KCl=3, 36 моль
 • Выразите концентрацию 50% (по весу) водного раствора Ag. NO 3 через молярность, моляльность, и мольную долю. Плотность раствора при 18 С 1, 668 г/см 3. m(Ag. NO 3)=50 г m(H 2 O)=50 г mраствора=100 г моля
• Выразите концентрацию 50% (по весу) водного раствора Ag. NO 3 через молярность, моляльность, и мольную долю. Плотность раствора при 18 С 1, 668 г/см 3. m(Ag. NO 3)=50 г m(H 2 O)=50 г mраствора=100 г моля
 а) см 3 0, 29 моля Ag. NO 3 содержится в 59, 95 см 3 р-ра С молей Ag. NO 3 содержится в 1000 см 3 р-ра моль/л б) 0, 29 моля Ag. NO 3 содержится в 50 г воды m молей Ag. NO 3 содержится в 1000 г воды моль/1 кг воды
а) см 3 0, 29 моля Ag. NO 3 содержится в 59, 95 см 3 р-ра С молей Ag. NO 3 содержится в 1000 см 3 р-ра моль/л б) 0, 29 моля Ag. NO 3 содержится в 50 г воды m молей Ag. NO 3 содержится в 1000 г воды моль/1 кг воды
 в)
в)
 • Выразите концентрацию водного раствора Ag. NO 3 через весовой процент, моляльность и мольную долю, если в 1 л этого раствора содержится 1, 405 моля Ag. NO 3, а плотность раствора при 20 С равна 1, 194 г/см 3. mр-ра=Vр-ра=1000. 1, 194 = 1194 г m(Ag. NO 3) = 1, 405. 170 = 238, 85 г m(H 2 O)=mр-ра- m(Ag. NO 3) = 1194 -238, 85 = 955, 15 г
• Выразите концентрацию водного раствора Ag. NO 3 через весовой процент, моляльность и мольную долю, если в 1 л этого раствора содержится 1, 405 моля Ag. NO 3, а плотность раствора при 20 С равна 1, 194 г/см 3. mр-ра=Vр-ра=1000. 1, 194 = 1194 г m(Ag. NO 3) = 1, 405. 170 = 238, 85 г m(H 2 O)=mр-ра- m(Ag. NO 3) = 1194 -238, 85 = 955, 15 г
 а) б) 1, 405 моля Ag. NO 3 содержится в 955, 15 г воды m молей Ag. NO 3 содержится в 1000 г воды моль/1 кг воды в) молей
а) б) 1, 405 моля Ag. NO 3 содержится в 955, 15 г воды m молей Ag. NO 3 содержится в 1000 г воды моль/1 кг воды в) молей
 • Водный раствор Cu(NO 3)2 содержит 1, 33 моля Cu(NO 3)2 в 1000 г воды. Выразите концентрацию раствора через весовые проценты, молярность и мольную долю, если плотность раствора при 20 С составляет 1, 189 г/см 3. г m(H 2 O) = 1000 г. mр-ра = 1000+250, 04 = 1250, 04 г.
• Водный раствор Cu(NO 3)2 содержит 1, 33 моля Cu(NO 3)2 в 1000 г воды. Выразите концентрацию раствора через весовые проценты, молярность и мольную долю, если плотность раствора при 20 С составляет 1, 189 г/см 3. г m(H 2 O) = 1000 г. mр-ра = 1000+250, 04 = 1250, 04 г.
 а) б) см 3 1, 33 моля Cu(NO 3)2 содержится в 1051, 3 см 3 С молей Cu(NO 3)2 содержится в 1000 см 3 моль/л в) молей
а) б) см 3 1, 33 моля Cu(NO 3)2 содержится в 1051, 3 см 3 С молей Cu(NO 3)2 содержится в 1000 см 3 моль/л в) молей
 • Выразите концентрацию водного раствора через весовой процент, моляльность и молярность, если мольная доля HCl в этом растворе равна 0, 05, а плотность его при 18 С равна 1, 05 г/см 3. а)
• Выразите концентрацию водного раствора через весовой процент, моляльность и молярность, если мольная доля HCl в этом растворе равна 0, 05, а плотность его при 18 С равна 1, 05 г/см 3. а)
 mр-ра = 100 г. m. HCl = 9, 64 г. m(H 2 O) = 100 – 9, 64 = 90, 36 г. б) 0, 26 моль HCl содержится в 90, 36 г. воды m молей HCl содержится в 1000 г. воды моль/кг. Воды в) см 3
mр-ра = 100 г. m. HCl = 9, 64 г. m(H 2 O) = 100 – 9, 64 = 90, 36 г. б) 0, 26 моль HCl содержится в 90, 36 г. воды m молей HCl содержится в 1000 г. воды моль/кг. Воды в) см 3
 моля 0, 26 моля содержится в 95, 24 см 3 С молей содержится в 1000 см 3 моль/л
моля 0, 26 моля содержится в 95, 24 см 3 С молей содержится в 1000 см 3 моль/л
 Парциальные мольные величины • Экстенсивные свойства пропорциональны количеству вещества. V, U, H, G, S, Cp, m. • Интенсивные свойства не зависят от количества вещества. р, Т. Обладают общим свойством выравнивания.
Парциальные мольные величины • Экстенсивные свойства пропорциональны количеству вещества. V, U, H, G, S, Cp, m. • Интенсивные свойства не зависят от количества вещества. р, Т. Обладают общим свойством выравнивания.
 • Парциальная мольная величина компонента – частная производная от какой либо экстенсивной величины g по числу молей ni этого компонента раствора при постоянстве р, Т и чисел молей остальных компонентов.
• Парциальная мольная величина компонента – частная производная от какой либо экстенсивной величины g по числу молей ni этого компонента раствора при постоянстве р, Т и чисел молей остальных компонентов.
 • Физический смысл: парциальная мольная величина i-ого компонента характеризует изменение данного экстенсивного свойства раствора (g) при добавлении 1 моль i-ого компонента к столь большому количеству раствора при постоянных температуре и давлении, что добавление этого количества компонента практически не меняет состава раствора.
• Физический смысл: парциальная мольная величина i-ого компонента характеризует изменение данного экстенсивного свойства раствора (g) при добавлении 1 моль i-ого компонента к столь большому количеству раствора при постоянных температуре и давлении, что добавление этого количества компонента практически не меняет состава раствора.
 • Парциальный мольный объем: • Парциальная мольная энтальпия: • Парциальная мольная свободная энергия (химический потенциал):
• Парциальный мольный объем: • Парциальная мольная энтальпия: • Парциальная мольная свободная энергия (химический потенциал):
 • Величина отражает тенденцию вещества покинуть данную фазу и является мерой его рассеиваемости. Если i(раствор) > i(пар) – испарение вещества. Если i(раствор) < i(пар) – конденсация вещества
• Величина отражает тенденцию вещества покинуть данную фазу и является мерой его рассеиваемости. Если i(раствор) > i(пар) – испарение вещества. Если i(раствор) < i(пар) – конденсация вещества
 • Пусть пар обладает свойствами идеального газа. При равновесии
• Пусть пар обладает свойствами идеального газа. При равновесии
 где Gi – мольная свободная энергия чистого компонента при давлении, равном его парциальному давлению в смеси. pi – парциальное давление данного компонента в газовой фазе над раствором. Химический потенциал компонента в растворе:
где Gi – мольная свободная энергия чистого компонента при давлении, равном его парциальному давлению в смеси. pi – парциальное давление данного компонента в газовой фазе над раствором. Химический потенциал компонента в растворе:
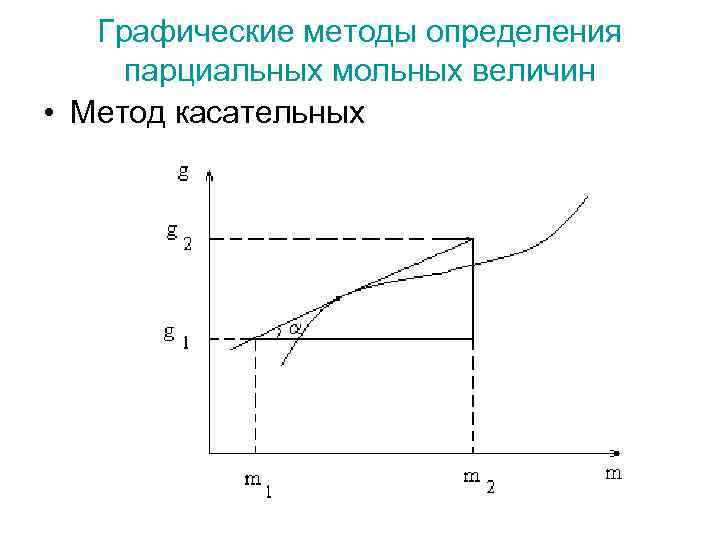 Графические методы определения парциальных мольных величин • Метод касательных
Графические методы определения парциальных мольных величин • Метод касательных
 n 2=m Число молей растворителя , где M 1 – молярная масса растворителя
n 2=m Число молей растворителя , где M 1 – молярная масса растворителя
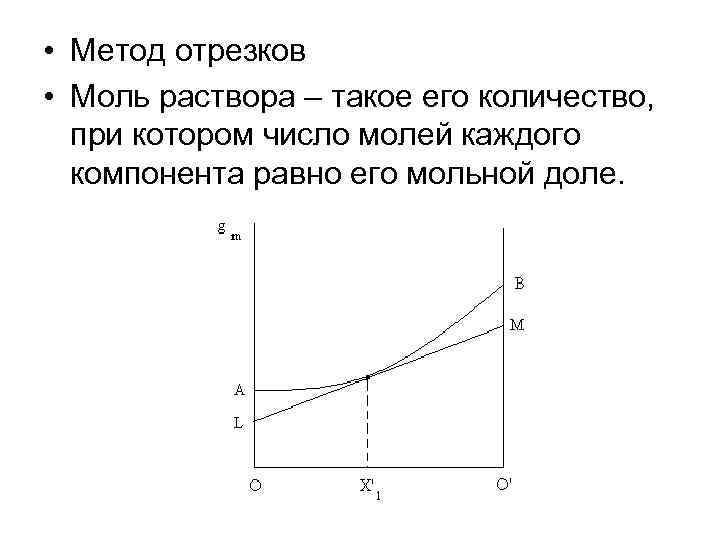 • Метод отрезков • Моль раствора – такое его количество, при котором число молей каждого компонента равно его мольной доле.
• Метод отрезков • Моль раствора – такое его количество, при котором число молей каждого компонента равно его мольной доле.
 • Отрезки ОА и ОВ представляют собой соответственно мольные свойства чистых компонентов g 1 m и g 2 m • Отрезки ОL и O’M равны парциальным величинам и
• Отрезки ОА и ОВ представляют собой соответственно мольные свойства чистых компонентов g 1 m и g 2 m • Отрезки ОL и O’M равны парциальным величинам и
 Уравнения Гиббса-Дюгема • Если раствор находится при Т и р = const, то g= (n 1, n 2, …. . nk). Тогда или (1)
Уравнения Гиббса-Дюгема • Если раствор находится при Т и р = const, то g= (n 1, n 2, …. . nk). Тогда или (1)
 где dg- изменение экстенсивного свойства раствора при добавлении к нему dn 1 молей первого компонента, dn 2 молей второго компонента и т. д. небольшими порциями в таком соотношении, чтобы состав раствора не изменялся. Первое уравнение Гиббса-Дюгема Для 1 моля р-ра
где dg- изменение экстенсивного свойства раствора при добавлении к нему dn 1 молей первого компонента, dn 2 молей второго компонента и т. д. небольшими порциями в таком соотношении, чтобы состав раствора не изменялся. Первое уравнение Гиббса-Дюгема Для 1 моля р-ра
 • Если одновременно изменяется состав раствора и его количество (2) Приравняв (1) и (2) получим второе уравнение Гиббса-Дюгема
• Если одновременно изменяется состав раствора и его количество (2) Приравняв (1) и (2) получим второе уравнение Гиббса-Дюгема
 • Если обе части уравнения поделить на ni: Разделим это уравнение на d. X 1 при постоянных p и Т Для бинарного раствора Х 1+Х 2=1 и d. X 1=-d. X 2
• Если обе части уравнения поделить на ni: Разделим это уравнение на d. X 1 при постоянных p и Т Для бинарного раствора Х 1+Х 2=1 и d. X 1=-d. X 2
 Возьмем в качестве парциальной мольной величины химический потенциал
Возьмем в качестве парциальной мольной величины химический потенциал


