Тератология или ошибки развития Тератология — это наука,


Тератология или ошибки развития

Тератология — это наука, занимающаяся изучением причин происхождения, механизмов формирования и проявления врожденных пороков развития. Важнейшим разделом этой науки является медицинская тератология, которая основное внимание уделяет клиническому проявлению, диагностике этих заболеваний, разрабатывает методы их лечения и профилактики.

Тератогенез - это возникновение пороков развития у плода под влиянием тератогенных факторов (радиация, химические, лекарственные вещества, инфекции). Тератогенным считается такое влияние, которое приводит к пороку развития эмбриона или плода, развивавшегося до этого нормально. Пороки развития, т.е. тератогенные эффекты могут проявляться как анатомическими дефектами (собственно уродства), так и генными или цитогенетическими нарушениями (биохимические и функциональные нарушения).

Вредные (тератогенные) факторы, вызывающие аномальное развитие плода: Недостаточное и несбалансированное (неправильное) питание матери, кислородная недостаточность Различные заболевания матери, особенно острые (коревая краснуха, скарлатина, грипп, вирусный гепатит, паротит и др.) и хронические инфекции (листериоз, туберкулёз, токсоплазмоз, сифилис и др.) Осложнения беременности - токсикозы и присоединившиеся болезни Различные лекарственные средства, особенно гормональные препараты, применяемые во время беременности Вредные производственные факторы и химические вещества, загрязняющие окружающую среду; высокая температура производственных помещений, шум, пыль, повышенная физическая нагрузка, вынужденное положение тела, напряжение зрения и т.д. Ионизирующие излучения Вредные привычки (курение, употребление алкоголя, наркомания, токсикомания)

Периоды, в которых чувствительность к тератогенным фактором была повышена, назвали "критическими". Индивидуальное развитие представляет собой ряд последовательных этапов, различающихся скоростями развития органов или их систем. Наибольшая скорость развития наблюдается в критические, узловые периоды эмбриогенеза, такие, как имплантация, образование плаценты или нервной системы, формирование конечностей и др. На ранних стадиях эмбриогенеза критические периоды относятся к развитию всего организма, позднее они выявляются в развитии отдельных органов — тех, которые в данный момент претерпевают наиболее активные формообразовательные процессы.

Три основных положения Стоккрада (1921): один и тот же тератоген при воздействии на разных стадиях развития может вызывать различные аномалии; одна и та же аномалия может быть следствием действия разных тератогенов; тип аномалии зависит от стадии развития.

Краткосрочное возрастание чувствительности в эти периоды в зародыше происходят важнейшие формообразовательные процессы, определяющие судьбу зачатков отдельных органов или зародыша в целом. Это, например, первые деления дробления зиготы, имплантация, плацентация, начало образования нервной системы или закладка других крупных систем органов (см. табл.).

Красным цветом отмечены стадии наибольшей, серым - наименьшей чувствительности зародыша к тератогенам.

Согласно современным представлениям о тератогенезе: В первые две недели развития воздействие внешних тератогенов обычно приводит к гибели зародыша; с 3-й по 8-ю недели - к крупным морфологическим отклонениям; начиная с 9-й недели у зародыша, как правило, возникают физиологические дефекты и малые морфологические отклонения.

Внешние факторы-тератогены, действующие в периоды раннего эмбрионального развития, приводят либо к гибели зародыша, либо к аномалиям его строения. Антенатальная (то есть до рождения) гибель у человека, вызванная нарушениями внутриутробной жизни, достигает 70 %. То есть из каждых десяти зачатий семь заканчиваются смертью зародыша.

Сейчас не подлежит сомнению, что: эмбрион более чувствителен к внешним воздействиям, чем взрослый организм. на протяжении всей беременности восприимчивость зародыша и плода к действию чужеродных факторов различна: на одних сроках беременности действие тератогена может быть максимальным и вызывать гибель зародыша или формирование анатомических уродств, на других - оно может быть минимальным или отсутствовать совсем. на ранних этапах развития повреждаемость закладок различных органов зародыша очень высока, но со временем, после формирования органов, она понижается в плане анатомических уродств, но повышается в плане функциональных нарушений.

Аномалии развития, уродства возникают в период органогенеза, т. е. тогда, когда закладки органов наиболее активно развиваются, когда они возникают из группы малоспециализированных клеток, устанавливаются их форма, соотношения частей. Органогенез заканчивается примерно к началу третьего месяца беременности.

Первые два месяца являются важнейшими в развитии эмбриона человека. Первые две-две с половиной недели развития, которые играют, главную роль в судьбе зародыша, обычно еще не воспринимаются женщиной как беременность. Поэтому в этот период для нее особенно велика опасность подвергнуться нежелательному воздействию — безвредному для взрослого, но пагубному для зародыша. Односторонность представлений о "двух хороших месяцах" заключается в том, что и последующие месяцы чрезвычайно важны для нормального развития плода. Тератогенные воздействия в плодном периоде приводят к различным функциональным отклонениям, в том числе к нарушениям психики и поведенческих реакций, к нарушениям обмена веществ и другим отклонениям, не носящим выраженный анатомический характер.

Согласно современным представлениям биологии развития, в каждой клетке зародыша подавляющая часть генетической информации, закодированной в ДНК, находится в неактивном состоянии; "работают" лишь немногие гены — контролирующие синтез тех белков, которые в данный момент нужны клетке для выполнения определенных функций. Естественно, что в ходе эмбриогенеза происходит изменение выборочной активности генов: только что работавшие — "замолкают", нередко навсегда, другие, наоборот, включаются в активную деятельность.

Смысл этих процессов понятен: зачем зародышу, например, синтезировать белки хрусталика, если еще и глаза-то нет? И зачем хрусталиковые белки нужны в клетках, которым суждено стать, допустим, зачатком мышечной системы? Белки хрусталика начнут синтезироваться только там и только тогда, где и когда в этом возникнет необходимость (хотя гены этих белков есть в каждой клетке организма). Таким образом, начало образования новых для зародыша систем органов связано с реализацией новых объемов генетической информации.

В относительно коротком временном интервале (критическом периоде) решается судьба группы клеток, определяется путь их дальнейшего развития. Данные процессы неразрывно связаны с возрастающей способностью группы клеток воспринимать внешние по отношению к ней сигналы, которые исходят от других клеток и необходимы для возникновения качественных различий между частями развивающегося организма.

A теперь представим себе, что ожидаемый клетками сигнал окажется не тем, которым определяется нормальный ход событий. Клетки могут воспринять и его, в том случае, когда восприятие внешнего сигнала не отличается высокой специфичностью, поскольку клетки эмбриона не в состоянии отличить изменяющий их сигнал от нормального. Но даже если они такой сигнал и различают, то не могут ему противодействовать, если действие внешнего фактора превышает некий физиологический порог, физиологическую норму. Таким образом закладывается начало аномалии развития или анатомического уродства.

Возникновения дефектов в закладке того или иного органа будет зависеть от "сродства" этих клеток к конкретному альтерирующему фактору, т.е., например, клетки нервной системы должны иметь "сродство" к сигналу конкретного тератогена, к которому клетки, например, сердечной мышцы такой чувствительности не имеют. В таких случаях у зародыша поражаются не все закладки, а только те, которые воспринимают сигнал этого тератогена, вызывающего уродства преимущественно в определенных системах. Критические периоды в таком случае не будут совпадать по времени.

Не исключен и вариант, когда сигнал альтерирующего фактора обладает широким спектром тератогенного действия и поражает все закладки, находящиеся к моменту действия тератогена в стадии активного формирования. Судя по всему именно с этим связано проявление эмбриотоксического действия (гибели зародыша). В зависимости от того на какой стадии закладки органов придет родственный клеткам альтерирующий сигнал, будет поражен тот или иной орган и сформируется, соответственно, уродство в той или иной системе.

Например, сигнал, влияющий на процесс закрытие нервной трубки, поступивший к клеткам в период формирования нервной системы, приведет а анатомическим уродствам нервной системы. Однако если этот же сигнал поступит к зародышу после смыкания нервных валиков, то "разомкнуть" он их уже не сможет, то есть анатомического уродства не будет, но это не значит, что нервная система не будет поражена. В закладках и головного, и спинного мозга еще долго будут проходить сложные формообразовательные процессы, которые в не меньшей степени подвержены тератогенезу, но сам тип уродства будет, конечно, иной.

В других случаях воздействие альтерирующего фактора может проявляться только в определенный, относительно короткий промежуток времени, за пределами которого эмбрион будет нечувствителен к его влиянию. Известны варианты, когда альтерирующие факторы вызывали различные уродства на той стадии развития, когда наблюдалось воздействие данного тератогена.

Для талидомида, например, определены такие критические периоды: применение этого вещества на 21—22-й дни беременности приводит к недоразвитию или полному отсутствию ушей и параличу черепно-мозговых нервов у человеческого зародыша; прием талидомида на 24—27-й дни вызывает максимальную фокомелию рук, а еще через два дня — ног; 34—36-дневный зародыш отреагирует на талидомид недоразвитием пальцев и сужением некоторых отделов кишечника. При длительном приеме лекарства беременной женщиной у зародыша могут возникнуть все эти аномалии. Если же талидомид применялся изредка, от случая к случаю, то ребенок приобретает лишь отдельные "талидомидные" пороки: пострадают органы, морфогенез которых во времени совпал с употреблением препарата.

На поздних сроках беременности, когда все основные органогенезы уже практически окончены, плод на тератогены будет реагировать иначе. Анатомические aномалии у плода в это время не возникают — тератогены не могут разрушить уже сформировавшийся орган, их действие связано, с вмешательством в процесс формирования, но даже незадолго до рождения альтерирующие факторы небезопасны для плода: они могут не только осложнить течение родов, это было бы еще полбеды, гораздо хуже то, что повреждения в конце плодного периода зачастую приводят к нарушениям нормальной работы сердечно-сосудистой, нервной, эндокринной и половой систем плода, т. е. к возникновению функциональных нарушений.

Ситуация усугубляется еще и тем, что выявить эти нарушения обычно удается не скоро. Например, отклонения в высшей нервной деятельности обнаружатся только ко времени, когда ребенок должен будет совершать довольно сложные поведенческие акты. Аномалии репродуктивной системы проявят себя с наступлением половой зрелости.

Таким образом, на начальных этапах беременности альтерирующие воздействия преимущественно вызывают либо гибель зародыша (особенно это характерно для первых двух-трех недель), либо анатомические аномалии, уродства. Чем ближе срок наступления родов, тем меньше вероятность возникновения грубых структурных нарушений, но выше опасность появления нарушений функциональных.

Существуют две возможности поступления тератогенных агентов к развивающемуся организму: 1. прямым путем, без опосредования материнским организмом (например, ионизирующая радиация, микроволны, ультразвук). В этом случае альтерирующий сигнал не изменяется качественно. При прохождении через организм матери может незначительно снизится лишь интенсивность, но не количество, и то как подействует ионизирующая радиация, зависит только от ее характеристик и, конечно, от зародыша. Генетическое, биохимическое, физиологическое и любое другое состояние материнского организма при этом играет незначительную роль 2. непрямым путем, например, тепло, холод, травма. Действие таких тератогенных факторов будет вначале компенсироваться специальными механизмами поддержания постоянства внутренней среды, то есть механизмами, противодействующими такому влиянию в организме матери.

Что же касается воздействия химических агентов, то ситуация еще сложнее — противодействие здесь многостороннее. Зависимость "доза тератогена" - "последствия". Должны существовать какие-то совсем низкие концентрации веществ, не вызывающие в зародыше никаких последствий. Постепенное увеличение их дозы должно привести к постепенному нарастанию тератогенного эффекта, а затем и к смерти зародыша.

Например, в США на полномасштабные испытания биологической активности выпускаемых пестицидов, которые продолжаются по нескольку лет, тратится в среднем 13 миллионов долларов для каждого вещества. Понятно, что тератологические испытания в данном случае лишь часть общих, но, очевидно, некоторое представление о затратах получить можно. Нельзя не учитывать и то, что зародыш — не застывшая система, один и тот же тератоген может проявлять на начальных сроках беременности только эмбриотоксическую активность, позднее — как эмбриотоксическую, так и тератогенную, причем иногда при очень небольшом изменении дозы.

Например, актиномицин Д вызывает гибель у одних эмбрионов практически в той же концентрации, при которой у других наблюдается возникновение уродств. Увеличение дозы в определенное количество раз вовсе не обязательно вызывает возрастание числа уродливых зародышей в точно такой же пропорции. Иногда возрастание концентрации тератогена лишь вдвое может привести к изменению эффекта от минимального до максимального. Другими словами, сложностей при построении кривых "доза— эффект" для каждого конкретного вещества много.

Однако уже только представление о существовании зависимости между концентрацией вещества и вызываемыми им последствиями чрезвычайно важно и актуально. Понимание этой проблемы связано в первую очередь с определением так называемых пороговых доз тератогена, иными словами, для любого тератогена можно подобрать некую — пороговую — концентрацию, ниже которой он не будет вызывать уродства или гибель зародыша. Вроде бы все ясно: идет ли речь о лекарстве или о содержании каких-нибудь веществ в воздухе либо воде,— нужно стараться лишь не превышать эти пороговые уровни. Но уже в начале 70-х годов было показано, что некоторые тератогены имеют еще и мутагенную активность, то есть вызывают изменения в наследственном аппарате клеток.

Действительно, такая прямо пропорциональная зависимость во многих случаях существует. Во многих, но не во всех. Утверждать иначе означало бы неоправданно упрощать реальную ситуацию, и так достаточно сложную. Прежде всего, сложности возникают при определении того, что именно считать тератогенным эффектом. Если только появление анатомических дефектов, то тем самым сужаются представления о возможном проявлении отдаленных последствий вредного фактора, а их изучение — задача сложная, трудоемкая и дорогостоящая.

При этом иногда особенно страдают формирующиеся половые клетки, иначе говоря, неблагоприятный эффект оказывается отсроченным — он проявляется лишь в следующем поколении. Разумеется, мутации могут возникнуть и в других клетках. Главная же опасность здесь заключается в том, что, по-видимому, для мутагенов пороговых доз не существует: достаточно вызвать нарушения в одной клетке, и, по крайней мере, теоретически аналогичные нарушения в результате делений измененной клетки будут скопированы в очень широких пределах.

Пока точно неизвестно, все ли тератогены обладают подобными, свойствами. Но даже если и не все, а лишь часть, то, во-первых, требуется знать, какие именно из них мутагенны, во-вторых, вопрос о пороговой тератогенной дозе при данных обстоятельствах приобретает совершенно иную окраску: рассуждения о пороге теряют смысл. Поэтому речь должна идти не о недопустимости превышения содержания тератогена, а о полном его устранении от контактов с людьми. К сожалению, в реальной жизни соблюсти это условие, как правило, невозможно. Но отказаться от добровольных тератогенов, таких как курение, прием алкоголя, наркотиков, самостоятельное использование лекарственных препаратов - просто необходимо!

Пороки развития — стойкие морфологические изменения органа, системы или организма, которые выходят за пределы вариаций их строения и возникают внутриутробно в результате нарушений развития зародыша или (много реже) после рождения ребенка как следствие нарушения дальнейшего формирования органов. Термином «дисплазия» обычно принято обозначать нарушения развития гонад. Врожденными аномалиями (малыми пороками) чаще называют пороки развития, не сопровождающиеся нарушениями функций органа. Например, деформации ушных раковин, не обезображивающие больного и не отражающиеся на функции органа слуха.

Частота пороков развития, по различным данным, колеблется от 2,7% до 16,3%, что зависит преимущественно от полноты учета и возраста обследуемых. В популяции частота пороков развития достаточно стабильна. Однако, в перинатальной и ранней детской смертности их удельный вес из года в год возрастает, что связывают главным образом со снижением смертности от внутриутробной асфиксии, родовых травм и инфекций.

К порокам развития относятся: аплазия, врожденные гипоплазия и гиперплазия, макросомия, гетеротопия, гетероплазия, эктопия, врожденный стеноз, атрезия и др.

Аплазия (агенезия) — врожденное отсутствие органа. Врожденная гипоплазия (гипотрофия) — недоразвитие органа, проявляющееся дефицитом его массы или уменьшением размеров, превышающим отклонение от средних для данного возраста показателей. Врожденная гиперплазия (гипертрофия) — увеличение массы органа или его размеров за счет возрастания числа или объема клеток. Макросомия (гигантизм) — увеличение длины тела. Гетеротопия (дистопия) — наличие клеток или тканей одного органа в другом или в тех зонах того же органа, где их не должно быть в норме.

Дистопию тканей нередко называют хористией, а дистопию с опухолевидным разрастанием — гамартией. Гетероплазия — нарушение дифференцировки клеток в пределах одной и той же ткани (например, наличие клеток плоского эпителия в дивертикуле Меккеля). Эктопия — расположение органа в необычном месте. Возможно увеличение числа органов или их частей, например удвоение матки, двойная дуга аорты. Врожденный стеноз — сужение канала или отверстия. Атрезия — отсутствие естественного канала или отверстия.

Персистирование — сохранение эмбриональных структур, в норме исчезающих к определенному периоду развития (например, наличие овального окна в межпредсердной перегородке у ребенка, достигшего возраста 1 года). Встречается неразделение (слияние) органов или двух монозиготных близнецов. Дизрафия (арафия) — незаращение эмбриональных щелей. Хейлогнатопалатосхиз — расщелина верхней губы, верхней челюсти и неба. Краниорахисхиз — несмыкание костей черепа и позвоночника, обычно сопровождающееся развитием черепно-мозговых и спинномозговых грыж.

В зависимости от этиологии все пороки развития разделяют на возникшие в результате: генных мутаций (мономутантные пороки развития); хромосомных и геномных мутаций (хромосомные синдромы); комбинированного воздействия генных мутаций и факторов внешней по отношению к зародышу среды (мультифакториальные пороки развития); тератогенных факторов (группа бластопатий, эмбриопатий и фетопатий).

около 20% всех пороков развития составляют мономутантные формы, 9—12% — хромосомные синдромы, до 65% — мультифакториальные пороки развития. Таким образом, подавляющее большинство пороков развития обусловлено (или связано) с изменениями наследственного материала и лишь 2—5% индуцировано непосредственно тератогенными факторами.

В основе мономутантного порока лежит мутация одного гена, произошедшая в половых клетках родителей или более отдаленных предков больного. Передача мономутантных пороков развития от родителей детям определяется законами наследственности.

В зависимости от типа наследования такие пороки развития могут быть доминантными (например, некоторые формы полидактилии, поликистоз почек взрослого типа, Марфана синдром) и рецессивными (например, инфантильный поликистоз почек, синдром Меккеля). При доминантно-наследуемых пороков развития у одного из родителей обычно обнаруживается аналогичный порок. При рецессивном наследовании родители здоровы, но являются носителями измененного гена.

Хромосомные синдромы (хромосомные болезни) — группа пороков развития, индуцированных численными или структурными изменениями хромосом. К нарушениям числа хромосом относятся трисомии, когда имеются добавочные хромосомы, и моносомии, когда одна из хромосом отсутствует.

Основными структурными изменениями хромосом, приводящими к порокам развития, являются частичные трисомии и частичные моносомии (делеции). Хромосомные синдромы проявляются множественными, реже системными пороками развития (случаи моно- или трисомии Х у женщин и дисомия Х у мужчин).

У ребенка с каким-либо хромосомным синдромом, как правило, наблюдается большое число пороков развития. Их комплекс создает довольно специфический для большинства хромосомных синдромов патологический морфотип. Известны синдромы, обусловленные мутациями практически любой хромосомы. Из них наиболее часто встречаются синдром Дауна, Клайнфелтера синдром, Шерешевского — Тернера синдром, синдромы Патау, Эдвардса, синдромы частичных моносомии по 4, 5 и 18-й хромосомам.

Для возникновения пороков развития мультифакториальной группы необходимы наследственная предрасположенность, которая обусловлена группой патологических генов, достигших определенной (надпороговой) концентрации, и воздействие неблагоприятных факторов среды. К этой группе относятся большинство врожденных пороков сердца, расщелин губы и неба, анэнцефалия, врожденные пилоростеноз, мегаколон, косолапость, врожденный вывих бедра, дисплазии почек и многие другие.

Причиной пороков развития у человека являются лишь немногие из большого перечня тератогенных факторов, известных в тератологии. К таковым, в частности, относятся некоторые вирусы (краснухи, лимфоцитарного хориоменингита), возбудители токсоплазмоза, листериоза, воздействие ионизирующего излучения в суммарной дозе на плод более 0,05 Гр за период органогенеза, некоторые лекарственные препараты (талидомид, варфарин, цитостатики, прогестин, этистерон, метилтестостерон), этиловый алкоголь, сахарный диабет.

Патогенез пороков развития (тератогенез) Формирование пороков развития происходит в результате нарушения процессов размножения, миграции и дифференцировки клеток, гибели отдельных клеточных масс, замедления их рассасывания, нарушения адгезии тканей. Остановка или замедление размножения клеток приводит к аплазии или гипоплазии органа, а также к нарушению слияния формирующих его отдельных эмбриональных структур, например при многих дизрафиях. В результате нарушения миграции клеток могут развиться гетеротопии, агенезии и ряд сложных пороков.

Например, тяжелые симметричные расщелины лица образуются в результате нарушения миграции клеток нейроэктодермального гребня в максиллярные отростки. Нарушение дифференциации клеток, возможное в любом периоде эмбриогенеза, обусловливает агенезии органов, их морфологическую и функциональную незрелость, а также персистирование эмбриональных структур. Избыточная гибель клеток, отмирающих в процессе нормального эмбриогенеза (например, происходящая при рассасывании межпальцевых перепонок), лежит в основе эктродактилии — аплазии средних пальцев кистей или стоп (клешнеобразные кисть и стопа).

Задержка физиологического распада клеток (например, при реканализации кишечной трубки и открытии естественных отверстий) может приводить к атрезии, стенозу. В основе формирования некоторых пороков развития лежат циркуляторные расстройства, обусловленные тромбозом, сдавлением, кровоизлиянием. Тератогенный эффект инфекций чаще связан с цитолитическим действием.

Формирование большинства П. р. происходит в первые 8—10 нед. беременности. Выделяют два критических периода, в течение которых зародыш наиболее чувствителен к действию повреждающих факторов. Первый из них приходится на конец 1-й — начало 2-й недели беременности. Повреждающее воздействие в этот период в основном приводит к гибели зародыша. Аналогичное воздействие во втором критическом периоде (3—6-я неделя) чаще индуцирует порок развития.

С целью установления возможной этиологии П. р. целесообразно время действия предполагаемого фактора сопоставлять не с критическим, а с тератогенетическим терминационным периодом (ТТП). Под тератогенетическим терминационным периодом (ТТП). понимают предельный срок, в течение которого повреждающий фактор может обусловить развитие конкретного П. р. Например, ТТП двухкамерного сердца — до 34-го дня, дефекта межпредсердной перегородки — до 55-го дня беременности. ТТП персистирования артериального протока, крипторхизма, многих П. р. зубов выходит за пределы беременности, т.к. окончательное формирование этих структур не завершается в период внутриутробного развития.

Пороки развития разделяют по их этиологии, времени возникновения и объекту повреждения, последовательности формирования, распространенности. Различают первичные П. р. (обусловленные непосредственным воздействием повреждающего фактора) и вторичные, являющиеся осложнением первичных.

По распространенности выделяют: изолированные (одиночные, локальные) П. р., локализованные в одном органе; системные П. р. (в пределах одной системы, например хондродисплазия); множественные П. р., развивающиеся в органах двух и более систем (например, сочетание расщелины губы с полидактилией).

Изолированные и системные пороки развития классифицируют по анатомическому признаку на пороки развития ц.н.с., сердца и сосудов, дыхательной системы и др.

Множественные П. р. разделяют на синдромы и неклассифицированные комплексы. Под синдромами понимают устойчивые сочетания первичных П. р., возникновение которых индуцировано общим этиологическим фактором (мутацией или тератогенным воздействием). В тех случаях, когда комплекс обнаруженных у больного П. р. не укладывается ни в один из известных синдромов, пользуются термином «неклассифицированный комплекс врожденных пороков» или «множественные пороки, неуточненные».

Среди всех пороков развития одно из первых мест занимают аномалии опорно-двигательного аппарата, при этом 3/4 их приходится на пороки развития конечностей. Международная классификация пороков развития опорно-двигательного аппарата (1975) включает 7 групп.

Аномалии, возникающие в результате недостаточности формирования частей конечностей. В эту группу входят следующие пороки развития конечностей. 1. Амелия— полное отсутствие конечности (исключая плечевой пояс и таз). Различают верхнюю и нижнюю амелию, в частности, отсутствие двух верхних конечностей (абрахия), одной верхней конечности (монобрахия), двух нижних конечностей (апус), одной нижней конечности (монопус).

2. Фокомелия (тюленеобразные конечности) — отсутствие проксимальных и (или) средних частей конечности и соответствующих суставов (плечевого, тазобедренного). Различают проксимальную, дистальную и полную фокомелию. Проксимальная фокомелия — отсутствие плеча или бедра, дистальная — отсутствие предплечья (радиоульнарная форма) или голени (тибиофибулярная форма), полная фокомелия — отсутствие плеча и предплечья или бедра и голени. Соответственно вполне сформированная кисть или стопа может отходить непосредственно от туловища (полная фокомелия), соединяться с ним посредством сохранившихся костей предплечья, голени (проксимальная форма) или прикрепляться к плечу, бедру (дистальная форма). Фокомелия бывает одно- и двусторонней, иногда в процесс вовлекаются все четыре конечности.

Перомелия — вариант фокомелии, сочетающейся с недоразвитием кистей или стоп. Различают полную (рука или нога отсутствует, соответствующий отдел туловища заканчивается одним рудиментарным пальцем или кожным выступом) и неполную (плечо или бедро недоразвито, заканчивается также одним рудиментарным пальцем или кожным выступом) формы. Встречаются также лучевая и локтевая косорукость, аплазия большеберцовой кости, аплазия малоберцовой кости, адактилия — отсутствие пальцев, афалангия — отсутствие фаланг, монодактилия — наличие одного пальца на кисти или стопе, ахейрия — отсутствие кисти. Расщепление кисти (эктродактилия, клешнеобразная кисть, «кисть омара») — аплазия центральных компонентов кисти (пальцев и нередко пястных костей) с бороздой (расщелиной) на месте отсутствующих костей.

Выделяют типичные и атипичные формы. Типичная форма характеризуется аплазией III пальца и (нередко) соответствующей пястной кости, а также (иногда) дистального ряда костей запястья, что обусловливает наличие глубокой расщелины. Атипичная расщелина проявляется недоразвитием (реже отсутствием) средних пальцевых компонентов кисти или стопы. При атипичной форме расщелина неглубокая, но широкая; иногда она имеет вид чрезмерно широкого межпальцевого промежутка. Чаще встречается расщепление правой кисти.

II. Аномалии, возникающие в результате недостаточной дифференцировки частей конечности. К ним относятся П. р. лопатки (ладьевидная лопатка, поднятая лопатка), синостозы, синдактилии, брахидактилия, врожденная косолапость, врожденный вывих бедра, артрогрипоз, клинодактилия — укорочение средней фаланги пальцев кистей (чаще V пальца), обычно являющиеся составным компонентом синдромов множественных П. р., особенно хромосомных.

Камптодактилия (кампилодактилия) — сгибательная контрактура проксимальных межфаланговых суставов пальцев кисти. В процесс может вовлекаться любой палец, кроме I. Встречается редко. Сиреномелия (симподия, симмелия, синдром каудальной регрессии) — слияние нижних конечностей. Слияние может касаться мягких тканей и (чаще) некоторых длинных трубчатых костей, а также сопровождаться гипо- и (или) аплазией отдельных костей конечностей и таза.

Стопы могут отсутствовать (sympus apus), бывают сформированы две (sympus dipus) или одна стопа (sympus monopus). Иногда имеется одна рудиментарная стопа с единственным пальцем. Сиреномелия сопровождается аплазией наружных и внутренних половых органов, аплазией мочевой системы, атрезией заднепроходного отверстия и прямой кишки, аплазией одной пупочной артерии.

III. Аномалии, обусловленные удвоением: полидактилия, диплоподия — удвоение стопы, полимелия — увеличение числа нижних конечностей. Полимелия может быть симметричной и асимметричной, обычно сочетается с П. р., несовместимыми с жизнью.

IV. Аномалии, обусловленные чрезмерным ростом. Включают макотородактилию и гигантизм конечности (парциальный гигантизм, односторонняя макросомия, гемигипертрофия) — крайне редкий П. р., проявляющийся односторонним увеличением относительно пропорционально развитой конечности. V. Аномалии, обусловленные недостаточным ростом. В их число входят аномалии, проявляющиеся гипоплазией различных отделов костей конечностей.

VI. Врожденные перетяжки — порок развития амниона в виде тканевых тяжей, проходящих внутри плодовместилища и связывающих между собой плодовую поверхность последа с поверхностью плода, разные точки плодовой поверхности последа и несколько точек поверхности плода. VII. Генерализованные (системные) скелетные деформации. В их основе лежит нарушение эмбриогенеза соединительной ткани, включая костную ткань. К этой группе относятся хондродисплазии, остеодисплазии.

Клинические проявления пороков развития и прогноз зависят - насколько жизненно важным является пораженный орган, - от степени нарушения его функций, - от присоединившихся осложнений.

Грубые пороки развития жизненно важных органов, в т. ч. большинство хромосомных синдромов, обусловленных патологией аутосом, летальны. Около 40% пороков развития проявляются лишь в дальнейшей жизни ребенка, некоторые односторонние (например, арения) могут протекать бессимптомно.

Большинство П. р. корригируют хирургическим путем, отдельные, например врожденный вывих бедра, успешно лечат консервативными методами. При П. р., непосредственно угрожающих жизни ребенка (например, атрезии заднего прохода), операцию производят в первые дни после рождения. В большинстве же случаев хирургическую коррекцию осуществляют после 6 мес. (расщелины губы) или в еще более старшем возрасте (П. р. сердца и крупных сосудов, большинство П. р. мочеполовой системы, опорно-двигательного аппарата).

Выделяют массовую и индивидуальную (семейную) профилактику П. р. Массовая профилактика — комплекс мер, направленных на защиту человека от действия мутагенных и тератогенных факторов, охрану окружающей среды и т.п. Индивидуальная (семейная) профилактика осуществляется путем медико-генетическою консультирования и пренатальной диагностики.
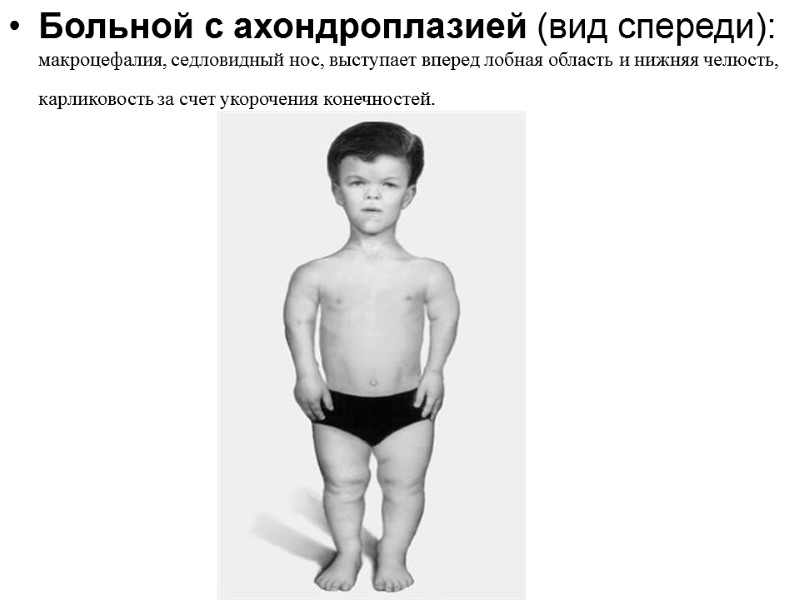
Больной с ахондроплазией (вид спереди): макроцефалия, седловидный нос, выступает вперед лобная область и нижняя челюсть, карликовость за счет укорочения конечностей.
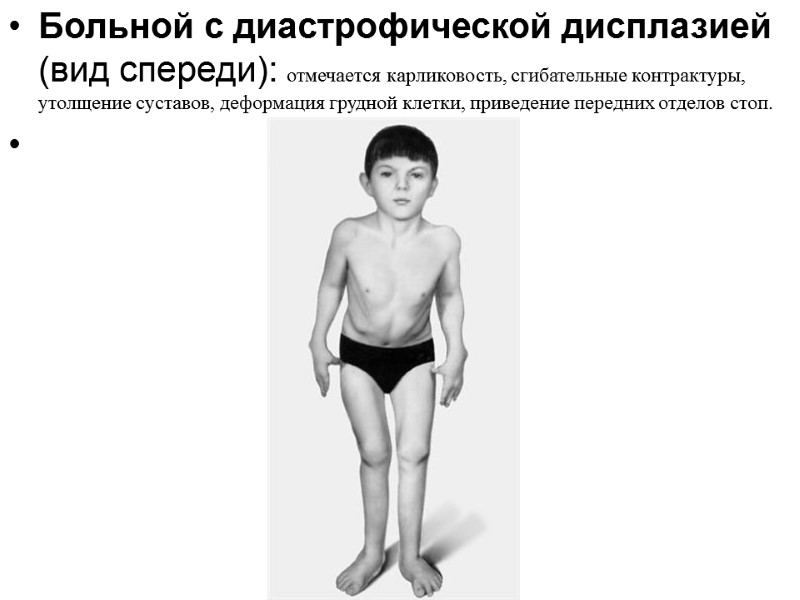
Больной с диастрофической дисплазией (вид спереди): отмечается карликовость, сгибательные контрактуры, утолщение суставов, деформация грудной клетки, приведение передних отделов стоп.
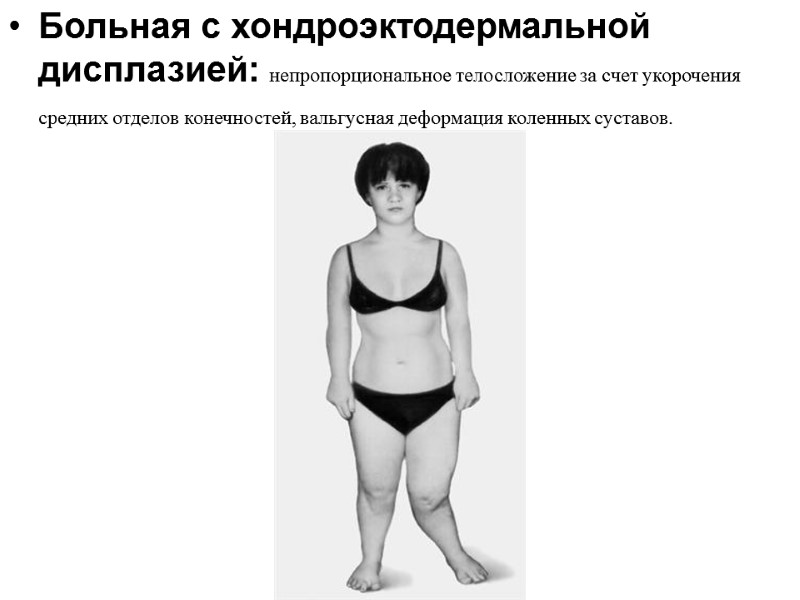
Больная с хондроэктодермальной дисплазией: непропорциональное телосложение за счет укорочения средних отделов конечностей, вальгусная деформация коленных суставов.

Псевдоахондроплазия у матери и дочери: лица больных не изменены, отмечается карликовость за счет укорочения конечностей.
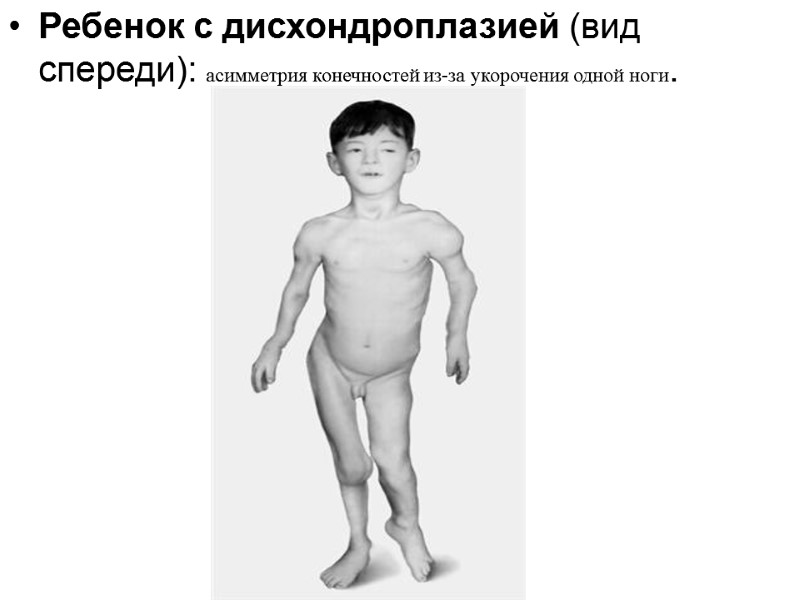
Ребенок с дисхондроплазией (вид спереди): асимметрия конечностей из-за укорочения одной ноги.
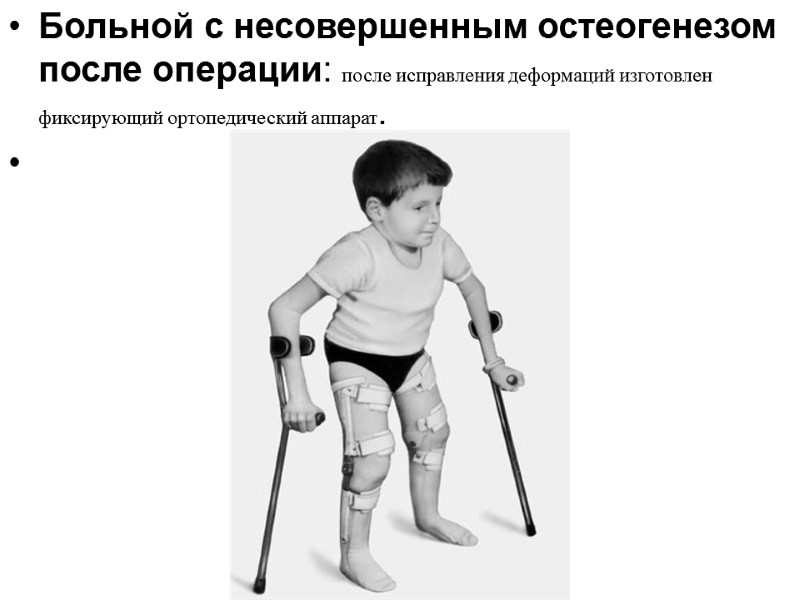
Больной с несовершенным остеогенезом после операции: после исправления деформаций изготовлен фиксирующий ортопедический аппарат.
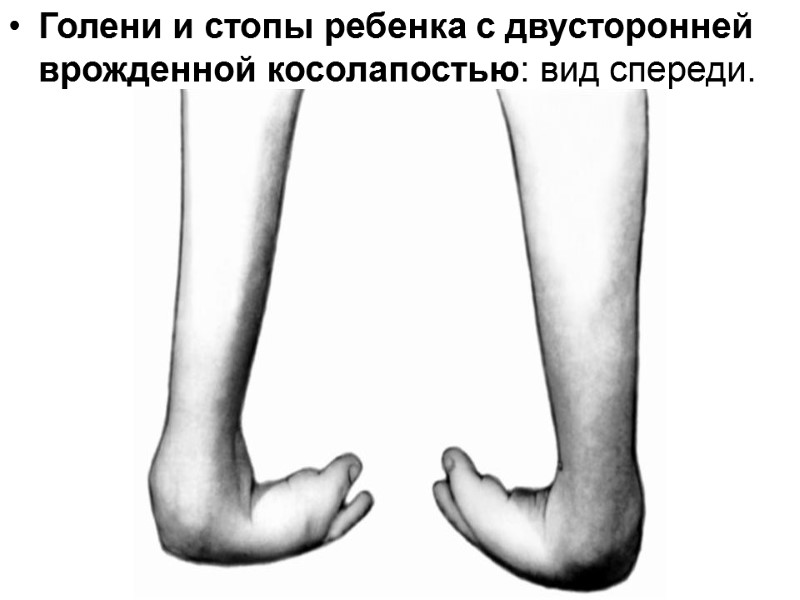
Голени и стопы ребенка с двусторонней врожденной косолапостью: вид спереди.
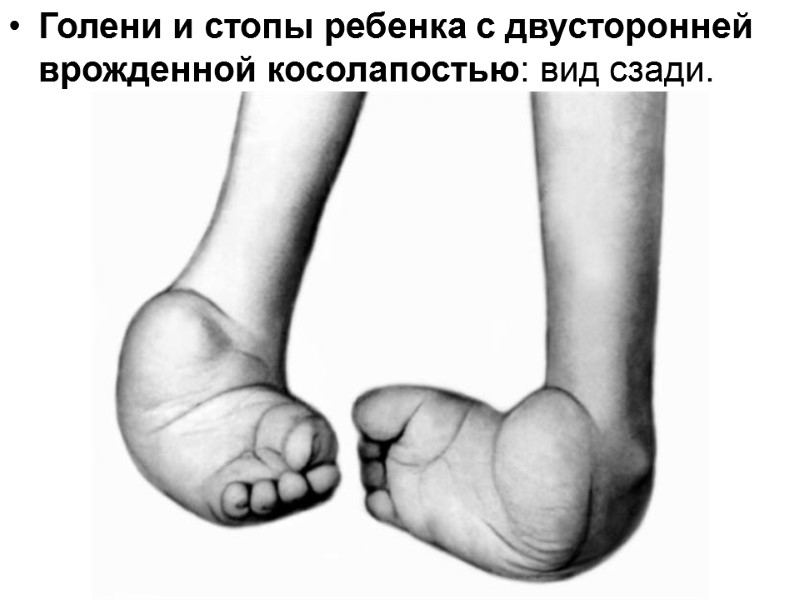
Голени и стопы ребенка с двусторонней врожденной косолапостью: вид сзади.

Больной с двусторонней врожденной косорукостью, сочетающейся с недоразвитием и укорочением верхних конечностей, трехпалыми кистями.
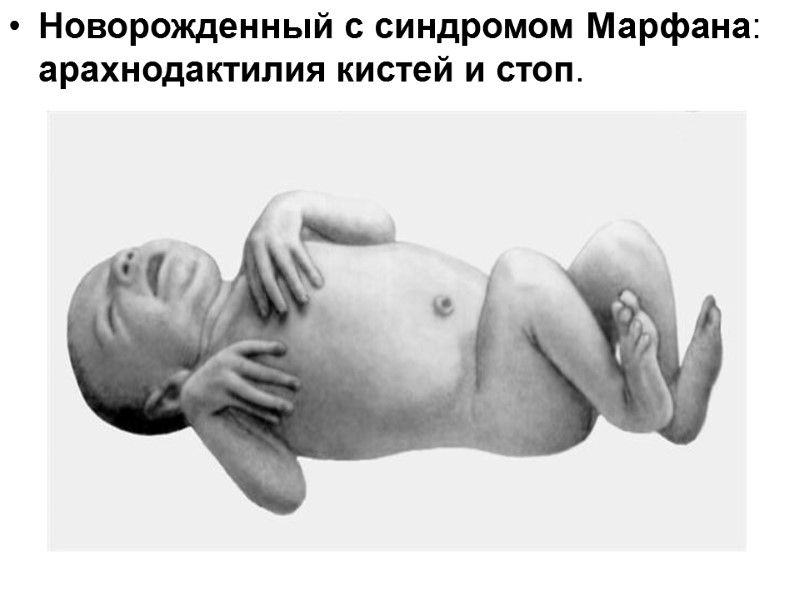
Новорожденный с синдромом Марфана: арахнодактилия кистей и стоп.
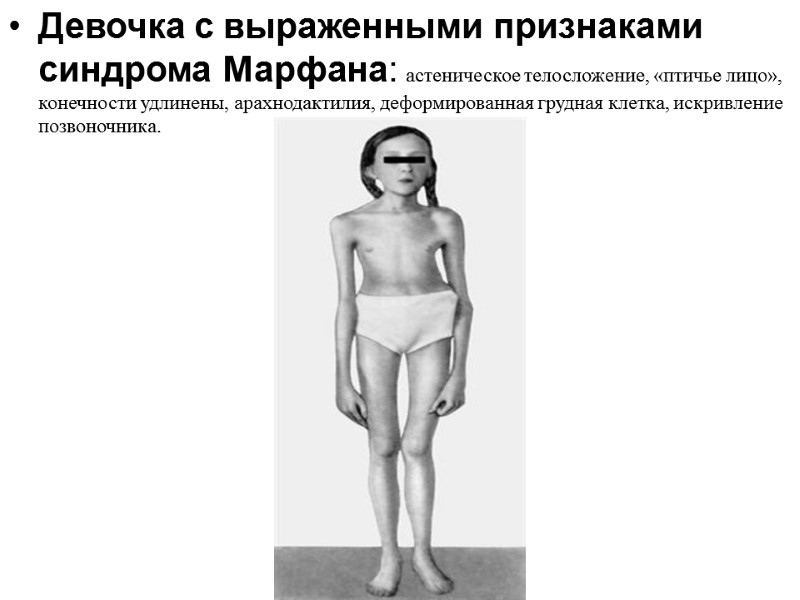
Девочка с выраженными признаками синдрома Марфана: астеническое телосложение, «птичье лицо», конечности удлинены, арахнодактилия, деформированная грудная клетка, искривление позвоночника.
5214-teratologia_zao_83_sl.ppt
- Количество слайдов: 83

