ЛЕКЦИЯ 8. ТЕПЛОВЫЕ СОСТОЯНИЯ.ppt
- Количество слайдов: 94

ТЕПЛОВЫЕ СОСТОЯНИЯ ЛЕКЦИЯ 8 НОЯБРЯ

Тепловые состояния как результат воздействия «теплого» окружения Движение Видимое Невидимое (механическое перемещение тел в пространстве) (тепловое, хаотическое блуждание молекул)

• Механическое перемещение подвержено воздействию трения, а потому со временем может прекратиться, если нет вынуждающей силы Часы следует заводить!

• Тепловое движение молекул продолжается бесконечно долго благодаря контакту с термостатом, который хаотически «подпитывает» его энергией.

. Для распространения запаха духов в комнате нужно несколько минут. Скорость молекул 450 - 500 м/сек Причина замедления – молекулы движутся хаотически, сталкиваясь друг с другом

интенсивность хаотичности движения молекул возрастает с увеличением доступного объема Хаотичность меньше Хаотичность больше
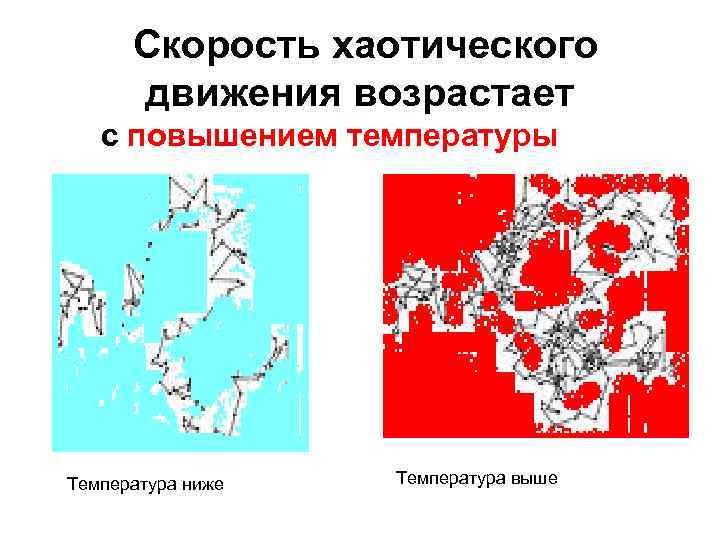
Скорость хаотического движения возрастает с повышением температуры Температура ниже Температура выше

Что такое температура? Холодно необходимо сравнение с другим телом! Тепло Операциональное определение: Длина – то, что измеряется линейкой; Температура – то, что измеряется термометром.
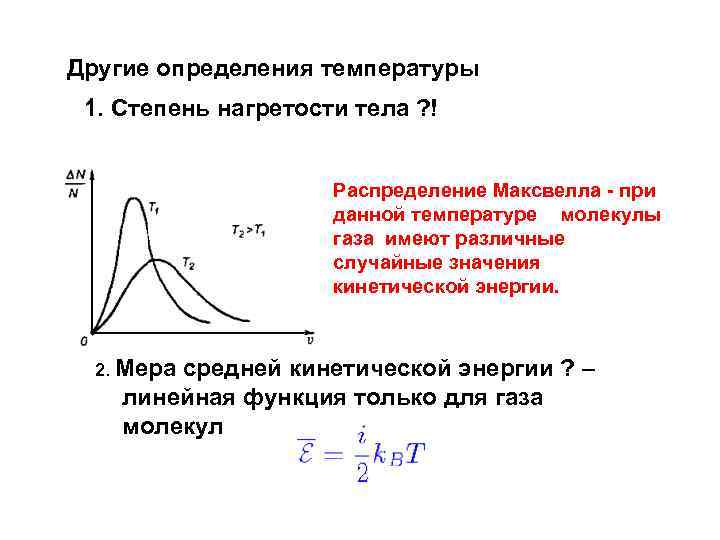
Другие определения температуры 1. Степень нагретости тела ? ! Распределение Максвелла - при данной температуре молекулы газа имеют различные случайные значения кинетической энергии. 2. Мера средней кинетической энергии ? – линейная функция только для газа молекул

Тепловому излучению также можно сопоставить температуру Закон Стефана - Больцмана - парабола четвертой степени ! Тепло (холодно)– (наречие) – субъективное ощущение. Теплота – энергия, передаваемая при контакте в процессе, приводящем к изменению заселенности энергетических состояний. Работа – энергия, передаваемая при механическом контакте в процессе, сопровождающемся изменением макропараметров тела (объема, давления…)

Из истории понятия «температура»
1. Бытовое представление: тепло – холодно 2. Медицина: болезнь – здоровье Лекарства охлаждение (увлажнение) согревание (сухость)

Гален (II век нэ, врач): Четыре «градуса лекарств» градус – ступень (лат. ) Дата рождения: 129 или 131 Место рождения: Пергам Дата смерти: около 200 или около 210 Научная сфера: медицина, анатомия

Четыре «градуса лекарств» градус – ступень (лат. ) ТЕПЛО ХОЛОД ВЛАЖНОСТЬ СУХОСТЬ Каждый ГРАДУС делился на три части Лекарства состояли из смеси 1/3 долей разных градусов В итоге существовала 12 -градусная шкала лекарств!

Нужная смесь лекарств называлась температура Температура (лат. – правильное смешение) - нормальное состояние (мед. термин до XVIII в. ) - соразмерность (муз. термин)

Для повседневного обихода и для науки нужен прибор, измеряющий температуру. Термометр

Различные виды термометров

Термометрические тела • В качестве термометрического тела могут выступать любые среды, свойства которых (механические, электрические, магнитные, оптические и др. ) однозначно реагируют на изменение температуры термопара пирометр Биметаллическая пластина

Термометрические жидкости : ртуть, спирт, вода и т. д. - их объем V однозначно связан с Т Для воды вблизи – 40 С функция Т(V) двузначна, поэтому вода не используется как термометрическое тело в этой температурной области.

история термометра Галилей (Италия) – первый термометр 17 в. Ньютон (Англия ) 18 в. 19 в. Фаренгейт – Голландия Цельсий – Швеция Кельвин - Англия

Фаренгейт (1686 – 1736) – ртутный термометр 1724 г. Цельсий (1701 – 1744) шкала Цельсия 1742 г.

Температурные шкалы Фаренгейта (0 F) и Цельсия (0 С) • Фаренгейт– изобретатель ртутного термометра 00 – низшая температура зимой в Ирландии; 1000 – температура тела человека; (1686 – 1736)

Цельсий (1701 – 1744) • 00 – кипение воды 1000 – таяние льда • Градус Цельсия больше градуса Фаренгейта и совпадает градусом Кельвина ! с
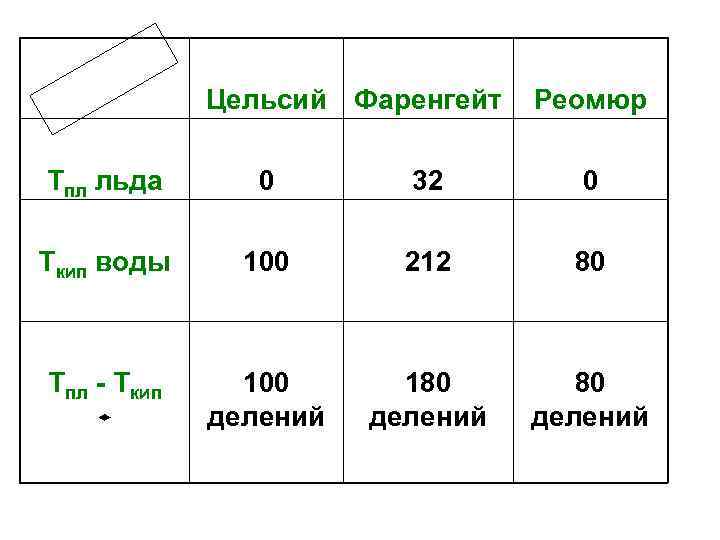
Цельсий Фаренгейт Реомюр Тпл льда 0 32 0 Ткип воды 100 212 80 Тпл - Ткип 100 делений 180 делений

Лорд Кельвин (Уильям Томсон) - создатель абсолютной шкалы - 1848 г. (1824 -1907)

Абсолютная шкала Кельвина • абсолютный нуль — наиболее низкая возможная температура, при которой ничего не может быть холоднее

Пересчет показаний термометров 0 F = t 0 (C)· 1, 8 +32; 100 0 F ~ 37 0 C T (K) = T 0 C + 273, 150
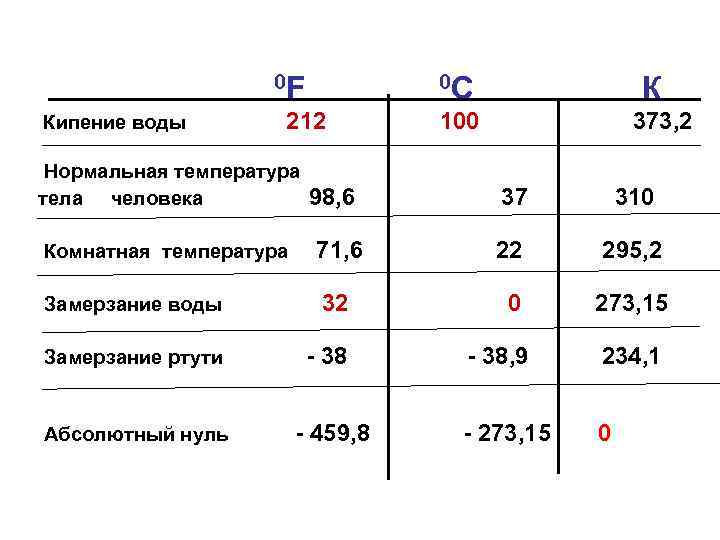
0 F Кипение воды 0 С 212 Нормальная температура тела человека 98, 6 К 100 373, 2 37 310 Комнатная температура 71, 6 22 295, 2 Замерзание воды 32 0 273, 15 Замерзание ртути - 38, 9 234, 1 Абсолютный нуль - 459, 8 - 273, 15 0
Понятие температуры в быту Температура – то, что измеряется термометром Холодно? Тепло ? необходимо сравнение с другим телом! Каков физический смыл температуры? Как измеряется температура? С чем сравнивается характеристика объекта?

Два типа величин, описывающих свойства объектов : 1. Характеристики объектов, выражаемые количественными числительными (сколько? ) • Если несколько объектов образуют систему, их однородные характеристики можно складывать ! • Такие величины называются аддитивными
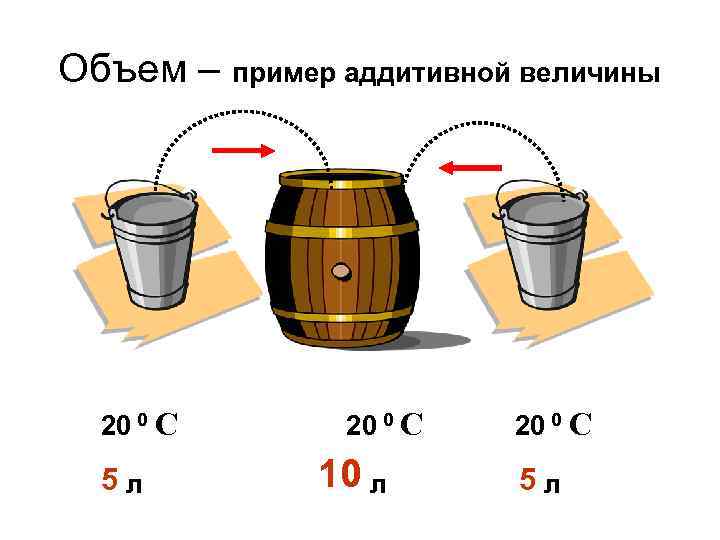
Объем – пример аддитивной величины 20 0 С 5 л 20 0 С 10 л 20 0 С 5 л

Длительность процессов время движения + время нахождения в покое Суммарная длительность движения и покоя находится путем сложения. Это аддитивная величина!
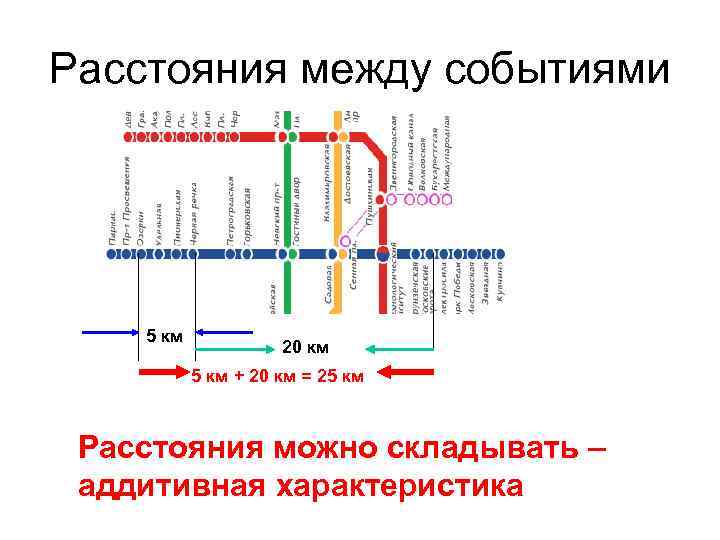
Расстояния между событиями 5 км 20 км 5 км + 20 км = 25 км Расстояния можно складывать – аддитивная характеристика

Другой тип характеристик 2. Своеобразные метки состояний целостной системы из объекта и его окружения Они выражаются порядковыми (который? ) числительными Подобные величины называются неаддитивными

• Особенность порядковых числительных – в том, что их бессмысленно складывать Который фонарь? Нельзя «сложить» второй и пятый фонари !

Момент времени – метка события - порядковое числительное Который час? Второй час ночи! Второй год жизни

Моменты времени совершения двух событий складывать нельзя! Событие А Событие B
Координаты разных событий – это метки, характеризующие местоположение событий Их также нельзя складывать x 1 x 2 x 3 x

При сливании двух порций воды их температуры 80 0 С не суммируются! ≠ 1200 С 400 С ТЕМПЕРАТУРА – НЕАДДИТИВНАЯ ХАРАКТЕРИСТИКА

Следствие неаддитивности температуры • Температуры тел при их соединении не складываются, как складываются их длины, массы, объемы. • Для температуры нет эталонного объекта, прикладывая который многократно (как эталон метра) можно было бы измерить температуру. • Что показывает термометр? - 1. существование особого состояния объекта в контакте с окружением, называемого тепловым равновесием в данных условиях - 2. указывает на отличие особенностей данных условий контакта от иных возможных внешних условий, создаваемых окружением

На пути к равновесию: холодное молоко перемешивается с горячим кофе, и со временем все элементы смеси остывают, становясь такими же, как воздух в комнате. В холодильнике остывание будет более значительным Объект и его окружение приобретают общую характеристику Т: Т смеси =Т окружения =Т Такое состояние называется тепловым равновесием (ТР ), а общая характеристика - температурой

Нулевой закон тепловых процессов • Только состоянию теплового равновесия можно приписать определенную температуру • В состоянии теплового равновесия температуры объекта и его окружения равны.

Температура является условной «меткой» ТР, общей и для объекта и для окружения. Ее можно было бы характеризовать не числовой, а цветной шкалой, используя вместо градусов – оттенки спектра. . 40 о С = «ярко красное состояние»

Температура и частота ИЗЛУЧЕНИЯ • Каждому цветовому участку спектра можно сопоставить свою частоту и длину волны, которые также относятся к неаддитивным характеристикам. • В этом проявляется определенная связь между температурой окружения и частотой тех колебательных процессов, которые в нем происходят • Обе эти величины неаддитивны и характеризуют в целом и совместно объект и его окружение

Итак, температура • Это лишь условная метка состояния теплового равновесия • Правильно было бы говорить: десятый, а не десять градусов; сотый, а не сто градусов по Цельсию – т. е. пользоваться порядковыми, а не количественными числительными !!! - Гегель

Вывод: температура 1. неаддитивна (addition –сумма), т. е. не подчиняется правилу сложения 2. как физическая величина принципиально отличается от таких, как масса, объем, энергия и т. д. , КОТОРЫЕ ЯВЛЯЮТСЯ АДДИТИВНЫМИ 3. ОНА «НАВЯЗАНА» ОБЪЕКТУ ОКРУЖЕНИЕМ И ОПИСЫВАЕТ ОДНОВРЕМЕННО И ОБЪЕКТ И ВНЕШНИЕ УСЛОВИЯ, В КОТОРЫХ ОН НАХОДИТСЯ
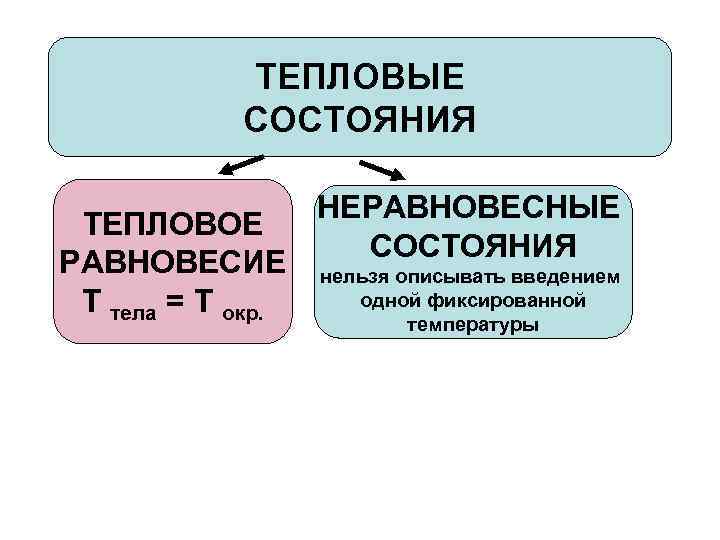
ТЕПЛОВЫЕ СОСТОЯНИЯ ТЕПЛОВОЕ РАВНОВЕСИЕ Т тела = Т окр. НЕРАВНОВЕСНЫЕ СОСТОЯНИЯ нельзя описывать введением одной фиксированной температуры

ТЕПЛОВОЕ РАВНОВЕСИЕ (ТР) – фундаментальная модель неклассического описания тепловых процессов Это состояние объекта и окружения (термостата), которое система приобретает через определенное время после установления теплового контакта (для медицинского термометра ≈ 10 мин. ). При прочих неизменных внешних условиях состояние ТР продолжается бесконечно долго.

Достигнув состояния ТР с термостатом (окружением), объект «забывает» свою предыдущую историю. (для остывшего до комнатной температуры стакана чая нельзя вычислить исходную температуру!) Самопроизвольно объект не может вернуться в предшествовавшее данному состояние ТР. Достижение состояния ТР - необратимый процесс!
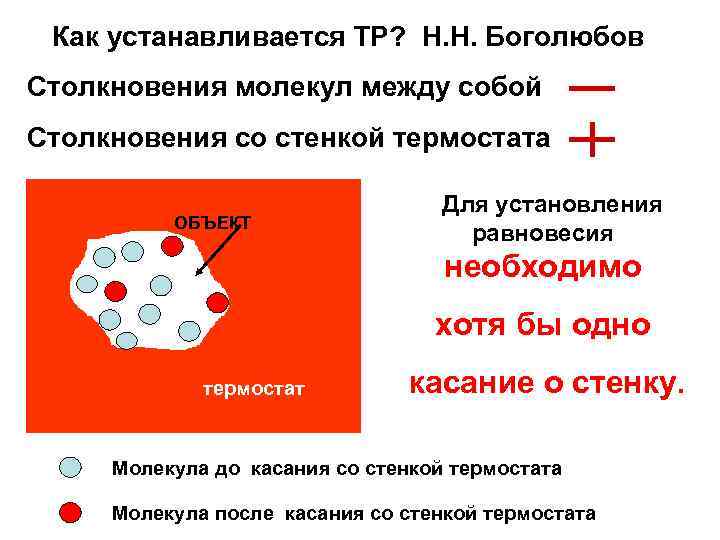
Как устанавливается ТР? Н. Н. Боголюбов Столкновения молекул между собой Столкновения со стенкой термостата ОБЪЕКТ Для установления равновесия необходимо хотя бы одно термостат касание о стенку. Молекула до касания со стенкой термостата Молекула после касания со стенкой термостата

ОСОБЕННОСТЬ СОСТОЯНИЯ ТЕПЛОВОГО РАВНОВЕСИЯ: • Равновесные тепловые состояния – результат длительного стохастического воздействия окружения (термостата). В этом случае : энергия молекулы Е становится случайной величиной, т. е. в принципе она может принимать любые значения, но с разной вероятностью в зависимости от E, а также испытывать флуктуации относительно своего среднего значения. •
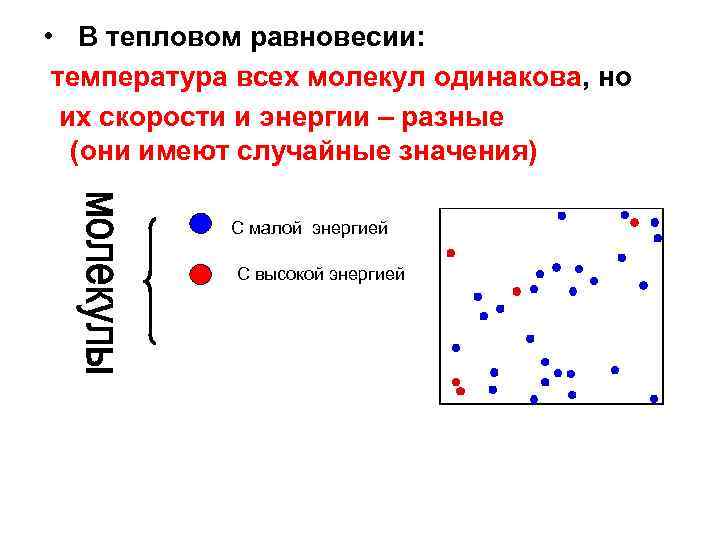
• В тепловом равновесии: температура всех молекул одинакова, но их скорости и энергии – разные (они имеют случайные значения) С малой энергией С высокой энергией
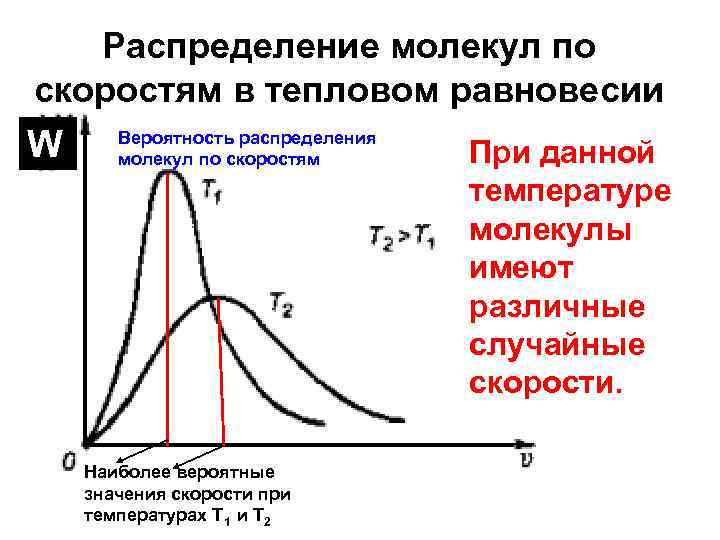
Распределение молекул по скоростям в тепловом равновесии W Вероятность распределения молекул по скоростям Наиболее вероятные значения скорости при температурах Т 1 и Т 2 При данной температуре молекулы имеют различные случайные скорости.

Современный смысл температуры: ( то, что измеряется термометром) - это характеристика объекта не самого по себе, а объекта в равновесном контакте с окружением.

Температура - это характеристика, которая вводится для описания ТР Температура характеризует систему в целом, т. е. совместно объект и окружение Так, термометр показывает «свою собственную» температуру, но она равна температуре тела, с которым он находится в состоянии ТР

Хаотичность и упорядоченность Порядок реализуется единственным способом, беспорядок – множеством вариантов Вероятность беспорядка выше, чем порядка

Беспорядок и вероятность Порядок осуществляется единственным способом из множества возможных комбинаций. Вероятность обнаружить беспорядок значительно выше, если число возможных комбинаций велико

Мерой неупорядоченности системы является Энтропия : • Чем проще система, тем она более однородна и менее упорядочена. • В наиболее однородном состоянии система имеет максимум энтропии • Тепловое равновесие – наиболее однородное (неупорядоченное) состояние – характеризуется максимумом энтропии

Второй закон тепловых процессов • Энтропия объекта либо не изменяется, либо возрастает Стохастическое воздействие «теплого» окружения описывается фундаментальной константой Больцмана k. B = 1, 38 ∙ 10 -23 Дж/K, имеющей смысл минимальной энтропии

Хаотичность, вероятность и энтропия • Чем больше хаотичность объекта, тем больше число способов ее реализации • Чем больше Связь между энтропией S и хаотичность числом способов объекта, тем больше его реализации состояния W энтропия

Л. Больцман S= k log W 1844 -1906

Константа Больцмана k. B Именем Людвига Больцмана названа мировая постоянная – константа стохастического теплового воздействия k. B = 1, 38 ∙ 10 -23 Дж/K

Хаос, симметрия и Энтропия 2 1 3 4 5 У кажущегося симметричным объекта не так много осей симметрии Бесконечное множество осей симметрии Чем больше хаос в системе, тем больше элементов симметрии (выше симметрия)
В живой природе Уровень организации (сложности) возрастает. Симметрия уменьшается.
Симметрия человека Уровень сложности растет. Симметрия падает • Уменьшение энтропии свидетельствует о повышении неоднородности (сложности) объекта

Тепловые процессы, энергия и энтропия
Давняя мечта человека: Источники энергии • механические • получать полезную работу тепловые электрические

При всяком контакте с окружением • Объект может получать от него или отдавать ему определенную энергию. • В зависимости от типа воздействия окружения эта энергия описывается разными характеристиками

ХАРАКТЕРИСТИКИ передаваемой энергии: При контролируемом воздействии совершается работа А при расширении газа под давлением p от объема V 1 до объема V 2

При стохастическом тепловом воздействии энергетическая характеристика- теплота Q При нагревании тела массой m от температуры Т 1 до Т 2 передается энергия в форме теплоты

Теплота и работа это два различных способа обмена энергией между телом и окружением за счет контакта Что же происходит с энергией тела, если ему передается энергия в форме работы или теплоты?

До сих пор мы сталкивались со следующими видами энергии: • Кинетическая – за счет движения тела как целого • Потенциальная – за счет внешнего поля (напр. , - тяжести…) • Энергия покоя (за счет наличия массы)

Теперь – надо учитывать энергию движения и взаимодействия молекул, участвующих в хаотическом тепловом движении. • средняя энергия хаотического движения всех частиц объекта называется внутренней энергией тела U. Это характеристика состояния объекта
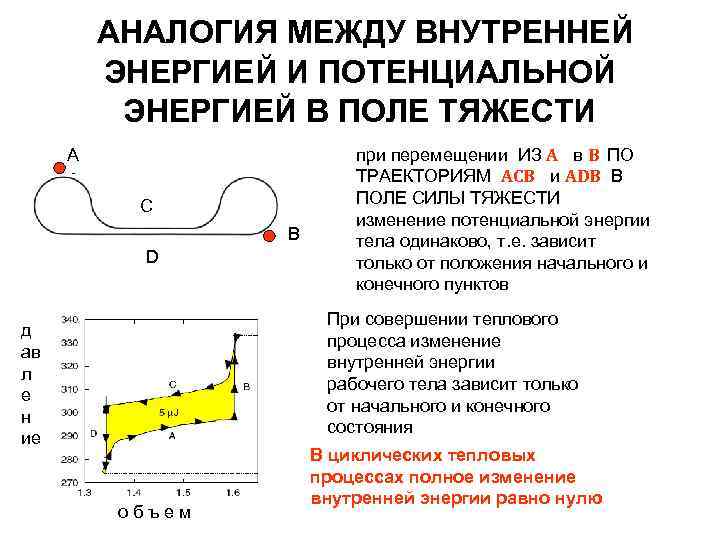
АНАЛОГИЯ МЕЖДУ ВНУТРЕННЕЙ ЭНЕРГИЕЙ И ПОТЕНЦИАЛЬНОЙ ЭНЕРГИЕЙ В ПОЛЕ ТЯЖЕСТИ А C В D при перемещении ИЗ А в В ПО ТРАЕКТОРИЯМ ACB и ADB В ПОЛЕ СИЛЫ ТЯЖЕСТИ изменение потенциальной энергии тела одинаково, т. е. зависит только от положения начального и конечного пунктов При совершении теплового процесса изменение внутренней энергии рабочего тела зависит только от начального и конечного состояния д ав л е н ие объем В циклических тепловых процессах полное изменение внутренней энергии равно нулю

Что бы ни происходило с объектом, • при возвращении в исходное состояние с прежними значениями температуры и объема его внутренняя энергия не изменяется • внутренняя энергия – зависит только от состояния объекта, ХАРАКТЕРИЗУЕМОГО ДАВЛЕНИЕМ И ТЕМПЕРАТУРОЙ

Кроме того, при контакте с окружением в тепловых процессах тело может получать или отдавать энергию теплового хаотического движения частиц. Эту энергию называют теплотой и обозначают Q. Она не характеризует состояние тела, а передается от более нагретого к менее нагретому телу.

От чего зависит внутренняя энергия? • Хаотичность перемещения частиц определяется: их скоростью, которая увеличивается с температурой ; доступным объемом – который изменяется при совершении работы А • Итак, внутренняя энергия U зависит от ТЕМПЕРАТУРЫ и ОБЪЕМА, которые определяют состояние

Баланс энергии для нециклических тепловых процессов (дебет = кредиту) ПРИХОД ЭНЕРГИИ Q - от нагревателя РАСХОД ЭНЕРГИИ Δ U – изменение внутренней энергии A – работа Первый закон термодинамики- науки о тепловых процессах. В НЕМ ПОДЧЕРКИВАЕТСЯ, ЧТО ПРИ ТЕПЛОВОМ СТОХАСТИЧЕСКОМ ВОЗДЕЙСТВИИ НЕОБХОДИМО УЧИТЫВАТЬ ИЗМЕНЕНИЕ ВНУТРЕННЕЙ ЭНЕРГИИ

НЕРАВНОЦЕННОСТЬ РАЗНЫХ ВИДОВ ЭНЕРГИИ • ЭНЕРГИЯ – ЭТО ХАРАКТЕРИСТИКА, УКАЗЫВАЮЩАЯ, СКОЛЬКО РАБОТЫ МОЖЕТ СОВЕРШИТЬ ТЕЛО • С ЭТОЙ ТОЧКИ ЗРЕНИЯ, ВНУТРЕННЯЯ ЭНЕРГИЯ – ОБЛАДАЕТ «НИЗКИМ» КАЧЕСТВОМ- ОНА НЕ МОЖЕТ БЫТЬ ПОЛНОСТЬЮ ИСТРАЧЕНА НА СОВЕРШЕНИЕ РАБОТЫ

«Неконвертируемость» теплоты : Работа может быть полностью переведена в теплоту A → Q , но теплота в работу Q → A переходит лишь частично. Остальная часть переходит в окружение – это «плата» за процесс! Для совершения полного цикла нужна дополнительная энергетическая «дотация» из окружения

• механика Контролируемое воздействие несет энергию, которая может быть целиком передана стохастическому движению • тепловые процессы Неконтролируемое воздействие несет энергию, которая не может быть целиком передана регулярному движению При стохастическом тепловом воздействии часть энергии «в виде налога» безвозвратно теряется благодаря усилению стохастичности в объекте
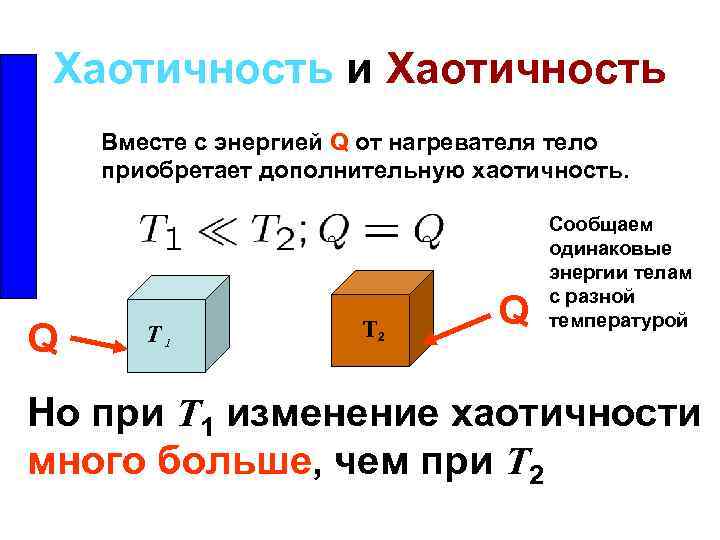
Хаотичность и Хаотичность Вместе с энергией Q от нагревателя тело приобретает дополнительную хаотичность. Q T 1 T 2 Q Сообщаем одинаковые энергии телам с разной температурой Но при T 1 изменение хаотичности много больше, чем при T 2

Хаотичность и энтропия • Рост хаотичности характеризуется изменением особой величины – энтропии S. Её изменение ΔS должно зависеть как от полученной теплоты δQ, так и от температуры Т

Энтропия и энергия –что важнее? • В гигантской фабрике естественных процессов принцип энтропии играет роль директора, который предписывает вид и течение всех сделок. • Закон сохранения энергии (баланса энергии) играет роль бухгалтера, который приводит в равновесие дебет и кредит Арнольд Зоммерфельд

Проблема «тепловой смерти» • Приближение к ТР неизбежно ведет к разрушению структуры объекта. Нет ли противоречия между этим императивом и существованием жизни (упорядоченностью) ? ? ?

Роль Солнца в существовании жизни на Земле Солнце – источник энергии, но температура Земли ТЗ = const. В среднем Земля получает столько же энергии, сколько отдает ночью.

Различие в качестве получаемой и отдаваемой энергии: Получаемое излучение находится в желтой части спектра (свет). Эта энергия состоит из меньшего числа n+ больших порций

Отдаваемое излучение находится в красной части спектра (тепло). Эта энергия состоит из большего числа n- меньших порций

Отдаваемое излучение состоит из большего числа порций, они создают больший беспорядок и уносят большую энтропию Сброс энтропии за счет собственного теплового излучения много больше, чем поступление энтропии от Солнца ΔS_ >> ΔS + В результате энтропия Земли не возрастает и упорядоченность жизни сохраняется

Почему Солнце дает энергию с низкой энтропией? Это след ранних этапов возникновения мира. Исходное «сырье» для образования Солнца – однородный газ протонов имел низкую энтропию, что подтверждается однородностью температуры реликтового излучения. Т = 2, 7 К Точность 0, 1 К Точность 0, 00001 К

Гравитация и второе начало • Обычная ситуация При слабой гравитации энтропия растет при распаде структуры • В процессе эволюции При сильной гравитации энтропия растет в обратном процессе - при образовании структуры.

«Склеивание» протонов под действием гравитации при образовании Солнца увеличивало его энтропию, но она была бы существенно больше, если бы Солнце пришло в состояние теплового равновесия.

NB: угроза цивилизации За счет хозяйственной деятельности человечества происходит дополнительный рост энтропии Чтобы обеспечить ΔSхоз, что упорядоченность, свойственную процессу уменьшает отток энтропии жизни, необходимо ограничить рост ΔSхоз.

ЛЕКЦИЯ 8. ТЕПЛОВЫЕ СОСТОЯНИЯ.ppt