Теплотехника начало.ppt
- Количество слайдов: 30
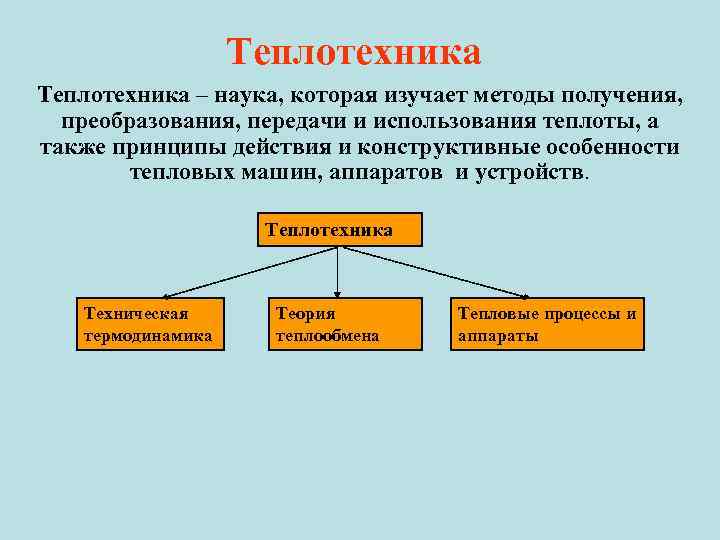
Теплотехника – наука, которая изучает методы получения, преобразования, передачи и использования теплоты, а также принципы действия и конструктивные особенности тепловых машин, аппаратов и устройств. Теплотехника Техническая термодинамика Теория теплообмена Тепловые процессы и аппараты
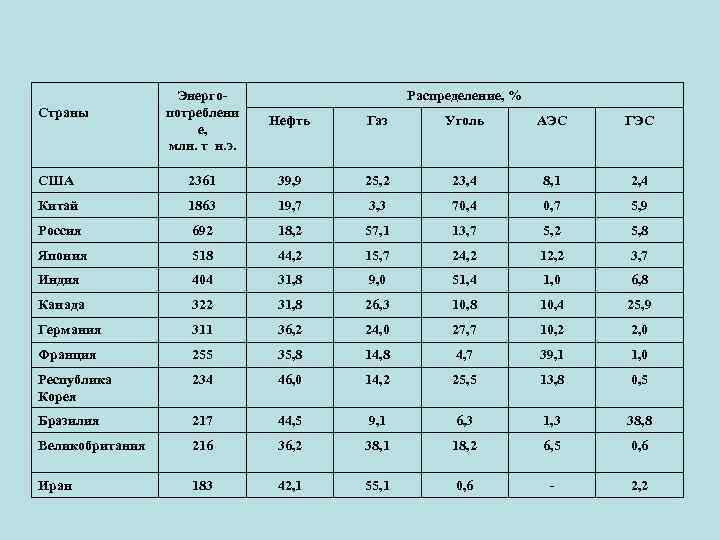
Энергопотреблени е, млн. т н. э. Нефть Газ Уголь АЭС ГЭС США 2361 39, 9 25, 2 23, 4 8, 1 2, 4 Китай 1863 19, 7 3, 3 70, 4 0, 7 5, 9 Россия 692 18, 2 57, 1 13, 7 5, 2 5, 8 Япония 518 44, 2 15, 7 24, 2 12, 2 3, 7 Индия 404 31, 8 9, 0 51, 4 1, 0 6, 8 Канада 322 31, 8 26, 3 10, 8 10, 4 25, 9 Германия 311 36, 2 24, 0 27, 7 10, 2 2, 0 Франция 255 35, 8 14, 8 4, 7 39, 1 1, 0 Республика Корея 234 46, 0 14, 2 25, 5 13, 8 0, 5 Бразилия 217 44, 5 9, 1 6, 3 1, 3 38, 8 Великобритания 216 36, 2 38, 1 18, 2 6, 5 0, 6 Иран 183 42, 1 55, 1 0, 6 - 2, 2 Страны Распределение, %

ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА Базируется на двух основных законах (началах) термодинамики: I закон термодинамики - закон превращения и сохранения энергии; II закон термодинамики – устанавливает условия , необходимые для превращения тепловой энергии в механическую в системах, состоящих из большого количества частиц. Объектом исследования является термодинамическая система. Изолированная система - система не взаимодействующая с окружающей средой. Адиабатная (теплоизолированная) система –имеет адиабатную оболочку, которая исключает обмен теплотой с окружающей средой. Однородная система – система, имеющая во всех своих частях одинаковый состав и физические свойства. Гомогенная система – однородная система по составу и физическому строению (лед, вода, газы). Гетерогенная система – система, состоящая из нескольких гомогенных частей (фаз) с различными физическими свойствами, отделенных одна от другой видимыми поверхностями раздела (лед и вода, вода и пар).

Параметры состояния Удельный объем – величина, определяемая отношением объема вещества к его массе. υ = V / m , [м 3/кг] , Плотность вещества – величина, определяемая отношением массы к объему вещества. ρ = m / V , [кг/м 3], υ = 1 / ρ ; ρ = 1 / υ ; υ. ρ = 1. Давление – с точки зрения молекулярно-кинетической теории есть средний результат ударов молекул газа, находящихся в непрерывном хаотическом движении, о стенку сосуда, в котором заключен газ. Р = F / S ; [Па] = [Н/м 2] Внесистемные единицы давления: 1 кгс/м 2 = 9, 81 Па = 1 мм. водн. ст. 1 ат. (техн. атмосфера) = 1 кгс/см 2 = 98, 1 к. Па. 1 атм. (физическая атмосфера) = 101, 325 к. Па = 760 мм. рт. ст. 1 ат. = 0, 968 атм. 1 мм. рт. ст. = 133, 32 Па. 1 бар = 0, 1 МПа = 100 к. Па = 105 Па.

Первый закон термодинамики I закон термодинамики - закон превращения и сохранения энергии; Q = (U 2 – U 1) + L , где Q - количества теплоты подведенная (отведенная) к системе; L - работа, совершенная системой (над системой); (U 2 – U 1) - изменение внутренней энергии в данном процессе. Если: Q > 0 – теплота подводится к системе; Q < 0 – теплота отводится от системы; L > 0 –работа совершается системой; L < 0 – работа совершается над системой. Для единицы массы вещества уравнение первого закона термодинамики имеет вид: q = Q /m = (u 2 – u 1) + l.
![Теплоемкость газа С = d. Q / d. T , [Дж /К] Различают следующие Теплоемкость газа С = d. Q / d. T , [Дж /К] Различают следующие](https://present5.com/presentation/181705662_345508959/image-6.jpg)
Теплоемкость газа С = d. Q / d. T , [Дж /К] Различают следующие удельные теплоемкости: массовую – с = С / m , [Дж/кг] ; молярную – сμ = С / ν , [Дж/моль] , (где ν – количество вещества моль); объемную – сv = С / V = с·ρ , [Дж/м 3] , (где - ρ = m / V - плотность вещества). Различают теплоемкости Ср при постоянном давлении (изобарный) и при постоянном объеме Сv(изохорный). Между изобарными и изохорными теплоемкостями существует следующая зависимость- уравнение Майера: ср - сv = R сpμ- сvμ = Rμ. Средняя теплоемкость в интервале температур от t 1 до t 2 : Cm = Δq/ΔT q = cm(t 2 – t 1)

Универсальное уравнение состояния идеального газа Для 1 кг массы газа Р·υ = R·Т Для произвольного количества газа массой m : Р·V = m·R·Т Универсальное уравнение состояния для 1 кг газа, которое называют уравнением Клапейрона-Менделеева: Р·υ = Rμ·Т/μ , где: μ - молярная (молекулярная) масса газа, (кг/кмоль); Rμ = 8314, 20 Дж/кмоль (8, 3142 к. Дж/кмоль) - универсальная газовая постоянная и представляет работу 1 кмоль идеального газа в процессе при постоянном давлении и при изменении температуры на 1 градус Зная Rμ можно найти газовую постоянную R = Rμ/μ. Для произвольной массы газа уравнение Клапейрона-Менделеева Р·V = m·Rμ·Т/μ

Смесь идеальных газов Газовая смесь подчиняется закону Дальтона: Общее давление смеси газов равно сумме парциальных давлений отдельных газов, составляющих смесь. Р = Р 1 + Р 2 + Р 3 +. . . + Рn = ∑ Рi , где Р 1, Р 2, Р 3. . . Рn – парциальные давления. Состав смеси задается объемными, массовыми и мольными долями, которые определяются соответственно по следующим формулам: r 1 = V 1 / Vсм ; r 2 = V 2 / Vсм ; … rn = Vn / Vсм , g 1 = m 1 / mсм ; g 2 = m 2 / mсм ; … gn = mn/ mсм , r 1′ = ν 1 / νсм ; r 2′ = ν 2 / νсм ; … rn′ = νn / νсм , где V 1 ; V 2 ; … Vn ; Vсм –объемы компонентов и смеси; m 1 ; m 2 ; … mn ; mсм – массы компонентов и смеси; ν 1 ; ν 2 ; … νn ; νсм – количество вещества (киломолей) компонентов и смеси.

Для идеального газа по закону Дальтона: r 1 = r 1 ′ ; r 2 = r 2 ′ ; … rn = rn′. Так как V 1 +V 2 + … + Vn = Vсм r 1 + r 2 + … + rn = 1 , g 1 + g 2 + … + gn = 1. и m 1 + m 2 + … + mn = mсм , то Связь между объемными и массовыми долями следующее: g 1 = r 1∙μ 1/μсм ; g 2 = r 2∙μ 2 /μсм ; … gn = rn∙μn /μсм , где: μ 1 , μ 2 , … μn , μсм – молекулярные массы компонентов и смеси. Молекулярная масса смеси: μсм = μ 1 r 1 + r 2 μ 2+ … + rn μn. Газовая постоянная смеси: Rсм = g 1 R 1 + g 2 R 2 + … + gn Rn = = Rμ (g 1/μ 1 + g 2/μ 2+ … + gn/μn ) = = 1 / (r 1/R 1 + r 2/R 2+ … + rn/Rn). Удельные массовые теплоемкости смеси: ср см. = g 1 ср 1 + g 2 ср 2 + … + gnср n. сv см. = g 1 сv 1 + g 2 сv 2 + … + gnсv n. Удельные молярные (молекулярные) теплоемкости смеси: срμ см. = r 1 срμ 1 + r 2 срμ 2+ … + rn срμ n. сvμ см. = r 1 сvμ 1 + r 2 сvμ 2+ … + rn сvμ n.

Второй закон термодинамики 1 формулировка (Оствальда): "Вечный двигатель 2 -го рода невозможен". 2 -я формулировка (Клаузиуса): "Теплота не может самопроизвольно переходит от более холодного тела к более нагретому". 3 -я формулировка (Карно): "Там где есть разница температур, возможно совершение работы". Энтропия d. S = d. Q / T [Дж/К] или для удельной энтропии: ds = dq / T [Дж/(кг·К)] Так как энтропия не зависит от вида процесса и определяется начальными и конечными состояниями рабочего тела, то находят только ее изменение в данном процессе, которые можно найти по следующим уравнениям: Δs = cv·ln(T 2/T 1) + R·ln(υ 2/υ 1) ; Δs = cp·ln(T 2/T 1) - R·ln(P 2/P 1) ; Δs = cv·ln(Р 2/Р 1) + cр·ln(υ 2/υ 1). Если энтропия системы возрастает (Δs > 0), то системе подводится тепло. Если энтропия системы уменьшается (Δs < 0), то системе отводится тепло. Если энтропия системы не изменяется (Δs = 0, s = Const), то системе не подводится и не отводится тепло (адиабатный процесс).

Цикл и теоремы Карно Термический коэффициент полезного действия (т. к. п. д. ). ηt = Lц / Qц , или ηt = (Q 1 – Q 2) / Q 1. Для обратимого цикла Карно т. к. п. д. определяется по формуле: ηt к = (Т 1 – Т 2) / Т 1.

Термодинамические процессы Основные процессы термодинамики : изохорный, изотермический, изобарный и адиабатный Δu = сvм|0 t 2·t 2 - сvм|0 t 1·t 1, или, при постоянной теплоемкости, ΔU = m·сv·(t 2 - t 1) Вычисляется работа: L = P·(V 2 – V 1) Определяется количество теплоты в процессе: q = cx·(t 2 - t 1) Определяется изменение энтальпии : Δi = (i 2 – i 1) = сpм|0 t 2·t 2 – сpм|0 t 1·t 1, или при постоянной теплоемкости: Δi = сp·(t 2 – t 1) Определяется изменение энтропии: Δs = cv·ln(T 2/T 1) + R·ln(υ 2/υ 1) Δs = cp·ln(T 2/T 1) - R·ln(P 2/P 1) Δs = cv·ln(T 2/T 1) + cp·ln(υ 2/υ 1) Все процессы рассматриваются как обратимые
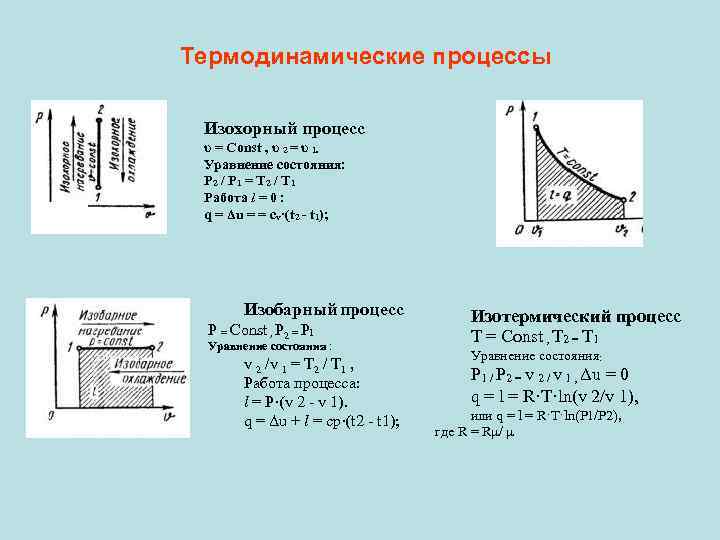
Термодинамические процессы Изохорный процесс υ = Const , υ 2 = υ 1. Уравнение состояния: P 2 / P 1 = T 2 / T 1 Работа l = 0 : q = Δu = = сv·(t 2 - t 1); Изобарный процесс P = Const , P 2 = P 1 Уравнение состояния : v 2 /v 1 = T 2 / T 1 , Работа процесса: l = P·(v 2 - v 1). q = Δu + l = ср·(t 2 - t 1); Изотермический процесс Т = Const , Т 2 = Т 1 Уравнение состояния: P 1 / P 2 = v 2 / v 1 , Δu = 0 q = l = R·T·ln(v 2/v 1), или q = l = R·T·ln(P 1/P 2), где R = Rμ/ μ

. q Адиабатный процесс =0. Уравнение состояния: P· vk = Const, где k = cp / cv – показатель адиабаты. l = -Δu = -сv·(t 2 – t 1) = сv·(t 1 – t 2), l = R·(T 1 – T 2) / (k -1) l = R·T 1·[1 – (v 1/ v 2) k -1) ]/(k – 1) l = R·T 2·[1 – (P 2/P 1) (k -1)/ k)] /(k – 1). Политропный процесс Уравнение состояния: P· vn = Const, где n – показатель политропы при n = ± ∞ v = Const, (изохорный), n=0 P = Const, (изобарный), n = 1 T = Const, (изотермический), n = k P· vk= Const, (адиабатный). l = R·(T 1 – T 2) / (n – 1); l = R·T 1·[1 – (v 1/ v 2) n-1] /(n – 1); l = R·T 2·[1 – (P 2/P 1) (n-1)/ n] /(n – 1). Теплота процесса: q = cn ·(T 2 – T 1), где cn = cv ·(n - k)/(n – 1) – массовая теплоемкость политропного процесса.

Реальные газы. Водяной пар. Влажный воздух Свойства реальных газов Реальные газы отличаются от идеальных газов тем, что молекулы этих газов имеют объемы и связаны между собой силами взаимодействия P·V/(R·T)=c, где С – коэффициент сжимаемости. P·V = R·[1 - Σv/(v + 1)·Bv / vv] Bv – вириальные коэффициенты, выражаются через потенциальные энергию взаимодействия молекул данного газа и температуру Т. При учете первых двух коэффициентов: P·V = R·(1 – А/V- B/ V 2), где А и В - первый и второй вириальные коэффициенты, являющиеся функцией только температуры.

Основы теории теплообмена Перенос теплоты может передаваться тремя способами: теплопроводностью; конвекцией; излучением (радиацией). Температурное поле. Уравнение теплопроводности Закон Фурье: Тепловой поток, передаваемая теплопроводностью, пропорциональна градиенту температуры и площади сечения, перпендикулярного направлению теплового потока. Q = -λ∙F∙ ∂t/∂n, или q = -λ ∙ ∂t/∂n ∙no = -λ∙gradt , где: q – вектор плотности теплового потока; λ – κоэффициент теплопроводности, [Вт/(м∙К)].

Однородная плоская стенка Температуры поверхностей стенки –tст1 и tст2. Плотность теплового потока: q = -λ∙ ∂t/∂n = - λ∙ ∂t/∂x = - λ∙ (t cт2 – t cт1)/(xcт2 - xcт1), или q = λ∙ (tcт2 - tcт1)/(xcт2 - xcт1)∙ Δt/Δx Тогда q = λ/δ∙(tст1 – tст2) = λ/δ∙Δt, Если R =δ/λ -термическое сопротивление n теплопроводности стенки [(м 2∙К)/Вт], то плотность теплового потока: q = (tст1 – tст2)/R. Общее количество теплоты через поверхность F за время τ : Q = q∙F∙τ = (tст1 – tст2)/R·F∙τ. Температура тела в точке с координатой х : tx = tст1 – (tст1 – tст2)∙x/ δ.
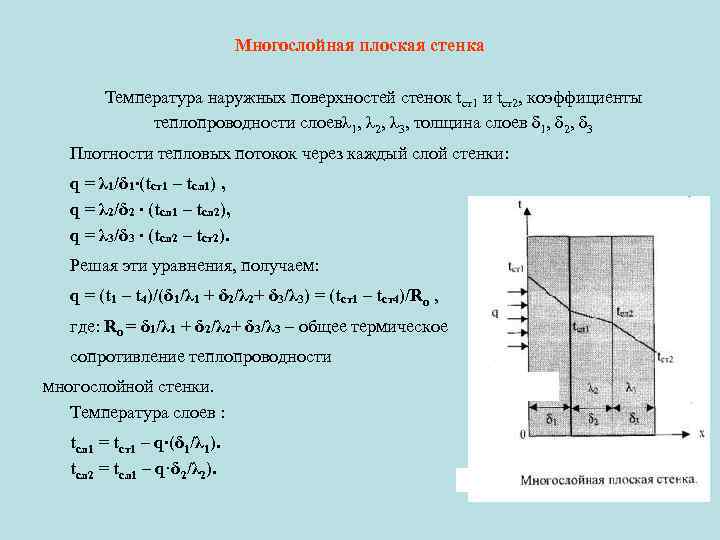
Многослойная плоская стенка Температура наружных поверхностей стенок tст1 и tст2, коэффициенты теплопроводности слоевλ 1, λ 2, λ 3, толщина слоев δ 1, δ 2, δ 3 Плотности тепловых потокок через каждый слой стенки: q = λ 1/δ 1∙(tст1 – tсл 1) , q = λ 2/δ 2 ∙ (tсл 1 – tсл 2), q = λ 3/δ 3 ∙ (tсл 2 – tст2). Решая эти уравнения, получаем: q = (t 1 – t 4)/(δ 1/λ 1 + δ 2/λ 2+ δ 3/λ 3) = (tст1 – tст4)/Ro , где: Ro = δ 1/λ 1 + δ 2/λ 2+ δ 3/λ 3 – общее термическое сопротивление теплопроводности многослойной стенки. Температура слоев : tсл 1 = tст1 – q∙(δ 1/λ 1). tсл 2 = tсл 1 – q·δ 2/λ 2).

Конвективный теплообмен Факторы, влияющие на конвективный теплообмен Природа возникновения движения жидкости Режим движения жидкости Физические свойства жидкостей и газов -коэффициент теплопроводности (λ), -удельная теплоемкость (с), -плотность (ρ), -коэффициент температуропроводности (а = λ/cр·ρ), -коэффициент динамической вязкости (μ) или -кинематической вязкости (ν = μ/ρ), -температурный коэффициент объемного расширения (β =1/l. l/d. Т). Форма

Конвективный теплообмен Закон Ньютона-Рихмана Количество теплоты, передаваемая конвективным теплообменом прямо пропорционально разности температур поверхности тела (t'ст)и окружающей среды (t'ж): Q = α · (t'ст - t'ж)·F , или q = α · (t'ст - t'ж) , где коэффициент теплоотдачи [Вт/(м 2 К)], характеризует интенсивность теплообмена между поверхностью тела и окружающей средой. Коэффициент теплоотдачи является функцией этих параметров : α = f 1(Х; Ф; lo; xc; yc; zc; wo; θ; λ; а; ср; ρ; ν; β) , где: Х – характер движения среды (свободная, вынужденная); Ф – форма поверхности; lo – характерный размер поверхности (длина, высота, диаметр и т. д. ); xc; yc; zc – координаты; wo – скорость среды (жидкость, газ); θ = (t'ст - t'ж) – температурный напор; λ – коэффициент теплопроводности среды; а – коэффициент температуропроводности среды; ср –изобарная удельная теплоемкость среды; ρ –плотность среды; ν – коэффициент кинематической вязкости среды; β – температурный коэффициент объемного расширения среды. •

Критериальные уравнения конвективного теплообмена Nu = f 2(Х; Ф; X 0; Y 0; Z 0; Re; Gr; Pr) , где: X 0; Y 0; Z 0 – безразмерные координаты; Nu = α ·l 0/λ - критерий Нуссельта (безразмерный коэффициент теплоотдачи), характеризует теплообмен между поверхностью стенки и жидкостью (газом); Re = w·l 0/ν - критерий Рейнольдса, характеризует соотношение сил инерции и вязкости и определяет характер течения жидкости (газа); Gr = (β·g·l 03·Δt)/ν 2 - критерий Грасгофа, характеризует подьемную силу, возникающую в жидкости (газе) вследствие разности плотностей; Pr = ν/а = (μ·cp)/λ - критерий Прандтля, характеризует физические свойства жидкости (газа); l 0 – определяющий размер (длина, высота, диаметр).

Расчетные формулы конвективного теплообмена Свободная конвекция в неограниченном пространстве Горизонтальная труба диаметром d при 103<(Gr··Pr)жd <108 Nuжdср. = 0, 5·(Grжd ·Pr ж)0, 25 (Pr ж/Prст)0, 25 Вертикальная труба и пластина: 1). ламинарное течение - 103<(Gr ·Pr)ж <109: Nuжdср = 0, 75· (Grжd ·Pr ж)0, 25·(Pr ж/Prст)0, 25 2). турбулентное течение - (Gr ·Pr)ж > 109: Nuжdср. = 0, 15· (Grжd ·Pr ж)0, 33 ·(Pr ж/Prст)0, 25 Значения Grжd и Pr ж берутся при температуре жидкости (газа), а Prст при температуре поверхности стенки. .

Вынужденная конвекция а). Течение жидкости в гладких трубах круглого сечения. 1). ламинарное течение – Re < 2100 Nuжdср = 0, 15·Reжd 0, 33·Prж 0, 33·(Grжd·Prж)0, 1·(Prж/Prст)0, 25·εl , где εl - коэффициент, учитывающий изменение среднего коэффициента теплоотдачи по длине трубы и зависит от отношения длины трубы к его диаметру (l/d). 2). переходной режим – 2100 < Re < 104 Nuжdср = К 0·Prж 0, 43·(Prж/Prст)0, 25·εl Коэффициент К 0 зависит от критерия Рейнольдса Re

Обтекание горизонтальной поверхности 1). ламинарное течение – Re < 4· 104 Nuжdср = 0, 66·Reжd 0, 5·Prж 0, 33 ·(Prж/Prст)0, 25 2). турбулентное течение – Re > 4· 104 Nuжdср = 0, 037·Reжd 0, 5·Prж 0, 33 ·(Prж/Prст)0, 25 Поперечное обтекание одиночной трубы (угол атаки j = 900) 1). при Reжd = 5 - 103 Nuжdср = 0, 57·Reж 0, 5·Prж 0, 38 ·(Prж/Prст)0, 25 2). при Reжd = 103 -2· 105 Nuжdср = 0, 25 ·Reж 0, 6·Prж 0, 38 ·(Prж/Prст)0, 25

Тепловое излучение Космические лучи l = (0, 1 – 10)о. А (ангстрем 1 о. А = 10 -10 м). Гамма-лучи имеют длину волны до 10 о. А ; лучи Рентгена – l = (10 -200) о. А; ультрафиолетовые лучи – л = (200 о. А - 0, 4 мк (1 мк — 0, 001 мм), световые лучи – l = (0, 4 -0, 8)мк, инфракрасные или тепловые лучи – l = (0, 8 – 400) мк, радио или электромагнитные лучи - l > 400 мк. Из всех лучей наибольший интерес для теплопередачи представляют тепловые лучи с l = (0, 8 – 40) мк. Q = QA + QR + QD , A + R + D = 1 А - коэффициент поглощения. R - коэффициент отражения D - коэффициент проницаемости. Для большинства твердых тел, практически не пропускающих сквозь себя лучистую энергию, А + R = 1.

Основные законы теплового излучения Закон Планка Закон смещения Вина Максимумы кривых с повышением температуры смещаются в сторону более коротких волн lms = 2, 9 / T, где lms - длина волны, отвечающая максимальному значению Isl Интенсивности излучения абсолютно черного тела Isl и любого реального тела Il зависят от температуры и длины волны.

Основные законы теплового излучения Закон Стефана-Больцмана Тепловой поток, излучаемый единицей поверхности черного тела в интервале длин волн от l до l + dl: d. Es = Isldl. d. Es и называется лучеиспускательной способностью абсолютно черного тела для длин волн l+dl. Вся же площадь между любой кривой Т = const и осью абсцисс равна интегральному излучению черного тела в пределах от l = 0 до l = ∞ при данной температуре. Интегральное излучение (тепловой поток) абсолютно черного тела прямо пропорционально четвертой степени его абсолютной температуры Es = Сs (Т/100)4 , где Сs = 5, 67 Вт/(м 2 К 4) - коэффициент излучения абсолютно черного тела.

Основные законы теплового излучения Закон Кирхгофа Е = Еs*А или Е /А = Еs/Аs = Сs*(Т/100)4 Отношение лучеиспускательной способности тела (Е) к его поглощательной способности (А) одинаково для всех серых тел, находящихся при одинаковых температурах и равно лучеиспускательной способности абсолютно черного тела при той же температуре.

Закон Ламберта d 2 Qn = d. Qn*dω*cos φ. Наибольшее количество лучистой энергии для абсолютно черного тела и для тел, обладающих диффузным излучением при φ = 0 - 60°излучается в перпендикулярном направлении к поверхности излучения (φ = 0).

Теплопередача через плоскую стенку Q = (t'ж – t''ж) • F • К, где К = 1 / (1/α 1 +d / λ + 1/α 2) – коэффициент теплопередачи, или R 0 = 1/К = (1/ α 1 + d/λ + 1/ α 2) – полное термическое сопротивление теплопередачи через однослойную плоскую стенку. 1/ α 1, 1/ α 2 – термические сопротивления теплоотдачи поверхностей стенки; d/λ термическое сопротивление стенки.
Теплотехника начало.ppt