 Теория химического строения органических соединений Урок 9 класса. Реакции ионного обмена 21. 09. 2016 1
Теория химического строения органических соединений Урок 9 класса. Реакции ионного обмена 21. 09. 2016 1
 Принцип Ле Шателье Вспомним принцип Ле Шателье: Если на систему, находящуюся в равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия 22. 09. 2016 2
Принцип Ле Шателье Вспомним принцип Ле Шателье: Если на систему, находящуюся в равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия 22. 09. 2016 2
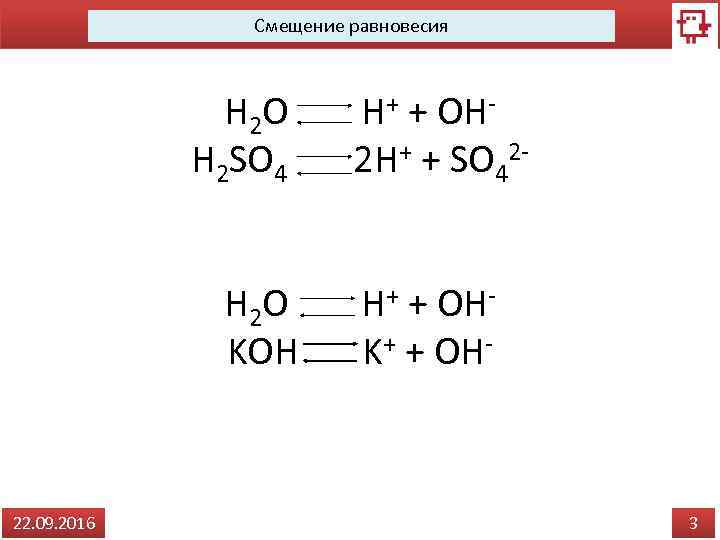 Смещение равновесия H 2 O H+ + OHH 2 SO 4 2 H+ + SO 42 H 2 O H+ + OHKOH K+ + OH- 22. 09. 2016 3
Смещение равновесия H 2 O H+ + OHH 2 SO 4 2 H+ + SO 42 H 2 O H+ + OHKOH K+ + OH- 22. 09. 2016 3
 Задачи 1) Найдите водородный показатель раствора азотной кислоты (HNO 3), если его молярная концентрация равна 0, 178 моль/л. 2) Найти p. H H 2 SO 4 в растворе с C=0, 05 моль/л 3) Найти концентрацию KOH , p. H=14; 22. 09. 2016 4
Задачи 1) Найдите водородный показатель раствора азотной кислоты (HNO 3), если его молярная концентрация равна 0, 178 моль/л. 2) Найти p. H H 2 SO 4 в растворе с C=0, 05 моль/л 3) Найти концентрацию KOH , p. H=14; 22. 09. 2016 4
![p. H Когда [H+] > [OH−] говорят, что раствор является кислотным, а при [OH−] p. H Когда [H+] > [OH−] говорят, что раствор является кислотным, а при [OH−]](https://present5.com/presentation/344780962_437974391/image-5.jpg) p. H Когда [H+] > [OH−] говорят, что раствор является кислотным, а при [OH−] > [H+] — основным. p. H = 7 – нейтральный раствор. Кислоты 22. 09. 2016 Щёлочи 5
p. H Когда [H+] > [OH−] говорят, что раствор является кислотным, а при [OH−] > [H+] — основным. p. H = 7 – нейтральный раствор. Кислоты 22. 09. 2016 Щёлочи 5
 Определение кислотности раствора 22. 09. 2016 6
Определение кислотности раствора 22. 09. 2016 6
 Определение галогенид-ионов Галогенид-ионы определяются при взаимодействиями с солями серебра: Ag. NO 3 + KCl = KNO 3 + Ag. Cl (белый) Ag. NO 3 + KBr = KNO 3 + Ag. Br (светло-желтый) Ag. NO 3 + KI = KNO 3 + Ag. I (желтый) 22. 09. 2016 7
Определение галогенид-ионов Галогенид-ионы определяются при взаимодействиями с солями серебра: Ag. NO 3 + KCl = KNO 3 + Ag. Cl (белый) Ag. NO 3 + KBr = KNO 3 + Ag. Br (светло-желтый) Ag. NO 3 + KI = KNO 3 + Ag. I (желтый) 22. 09. 2016 7
 Определение галогенид-ионов Качественная реакция на соли меди: Cu 2+ +2 OH— → Cu(OH)2↓ Качественные реакции на сульфид-ион (осадки черного цвета): Fe 2+ + S 2 - → Fe. S↓ Ni 2+ + S 2 - → Ni. S↓ Cu 2+ + S 2 - → Cu. S↓ Pb 2+ + S 2 - → Pb. S↓ Hg 2+ + S 2 - → Hg. S↓ Ag+ + S 2 - → Ag 2 S↓ 22. 09. 2016 8
Определение галогенид-ионов Качественная реакция на соли меди: Cu 2+ +2 OH— → Cu(OH)2↓ Качественные реакции на сульфид-ион (осадки черного цвета): Fe 2+ + S 2 - → Fe. S↓ Ni 2+ + S 2 - → Ni. S↓ Cu 2+ + S 2 - → Cu. S↓ Pb 2+ + S 2 - → Pb. S↓ Hg 2+ + S 2 - → Hg. S↓ Ag+ + S 2 - → Ag 2 S↓ 22. 09. 2016 8
 Барий и сульфат-ион Ba 2+ + SO 4 -2 → Ba. SO 4↓ Белый осадок качественная реакция на соли бария; нерастворимый в кислотах качественная реакция на сульфат-ионы; Сa(OH)2 + SO 2 = Ca. SO 3↓ + H 2 O избыток SO 2: Ca. SO 3↓ + H 2 O + SO 2 = Ca(HSO 3)2; растворение в кислотах: Ca. SO 3 + 2 H+ → SO 2↑ + H 2 O + Ca 2+ Белый осадок образуется при пропускании газа без цвета с резким запахом через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах 22. 09. 2016 9
Барий и сульфат-ион Ba 2+ + SO 4 -2 → Ba. SO 4↓ Белый осадок качественная реакция на соли бария; нерастворимый в кислотах качественная реакция на сульфат-ионы; Сa(OH)2 + SO 2 = Ca. SO 3↓ + H 2 O избыток SO 2: Ca. SO 3↓ + H 2 O + SO 2 = Ca(HSO 3)2; растворение в кислотах: Ca. SO 3 + 2 H+ → SO 2↑ + H 2 O + Ca 2+ Белый осадок образуется при пропускании газа без цвета с резким запахом через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах 22. 09. 2016 9
 Алюминий, цинк, фосфат-ион Al 3+ + 3 OH— = Al(OH)3↓ Zn 2+ + 2 OH— = Zn(OH)2↓ избыток щелочи: Al(OH)3 + Na. OH =Na[Al(OH)]4; избыток щелочи: Zn(OH)2 +2 Na. OH =Na 2[Zn(OH)]4; Белый осадок образуется при добавлении щелочи; растворяется в избытке щелочи 3 Ag+ + PO 43 - → Ag 3 PO 4↓ Осадок желтого цвета образуется приливании Ag. NO 3; растворим в кислотах; 22. 09. 2016 10
Алюминий, цинк, фосфат-ион Al 3+ + 3 OH— = Al(OH)3↓ Zn 2+ + 2 OH— = Zn(OH)2↓ избыток щелочи: Al(OH)3 + Na. OH =Na[Al(OH)]4; избыток щелочи: Zn(OH)2 +2 Na. OH =Na 2[Zn(OH)]4; Белый осадок образуется при добавлении щелочи; растворяется в избытке щелочи 3 Ag+ + PO 43 - → Ag 3 PO 4↓ Осадок желтого цвета образуется приливании Ag. NO 3; растворим в кислотах; 22. 09. 2016 10
 Цвет пламени Многие щелочные и щелочно-земельные металлы не имеют нерастворимых солей. Поэтому их определяют по цвету пламени. 22. 09. 2016 11
Цвет пламени Многие щелочные и щелочно-земельные металлы не имеют нерастворимых солей. Поэтому их определяют по цвету пламени. 22. 09. 2016 11