Теория сильных электролитов.pptx
- Количество слайдов: 44
 ТЕОРИЯ РАСТВОРОВ ЭЛЕКТРОЛИТОВ 12. 02. 2018 1
ТЕОРИЯ РАСТВОРОВ ЭЛЕКТРОЛИТОВ 12. 02. 2018 1
 План 1. Некоторые положения теории растворов электролитов, используемые в аналитической химии (в аналитике). 2. Степень электролитической диссоциации α. Сильные и слабые электролиты. 3. Теория сильных и слабых электролитов Дебая Хюккеля. Активность, коэффициент активности. Ионная сила растворов. 4. Ионное произведение воды. Водородный показатель р. Н. 12. 02. 2018 Русецкая О. П. 2
План 1. Некоторые положения теории растворов электролитов, используемые в аналитической химии (в аналитике). 2. Степень электролитической диссоциации α. Сильные и слабые электролиты. 3. Теория сильных и слабых электролитов Дебая Хюккеля. Активность, коэффициент активности. Ионная сила растворов. 4. Ионное произведение воды. Водородный показатель р. Н. 12. 02. 2018 Русецкая О. П. 2
 1. Некоторые положения теории растворов электролитов, используемые в аналитической химии Если при взаимодействии ионов растворенного вещества с молекулами растворителя ионы окружаются нейтральными молекулами растворителя с образованием сольватокомплекса, то такое явление называется сольватацией, а для водных растворов гидратацией. Мп+ + m. H 2 O = [M(H 2 O)m]n+ Так, например, может образоваться аквокомплекс никеля(II): Ni 2+ + 6 Н 2 О ∙═ [Ni(H 2 O)6]2+ 12. 02. 2018 Русецкая О. П. 3
1. Некоторые положения теории растворов электролитов, используемые в аналитической химии Если при взаимодействии ионов растворенного вещества с молекулами растворителя ионы окружаются нейтральными молекулами растворителя с образованием сольватокомплекса, то такое явление называется сольватацией, а для водных растворов гидратацией. Мп+ + m. H 2 O = [M(H 2 O)m]n+ Так, например, может образоваться аквокомплекс никеля(II): Ni 2+ + 6 Н 2 О ∙═ [Ni(H 2 O)6]2+ 12. 02. 2018 Русецкая О. П. 3
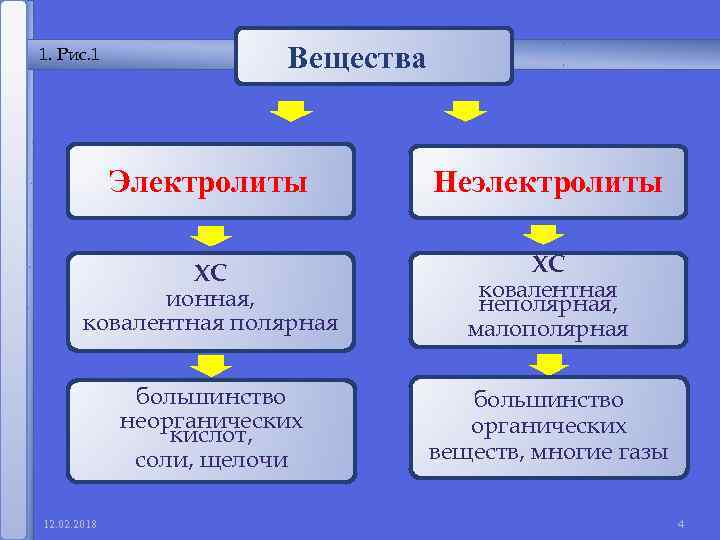 1 1. Рис. 1 Вещества Электролиты Неэлектролиты ХС ионная, ковалентная полярная ХС ковалентная неполярная, малополярная большинство неорганических кислот, соли, щелочи большинство органических веществ, многие газы 12. 02. 2018 4
1 1. Рис. 1 Вещества Электролиты Неэлектролиты ХС ионная, ковалентная полярная ХС ковалентная неполярная, малополярная большинство неорганических кислот, соли, щелочи большинство органических веществ, многие газы 12. 02. 2018 4
 1. Электролиты и неэлектролиты Электролиты - это вещества, растворы и расплавы которых проводят электрический ток. Кислоты: HCl; HNO 3; H 2 SO 4 Щелочи: Na. OH; KOH; Ba(OH)2 Соли: Na. Cl; Cu. SO 4; Al(NO 3)3 12. 02. 2018 5
1. Электролиты и неэлектролиты Электролиты - это вещества, растворы и расплавы которых проводят электрический ток. Кислоты: HCl; HNO 3; H 2 SO 4 Щелочи: Na. OH; KOH; Ba(OH)2 Соли: Na. Cl; Cu. SO 4; Al(NO 3)3 12. 02. 2018 5
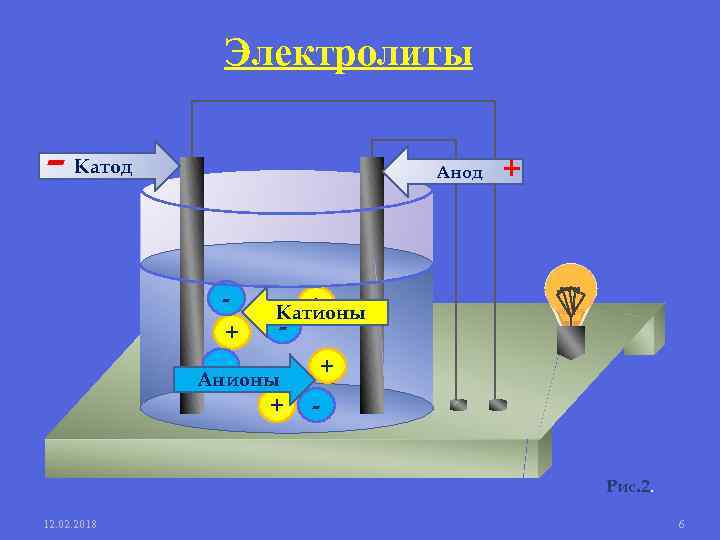 Электролиты - Катод Анод + - + + Катионы - Анионы + + Рис. 2. 12. 02. 2018 6
Электролиты - Катод Анод + - + + Катионы - Анионы + + Рис. 2. 12. 02. 2018 6
 1. Электролиты и неэлектролиты Неэлектролиты - это вещества, растворы или расплавы которых не проводят электрический ток. Органические вещества: сахар, ацетон, бензин, керосин, глицерин, этиловый спирт, бензол и др. Газы: кислород, водород, азот и др. 12. 02. 2018 7
1. Электролиты и неэлектролиты Неэлектролиты - это вещества, растворы или расплавы которых не проводят электрический ток. Органические вещества: сахар, ацетон, бензин, керосин, глицерин, этиловый спирт, бензол и др. Газы: кислород, водород, азот и др. 12. 02. 2018 7
 Неэлектролиты - Катод Анод + Рис. 3. 12. 02. 2018 8
Неэлектролиты - Катод Анод + Рис. 3. 12. 02. 2018 8
 Образование раствора это сложный процесс. В ряде растворов в результате взаимодействия растворен ного вещества и растворителя происходит электролитическая диссоциация растворенного вещества образование ионов. Растворы, ко торые е проводят электриче ский ок, называют н т растворами неэлектролитов, а растворы, в той или иной степени, проводя щие электрический ток, рас творами электролитов. Проводники, прохождение через которые электрического тока вызы вает еремещение вещества в виде п ионов (ионная проводимость) и хи мические превращения (электрохимические реакции), называются элек тролитами. Электрическая проводимость растворов электролитов обусловлена тем, что основания, кислоты и соли в растворах распадаются на ионы – подвергаются электролитической диссоциации. 12. 02. 2018 Русецкая О. П. 9
Образование раствора это сложный процесс. В ряде растворов в результате взаимодействия растворен ного вещества и растворителя происходит электролитическая диссоциация растворенного вещества образование ионов. Растворы, ко торые е проводят электриче ский ок, называют н т растворами неэлектролитов, а растворы, в той или иной степени, проводя щие электрический ток, рас творами электролитов. Проводники, прохождение через которые электрического тока вызы вает еремещение вещества в виде п ионов (ионная проводимость) и хи мические превращения (электрохимические реакции), называются элек тролитами. Электрическая проводимость растворов электролитов обусловлена тем, что основания, кислоты и соли в растворах распадаются на ионы – подвергаются электролитической диссоциации. 12. 02. 2018 Русецкая О. П. 9
 Термии «ион» впервые ввел английский физик М. Фарадей (1791 1867). Теория электролитической диссоциации (ТЭД) была предложена шведским ученым Сванте Аррениусом в 1887 г. (Нобелевская премия 1902 г. ). Позднее ТЭД развивалась и совершенствовалась. Современная теория водных растворов электролитов помимо теории электролитической диссоциации С. Аррениуса включает в себя представления о гидратации ионов (И. А. Каблуков, В. А. Кистяковский), теорию сильных электролитов (П. Й. Дебай, Э. А. Хюккель, 1923 г. ). 12. 02. 2018 Русецкая О. П. 10
Термии «ион» впервые ввел английский физик М. Фарадей (1791 1867). Теория электролитической диссоциации (ТЭД) была предложена шведским ученым Сванте Аррениусом в 1887 г. (Нобелевская премия 1902 г. ). Позднее ТЭД развивалась и совершенствовалась. Современная теория водных растворов электролитов помимо теории электролитической диссоциации С. Аррениуса включает в себя представления о гидратации ионов (И. А. Каблуков, В. А. Кистяковский), теорию сильных электролитов (П. Й. Дебай, Э. А. Хюккель, 1923 г. ). 12. 02. 2018 Русецкая О. П. 10
 2. Электролитическая диссоциация - процесс распада молекул электролита на ионы в растворе или расплаве. С. Аррениус Теория электролитической диссоциации. 1887 г. 12. 02. 2018 11
2. Электролитическая диссоциация - процесс распада молекул электролита на ионы в растворе или расплаве. С. Аррениус Теория электролитической диссоциации. 1887 г. 12. 02. 2018 11
 2. Электролитическая диссоциация Аррениус Сванте Август С. Аррениус (1859 – 1927) 12. 02. 2018 ØШведский ученый, академик. ØВ 1887 году сформулировал основные положения теории электролитической диссоциации. ØВ 1903 г. награжден Нобелевской премией. ØПроводил исследования во многих других областях науки. 12
2. Электролитическая диссоциация Аррениус Сванте Август С. Аррениус (1859 – 1927) 12. 02. 2018 ØШведский ученый, академик. ØВ 1887 году сформулировал основные положения теории электролитической диссоциации. ØВ 1903 г. награжден Нобелевской премией. ØПроводил исследования во многих других областях науки. 12
 Основные положения теории электролитической диссоциации. 1. Электролиты в растворах самопроизвольно распадаются на ионы под действием молекул растворителя. Такой процесс называется электролитической диссоциацией. Диссоциация также может происходить при плавлении твердых электролитов (термическая диссоциация электролитов). 2. Ионы отличаются от атомов по составу и по свойствам. В водных растворах ионы находятся в гидратированном состоянии. 3. В растворах или расплавах электролитов ионы движутся хаотично, но при пропускании через раствор или расплав электролита электрического тока, ионы приобретают направленное движение: катионы перемещаются к катоду, анионы – к аноду. Раствор или расплав электролита является проводником с ионной проводимостью – проводником II рода. 12. 02. 2018 Русецкая О. П. 13
Основные положения теории электролитической диссоциации. 1. Электролиты в растворах самопроизвольно распадаются на ионы под действием молекул растворителя. Такой процесс называется электролитической диссоциацией. Диссоциация также может происходить при плавлении твердых электролитов (термическая диссоциация электролитов). 2. Ионы отличаются от атомов по составу и по свойствам. В водных растворах ионы находятся в гидратированном состоянии. 3. В растворах или расплавах электролитов ионы движутся хаотично, но при пропускании через раствор или расплав электролита электрического тока, ионы приобретают направленное движение: катионы перемещаются к катоду, анионы – к аноду. Раствор или расплав электролита является проводником с ионной проводимостью – проводником II рода. 12. 02. 2018 Русецкая О. П. 13
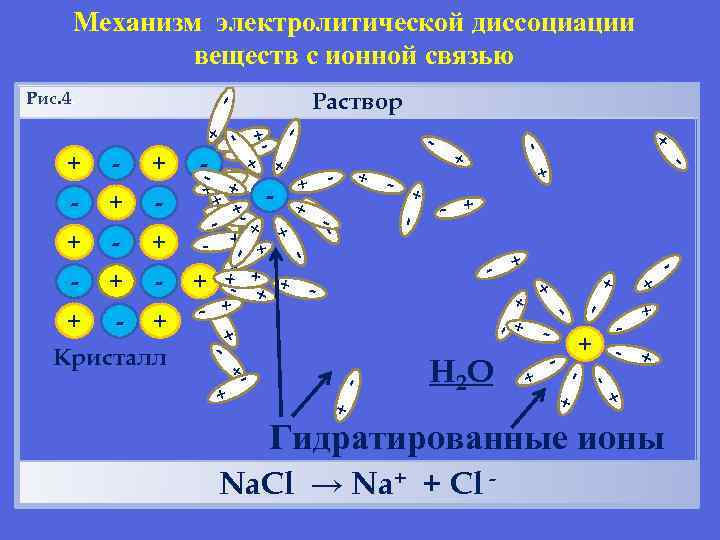 Механизм электролитической диссоциации веществ с ионной связью + + - - - +- - + + + - + - - + + + Н 2 О - - + + - + + + - + - + + + + -- - Кристалл + + - - + + - + - - Раствор + Рис. 4. Гидратированные ионы Na. Cl → Na+ + Cl - -
Механизм электролитической диссоциации веществ с ионной связью + + - - - +- - + + + - + - - + + + Н 2 О - - + + - + + + - + - + + + + -- - Кристалл + + - - + + - + - - Раствор + Рис. 4. Гидратированные ионы Na. Cl → Na+ + Cl - -
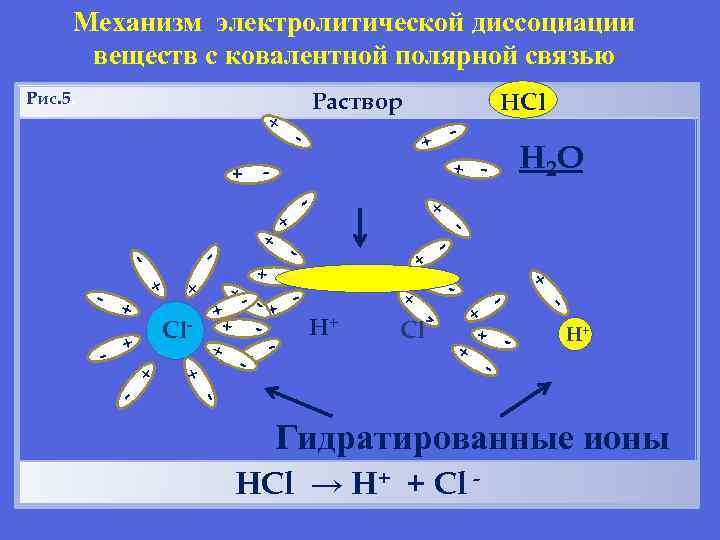 Механизм электролитической диссоциации веществ с ковалентной полярной связью Рис. 5. Раствор + + - - + + + + -- + -+ - - + + H+ - - - + + + - Cl - + + + - + Сl + + Н 2 О + + - HCl Н+ - - Гидратированные ионы НCl → Н+ + Cl - -
Механизм электролитической диссоциации веществ с ковалентной полярной связью Рис. 5. Раствор + + - - + + + + -- + -+ - - + + H+ - - - + + + - Cl - + + + - + Сl + + Н 2 О + + - HCl Н+ - - Гидратированные ионы НCl → Н+ + Cl - -
 2. Степень электролитической диссоциации α. Сильные и слабые электролиты + ++ + + + Сильные и слабые Рис. 6. 16
2. Степень электролитической диссоциации α. Сильные и слабые электролиты + ++ + + + Сильные и слабые Рис. 6. 16
 2. Степень электролитической диссоциации (α) отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе. n α = N Сильные электролиты α > 30% Слабые электролиты α< 30% 12. 02. 2018 17
2. Степень электролитической диссоциации (α) отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе. n α = N Сильные электролиты α > 30% Слабые электролиты α< 30% 12. 02. 2018 17
 2. Сильные и слабые электролиты Электролиты Соли Сильные (α >30%) Слабые (α < 30%) практически все Hg 2 Cl 2 , некоторые cоли тяжелых металлов гидроксиды щелочных и щелочноземельных металлов водный раствор аммиака Основания растворимые в воде нерастворимые - все Кислоты HI, HBr, HCl кислородосодержащие HCl. O 4 H 2 SO 4, HNO 3 бескислородные HF, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, Н 3 РO 4, CH 3 COOH и др.
2. Сильные и слабые электролиты Электролиты Соли Сильные (α >30%) Слабые (α < 30%) практически все Hg 2 Cl 2 , некоторые cоли тяжелых металлов гидроксиды щелочных и щелочноземельных металлов водный раствор аммиака Основания растворимые в воде нерастворимые - все Кислоты HI, HBr, HCl кислородосодержащие HCl. O 4 H 2 SO 4, HNO 3 бескислородные HF, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, Н 3 РO 4, CH 3 COOH и др.
 Степень диссоциации (ионизации) α численно выражается либо в долях единицы, либо в процентах. Если α = 1 (т. е. 100 %), то все исходные частицы в растворе распались на ионы (nдисс = nисх); если α < 1 (т. е. меньше 100%), то не все исходные частицы распались на ионы, а только часть их (nдисс < nисх). Степень электролитической диссоциации зависит от природы электролита, его концентрации в растворе и температуры. С разбавлением и с повышением температуры степень электролитической диссоциации возрастает. С позиций современной электростатической теории сильные электролиты диссоциируют необратимо, а слабые электролиты – обратимо. В концентрированных растворах сильные электролиты частично, в очень небольшой степени, ассоциированы. 12. 02. 2018 Русецкая О. П. 19
Степень диссоциации (ионизации) α численно выражается либо в долях единицы, либо в процентах. Если α = 1 (т. е. 100 %), то все исходные частицы в растворе распались на ионы (nдисс = nисх); если α < 1 (т. е. меньше 100%), то не все исходные частицы распались на ионы, а только часть их (nдисс < nисх). Степень электролитической диссоциации зависит от природы электролита, его концентрации в растворе и температуры. С разбавлением и с повышением температуры степень электролитической диссоциации возрастает. С позиций современной электростатической теории сильные электролиты диссоциируют необратимо, а слабые электролиты – обратимо. В концентрированных растворах сильные электролиты частично, в очень небольшой степени, ассоциированы. 12. 02. 2018 Русецкая О. П. 19
 Сильные (неассоциированные) электролиты в не слишком концентрированных растворах распадаются на ионы практически полностью. Это большинство солей, сильные кислоты, сильные основания. Например, в растворах хлорида натрия Na. Cl, хлороводородной кислоты HCl, rидpоксида атрия Na. OH диссоциация на н ионы осуществляется нацело: Na. Cl → Na+ +Сl НСl + Н 2 О → Н 3 O+ + Cl или упрощенно: HCl → H+ +Сl Na. OH → Na+ +ОН Для сильных электролитов степень их ионизации α = 1 (100 %). 12. 02. 2018 Русецкая О. П. 20
Сильные (неассоциированные) электролиты в не слишком концентрированных растворах распадаются на ионы практически полностью. Это большинство солей, сильные кислоты, сильные основания. Например, в растворах хлорида натрия Na. Cl, хлороводородной кислоты HCl, rидpоксида атрия Na. OH диссоциация на н ионы осуществляется нацело: Na. Cl → Na+ +Сl НСl + Н 2 О → Н 3 O+ + Cl или упрощенно: HCl → H+ +Сl Na. OH → Na+ +ОН Для сильных электролитов степень их ионизации α = 1 (100 %). 12. 02. 2018 Русецкая О. П. 20
 Слабые (ассоциированные) электролиты в растворах диссоциированы частично. Это слабые кислоты, слабые основания, комплексные соединения (их внутренняя сфера), некоторые соли ртути (II), например, g. Cl 2, Hg(CN)2. Так, в водных растворах H уксусная кислота и аммиак лишь частично ионизированы: СН 3 СООН + Н 2 О = Н 3 O+ + CН 3 СОО (или упрощенно: СН 3 СООН = Н+ + СН 3 СОО ) NН 3 · Н 2 О = NН 4+ + ОН Обычно степень диссоциации α для слабых электролитов очень мала (α « 1) и уменьшается с ростом концентрации раствора. 12. 02. 2018 Русецкая О. П. 21
Слабые (ассоциированные) электролиты в растворах диссоциированы частично. Это слабые кислоты, слабые основания, комплексные соединения (их внутренняя сфера), некоторые соли ртути (II), например, g. Cl 2, Hg(CN)2. Так, в водных растворах H уксусная кислота и аммиак лишь частично ионизированы: СН 3 СООН + Н 2 О = Н 3 O+ + CН 3 СОО (или упрощенно: СН 3 СООН = Н+ + СН 3 СОО ) NН 3 · Н 2 О = NН 4+ + ОН Обычно степень диссоциации α для слабых электролитов очень мала (α « 1) и уменьшается с ростом концентрации раствора. 12. 02. 2018 Русецкая О. П. 21
 Рассмотрим, диссоциацию слабой одноосновной кислоты НАn при диссоциации которой наступает химическое равновесие: НАn ↔ Н+ + Аn Согласно закону действующих масс для химического равновесия справедливо: [Н+][ Аn ] = К [ НАn] [Н+], [ Аn ] и [ НАn] – равновесные концентрации ионов и недиссоциированных молекул. В данном случае константа химического равновесия называется константой диссоциации (ионизации). 12. 02. 2018 Русецкая О. П. 22
Рассмотрим, диссоциацию слабой одноосновной кислоты НАn при диссоциации которой наступает химическое равновесие: НАn ↔ Н+ + Аn Согласно закону действующих масс для химического равновесия справедливо: [Н+][ Аn ] = К [ НАn] [Н+], [ Аn ] и [ НАn] – равновесные концентрации ионов и недиссоциированных молекул. В данном случае константа химического равновесия называется константой диссоциации (ионизации). 12. 02. 2018 Русецкая О. П. 22
 Для одноосновной кислоты концентрация диссоциированных молекул равна концентрации ионов, т. е. Сα (концентрация диссоциированных молекул). Отсюда Кд = Сα ∙ Сα / (С Сα) = С∙α 2/ (1 α), где С – общая концентрация; α – степень диссоциации; С Сα концентрация недиссоциированных молекул. Данное уравнение математическое выражение закона разбавления Оствальда. При α << 1 величина 1 α → 1. Тогда Кд = С∙α 2 Отсюда α = √Кд/С Из уравнения следует: 1. При разбавлении раствора степень диссоциации увеличивается. 2. Чем больше константа диссоциации, тем больше степень диссоциации при одинаковой концентрации растворов. 12. 02. 2018 Русецкая О. П. 23
Для одноосновной кислоты концентрация диссоциированных молекул равна концентрации ионов, т. е. Сα (концентрация диссоциированных молекул). Отсюда Кд = Сα ∙ Сα / (С Сα) = С∙α 2/ (1 α), где С – общая концентрация; α – степень диссоциации; С Сα концентрация недиссоциированных молекул. Данное уравнение математическое выражение закона разбавления Оствальда. При α << 1 величина 1 α → 1. Тогда Кд = С∙α 2 Отсюда α = √Кд/С Из уравнения следует: 1. При разбавлении раствора степень диссоциации увеличивается. 2. Чем больше константа диссоциации, тем больше степень диссоциации при одинаковой концентрации растворов. 12. 02. 2018 Русецкая О. П. 23
 3. Теория сильных электролитов Обычно для слабых электролитов не учитывается действие электростати ческих сил между разноименно заряженными ионами. Так концентрация ионов в растворах слабых электролитов невелика и ионы находятся на достаточно больших расстояниях друг от друга, такое упрощение допускается. Но в растворах сильных элект ролитов концентрация ионов достаточно высока, а расстояния между ними невелики. Это учтено при создании теории сильных электролитов (разработана голландским ученым Петером Дебаем и немецким ученым Эрихом Хюккелем в 1923 1925 гг. ). 12. 02. 2018 Русецкая О. П. 24
3. Теория сильных электролитов Обычно для слабых электролитов не учитывается действие электростати ческих сил между разноименно заряженными ионами. Так концентрация ионов в растворах слабых электролитов невелика и ионы находятся на достаточно больших расстояниях друг от друга, такое упрощение допускается. Но в растворах сильных элект ролитов концентрация ионов достаточно высока, а расстояния между ними невелики. Это учтено при создании теории сильных электролитов (разработана голландским ученым Петером Дебаем и немецким ученым Эрихом Хюккелем в 1923 1925 гг. ). 12. 02. 2018 Русецкая О. П. 24
 Сильные электролиты в водных растворах практически полностью ионизированы. При достаточно высокой концентрации ионов и малыми расстояниями между ними (особенно в концентрированных растворах) ионы взаимодействуют между собой. Это межионное взаимодействие приводит к тому, что движение ионов затруднено, а каждый из ионов (рассматривается как заряженная частица) окружен как бы роем противоположно заряженных частиц, так называемой ионной атмосферой, а взаимодействие иона с ионной атмосферой имеет электростатический (кулоновский) характер. При этом каждый из ионов, составляющих ионную атмосферу, сам в свою очередь является центром ионной атмосферы, окружающей его. В результате этого проявляется тенденция к закономерному размещению ионов по всему объему раствора. 12. 02. 2018 Русецкая О. П. 25
Сильные электролиты в водных растворах практически полностью ионизированы. При достаточно высокой концентрации ионов и малыми расстояниями между ними (особенно в концентрированных растворах) ионы взаимодействуют между собой. Это межионное взаимодействие приводит к тому, что движение ионов затруднено, а каждый из ионов (рассматривается как заряженная частица) окружен как бы роем противоположно заряженных частиц, так называемой ионной атмосферой, а взаимодействие иона с ионной атмосферой имеет электростатический (кулоновский) характер. При этом каждый из ионов, составляющих ионную атмосферу, сам в свою очередь является центром ионной атмосферы, окружающей его. В результате этого проявляется тенденция к закономерному размещению ионов по всему объему раствора. 12. 02. 2018 Русецкая О. П. 25
 Снижение подвижности ионов уменьшает их степень участия в процессах, происходящих в растворе, создаётся эффект снижения концентрации электролита. Для оценки способности ионов к химическим реакциям в раство рах сильных электролитов пользуются понятием активность ионов (а). Активность иона – это его эффективная или условная концент рация, соответственно которой он участвует в реакциях, происходящих в растворе электролита. а= f· с Коэффициент активности характеризует влияние электростатичес ких ил на способность иона к химическим с действиям. При f < 1 движение иона в растворе замедлено. Например, в 0, 1 М растворе НС 1 активность иона Н+ равна 0, 0814. Это означает, что в химических реакциях ион водорода действует так, как будто концентрация его составляет не 0, 1 моль/л, а только 0, 0814 моль/л. Тогда коэффициент активности водорода: f = 0, 0814 / 0, 1 = 0, 814. 12. 02. 2018 Русецкая О. П. 26
Снижение подвижности ионов уменьшает их степень участия в процессах, происходящих в растворе, создаётся эффект снижения концентрации электролита. Для оценки способности ионов к химическим реакциям в раство рах сильных электролитов пользуются понятием активность ионов (а). Активность иона – это его эффективная или условная концент рация, соответственно которой он участвует в реакциях, происходящих в растворе электролита. а= f· с Коэффициент активности характеризует влияние электростатичес ких ил на способность иона к химическим с действиям. При f < 1 движение иона в растворе замедлено. Например, в 0, 1 М растворе НС 1 активность иона Н+ равна 0, 0814. Это означает, что в химических реакциях ион водорода действует так, как будто концентрация его составляет не 0, 1 моль/л, а только 0, 0814 моль/л. Тогда коэффициент активности водорода: f = 0, 0814 / 0, 1 = 0, 814. 12. 02. 2018 Русецкая О. П. 26
 При f = 1 ион действует в растворе соответственно своей действительной концен трации, этом случае в a = с. Однако, это происходит лишь в раство рах слабых электролитов или в очень разбавленных растворах силь ных лектролитов, когда расстояния э между ионами достаточно велики. Обычно для сильных электролитов активность ионов существенно отли чается от их концентрации. Поэтому при точных расчетах в уравнение закона действующих масс должны входить активности ионов, а не их концентрации. 12. 02. 2018 Русецкая О. П. 27
При f = 1 ион действует в растворе соответственно своей действительной концен трации, этом случае в a = с. Однако, это происходит лишь в раство рах слабых электролитов или в очень разбавленных растворах силь ных лектролитов, когда расстояния э между ионами достаточно велики. Обычно для сильных электролитов активность ионов существенно отли чается от их концентрации. Поэтому при точных расчетах в уравнение закона действующих масс должны входить активности ионов, а не их концентрации. 12. 02. 2018 Русецкая О. П. 27
 Значение коэффициента активности иона зависит от следующих факторов: 1. От концентрации и заряда иона. 2. От температуры. 3. От концентрации других ионов. 4. От параметров ионной атмосферы ее размеров и плотности. На величину коэффициента активности оказывает влияние общая концентрация всех ионов в растворе. Это учитывают с помощью понятия ионной силы раствора электролита. 12. 02. 2018 Русецкая О. П. 28
Значение коэффициента активности иона зависит от следующих факторов: 1. От концентрации и заряда иона. 2. От температуры. 3. От концентрации других ионов. 4. От параметров ионной атмосферы ее размеров и плотности. На величину коэффициента активности оказывает влияние общая концентрация всех ионов в растворе. Это учитывают с помощью понятия ионной силы раствора электролита. 12. 02. 2018 Русецкая О. П. 28
 Параметры ионной атмосферы определяются ионной силой раствора I. Ионная сила раствора I – величина, характеризующая интенсивность электростатического поля всех ионов в растворе, которая равна полусумме произведений молярной концентрации каждого иона на квадрат его заряда: I = ½ (c 1 z 12 + c 2 z 22 +. . . + cizi 2) = ½ ∑ cizi 2 В разбавленных растворах (I ≤ 10 2) коэффициент активности иона рассчитывается по предельному закону Дебая: lg f i = A zi 2 √I , где А – величина, вычисляемая теоретически. 12. 02. 2018 Русецкая О. П. 29
Параметры ионной атмосферы определяются ионной силой раствора I. Ионная сила раствора I – величина, характеризующая интенсивность электростатического поля всех ионов в растворе, которая равна полусумме произведений молярной концентрации каждого иона на квадрат его заряда: I = ½ (c 1 z 12 + c 2 z 22 +. . . + cizi 2) = ½ ∑ cizi 2 В разбавленных растворах (I ≤ 10 2) коэффициент активности иона рассчитывается по предельному закону Дебая: lg f i = A zi 2 √I , где А – величина, вычисляемая теоретически. 12. 02. 2018 Русецкая О. П. 29
 Она зависит от температуры, диэлектрической проницаемости растворителя и некоторых других его свойств. Для водных растворов при 250 С А = 0, 512. При средних концентрациях раствора (I = 0, 5… 0, 8; т. е. I ≤ 0, 1 ) коэффициент активности иона может быть рассчитан по уравнению Дэвис, также основанному на теории Дебая Хюккеля: A zi 2 √I lg f i = + const I, 1+ √I где const – некоторая постоянная, определяемая опытным путем для каждой системы. 12. 02. 2018 Русецкая О. П. 30
Она зависит от температуры, диэлектрической проницаемости растворителя и некоторых других его свойств. Для водных растворов при 250 С А = 0, 512. При средних концентрациях раствора (I = 0, 5… 0, 8; т. е. I ≤ 0, 1 ) коэффициент активности иона может быть рассчитан по уравнению Дэвис, также основанному на теории Дебая Хюккеля: A zi 2 √I lg f i = + const I, 1+ √I где const – некоторая постоянная, определяемая опытным путем для каждой системы. 12. 02. 2018 Русецкая О. П. 30
 4. Ионное произведение воды. Водородный показатель р. Н. хороший растворитель, Вода – т. к. молекулы воды полярны. слабый амфотерный Вода – электролит. Н 2 О + Н 2 О 12. 02. 2018 Н 3 О+ + ОН- ион гидроксония 104, 50 Механизм ЭД Н+ + ОН- «Капля воды и камень точит» 31
4. Ионное произведение воды. Водородный показатель р. Н. хороший растворитель, Вода – т. к. молекулы воды полярны. слабый амфотерный Вода – электролит. Н 2 О + Н 2 О 12. 02. 2018 Н 3 О+ + ОН- ион гидроксония 104, 50 Механизм ЭД Н+ + ОН- «Капля воды и камень точит» 31
![Константа равновесия этой реакции равна: [H 3 O+][ОН ] K = или [H 3 Константа равновесия этой реакции равна: [H 3 O+][ОН ] K = или [H 3](https://present5.com/presentation/208984867_428488997/image-32.jpg) Константа равновесия этой реакции равна: [H 3 O+][ОН ] K = или [H 3 O+][ОН ] = К[H 2 O]2 [H 2 O]2 Для простоты записи гидротированный ион водорода обычно обозначают символом Н+, а не H 3 O+, и схему диссоциации воды записывают упрощенно: H 2 O = Н+ + ОН Константу равновесия можно записать: [Н+][ОН ] K = или [Н+][ОН ] = К[H 2 O] [H 2 O] 12. 02. 2018 Русецкая О. П. 32
Константа равновесия этой реакции равна: [H 3 O+][ОН ] K = или [H 3 O+][ОН ] = К[H 2 O]2 [H 2 O]2 Для простоты записи гидротированный ион водорода обычно обозначают символом Н+, а не H 3 O+, и схему диссоциации воды записывают упрощенно: H 2 O = Н+ + ОН Константу равновесия можно записать: [Н+][ОН ] K = или [Н+][ОН ] = К[H 2 O] [H 2 O] 12. 02. 2018 Русецкая О. П. 32
 Ввиду слишком слабой ионизации воды можно принять концентрацию молекул воды как величину постоянную. Тогда получится: [Н+][ОН ] = КW Константа КW – ионное произведение воды. Установлено, что константа ионизации воды при 24 о. С равна 1, 0∙ 10 14. [Н+][ОН ] =1, 0∙ 10 14. При диссоциации воды образуется одинаковое число ионов Н+ и ОН , т. е. в чистой воде : [Н+] = [ОН ] = √К W = √ 1, 0∙ 10 14 = 1, 0 ∙ 10 7 моль/л Растворы, содержащие одинаковое количество Н+ и ОН , называются нейтральными. Если к нейтральному раствору прибавить кислоту, то водородные ионы ее соединяются с гидроксильными ионами воды, образуя недиссоциированную молекулу воды, а [Н+] возрастает; одновременно [ОН ] уменьшается. 12. 02. 2018 Русецкая О. П. 33
Ввиду слишком слабой ионизации воды можно принять концентрацию молекул воды как величину постоянную. Тогда получится: [Н+][ОН ] = КW Константа КW – ионное произведение воды. Установлено, что константа ионизации воды при 24 о. С равна 1, 0∙ 10 14. [Н+][ОН ] =1, 0∙ 10 14. При диссоциации воды образуется одинаковое число ионов Н+ и ОН , т. е. в чистой воде : [Н+] = [ОН ] = √К W = √ 1, 0∙ 10 14 = 1, 0 ∙ 10 7 моль/л Растворы, содержащие одинаковое количество Н+ и ОН , называются нейтральными. Если к нейтральному раствору прибавить кислоту, то водородные ионы ее соединяются с гидроксильными ионами воды, образуя недиссоциированную молекулу воды, а [Н+] возрастает; одновременно [ОН ] уменьшается. 12. 02. 2018 Русецкая О. П. 33
 Для характеристики кислотности раствора Зеренсеном был введен водородный показатель р. Н, определяемый как отрицательный десятичный логарифм активности ионов водорода: р. Н = lg а. Н+ При проведении расчетов вместо активности ионов водорода подставляют их концентрацию: р. Н = lg [Н+] и р. ОН = lg [ОН ] Водородный показатель есть десятичный логарифм концентрации водородных ионов, взятый с обратным знаком. В воде и нейтральных растворах р. Н < 7 < р. ОН, в щелочных растворах р. Н > 7 > р. ОН. Величины р. Н количественно характеризуют кислотность и щелочность растворов. Если пролагорифмировать выражение: [Н+][ОН ] = К W = 1, 0∙ 10 14, то получим: lg. К W = р. Н + р. ОН = 14 12. 02. 2018 Русецкая О. П. 34
Для характеристики кислотности раствора Зеренсеном был введен водородный показатель р. Н, определяемый как отрицательный десятичный логарифм активности ионов водорода: р. Н = lg а. Н+ При проведении расчетов вместо активности ионов водорода подставляют их концентрацию: р. Н = lg [Н+] и р. ОН = lg [ОН ] Водородный показатель есть десятичный логарифм концентрации водородных ионов, взятый с обратным знаком. В воде и нейтральных растворах р. Н < 7 < р. ОН, в щелочных растворах р. Н > 7 > р. ОН. Величины р. Н количественно характеризуют кислотность и щелочность растворов. Если пролагорифмировать выражение: [Н+][ОН ] = К W = 1, 0∙ 10 14, то получим: lg. К W = р. Н + р. ОН = 14 12. 02. 2018 Русецкая О. П. 34
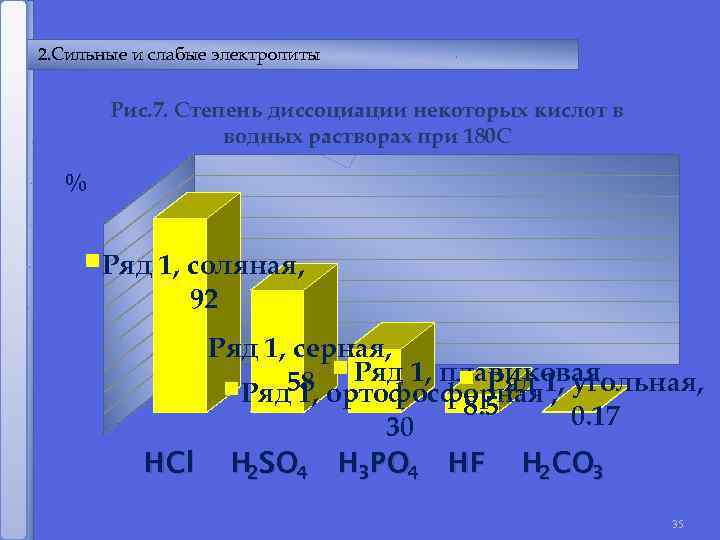 2. Сильные и слабые электролиты Рис. 7. Степень диссоциации некоторых кислот в водных растворах при 180 С % Ряд 1, соляная, 92 Ряд 1, серная, Ряд 1, плавиковая, 58 ортофосфорная 1, угольная, Ряд 1, 8. 5 0. 17 30 HCl H 2 SO 4 H 3 PO 4 HF H 2 CO 3 35
2. Сильные и слабые электролиты Рис. 7. Степень диссоциации некоторых кислот в водных растворах при 180 С % Ряд 1, соляная, 92 Ряд 1, серная, Ряд 1, плавиковая, 58 ортофосфорная 1, угольная, Ряд 1, 8. 5 0. 17 30 HCl H 2 SO 4 H 3 PO 4 HF H 2 CO 3 35
 Диссоциация кислот 5. Диссоциация кислот, оснований, солей Кислоты - это сложные вещества, при диссоциации которых в водных растворах в качестве катионов отщепляются только ионы водорода. НCl → + Cl Н+ Н 2 SO 4 → 2 + SO 4 2 Н+ Н 2 CO 3 12. 02. 2018 + Н 2 Н+ CO 3 2 + 36
Диссоциация кислот 5. Диссоциация кислот, оснований, солей Кислоты - это сложные вещества, при диссоциации которых в водных растворах в качестве катионов отщепляются только ионы водорода. НCl → + Cl Н+ Н 2 SO 4 → 2 + SO 4 2 Н+ Н 2 CO 3 12. 02. 2018 + Н 2 Н+ CO 3 2 + 36
 Диссоциация оснований Основания - это сложные вещества, при диссоциации которых в водных растворах в качестве анионов отщепляются только гидроксид ионы. KOH → K Ca(OH) 2 Мe(OH) n 12. 02. 2018 + + OН Ca 2+ n+ Me - ОН + 2 OН - - + n OН - 37
Диссоциация оснований Основания - это сложные вещества, при диссоциации которых в водных растворах в качестве анионов отщепляются только гидроксид ионы. KOH → K Ca(OH) 2 Мe(OH) n 12. 02. 2018 + + OН Ca 2+ n+ Me - ОН + 2 OН - - + n OН - 37
 Диссоциация солей Соли - это сложные вещества, которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка. Na. Cl → + + Сl. Na 2 SO 4 → 2 + SO 4 2 K K+ 3+ Al(NO 3)3 → Al + 3 NO 3 n+ (кислотный остаток) Me 12. 02. 2018 в 38
Диссоциация солей Соли - это сложные вещества, которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка. Na. Cl → + + Сl. Na 2 SO 4 → 2 + SO 4 2 K K+ 3+ Al(NO 3)3 → Al + 3 NO 3 n+ (кислотный остаток) Me 12. 02. 2018 в 38
 Электролитическая диссоциация 6. О значении электролитов для живых организмов ØЭлектролиты – составная часть жидкостей и плотных тканей живых организмов. Ионы Na+, K+, Ca 2+, Mg 2+, H+; OH-; Cl-; SO 4 -2; имеют НCO 3 большое значение для физиологических и биохимических процессов: Øионы H+; OH- играют большую роль в работе ферментов, обмене веществ, переваривании пищи и др. Øпри нарушении водно солевого обмена в медицине применяется физиологический раствор – 0, 85% раствор Na. Cl; Øионы I - влияют на работу щитовидной железы. 39
Электролитическая диссоциация 6. О значении электролитов для живых организмов ØЭлектролиты – составная часть жидкостей и плотных тканей живых организмов. Ионы Na+, K+, Ca 2+, Mg 2+, H+; OH-; Cl-; SO 4 -2; имеют НCO 3 большое значение для физиологических и биохимических процессов: Øионы H+; OH- играют большую роль в работе ферментов, обмене веществ, переваривании пищи и др. Øпри нарушении водно солевого обмена в медицине применяется физиологический раствор – 0, 85% раствор Na. Cl; Øионы I - влияют на работу щитовидной железы. 39
 6. Рис. 8. Характерные симптомы дефицита химических элементов в организме человека Ионы Са 2+ Mg 2+ Fe 2+ Zn 2+ Mn 2+ Типичный симптом Замедление роста скелета Мускульные судороги Анемия, нарушение иммунной системы Повреждение кожи, замедление полового созревания Учащение депрессий, дерматиты 40
6. Рис. 8. Характерные симптомы дефицита химических элементов в организме человека Ионы Са 2+ Mg 2+ Fe 2+ Zn 2+ Mn 2+ Типичный симптом Замедление роста скелета Мускульные судороги Анемия, нарушение иммунной системы Повреждение кожи, замедление полового созревания Учащение депрессий, дерматиты 40
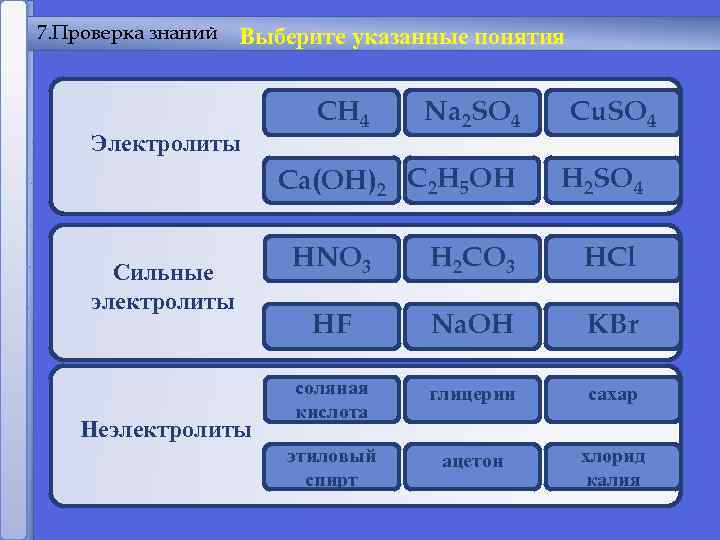 7. Проверка знаний Выберите указанные понятия Электролиты CH 4 Cu. SO 4 Na 2 SO 4 Ошибка Молодец C 2 H 5 OH Молодец Ca(OH)2 Ошибка H 2 SO 4 Сильные электролиты Неэлектролиты HNO 3 HCl H 2 CO 3 Молодец Ошибка Молодец Na. OH KBr HF Ошибка Молодец соляная Ошибка кислота сахар глицерин Молодец этиловый хлорид ацетон Молодец Ошибка спирт калия
7. Проверка знаний Выберите указанные понятия Электролиты CH 4 Cu. SO 4 Na 2 SO 4 Ошибка Молодец C 2 H 5 OH Молодец Ca(OH)2 Ошибка H 2 SO 4 Сильные электролиты Неэлектролиты HNO 3 HCl H 2 CO 3 Молодец Ошибка Молодец Na. OH KBr HF Ошибка Молодец соляная Ошибка кислота сахар глицерин Молодец этиловый хлорид ацетон Молодец Ошибка спирт калия
 Электролитическая диссоциация 7. Проверка знаний Электролитическая диссоциация Основные положения является Электролитами процесс протекает под Слабым электролитомэлектролитической электролитов в растворахраспада _______. в растворах – этоне являются ____. диссоциации сформулировал действием _____. электролита на _____. ученый ______. Вопрос 1 Вопрос 2 Вопрос 3 Вопрос 4 Вопрос 5 12. 02. 2018 А электрического Д. И. Менделеев атомы оксиды KCl тока B С молекул М. В. Ломоносов молекулы Na. OH соли растворителя D температуры электроны М. Фарадей щелочи H 2 S катализатора ионы С. Аррениус кислоты HNO 3 42
Электролитическая диссоциация 7. Проверка знаний Электролитическая диссоциация Основные положения является Электролитами процесс протекает под Слабым электролитомэлектролитической электролитов в растворахраспада _______. в растворах – этоне являются ____. диссоциации сформулировал действием _____. электролита на _____. ученый ______. Вопрос 1 Вопрос 2 Вопрос 3 Вопрос 4 Вопрос 5 12. 02. 2018 А электрического Д. И. Менделеев атомы оксиды KCl тока B С молекул М. В. Ломоносов молекулы Na. OH соли растворителя D температуры электроны М. Фарадей щелочи H 2 S катализатора ионы С. Аррениус кислоты HNO 3 42
 Механизм электролитической диссоциации Na. Cl ØРазрушение кристаллической решетки под действием молекул воды. ØГидратация Na. Cl + n. Н 2 О →Na+ (Н 2 О)х + Сl-(Н 2 О)n-х Na. Cl → Na+ + Cl - Механизм ЭД HCl ØПоляризация связи в молекуле НСl под действием молекул воды. ØГидратация HCl + n. Н 2 О →H+ (Н 2 О)х + Сl-(Н 2 О)n-х + + Cl НCl → Н 12. 02. 2018 Механизм ЭД 43
Механизм электролитической диссоциации Na. Cl ØРазрушение кристаллической решетки под действием молекул воды. ØГидратация Na. Cl + n. Н 2 О →Na+ (Н 2 О)х + Сl-(Н 2 О)n-х Na. Cl → Na+ + Cl - Механизм ЭД HCl ØПоляризация связи в молекуле НСl под действием молекул воды. ØГидратация HCl + n. Н 2 О →H+ (Н 2 О)х + Сl-(Н 2 О)n-х + + Cl НCl → Н 12. 02. 2018 Механизм ЭД 43
 Благодарю за внимание! 12. 02. 2018 44
Благодарю за внимание! 12. 02. 2018 44


