Теория кислот и оснований.ppt
- Количество слайдов: 14
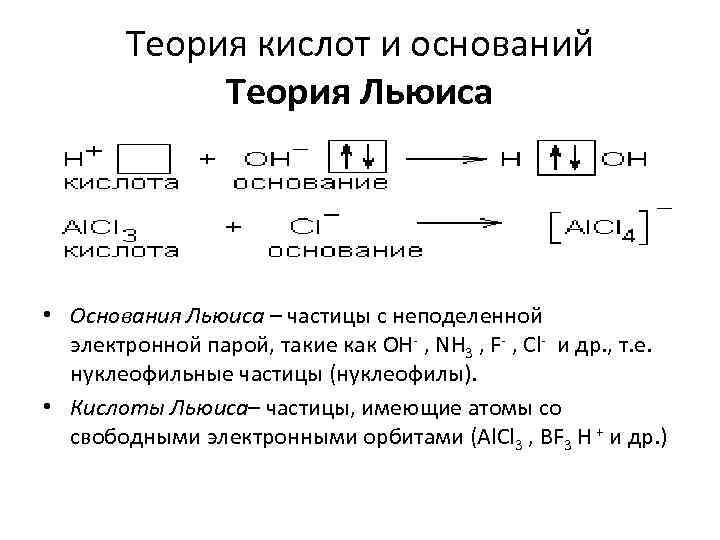 Теория кислот и оснований Теория Льюиса • Основания Льюиса – частицы с неподеленной электронной парой, такие как OH- , NH 3 , F- , Cl- и др. , т. е. нуклеофильные частицы (нуклеофилы). • Кислоты Льюиса– частицы, имеющие атомы со свободными электронными орбитами (Al. Cl 3 , BF 3 Н + и др. )
Теория кислот и оснований Теория Льюиса • Основания Льюиса – частицы с неподеленной электронной парой, такие как OH- , NH 3 , F- , Cl- и др. , т. е. нуклеофильные частицы (нуклеофилы). • Кислоты Льюиса– частицы, имеющие атомы со свободными электронными орбитами (Al. Cl 3 , BF 3 Н + и др. )
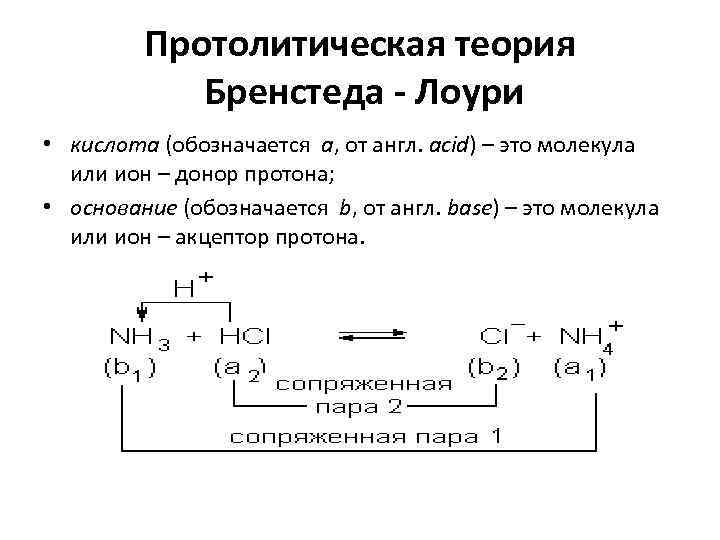 Протолитическая теория Бренстеда - Лоури • кислота (обозначается а, от англ. acid) – это молекула или ион – донор протона; • основание (обозначается b, от англ. base) – это молекула или ион – акцептор протона.
Протолитическая теория Бренстеда - Лоури • кислота (обозначается а, от англ. acid) – это молекула или ион – донор протона; • основание (обозначается b, от англ. base) – это молекула или ион – акцептор протона.
 Протолитическая теория Бренстеда - Лоури • Амфолит – молекула или ион, способный быть как донором, так и акцептором протона в зависимости от партнера по реакции. • • HCO 3 - + H 3 O+ = H 2 CO 3 + H 2 O (b 1) (a 2) (a 1) (b 2) HCO 3 - + OH- = CO 32 - + H 2 O (a 1) (b 2) (b 1) (a 2) H 3 N+ – CH(R) – COO- + H 3 O+ = H 3 N+ – CH(R) – COOH + H 2 O (b 1) (a 2) (a 1) (b 2) H 3 N+ – CH(R) – COO- + OH- = H 2 N – CH(R) – COO- + H 2 O (a 1) (b 2) (b 1) (a 2)
Протолитическая теория Бренстеда - Лоури • Амфолит – молекула или ион, способный быть как донором, так и акцептором протона в зависимости от партнера по реакции. • • HCO 3 - + H 3 O+ = H 2 CO 3 + H 2 O (b 1) (a 2) (a 1) (b 2) HCO 3 - + OH- = CO 32 - + H 2 O (a 1) (b 2) (b 1) (a 2) H 3 N+ – CH(R) – COO- + H 3 O+ = H 3 N+ – CH(R) – COOH + H 2 O (b 1) (a 2) (a 1) (b 2) H 3 N+ – CH(R) – COO- + OH- = H 2 N – CH(R) – COO- + H 2 O (a 1) (b 2) (b 1) (a 2)
 Типы протолитических процессов Процесс Нейтрализация Уравнение реакции (пример) H 3 O+ + OH- = 2 H 2 O CH 3 COOH + CH 3 NH 2 = CH 3 COO- + CH 3 NH 3+ Ионизация NH 3 + H 2 O = NH 4+ + OHCH 3 COOH + H 2 O = CH 3 COO- + H 3 O+ Автоионизация H 2 O + H 2 O = H 3 O+ + OH- (автопротолиз) NH 3 + NH 3 = NH 4+ + NH 2 - Гидролиз CO 32 - + H 2 O = HCO 3 - + OH- (ионный) Cu(H 2 O)2+ + H 2 O = Cu(OH)+ + H 3 O+
Типы протолитических процессов Процесс Нейтрализация Уравнение реакции (пример) H 3 O+ + OH- = 2 H 2 O CH 3 COOH + CH 3 NH 2 = CH 3 COO- + CH 3 NH 3+ Ионизация NH 3 + H 2 O = NH 4+ + OHCH 3 COOH + H 2 O = CH 3 COO- + H 3 O+ Автоионизация H 2 O + H 2 O = H 3 O+ + OH- (автопротолиз) NH 3 + NH 3 = NH 4+ + NH 2 - Гидролиз CO 32 - + H 2 O = HCO 3 - + OH- (ионный) Cu(H 2 O)2+ + H 2 O = Cu(OH)+ + H 3 O+
 Протолитическая теория Бренстеда - Лоури • Любая протолитическая реакция представляет собой конкуренцию оснований за протон. Выигрывает конкуренцию более сильное основание, т. к. сильнее акцептирует протон. • Кислотно-основные свойства вещества проявляются только при взаимодействии его с другими веществами или растворителем, т. е. понятия «кислота» и «основание» являются относительными. • CH 3 COOH + H 2 O = CH 3 COO- + H 3 O+ • CH 3 COOH + H 2 SO 4 (безводн) = CH 3 COOH 2 + HSO 4 • В водном растворе самой сильной кислотой является ион гидроксония H 3 O+ , а самым сильным основанием – гидроксильный ион ОН-.
Протолитическая теория Бренстеда - Лоури • Любая протолитическая реакция представляет собой конкуренцию оснований за протон. Выигрывает конкуренцию более сильное основание, т. к. сильнее акцептирует протон. • Кислотно-основные свойства вещества проявляются только при взаимодействии его с другими веществами или растворителем, т. е. понятия «кислота» и «основание» являются относительными. • CH 3 COOH + H 2 O = CH 3 COO- + H 3 O+ • CH 3 COOH + H 2 SO 4 (безводн) = CH 3 COOH 2 + HSO 4 • В водном растворе самой сильной кислотой является ион гидроксония H 3 O+ , а самым сильным основанием – гидроксильный ион ОН-.
 Автопротолиз воды • Для реакции автопротолиза воды: Н 2 О + Н 2 О = Н 3 О + ОН- • эффективная константа равновесия: • Kw = Кионизации • C(H 2 O) = C(H 3 O+ ) • C(OH- ) = 1 • 10 -14 • (при Т=298 К) • Константу Кw называют константой автопротолиза воды (ионным произведением воды). На основании величины Кw определяется шкала р. Н. • р. Н – водородный показатель, равный • р. Н = - lg c (Н 3 О+)
Автопротолиз воды • Для реакции автопротолиза воды: Н 2 О + Н 2 О = Н 3 О + ОН- • эффективная константа равновесия: • Kw = Кионизации • C(H 2 O) = C(H 3 O+ ) • C(OH- ) = 1 • 10 -14 • (при Т=298 К) • Константу Кw называют константой автопротолиза воды (ионным произведением воды). На основании величины Кw определяется шкала р. Н. • р. Н – водородный показатель, равный • р. Н = - lg c (Н 3 О+)
 Ионизация • Количественной характеристикой силы кислот и оснований служат константы ионизации кислоты – константа кислотности Ка или основания – константа основности Кв ), • показатель кислотности • р. Ка = -lg Ка • показатель основности • р. Кв = -lg Кв
Ионизация • Количественной характеристикой силы кислот и оснований служат константы ионизации кислоты – константа кислотности Ка или основания – константа основности Кв ), • показатель кислотности • р. Ка = -lg Ка • показатель основности • р. Кв = -lg Кв
 Ионизация • • • Для процессов ионизации сопряженной пары: кислоты (А) и основания (В) A + H 2 O = B + H 3 O+ B + H 2 O = A + OH- константы кислотности константа основности • тогда Ka · Kb = c(H 3 O+) · c(OH-) = Kw или p. Ka + p. Kb = p. Kw = 14 • • • аналогично получаем (р. ОН=-lg c(OH–): p. H + p. OH = 14 •
Ионизация • • • Для процессов ионизации сопряженной пары: кислоты (А) и основания (В) A + H 2 O = B + H 3 O+ B + H 2 O = A + OH- константы кислотности константа основности • тогда Ka · Kb = c(H 3 O+) · c(OH-) = Kw или p. Ka + p. Kb = p. Kw = 14 • • • аналогично получаем (р. ОН=-lg c(OH–): p. H + p. OH = 14 •
 Расчет р. Н в растворе слабой кислоты или основания • c(H 3 O+) = • Логарифмируя левую и правую части уравнения и меняя знаки, получим: • -lg c(H 3 O+) = 0, 5 (-lg. Ka – lg c(A)) • p. H = 0, 5 (р. Ka – lg c(A)) - кислота • p. H = 14 - 0, 5 (р. Kb – lg c(B)) - основание
Расчет р. Н в растворе слабой кислоты или основания • c(H 3 O+) = • Логарифмируя левую и правую части уравнения и меняя знаки, получим: • -lg c(H 3 O+) = 0, 5 (-lg. Ka – lg c(A)) • p. H = 0, 5 (р. Ka – lg c(A)) - кислота • p. H = 14 - 0, 5 (р. Kb – lg c(B)) - основание
 Расчет р. Н в растворе сильной кислоты или основания • Сильная кислота • р. Н = - lg α (НА) Сильное основание р. Н = 14 - lg α (В)
Расчет р. Н в растворе сильной кислоты или основания • Сильная кислота • р. Н = - lg α (НА) Сильное основание р. Н = 14 - lg α (В)
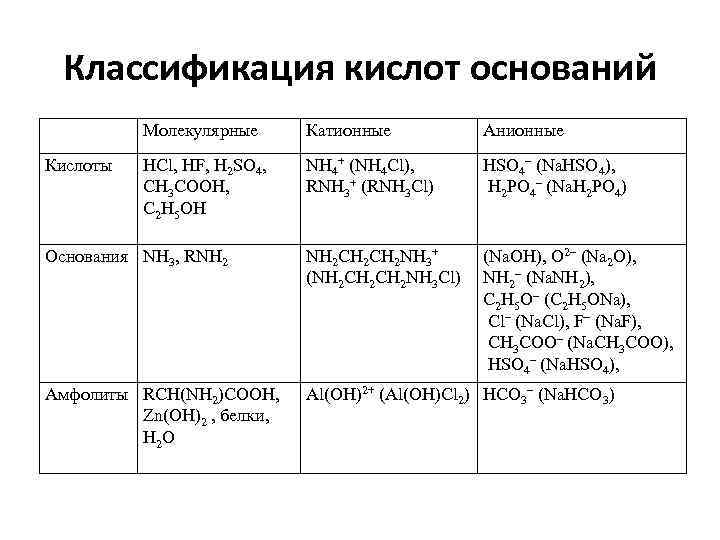 Классификация кислот оснований Молекулярные Катионные Анионные HCl, HF, H 2 SO 4, CH 3 COOH, C 2 H 5 OH NH 4+ (NH 4 Cl), RNH 3+ (RNH 3 Cl) HSO 4– (Na. HSO 4), H 2 PO 4– (Na. H 2 PO 4) Основания NH 3, RNH 2 CH 2 NH 3+ (NH 2 CH 2 NH 3 Cl) (Na. OH), O 2– (Na 2 O), NH 2– (Na. NH 2), C 2 H 5 O– (C 2 H 5 ONa), Cl– (Na. Cl), F– (Na. F), CH 3 COO– (Na. CH 3 COO), HSO 4– (Na. HSO 4), Амфолиты RCH(NH 2)COOH, Zn(OH)2 , белки, H 2 O Al(OH)2+ (Al(OH)Cl 2) HCO 3– (Na. HCO 3) Кислоты
Классификация кислот оснований Молекулярные Катионные Анионные HCl, HF, H 2 SO 4, CH 3 COOH, C 2 H 5 OH NH 4+ (NH 4 Cl), RNH 3+ (RNH 3 Cl) HSO 4– (Na. HSO 4), H 2 PO 4– (Na. H 2 PO 4) Основания NH 3, RNH 2 CH 2 NH 3+ (NH 2 CH 2 NH 3 Cl) (Na. OH), O 2– (Na 2 O), NH 2– (Na. NH 2), C 2 H 5 O– (C 2 H 5 ONa), Cl– (Na. Cl), F– (Na. F), CH 3 COO– (Na. CH 3 COO), HSO 4– (Na. HSO 4), Амфолиты RCH(NH 2)COOH, Zn(OH)2 , белки, H 2 O Al(OH)2+ (Al(OH)Cl 2) HCO 3– (Na. HCO 3) Кислоты
 Гидролиз частный случай кислотно-основного взаимодействия ионов соли с молекулами воды Гидролиз по аниону : An- + H 2 O = HAn + OH– Домножая числитель и знаменатель на с (Н 3 О+), и учитывая и выражение для константы кислотности HAn получаем: p. Kh = 14 - p. Ka
Гидролиз частный случай кислотно-основного взаимодействия ионов соли с молекулами воды Гидролиз по аниону : An- + H 2 O = HAn + OH– Домножая числитель и знаменатель на с (Н 3 О+), и учитывая и выражение для константы кислотности HAn получаем: p. Kh = 14 - p. Ka
 гидролиз • р. Н в растворе соли, гидролизующейся по аниону • p. H = 7+0, 5 (p. Ka + lg -)) c(An • р. Н в растворе соли, гидролизующейся по катиону • p. H = 7 - 0, 5 (p. Kb - lg n+)) c(Kat
гидролиз • р. Н в растворе соли, гидролизующейся по аниону • p. H = 7+0, 5 (p. Ka + lg -)) c(An • р. Н в растворе соли, гидролизующейся по катиону • p. H = 7 - 0, 5 (p. Kb - lg n+)) c(Kat
 Кислотность биожидкостей • Для количественной характеристики кислотных свойств биожидкостей пользуются величинами общей, активной и потенциальной кислотности. • Общая кислотность – это концентрация всех имеющихся в растворе ионов водорода. • Она складывается из концентрации свободных (гидратированных) ионов H+ - активной кислотности и концентрации ионов H+ , связанных в молекулы или ионы слабых кислот – потенциальная кислотность, т. е. : C(H+) общ =C(H+)акт + C(H+)потенц. • Мерой активной кислотности является значение p. H.
Кислотность биожидкостей • Для количественной характеристики кислотных свойств биожидкостей пользуются величинами общей, активной и потенциальной кислотности. • Общая кислотность – это концентрация всех имеющихся в растворе ионов водорода. • Она складывается из концентрации свободных (гидратированных) ионов H+ - активной кислотности и концентрации ионов H+ , связанных в молекулы или ионы слабых кислот – потенциальная кислотность, т. е. : C(H+) общ =C(H+)акт + C(H+)потенц. • Мерой активной кислотности является значение p. H.


